文档内容
课时检测(五十五) 强弱电解质的比较、电离平衡常数的应用及计算
1.(2024·北京海淀区模拟)25 ℃时,下列事实不能说明一水合氨是弱电解质的是( )
A.醋酸铵溶液pH=7
B.0.01 mol·L-1氨水pH约为10.6
C.氯化铵溶液可以除铁锈
D.氨水与氯化铁溶液混合产生沉淀
2.已知25 ℃时,CH COOH的K 为1.75×10-5,HCN的K 为6.2×10-10,HCO 的K 为4.5×10-
3 a a 2 3 a1
7,K 为4.7×10-11。下列相关表达或说法正确的是( )
a2
A.CH COOH===CHCOO-+H+
3 3
B.HCO 2H++CO
2 3
C.2CN-+ ⥫⥬H
2
O+CO
2
===2HCN+CO
D.25 ℃时,反应CH COOH+CN-⥫⥬ HCN+CH COO-的化学平衡常数数量级为104
3 3
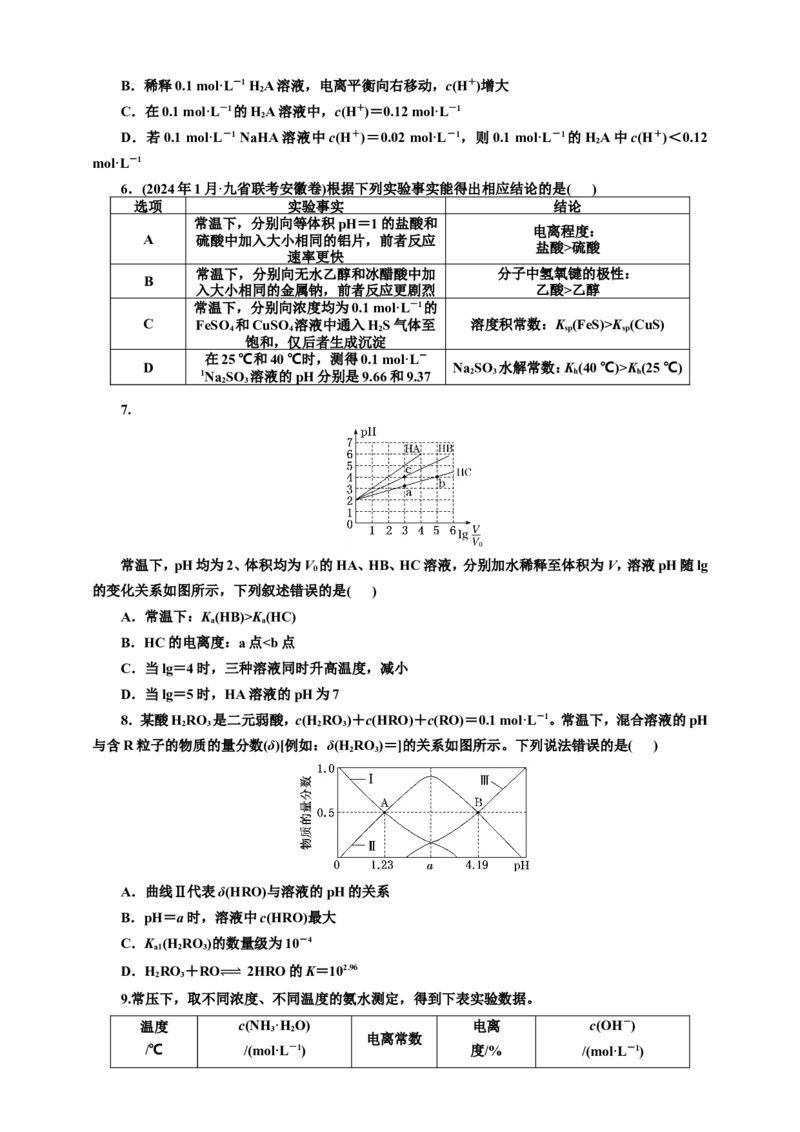
3.
已知物质的电阻率与导电能力成反比,物质的电阻率越大,导电能力越弱。室温条件下,向20 mL
浓度均为0.1 mol·L-1 HA和CH COOH的混合液中滴加0.1 mol·L-1的NH ·HO,测得混合液的电阻
3 3 2
率与加入NH ·HO 的体积(V)的关系如图所示。下列说法错误的是( )
3 2
A.HA是强酸
B.室温条件下,等浓度的HA和CH COOH溶液中c(H+)前者小
3
C.ab段发生的反应是HA+NH ·HO===NHA+HO
3 2 4 2
D.c点溶液中的溶质为NH A和CH COONH
4 3 4
4.25 ℃,HCN溶液中各离子的分布系数δ[如δ(CN-)=]随pH变化的关系如图所示,下列表述正
确的是( )
A.HCN的K 数量级为10-9
a
B.0.1 mol·L-1 NaCN溶液的pH=11.1
C.用标准NaOH溶液滴定未知浓度的HCN溶液时可选用甲基橙试液作指示剂
D.将同体积同浓度的HCN溶液和NaCN溶液混合,所得溶液:c(CN-)>c(HCN)
5.某二元酸(H A)在水中的电离方程式为HA===H++HA-,HA-⥫⥬ H++A2-(25 ℃时,K =
2 2 a
1.0×10-2),下列有关说法正确的是( )
A.HA是弱酸
2B.稀释0.1 mol·L-1 HA溶液,电离平衡向右移动,c(H+)增大
2
C.在0.1 mol·L-1的HA溶液中,c(H+)=0.12 mol·L-1
2
D.若0.1 mol·L-1 NaHA溶液中c(H+)=0.02 mol·L-1,则0.1 mol·L-1的HA中c(H+)<0.12
2
mol·L-1
6.(2024年1月·九省联考安徽卷)根据下列实验事实能得出相应结论的是( )
选项 实验事实 结论
常温下,分别向等体积pH=1的盐酸和
电离程度:
A 硫酸中加入大小相同的铝片,前者反应
盐酸>硫酸
速率更快
常温下,分别向无水乙醇和冰醋酸中加 分子中氢氧键的极性:
B
入大小相同的金属钠,前者反应更剧烈 乙酸>乙醇
常温下,分别向浓度均为0.1 mol·L-1的
C FeSO 和CuSO 溶液中通入HS气体至 溶度积常数:K (FeS)>K (CuS)
4 4 2 sp sp
饱和,仅后者生成沉淀
在25 ℃和40 ℃时,测得0.1 mol·L-
D Na SO 水解常数:K (40 ℃)>K (25 ℃)
1Na SO 溶液的pH分别是9.66和9.37 2 3 h h
2 3
7.
常温下,pH均为2、体积均为V 的HA、HB、HC溶液,分别加水稀释至体积为V,溶液pH随lg
0
的变化关系如图所示,下列叙述错误的是( )
A.常温下:K (HB)>K (HC)
a a
B.HC的电离度:a点10-9.2=K (HCN),CN-的水解大于HCN的电离,则c(CN-)硫酸,A不符合题意;分子中氢氧键的极性越大,越容易电离出氢离子,与钠反应越剧烈,则根据实验事实可得出分子中氢氧键的极性:乙醇>乙酸,B不符合题意;FeSO 和CuSO 组成相似,
4 4
K 越小越容易产生沉淀,则根据选项的实验事实可得出溶度积常数:K (FeS)>K (CuS),C符合题意;
sp sp sp
升高温度,溶液pH减小,不能说明升高温度促进水解使平衡正向移动,则不能得出Na SO 水解常数:
2 3
K (40 ℃)>K (25 ℃),D不符合题意。
h h
7.D A项:由题图可知,HA稀释10倍pH增大1,则HA为强酸,HB、HC稀释10倍,pH增大
值小于1,则HB、HC为弱酸,HB、HC稀释同等倍数,pH的改变值:HB>HC,酸性:HB>HC,常温下,
K (HB)>K (HC),正确;B项:对于HC,b点稀释的倍数大于a点,加水稀释促进弱酸的电离,HC的电
a a
离度:a点c,则a、b、c、
d之间的关系是b>a=d>c。(4)①强酸制弱酸,根据HB(少量)+2A-===B2-+2HA,可知A-、B2-、HB-
2
三种阴离子结合H+由难到易的顺序为HB-、B2-、A-。②铜离子和硫化氢之所以能生成硫化铜沉淀,
是因为硫化铜既难溶于水,又难溶于酸,故能发生该反应。
答案:(1)CD (2)再通入氯气;加入碳酸钙;加入次氯酸钠 (3)b>a=d>c
(4)HB-、B2-、A- 铜离子和硫化氢之所以能生成硫化铜沉淀,是因为硫化铜既难溶于水,又难溶
于酸,故能发生该反应