文档内容
课时检测(四十二) 反应热的相关计算
1.(2024·厦门模拟)关于下列ΔH的判断正确的是( )
CO(aq)+H+(aq)===HCO(aq) ΔH
1
CO(aq)+HO(l) HCO(aq)+OH-(aq) ΔH
2 2
OH-(aq)+H+(aq)=⥫=⥬=H
2
O(l) ΔH
3
OH-(aq)+CH COOH(aq)===CHCOO-(aq)+HO(l) ΔH
3 3 2 4
A.ΔH<0,ΔH<0 B.ΔH<ΔH
1 2 1 2
C.ΔH<0,ΔH>0 D.ΔH>ΔH
3 4 3 4
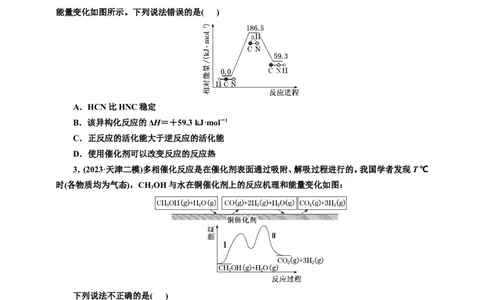
2.(2024·天津模拟)理论研究表明,在101 kPa和298 K下,HCN(g) HNC(g)异构化反应过程的
能量变化如图所示。下列说法错误的是( ) ⥫⥬
A.HCN比HNC稳定
B.该异构化反应的ΔH=+59.3 kJ·mol-1
C.正反应的活化能大于逆反应的活化能
D.使用催化剂可以改变反应的反应热
3.(2023·天津二模)多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T ℃
时(各物质均为气态),CH OH与水在铜催化剂上的反应机理和能量变化如图:
3
下列说法不正确的是( )
A.反应CH OH(g)+HO(g)===CO(g)+3H(g)的ΔS>0
3 2 2 2
B.选择合适的催化剂可降低反应Ⅰ和反应Ⅱ的活化能
C.1 mol CH OH(g)和1 mol H O(g)的总能量大于1 mol CO (g)和3 mol H (g)的总能量
3 2 2 2
D.反应Ⅱ的热化学方程式为
CO(g)+HO(g)===H (g)+CO (g) ΔH<0
2 2 2
4.(2024·烟台高三模拟)N O和CO是环境污染性气体,可在PtO+表面转化为无害气体,其总反
2 2
应为NO(g)+CO(g)===CO(g)+N(g) ΔH,有关化学反应的物质变化过程及能量变化过程分别如图
2 2 2
甲、乙所示。下列说法不正确的是( )A.NO发生还原反应
2
B.ΔH=-226 kJ·mol-1
C.由图乙知该反应正反应的活化能小于逆反应的活化能
D.为了实现转化,需不断向反应器中补充 PtO+和 PtO
2 2
5.(2023·重庆高三二模)火箭发射时可以用液态肼作燃料,NO 作氧化剂。相关物质的能量转化关
2
系如下:
已知 NH(l) NH(g) ΔH=+9.7 kJ·mol-1,则 2NH(l)+2NO (g)===3N (g)+4HO(g)
2 4 2 4 2 4 2 2 2
ΔH( kJ·mol-1⥫)=⥬( )
A.-1 134.4 B.-1 153.8
C.-1 631.7 D.-1 054.4
6.利用含硫物质的热化学循环实现太阳能的转化与存储的过程如图所示,下列说法错误的是(
)
已知:
反应Ⅰ.2HSO (l)===2SO(g)+2HO(g)+O(g) ΔH=a kJ·mol-1
2 4 2 2 2 1
反应Ⅲ.S(s)+O(g)===SO(g) ΔH=b kJ·mol-1
2 2 3
A.反应Ⅰ中反应物的总能量小于生成物的总能量
B.反应Ⅱ的热化学方程式为
3SO (g)+2HO(g)===2H SO (l)+S(s) ΔH=(-a-b)kJ·mol-1
2 2 2 4 2
C.用S(g)替代反应Ⅲ中的S(s),反应焓变为ΔH,则ΔH<ΔH
4 3 4
D.上述循环过程中至少涉及4种能量转化形式
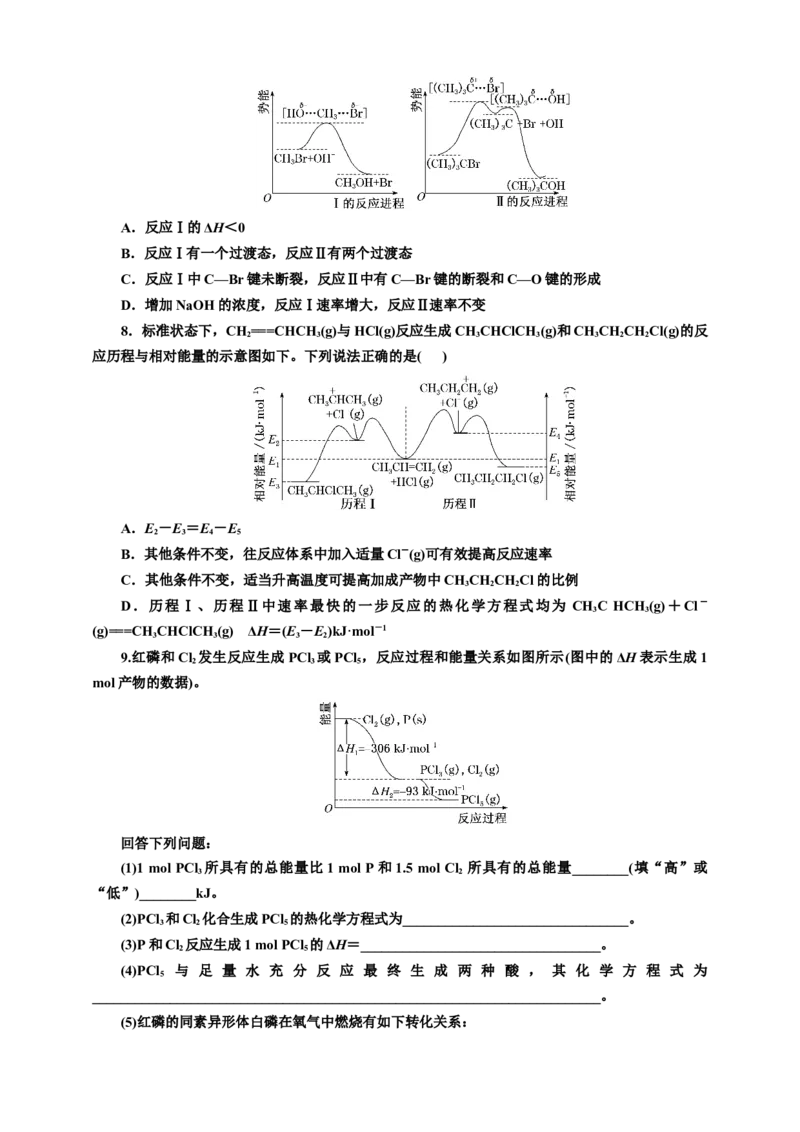
7.如图分别代表溴甲烷和三级溴丁烷发生水解的反应历程。下列说法不正确的是( )
Ⅰ.CHBr+NaOH―→CH OH+NaBr
3 3
Ⅱ.(CH)CBr+NaOH―→(CH)COH+NaBr
3 3 3 3A.反应Ⅰ的ΔH<0
B.反应Ⅰ有一个过渡态,反应Ⅱ有两个过渡态
C.反应Ⅰ中C—Br键未断裂,反应Ⅱ中有C—Br键的断裂和C—O键的形成
D.增加NaOH的浓度,反应Ⅰ速率增大,反应Ⅱ速率不变
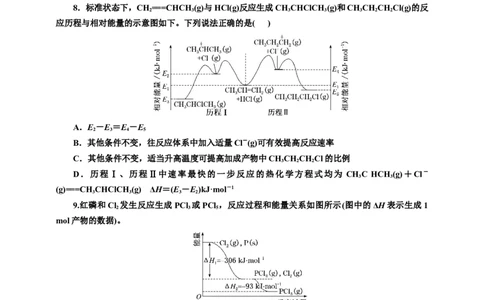
8.标准状态下,CH ===CHCH (g)与HCl(g)反应生成CH CHClCH (g)和CH CH CH Cl(g)的反
2 3 3 3 3 2 2
应历程与相对能量的示意图如下。下列说法正确的是( )
A.E -E =E -E
2 3 4 5
B.其他条件不变,往反应体系中加入适量Cl-(g)可有效提高反应速率
C.其他条件不变,适当升高温度可提高加成产物中CH CH CH Cl的比例
3 2 2
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式均为 CH C HCH (g)+Cl-
3 3
(g)===CHCHClCH (g) ΔH=(E -E )kJ·mol-1
3 3 3 2
9.红磷和Cl 发生反应生成PCl 或PCl ,反应过程和能量关系如图所示(图中的ΔH表示生成1
2 3 5
mol产物的数据)。
回答下列问题:
(1)1 mol PCl 所具有的总能量比1 mol P和1.5 mol Cl 所具有的总能量________(填“高”或
3 2
“低”)________kJ。
(2)PCl 和Cl 化合生成PCl 的热化学方程式为________________________________。
3 2 5
(3)P和Cl 反应生成1 mol PCl 的ΔH=__________________________________。
2 5
(4)PCl 与 足 量 水 充 分 反 应 最 终 生 成 两 种 酸 , 其 化 学 方 程 式 为
5
________________________________________________________________________。
(5)红磷的同素异形体白磷在氧气中燃烧有如下转化关系:其中ΔH=____________(用含ΔH 和ΔH 的代数式表示)。
2 1 3
10.(2024·成都高三模拟)化学反应过程中,不仅有物质的变化,同时还伴随有能量的变化。
(1)已知常温下红磷比白磷稳定,在下列反应中:
①4P(红磷,s)+5O(g)===PO (s) ΔH=-Q kJ·mol-1
2 4 10 1
②P(白磷,s)+5O(g)===PO (s) ΔH=-Q kJ·mol-1
4 2 4 10 2
若Q、Q 均大于零,则Q 和Q 的关系为________(填字母)。
1 2 1 2
A.Q<Q B.Q=Q
1 2 1 2
C.Q>Q D.无法确定
1 2
(2)已知拆开1 mol HCl分子中的化学键需要消耗431 kJ能量,根据下面的能量图回答下列问题:
分别写出③④的数值:________、________。
(3)火箭推进器中装有强还原剂肼(N H)和强氧化剂(H O),当它们混合时,即产生大量的N 和水
2 4 2 2 2
蒸气,并放出大量的热。已知64 g液态肼和足量HO 反应生成氮气和水蒸气放出Q kJ的热量,写出
2 2 3
该反应的热化学方程式:________________________________
________________________________________________________________________。
(4)已知在常温常压下:
2CH OH(l)+3O(g)===2CO(g)+4HO(g) ΔH=-1 275.6 kJ·mol-1
3 2 2 2
HO(l)===H O(g) ΔH=+44.0 kJ·mol-1
2 2
写出表示甲醇燃烧热的热化学方程式:____________________________________
________________________________________________________________________。
(5)已知:N(g)+O(g)===2NO(g) ΔH=+180.5 kJ·mol-1
2 2 1
C(s)+O(g)===CO(g) ΔH=-393.5 kJ·mol-1
2 2 2
2C(s)+O(g)===2CO(g) ΔH=-221.0 kJ·mol-1
2 3
若 某 反 应 的 平 衡 常 数 表 达 式 为 K = , 请 写 出 此 反 应 的 热 化 学 方 程 式 :
________________________________________________________________________。
11.(1)航天员呼吸产生的CO 利用Bosch反应:CO (g)+2H(g) C(s)+2HO(g) ΔH,再电解水
2 2 2 2
可实现O 的循环利用。热力学中规定由最稳定单质生成1 mol某⥫物⥬质的焓变称为该物质的标准生成
2
焓(符号:ΔH),最稳定单质的标准生成焓规定为0。已知上述反应式中:ΔH(CO)=-394 kJ·mol-1,
f f 2
ΔH(H )=0 kJ·mol-1,ΔH(C)=0 kJ·mol-1,ΔH(H O)=-242 kJ·mol-1,则ΔH=________kJ·mol-1。
f 2 f f 2
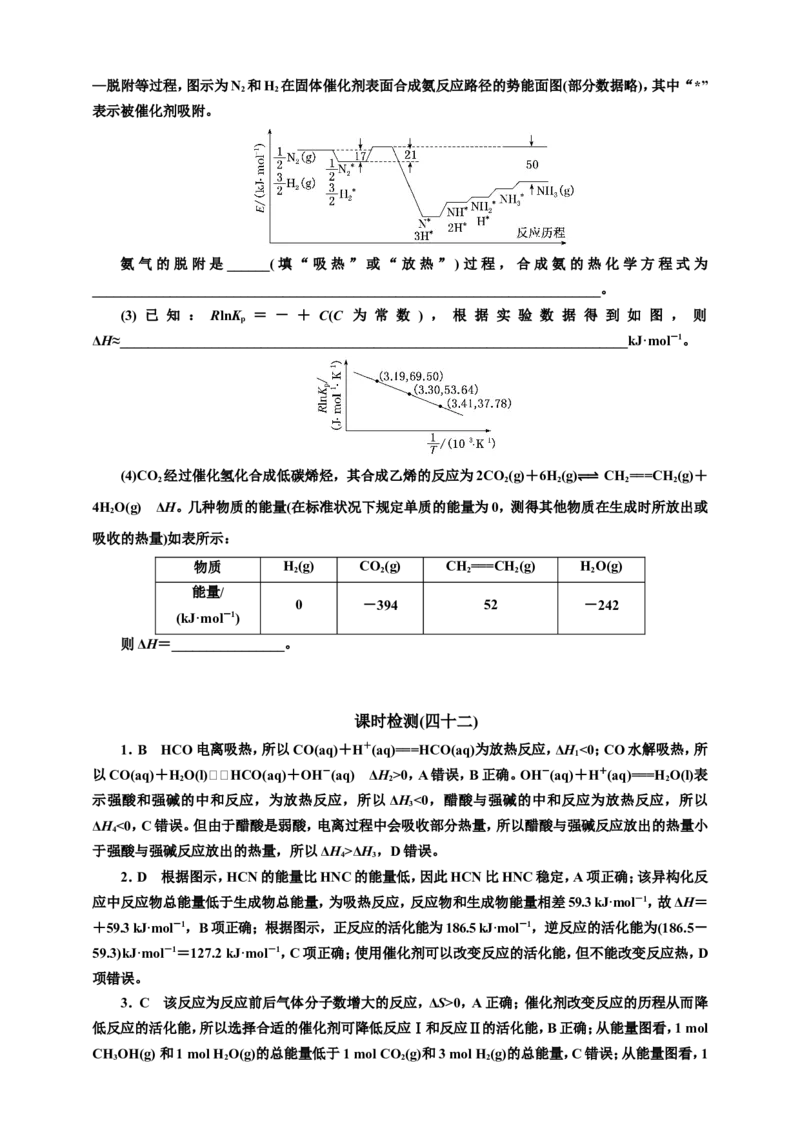
(2)目前HaberBosch法是工业合成氨的主要方式,其生产条件需要高温高压。为了有效降低能耗,
过渡金属催化还原氮气合成氨被认为是具有巨大前景的替代方法。催化过程一般有吸附—解离—反应—脱附等过程,图示为N 和H 在固体催化剂表面合成氨反应路径的势能面图(部分数据略),其中“*”
2 2
表示被催化剂吸附。
氨气的脱附是______(填“吸热”或“放热”)过程,合成氨的热化学方程式为
________________________________________________________________________。
(3) 已 知 : RlnK = - + C(C 为 常 数 ) , 根 据 实 验 数 据 得 到 如 图 , 则
p
ΔH≈________________________________________________________________________kJ·mol-1。
(4)CO 经过催化氢化合成低碳烯烃,其合成乙烯的反应为2CO (g)+6H(g) CH ===CH(g)+
2 2 2 2 2
4HO(g) ΔH。几种物质的能量(在标准状况下规定单质的能量为0,测得其他物⥫质⥬在生成时所放出或
2
吸收的热量)如表所示:
物质 H(g) CO (g) CH ===CH(g) HO(g)
2 2 2 2 2
能量/
0 -394 52 -242
(kJ·mol-1)
则ΔH=________________。
课时检测(四十二)
1.B HCO电离吸热,所以CO(aq)+H+(aq)===HCO(aq)为放热反应,ΔH<0;CO水解吸热,所
1
以CO(aq)+HO(l)HCO(aq)+OH-(aq) ΔH>0,A错误,B正确。OH-(aq)+H+(aq)===H O(l)表
2 2 2
示强酸和强碱的中和反应,为放热反应,所以ΔH<0,醋酸与强碱的中和反应为放热反应,所以
3
ΔH<0,C错误。但由于醋酸是弱酸,电离过程中会吸收部分热量,所以醋酸与强碱反应放出的热量小
4
于强酸与强碱反应放出的热量,所以ΔH>ΔH,D错误。
4 3
2.D 根据图示,HCN的能量比HNC的能量低,因此HCN比HNC稳定,A项正确;该异构化反
应中反应物总能量低于生成物总能量,为吸热反应,反应物和生成物能量相差59.3 kJ·mol-1,故ΔH=
+59.3 kJ·mol-1,B项正确;根据图示,正反应的活化能为186.5 kJ·mol-1,逆反应的活化能为(186.5-
59.3)kJ·mol-1=127.2 kJ·mol-1,C项正确;使用催化剂可以改变反应的活化能,但不能改变反应热,D
项错误。
3.C 该反应为反应前后气体分子数增大的反应,ΔS>0,A正确;催化剂改变反应的历程从而降
低反应的活化能,所以选择合适的催化剂可降低反应Ⅰ和反应Ⅱ的活化能,B正确;从能量图看,1 mol
CH OH(g) 和1 mol H O(g)的总能量低于1 mol CO (g)和3 mol H (g)的总能量,C错误;从能量图看,1
3 2 2 2mol CO(g)和1 mol H O(g)的总能量高于1 mol H (g)和1 mol CO (g),所以反应Ⅱ为放热反应,ΔH<0,
2 2 2
D正确。
4.D 反应NO+CO===CO+N 中,N元素化合价降低,NO为氧化剂,发生还原反应,故A正
2 2 2 2
确;反应物能量高于生成物,反应为放热反应,反应焓变 ΔH=134 kJ·mol-1-360 kJ·mol-1=-226
kJ·mol-1,故B正确;由题图乙知该反应正反应的活化能E 小于逆反应的活化能E ,故C正确;PtO+
a b 2
和PtO是催化剂,催化剂在化学反应的前后化学性质和质量是不变的,无需不断补充,故D错误。
2
5.A 根据图示信息和已知信息,可得反应:
①N(g)+O(g)===NO(g) ΔH=+33.2 kJ·mol-1;
2 2 2
②O(g)+NH(g)===N (g)+2HO(g) ΔH=-543.7 kJ·mol-1;
2 2 4 2 2
③NH(l)N H(g) ΔH=+9.7 kJ·mol-1。
2 4 2 4
根据盖斯定律,②×2+③×2-①×2 可得 2NH(l)+2NO (g)===3N (g)+4HO(g) ΔH=-
2 4 2 2 2
543.7×2+9.7×2-33.2×2=-1 134.4 kJ·mol-1。
6.C 反应Ⅰ为在热能作用下HSO 的分解反应,为吸热反应,则反应物的总能量小于生成物的
2 4
总能量,A正确;由盖斯定律可知,-(反应Ⅰ+反应Ⅲ)得反应:3SO (g)+2HO(g)===2H SO (l)+S(s)
2 2 2 4
ΔH=(-a-b)kJ·mol-1,B正确;气态硫单质所具有的能量高于固态硫单质所具有的能量,故用S(g)
2
替代反应Ⅲ中的S(s),反应放热更多,放热焓变为负值,则ΔH>ΔH,C错误;题述循环过程中涉及太
3 4
阳能、热能、化学能、电能等至少4种能量转化形式,D正确。
7.AC 反应Ⅰ中反应物的总能量高于生成物的总能量,为放热反应,ΔH<0,A符合题意;由题
图可知,反应Ⅰ有一个过渡态,反应Ⅱ有两个过渡态,B不符合题意;反应Ⅰ中CH Br转化成CH OH,
3 3
有C—Br键的断裂,反应Ⅱ中(CH)CBr转化成(CH)COH,有C—Br键的断裂和C—O键的形成,C
3 3 3 3
符合题意;反应Ⅱ卤代烃先自身转变为过渡态,然后氢氧根离子与过渡态的烃结合,氢氧化钠不直接
与卤代烃一起转化到活化态,所以增加氢氧化钠的浓度不能使反应Ⅱ速率增大,D不符合题意。
8.C E -E 、E -E 对应二者的反应物、生成物均不同,反应的焓变不同,故E -E ≠E -E ,A
2 3 4 5 2 3 4 5
错误;由图可知,历程Ⅰ、历程Ⅱ的决速步均为第一步,故其他条件不变,往反应体系中加入适量Cl-
(g) 不会提高反应速率,B错误;由题图可知,历程Ⅱ的最大活化能更大,受温度的影响更大,故其他条
件不变,适当升高温度可提高加成产物中CH CH CH Cl的比例,C正确;由题图可知,历程Ⅰ中速率
3 2 2
最快的一步反应的热化学方程式为 CH C HCH (g)+Cl-(g)===CHCHClCH (g) ΔH=(E -
3 3 3 3 3
E )kJ·mol-1,历程Ⅱ中速率最快的一步反应的热化学方程式为 CH CH C H(g)+Cl-
2 3 2 2
(g)===CHCH CH Cl(g) ΔH=(E -E )kJ·mol-1,D错误。
3 2 2 5 4
9.解析:(1)根据图示可得热化学方程式P(s)+Cl (g)===PCl(g) ΔH=-306 kJ·mol-1,故 1 mol
2 3 1
PCl 所具有的总能量比1 mol P和 1.5 mol Cl 所具有的总能量低306 kJ。(2)根据图示可得PCl 和Cl
3 2 3 2
化合生成PCl 的热化学方程式为PCl (g)+Cl (g)===PCl(g) ΔH=-93 kJ·mol-1。(3)由题图可知,P
5 3 2 5
和Cl 分两步反应生成PCl ,故ΔH=-306 kJ·mol-1+(-93 kJ·mol-1)=-399 kJ·mol-1。(4)PCl 与足
2 5 5
量水充分反应最终生成HPO 与HCl两种酸,所以其化学方程式为PCl +4HO===H PO+5HCl。(5)
3 4 5 2 3 4
根据盖斯定律,有ΔH=ΔH+ΔH,所以ΔH=ΔH-ΔH。
3 2 1 2 3 1
答案:(1)低 306
(2)PCl (g)+Cl (g)===PCl(g)ΔH=-93 kJ·mol-1
3 2 5
(3)-399 kJ·mol-1 (4)PCl +4HO===H PO+5HCl
5 2 3 4
(5)ΔH-ΔH
3 110.解析:(1)已知常温下红磷比白磷稳定,说明红磷具有的能量低,则4P(红磷,s)===P(白磷,s)
4
ΔH>0,根据盖斯定律,①-②得到4P(红磷,s)===P(白磷,s) ΔH=Q-Q>0,所以Q>Q。(2)已知拆
4 2 1 2 1
开1 mol HCl分子中的化学键需要消耗431 kJ能量,则合成2 mol HCl分子中的化学键放出能量为
431 kJ×2=862 kJ,由题图可知反应:H(g)+Cl (g)===2HCl(g) ΔH=-183 kJ·mol-1,设反应物断裂
2 2
需要吸收能量为x kJ,有-183 kJ=-862 kJ+x kJ,解得x=679。(3)64 g即2 mol液态肼和足量HO
2 2
反应生成氮气和水蒸气放出Q kJ的热量,则1 mol液态肼与足量HO 反应时放出的热量是0.5Q
3 2 2 3
kJ,热化学方程式为NH(l)+2HO(l)===N (g)+4HO(g) ΔH=-0.5Q kJ·mol-1。(4)将题给热化学
2 4 2 2 2 2 3
方程式依次编号为①②,根据盖斯定律,-②×2得到甲醇燃烧热的热化学方程式为 CH OH(l)+
3
O(g)===CO(g)+2HO(l) ΔH=-725.8 kJ·mol-1。(5)由K=可得该反应为 2NO+2CO===N +
2 2 2 2
2NO ,将题给三个热化学方程式依次编号为①②③,根据盖斯定律,②×2-①-③得到2NO(g)+
2
2CO(g)===N (g)+2CO (g) ΔH=-746.5 kJ·mol-1。
2 2
答案:(1)A (2)679 862 (3)N H(l)+2HO(l)===N (g)+4HO(g) ΔH=-0.5Q kJ·mol-1
2 4 2 2 2 2 3
(4)CHOH(l)+O(g)===CO(g)+2HO(l)
3 2 2 2
ΔH=-725.8 kJ·mol-1
(5)2NO(g)+2CO(g)===N (g)+2CO (g)
2 2
ΔH=-746.5 kJ·mol-1
11.解析:(1)ΔH=ΔH(C)+2ΔH(H O)-ΔH(CO)-2ΔH(H )=0+2×(-242 kJ·mol-1)-(-394
f f 2 f 2 f 2
kJ·mol-1)-0=-90 kJ·mol-1。(2)由势能面图可知,氨气从催化剂上脱离时势能面在升高,为吸热过
程;由题图可知,0.5 mol氮气和1.5 mol 氢气转变成1 mol氨气的反应热为-17 kJ·mol-1+21 kJ·mol
-1-50 kJ·mol-1=-46 kJ·mol-1,则合成氨的热化学方程式为N(g)+3H(g)2NH(g) ΔH=-92
2 2 3
kJ·mol-1。(3)将(3.19,69.50)、(3.30,53.64)代入RlnK =-+C得 69.50=×3.19×10-3+C、53.64=
p
×3.30×10-3+C,联立求解得ΔH≈144.2 kJ·mol-1。(4)反应焓变等于生成物总能量减去反应物总能量,
则该反应的焓变ΔH=52 kJ·mol-1+(-242 kJ·mol-1)×4-(-394 kJ·mol-1)×2-0=-128 kJ·mol-1。
答案:(1)-90 (2)吸热
N(g)+3H(g)2NH(g) ΔH=-92 kJ·mol-1
2 2 3
(3)144.2 kJ·mol-1 (4)-128 kJ·mol-1