文档内容
专题 01 物质及其变化
1.下列回收物属于金属制品的是( )
A.图甲:矿泉水瓶 B.图乙:废弃报刊
C.图丙:易拉罐 D.图丁:旧衣物
2.下列物质的水溶液能导电,且属于电解质的是( )
A.Cu B.CO C.CHOH D.KNO
2 3 3
3.下列物质间的转化,不能通过一步反应实现的是 ( )
A.S→SO B.NaSiO→HSiO C.Fe→FeCl D.CuO→Cu(OH)
2 2 3 2 3 3 2
4.下列属于氧化还原反应,且氧化剂和还原剂为同一种物质的是( )
A.MgO+2HCl=MgCl +H O B.C+H O(g) CO+H
2 2 2 2
C.8NH +6NO 7N+12H O D.2NaO+2H O=4NaOH+O ↑
3 2 2 2 2 2 2 2
5.新型冠状病毒肆虐流行,严重威胁着人类的健康。使用含氯泡腾片【主要成分为二氧化氯(ClO )】
2
可有效杀死病毒。下列关于二氧化氯(ClO )的说法正确的是( )
2
A.ClO 属于有机物 B.ClO 属于酸
2 2
C.ClO 属于盐类 D.ClO 属于氧化物
2 2
6.随着人们对物质组成和性质研究的深入,物质的分类更加多样化。下列有关说法正确的是( )
A.NaO、Al O、Fe O 都是碱性氧化物 B.磁铁矿、盐酸、绿矾都是混合物
2 2 2 3 2 3
C.CHCOOH、NH ·H O、HClO都是弱电解质 D.烧碱、纯碱、熟石灰都是碱
3 3 2
7.分类是科学研究的重要方法,下列物质分类不正确的是( )A.化合物:干冰,冰水混合物,烧碱,小苏打
B.非电解质:乙醇,四氯化碳,氯气,葡萄糖
C.同素异形体:活性炭,C ,石墨烯,金刚石
60
D.混合物:空气,纯净矿泉水,水玻璃,漂白粉
8.向烧杯中加入25mL蒸馏水,加热至沸腾,向沸水中逐滴加入6滴FeCl 饱和溶液。继续加热至液
3
体呈红棕色,停止加热,就制得了Fe(OH) 胶体。下列有关胶体的叙述不正确的是( )
3
A.胶体是一种分散系,属于混合物
B.胶体的本质特征是能发生丁达尔效应
C.胶体分散质粒子直径介于10-9 -10-7m之间
D.利用丁达尔现象是区分胶体和溶液的一种常用方法
9.从物质类别的视角认识物质间的转化关系是学习化学的重要方法之一。单质X经下图所示过程可
转化为含氧酸W。下列说法正确的是( )
X Y Z W
A.X是金属钠 B.Y一定能使品红溶液褪色
C.W的浓溶液见光一定会分解 D.Z中氧元素的质量分数一定高于Y
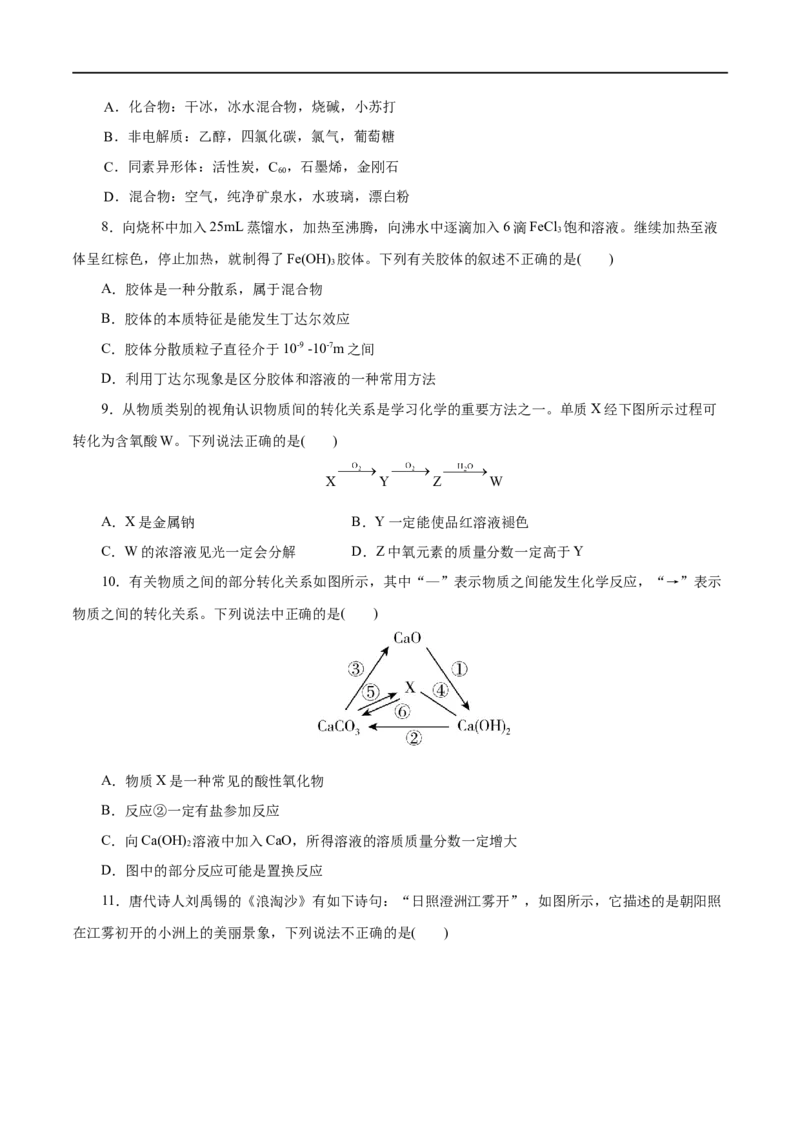
10.有关物质之间的部分转化关系如图所示,其中“—”表示物质之间能发生化学反应,“→”表示
物质之间的转化关系。下列说法中正确的是( )
A.物质X是一种常见的酸性氧化物
B.反应②一定有盐参加反应
C.向Ca(OH) 溶液中加入CaO,所得溶液的溶质质量分数一定增大
2
D.图中的部分反应可能是置换反应
11.唐代诗人刘禹锡的《浪淘沙》有如下诗句:“日照澄洲江雾开”,如图所示,它描述的是朝阳照
在江雾初开的小洲上的美丽景象,下列说法不正确的是( )A.该诗句描述的现象为丁达尔效应
B.胶体的分散质粒子的直径在10-9~10-7m之间
C.以Fe(OH) 为分散质形成的任何分散系都能发生丁达尔效应
3
D.利用该现象可以区分胶体和溶液
12.2021年新冠肺炎疫情夺走了至少330万人的生命,化学在攻克这一世界难题中功不可没,“新型
冠状病毒”由蛋白质外壳和单链核酸组成,直径为60-140 nm,怕酒精,不耐高温。下列说法不正确的是(
)
A.“新型冠状病毒”扩散到空气中不可能形成胶体
B.“新型冠状病毒”扩散到空气中形成的分散系可能具有一定的稳定性
C.蛋白质、酒精属于有机物
D.减少外出、勤通风可有效预防“新型冠状病毒”感染
13.下列离子方程式书写不正确的是( )
A.将石灰乳加入海水沉淀池得到氢氧化镁∶ Ca(OH) +Mg2+=Mg(OH) ↓+Ca2+
2 2
B.用稀KMnO 酸性溶液检验火柴头燃烧产生的气体中含有SO ∶MnO -+SO+4H+=Mn2++SO2-+2H O
4 2 4 2 4 2
C.泡沫灭火器反应原理∶3HCO -+Al3+=3CO ↑+Al(OH) ↓
3 2 3
D.实验室用过量NaOH溶液吸收SO ∶2OH-+SO=SO2-+H O
2 2 3 2
14.下列离子方程式书写正确的是( )
A.FeCl 溶液和Cu混合:FeCl +Cu = Fe2++Cu2+ +3Cl-
3 3
B.甲醛溶液中加入足量的银氨溶液并加热:HCHO+2[Ag(NH )]++2OH﹣ HCOO-+NH+
3 2 4
+2Ag↓+3NH+H O
3 2
C.碳酸氢钠的水解方程式:HCO -+H O CO2-+H O+
3 2 3 3
D.Ca(HCO ) 溶液中加入过量氨水:Ca2++2HCO-+2NH•H O=CaCO ↓+2H O+2NH ++CO 2-
3 2 3 3 2 3 2 4 3
15.下列对应的离子方程式正确的是( )A.酸性高锰酸钾溶液和草酸溶液反应:2 MnO- +16H++5 C O2- ═2Mn2++10CO ↑+8H O
4 2 4 2 2
B.向氯化铁溶液中通入过量二氧化硫:2Fe3++3SO+6H O═2Fe+3SO 2-+12H+
2 2 4
C.银和稀硝酸反应:3Ag+4H++ NO -═3Ag++2H O+NO↑
3 2
D.向氯水中加入碳酸钠:Cl+CO 2-═Cl-+ClO-+CO ↑
2 3 2
16.下列指定反应的离子方程式正确的是( )
A.金属钠投到MgCl 溶液中:2Na+Mg2+=2Na++Mg
2
B.向NaAlO 溶液中滴加NaHCO 溶液产生白色沉淀:AlO-+HCO -+HO=Al(OH) ↓+CO2-
2 3 2 3 2 3 3
C.室温下用稀HNO 溶解铜:Cu+2NO -+2H+=Cu2++2NO ↑+HO
3 3 2 2
D.向NaSiO 溶液中滴加稀盐酸:NaSiO+2H+=HSiO↓+2Na+
2 3 2 3 2 3
17.下列化学(或离子)方程式中,不能正确表达所指定的现象变化的是( )
A.把盛装浓氨水、浓盐酸的两敞口容器靠近,空气中出现“白烟”:NH +H+=NH +
3 4
B.把石灰浆涂抹在墙面上,第二天墙面上“更潮湿”:Ca(OH) +CO=CaCO ↓+HO
2 2 3 2
C.向FeCl 溶液中滴入KSCN溶液,溶液“变红”:Fe3++3SCN-=Fe(SCN)
3 3
D.向AlCl 溶液中投入CuO粉末,溶液中出现“白色沉淀”:3HO+3CuO+2AlCl =2Al(OH) +
3 2 3 3
3CuCl
2
18.下列指定反应的离子方程式正确的是( )
A.用HO 从酸化的海带灰浸出液中提取碘:2I-+HO=I+2OH-
2 2 2 2 2
B.向碳酸氢铵溶液中加入过量的NaOH溶液:NH ++OH-=NH ·H O
4 3 2
C.向明矾溶液中加入Ba(OH) 溶液至生成沉淀的物质的量最多:Al3++2SO 2-+2Ba2++4OH-=
2 4
2BaSO↓+AlO-+2HO
4 2 2
D.等体积、等物质的量浓度的NaHCO 溶液与Ba(OH) 溶液混合:HCO -+Ba2++OH-=BaCO ↓+
3 2 3 3
HO
2
19.制备(NH )Fe(SO )·6H O的实验中,需对过滤出产品的母液(pH<1)进行处理。室温下,分别取母
4 2 4 2 2
液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是( )
A.通入过量Cl:Fe2+、H+、NH +、Cl–、SO 2–
2 4 4
B.加入少量NaClO溶液:NH +、Fe2+、H+、SO 2–、ClO–
4 4
C.加入过量NaOH溶液:Na+、Fe2+、NH +、SO 2–、OH–
4 4
D.加入过量NaClO和NaOH的混合溶液:Na+、SO 2–、Cl–、ClO–、OH–
4
20.常温下,下列各组离子在指定溶液中可能大量共存的是( )
A.无色透明的溶液中:K+、NH +、MnO -、CO2-
4 4 3
B.c(I-)=0.10mol·L-1的溶液中:Al3+、Fe3+、Cl-、NO -
3C.pH=1的溶液中:NH +、Na+、SO 2-、Br-
4 4
D.水电离出的c(H+)=10-13mol·L-1的溶液中:Mg2+、K+、Cl-、HCO -
3
21.下列各组离子在指定溶液中能大量共存的是( )
A.在20 ℃ pH=10的溶液中:Na+、CHCHO、Ag(NH)、NO
3 3
B.溶液中能大量共存,通入CO 后仍能大量共存:K+、Ca2+、Cl-、NO
2
C.与镁反应只产生氢气的溶液中:NO、Cl-、H+、Al3+
D. c(H+)与c(OH-)/c(H+)=1.0×10-12溶液中:Cl-、K+、SO、CHCOO-
3
22.下列各溶液中一定能大量共存的离子组是( )
A.加入铝粉有氢气生成的溶液中:Mg2+、Cu2+、SO、K+
B.使pH试纸呈红色的溶液中:Fe2+、I-、NO、Cl-
C.常温下,c(H+)=10-14 mol·L-1的溶液中:Na+、AlO、S2-、SO
D.常温下,水电离出的c(H+)与c(OH-)乘积为10-28的溶液中:K+、Na+、HCO、Ca2+
23.室温下,下列各组离子能大量共存的是( )
A.pH=7的溶液中:Fe3+、Mg2+、SO、Cl-
B.NaHS溶液中:SO、K+、Cl-、Cu2+
C.K /c(H+)=10-13 mol·L-1的溶液中:NH、Mg2+、SO
w
D.通入大量CO 的溶液中:Na+、ClO-、CHCOO-、HCO
2 3
24.下列离子方程式的书写及评价均合理的是( )
选项 离子方程式 评价
将2 mol Cl 通入到含1 mol FeI 的溶液中:2Fe2++ 正确;Cl 过量,可将Fe2+、I-
2 2 2
A
2I-+2Cl===2Fe3++4Cl-+I 均氧化
2 2
Mg(HCO ) 溶液与足量的NaOH溶液反应:Mg2+ 正确;酸式盐与碱反应生成正盐
3 2
B
+HCO+OH-===MgCO↓+HO 和水
3 2
过量SO 通入到NaClO溶液中:SO +HO+ClO- 正确;说明酸性:HSO 强于
2 2 2 2 3
C
===HClO+HSO HClO
1 mol/L的NaAlO 溶液和2.5 mol/L的HCl溶液
2
正确;AlO与Al(OH) 消耗的H+
3
D 等体积互相均匀混合:2AlO+5H+===Al3++
的物质的量之比为2∶3
Al(OH) ↓+HO
3 2
25.关于微粒在指定溶液中能否大量共存的评价正确的是( )
选项 溶液 微粒 评价
A 8% H O 水溶液 Fe3+、Mg2+、SO、Na+ 可以大量共存
2 2
NO能将SO氧化而不能大
B 室温下pH=12的水溶液 NO、Na+、SO、K+
量共存
NH Cl溶液显酸性,
4
C 1 mol·L-1的NH Cl溶液 Ba2+、OH-、NH ·H O
4 3 2
NH ·H O不能大量共存
3 2
D NaHSO 水溶液 I-、K+、CHCOO-、Br- CHCOO-能与
4 3 3NaHSO 溶液反应,不能
4
大量共存
26.下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是( )
物质(括号内为杂质) 除杂试剂
A FeCl 溶液(FeCl ) Fe粉
2 3
B NaCl溶液(MgCl ) NaOH溶液、稀HCl
2
C Cl(HCl) HO、浓HSO
2 2 2 4
D NO(NO ) HO、无水CaCl
2 2 2
27.Cl 是纺织工业中常用的漂白剂,NaSO 可作漂白布匹后的“脱氯剂”,SO2-和Cl 反应的产物
2 2 2 3 2 3 2
之一为SO 2-。下列说法中不正确的是( )
4
A.该反应中Cl 发生还原反应
2
B.根据该反应可判断还原性:SO2->Cl-
2 3
C.脱氯反应后,溶液的酸性增强
D.SO 与氯气的漂白原理相同,所以也可以用SO 作纺织工业的漂白剂
2 2
28.已知HSO +I+HO===H SO +2HI,将0.1 mol Cl 通入100 mL含等物质的量的HI与HSO 的混
2 3 2 2 2 4 2 2 3
合溶液中,有一半的HI被氧化,则下列说法正确的是( )
A.物质的还原性:HI>HSO >HCl
2 3
B.HSO 的物质的量浓度为0.6 mol·L-1
2 3
C.若再通入0.05 mol Cl ,则恰好能将HI和HSO 完全氧化
2 2 3
D.通入0.1 mol Cl 发生反应的离子方程式为5Cl+4HSO +2I-+4HO===4SO+I+10Cl-+16H+
2 2 2 3 2 2
29.向CuSO 溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,溶液变为棕色。再向反应后
4
的混合物中不断通入SO 气体,溶液逐渐变成无色。下列分析正确的是( )
2
A.上述实验条件下,物质的氧化性:Cu2+>I >SO
2 2
B.通入SO 时,SO 与I 反应,I 作还原剂
2 2 2 2
C.通入SO 后溶液逐渐变成无色,体现了SO 的漂白性
2 2
D.滴加KI溶液时,转移2 mol e-时生成1 mol白色沉淀
30.某电镀厂废水中含有酸性重铬酸钾(K Cr O)溶液,己知Cr(VI)毒性是Cr(III)的100倍,现用硫酸
2 2 7
亚铁溶液(恰好完全反应)还原该废水,然后再调节pH为6~8,使Cr(III)转化为沉淀除去。下列说法正确的
是( )
A.KCr O 溶液中Cr O2-部分转化为铬酸根,铬元素价态发生变化
2 2 7 2 7
B.还原性:Cr3+>Fe2+
C.上述除铬过程中,溶液中pH先减小后增大D.除污完成后生成42.4kg沉淀,则还原过程中转移电子的物质的量为300mol
31.用高铁酸钠(Na FeO)对河湖水消毒是城市饮水处理的新技术。已知反应 Fe O +
2 4 2 3
3NaO=====2NaFeO+NaO,下列说法正确的是( )
2 2 2 4 2
A.NaO 既是氧化剂又是还原剂
2 2
B.3 mol Na O 发生反应,有12 mol电子转移
2 2
C.在NaFeO 中Fe为+4价,具有强氧化性,能消毒杀菌
2 4
D.NaFeO 既是氧化产物又是还原产物
2 4
32.NaNO 是一种食品添加剂,它能致癌。酸性KMnO 溶液与NaNO 反应的化学方程式是:MnO+
2 4 2
NO+→Mn2++NO+HO。下列叙述中正确的是( )
2
A.该反应中NO被还原
B.反应过程中溶液的pH减小
C.生成1 mol NaNO 需消耗0.4 mol KMnO
3 4
D.中的粒子是OH-
33.含有砒霜(As O)的试样和锌、盐酸混合反应,生成的砷化氢(AsH)在热玻璃管中完全分解成单质
2 3 3
砷和氢气。若砷的质量为1.50 mg,则下列说法正确的是( )
A.被氧化的砒霜为1.98 mg B.分解产生的氢气为0.672 mL
C.和砒霜反应的锌为3.90 mg D.转移的电子总数为6×10-5N
A
34.将11.2 g的Mg、Cu混合物完全溶解于足量的硝酸中,收集反应产生的X气体。再向所得溶液中
加入足量的NaOH溶液,产生21.4 g沉淀。根据题意推断气体X的成分可能是( )
A.0.6 mol NO
B.0.1 mol NO、0.2 mol NO 和0.05 mol NO
2 2 4
C.0.2 mol NO 和0.1 mol NO
2 2 4
D.0.3 mol NO 和0.3 mol NO
2
35.已知溶液中可发生反应:2FeBr +Br ===2FeBr ,现向100 mL的FeBr 溶液中通入3.36 L Cl (标准
2 2 3 2 2
状况),充分反应后测得溶液中Cl-和Br-的物质的量浓度相等,则原FeBr 溶液的物质的量浓度为( )
2
A.2 mol·L-1 B.1 mol·L-1 C.0.4 mol·L-1 D.0.2 mol·L-1
36.高铁酸钾是一种新型、高效、多功能水处理剂,工业上采用向KOH溶液中通入氯气,然后再加
入Fe(NO ) 溶液的方法制备KFeO,发生反应:
3 3 2 4
①C1 +KOH→KC1+KC1O+KC1O +H O(未配平);
2 3 2
②2Fe(NO )+3KC1O+10KOH===2K FeO+6KNO +3KC1+5H O。
3 3 2 4 3 2
下列说法正确的是( )
A.若反应①中n(ClO-):n(C1O-)=5:1,则氧化剂与还原剂的物质的量之比为2:1
3
B.反应①中每消耗4molKOH,吸收标准状况下22.4LCl
2
C.氧化性:KFeO>KC1O
2 4D.若反应①的氧化产物只有KC1O,则得到0.2molKFeO 时消耗0.3molC1
2 4 2