文档内容
专题 03 离子反应方程式和离子共存
(本卷共19小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5
第I卷 (选择题共50分)
一、选择题:本题共10个小题,每小题3分,共30分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.下列离子方程式书写正确的是
A.NaSO 溶液在空气中易被氧化:SO +O =SO
2 3 2
B.酸性高锰酸钾溶液与稀草酸反应:5C O +2MnO +16H+=2Mn2++10CO↑+8HO
2 2 2
C.AgNO 的溶液中滴加NaCl溶液:Ag++Cl-=AgCl↓
3
D.NH HCO 溶液加入过量NaOH溶液加热:NH +OH-=NH·H O
4 3 3 2
2.常温下,下列各组离子在指定溶液中能大量共存的是
①使甲基橙变红色的溶液: 、 、 、
②由水电离出的 的溶液中: 、 、 、
③无色溶液中: 、 、
④0.1 溶液: 、 、 、
⑤在 的溶液中: 、 、 、
A.②⑤ B.①②⑤ C.②④ D.②③⑤
3.下列指定反应的离子方程式正确的是是
A.氯化铁溶液腐蚀铜箔制印刷电路板:2Fe3++3Cu=2Fe+3Cu2+
B.浓硝酸与过量铁粉:Fe+6H++3 =Fe3++3NO↑+3H O
2 2
C.酸性高锰酸钾溶液与过氧化氢溶液:2 +5H O+6H+=2Mn2++5O ↑+8H O
2 2 2 2D.过量碳酸氢钙溶液与澄清石灰水:2 +Ca2++2OH-=CaCO ↓+ +2H O
3 2
4.常温下,下列各组离子在指定溶液中能大量共存的是
A.pH=12的无色溶液:Na+、K+、 、
B.0.1mol·L-1氨水:Na+、K+、OH-、
C.5%H O 溶液: 、Na+、 、
2 2
D.0.1mol·L-1盐酸:Na+、K+、 、
5.下列反应的离子方程式中正确的是
A.向 溶液中通入 气体:
B.碳酸钡加入稀硫酸:
C.向碳酸氢钙溶液中加入过量氢氧化钠:
D.等物质的量的 、 和 溶液混合:
6.下列实验对应的离子方程式不正确的是
A.将碳酸氢钙溶液与过量的澄清石灰水混合:
B.将 通入冷的NaOH溶液:
C.在饱和 溶液中通入过量 后有晶体析出:
D.向氨水中滴入少量硝酸银溶液:
7.常温下,下列各组离子在指定溶液中一定能大量共存的是
A.在新制饱和氯水中: 、 、 、
B.在能使红色石蕊试纸变蓝的溶液中: 、 、 、
C.在加入铝粉能产生 的溶液中: 、 、 、D.在 的溶液中: 、 、 、
8.对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
选项 粒子组 判断和分析
、 、 、
A 能大量共存,粒子间不反应
不能大量共存,因只发生反应:
B
、 、 、
C 、 、 、 能大量共存,粒子间不反应
D
、 、 、 不能大量共存,因发生反应:
9.下列过程中的化学反应,相应的离子方程式书写正确的是
A.用足量氨水吸收SO :
2
B.硫酸酸化的淀粉碘化钾溶液久置后变蓝:2I—+O +4H+=I +2H O
2 2 2
C.向 溶液中滴加 溶液至混合溶液恰好为中性:
D.向含氯化铁的氯化镁溶液中加入氧化镁:2Fe3++3MgO+3HO=2Fe(OH) ↓+3Mg2+
2 3
10.加入(NH )Fe(SO )•6H O晶体后仍能大量存在的离子组是
4 2 4 2 2
A.Na+、H+、Cl-、NO B.Na+、Mg2+、Cl-、SO
C.K+、Ba2+、OH-、I- D.Na+、S2-、Br-、ClO-
二、选择题:本题共5个小题,每小题4分,共20分。在每小题给出的四个选项中,只有一项或两项是
符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只选一个
且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
11.下列离子方程式正确的是
A.向含 的 溶液中加入适量 :
B.向 溶液中加入过量氨水:
C. 加入足量稀硝酸中:
D.向漂白粉溶液中通入过量的SO :ClO-+SO +HO= +HClO
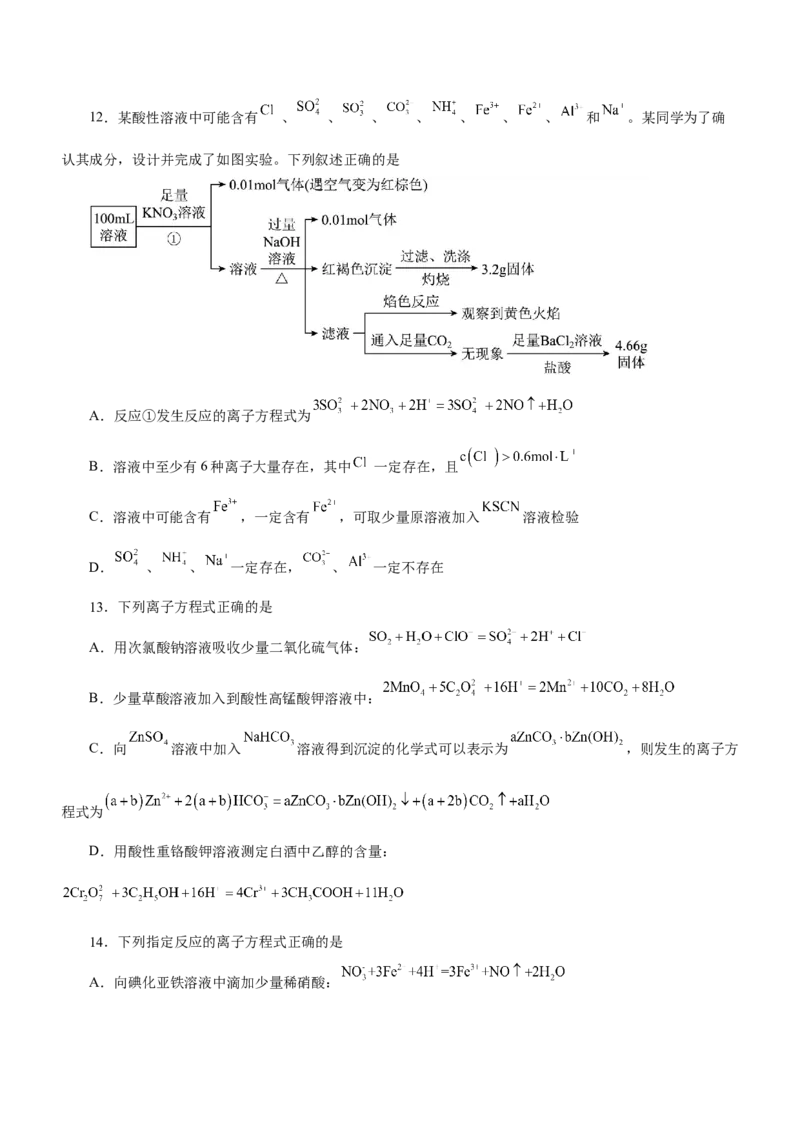
2 2 212.某酸性溶液中可能含有 、 、 、 、 、 、 、 和 。某同学为了确
认其成分,设计并完成了如图实验。下列叙述正确的是
A.反应①发生反应的离子方程式为
B.溶液中至少有6种离子大量存在,其中 一定存在,且
C.溶液中可能含有 ,一定含有 ,可取少量原溶液加入 溶液检验
D. 、 、 一定存在, 、 一定不存在
13.下列离子方程式正确的是
A.用次氯酸钠溶液吸收少量二氧化硫气体:
B.少量草酸溶液加入到酸性高锰酸钾溶液中:
C.向 溶液中加入 溶液得到沉淀的化学式可以表示为 ,则发生的离子方
程式为
D.用酸性重铬酸钾溶液测定白酒中乙醇的含量:
14.下列指定反应的离子方程式正确的是
A.向碘化亚铁溶液中滴加少量稀硝酸:B.用NaClO溶液吸收少量 :
C. 溶液中加足量的烧碱溶液:
D. 溶液中滴加 溶液至 恰好沉淀完全:
15.下列方程式书写正确的是
A.硝酸铁溶液中加入少量碘化氢:
B.偏铝酸钠溶液和碳酸氢钠溶液反应:
C.饱和 溶液中通入过量 :
D.在复盐 溶液中逐滴加入 溶液,可能发生反应:
第II卷 (非选择题共50分)
三、非选择题:本题共4个小题,共50分。
16.(10分)由下表中离子组成的五种可溶性物质A、B、C、D、E(组成该五种物质的阴、阳离子均不
相同),其中A、B、C是盐,且只有C中阴、阳离子数目之比为1:1,D是酸,E是碱,B的溶液与D的溶液
反应有气体生成。
阴离子
、 、 、 、
阳离子 、 、 、 、
(1)A、B、C的化学式依次为_______、_______、_______。
(2)D的溶液与E的溶液反应可生成白色沉淀,则二者反应的离子方程式为_______。
(3)可用试剂F鉴别A、B、C,则F的化学式为_______。
17.(11分)某溶液可能含有Na+、K+、Mg2+、Cu2+等阳离子及MnO 、SiO 、AlO 、CO 、SO 、
Cl-等阴离子,已知:①该溶液呈无色;②经测定溶液的pH=12;③取少量溶液,加入100 mL 2 mol/L足量稀盐酸进行酸化,有白色沉淀生成,还得到一种无色无味的气体,该气体使足量的澄清石灰水变浑浊。对酸化后
的溶液过滤,得到滤液甲。
(1)由①②③可判断:原溶液中一定不存在的离子是_______,一定存在的离子是_______。
(2)将滤液甲分成两等份,一份中逐滴加入氨水有白色胶状沉淀产生,说明原溶液中一定有_______(填离子
符号),写出生成沉淀的离子方程式为_______;另一份中加入足量的Ba(NO ) 溶液,有白色沉淀生成,说明原
3 2
溶液中一定有_______(填离子符号),过滤得到滤液乙。
(3)往滤液乙中加入足量的AgNO 溶液,过滤、洗涤、干燥得固体26.5 g,则原溶液中是否有Cl-
3
_______(填“是”或“否”)。
18.(15分)某化学兴趣小组对仅含下表中某些离子的工业废水进行研究,该废水呈无色,废水中各种
离子的物质的量浓度相等,均为 (忽略水的电离、离子的水解)。
阳离子
、 、 、 、 、 、 、
阴离子
、 、 、 、
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.取废水5 mL,滴加几滴稀氨水有沉淀生成,且溶液中离子种类增加。
Ⅱ.用铂丝蘸取废水,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰。
Ⅲ.另取废水少许,加入过量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
Ⅳ.将Ⅲ中所得溶液分成两份,一份滴入KSCN溶液,溶液不变红;另一份加入 溶液,有白色沉淀生
成。
回答下列问题:
(1)该废水中一定存在的阳离子是_______,一定存在的阴离子是_______。
(2)该废水与过量的NaOH溶液反应,产生的沉淀是_______(填化学式)。
(3)Ⅲ中加入盐酸生成无色气体的离子方程式是_______。
(4)若向Ⅲ中所得的溶液中加入过量 溶液,充分反应后过滤;然后向所得滤液中加入 溶
液,观察到有白色沉淀生成。
①该白色沉淀是_______(填化学式)。
②仅根据此实验现象,_______(填“能”或“不能”)说明该废水中一定存在该白色沉淀中的阴离子,其
原因是_______。
(5)乙同学取200 mL该工业废水,向其中加入足量的氨水,充分反应后过滤、洗涤、灼烧沉淀至恒重,得到的固体质量为_______g(保留2位小数)。
19.(14分)Ⅰ.某废水中可能含有下列离子中的若干种:Fe3+、Al3+、Fe2+、Cu2+、Cl-、CO 、NO 、SO
、SiO 。现进行如下实验:
Ⅰ.取少量溶液,加入KSCN溶液,无明显变化
Ⅱ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色
Ⅲ.向Ⅱ中所得溶液中加入BaCl 溶液,有白色沉淀生成
2
Ⅳ.向Ⅱ中所得溶液中加入过量浓氨水,仅有红褐色沉淀生成,过滤,在所得溶液中加入盐酸至酸性时,
再加入氢氧化钠溶液,有蓝色沉淀生成
请回答下列问题:
(1)该废水一定含有的离子是_______;
(2)实验Ⅱ中加入盐酸生成无色气体的离子方程式是_______;
(3)过滤除去Ⅳ中的蓝色沉淀,调整溶液的pH为10.7左右时,加入铝粉,反应产生氨气和氮气的体积比为
1:4,其离子方程式为Al+NO +OH- AlO +NH+N +H O(未配平)。若除去0.2molNO ,消耗铝
3 2 2
_______g。
Ⅱ.某混合液中,可能大量含有的离子如下:
阳离子:H+、K+、Al3+、NH 、Mg2+阴离子:Cl-、Br-、OH-、CO 、AlO
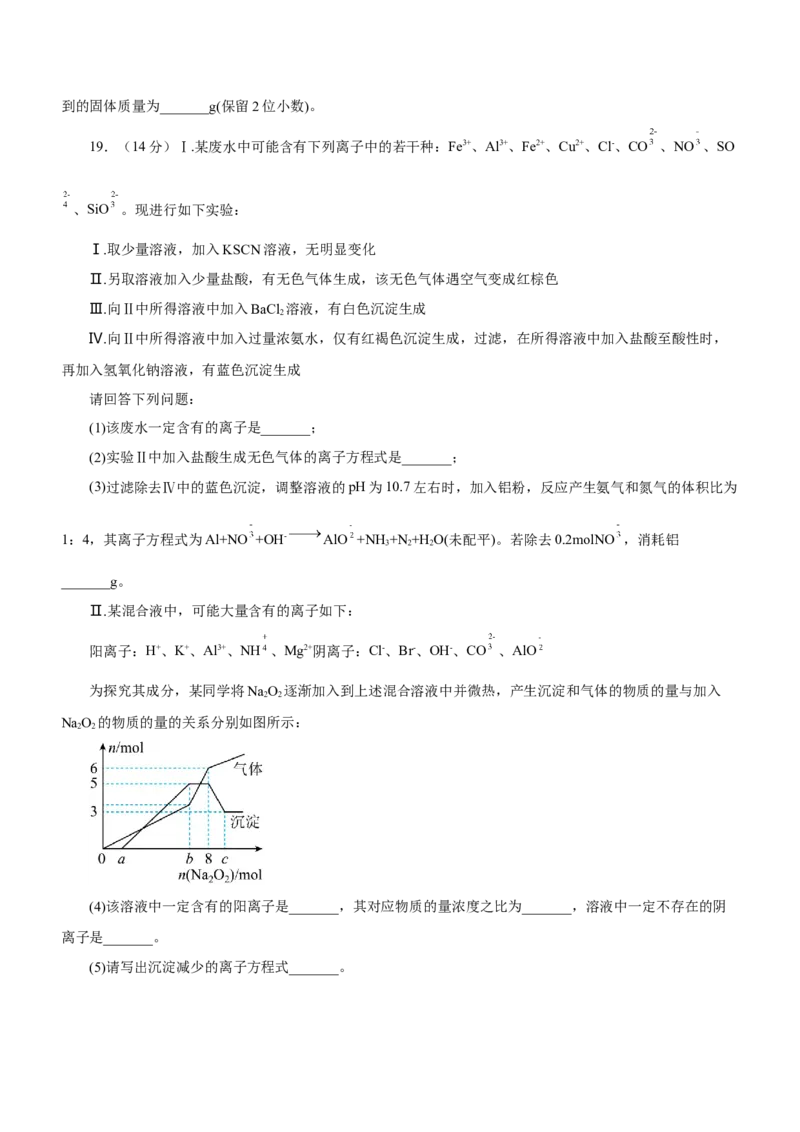
为探究其成分,某同学将NaO 逐渐加入到上述混合溶液中并微热,产生沉淀和气体的物质的量与加入
2 2
NaO 的物质的量的关系分别如图所示:
2 2
(4)该溶液中一定含有的阳离子是_______,其对应物质的量浓度之比为_______,溶液中一定不存在的阴
离子是_______。
(5)请写出沉淀减少的离子方程式_______。