文档内容
专题03 离子反应
2021年化学高考题
一、单选题
1.(2021·浙江高考真题)不能正确表示下列变化的离子方程式是
CO22H=CO H O
A.碳酸镁与稀盐酸反应: 3 2 2
HSOH O H SO OH
B.亚硫酸氢钠的水解: 3 2 2 3
Zn2OH2H O=Zn(OH) 2 H
C.锌溶于氢氧化钠溶液: 2 4 2
NONH N 2H O
D.亚硝酸钠与氯化铵溶液受热反应: 2 4 2 2
【KS5U答案】A
【详解】
A.碳酸镁与稀盐酸反应生成氯化镁、二氧化碳和水,反应的离子方程式为MgCO+2H+=Mg2+
3
+HO+CO↑,故A错误;
2 2
B.亚硫酸氢钠是弱酸的酸式盐,在溶液中水解生成亚硫酸和氢氧化钠,水解的离子方程式
为HSO3+HO HSO+OH-,故B正确;
2 2 3
C.锌与氢氧化钠溶液反应生成偏锌酸钠和氢气,反应的离子方程式为Zn+2OH-
+2HO=[Zn(OH)]-+H↑,故C正确;
2 4 2
D.亚硝酸钠溶液与氯化铵溶液共热反应生成氯化钠、氮气和水,反应的离子方程式为NO2
Δ
+NH4 N↑+2HO,故D正确;
2 2
故选A。
2.(2021·浙江高考真题)下列物质属于弱电解质的是
A.CO B.HO C.HNO D.NaOH
2 2 3
【KS5U答案】B
【分析】
在水溶液中或熔融状态下不能够完全电离的电解质叫做若电解质。
【详解】A.CO 在水溶液中或熔融状态下不能够电离,为非电解质,A不符合题意;
2
B.HO在水溶液中或熔融状态下能够部分电离,为弱电解质,B符合题意;
2
C.HNO 为一种强酸,在水溶液中或熔融状态下能够完全电离,为强电解质,C不符合题意;
3
D.NaOH为一种强碱,在水溶液中或熔融状态下能够完全电离,为强电解质,D不符合题意;
故答案选B。
3.(2021·广东)宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应
的反应方程式书写正确的是
Na O Na O H O2NaOHO
A. 2 2放入水中: 2 2 2 2
H O(g) 3H O2FeFe O 3H
B. 2 通过灼热铁粉: 2 2 3 2
CuH SO CuSO H
C.铜丝插入热的浓硫酸中: 2 4 4 2
SO KMnO 5SO 2H O2MnO 5SO2 4H 2Mn2
D. 2通入酸性 4溶液中: 2 2 4 4
【KS5U答案】D
【详解】
Na O 2Na O 2H O4NaOHO
A. 2 2放入水中化学方程式应该是: 2 2 2 2 ,A选项中氧元素不
守恒,A错误;
H O(g)
B. 2 通过灼热铁粉应高温条件下生成四氧化三铁和氢气,B错误;
C.铜丝插入热的浓硫酸中生成的气体不是氢气,应是二氧化硫,C错误;
D.
SO
2通入酸性
KMnO
4溶液中,
SO
2被
MnO-
4氧化为
SO2
4
-
,
MnO-
4被
SO
2还原为
Mn2+
,再根
据得失电子守恒、电荷守恒和元素守恒可得离子方程式为
5SO 2H O2MnO 5SO2 4H 2Mn2
2 2 4 4 ,D正确;
故选D。
4.(2021·全国高考真题)下列过程中的化学反应,相应的离子方程式正确的是
CO2CaSO CaCO SO2
A.用碳酸钠溶液处理水垢中的硫酸钙: 3 4 3 4
Fe4H NO Fe3 NO2H O
B.过量铁粉加入稀硝酸中: 3 2Al3 4OH AlO 2H O
C.硫酸铝溶液中滴加少量氢氧化钾溶液: 2 2
Cu2 S2 CuS
D.氯化铜溶液中通入硫化氢:
【KS5U答案】A
【详解】
A.硫酸钙微溶,用碳酸钠溶液处理水垢中的硫酸钙转化为难溶的碳酸钙,离子方程式为:C
O2 O2
3 +CaSO=CaCO+S 4 ,故A正确;
4 3
B.过量的铁粉与稀硝酸反应生成硝酸亚铁、一氧化氮和水,离子方程式应为:3Fe+8H++2N
O
3=3Fe2++2NO↑+4HO,故B错误;
2
C.硫酸铝溶液与少量氢氧化钾溶液反应生成氢氧化铝沉淀和硫酸钾,离子方程式应为:Al3+
+3OH-=Al(OH)↓,故C错误;
3
D.硫化氢为弱电解质,书写离子方程式时不能拆,离子方程式应为:Cu2++HS=CuS↓+2H+,
2
故D错误;
答案选A。
5.(2021·湖南高考真题)对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
粒子组 判断和分析
不能大量共存,因发生反应:
A Na、Al3、Cl、NH
3
H
2
O
Al3 4NH H O=AlO 4NH 2H O
3 2 2 4 2
不能大量共存,因发生反应:
B H、K、S O2、SO2
2 3 4 2H S O2=SSO H O
2 3 2 2
C Na、Fe3、SO2
4
、H
2
O
2
能大量共存,粒子间不反应
D H、Na、Cl、MnO 能大量共存,粒子间不反应
4
A.A B.B C.C D.D
【KS5U答案】B
【详解】
O
A.Al3+和NH HO生成Al(OH) 沉淀而不是生成Al 2,故A错误;
3 2 3O2 O2
B.S 3 和H+反应生成单质硫、二氧化硫和水,离子方程式为:2H++ S 3 =S↓+SO↑+HO,
2 2 2 2
故B正确;
C.Fe3+可以将HO 氧化得Fe2+和O,不能大量共存,故C错误;
2 2 2
O
D.在酸性条件下Mn 4能将Cl-氧化为Cl,不能大量共存,故D错误;
2
答案选B。
6.(2021·浙江高考真题)下列物质属于强电解质的是
A.KOH B.HPO C.SO D.CHCHO
3 4 3 3
【KS5U答案】A
【分析】
在水溶液中或熔融状态下能够完全电离的化合物为强电解质。
【详解】
A.KOH在水溶液中或熔融状态下能够完全电离出K+和OH-,KOH为强电解质,A符合题意;
B.HPO 在水溶液中或熔融状态下能不够完全电离,HPO 为弱电解质,B不符合题意;
3 4 3 4
C.SO 在水溶液中或熔融状态下不能电离,SO 属于非电解质,C不符合题意;
3 3
D.CHCHO在水溶液中或熔融状态下不能电离,CHCHO属于非电解质,D不符合题意;
3 3
故答案选A。
7.(2021·浙江高考真题)下列反应的方程式不正确的是
2
A.石灰石与醋酸反应:CO3 +2CHCOOH=2CHCOO- +CO↑+HO
3 3 2 2
通电
B.铜片上电镀银的总反应(银作阳极,硝酸银溶液作电镀液):Ag(阳极) Ag(阴极)
C.铜与稀硝酸反应:3Cu+2NO3+8H+=3Cu2+ +2NO↑+4HO
2
2
D.明矾溶液中加入少量氢氧化钡溶液:2Al3+ +3SO4 + 3Ba2++6OH-=2Al(OH)↓+ 3BaSO↓
3 4
【KS5U答案】A
【详解】
A.碳酸钙难溶于水,在离子方程式中应以化学式保留,石灰石与醋酸反应的离子方程式为
CaCO+2CHCOOH=Ca2++2CHCOO-+HO+CO↑,A错误;
3 3 3 2 2
B.银作阳极,阳极的电极反应式为Ag-e-=Ag+,铜片作阴极,阴极的电极反应式为Ag++e-通电
=Ag,总反应为Ag(阳极) Ag(阴极),B正确;
NO-
C.Cu与稀硝酸反应生成Cu(NO)、NO和水,反应的离子方程式为3Cu+8H++2 3=3Cu2+
3 2
+2NO↑+4HO,C正确;
2
D.明矾溶液中加入少量Ba(OH) 溶液,参与反应的Ba2+与OH-物质的量之比为1:2,生成的
2
SO2-
Al(OH) 与BaSO 沉淀物质的量之比为2:3,反应的离子方程式为2Al3++3 4 +3Ba2++6OH-
3 4
=2Al(OH)↓+3BaSO↓,D正确;
3 4
答案选A。
2021年化学高考模拟题
一、单选题
1.(2021·九龙坡区·重庆市育才中学高三二模)下列反应的离子方程式正确的是
A.铝和氢氧化钠溶液反应:Al+3OH-=Al(OH)↓
3
SO2
B.向稀HNO 中滴加NaSO 溶液: 3 +2H+=SO↑+HO
3 2 3 2 2
HCO CO2
C.NaHCO 溶液中加足量Ba(OH) 溶液:2 3+Ba2++2OH-=BaCO↓+2HO+ 3
3 2 3 2
D.向CuSO 溶液中加入NaO:2NaO+2Cu2++2HO=4Na++2Cu(OH)↓+O↑
4 2 2 2 2 2 2 2
【KS5U答案】D
【详解】
AlO
A.铝和氢氧化钠溶液反应:2Al+2OH-+2HO =2 2+3 H↑;故A错误;
2 2
SO2 NO SO2
B.向稀HNO 中滴加NaSO 溶液:3 3 +2H++2 3=3 4 +2NO↑+HO;故B错误;
3 2 3 2
HCO
C.NaHCO 溶液中加足量Ba(OH) 溶液: 3+Ba2++OH-=BaCO↓+HO;故C错误;
3 2 3 2
D.向CuSO 溶液中加入NaO:2NaO+2Cu2++2HO=4Na++2Cu(OH)↓+O↑;故D正确。
4 2 2 2 2 2 2 2
综上所述,答案为D。
2.(2021·福建省南安第一中学高三二模)常温下,下列说法正确的是HCO- SO2- SO2-
A.某溶液中含有 3、 3 、 4 和Na+,若向其中加入NaO,充分反应后,四种离子的
2 2
SO2-
浓度不变的是 4 (忽略反应前后溶液体积的变化)
NH+ SO2-
B.水电离的c (H+)=10-12mol·L—1的溶液中,下列离子能大量共存: 4、Na+、 4 、
水
HCO-
3
C.氢氧化铁溶于HI溶液中的离子方程式为:2Fe(OH)+6H++2I—=2Fe2++I+6HO
3 2 2
SO2-
D.NaHS溶液中,下列离子能大量共存:K+、Al3+、Cl—、 4
【KS5U答案】C
【详解】
A.向溶液中加入具有强氧化性的过氧化钠固体,过氧化钠能将溶液中的亚硫酸根离子氧化
为硫酸根离子,溶液中硫酸根离子浓度会增大,故A错误;
B.水电离的c (H+)=10-12mol·L—1的溶液可能为酸溶液,也可能为碱溶液,酸溶液中,氢离
水
子与碳酸氢根离子反应,不能大量共存,碱溶液中,氢氧根离子与铵根离子、碳酸氢根离子
反应,不能大量共存,故B错误;
C.氢氧化铁溶于氢碘酸溶液的反应为氢氧化铁与氢碘酸溶液反应生成碘化亚铁、碘和水,
反应的离子方程式为2Fe(OH)+6H++2I—=2Fe2++I+6HO,故C正确;
3 2 2
D.在硫氢化钠溶液中,硫氢根离子与铝离子会发生双水解反应生成氢氧化铝沉淀和硫化氢
气体,不能大量共存,故D错误;
故选C。
3.(2021·重庆第二外国语学校高三三模)下列有关反应的离子方程式正确的是
Sn+Fe3+=Sn4++Fe2+
A.Sn溶于FeCl 溶液:
3
2Ag++H S=Ag S+2H+
B.[Ag(NH)]OH溶液中通入HS: 2 2
3 2 2
C.Cr(OH)(s)中同时加入NaOH溶液和HO 制NaCrO:
3 2 2 2 4
2Cr(OH) +3H O +4OH-=2CrO2-+8H O
3 2 2 4 2
HSO-+Ba2++OH-=BaSO +H O
D.NHHSO 溶液中加入足量Ba(OH) 溶液: 3 3 2
4 3 2【KS5U答案】C
【详解】
Sn+4Fe3+=Sn4++4Fe2+
A.电荷不守恒、得失电子不守恒,正确的离子方程式为 ,A错误;
B.[Ag(NH)]OH溶液中银以[Ag(NH)]-存在,B错误;
3 2 3 2
C.碱性环境下Cr(OH) 被HO 氧化为铬酸根,反应的离子方程式为
3 2 2
2Cr(OH) +3H O +4OH-=2CrO2-+8H O
3 2 2 4 2 ,C正确;
D.NHHSO 溶液中加入足量Ba(OH) 溶液,铵根和亚硫酸氢根氨1:1反应,反应的离子方程式
4 3 2
NH++HSO-+Ba2++2OH-=BaSO +H O+NH H O
为 4 3 3 2 3 2 ,D错误;
选C。
4.(2021·重庆第二外国语学校高三三模)常温下,下列各组离子在指定溶液中一定能大
量共存的是
2
A.能使紫色石蕊试液变蓝的溶液:Na+、NH4、CO3 、ClO-
B.通入大量二氧化碳的溶液:K+、Ca2+、Cl-、NO3
2
C.含有硝酸钠的溶液:H+、Mg2+、I-、SO4
2
D.室温下,c(OH-)/c(H+)=1的溶液:K+、Fe3+、SO4 、Cl-
【KS5U答案】B
【详解】
A.能使紫色石蕊试液变蓝的溶液显碱性,溶液中存在大量的OH-,OH-、NH4能够反应生成
NH·HO,不能大量共存,故A不选;
3 2
B.K+、Ca2+、Cl-、NO3离子间不发生反应,通入大量二氧化碳后也不反应,能够大量共存,
故B选;
C.硝酸钠在酸性溶液中具有强氧化性,NO3、H+、I-能够发生氧化还原反应,不能大量共存,
故C不选;
D.室温下,c(OH-)/c(H+)=1的溶液显中性,含Fe3+水解呈酸性,不能大量存在,故D不选;故选B。
5.(2021·重庆市第十一中学校高三二模)下列离子方程式书写正确的是
A.钠投入水中:Na+2HO=Na++2OH-+H↑
2 2
2ClOCO H O2HClOCO2
B.NaClO溶液中通入过量CO: 2 2 3
2
C.沸水中滴入几滴FeCl 饱和溶液:Fe3++3OH-=Fe(OH)(胶体)
3 3
SO Cl 2H O4H2ClSO2
D.饱和氯水中通入SO 至溶液颜色褪去: 2 2 2 4
2
【KS5U答案】D
【详解】
A.电荷不守恒,正确的为2Na+2HO=2Na++2OH-+H↑,A错误;
2 2
ClOCO H OHClOHCO
B.过量的CO 生成HCO3,正确的为 2 2 3,B错误;
2
C.水是弱电解质,不可拆,正确的为Fe3++3HO=Fe(OH)(胶体)+3H+,C错误;
2 3
SO Cl 2H O4H2ClSO2
D.氯气在水中和SO 发生氧化还原反应, 2 2 2 4 ,D正确;
2
故选:D。
6.(2021·安徽高三一模)下列反应中,现象和方程式都正确的是
浓硫酸
A.向胆矾粉末中加入适量浓硫酸,粉末由白色变成蓝色:CuSO•5HO CuSO+5HO
4 2 4 2
B.Fe加入FeCl 溶液中,溶液由黄色变成浅绿色:Fe+Fe3+=2Fe2+
3
Δ
C.NaO固体在空气中加热后,由白色变为淡黄色:NaO+CO NaCO
2 2 2 2 3
D.向Mg(OH) 悬浊液中滴加足量Fe(SO) 溶液,白色沉淀转化红褐色沉淀:3Mg(OH)(s)
2 2 4 3 2
+2Fe3+=2Fe(OH)(s)+3Mg2+
3
【KS5U答案】D
【详解】
A.浓硫酸具有吸水性,胆矾晶体中的结晶水被吸收,所以胆矾由蓝色变为无色,故A错误;
B.Fe加入FeCl 溶液中,发生的反应为:Fe+2Fe3+=3Fe2+,溶液由黄色变成浅绿色,故B错误;
3
Δ
2Na OO 2Na O
2 2 2 2
C.NaO固体在空气中加热后,由白色变为淡黄色,反应为: ,故C错
2
误;D.向Mg(OH) 悬浊液中滴加足量Fe(SO) 溶液,白色沉淀转化红褐色沉淀:3Mg(OH)(s)
2 2 4 3 2
+2Fe3+=2Fe(OH)(s)+3Mg2+,故D正确;
3
故答案为D。
7.(2021·浙江高三其他模拟)下列有关方程式表示不正确的是
通电
A.用银电极电解AgNO 溶液:4Ag++2HO 4Ag+O↑+4H+
3 2 2
2
B.用重铬酸钾法测定白酒中乙醇的含量:2CrO7 +3CHOH+16H+=4Cr3++3CHCOOH+11HO
2 2 5 3 2
HCO
C.已知酸性:HCO>HCN> 3,则向NaCN溶液中通入少量的CO 时:CN-+CO+HO=HCN+
2 3 2 2 2
HCO
3
HCO
D.碳酸氢钡与少量的氢氧化钠溶液反应:Ba2++OH-+ 3=BaCO↓+HO
3 2
【KS5U答案】A
【详解】
A.Ag电极是活性电极,阳极上Ag失去电子变为Ag+进入溶液,而不是水电离产生的OH-失去
电子;阴极上溶液中的Ag+得到电子变为单质Ag,方程式不符合反应事实,A错误;
B.反应符合事实,遵循物质的拆分原则,遵循电荷守恒、原子守恒、电子守恒,B正确;
C.符合复分解反应的规律,遵循物质拆分原则及原子守恒、电荷守恒,C正确;
D.酸式盐与碱反应时,以不足量的碱NaOH为标准,假设其物质的量为1,然后根据需要写
出其它微粒数目,配平方程式,符合反应事实,遵循电荷守恒、原子守恒,D正确;
故合理选项是A。
8.(2021·浙江高三其他模拟)下列物质属于电解质,且在熔融态能导电的是
A.硫酸 B.氯化铝 C.生石灰 D.苯酚
【KS5U答案】C
【详解】
SO2
A.硫酸由分子构成,溶于水会发生电离产生自由移动的H+、 4 ,因此属于电解质,但在
熔融状态下不能发生电离,因而不能导电,A不符合题意;
B.氯化铝是共价化合物,由分子构成,在熔融状态下不能发生电离,因而不能导电。在水
溶液中能够发生电离产生自由移动的Al3+、Cl-,因此属于电解质,B不符合题意;C.生石灰是CaO,属于离子化合物,在熔融状态下会发生电离,产生自由移动的Ca2+、O2-而
能够导电,属于电解质,C符合题意;
D.苯酚俗称石炭酸,由分子构成,能够微弱的电离产生离子,因此属于电解质;但在熔融
状态下不能电离,因而不能导电,D不符合题意;
故合理选项是C。
9.(2021·阜新市第二高级中学高三其他模拟)常温下,下列各组离子在指定溶液中一定
能大量共存的是
SO2-
A.1.0mol•L-1KNO 溶液:H+、Fe2+、Cl-、 4
3
SO2-
B.透明的溶液:Cu2+、Fe3+、 4 、Cr3+
HCO- SO2-
C.含有大量Ba2+的溶液: 3、Fe3+、SCN-、 4
D.使甲基橙变红的溶液:Na+、Cl-、CHCOO-、Fe2+
3
【KS5U答案】B
【详解】
NO-
A.Fe2+是常见的还原性离子,与H+和 3发生氧化还原反应而不能大量共存,A不符题意;
SO2-
B.透明的溶液中Cu2+、Fe2+、 4 、Cr3+之间不发生反应,故能大量共存,B符合题意;
SO2- HCO-
C. 4 与Ba2+反应而不能大量共存,Fe3+与SCN-、 3反应而不能大量共存,C不符题意;
D.使甲基橙变红的溶液为酸性溶液,醋酸根离子为弱酸阴离子,可以结合溶液中的氢离子形
成弱电解质醋酸而不能大量共存,D不符题意;
故选B。
10.(【一飞冲天】新华中学高三模拟化学.)常温下,下列溶液中各组离子一定能够大量
共存的是
2- -
A.c(H+)/c(OH-)=1.0 ×10-12的溶液: K+、 Na+、CO3 、AlO2
2-
B.水电离出来的c(OH-)=1.0 ×10-13mol/L的溶液: K+、 Cl-、S2- 、SO3
+ 2- 2-
C.使甲基橙变红色的溶液中:Na+、NH4、 SO3 、SO3
2
D.通入足量SO 后的溶液: Na+、 Ba2+、ClO-、CHCOO-
2 3【KS5U答案】A
【详解】
2- -
A.c(H+)/c(OH-)=1.0×10-12的溶液显碱性,K+、Na+、CO3 、AlO2之间不反应,可以大量共存,
A选;
2-
B.水电离出来的c(OH-)=1.0 ×10-13mol/L的溶液如果显酸性S2-、SO3 和氢离子反应生成单
质硫和水,不能大量共存,B不选;
2- 2-
C.使甲基橙变红色的溶液显酸性,酸性溶液中SO3 、SO3 均与氢离子反应,不能大量共存,
2
C不选;
D.通入足量SO 后的溶液中ClO-能氧化二氧化硫,CHCOO-能与氢离子结合生成醋酸,均不能
2 3
大量共存,D不选;
答案选A。
11.(2021·吉林东北师大附中高三其他模拟)常温下,下列各组离子在指定溶液中一定能
大量共存的是
+ 2-
A.含有 Fe2+的溶液:K+、NH4 、SO4 、[Fe(CN) ]3 -
6
- +
B.能溶解 Al(OH) 的溶液:Na+ 、F- 、NO3、NH4
3
- 2-
C.含有I- 的溶液:Al3+、H+、MnO4 、SO4
+ -
D.含有 NH4的溶液:Na+、K+、HCO3 、Cl -
【KS5U答案】D
【详解】
A.Fe2+与[Fe(CN) ]3 –反应生成蓝色沉淀,含有 Fe2+的溶液中不能大量含有[Fe(CN) ]3 -,
6 6
故不选A;
B.能溶解 Al(OH) 的溶液呈强酸性或强碱性,酸性条件下不能大量含有F-,碱性条件下不能
3
+
大量含有NH4,故不选B;
- -
C. I- 能被MnO4氧化为I,含有I- 的溶液中不能大量含有MnO4,故不选C;
2+ - +
D.NH4、Na+、K+、HCO3 、Cl –相互之间不反应,含有 NH4的溶液可以大量含有Na+、K+、
-
HCO3 、Cl -,故选D。
选D。
12.(2021·青龙满族自治县第一中学高三其他模拟)下列说法不正确的是
2 2
A.用碳酸钠溶液处理锅炉水垢:CaSO(s)+CO3 CaCO(s)+SO4
4 3
B.湿润的淀粉碘化钾试纸遇氯气变蓝:3Cl+I-+3HO=6Cl-+IO3+6H+
2 2
高温
C.铝粉和氧化铁组成的铝热剂用于焊接钢轨:2Al+FeO AlO+2Fe
2 3 2 3
D.用FeCl 溶液“腐蚀”覆铜板:2Fe3++ Cu = 2Fe2++ Cu2+
3
【KS5U答案】B
【详解】
A.硫酸钙的溶解度大于碳酸钙的溶解度,溶解度大的物质能向溶解度小的物质转化,所以
锅炉水垢中的硫酸钙可用碳酸钠溶液处理,使之转化为碳酸钙,沉淀转换的实质就是沉淀溶
2
解平衡的移动,平衡一般向生成更难溶物质的方向移动,则离子反应为:CaSO(s)+CO3
4
2
CaCO(s)+SO4 ,A正确;
3
B.湿润的淀粉碘化钾试纸遇氯气变蓝是由于氯气与碘离子反应生成碘单质,碘单质遇淀粉
变蓝,发生的反应为: Cl+2I-=I+2Cl-, B错误;
2 2
C.铝粉和氧化铁组成的铝热剂发生反应生成熔融态的铁单质,可用于焊接钢轨,发生的反
高温
应为:2Al+FeO AlO+2Fe,C正确;
2 3 2 3
D.用FeCl 溶液“腐蚀”覆铜板时Fe3+将Cu氧化,离子方程式为2Fe3++ Cu = 2Fe2++ Cu2+,D
3
正确;
综上所述答案为B。
13.(【一飞冲天】8.宝坻一中三模)下列反应的离子方程式表达正确的是通电
A.用铜电极电解MgCl 溶液:Mg2++2Cl-+2HO H↑+C1↑+Mg(OH)↓
2 2 2 2 2
B.某消毒液的主要成分为NaClO,加白醋可增强消毒效果:CHCOOH+ClO-=HClO+CHCOO-
3 3
MnO C O2
C.向草酸溶液中逐滴加入酸性高锰酸钾溶液,溶液褪色:2 4 +5 2 4 +16H+=2Mn2+
+10CO↑+8HO
2 2
D.水浴加热银氨溶液与葡萄糖的混合溶液,出现银镜:CHOH(CHOH)CHO+2[Ag(NH)]OH
2 4 3 2
Δ
CHOH(CHOH)COOH+2Ag↓+4NH+HO
2 4 3 2
【KS5U答案】B
【详解】
A.由于Cu不是惰性电极,所以Cu会参与氧化还原反应,阳极Cu失去电子,生成Cu2+,阳极
电极反应式为Cu-2e-=Cu2+,阴极电极方程式为2HO+2e-=H↑+2OH-,故A错误;
2 2
B.由于HClO酸性较弱,则NaClO可与醋酸反应生成HClO,漂白性增强,离子方程式为
CHCOOH+ClO-=HClO+CHCOO-,故B正确;
3 3
C.向草酸溶液中逐滴加入酸性高锰酸钾溶液,溶液褪色,发生了氧化还原反应,由于草酸
MnO
是弱酸,在离子方程式中应保留分子式,其离子方程式为2 4 +5HCO+6H+=2Mn2+
2 2 4
+10CO↑+8HO,故C错误;
2 2
D.水浴加热银氨溶液与葡萄糖的混合溶液,葡萄糖中醛基被氧化生成羧基,出现银镜,该
Δ NH
反应的离子方程式为CHOH(CHOH)CHO+2[Ag(NH)]++2OH- CHOH(CHOH)COO-+ 4
2 4 3 2 2 4
+3NH+2Ag↓+HO,故D错误;
3 2
答案为B。
14.(2021·广东石门中学高三其他模拟)在水溶液中能大量共存的一组离子是
2
A.NH4、Na+、Br-、SO4 B.K+、NH4、OH-、NO3
2 2
C.Fe2+、H+、ClO-、Cl- D.Mg2+、H+、SiO3 、SO3
【KS5U答案】A
【详解】
A.各离子之间不发生反应,可大量共存,A正确;+
B.NH4与OH—结合生成弱碱NH·HO,无法大量共存,B错误;
3 2
C.ClO—与Fe2+ Cl—在酸性条件下均发生氧化还原反应,ClO—与H+结合成弱酸HClO,无法大
、
量共存,C错误;
2-
D.SiO3 、亚硫酸根离子 与H+反应,无法大量共存,D错误;
故选A。
15.(2021·天津高三一模)下列离子方程式正确的是
SO2-
A.用SO 溶液吸收溴蒸汽:SO+B +2HO= 4 +2Br-+4H+
2 2 r2 2
B.FeO溶于足量稀硝酸:FeO+2H+=Fe2++HO
2
C.用醋酸溶解水垢中的碳酸钙:CaCO+2H+=Ca2++CO↑+HO
3 2 2
D.腐蚀印刷线路板的反应:Fe3++Cu=Fe2++Cu2+
【KS5U答案】A
【详解】
SO2-
A.用SO 溶液吸收溴蒸汽反应生成硫酸和氢溴酸:SO+Br+2HO= 4 +2Br-+4H+,A正确;
2 2 2 2
NO
B.FeO溶于足量稀硝酸: 3+3FeO+10H+=NO +3Fe3++5HO,B错误;
2
C.用醋酸溶解水垢中的碳酸钙:CaCO+2CHCOOH=Ca2++CO↑+HO+2CHCOO-,C错误;
3 3 2 2 3
D.腐蚀印刷线路板的反应:2Fe3++Cu=2Fe2++Cu2+,D错误;
答案选A。
16.(2021·天津南开区·南开中学高三三模)下列离子方程式书写正确的是
A.用碳酸氢钠溶液检验水杨酸中的羧基: +2 → +2HO+2CO↑
2 2
HCO-
3
MnO- C O2-
B.用高锰酸钾标准溶液滴定草酸:2 4+16H++5 2 4 =2Mn2++10CO↑+8HO
2 2
通电
C.电解饱和食盐水:2Cl-+2H+ Cl↑+H↑
2 2
Δ
D.向NHHSO 溶液中加过量NaOH溶液并加热:NH+ +HSO- +2OH- NH↑+SO2- +2HO
4 3 4 3 3 3 2
【KS5U答案】D【详解】
A.酚羟基的酸性弱于碳酸,不能和碳酸氢根反应生成二氧化碳,A错误;
B.草酸为弱酸,在离子方程式中不能拆,B错误;
C.电解饱和食盐水时阴极是水电离出的氢离子放电,水是弱电解质,不能用H+表示,C错误;
D.向NHHSO 溶液中加过量NaOH,铵根和亚硫酸氢根都能反应,且加热会逸出氨气,D正确;
4 3
综上所答案为D。
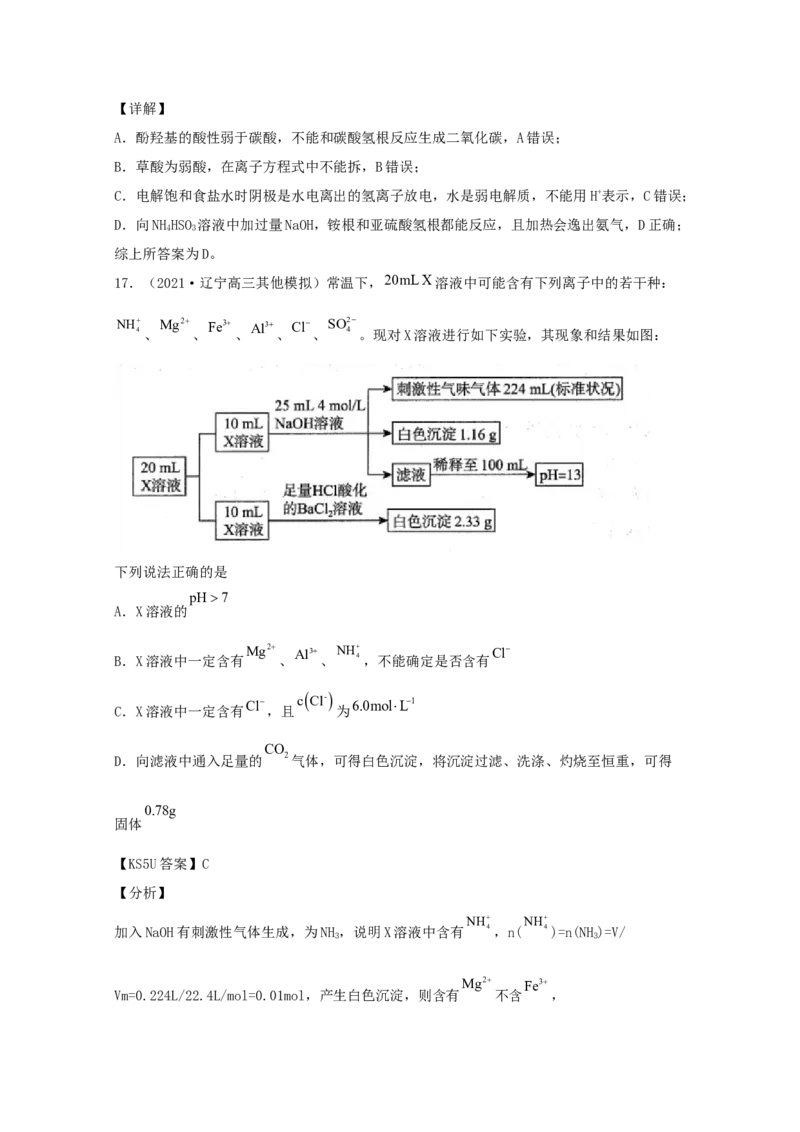
17.(2021·辽宁高三其他模拟)常温下,20mL X溶液中可能含有下列离子中的若干种:
NH
4
、
Mg2
、
Fe3
、
Al3
、
Cl
、
SO2
4
。现对X溶液进行如下实验,其现象和结果如图:
下列说法正确的是
pH7
A.X溶液的
Mg2 Al3 NH Cl
B.X溶液中一定含有 、 、 4,不能确定是否含有
Cl c
Cl-
6.0molL1
C.X溶液中一定含有 ,且 为
CO
D.向滤液中通入足量的 2气体,可得白色沉淀,将沉淀过滤、洗涤、灼烧至恒重,可得
0.78g
固体
【KS5U答案】C
【分析】
NH NH
加入NaOH有刺激性气体生成,为NH,说明X溶液中含有 4,n( 4)=n(NH)=V/
3 3
Mg2 Fe3
Vm=0.224L/22.4L/mol=0.01mol,产生白色沉淀,则含有 不含 ,n(Mg2+)=n(Mg(OH))=m/M=1.16g/58g/mol=0.02mol,由滤液稀释后氢氧根离子浓度,可知氢氧
2
化钠有剩余,反应消耗NaOH为:0.025L×4.00mol/L-0.1L×0.1mol/L=0.09mol,则与Al3+反
应的NaOH为0.09-0.01-0.02×2=0.04mol,则n(Al3+)=0.01mol;加入BaCl 产生白色沉淀,
2
SO2 SO2
则含有 4 ,n( 4 )=n(BaSO)=m/M=2.33g/233g/mol=0.01mol,由溶液呈电中性,
4
n(+)=0.01×1+0.02×2+0.01×3=0.08mol,n(-)=0.01×2=0.02mol,则一定含有Cl-,且
n(Cl-)=0.06mol;
【详解】
NH Mg2 SO2 Fe3
分析知,一定存在: 4、 、Al3+、Cl-、 4 ,一定不存在: ,
NH
A.溶液中存在 4、Al3+发生水解而溶液呈酸性,即pH<7,A错误;
Mg2 Al3 NH
B.X溶液中一定含有 、 、 4、Cl-,B错误;
C.X溶液中一定含有
Cl
,且n(Cl-)=0.06mol,在10mL溶液中
c
Cl-
=n/V=
6.0molL1
,C正
确;
D.滤液成分是NaAlO,通入CO 生成Al(OH),灼烧后得到AlO,分析知n(Al3+)=0.01mol,
2 2 3 2 3
则n(AlO)=2 n(Al3+)=0.02mol,m=nM=0.02mol×102g/mol=2.04g,D错误;
2 3
故选:C。
18.(2021·四川德阳市·高三二模)对于下列实验,能正确描述其反应的离子方程式是
SO2-
A.将少量SO 通入次氯酸钠溶液中:ClO-+SO+HO=Cl-+ 4 +2H+
2 2 2
CO2- SO2-
B.向含CaSO 的水垢中滴入饱和NaCO 溶液:CaSO(s)+ 3 (aq) 4 (aq)+CaCO(s)
4 2 3 4 3
电解
C.用铁电极电解饱和MgCl 溶液:Mg2++2C1-+2HO Mg(OH)↓+Cl↑+H↑
2 2 2 2 2
SO2- NH+
D.向(NH)Fe(SO) 溶液中加入含等物质的量溶质的Ba(OH) 溶液:Ba2++ 4 + 4+OH-
4 2 4 2 2
=BaSO↓+NH·HO
4 3 2
【KS5U答案】B
【详解】SO2-
A.将少量SO 通入次氯酸钠溶液中:3ClO-+SO+HO=Cl-+ 4 +2HClO,A错误;
2 2 2
CO2- SO2-
B.向含CaSO 的水垢中滴入饱和NaCO 溶液:CaSO(s)+ 3 (aq) 4 (aq)+CaCO(s),B
4 2 3 4 3
正确;
C.用铁电极电解饱和MgCl 溶液,铁失电子生成亚铁离子,没有氯气产生,C错误;
2
SO2-
D.向(NH)Fe(SO) 溶液中加入含等物质的量溶质的Ba(OH) 溶液:Fe2++ 4 +Ba2++2OH-
4 2 4 2 2
=BaSO↓+Fe(OH)↓,D错误;
4 2
答案选B。
19.(2021·梅州市梅江区梅州中学高三其他模拟)下列反应方程式书写不正确的是
A.用氢氟酸雕刻玻璃:SiO+4HF=SiF↑+2HO
2 4 2
电解
B.工业上用电解法制镁:MgCl(熔融) Mg+Cl↑
2 2
C.向H18O中投入NaO 固体:2H18O+2NaO=4Na++4OH-+18O↑
2 2 2 2 2 2 2
D.氢氧化亚铁暴露于空气中:4Fe(OH)+O+2HO=4Fe(OH)
2 2 2 3
【KS5U答案】C
【详解】
A.二氧化硅能和氢氟酸反应,可用氢氟酸雕刻玻璃:SiO+4HF=SiF↑+2HO,A正确;
2 4 2
电解
B.镁是活泼的金属,工业上用电解熔融的氯化镁制镁:MgCl(熔融) Mg+Cl↑,B正确;
2 2
C.过氧化钠和水反应中过氧化钠既是氧化剂也是还原剂,向H18O中投入NaO 固体:
2 2 2
2H18O+2NaO=4Na++218OH-+2OH-+O↑,C错误;
2 2 2 2
D.氢氧化亚铁暴露于空气中易被氧化为氢氧化铁:4Fe(OH)+O+2HO=4Fe(OH),D正确;
2 2 2 3
答案选C。
20.(2021·四川高三一模)下列指定反应的离子方程式正确的是
NH+
A.0.1mol/LAgNO 溶液中加入过量氨水:Ag++NH·HO=AgOH↓+ 4
3 3 2
NO-
B.NO 通入水中制硝酸:2NO+HO=2H++ 3+NO
2 2 2
C O2-
C.NaOH溶液与过量HCO 溶液反应:HCO+2OH-= 2 4 +2HO
2 2 4 2 2 4 2
D.KOH溶液溶解Al(OH) 固体:Al(OH)+OH-=[Al(OH)]-
3 3 4【KS5U答案】D
【详解】
A.AgNO 溶液中加入过量氨水,生成的AgOH会被氨水溶解,生成Ag(NH)OH,离子方程式为:
3 3 2
NH+
Ag++NH·HO=AgOH↓+ 4、AgOH+2NH·HO =[Ag(NH)]++OH-+2HO,故A错误;
3 2 3 2 3 2 2
B.NO 通入水中制硝酸,选项中的离子方程式的电荷不守恒,正确的离子方程式为:
2
NO-
3NO+HO=2H++2 3+NO,故B错误;
2 2
C O-
C.HCO 是过量的,应该生成酸式盐:HCO+OH-=H 2 4+HO,故C错误;
2 2 4 2 2 4 2
D.Al(OH) 是两性氢氧化物,可以和KOH反应生成盐,离子方程式为:Al(OH)+OH-
3 3
=[Al(OH)]-,故D正确;
4
故选D。
21.(2021·重庆市长寿中学校高三其他模拟)下列有关离子方程式的书写正确的是
NH+
A.向饱和NaCl溶液中依次通人足量NH 与CO:Na++NH+CO+HO=NaHCO↓+ 4
3 2 3 2 2 3
B.向BaCl 溶液中通入SO:Ba2++SO+2HO=BaSO↓+2H+
2 2 2 2 3
通电
C.电解MgCl 溶液:2Cl-+2HO Cl↑+H↑+2OH-
2 2 2 2
S O2-
D.NaSO 溶液与硝酸溶液混合: 2 3 +2H+=S↓+SO↑+HO
2 2 3 2 2
【KS5U答案】A
【详解】
A.饱和NaCl溶液中通NH、CO 反应生成NaHCO 和NHCl,由于溶液饱和会析出溶解度较小的
3 2 3 4
NH+
NaHCO,对应离子方程式为:Na++NH+CO+HO= NaHCO↓+ 4,A正确;
3 3 2 2 3
B.BaCl 与SO 不发生反应,B错误;
2 2
C.电解MgCl 溶液生成的OH-会与Mg2+继续反应生成Mg(OH) 沉淀,正确离子方程式为:Mg2+
2 2
电解
+2Cl-+2HO Cl↑+H↑+Mg(OH)↓,C错误;
2 2 2 2
SO2-
D.硝酸具有强氧化性,NaSO 溶液被硝酸氧化会生成 4 ,D错误。
2 2 3故选A。
22.(2021·福建省福州第一中学)下列离子方程式书写正确的是
A.氧化亚铁溶于稀硝酸:FeO+2H+=Fe2++HO
2
B.向KClO溶液中滴加浓盐酸:ClO-+Cl-+2H+=Cl↑+HO
2 2
C.向Ca(ClO) 溶液中通入少量SO:Ca2++SO+HO+2ClO-=CaSO↓+2HClO
2 2 2 2 3
HCO
D.向Mg(HCO) 溶液中滴加足量NaOH溶液:Mg2++ 3+OH-=MgCO↓+HO
3 2 3 2
【KS5U答案】B
【详解】
NO
A.氧化亚铁溶于稀硝酸,稀硝酸氧化亚铁离子,会有NO生成,3FeO+4H++ 3+=Fe2++
NO↑+2HO,故A错误;
2
B.向KClO溶液中滴加浓盐酸,会生成氯气:ClO-+Cl-+2H+=Cl↑+HO,故B正确;
2 2
C.向Ca(ClO) 溶液中通入少量SO,次氯酸根会氧化二氧化硫变为硫酸根:Ca2++SO+HO+
2 2 2 2
3ClO-=CaSO↓+2HClO+Cl-,故C错误;
4
HCO
D.向Mg(HCO) 溶液中滴加足量NaOH溶液,镁离子变为氢氧化镁沉淀:Mg2++2 3+4OH-
3 2
CO2
=2 3 +Mg(OH)↓+2HO,故D错误。
2 2
综上所述,答案为B。
23.(2021·广东金山中学高三三模)下列反应的离子方程式表达不正确的是
SO2-
A.将SO 通入酸性FeCl 溶液中:SO+2Fe3++2HO=2Fe2++ 4 +4H+
2 3 2 2
B.某消毒液的主要成分为NaClO,加白醋可增强消毒效果:
CH COOH+ClO-=HClO+CH COO-
3 3
C.向草酸溶液中逐滴加入酸性高锰酸钾溶液,溶液褪色:
2MnO-+5C O2-+16H+=2Mn2++10CO +8H O
4 2 4 2 2
Ba2++2HCO-+2OH-=BaCO +CO2-+2H O
D.向碳酸氢钡溶液中加入过量氢氧化钾溶液: 3 3 3 2
【KS5U答案】C
【详解】A.将SO 通入酸性FeCl 溶液中,SO 有还原性,Fe3+有氧化性,反应的离子方程式:
2 3 2
SO2-
SO+2Fe3++2HO═2Fe2++ 4 +4H+,故A正确;
2 2
B.消毒液NaClO加白醋可增强漂白作用,发生反应为:CHCOOH+ClO-=HClO+CHCOO-,故B正
3 3
确;
C.草酸是弱酸,不能拆成离子形式,酸性高锰酸钾溶液与草酸溶液反应,Mn元素从+7降至
-
+2,C元素从+2升至+4,离子方程式:2MnO4+5HCO+6H+═2Mn2++8HO+10CO↑,故C错误;
2 2 4 2 2
D.碳酸氢钡溶液中加入过量的氢氧化钾溶液,以碳酸氢钡完全反应书写,离子方程式为
Ba2++2HCO-+2OH-=BaCO +CO2-+2H O
3 3 3 2 ,故D正确;
故选:C。
24.(2021·西藏昌都市第一高级中学高三其他模拟)下列有关说法正确的是
A.少量Ca(OH) 溶液和NaHCO 溶液反应的离子方程式:Ca2++OH-+HCO3=CaCO↓+HO
2 3 3 2
B.Fe2+与HO 在酸性溶液中反应的离子方程式:2Fe2++HO+2H+=2Fe3++2HO
2 2 2 2 2
2
C.pH=2的溶液中可能大量存在Na+、NH4、SiO3
D.新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-)
【KS5U答案】B
【详解】
A.NaHCO 溶液与少量Ca(OH) 溶液反应,离子方程式:2 HCO3+Ca2++2OH-=CaCO↓+2HO+CO
3 2 3 2
2
3 ,故A错误;
B.Fe2+与HO 在酸性溶液中的反应的离子反应为2Fe2++HO+2H+═2Fe3++2HO,故B正确;
2 2 2 2 2
2
C.pH=2的溶液呈酸性,H+、与SiO3 反应,在溶液中不能大量共存,故C错误;
D.新制氯水中加入固体NaOH溶液中存在电荷守恒c(Na+)+c(H+)=c(Cl- )+c(ClO- )+c(OH-
),故D错误;
故选:B。
SO2- NH+
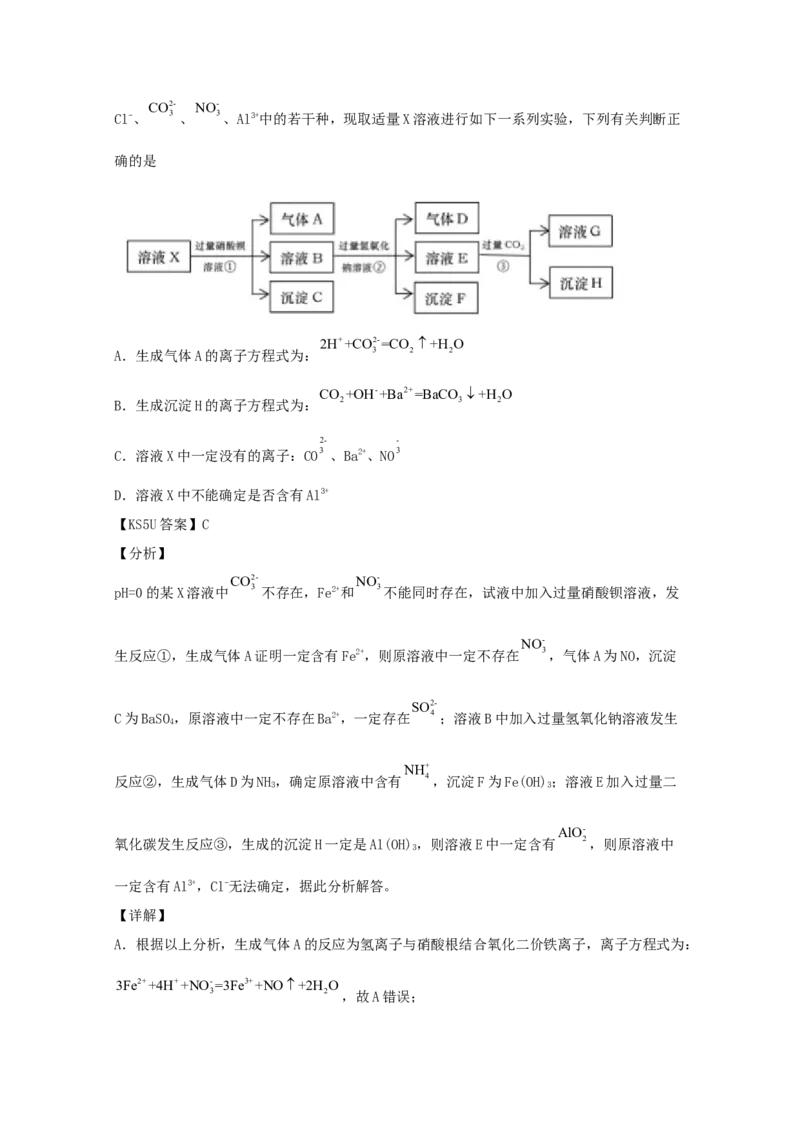
25.(2021·安徽安庆一中高三三模)某溶液pH=0,可能存在 4 、 4、Ba2+、Fe2+、CO2- NO-
Cl-、 3 、 3、Al3+中的若干种,现取适量X溶液进行如下一系列实验,下列有关判断正
确的是
2H++CO2-=CO +H O
A.生成气体A的离子方程式为: 3 2 2
CO +OH-+Ba2+=BaCO +H O
B.生成沉淀H的离子方程式为: 2 3 2
2- -
C.溶液X中一定没有的离子:CO3 、Ba2+、NO3
D.溶液X中不能确定是否含有Al3+
【KS5U答案】C
【分析】
CO2- NO-
pH=0的某X溶液中 3 不存在,Fe2+和 3不能同时存在,试液中加入过量硝酸钡溶液,发
NO-
生反应①,生成气体A证明一定含有Fe2+,则原溶液中一定不存在 3,气体A为NO,沉淀
SO2-
C为BaSO,原溶液中一定不存在Ba2+,一定存在 4 ;溶液B中加入过量氢氧化钠溶液发生
4
NH+
反应②,生成气体D为NH,确定原溶液中含有 4,沉淀F为Fe(OH);溶液E加入过量二
3 3
AlO-
氧化碳发生反应③,生成的沉淀H一定是Al(OH),则溶液E中一定含有 2,则原溶液中
3
一定含有Al3+,Cl-无法确定,据此分析解答。
【详解】
A.根据以上分析,生成气体A的反应为氢离子与硝酸根结合氧化二价铁离子,离子方程式为:
3Fe2++4H++NO-=3Fe3++NO+2H O
3 2 ,故A错误;AlO-
B.根据以上分析,生成沉淀H为向 2溶液中通过量的二氧化碳,离子方程式为:
AlO-+CO +2H O=Al(OH) +HCO-
2 2 2 3 3,故B错误;
CO2- NO-
C.根据以上分析,溶液X中一定没有的离子仅为: 3 、Ba2+、 3,故C正确;
SO2- NH+
D.根据以上分析,溶液X中一定含有的离子是∶H+、Fe2+、 4 、 4、Al3+,故Al3+一定有,
故D错误;
故选:C。
26.(2021·西藏拉萨市·高三二模)下列有关离子方程式的书写错误的是
A.向饱和NaCl溶液中依次通入足量NH 与CO:Na++NH+ CO+ HO=NaHCO↓+NH4
3 2 3 2 2 3
B.向硫酸铝溶液中加入过量氨水:Al3+ +3NH·HO=Al(OH)↓+ 3NH4
3 2 3
2
C.碳酸氢镁溶液与足量氢氧化钠溶液反应:Mg2++2HCO3+4OH-=Mg(OH)↓+2CO3 +2HO
2 2
2
D.草酸与足量酸性高锰酸钾溶液反应:2MnO4+5CO4 + 16H+=2Mn2++10CO↑+8HO
2 2 2
【KS5U答案】D
【详解】
A.向饱和NaCl溶液中依次通入足量NH 与CO,反应生成碳酸氢钠沉淀,Na++NH+ CO+
3 2 3 2
HO=NaHCO↓+NH4,A正确;
2 3
B.一水合氨为弱碱,不能溶解氢氧化铝,所以最终得到氢氧化铝沉淀,离子方程式为Al3+
+3NH·HO=Al(OH)↓+ 3NH4,B正确;
3 2 3
C.NaOH足量,碳酸氢根、镁离子都能和其反应,所以离子方程式为Mg2++2HCO3+4OH-
2
=Mg(OH)↓+2CO3 +2HO,C正确;
2 2
D.草酸为弱酸,不能写成离子,正确离子方程式为2MnO4+5HCO+ 6H+=2Mn2+
2 2 4
+10CO↑+8HO,D错误;
2 2综上所述答案为D。
27.(2021·惠来县第一中学高三月考)下列离子方程式正确的是
A.用HO 从酸化的海带灰浸出液中提取碘:2I-+HO+2H+=I+2HO
2 2 2 2 2 2
B.向碳酸氨铵溶液中加入过量的NaOH溶液:NH4+OH-= NH·HO
3 2
2
C.向饱和的碳酸钠溶液中通入足量的二氧化碳:CO +CO3 +HO= 2HCO3
2 2
D.过量SO 通入NaClO溶液中:SO +HO+ClO-= HClO+HSO3
2 2 2
【KS5U答案】A
【详解】
A. HO 具有氧化性,会将碘离子氧化为碘单质,离子方程式为 2I−+HO+2H+=I+HO ,故A
2 2 2 2 2 2
正确;
- + 2-
B.向碳酸氢铵溶液中加入过量的NaOH溶液:HCO3+NH4+2OH−=NH 3⋅H
2
O+CO3 +H
2
O,故B错误;
C.碳酸氢钠溶解度比碳酸钠小,向饱和的碳酸钠溶液中通入足量的二氧化碳生成碳酸氢钠
2-
沉淀:CO3 +2Na++CO+HO=2NaHCO↓,故C错误;
2 2 3
D.SO 具有还原性,NaClO具有氧化性,过量SO 通入NaClO溶液中,发生氧化还原反应:
2 2
2-
HO+SO+ClO−===SO4 +Cl−+2H+ ,故D错误;
2 2
故答案为A。
28.(2021·湖北武汉市·汉阳一中高三三模)下列指定反应的离子方程式正确的是
A.NaO 与H18O反应:2NaO+2H18O=4Na++4OH- +18O↑
2 2 2 2 2 2 2
B.向次氯酸钠溶液中通入少量的CO:ClO—+CO+HO=HClO+HCO3
2 2 2
C.FeCl 溶液中加过量NaS溶液:S2- + 2Fe3+ =S↓+2Fe2+
3 2
D.向Fe(OH) 胶体中加入HI溶液:Fe(OH)+3H+ =Fe3+ +3HO
3 3 2
【KS5U答案】B
【详解】
A.NaO 与H18O反应中过氧化钠既是氧化剂也是还原剂:2NaO+2H18O=4Na++2OH-+218OH-
2 2 2 2 2 2
+O↑,A错误;
2
B.由于碳酸的酸性强于次氯酸,但次氯酸强于碳酸氢根,则向次氯酸钠溶液中通入少量的
CO:ClO—+CO+HO=HClO+HCO3,B正确;
2 2 2
C.FeCl 溶液中加过量NaS溶液:3S2- + 2Fe3+ =S↓+2FeS↓,C错误;
3 2
D.向Fe(OH) 胶体中加入HI溶液生成氧化还原反应:2Fe(OH)+2I-+6H+ =I+2Fe2+ +6HO,D
3 3 2 2
错误;
答案选B。
29.(2021·福建厦门外国语学校高三其他模拟)下列反应的离子方程式正确的是
A.用CuSO 溶液除去电石气中的少量硫化氢:Cu2++S2-=CuS↓
4
2-
B.向NaClO溶液中通入少量SO:ClO-+SO+HO=SO4 +C1-+2H+
2 2 2
C.向稀AgNO 溶液中加入过量稀氨水:Ag++2NH·HO=[Ag(NH)]++2HO
3 3 2 3 2 2
2
D.向苯酚钠溶液中通入少量CO:CO+HO+2 →CO +2
2 2 2 3
【KS5U答案】C
【详解】
A.CuSO 溶液和硫化氢反应生成硫化铜沉淀和硫酸,反应的离子方程式是Cu2+
4
+HS=CuS↓+2H+,故A错误;
2
2-
B.向NaClO溶液中通入少量SO 生成硫酸钠、次氯酸、氯化钠,3ClO-+SO+HO=SO4 +C1-
2 2 2
+2HClO,故B错误;
C.向稀AgNO 溶液中加入过量稀氨水生成生成银氨溶液,反应的离子方程式是Ag+
3
+2NH·HO=[Ag(NH)]++2HO,故C正确;
3 2 3 2 2
D.向苯酚钠溶液中通入少量CO 生成苯酚和碳酸氢钠,反应的离子方程式是CO+HO+
2 2 2
→HCO + ,故D错误;
3
选C。
30.(2021·广东石门中学高三其他模拟)下列离子方程式错误的是
SO +3C1O-+H O=SO2-+Cl-+2HClO
A.少量SO 气体通入次氯酸钠溶液中: 2 2 4
2
Fe3++2OH-=FeOH
B.向NHFe(SO) 饱和溶液中滴加几滴NaOH溶液: 3
4 4 2
Fe O +6H+=2Fe3++3H O
C.氧化铁溶于HI溶液: 2 3 2SiO2-+2H O+2CO =2HCO-+H SiO
D.向硅酸钠水溶液中通入过量CO 气体: 3 2 2 3 2 3
2
【KS5U答案】C
【详解】
A.项中首先SO 与ClO—发生氧化还原反应,生成HSO 和Cl—,然后生成的HSO 继续与ClO—
2 2 4 2 4
发生复分解反应生成HClO,A项方程式正确;
NH+
B.中加入NaOH时先与Fe3+反应,再与 4反应,B项方程式正确;
Fe O + 6H+ + 2I- = 2Fe2+ + 3H O + I
C.项中Fe3+会与I—发生氧化还原反应,正确的应该是 2 3 2 2,
C项方程式错误;
HCO-
D.中当CO 过量时,生成的是 3和HSiO,D项方程式正确;
2 2 3
故选C。
31.(2021·哈尔滨市·黑龙江实验中学高三其他模拟)对于下列实验,能正确描述其反应
的离子方程式是
2
A.HCO 具有还原性:2MnO4+5CO4 +16H+=2Mn2++10CO↑+8HO
2 2 4 2 2 2
B.用铝粉和NaOH溶液反应制取少量H:Al+2OH-=AlO2+H↑
2 2
2
C.KClO碱性溶液与Fe(OH) 反应:3ClO-+2Fe(OH)=2FeO4 +3Cl-+4H++HO
3 3 2
D.同浓度同体积NHHSO 溶液与NaOH溶液混合:H++OH-=HO
4 4 2
【KS5U答案】D
【详解】
A.草酸是弱电解质,不可拆,草酸被高锰酸钾溶液氧化为二氧化碳,高锰酸钾被还原为
Mn2+,离子反应为:2 MnO4+6H++5HCO=2Mn2++10CO↑+8HO,故A错误;
2 2 4 2 2
B.用铝粉和NaOH溶液反应制取少量H,离子方程式为:2Al+2HO+2OH-═2 AlO2+3H↑,故
2 2 2
B错误;
2
C.碱性溶液中,KClO氧化Fe(OH),离子方程式为:3ClO-+2 Fe(OH)+4OH-=2 FeO4 +3Cl-
3 3
+5HO,故C错误;
2D.同浓度同体积NHHSO 溶液与NaOH溶液混合,只发生氢离子与氢氧根离子的反应,离子方
4 4
程式:H++OH-═HO,故D正确。
2
故选:D。
32.(2021·天津高三二模)下列离子方程式正确的是
Na S O H SO S O22H SSO H O
A. 2 2 3与稀 2 4混合: 2 3 2 2
HCOOH CO H O
B.碳酸氢钠溶液中加入氢氧化钠溶液: 3 2 2
FeOH FeOH 3H Fe33H O
C.向 3中加入氢碘酸溶液: 3 2
3Cu8H 2NO 3Cu2 2NO4H O
D.铜和浓硝酸反应: 3 2
【KS5U答案】A
【详解】
Na S O H SO
A. 2 2 3与稀 2 4混合反应生成二氧化硫和硫单质、水,离子方程式正确,故A正确;
B.碳酸氢钠溶液中加入氢氧化钠溶液反应生成碳酸钠和水,正确的离子方程式为:
HCOOH CO2-H O
3 3 2 ,故B错误;
FeOH
C.向 3中加入氢碘酸溶液发生酸碱中和反应和氧化还原反应,铁离子将碘离子氧化为
2FeOH 6H+2I- 2Fe2 6H O+I
碘单质,正确的离子方程式为: 3 2 2,故C错误;
D.铜和浓硝酸反应生成二氧化氮,正确的离子方程式为:
Cu4H 2NO Cu2 2NO 2H O
3 2 2 ,故D错误;
故选A。
33.(2021·辽宁高三三模)下列关于离子共存或离子方程式书写正确的是
2
A.某无色溶液中可能大量存在:H+、NH4、Cl-、CrO7
2
B.常温下,c(NH4)=c(Cl-)的NHCl和NH•HO的混合溶液中能大量存在:Fe3+、Cl-、NO3、
4 3 2
Al3+
C.向酸性KMnO 溶液中滴加HO:2MnO4+5HO+6H+=2Mn2++5O↑+8HO
4 2 2 2 2 2 2
通电
D.用惰性电极电解MgCl 水溶液:2Cl-+2HO 2OH-+Cl↑+H↑
2 2 2 2
【KS5U答案】C
【详解】
2
A.CrO7 有颜色,与溶液无色不符,故A错误;
2
B.常温下c(NH4)=c(Cl-)的NHCl和NH•HO的混合溶液呈中性,中性溶液中Fe3+完全水解生
4 3 2
成氢氧化铁沉淀,在中性溶液中不能大量存在,故B错误;
C.向酸性KMnO 溶液中滴加HO,发生氧化还原反应,根据得失电子守恒,电荷守恒和原子
4 2 2
守恒,反应的离子方程式为2MnO4+5HO+6H+═2Mn2++5O↑+8HO,故C正确;
2 2 2 2
通电
D.用惰性电极电解MgCl 水溶液,反应的离子方程式为Mg2++2Cl-+2HO
2 2
Mg(OH)↓+H↑+Cl↑,故D错误;
2 2 2
故选C。
34.(2021·广东茂名市·高三二模)化学与生活关系密切,解释下列应用的离子方程式正
确的是
选项 应用 解释(离子方程式)
A 淀粉—KI溶液(稀硫酸酸化)检验碘盐中含KIO 5I-+IO -+6H+=3I +3H O
3 3 2 2
B 电解饱和食盐水制氢气和氯气 2Cl-+2H+=Cl +H
2 2
C 醋酸用于除去水垢 2H++CaCO =Ca2++CO +H O
3 2 2
D 氯化铁用于蚀刻铜板 Fe3++Cu=Cu2++Fe2+
A.A B.B C.C D.D
【KS5U答案】A
【分析】
电解饱和食盐水的时候,注意水不拆,醋酸是弱电解质不能拆,另外离子方程式也要注意电
荷守恒问题。【详解】
A.电荷守恒,得失电子守恒,A正确;
通电
2Cl2H O Cl H 2OH
B.食盐水是中性,电解反应的离子方程式为 2 2 2 ,B错误;
C.醋酸是弱电解质,应该用分子式表示,正确的应该是
2CH COOH+CaCO =Ca2++ 2CH COO-+CO +H O
3 3 3 2 2 ,C错误;
2Fe3++Cu=Cu2++2Fe2+
D.电荷不守恒,正确的应该是 ,D错误;
【点睛】
弱酸是弱电解质不能拆;离子方程式要注意电荷守恒。
35.(2021·北京海淀区·人大附中高三三模)下列解释实验现象的离子方程式不正确的是
Cl +2OH-= Cl-+ClO-+H O
A.新制氯水中滴加NaOH溶液后,黄绿色褪去: 2 2
CO2+H O HCO+OH-
B.向NaCO 溶液中滴加酚酞溶液,溶液变红: 3 2 3
2 3
C.向Mg(OH) 悬浊液中滴加FeCl 溶液,生成红褐色沉淀:
2 3
3Mg(OH) +2 Fe3+=2Fe(OH) +3Mg2+
2 3
2S O2+4H+=SO2+3S+2H O
D.向NaSO 溶液中加入稀硫酸,溶液浑浊: 2 3 4 2
2 2 3
【KS5U答案】D
【详解】
A.新制氯水中滴加NaOH溶液后,黄绿色褪去,是氯气和氢氧化钠反应,反应的离子方程式
为:Cl+2OH-=Cl-+ClO-+HO,故A正确;
2 2
B.向NaCO 溶液中滴加酚酞溶液,溶液变红是碳酸根离子水解,溶液显碱性,反应的离子方
2 3
CO2+H O HCO+OH-
程式为 3 2 3 ,故B正确;
C.向Mg(OH) 悬浊液中滴加FeCl 溶液,生成红褐色沉淀,反应的离子方程式为:
2 3
3Mg(OH)+2Fe3+=2Fe(OH)+3Mg2+,故C正确;
2 3
D.向NaSO 溶液中加入稀硫酸,反应生成硫单质和二氧化硫气体,溶液变浑浊,反应的离
2 2 32-
子方程式为SO3 +2H+═SO↑+S↓+HO,故D错误;
2 2 2
故选D。
36.(2021·天津河西区·高三三模)下列能正确描述其变化的是
A.碳酸氢钠的电离:NaHCO
噲垐��
Na++HCO3
3
B.NO 通入水中制硝酸:2NO+HO=2H++NO3
2 2 2
C.向HO 溶液中滴加FeCl 溶液:2Fe3++HO=O↑+2H++2Fe2+
2 2 3 2 2 2
噲垐��
D.硬质酸钠溶液显碱性:C H COO-+HO C H COOH+OH-
17 35 2 17 35
【KS5U答案】D
【详解】
A.碳酸氢钠是弱酸的酸式盐,属于强电解质,其电离反应方程式为:NaHCO=Na++HCO3,故A
3
错误;
B.NO 通入水中发生反应生成硝酸和一氧化氮,其发生反应的离子方程式为:3NO+HO=2H+
2 2 2
+2NO3+ NO,故B错误;
C.向HO 溶液中滴加FeCl 溶液,FeCl 起了催化剂作用,故C 错误;
2 2 3 3
D.硬质酸钠属于强碱弱酸盐,所以硬质酸钠在水中发生了水解反应使溶液显碱性,所以该
噲垐��
反应的离子方程式为:C H COO-+HO C H COOH+OH-,故D正确;
17 35 2 17 35
故答案:D。
37.(2021·天津滨海新区·高三三模)下列离子方程式中正确的是
-
A.NaHCO 溶液与少量Ba(OH) 溶液混合:HCO3+ Ba2++OH-= BaCO↓+HO
3 2 3 2
B.CaO投入稀硫酸中:CaO+2H+=Ca2++HO
2
- SO2-
C.向稀硝酸中加入少量FeS:FeS+4H++3NO3=Fe3++ 4 +3NO↑+2HO
2
SO2-
D.SO 通入过量 NaClO溶液: HO+ SO+ClO-= 4 +2H++Cl-
2 2 2
【KS5U答案】C
【详解】- 2-
A.NaHCO 溶液与少量Ba(OH) 溶液混合:2HCO3+ Ba2++2OH-= BaCO↓+CO3 +2HO,故A错误;
3 2 3 2
SO2-
B.CaO投入稀硫酸中生成硫酸钙微溶,不拆:CaO+2H++ 4 =CaSO +HO,故B错误;
4 2
- SO2-
C.向稀硝酸中加入少量FeS,Fe和S均转化为高价态:FeS+4H++3NO3=Fe3++ 4
+3NO↑+2HO,故C正确;
2
D.SO 通入过量 NaClO溶液,反应生成得氢离子会和次氯酸根结合生成次氯酸: HO+
2 2
SO2-
SO+3ClO-= 4 +2HClO+Cl-,故D错误;
2
故选C。
38.(2021·湖南高三其他模拟)下列离子方程式能用于解释相应实验且书写正确的是
选项 实验 离子方程式
A FeS溶于足量稀硝酸 FeS+2H+=Fe2++HS↑
2
Δ
向沸水中滴加饱和FeCl 溶液并加热,得到红褐
B 3 Fe3++3HO Fe(OH)(胶体)+3H+
色液体 2 3
向NHHCO 溶液中加入过量Ba(OH) 稀溶液,有白
C 4 3 2 OH-+HCO+Ba2+=BaCO+HO
色沉淀产生 3 3 2
向KMnO 溶液(墨绿色)中加入适量醋酸,溶液变
D 2 4 3MnO24H 2MnO MnO 2H O
为紫色且有黑色沉淀生成 4 4 2 2
A.A B.B C.C D.D
【KS5U答案】B
【详解】
A.FeS固体与稀硝酸混合,硫离子和亚铁离子都被硝酸氧化,正确的离子方程式为:FeS+NO
3+4H+=Fe3++S↓+NO↑+2HO,A错误;
2
Δ
B.向沸水中滴加饱和FeCl 溶液并加热,得到氯化铁胶体,离子方程式为Fe3++3HO
3 2
Fe(OH)(胶体)+3H+,,B正确;
3
NH+ NH+
C.氢氧化钡过量, 4也会与OH-发生反应,离子方程式为 4+HCO3+Ba2++2OH-
=NH·HO+BaCO+HO,C错误;
3 2 3 22
D.醋酸为弱酸,不能写成离子,正确离子方程式为3MnO4 +4CHCOOH=2MnO4
3
+MnO+2HO+4CHCOO-,D错误;
2 2 3
综上所述答案为B。
39.(2021·江西高三二模)硫酸盐气溶胶作为PM2.5的主要构成成分,科学家最近发现了
一种“水分子桥”催化促进硫酸盐形成的化学机制如图所示,下列说法不正确的是
A.该机制可以解决SO 的空气污染问题
2
B.“水桥”的形成与氢键有关
C.HSO3与NO 间发生的总反应的离子方程式:HSO3+2NO+HO=2HNO+HSO4
2 2 2 2
D.电子传递可以促进HSO3中O—H键的解离,进而形成中间体SO3
【KS5U答案】A
【详解】
A.该机制可以解决二氧化氮形成的污染问题,A错误;
B.氢氧原子间的虚线表示氢键,所以水桥的形成与氢键有关,B正确;
C.从图分析HSO3与NO 间反应,最后得到亚硝酸和硫酸氢根离子,发生的总反应的离子方程
2
式:HSO3+2NO+HO=2HNO+HSO4,C正确;
2 2 2
D.电子传递可以促进HSO3中O—H键的解离,使氢原子与二氧化氮结合生成亚硝酸,同时形
成中间体SO3,D正确;
故选A。40.(2021·北京房山区·高三二模)下列解释实验事实的化学方程式正确的是
A.Na和Cl形成NaCl的过程:
B.用FeCl 溶液“腐蚀”覆铜板:Fe3++ Cu = Fe2+ + Cu2+
3
电解
C.用石墨电极电解CuCl 溶液:2Cl-+2H+ H↑+Cl↑
2 2 2
D.“84消毒液”中加少量醋增强漂白性:ClO-+H+= HClO
【KS5U答案】A
【详解】
A.NaCl为由钠离子和氯离子形成的离子化合物,其形成过程为:
,A正确;
B.选项所给离子方程式电荷不守恒,正确离子方程式为2Fe3++ Cu = 2Fe2+ + Cu2+,B错误;
电解
C.电解氯化铜溶液时,阴极Cu2+先放电,总反应为2Cl-+Cu2+ Cu+Cl↑,C错误;
2
D.醋酸为弱酸,不能写成离子,正确离子方程式为ClO-+CHCOOH=HClO+CHCOO-,D错误;
3 3
故选A。
41.(2021·广东珠海市·高三二模)下列关于离子共存或者离子反应的说法正确的是
0.1molL1CuSO K NH NO CO2
A. 4溶液可能大量存在: 、 4、 3、 3
CO OH HCO
B.用NaOH溶液吸收过量CO: 2 3
2
0.1molL1 K SO2 -
C. 氯化亚铁溶液:Na+、 、 4 、MnO4
Fe(OH) 3H Fe3 3H O
D.氢氧化铁和碘化氢溶液反应: 3 2
【KS5U答案】B
【详解】
0.1molL1CuSO
A. 4溶液中碳酸根离子与铜离子反应生成碳酸铜沉淀,不能大量共存,故A
错误;
B.氢氧化钠溶液与过量二氧化碳反应生成碳酸氢钠,反应的离子方程式为
CO OH HCO
2 3CO OH HCO
2 3,故B正确;
0.1molL1
C. 氯化亚铁溶液中高锰酸根离子能与亚铁离子发生氧化还原反应,不能大量共存,
故C错误;
D.氢氧化铁和碘化氢溶液反应生成碘化亚铁、碘和水,反应的离子方程式为
2Fe(OH) +6H++2I-=2Fe2++I +6H O
3 2 2 ,故D错误;
故选B。
42.(2021·辽宁高三其他模拟)某溶液中只可能含有
Na、NH、Fe2、Al3、Cl、SO2、CO2、AlO 0.1molL1
4 4 3 2 中的几种离子,各离子浓度均为 。
某同学进行了如下实验:
下列说法正确的是
A.无法确定原溶液中是否含有Na
NH、Fe2、Cl、SO2
B.原溶液中肯定存在的离子为 4 4
BaSO BaCO Al(OH)
C.沉淀A为 4,沉淀C为 3和 3
NH、Al3 Ba2
D.滤液X中大量存在的阳离子有 4 和
【KS5U答案】B
【详解】
CO2、AlO
加入过量稀硫酸无明显变化,说明溶液中无 3 2,前者会产生气体,后者会先产生沉
NO
淀后溶解 ;加入硝酸钡有气体产生,因为前面已经加入了硫酸, 3在酸性条件下具有强
氧化性,说明有亚铁离子存在且被氧化,沉淀A为硫酸钡;加入过量NaOH溶液有气体生成,NH CO CO
说明存在 4,气体为氨气,沉淀B为红褐色氢氧化铁沉淀;通入少量 2产生沉淀, 2
先与 OH 反应生成 CO 3 2 , CO 3 2 再与 Ba2 反应生成 BaCO 3沉淀,沉淀C为碳酸钡;因为存在
的离子浓度均为0.1molL1,从电荷守恒的角度出发,溶液中不存在Al3,只含有
NH
4
、Fe2、Cl、SO
4
2
才能保证电荷守恒,
Na
不能存在。
A.根据以上分析可知原溶液中不存在Na,A错误;
NH、Fe2、Cl、SO2
B.原溶液中肯定存在的离子有 4 4 ,B正确;
BaSO BaCO
C.沉淀A为 4,沉淀C为 3,C错误;
NH Fe2
D.滤液X中大量存在的阳离子有 4和 ,D错误;
答案选B。
43.(2021·湖北高三二模)下列离子方程式书写不正确的是
2-
A.将过量SO 气体通入NaClO溶液中:SO+HO+ClO-=SO4 +Cl-+2H+
2 2 2
B.标准状况下将112 mL氯气通入10 mL 1 mol·L-1溴化亚铁溶液中:2Fe2++4Br-
+3Cl=2Br+2Fe3++6Cl-
2 2
-
C.向FeSO 溶液中滴加NaHCO 溶液和稀氨水,产生大量白色沉淀:Fe2++HCO3
4 3
+
+NH·HO=FeCO↓+NH4+HO
3 2 3 2
2-
D.向明矾溶液中滴加Ba(OH) 溶液,使沉淀的物质的量最大时:2Al3++ 3SO4 + 3Ba2++6OH- =
2
2Al(OH)↓+3BaSO↓
3 4
【KS5U答案】B
【详解】
2- 2-
A.ClO-具有强氧化性,能将SO 氧化成SO4 ,则其离子方程式为:SO+HO+ClO-=SO4 +Cl-
2 2 2
+2H+,故A正确;
0.112L
B.标况下,112mL氯气的物质的量为nCl = =0.005mol,10 mL 1 mol·L-1溴化
2 22.4L/molnFeBr =0.01L1mol/L=0.01mol n Fe2 =0.01mol n Br =0.02mol
亚铁溶液中 2 , 、 ,
0.01molFe2 Cl 0.02molBr Cl Cl
需消耗0.005 2, 需消耗0.01mol 2, 2量不足,由于亚铁离子还
原性强于溴离子,所以该离子方程式为:2Fe2++Cl=2Fe3++2Cl-,故B错误;
2
C.FeSO 为强酸弱碱盐,其溶液因亚铁离子水解呈酸性,而NaHCO 溶液和稀氨水均呈碱性,
4 3
-
所以向FeSO 溶液中滴加NaHCO 溶液和稀氨水的离子方程式为:Fe2++HCO3
4 3
+
+NH·HO=FeCO↓+NH4+HO,故C正确;
3 2 3 2
D.明矾溶于水后会电离出铝离子,所以向明矾溶液中滴加Ba(OH) 溶液,使沉淀的物质的量
2
2-
最大时,则生成的氢氧化铝未溶解,则其离子方程式为:2Al3++ 3SO4 + 3Ba2++6OH- =
2Al(OH)↓+3BaSO↓,故D正确;
3 4
答案选B
44.(2021·云南曲靖市·高三二模)下列实验的反应原理用离子方程式表示正确的是
SO Na CO SO CO2 SO2 CO
A.少量 2通入 2 3溶液中: 2 3 3 2
电解
2Cl-+2HO Cl↑+H↑+2OH-
B.用惰性电极电解氯化镁溶液: 2 2 2
KAlSO
C.向 4 2溶液中加入足量Ba(OH) 溶液:
2
Al3 SO2Ba2 3OH BaSO Al(OH)
4 4 3
CuH O 2H Cu2 2H O
D.用双氧水和稀硫酸处理铜印刷电路板: 2 2 2
【KS5U答案】D
【详解】
2 2
A.SO 少量无法生成CO,离子方程式应为SO+2CO3 +HO=SO3 +2HCO3,A错误;
2 2 2 2
B.电解氯化镁溶液时阴极产生的氢氧根会和镁离子生成沉淀,离子方程式为Mg2++2Cl-+2HO
2
电解电解
Cl↑+H↑+Mg(OH)↓,B错误;
2 2 2
2
C.Ba(OH) 足量,最终会得到偏铝酸根,正确离子方程式为Al3++2SO4 +2Ba2++4OH-
2
=2BaSO↓+AlO2+2HO,C错误;
4 2
D.双氧水在酸性环境中会将Cu氧化为Cu2+,选项所给离子方程式无误,D正确;
综上所述答案为D。
45.(2021·广东高三其他模拟)常温下,下列各组离子在指定溶液中一定能大量共存的是
A.
c OH- =110-13molL-1
的溶液中:
Mg2 、K
、
SO2
4
、
NO
3
Na Cu2 HCO NO
B.使甲基橙呈红色的溶液: 、 、 3、 3
0.1molL1 KNO H Na SO2 S2
C. 的 3溶液: 、 、 4 、
D.
0.1molL1
的
BaCl
2溶液:
H
、
Na
、
Cl
、
SO2
4
【KS5U答案】A
【详解】
c OH- =110-13molL-1
A. 的溶液呈酸性,溶液中四种离子可以大量共存,A项正确;
HCO
B.使甲基橙呈红色的溶液量酸性, 3不能大量共存,B项错误;
NO
C.在酸性条件S2-与 3反应,不能大量共存,C项错误;
SO2
D.Ba2+与 4 反应生成BaSO,不能大量共存,D项错误;
4
答案选A。
46.(2021·广东高三其他模拟)下列指定反应的离子方程式正确的是
SO 2OH-+SO =SO2-+H O
A.用氨水吸收少量的 2气体: 2 3 2
B.
FeCl
3溶液与Cu的反应:
Cu+Fe3+=Cu2++Fe2+
NH N 3ClO-+2NH =N 3Cl-+3H O
C.加入NaClO将污水中的 3氧化成 2: 3 2 2NaHCO Ba(OH) HCO-+Ba2++OH-=BaCO H O
D. 3溶液中加入少量 2溶液: 3 3 2
【KS5U答案】C
【详解】
SO
A.用氨水吸收少量的 2气体生成亚硫酸铵和水,反应的离子方程式是2NH·HO+SO=2NH+
3 2 2 4
+SO2-+HO,故A错误;
3 2
B.
FeCl
3溶液与Cu的反应生成氯化亚铁和氯化铜,反应的离子方程式是
Cu+2Fe3+=Cu2++2Fe2+
,
故B错误;
NH N
C.加入NaClO将污水中的 3氧化成 2,反应的离子方程式是
3ClO-+2NH =N 3Cl-+3H O
3 2 2 ,故C正确 ;
NaHCO Ba(OH)
D. 3溶液中加入少量 2溶液生成碳酸钡沉淀、碳酸钠、水,反应的离子方程式
2HCO-+Ba2++2OH-=BaCO 2H O+CO2-
是 3 3 2 3 ,故D错误;
选C。
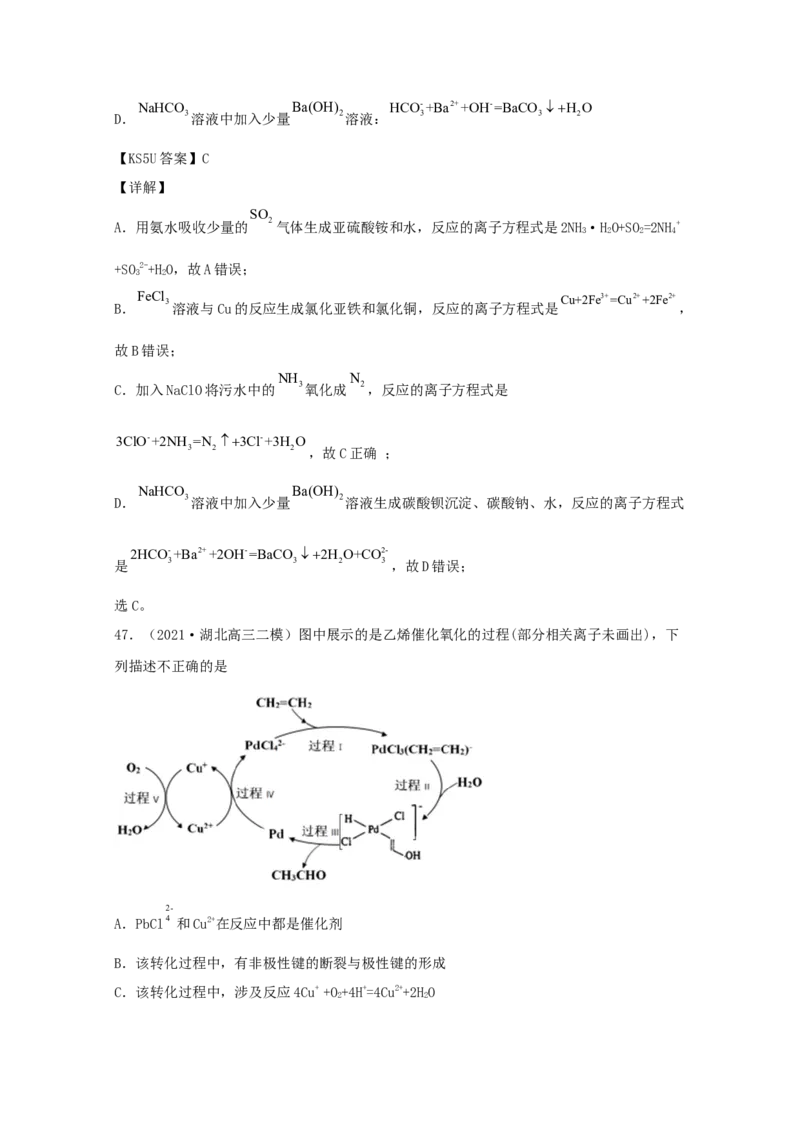
47.(2021·湖北高三二模)图中展示的是乙烯催化氧化的过程(部分相关离子未画出),下
列描述不正确的是
2-
A.PbCl4 和Cu2+在反应中都是催化剂
B.该转化过程中,有非极性键的断裂与极性键的形成
C.该转化过程中,涉及反应4Cu+ +O+4H+=4Cu2++2HO
2 2催化剂
D.乙烯催化氧化的反应方程式为CH=CH + O CHCHO+HO
2 2 2 3 2
【KS5U答案】D
【详解】
2 2
A.过程Ⅳ消耗Cu2+,过程Ⅴ生成Cu2+,过程Ⅰ消耗PbCl4 ,过程Ⅵ生成PbCl4 ,所以PbCl
2-
4 和Cu2+在反应中都是催化剂,故A正确;
B.过程V中O 转化为HO,O 中非极性键断裂,生成HO的过程中有极性键的形成,故B正确;
2 2 2 2
C.过程Ⅴ中O 与Cu+反应生成Cu2+,该过程的离子方程式为:4Cu+ +O+4H+=4Cu2++2HO,故C
2 2 2
正确;
D.反应中,CH=CH 最终被O 氧化为CHCHO,则乙烯催化氧化的反应方程式为:2CH=CH +
2 2 2 3 2 2
催化剂
O CHCHO,故D错误;
2 2 3
故选D。
48.(2021·重庆高三三模)能正确表示下列化学反应的离子方程式是()
电解
A.电解氯化镁溶液:Mg2++2HO+2Cl- H↑+Cl↑+Mg(OH)↓
2 2 2 2
2
B.硫酸镁溶液跟氢氧化钡溶液反应:SO4 +Ba2+=BaSO↓
4
C.金属镁与醋酸反应,有氢气产生:Mg+2H+=Mg2++H↑
2
D.碳酸钠溶液与盐酸反应,有气泡逸出:NaCO+2H+=2Na++HO+CO↑
2 3 2 2
【KS5U答案】A
【详解】
电解
A.用惰性电极电解氯化镁溶液的离子反应为Mg2++2HO+2Cl-
2
H↑+Cl↑+Mg(OH)↓,故A正确;
2 2 2
2-
B.硫酸镁溶液跟氢氧化钡溶液反应:Mg2++2OH-+SO4 +Ba2+═BaSO↓+Mg(OH)↓,故B错误;
4 2
C.醋酸为弱酸,应写成化学式,正确的离子方程式为 Mg+2CHCOOH=2CHCOO-+Mg2++H↑,故C
3 3 2
错误;2-
D.碳酸钠溶液与盐酸反应,有气泡逸出的离子反应为CO3 +2H+═HO+CO↑,故D错误;
2 2
故选:A。
49.(2021·天津高三三模)下列化学用语表述不正确的是
电解
Mg2++2Cl- Mg+Cl↑
A.电解MgCl 溶液: 2
2
K Fe(CN) Fe2:2Fe(CN) 3 3Fe2=Fe Fe(CN)
B.使用 3 6 检验 6 3 6 2
Al3 3HCO Al(OH) 3CO
C.泡沫灭火器工作原理: 3 3 2
D. NH 4 Cl 在水中发生水解: NH 4 H 2 O NH 3 H 2 OH
【KS5U答案】A
【详解】
通电
A.用惰性电极电解MgCl 溶液的离子反应为Mg2++2Cl-+2HO==Mg(OH)↓+H↑+Cl↑,故A错
2 2 2 2 2
误;
2Fe(CN) 3 3Fe2=Fe Fe(CN)
B.K 3 [Fe(CN) 6 ]检验Fe2+生成蓝色沉淀,离子反应为 6 3 6 2 ,故
B正确;
Al3 3HCO Al(OH) 3CO
C.发生相互促进水解反应生成沉淀和气体,离子反应为 3 3 2 ,
故C正确;
D.NHCl是强酸弱碱盐,铵根在水中能发生水解,存在平衡,用“ ”使溶液显酸性:
4
NH
4
H
2
O
NH
3
H
2
OH
,故D正确;
故选:A。
50.(2021·辽宁高三其他模拟)下列各组离子在给定条件下,因发生配合反应而不能大量
共存的一组是
pH2 K Na Cl CO2
A. 的溶液中: 、 、 、 3
B.含大量 Al(OH) 4 的溶液:Cu2、 NO 3 、 Mg2 、ClC.含有大量
Fe3
的溶液:
Na
、
NH
4
、
SO2
4
、
CN
SO K Na ClO SO2
D.溶解少量 2气体的溶液: 、 、 、 4
【KS5U答案】C
【分析】
分子或离子与金属离子结合形成很稳定的新的离子的过程叫配位反应,也称配合反应。
【详解】
pH2 CO2
A. 的溶液中,溶液中含有大量的H+,H+会与 3 反应生成二氧化碳和水,是复分解
反应,不是配合反应,故A错误;
Al(OH)
B. 4 和Cu2发生双水解反应,不是配合反应,故B错误;
Fe3 CN
C. 和 反应生成铁氰配合物,该反应为配合反应,故C正确;
SO ClO SO2
D. 2溶于水生成亚硫酸,亚硫酸具有还原性,会和 反应生成 4 和Cl-,发生的是氧
化还原反应,不是配合反应,故D错误;
答案选C。