文档内容
专题 04 氧化还原反应
1.(2021·广东高考真题)宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应的反应
方程式书写正确的是
A. 放入水中:
B. 通过灼热铁粉:
C.铜丝插入热的浓硫酸中:
D. 通入酸性 溶液中:
2.(2021·湖南高考真题) 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步
反应为 。下列说法错误的是
A.产生22.4L(标准状况) 时,反应中转移
B.反应中氧化剂和还原剂的物质的量之比为11:6
C.可用石灰乳吸收反应产生的 制备漂白粉
D.可用酸化的淀粉碘化钾溶液检验食盐中 的存在
3.(2021·浙江高考真题)关于反应KHIO +9HI=2KI+4I +6H O,下列说法正确的是
2 3 6 2 2
A. KHIO 发生氧化反应
2 3 6
B.KI是还原产物
C.生成12.7g I 时,转移0.1mol电子
2
D.还原剂与氧化剂的物质的量之比为7:1
4.(2021·浙江高考真题)关于化合物 的性质,下列推测不合理的是
A.具有强氧化性 B.与 溶液反应可生成两种钠盐C.与盐酸作用能产生氯气 D.水解生成盐酸和硝酸
5.(2021·浙江高考真题)关于反应8NH +6NO=7N +12H O,下列说法正确的是
3 2 2 2
A.NH 中H元素被氧化
3
B.NO 在反应过程中失去电子
2
C.还原剂与氧化剂的物质的量之比为3:4
D.氧化产物与还原产物的质量之比为4:3
6.(2021·浙江高考真题)下列“类比”合理的是
A.Na与HO反应生成NaOH和H,则Fe与HO反应生成Fe(OH) 和H
2 2 2 3 2
B.NaClO溶液与CO 反应生成NaHCO 和HClO,则NaClO溶液与SO 反应生成NaHSO 和HClO
2 3 2 3
C.NaN与盐酸反应生成NaCl和NH Cl,则MgN 与盐酸反应生成MgCl 和NH Cl
3 4 3 2 2 4
D.NaOH溶液与少量AgNO 溶液反应生成Ag O和NaNO ,则氨水与少量AgNO 溶液反应生成Ag O和
3 2 3 3 2
NH NO
4 3
1.(2021·上海静安区·高三二模)反应2NaSO+I → 2NaI+ Na SO 常用于定量分析。下列相关说法错误
2 2 3 2 2 4 6
的是
A.反应中,每生成1 mol Na SO,就有4 mol 电子发生转移
2 4 6
B.反应中,I 表现了氧化性
2
C.I 被还原,NaSO 是氧化产物
2 2 4 6
D.NaSO 溶液最好即配即用,久置空气易被氧化,可能生成NaSO
2 2 3 2 4
2.(2021·广东高三模拟)化学与生活密切相关,下列叙述不涉及氧化还原反应的是
A.煅烧贝壳,将产物投入海水中以获得
B.用小麦、大米、玉米、高粱、糯米五种粮食发酵酿酒
C.将在酒精灯上灼烧后的铜丝迅速插入乙醇中,能闻到刺激性气味
D.将乙烯通人酸性高锰酸钾溶液中,溶液紫色褪去
3.(2021·浙江高三三模)关于反应 ,下列说法不正确的是
A. 中 元素被氧化 B. 在反应过程中得到电子
C.还原剂与氧化剂的物质的量之比为 D. 既是氧化产物又是还原产物
4.(2021·安徽宣城市·高三二模)“84”消毒液和“洁厕灵”混用时,因易发生反应引起中毒,若反应为:
Na35ClO+2H37Cl=NaCl+Cl ↑+H O。下列说法正确的是[设N 为阿伏加德罗常数的值,已知:
2 2 AK(HClO)=3.0×10-8,K (H CO)=4.3×10-7,K (H CO)=5.6×10-11]
a1 2 3 a2 2 3
A.理论上,上述反应生成的1 mol Cl 含有的中子数为40 N
2 A
B.“84”消毒液在空气中会发生反应:NaClO+CO +H O=NaHCO +HClO
2 2 3
C.理论上,上述反应每转移N 个电子,氧化剂比还原剂少2g
A
D.为提高氯水中HClO的浓度,可加过量KCO 固体
2 3
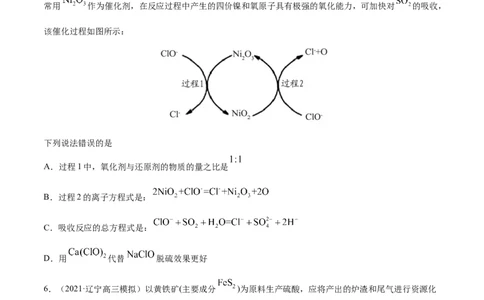
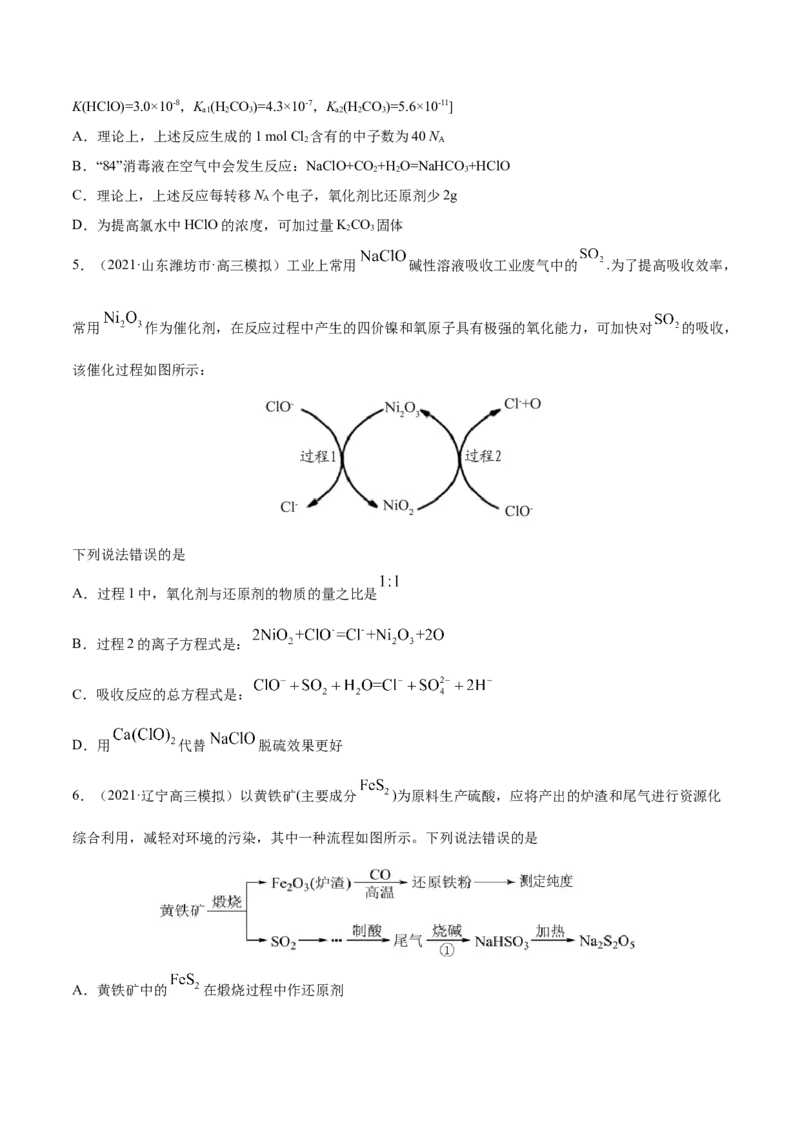
5.(2021·山东潍坊市·高三模拟)工业上常用 碱性溶液吸收工业废气中的 .为了提高吸收效率,
常用 作为催化剂,在反应过程中产生的四价镍和氧原子具有极强的氧化能力,可加快对 的吸收,
该催化过程如图所示:
下列说法错误的是
A.过程1中,氧化剂与还原剂的物质的量之比是
B.过程2的离子方程式是:
C.吸收反应的总方程式是:
D.用 代替 脱硫效果更好
6.(2021·辽宁高三模拟)以黄铁矿(主要成分 )为原料生产硫酸,应将产出的炉渣和尾气进行资源化
综合利用,减轻对环境的污染,其中一种流程如图所示。下列说法错误的是
A.黄铁矿中的 在煅烧过程中作还原剂B.欲得到更纯的 ,反应①应通入过量的 气体
C.还原铁粉用盐酸溶解后,可用 溶液滴定法来测定其纯度
D.加热 制备 的化学方程式为
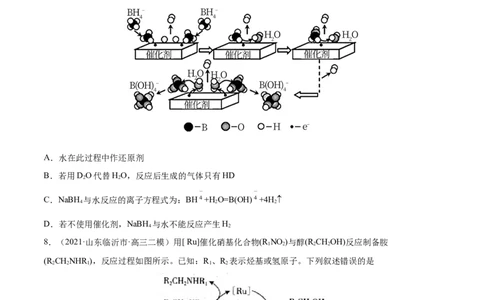
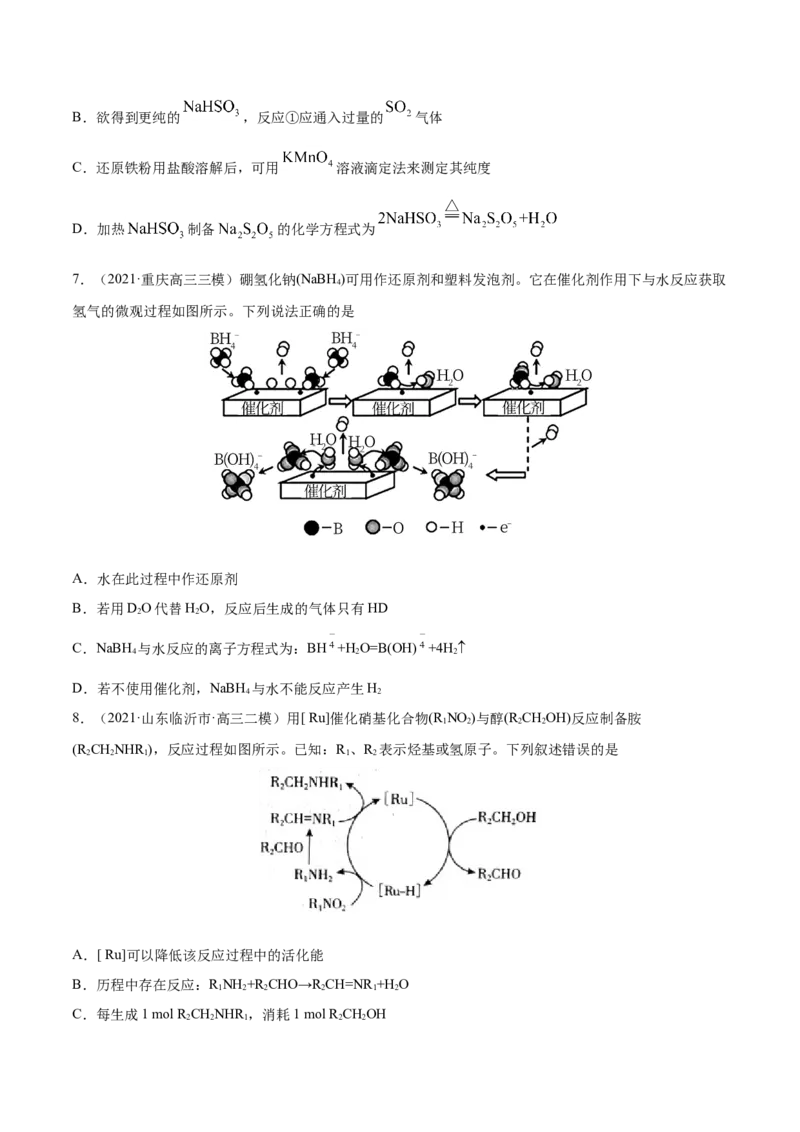
7.(2021·重庆高三三模)硼氢化钠(NaBH )可用作还原剂和塑料发泡剂。它在催化剂作用下与水反应获取
4
氢气的微观过程如图所示。下列说法正确的是
A.水在此过程中作还原剂
B.若用DO代替HO,反应后生成的气体只有HD
2 2
C.NaBH 与水反应的离子方程式为:BH +H O=B(OH) +4H
4 2 2
D.若不使用催化剂,NaBH 与水不能反应产生H
4 2
8.(2021·山东临沂市·高三二模)用[ Ru]催化硝基化合物(R NO )与醇(R CHOH)反应制备胺
1 2 2 2
(R CHNHR ),反应过程如图所示。已知:R 、R 表示烃基或氢原子。下列叙述错误的是
2 2 1 1 2
A.[ Ru]可以降低该反应过程中的活化能
B.历程中存在反应:R NH +R CHO→R CH=NR +H O
1 2 2 2 1 2
C.每生成1 mol R CHNHR ,消耗1 mol R CHOH
2 2 1 2 2D.制备CHCHNHCH 的原料可以是CHCHNO 和CHOH
3 2 3 3 2 2 3
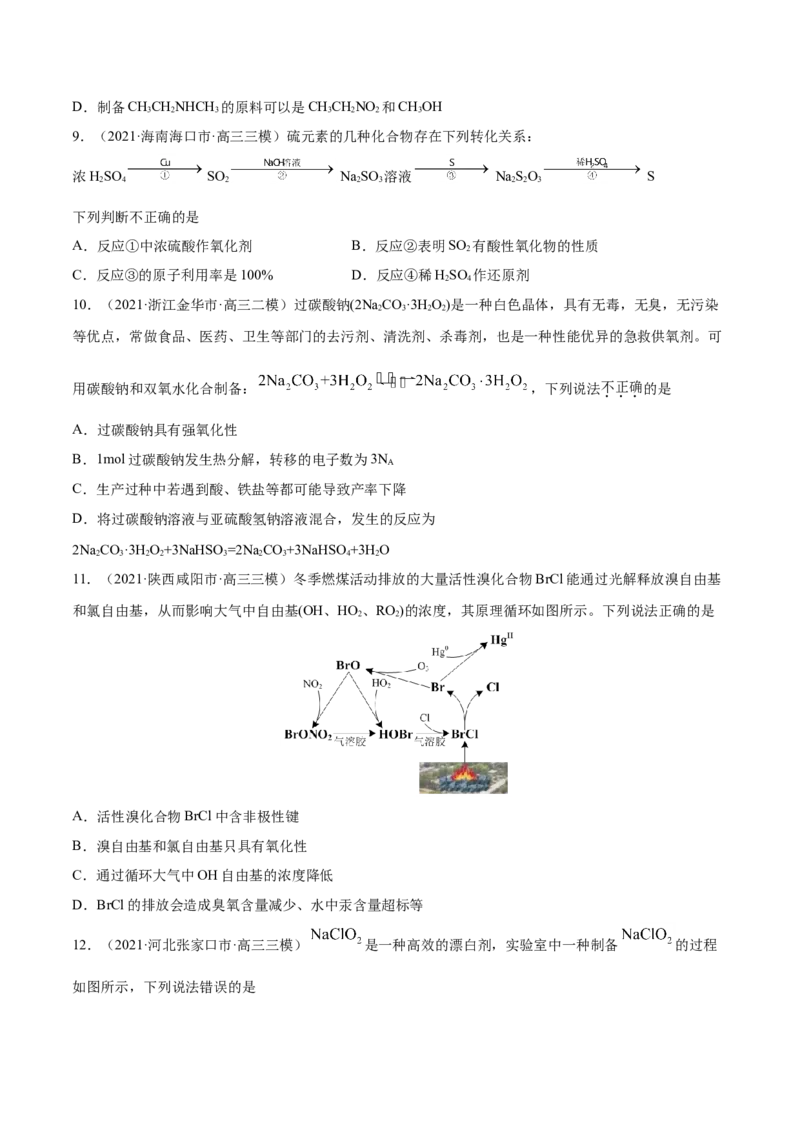
9.(2021·海南海口市·高三三模)硫元素的几种化合物存在下列转化关系:
浓HSO SO Na SO 溶液 NaSO S
2 4 2 2 3 2 2 3
下列判断不正确的是
A.反应①中浓硫酸作氧化剂 B.反应②表明SO 有酸性氧化物的性质
2
C.反应③的原子利用率是100% D.反应④稀HSO 作还原剂
2 4
10.(2021·浙江金华市·高三二模)过碳酸钠(2Na CO·3H O)是一种白色晶体,具有无毒,无臭,无污染
2 3 2 2
等优点,常做食品、医药、卫生等部门的去污剂、清洗剂、杀毒剂,也是一种性能优异的急救供氧剂。可
用碳酸钠和双氧水化合制备: ,下列说法不正确的是
A.过碳酸钠具有强氧化性
B.1mol过碳酸钠发生热分解,转移的电子数为3N
A
C.生产过种中若遇到酸、铁盐等都可能导致产率下降
D.将过碳酸钠溶液与亚硫酸氢钠溶液混合,发生的反应为
2NaCO·3H O+3NaHSO =2Na CO+3NaHSO +3H O
2 3 2 2 3 2 3 4 2
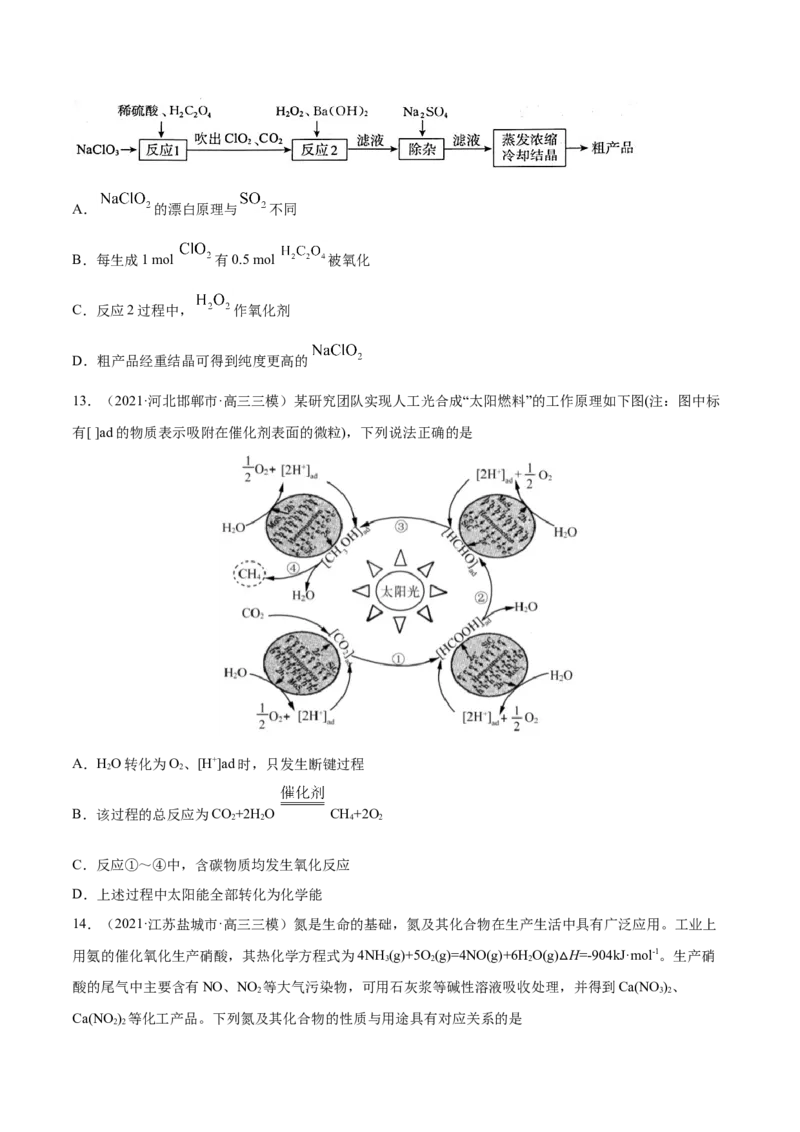
11.(2021·陕西咸阳市·高三三模)冬季燃煤活动排放的大量活性溴化合物BrCl能通过光解释放溴自由基
和氯自由基,从而影响大气中自由基(OH、HO 、RO)的浓度,其原理循环如图所示。下列说法正确的是
2 2
A.活性溴化合物BrCl中含非极性键
B.溴自由基和氯自由基只具有氧化性
C.通过循环大气中OH自由基的浓度降低
D.BrCl的排放会造成臭氧含量减少、水中汞含量超标等
12.(2021·河北张家口市·高三三模) 是一种高效的漂白剂,实验室中一种制备 的过程
如图所示,下列说法错误的是A. 的漂白原理与 不同
B.每生成1 mol 有0.5 mol 被氧化
C.反应2过程中, 作氧化剂
D.粗产品经重结晶可得到纯度更高的
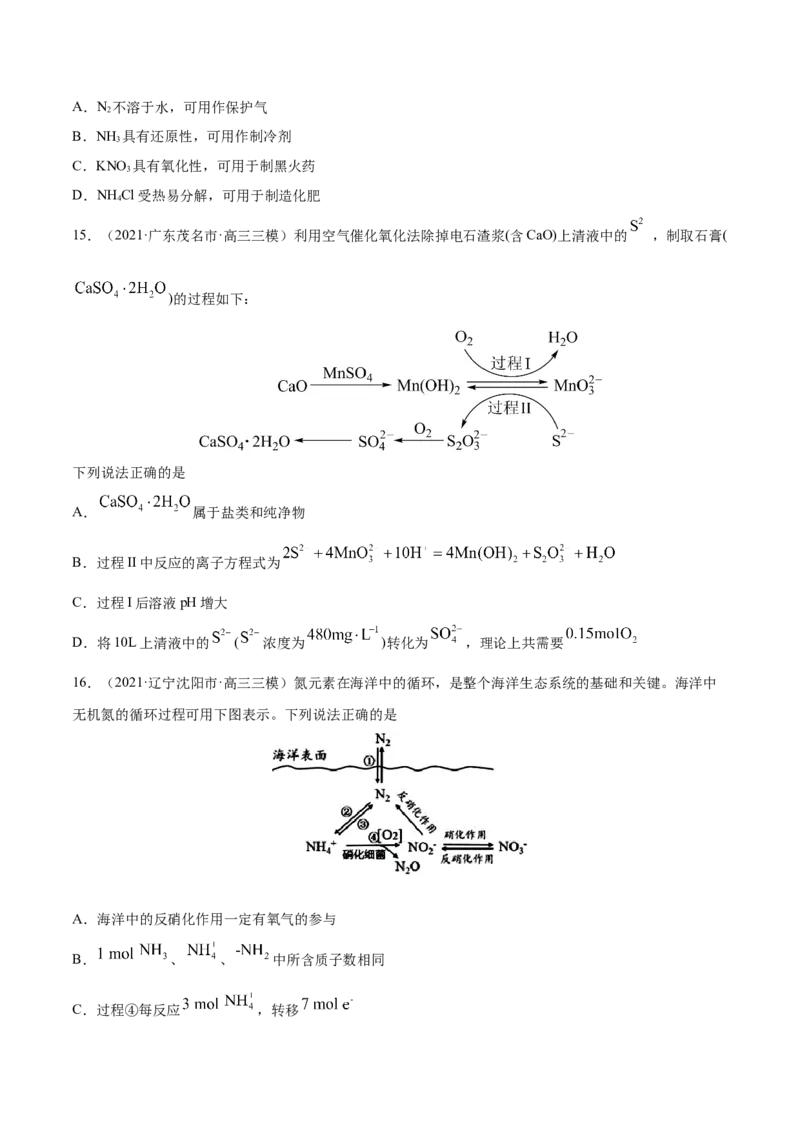
13.(2021·河北邯郸市·高三三模)某研究团队实现人工光合成“太阳燃料”的工作原理如下图(注:图中标
有[ ]ad的物质表示吸附在催化剂表面的微粒),下列说法正确的是
A.HO转化为O、[H+]ad时,只发生断键过程
2 2
B.该过程的总反应为CO+2H O CH +2O
2 2 4 2
C.反应①~④中,含碳物质均发生氧化反应
D.上述过程中太阳能全部转化为化学能
14.(2021·江苏盐城市·高三三模)氮是生命的基础,氮及其化合物在生产生活中具有广泛应用。工业上
用氨的催化氧化生产硝酸,其热化学方程式为4NH (g)+5O(g)=4NO(g)+6H O(g) H=-904kJ·mol-1。生产硝
3 2 2
酸的尾气中主要含有NO、NO 等大气污染物,可用石灰浆等碱性溶液吸收处理△,并得到Ca(NO )、
2 3 2
Ca(NO ) 等化工产品。下列氮及其化合物的性质与用途具有对应关系的是
2 2A.N 不溶于水,可用作保护气
2
B.NH 具有还原性,可用作制冷剂
3
C.KNO 具有氧化性,可用于制黑火药
3
D.NH Cl受热易分解,可用于制造化肥
4
15.(2021·广东茂名市·高三三模)利用空气催化氧化法除掉电石渣浆(含CaO)上清液中的 ,制取石膏(
)的过程如下:
下列说法正确的是
A. 属于盐类和纯净物
B.过程II中反应的离子方程式为
C.过程I后溶液pH增大
D.将10L上清液中的 ( 浓度为 )转化为 ,理论上共需要
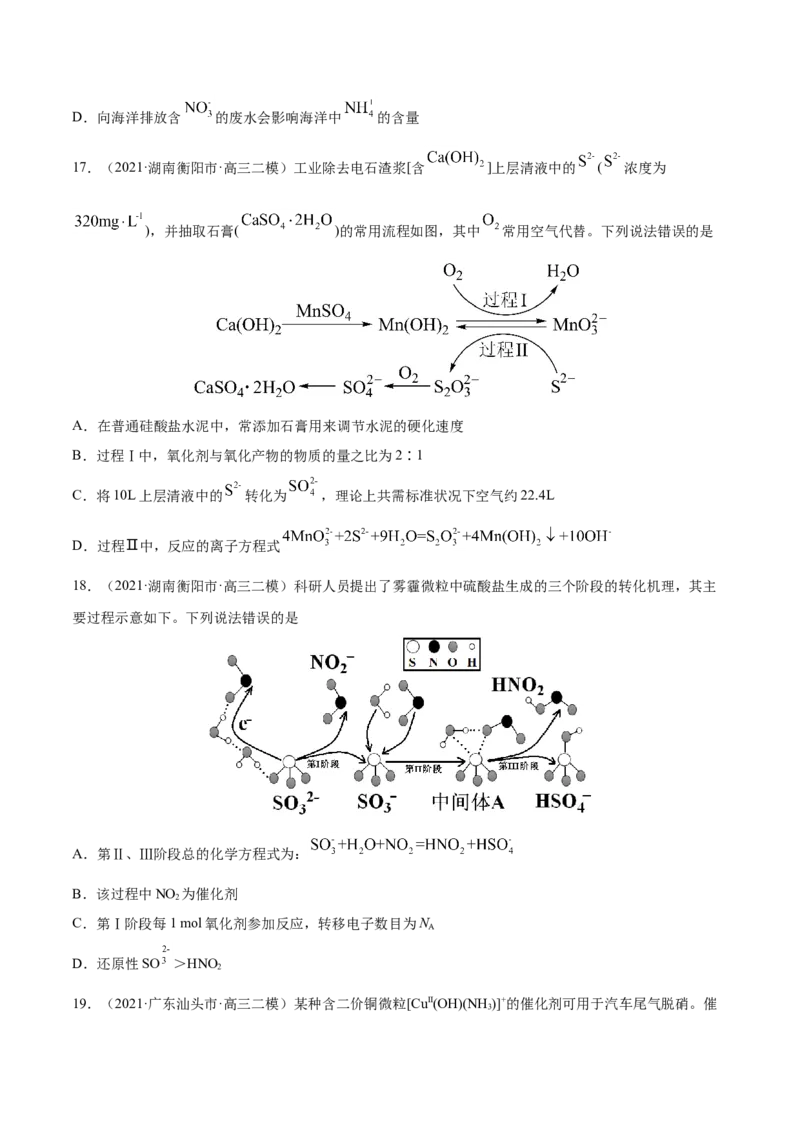
16.(2021·辽宁沈阳市·高三三模)氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中
无机氮的循环过程可用下图表示。下列说法正确的是
A.海洋中的反硝化作用一定有氧气的参与
B. 、 、 中所含质子数相同
C.过程④每反应 ,转移D.向海洋排放含 的废水会影响海洋中 的含量
17.(2021·湖南衡阳市·高三二模)工业除去电石渣浆[含 ]上层清液中的 ( 浓度为
),并抽取石膏( )的常用流程如图,其中 常用空气代替。下列说法错误的是
A.在普通硅酸盐水泥中,常添加石膏用来调节水泥的硬化速度
B.过程Ⅰ中,氧化剂与氧化产物的物质的量之比为2∶1
C.将10L上层清液中的 转化为 ,理论上共需标准状况下空气约22.4L
D.过程Ⅱ中,反应的离子方程式
18.(2021·湖南衡阳市·高三二模)科研人员提出了雾霾微粒中硫酸盐生成的三个阶段的转化机理,其主
要过程示意如下。下列说法错误的是
A.第Ⅱ、Ⅲ阶段总的化学方程式为:
B.该过程中NO 为催化剂
2
C.第Ⅰ阶段每1 mol氧化剂参加反应,转移电子数目为N
A
D.还原性SO >HNO
2
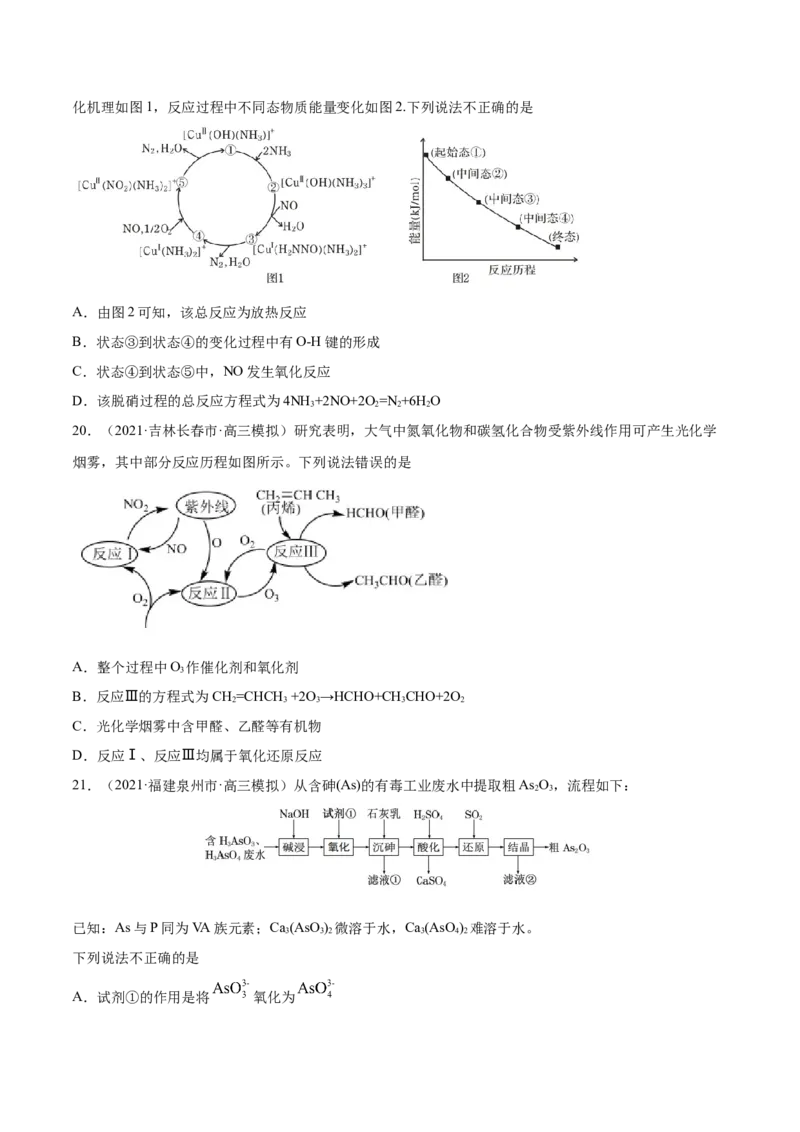
19.(2021·广东汕头市·高三二模)某种含二价铜微粒[CuII(OH)(NH )]+的催化剂可用于汽车尾气脱硝。催
3化机理如图1,反应过程中不同态物质能量变化如图2.下列说法不正确的是
A.由图2可知,该总反应为放热反应
B.状态③到状态④的变化过程中有O-H键的形成
C.状态④到状态⑤中,NO发生氧化反应
D.该脱硝过程的总反应方程式为4NH +2NO+2O=N +6H O
3 2 2 2
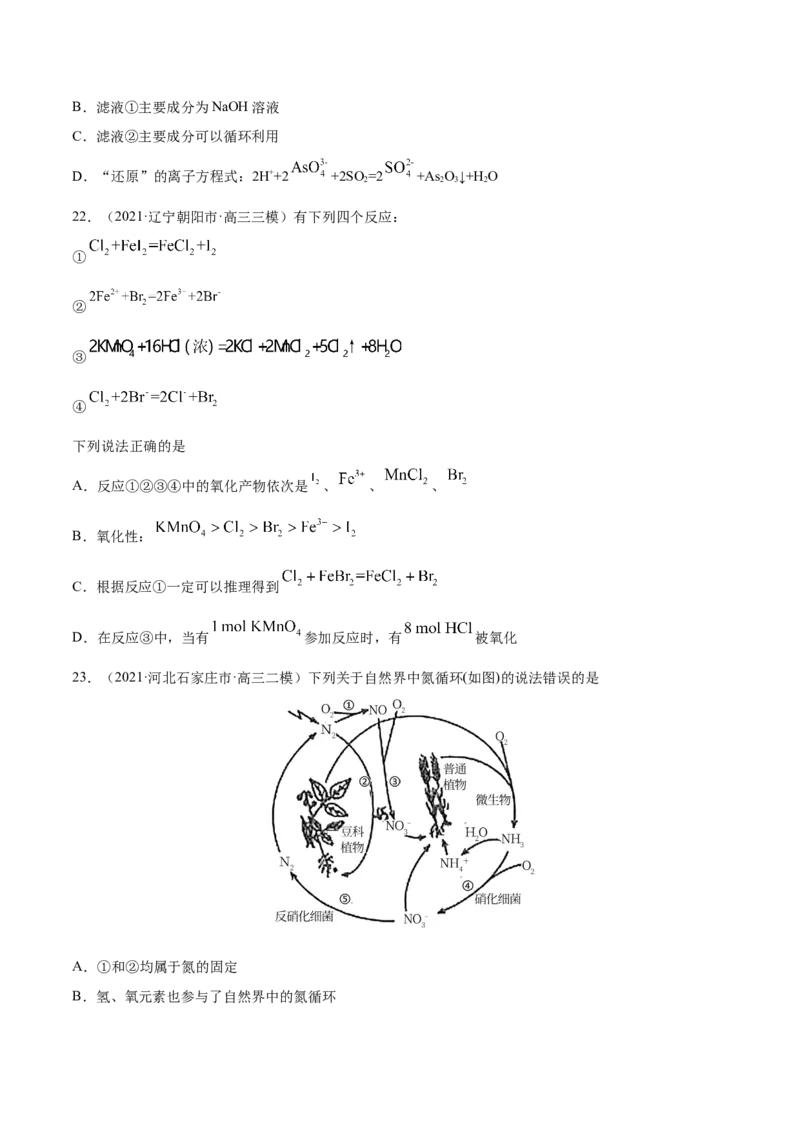
20.(2021·吉林长春市·高三模拟)研究表明,大气中氮氧化物和碳氢化合物受紫外线作用可产生光化学
烟雾,其中部分反应历程如图所示。下列说法错误的是
A.整个过程中O 作催化剂和氧化剂
3
B.反应Ⅲ的方程式为 CH=CHCH +2O →HCHO+CH CHO+2O
2 3 3 3 2
C.光化学烟雾中含甲醛、乙醛等有机物
D.反应Ⅰ、反应Ⅲ均属于氧化还原反应
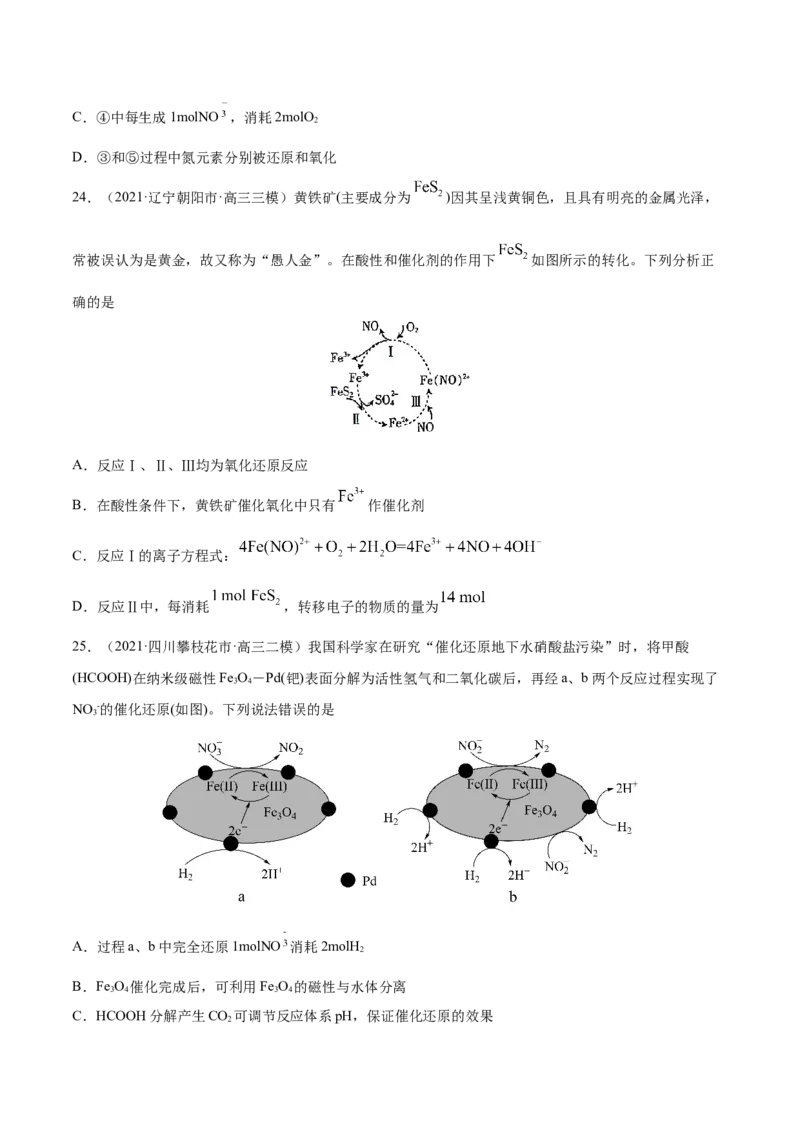
21.(2021·福建泉州市·高三模拟)从含砷(As)的有毒工业废水中提取粗As O,流程如下:
2 3
已知:As与P同为VA族元素;Ca (AsO) 微溶于水,Ca (AsO) 难溶于水。
3 3 2 3 4 2
下列说法不正确的是
A.试剂①的作用是将 氧化为B.滤液①主要成分为NaOH溶液
C.滤液②主要成分可以循环利用
D.“还原”的离子方程式:2H++2 +2SO=2 +AsO↓+H O
2 2 3 2
22.(2021·辽宁朝阳市·高三三模)有下列四个反应:
①
②
③
④
下列说法正确的是
A.反应①②③④中的氧化产物依次是 、 、 、
B.氧化性:
C.根据反应①一定可以推理得到
D.在反应③中,当有 参加反应时,有 被氧化
23.(2021·河北石家庄市·高三二模)下列关于自然界中氮循环(如图)的说法错误的是
A.①和②均属于氮的固定
B.氢、氧元素也参与了自然界中的氮循环C.④中每生成1molNO ,消耗2molO
2
D.③和⑤过程中氮元素分别被还原和氧化
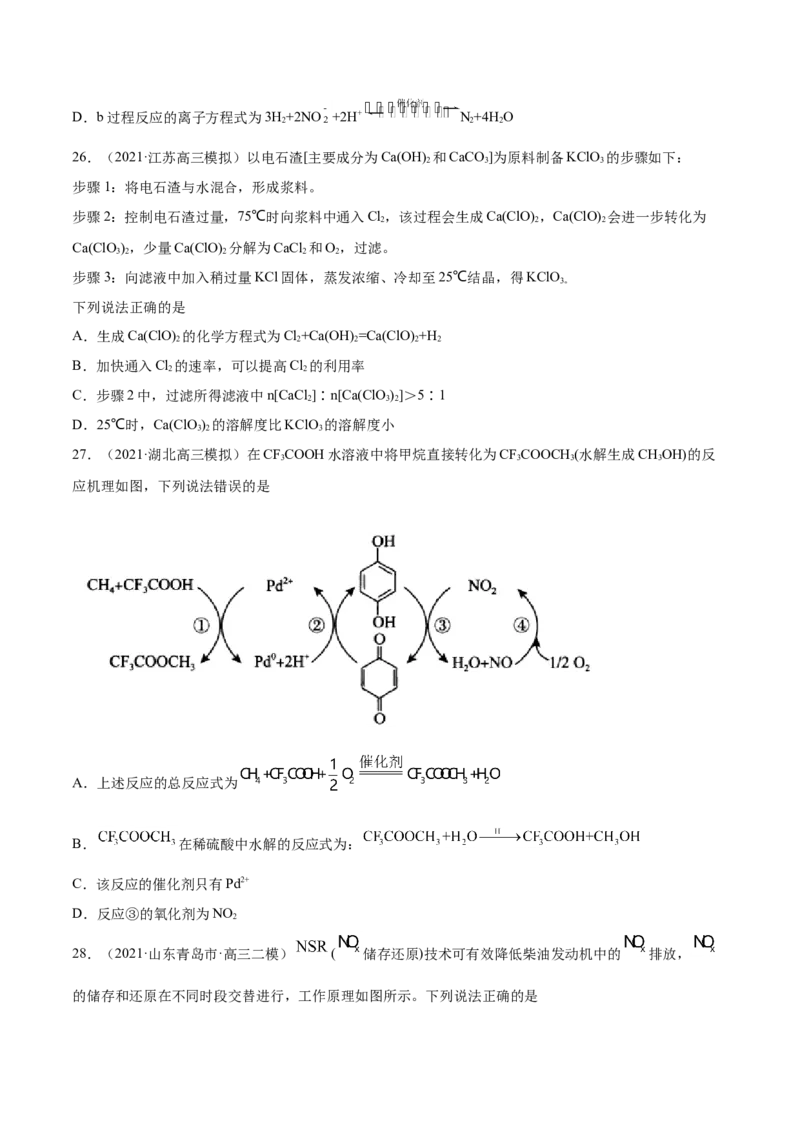
24.(2021·辽宁朝阳市·高三三模)黄铁矿(主要成分为 )因其呈浅黄铜色,且具有明亮的金属光泽,
常被误认为是黄金,故又称为“愚人金”。在酸性和催化剂的作用下 如图所示的转化。下列分析正
确的是
A.反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应
B.在酸性条件下,黄铁矿催化氧化中只有 作催化剂
C.反应Ⅰ的离子方程式:
D.反应Ⅱ中,每消耗 ,转移电子的物质的量为
25.(2021·四川攀枝花市·高三二模)我国科学家在研究“催化还原地下水硝酸盐污染”时,将甲酸
(HCOOH)在纳米级磁性Fe O-Pd(钯)表面分解为活性氢气和二氧化碳后,再经a、b两个反应过程实现了
3 4
NO -的催化还原(如图)。下列说法错误的是
3
A.过程a、b中完全还原1molNO 消耗2molH
2
B.Fe O 催化完成后,可利用Fe O 的磁性与水体分离
3 4 3 4
C.HCOOH分解产生CO 可调节反应体系pH,保证催化还原的效果
2D.b过程反应的离子方程式为3H+2NO +2H+ N+4H O
2 2 2
26.(2021·江苏高三模拟)以电石渣[主要成分为Ca(OH) 和CaCO ]为原料制备KClO 的步骤如下:
2 3 3
步骤1:将电石渣与水混合,形成浆料。
步骤2:控制电石渣过量,75℃时向浆料中通入Cl,该过程会生成Ca(ClO) ,Ca(ClO) 会进一步转化为
2 2 2
Ca(ClO ),少量Ca(ClO) 分解为CaCl 和O,过滤。
3 2 2 2 2
步骤3:向滤液中加入稍过量KCl固体,蒸发浓缩、冷却至25℃结晶,得KClO
3。
下列说法正确的是
A.生成Ca(ClO) 的化学方程式为Cl+Ca(OH) =Ca(ClO) +H
2 2 2 2 2
B.加快通入Cl 的速率,可以提高Cl 的利用率
2 2
C.步骤2中,过滤所得滤液中n[CaCl ]∶n[Ca(ClO )]>5∶1
2 3 2
D.25℃时,Ca(ClO ) 的溶解度比KClO 的溶解度小
3 2 3
27.(2021·湖北高三模拟)在CFCOOH水溶液中将甲烷直接转化为CFCOOCH (水解生成CHOH)的反
3 3 3 3
应机理如图,下列说法错误的是
A.上述反应的总反应式为
B. 在稀硫酸中水解的反应式为:
C.该反应的催化剂只有Pd2+
D.反应③的氧化剂为NO
2
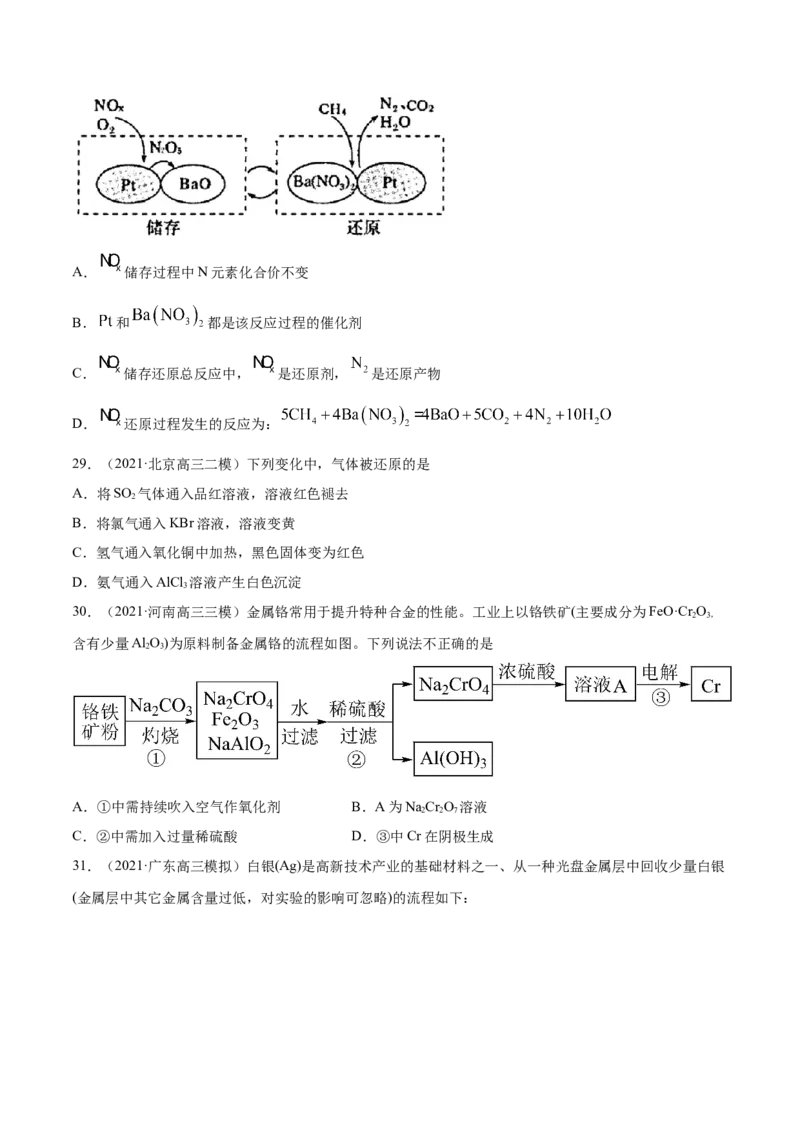
28.(2021·山东青岛市·高三二模) ( 储存还原)技术可有效降低柴油发动机中的 排放,
的储存和还原在不同时段交替进行,工作原理如图所示。下列说法正确的是A. 储存过程中N元素化合价不变
B. 和 都是该反应过程的催化剂
C. 储存还原总反应中, 是还原剂, 是还原产物
D. 还原过程发生的反应为:
29.(2021·北京高三二模)下列变化中,气体被还原的是
A.将SO 气体通入品红溶液,溶液红色褪去
2
B.将氯气通入KBr溶液,溶液变黄
C.氢气通入氧化铜中加热,黑色固体变为红色
D.氨气通入AlCl 溶液产生白色沉淀
3
30.(2021·河南高三三模)金属铬常用于提升特种合金的性能。工业上以铬铁矿(主要成分为FeO·Cr O
2 3,
含有少量Al O)为原料制备金属铬的流程如图。下列说法不正确的是
2 3
A.①中需持续吹入空气作氧化剂 B.A为NaCr O 溶液
2 2 7
C.②中需加入过量稀硫酸 D.③中Cr在阴极生成
31.(2021·广东高三模拟)白银(Ag)是高新技术产业的基础材料之一、从一种光盘金属层中回收少量白银
(金属层中其它金属含量过低,对实验的影响可忽略)的流程如下:下列叙述不正确的是
A.“氧化”阶段需在80℃条件下进行,可用水浴加热
B.“操作1”所用到的玻璃仪器是玻璃棒、烧杯、漏斗
C.若“还原”过程通过原电池来实现,则N 为正极产物
2
D.“还原”过程中参加反应的n[Ag(NH) ]∶n[N H·H O]=4∶1
3 2 4 2
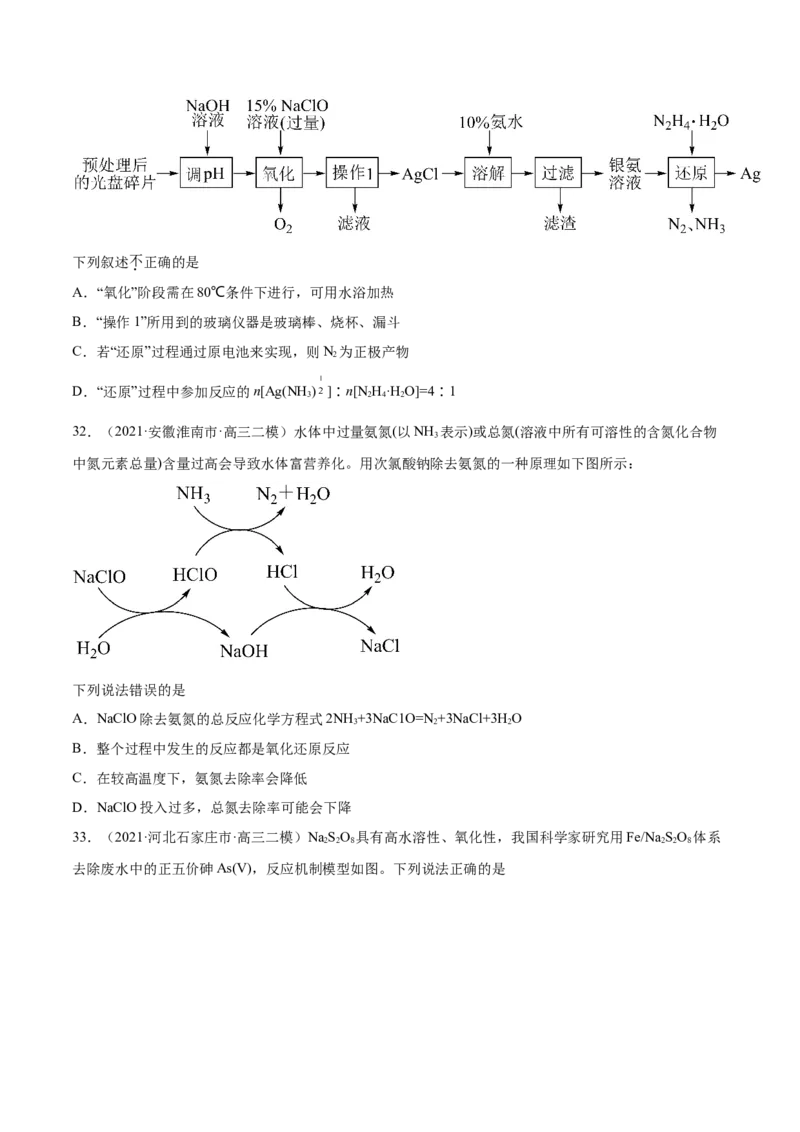
32.(2021·安徽淮南市·高三二模)水体中过量氨氮(以NH 表示)或总氮(溶液中所有可溶性的含氮化合物
3
中氮元素总量)含量过高会导致水体富营养化。用次氯酸钠除去氨氮的一种原理如下图所示:
下列说法错误的是
A.NaClO除去氨氮的总反应化学方程式2NH +3NaC1O=N +3NaCl+3HO
3 2 2
B.整个过程中发生的反应都是氧化还原反应
C.在较高温度下,氨氮去除率会降低
D.NaClO投入过多,总氮去除率可能会下降
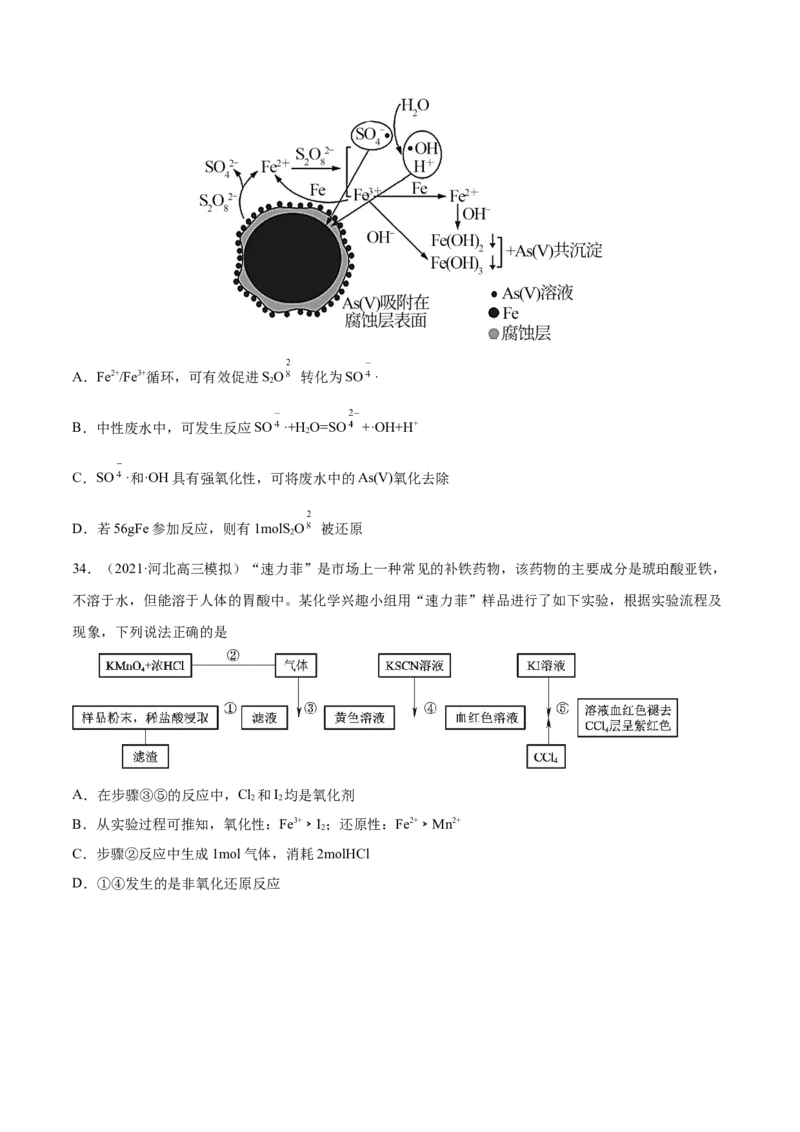
33.(2021·河北石家庄市·高三二模)NaSO 具有高水溶性、氧化性,我国科学家研究用Fe/Na SO 体系
2 2 8 2 2 8
去除废水中的正五价砷As(V),反应机制模型如图。下列说法正确的是A.Fe2+/Fe3+循环,可有效促进SO 转化为SO ·
2
B.中性废水中,可发生反应SO ·+H O=SO +·OH+H+
2
C.SO ·和·OH具有强氧化性,可将废水中的As(V)氧化去除
D.若56gFe参加反应,则有1molS O 被还原
2
34.(2021·河北高三模拟)“速力菲”是市场上一种常见的补铁药物,该药物的主要成分是琥珀酸亚铁,
不溶于水,但能溶于人体的胃酸中。某化学兴趣小组用“速力菲”样品进行了如下实验,根据实验流程及
现象,下列说法正确的是
A.在步骤③⑤的反应中,Cl 和I 均是氧化剂
2 2
B.从实验过程可推知,氧化性:Fe3+﹥I;还原性:Fe2+﹥Mn2+
2
C.步骤②反应中生成1mol气体,消耗2molHCl
D.①④发生的是非氧化还原反应