文档内容
专题 05 元素及其化合物的性质与应用
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.(2024·山西吕梁高三联考)下列说法正确的是( )
A.Cl 和Br 分别与Fe2+反应得到Cl-和 Br-
2 2
B.加热NaI与浓HPO 混合物可制备HI,说明HPO 比HI酸性强
3 4 3 4
C.1mol SO 与1mol NO 分别通入1L水中可产生相同浓度的HSO 和HNO
3 2 2 4 3
D.浓HNO 和稀HNO 与Cu反应的还原产物分别为NO 和NO,故稀HNO 氧化性更强
3 3 2 3
2.对下列事实的解释正确的是( )
A.氯气可以使湿润的有色布条褪色,是因为氯气具有漂白性
B.医疗上可用硫酸钡作x射线透视肠胃的内服药,是因为硫酸钡不溶于酸
C.向50mL18mol·L-1 的HSO 溶液中加入足量的铜片加热充分反应后,被还原的HSO 的物质的量等
2 4 2 4
于0.45mol
D.常温下,浓HSO 可以用铝制容器贮存,说明铝与浓HSO 不反应
2 4 2 4
3.(2024·天津高三期中)类比推理是化学中常用的思维方法。下列推理正确的是( )
A.Na与O 在加热条件下反应生成NaO,故可推测Li与O 在加热条件下反应生成LiO
2 2 2 2 2 2
B.BaSO 可用作医疗X射线检查的内服药剂,俗称“钡餐”,故可推测BaCO 也用作“钡餐”
4 3
C.工业上采用电解熔融NaCl的方法冶炼金属钠,故工业上也可用电解熔融AlCl 的方法冶炼金属铝
3
D.SO 与HO反应生成HSO ,故可推测SSO 与NaO 反应生成NaSO
2 2 2 4 2 2 2 2 4
4.(2024·浙江高三选考模拟)下列关于元素及其化合物的性质说法正确的是( )
A.工业上利用水和NO 反应制备硝酸
2
B.工业上用焦炭和金刚砂反应制备粗硅
C.用铁与浓硫酸常温下反应制备SO
2
D.La-Ni储氢合金在加热条件下可与氢气反应生成稳定的金属氢化物
5.根据下列各反应现象所归纳的元素性质不正确的是( )
A.将一小块钠投入到盛有硫酸铜溶液的烧杯中,发现没有紫红色的铜析出。不能说明钠的金属性比铜
弱
B.用湿润的淀粉碘化钾试纸放置在有氯气产生的导管上端,发现试纸变蓝。说明氯元素的非金属性比
碘元素强
C.把HS气体和Cl 在集气瓶中混合,一段时间后发现瓶壁有淡黄色固体析出。说明Cl的非金属性比
2 2
S强
D.将0.1 mol Na、Mg、Al分别与足量稀盐酸反应,除共同产生H 外,还分别生成了NaCl、MgCl 、
2 2
AlCl ,金属失去的电子数分别为0.1 mol、0.2 mol、0.3 mol。说明这三种金属的活泼性为:Al>Mg>
3
Na6.在火星上工作的美国“勇气号”、“机遇号”探测车的一个重要任务就是收集有关 Fe O 及硫酸盐
2 3
的信息,以证明火星上存在或曾经存在过水。以下叙述正确的是( )
A.铝热剂就是单指Fe O 粉和铝粉的混合物
2 3
B.检验从火星上带回来的红色物质是否是Fe O 的操作步骤为:样品→粉碎→加水溶解→过滤→向滤
2 3
液中滴加KSCN溶液
C.还原a mol Fe O 所需H、Al、CO的物质的量之比为3∶2∶3
2 3 2
D.明矾属于硫酸盐,含结晶水,是混合物
7.(2024·湖北荆州·高三荆州中学校考阶段练习)已知水合肼(N H•H O)具有较强还原性,通常可被氧
2 4 2
化为N。现用如图流程可制得较纯的单质Pt,下列有关说法不正确的是( )
2
A.王水是由浓盐酸与浓硝酸组成,与粗Pt反应时浓硝酸表现出强氧化性
B.已知H[PtCl ]是配合物,则中心原子是Pt,配位数为6
2 6
C.脱硝除去残余的HNO 和氮氧化物,主要目的是防止其污染环境
3
D.由PtO 制得1mol纯Pt,理论上至少需要1molN H•H O作还原剂
2 2 4 2
8.在一定温度和催化剂作用下,NO跟NH 可以发生反应生成N 和HO。现有NO和NH 的混合物
3 2 2 3
1mol,充分反应后所得产物中,经还原得到的N 比经氧化得到的N 多1.4g。已知反应的化学方程式:
2 2
4NH +6NO 5N+6H O,则下列说法正确的是( )
3 2 2
A.当转移的电子数约为3.612×1023时,则标况下有4.48L氨气被还原
B.氧化产物和还原产物的物质的量比为3:2
C.若以上反应进行完全,原混合物中NO与NH 的物质的量之比为可能为3:7
3
D.若有混合物中有0.2molNH ,则参与反应的NO为0.8mol
3
9.已知甲、乙、丙三种物质均含有同种元素X,其转化关系如下:
的
下列说法错误 是( )
A.若A为NaOH溶液,乙为白色沉淀,则X可能为短周期金属元素
B.若A为硝酸,X为金属元素,则甲与乙反应可生成丙
C.若A为氧气,丙在通常状况下为红棕色气体,则甲可能为非金属单质
D.若乙为NaHCO ,则甲或丙可能是CO
3 2
10.下列关于置换反应A+X→B+Y(其中A、B为单质,X和Y为化合物,反应条件已略去)的描述
中,正确的是( )
A.若X是氧化物,则Y也一定是氧化物
B.若X为不含有金属元素的化合物,则B一定是一种非金属单质C.若A为金属单质,则B一定为一种非金属单质
D.若X为含有金属元素的化合物,则Y一定是一种含有金属元素的化合物
11.(2024·江西赣州高三联考)铜元素的价类二维图如图,下列有关说法正确的是( )
A.a可直接转化为e
B.b转化为c一定需要另加还原剂
C.新制的e可用于检验葡萄糖中的醛基
D.直接加热f溶液一定可得到f固体
12.(2023·河南省安阳市三模)某化学实验小组设计如下实验探究Zn与溶液中Fe3+发生反应的原理。
实验 试剂 现象
2 mL0.1 mol· L-1FeCl 溶 黄色溶液很快变浅,接着有无色气泡产生,固体中
I 3
液、过量锌粉 未检出铁单质
很快有大量气体产生,出现红褐色浑浊,30 min左
2 mL1 mol· L-1FeCl 溶
Ⅱ 3 右产生红褐色沉淀,溶液颜色变浅,产生少量铁单
液(pH≈0.70)、过量锌粉
质
下列说法错误的是( )
A.实验I说明Fe3+被还原为Fe2+
B.可用酸性高锰酸钾溶液检验实验I得到的溶液中含有Fe2+
C.实验Ⅱ发生了置换反应和复分解反应
D.实验说明Fe3+、H+与Zn的反应与离子浓度有关
13.NaFeO 是一种高效的水处理剂,下列用于解释事实的离子方程式中不正确的是( )
2 4
A.NaFeO 在酸性溶液中不稳定,与水反应生成 Fe3+和O ,离子方程式为:4FeO2-+10HO+4Fe3+
2 4 2 4 2
===20OH-+3O↑
2
B.工业上可用FeCl 、NaOH、NaClO三种物质反应制得NaFeO 离子方程式为:2Fe3++10OH-+
3 2 4
3ClO-===2FeO2-+3Cl-+5HO
4 2
C.NaFeO 消毒杀菌时得到的 Fe3+可以净水,Fe3+能产生净水物质的原因是:Fe3++
2 4
3HO===Fe(OH) (胶体)+3H+
2 3
D.工业上可用铁做阳极,电解浓NaOH溶液的方法制NaFeO,阳极的电极反应为:Fe-6e-+8OH-
2 4
===FeO2-+4HO
4 2
14.现有一NaSO 、NaSO 混合物样品ag,为了测定其中NaSO 的质量分数,设计了如下方案,其
2 3 2 4 2 3中明显不合理的是( )
A. 将样品配制成溶液VL,取其中25.00mL用标准KMnO 溶液滴定,消耗标准KMnO 溶液VmL
1 4 4 2
B. 向样品中加足量HO,再加足量BaCl 溶液,过滤,将沉淀洗涤、干燥,称量其质量为bg
2 2 2
C. 将样品与足量稀盐酸充分反应后,再加入足量BaCl 溶液,过滤,将沉淀洗涤、干燥,称量其质量
2
为cg
D. 将样品与足量稀盐酸充分反应,生成的气体依次通过盛有饱和 NaHSO 的洗气瓶、盛有浓HSO 的
3 2 4
洗气瓶、盛有碱石灰的干燥管Ⅰ、盛有碱石灰的干燥管Ⅱ,测定干燥管Ⅰ增重dg
15.下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
选项 陈述Ⅰ 陈述Ⅱ 判断
向浓盐酸中加入浓硫酸 浓盐酸易挥发,浓硫酸与水作用放出大
A Ⅰ对,Ⅱ对;有
可制备氯化氢气体 量的热
由于Cu具有还原性,浓HNO 具有氧
3
B Cu能与浓HNO 反应 化性,在任何条件下生成的气体一定是 Ⅰ对,Ⅱ错;无
3
NO
2
硫单质在纯氧中燃烧有
C 部分二氧化硫被氧化为SO Ⅰ对,Ⅱ对;无
少量SO 生成 3
3
硝酸铵和碱石灰共热用
D 铵盐与碱能发生复分解反应 Ⅰ对,Ⅱ对;有
于实验室制备NH
3
二、非选择题(本题包括4小题,共55分)
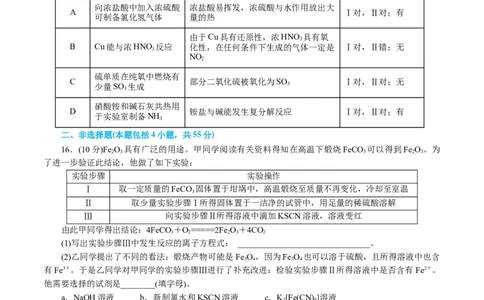
16.(10分)Fe O 具有广泛的用途。甲同学阅读有关资料得知在高温下煅烧FeCO 可以得到Fe O 。为
2 3 3 2 3
了进一步验证此结论,他做了如下实验:
实验步骤 实验操作
Ⅰ 取一定质量的FeCO 固体置于坩埚中,高温煅烧至质量不再变化,冷却至室温
3
Ⅱ 取少量实验步骤Ⅰ所得固体置于一洁净的试管中,用足量的稀硫酸溶解
Ⅲ 向实验步骤Ⅱ所得溶液中滴加KSCN溶液,溶液变红
由此甲同学得出结论:4FeCO+O=====2Fe O+4CO
3 2 2 3 2
(1)写出实验步骤Ⅲ中发生反应的离子方程式: _______________________________。
(2)乙同学提出了不同的看法:煅烧产物可能是Fe O,因为Fe O 也可以溶于硫酸,且所得溶液中也含
3 4 3 4
有Fe3+。于是乙同学对甲同学的实验步骤Ⅲ进行了补充改进:检验实验步骤Ⅱ所得溶液中是否含有 Fe2+。
他需要选择的试剂是________(填字母)。
a.NaOH溶液 b.新制氯水和KSCN溶液 c.K[Fe(CN) ]溶液
3 6
(3)丙同学认为即使得到了乙同学预期的实验现象,也不能确定煅烧产物的成分,你认为丙同学持此看
法的理由是______________________。
(4)丙同学进一步查阅资料得知煅烧FeCO 的产物中的确含有+2价铁元素。于是他设计了另一种由
3
FeCO 制取 Fe O 的方法:先向 FeCO 中依次加入试剂稀硫酸、________(填试剂名称)和氨水;再
3 2 3 3
________(填操作名称)、洗涤、灼烧,即可得到Fe O。
2 3
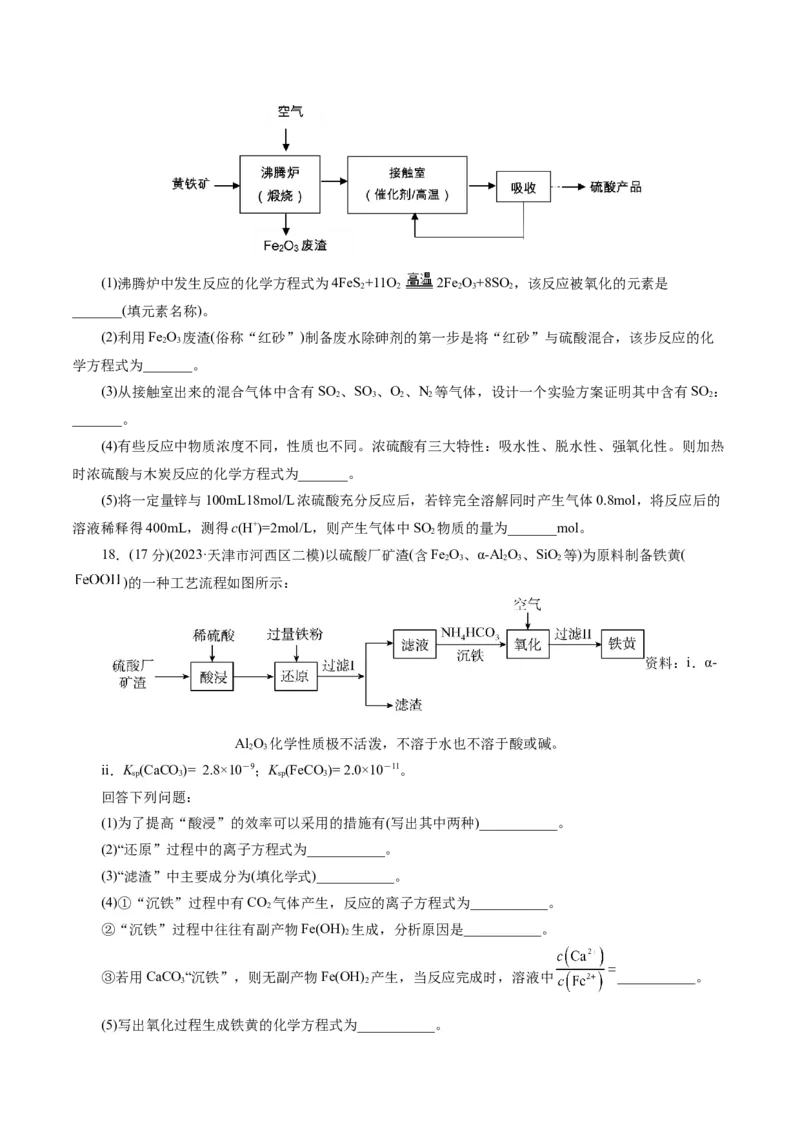
17.(13分)工业上用黄铁矿(FeS )为原料制备硫酸的流程如下:
2(1)沸腾炉中发生反应的化学方程式为4FeS+11O 2Fe O+8SO,该反应被氧化的元素是
2 2 2 3 2
_______(填元素名称)。
(2)利用Fe O 废渣(俗称“红砂”)制备废水除砷剂的第一步是将“红砂”与硫酸混合,该步反应的化
2 3
学方程式为_______。
(3)从接触室出来的混合气体中含有SO 、SO 、O、N 等气体,设计一个实验方案证明其中含有SO :
2 3 2 2 2
_______。
(4)有些反应中物质浓度不同,性质也不同。浓硫酸有三大特性:吸水性、脱水性、强氧化性。则加热
时浓硫酸与木炭反应的化学方程式为_______。
(5)将一定量锌与100mL18mol/L浓硫酸充分反应后,若锌完全溶解同时产生气体0.8mol,将反应后的
溶液稀释得400mL,测得c(H+)=2mol/L,则产生气体中SO 物质的量为_______mol。
2
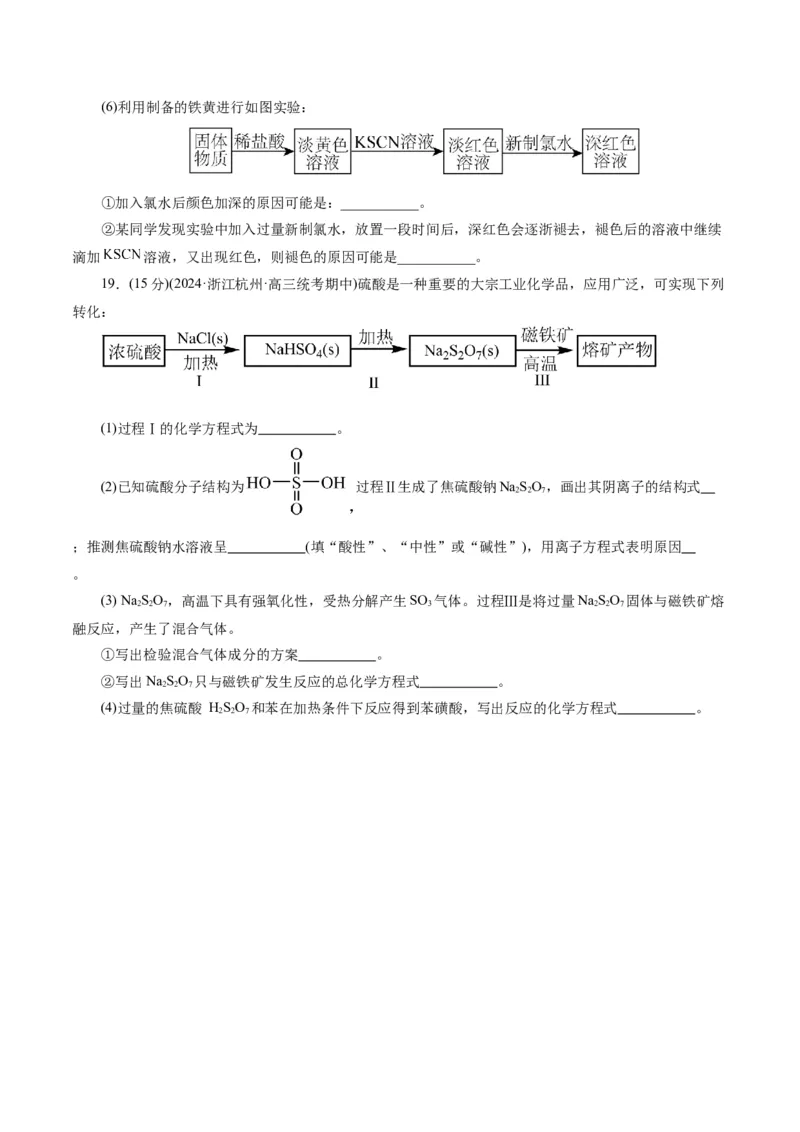
18.(17分)(2023·天津市河西区二模)以硫酸厂矿渣(含Fe O、α-Al O、SiO 等)为原料制备铁黄(
2 3 2 3 2
)的一种工艺流程如图所示:
资料:i.α-
Al O 化学性质极不活泼,不溶于水也不溶于酸或碱。
2 3
ii.K (CaCO)= 2.8×10-9;K (FeCO)= 2.0×10-11。
sp 3 sp 3
回答下列问题:
(1)为了提高“酸浸”的效率可以采用的措施有(写出其中两种)___________。
(2)“还原”过程中的离子方程式为___________。
(3)“滤渣”中主要成分为(填化学式)___________。
(4)①“沉铁”过程中有CO 气体产生,反应的离子方程式为___________。
2
②“沉铁”过程中往往有副产物Fe(OH) 生成,分析原因是___________。
2
③若用CaCO“沉铁”,则无副产物Fe(OH) 产生,当反应完成时,溶液中 ___________。
3 2
(5)写出氧化过程生成铁黄的化学方程式为___________。(6)利用制备的铁黄进行如图实验:
①加入氯水后颜色加深的原因可能是:___________。
②某同学发现实验中加入过量新制氯水,放置一段时间后,深红色会逐浙褪去,褪色后的溶液中继续
滴加 溶液,又出现红色,则褪色的原因可能是___________。
19.(15分)(2024·浙江杭州·高三统考期中)硫酸是一种重要的大宗工业化学品,应用广泛,可实现下列
转化:
(1)过程Ⅰ的化学方程式为 。
(2)已知硫酸分子结构为 过程Ⅱ生成了焦硫酸钠NaSO,画出其阴离子的结构式
2 2 7
;推测焦硫酸钠水溶液呈 (填“酸性”、“中性”或“碱性”),用离子方程式表明原因
。
(3) Na SO,高温下具有强氧化性,受热分解产生SO 气体。过程Ⅲ是将过量NaSO 固体与磁铁矿熔
2 2 7 3 2 2 7
融反应,产生了混合气体。
①写出检验混合气体成分的方案 。
②写出NaSO 只与磁铁矿发生反应的总化学方程式 。
2 2 7
(4)过量的焦硫酸 HSO 和苯在加热条件下反应得到苯磺酸,写出反应的化学方程式 。
2 2 7