文档内容
专题 05 化工生产中的重要非金属元素
1.二氧化硫能使溴水褪色,说明二氧化硫具有( )
A.还原性 B.氧化性 C.漂白性 D.酸性
2.下列物品或设备主要成分中含有单质硅的是( )
A.光导纤维 B.水晶项链 C.门窗玻璃 D.太阳能电池
3.下列物质可以用铝制容器存放的是( )
A.浓硝酸 B.稀硫酸 C.浓盐酸 D.浓氢氧化钠溶液
4.下列反应中,SO 表现氧化性的是( )
2
A.2SO +O 2SO
2 2 3
B.SO +HO HSO
2 2 2 3
C.2HS+SO ===3S↓+2HO
2 2 2
D.SO +2HO+Cl===H SO +2HCl
2 2 2 2 4
5.有关二氧化硫的说法错误的是( )
A.SO 通入NaSO 或NaHCO 溶液均能发生反应
2 2 3 3
B.SO 能使品红溶液褪色是因为它的氧化性
2
C.用酒精灯加热已被SO 褪色的品红溶液,可恢复原来的红色
2
D.SO 和O 混合后在催化剂存在的条件下加热,可生成三氧化硫
2 2
6.下列关于浓硫酸特性的叙述不正确的是( )
A.浓硫酸具有吸水性、脱水性和强氧化性等特性
B.浓硫酸能吸收气体中的水蒸气,常作氨气、二氧化硫等气体的干燥剂
C.浓硫酸可以吸收固体中的湿存水、结晶水合物中的结晶水
D.在反应C H O 浓硫酸12C+11HO,浓硫酸作脱水剂
12 22 11 2
→
7.下列关于氮及其化合物说法,不正确的是( )
A.氮气性质稳定,可用于工业制镁的冷却剂
B.NH 和NO 可用作航天飞机的燃料
2 4 2 4
C.碳酸氢铵常用作氮肥,不可与碱性肥料混用
D.硝酸可用于制造染料、塑料、炸药和硝酸盐
8.化学与生活、生产、科技密切相关。下列说法错误的有( )
A.工业生产玻璃、水泥、漂白粉,均需要用石灰石为原料
B.光导纤维的主要材料是SiO
2C.单质硅可用于制取通信芯片
D.“ ”飞机身使用的复合材料之一碳纤维,属于新型无机非金属材料
9.用来鉴别浓硫酸和稀硫酸的操作不正确的是( )
A.分别取10 mL溶液,质量大的是浓硫酸,质量小的是稀硫酸
B.观察液体流动性,流动性好的是稀硫酸,油状黏稠的是浓硫酸
C.把CuSO ·5H O晶体投入溶液中,逐渐变为白色粉末的是浓硫酸,晶体溶解的是稀硫酸
4 2
D.将铝片分别投入溶液,快速放出气体的是浓硫酸,放出气体慢的是稀硫酸
10.空气质量报告主要包括“空气污染指数”、“首要污染物”、“空气质量级别”、“空气质量状
况”等。下图为一报告截图,下列叙述错误的是( )
A.该市当天空气首要污染物是PM2.5 B.该市当天空气质量等级属于重度污染
C. 均可导致酸雨 D.污染物NO 可能主要来源于机动车尾气
2
11.下列说法正确的是( )
A.硫粉在过量的纯氧中燃烧可以生成SO
3
B.可以用澄清石灰水鉴别SO 和CO
2 2
C.SO 能使酸性KMnO 水溶液褪色,是因为SO 有漂白性
2 4 2
D.SO 通入到紫色石蕊试液中,溶液只变红不褪色
2
12.下列关于氮及其化合物的说法正确的是( )
A.N 分子的结构稳定,因而氮气不能支持任何物质的燃烧
2
B.液氨汽化时要吸收大量热,因而液氨可用作制冷剂
C.NO可用向上排空气法或排水法收集
D.浓硝酸保存在棕色瓶内是因为硝酸易挥发
13.下列说法不正确的是( )
A.在稀硫酸中加入铜粉,铜粉不溶解,再加入Cu(NO ) 固体,铜粉仍不溶解
3 2
B.某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性
C.铜与浓硝酸反应的离子方程式为Cu+4H++2NO===Cu2++2NO ↑+2HO
2 2
D.HNO→NO→NO ,以上各步变化均能通过一步实验完成
3 214.在探究SO 的性质实验中,下列根据实验现象得出的结论不正确的是( )
2
A.向SO 水溶液中滴加Ba(NO ) 溶液,产生的白色沉淀是BaSO
2 3 2 3
B.向溴水中通入SO ,溶液褪色,说明+4价硫具有还原性
2
C.将过量的SO 通入石蕊溶液中,溶液由紫色变为红色,说明SO 的水溶液显酸性
2 2
D.向SO 水溶液中加入NaHCO 粉末,有气泡产生,说明HSO 酸性强于HCO
2 3 2 3 2 3
15.《天工开物》记载:“凡埏泥造瓦,掘地二尺余,择取无砂粘土而为之”,“凡坯既成,干燥之
后,则堆积窖中燃薪举火”,“浇水转釉(主要为青色),与造砖同法”。下列说法错误的是( )
A.粘土是制作砖瓦和陶瓷的主要原料
B.“燃薪举火”使粘土发生复杂的物理化学变化
C.沙子和粘土的主要成分均为硅酸盐
D.烧制后自然冷却成红瓦,浇水冷却成青瓦
16.关于氮的变化关系图如图:
则下列说法不正确的是( )
A.路线①②③是工业生产硝酸的主要途径
B.路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径
C.上述所有反应都是氧化还原反应
D.上述反应中只有③属于氮的固定
17.实验小组同学探究FeSO 分解反应并检验反应产物(加热及加持装置略)。下列有关FeSO 分解的说
4 4
法不正确的是( )
A.Ⅰ中固体变为红棕色,说明反应生成了Fe O
2 3
B.Ⅰ中反应需持续加热,说明FeSO 分解是吸热反应
4
C.Ⅱ中品红溶液颜色褪去,说明反应生成了SO
2
D.Ⅲ中未产生白色沉淀,说明反应未生成SO
3
18.(2021•河北选择性考试)硫和氮及其化合物对人类生存和社会发展意义重大,但硫氧化物和氮氧化
物造成的环境问题也日益受到关注,下列说法正确的是( )
A.NO 和SO 均为红棕色且有刺激性气味的气体,是酸雨的主要成因
2 2B.汽车尾气中的主要大气污染物为NO、SO 和PM2.5
2
C.植物直接吸收利用空气中的NO和NO 作为肥料,实现氮的固定
2
D.工业废气中的SO 可采用石灰法进行脱除
2
19.(2021•河北选择性考试)关于非金属含氧酸及其盐的性质,下列说法正确的是( )
A.浓HSO 具有强吸水性,能吸收糖类化合物中的水分并使其炭化
2 4
B.NaClO、KClO 等氯的含氧酸盐的氧化性会随溶液的pH减小而增强
3
C.加热NaI与浓HPO 混合物可制备HI,说明HPO 比HI酸性强
3 4 3 4
D.浓HNO 和稀HNO 与Cu反应的还原产物分别为NO 和NO,故稀HNO 氧化性更强
3 3 2 3
20.二氧化硅(SiO)又称硅石,是制备硅及其化合物的重要原料。下列说法正确的是( )
2
A.SiO 既能与HF反应, 又能与NaOH反应,属于两性氧化物
2
B.SiO 和Si都是光导纤维材料
2
C.利用SiO 与NaOH溶液反应可制取“水玻璃”
2
D.图中所示转化反应都是非氧化还原反应
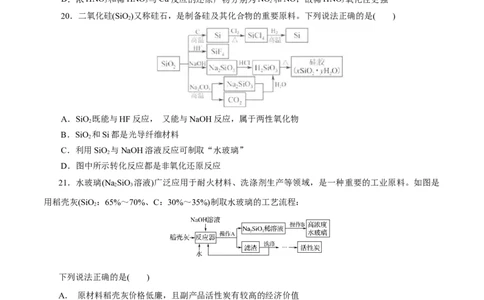
21.水玻璃(Na SiO 溶液)广泛应用于耐火材料、洗涤剂生产等领域,是一种重要的工业原料。如图是
2 3
用稻壳灰(SiO:65%~70%、C:30%~35%)制取水玻璃的工艺流程:
2
下列说法正确的是( )
A. 原材料稻壳灰价格低廉,且副产品活性炭有较高的经济价值
B. 操作A与操作B完全相同
C. 该流程中硅元素的化合价发生改变
D. 反应器中发生的复分解反应为SiO+2NaOH===Na SiO+HO
2 2 3 2
22.绿水青山是习近平总书记构建美丽中国的伟大构想,某工厂拟综合处理含 NH +废水和工业废气
4
主要含N 、CO 、SO 、NO、CO,不考虑其他成分 ,设计了如图流程。已知:NO+NO +2OH-=2NO-
2 2 2 2 2+H O,下列说法正确的是
2
A.固体1中主要含有CaCO 、CaSO
3 3
B.X可以是空气,且需过量
C.处理含NH +废水时,发生的反应:NH ++5NO-+4H+==6NO↑+4H O
4 4 2 2
D.捕获剂所捕获的气体主要是CO
23.物质的类别和核心元素的化合价是研究物质化学性质的两个重要角度。硫元素的价类二维图如图
所示(其中h、g的阳离子均为 ),下列说法正确的是( )
A.b到d可直接转化
B.工业上,在常温下可以用铁罐储存f的浓溶液
C.c能将滴有酚酞的氢氧化钠稀溶液变为无色,表现其漂白性
D.将氯化钡溶液分别滴入h和g的稀溶液中,现象不同
24.工业上常采用生物硝化法将NH转化为NO来处理氨氮废水,工作流程如图,下列说法错误的是(
)
A.生物硝化法处理废水,会导致水体pH逐渐下降:NH+2O===NO+2H++HO
2 2
B.长期过量使用NH Cl等铵态化肥,易导致土壤酸化,水体富营养化
4
C.检验NH所需的试剂是浓NaOH溶液、湿润的蓝色石蕊试纸
D.微生物保持活性的pH范围为7~9,可以加入石灰石来调节水体的pH
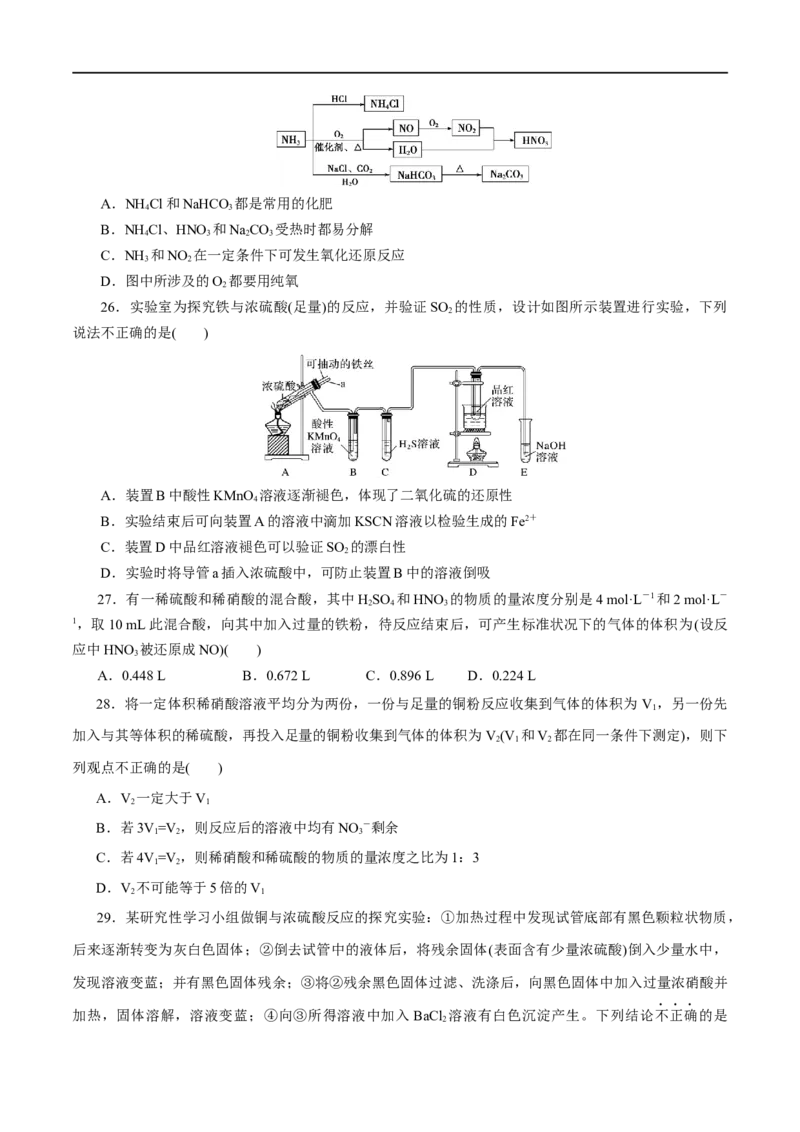
25.NH 是一种重要的化工原料,可以制备一系列物质(见下图),下列说法正确的是( )
3A.NH Cl和NaHCO 都是常用的化肥
4 3
B.NH Cl、HNO 和NaCO 受热时都易分解
4 3 2 3
C.NH 和NO 在一定条件下可发生氧化还原反应
3 2
D.图中所涉及的O 都要用纯氧
2
26.实验室为探究铁与浓硫酸(足量)的反应,并验证SO 的性质,设计如图所示装置进行实验,下列
2
说法不正确的是( )
A.装置B中酸性KMnO 溶液逐渐褪色,体现了二氧化硫的还原性
4
B.实验结束后可向装置A的溶液中滴加KSCN溶液以检验生成的Fe2+
C.装置D中品红溶液褪色可以验证SO 的漂白性
2
D.实验时将导管a插入浓硫酸中,可防止装置B中的溶液倒吸
27.有一稀硫酸和稀硝酸的混合酸,其中HSO 和HNO 的物质的量浓度分别是4 mol·L-1和2 mol·L-
2 4 3
1,取10 mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的气体的体积为(设反
应中HNO 被还原成NO)( )
3
A.0.448 L B.0.672 L C.0.896 L D.0.224 L
28.将一定体积稀硝酸溶液平均分为两份,一份与足量的铜粉反应收集到气体的体积为 V ,另一份先
1
加入与其等体积的稀硫酸,再投入足量的铜粉收集到气体的体积为V(V 和V 都在同一条件下测定),则下
2 1 2
列观点不正确的是( )
A.V 一定大于V
2 1
B.若3V=V ,则反应后的溶液中均有NO -剩余
1 2 3
C.若4V=V ,则稀硝酸和稀硫酸的物质的量浓度之比为1:3
1 2
D.V 不可能等于5倍的V
2 1
29.某研究性学习小组做铜与浓硫酸反应的探究实验:①加热过程中发现试管底部有黑色颗粒状物质,
后来逐渐转变为灰白色固体;②倒去试管中的液体后,将残余固体(表面含有少量浓硫酸)倒入少量水中,
发现溶液变蓝;并有黑色固体残余;③将②残余黑色固体过滤、洗涤后,向黑色固体中加入过量浓硝酸并
加热,固体溶解,溶液变蓝;④向③所得溶液中加入BaCl 溶液有白色沉淀产生。下列结论不正确的是
2( )
A.铜与浓硫酸反应生成的白色固体是CuSO B.①中灰白色固体不可能含有CuO
4
C.②中的黑色固体可能含有CuS或Cu S D.④中所得的白色沉淀是BaSO
2 3
30.某氮肥样品可能含有NH HCO 、NH Cl、NH NO 中的一种或几种。为探究其成分,称取该样品
4 3 4 4 3
0.500 0 g,溶解配成100 mL溶液,加过量浓NaOH溶液,加热,将产生的氨气通入60.00 mL 0.100 0 mol·L
-1的HSO 溶液中(设产生的NH 全部逸出),剩余的HSO 溶液能消耗20.00 mL 0.225 0 mol·L-1的NaOH
2 4 3 2 4
溶液。下列说法正确的是( )
A.吸收NH 消耗的HSO 为6.000×10-3 mol
3 2 4
B.上述过程共产生NH 268.8 mL(标准状况下)
3
C.该样品中NH的质量分数为43.2%
D.该氮肥样品必含NH Cl
4