文档内容
专题10 电化学
2021年化学高考题
一、单选题
1.(2021·山东高考真题)以KOH溶液为离子导体,分别组成CHOH—O、NH—O、
3 2 2 4 2
(CH)NNH—O 清洁燃料电池,下列说法正确的是
3 2 2 2
A.放电过程中,K+均向负极移动
B.放电过程中,KOH物质的量均减小
C.消耗等质量燃料,(CH)NNH—O 燃料电池的理论放电量最大
3 2 2 2
D.消耗1molO 时,理论上NH—O 燃料电池气体产物的体积在标准状况下为11.2L
2 2 4 2
【KS5U答案】C
【分析】
碱性环境下,甲醇燃料电池总反应为:2CHOH+3O+4KOH=2KCO+6HO;NH-O 清洁燃料电池总
3 2 2 3 2 2 4 2
反应为:NH+O=N+2HO;偏二甲肼[(CH)NNH]中C和N的化合价均为-2价,H元素化合价为
2 4 2 2 2 3 2 2
+1价,所以根据氧化还原反应原理可推知其燃料电池的总反应为:
(CH)NNH+4O+4KOH=2KCO+N+6HO,据此结合原电池的工作原理分析解答。
3 2 2 2 2 3 2 2
【KS5U解析】
A.放电过程为原电池工作原理,所以钾离子均向正极移动,A错误;
B.根据上述分析可知,NH-O 清洁燃料电池的产物为氮气和水,其总反应中未消耗KOH,所
2 4 2
以KOH的物质的量不变,其他两种燃料电池根据总反应可知,KOH的物质的量减小,B错误;
C.理论放电量与燃料的物质的量和转移电子数有关,设消耗燃料的质量均为mg,则甲醇、
mg mg
6 4
NH 和(CH)NNH 放电量(物质的量表达式)分别是:32g/mol 、32g/mol 、
2 4 3 2 2
mg
16
60g/mol ,通过比较可知(CH)NNH 理论放电量最大,C正确;
3 2 2
D.根据转移电子数守恒和总反应式可知,消耗1molO 生成的氮气的物质的量为1mol,在标
2
准状况下为22.4L,D错误;
故选C。
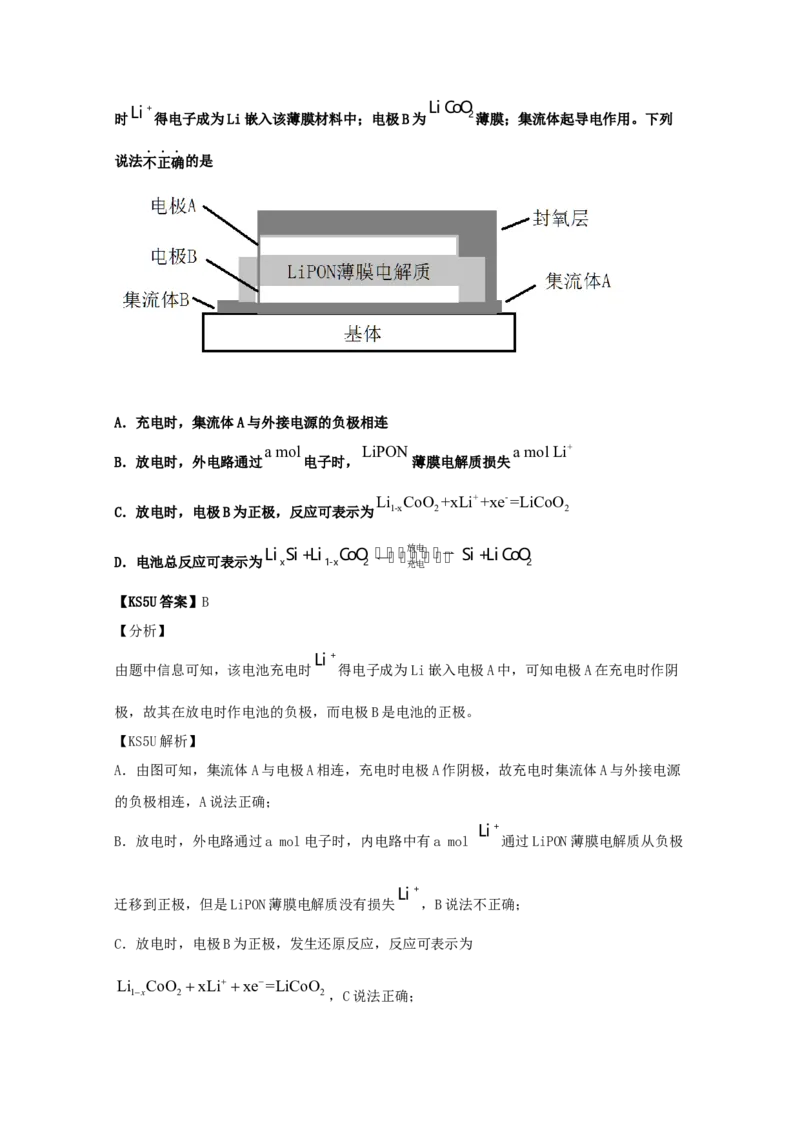
2.(2021·浙江)某全固态薄膜锂离子电池截面结构如图所示,电极A为非晶硅薄膜,充电时
Li+
得电子成为Li嵌入该薄膜材料中;电极B为
LiCoO
2薄膜;集流体起导电作用。下列
说法不正确的是
A.充电时,集流体A与外接电源的负极相连
a mol LiPON a mol Li+
B.放电时,外电路通过 电子时, 薄膜电解质损失
Li CoO +xLi++xe-=LiCoO
C.放电时,电极B为正极,反应可表示为 1-x 2 2
D.电池总反应可表示为 Li x Si+Li 1-x CoO 2 放 充 电 电 Si+LiCoO 2
【KS5U答案】B
【分析】
Li+
由题中信息可知,该电池充电时 得电子成为Li嵌入电极A中,可知电极A在充电时作阴
极,故其在放电时作电池的负极,而电极B是电池的正极。
【KS5U解析】
A.由图可知,集流体A与电极A相连,充电时电极A作阴极,故充电时集流体A与外接电源
的负极相连,A说法正确;
Li+
B.放电时,外电路通过a mol电子时,内电路中有a mol 通过LiPON薄膜电解质从负极
Li+
迁移到正极,但是LiPON薄膜电解质没有损失 ,B说法不正确;
C.放电时,电极B为正极,发生还原反应,反应可表示为
Li CoO xLi xe=LiCoO
1x 2 2,C说法正确;D.电池放电时,嵌入在非晶硅薄膜中的锂失去电子变成
Li+
,正极上
Li
1x
CoO
2得到电子和
充电
Li SiLi CoO SiLiCoO
Li+变为 LiCoO 2 ,故电池总反应可表示为 x 1x 2 放电 2,D说法正确。
综上所述,相关说法不正确的是B,本题选B。
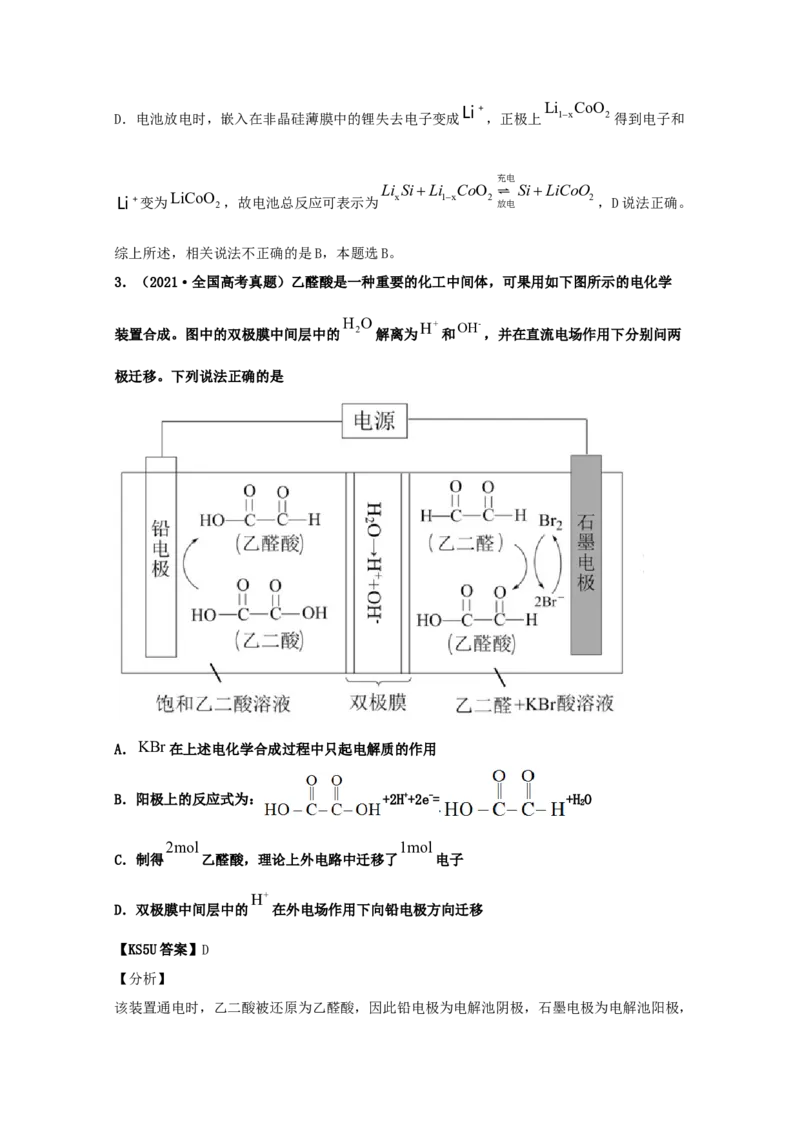
3.(2021·全国高考真题)乙醛酸是一种重要的化工中间体,可果用如下图所示的电化学
装置合成。图中的双极膜中间层中的
H
2
O
解离为
H+
和
OH-
,并在直流电场作用下分别问两
极迁移。下列说法正确的是
A.KBr在上述电化学合成过程中只起电解质的作用
B.阳极上的反应式为: +2H++2e-= +HO
2
2mol 1mol
C.制得 乙醛酸,理论上外电路中迁移了 电子
H+
D.双极膜中间层中的 在外电场作用下向铅电极方向迁移
【KS5U答案】D
【分析】
该装置通电时,乙二酸被还原为乙醛酸,因此铅电极为电解池阴极,石墨电极为电解池阳极,阳极上Br-被氧化为Br,Br 将乙二醛氧化为乙醛酸,双极膜中间层的H+在直流电场作用下移
2 2
向阴极,OH-移向阳极。
【KS5U解析】
A.KBr在上述电化学合成过程中除作电解质外,同时还是电解过程中阳极的反应物,生成的
Br 为乙二醛制备乙醛酸的中间产物,故A错误;
2
B.阳极上为Br-失去电子生成Br,Br 将乙二醛氧化为乙醛酸,故B错误;
2 2
C.电解过程中阴阳极均生成乙醛酸,1mol乙二酸生成1mol乙醛酸转移电子为2mol,1mol
乙二醛生成1mol乙醛酸转移电子为2mol,根据转移电子守恒可知每生成1mol乙醛酸转移电
子为1mol,因此制得2mol乙醛酸时,理论上外电路中迁移了2mol电子,故C错误;
D.由上述分析可知,双极膜中间层的H+在外电场作用下移向阴极,即H+移向铅电极,故D正
确;
综上所述,说法正确的是D项,故答案为D。
Co
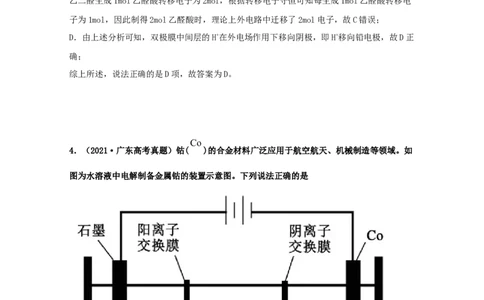
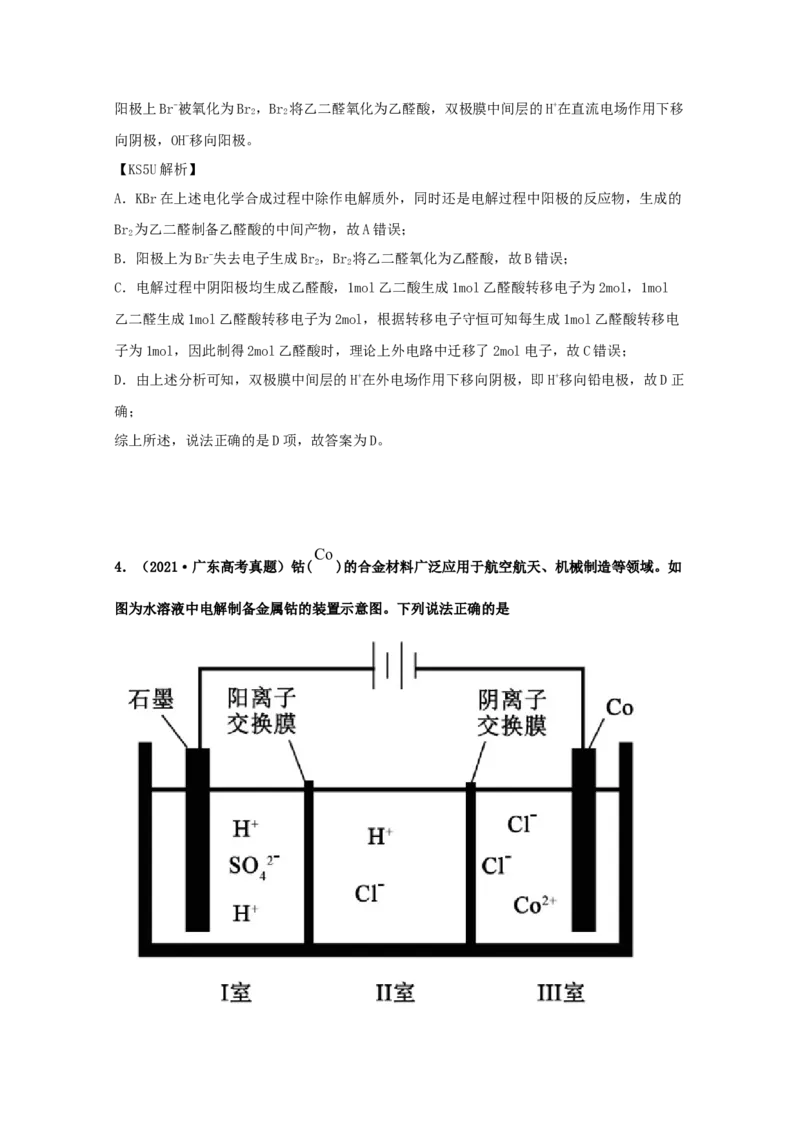
4.(2021·广东高考真题)钴( )的合金材料广泛应用于航空航天、机械制造等领域。如
图为水溶液中电解制备金属钴的装置示意图。下列说法正确的是pH
A.工作时,Ⅰ室和Ⅱ室溶液的 均增大
1molCo 16g
B.生成 ,Ⅰ室溶液质量理论上减少
C.移除两交换膜后,石墨电极上发生的反应不变
通电
D.电解总反应:2Co2 2H O 2CoO 4H
2 2
【KS5U答案】D
【分析】
由图可知,该装置为电解池,石墨电极为阳极,水在阳极失去电子发生氧化反应生成氧气和
氢离子,电极反应式为2HO-4e-=O↑+4H+,Ⅰ室中阳离子电荷数大于阴离子电荷数,放电生
2 2
成的氢离子通过阳离子交换膜由Ⅰ室向Ⅱ室移动,钴电极为阴极,钴离子在阴极得到电子发
生还原反应生成钴,电极反应式为Co2++2e-=Co,Ⅲ室中阴离子电荷数大于阳离子电荷数,氯
通电
离子过阴离子交换膜由Ⅲ室向Ⅱ室移动,电解的总反应的离子方程式为2Co2++2HO 2 Co
2
+O↑+4H+。
2
【KS5U解析】
A.由分析可知,放电生成的氢离子通过阳离子交换膜由Ⅰ室向Ⅱ室移动,使Ⅱ室中氢离子
浓度增大,溶液pH减小,故A错误;
B.由分析可知,阴极生成1mol钴,阳极有1mol水放电,则Ⅰ室溶液质量减少18g,故B错
误;
C.若移除离子交换膜,氯离子的放电能力强于水,氯离子会在阳极失去电子发生氧化反应
生成氯气,则移除离子交换膜,石墨电极的电极反应会发生变化,故C错误;
通电
D.由分析可知,电解的总反应的离子方程式为2Co2++2HO 2 Co +O↑+4H+,故D正确;
2 2
故选D。
CO CO
5.(2021·广东高考真题)火星大气中含有大量 2,一种有 2参加反应的新型全固态
电池有望为火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
CO
A.负极上发生还原反应 B. 2在正极上得电子
C.阳离子由正极移向负极 D.将电能转化为化学能【KS5U答案】B
【KS5U解析】
根据题干信息可知,放电时总反应为4Na+3CO=2NaCO+C。
2 2 3
A.放电时负极上Na发生氧化反应失去电子生成Na+,故A错误;
B.放电时正极为CO 得到电子生成C,故B正确;
2
C.放电时阳离子移向还原电极,即阳离子由负极移向正极,故C错误;
D.放电时装置为原电池,能量转化关系为化学能转化为电能和化学能等,故D错误;
综上所述,符合题意的为B项,故答案为B。
6.(2021·河北高考真题)K—O 电池结构如图,a和b为两个电极,其中之一为单质钾片。
2
关于该电池,下列说法错误的是
A.隔膜允许K+通过,不允许O 通过
2
B.放电时,电流由b电极沿导线流向a电极;充电时,b电极为阳极
C.产生1Ah电量时,生成KO 的质量与消耗O 的质量比值约为2.22
2 2
D.用此电池为铅酸蓄电池充电,消耗3.9g钾时,铅酸蓄电池消耗0.9g水
【KS5U答案】D
【分析】
由图可知,a电极为原电池的负极,单质钾片失去电子发生氧化反应生成钾离子,电极反应
式为K—e-=K+,b电极为正极,在钾离子作用下,氧气在正极得到电子发生还原反应生成超氧
化钾;据以上分析解答。
【KS5U解析】
K
A.金属性强的金属钾易与氧气反应,为防止钾与氧气反应,电池所选择隔膜应允许 通过,
O
不允许 2通过,故A正确;
B.由分析可知,放电时,a为负极,b为正极,电流由b电极沿导线流向a电极,充电时,b
电极应与直流电源的正极相连,做电解池的为阳极,故B正确;C.由分析可知,生成1mol超氧化钾时,消耗1mol氧气,两者的质量比值为1mol×71g/
mol:1mol×32g/mol≈2.22:1,故C正确;
D.铅酸蓄电池充电时的总反应方程式为2PbSO+2HO=PbO+Pb+2HSO,反应消耗2mol水,
4 2 2 2 4
3.9g
转移2mol电子,由得失电子数目守恒可知,耗 钾时,铅酸蓄电池消耗水的质量为
3.9g
39g/mol×18g/mol=1.8g,故D错误;
故选D。
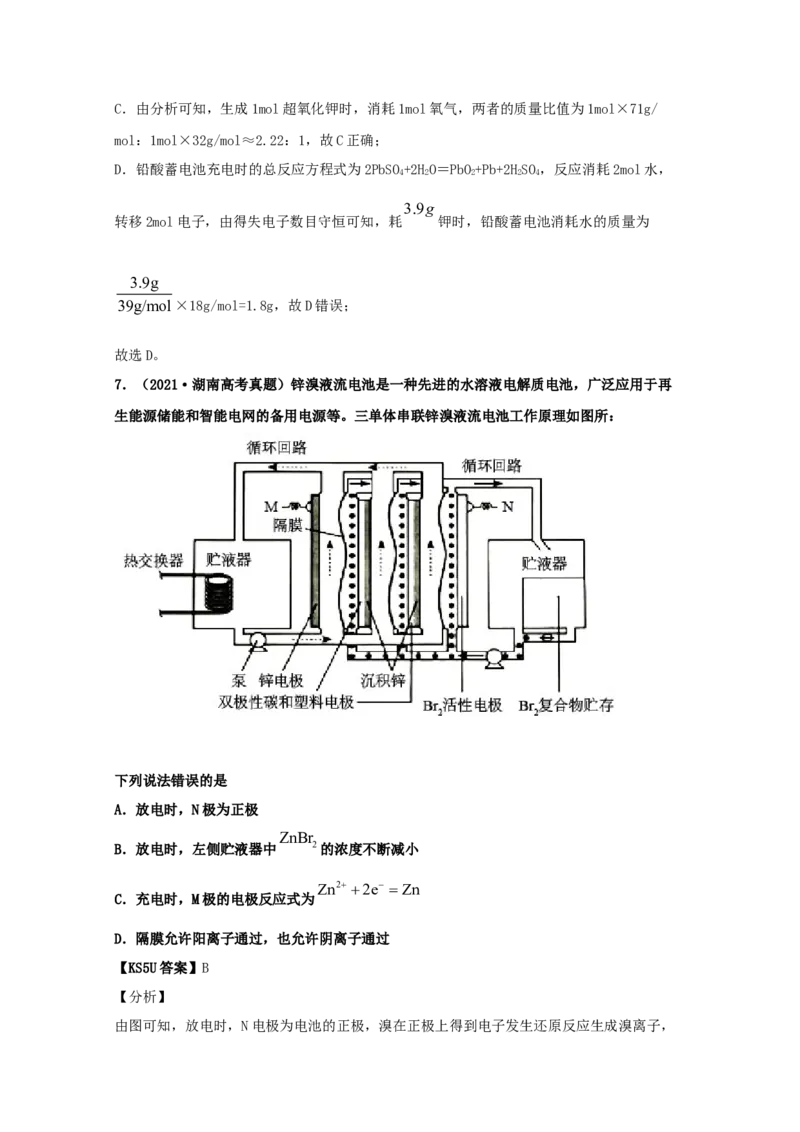
7.(2021·湖南高考真题)锌溴液流电池是一种先进的水溶液电解质电池,广泛应用于再
生能源储能和智能电网的备用电源等。三单体串联锌溴液流电池工作原理如图所:
下列说法错误的是
A.放电时,N极为正极
ZnBr
B.放电时,左侧贮液器中 2的浓度不断减小
Zn2 2e Zn
C.充电时,M极的电极反应式为
D.隔膜允许阳离子通过,也允许阴离子通过
【KS5U答案】B
【分析】
由图可知,放电时,N电极为电池的正极,溴在正极上得到电子发生还原反应生成溴离子,电极反应式为Br+2e—=2Br—,M电极为负极,锌失去电子发生氧化反应生成锌离子,电极反
2
应式为Zn—2e—=Zn2+,正极放电生成的溴离子通过离子交换膜进入左侧,同时锌离子通过交
换膜进入右侧,维持两侧溴化锌溶液的浓度保持不变;充电时,M电极与直流电源的负极相
连,做电解池的阴极,N电极与直流电源的正极相连,做阳极。
【KS5U解析】
A.由分析可知,放电时,N电极为电池的正极,故A正确;
B.由分析可知,放电或充电时,左侧储液器和右侧储液器中溴化锌的浓度维持不变,故B错
误;
C.由分析可知,充电时,M电极与直流电源的负极相连,做电解池的阴极,锌离子在阴极上
得到电子发生还原反应生成锌,电极反应式为Zn2++2e—=Zn,故C正确;
D.由分析可知,放电或充电时,交换膜允许锌离子和溴离子通过,维持两侧溴化锌溶液的
浓度保持不变,故D正确;
故选B。
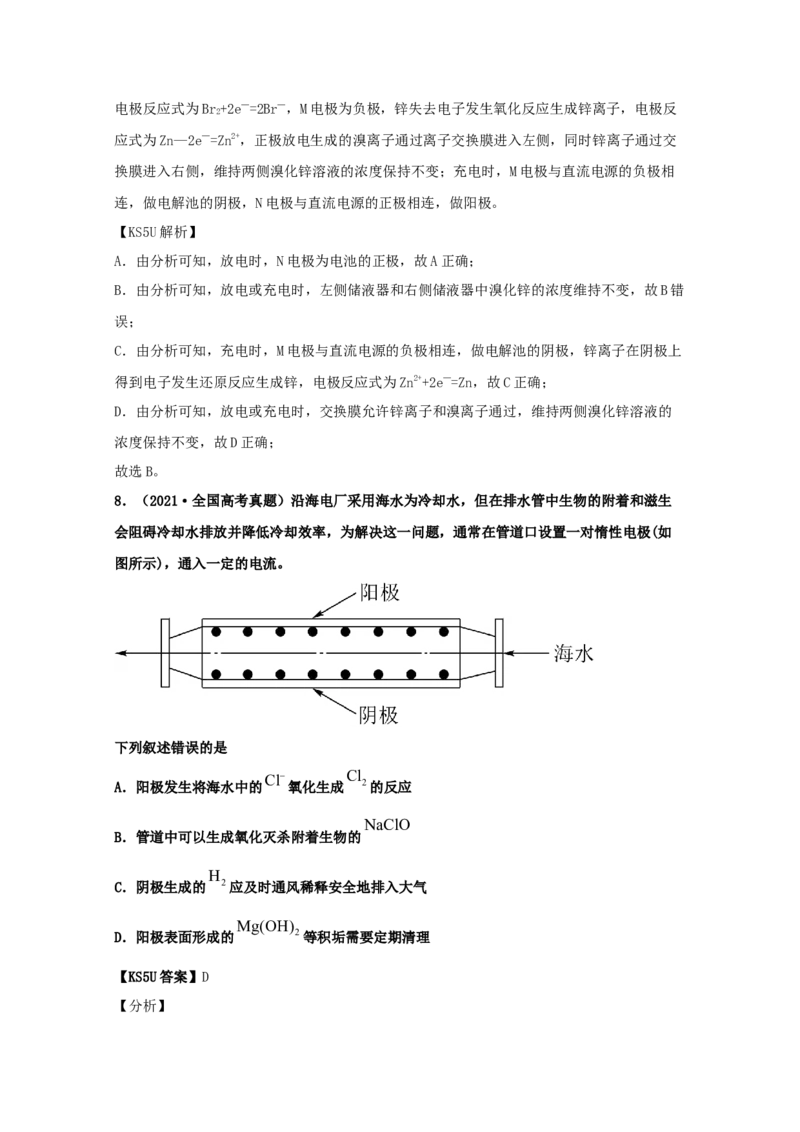
8.(2021·全国高考真题)沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生
会阻碍冷却水排放并降低冷却效率,为解决这一问题,通常在管道口设置一对惰性电极(如
图所示),通入一定的电流。
下列叙述错误的是
Cl Cl
A.阳极发生将海水中的 氧化生成 2的反应
NaClO
B.管道中可以生成氧化灭杀附着生物的
H
C.阴极生成的 2应及时通风稀释安全地排入大气
Mg(OH)
D.阳极表面形成的 2等积垢需要定期清理
【KS5U答案】D
【分析】海水中除了水,还含有大量的Na+、Cl-、Mg2+等,根据题干信息可知,装置的原理是利用惰性
电极电解海水,阳极区溶液中的Cl-会优先失电子生成Cl,阴极区HO优先得电子生成H 和
2 2 2
OH-,结合海水成分及电解产物分析解答。
【KS5U解析】
A.根据分析可知,阳极区海水中的Cl-会优先失去电子生成Cl,发生氧化反应,A正确;
2
B.设置的装置为电解池原理,根据分析知,阳极区生成的Cl 与阴极区生成的OH-在管道中
2
会发生反应生成NaCl、NaClO和HO,其中NaClO具有强氧化性,可氧化灭杀附着的生物,B
2
正确;
C.因为H 是易燃性气体,所以阳极区生成的H 需及时通风稀释,安全地排入大气,以排除
2 2
安全隐患,C正确;
D.阴极的电极反应式为:2HO+2e-=H↑+2OH-,会使海水中的Mg2+沉淀积垢,所以阴极表面会
2 2
形成Mg(OH) 等积垢需定期清理,D错误。
2
故选D。
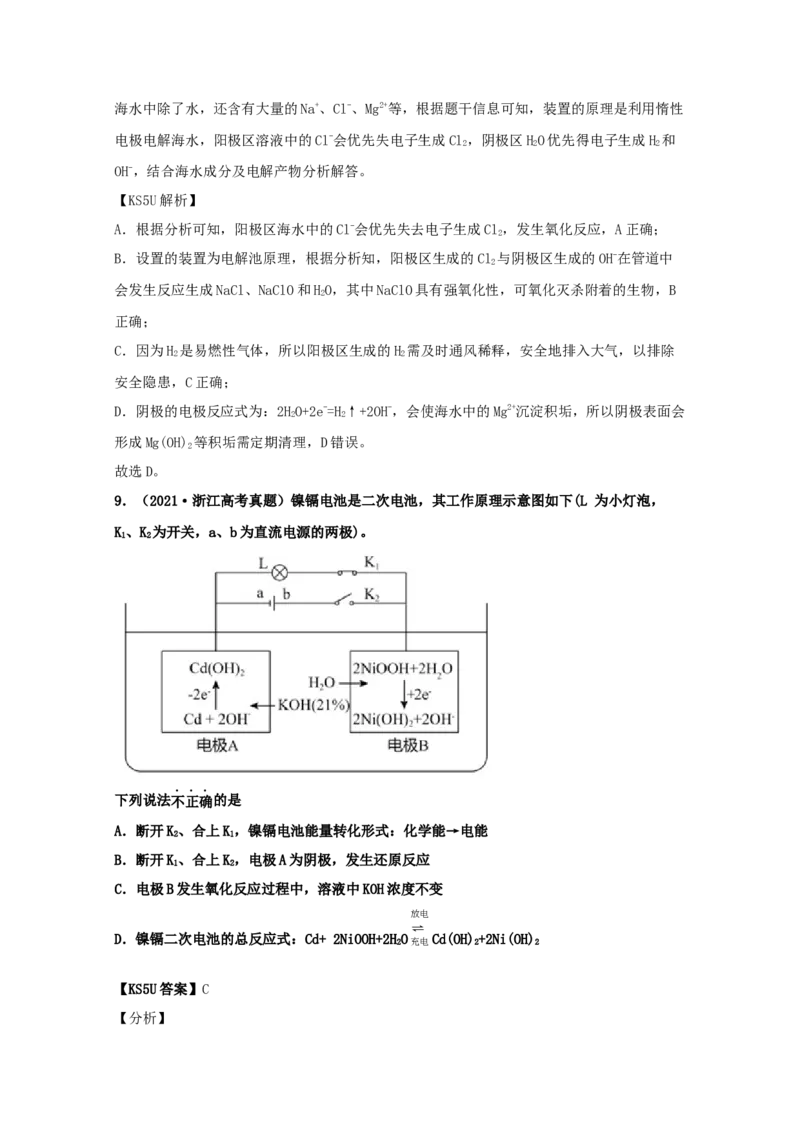
9.(2021·浙江高考真题)镍镉电池是二次电池,其工作原理示意图如下(L 为小灯泡,
K、K 为开关,a、b为直流电源的两极)。
1 2
下列说法不正确的是
A.断开K、合上K,镍镉电池能量转化形式:化学能→电能
2 1
B.断开K、合上K,电极A为阴极,发生还原反应
1 2
C.电极B发生氧化反应过程中,溶液中KOH浓度不变
放电
D.镍镉二次电池的总反应式:Cd+ 2NiOOH+2HO Cd(OH)+2Ni(OH)
2 充电 2 2
【KS5U答案】C
【分析】根据图示,电极A充电时为阴极,则放电时电极A为负极,负极上Cd失电子发生氧化反应生
成Cd(OH),负极反应式为Cd-2e-+2OH-=Cd(OH),电极B充电时为阳极,则放电时电极B为正
2 2
极,正极上NiOOH得电子发生还原反应生成Ni(OH),正极反应式为2NiOOH+2e-
2
+2HO=2Ni(OH)+2OH-,放电时总反应为Cd+2NiOOH+2HO=Cd(OH)+2Ni(OH),据此分析作答。
2 2 2 2 2
【KS5U解析】
A.断开K、合上K,为放电过程,镍镉电池能量转化形式:化学能→电能,A正确;
2 1
B.断开K、合上K,为充电过程,电极A与直流电源的负极相连,电极A为阴极,发生还原
1 2
反应,电极反应式为Cd(OH)+2e-=Cd+2OH-,B正确;
2
C.电极B发生氧化反应的电极反应式为2Ni(OH)-2e-+2OH-=2NiOOH+2HO,则电极A发生还原
2 2
反应的电极反应式为Cd(OH)+2e-=Cd+2OH-,此时为充电过程,总反应为Cd(OH)+2Ni(OH)
2 2 2
通电
Cd+2NiOOH+2HO,溶液中KOH浓度减小,C错误;
2
D.根据分析,放电时总反应为Cd+2NiOOH+2HO=Cd(OH)+2Ni(OH),则镍镉二次电池总反应
2 2 2
放电
式为Cd+2NiOOH+2HO Cd(OH)+2Ni(OH),D正确;
2 充电 2 2
答案选C。
二、工业流程题
10.(2021·山东高考真题)工业上以铬铁矿(FeCrO,含Al、Si氧化物等杂质)为主要原料
2 4
制备红矾钠(NaCrO•2HO)的工艺流程如图。回答下列问题:
2 2 7 2
(1)焙烧的目的是将FeCrO 转化为NaCrO 并将Al、Si氧化物转化为可溶性钠盐,焙烧时气
2 4 2 4
体与矿料逆流而行,目的是___。
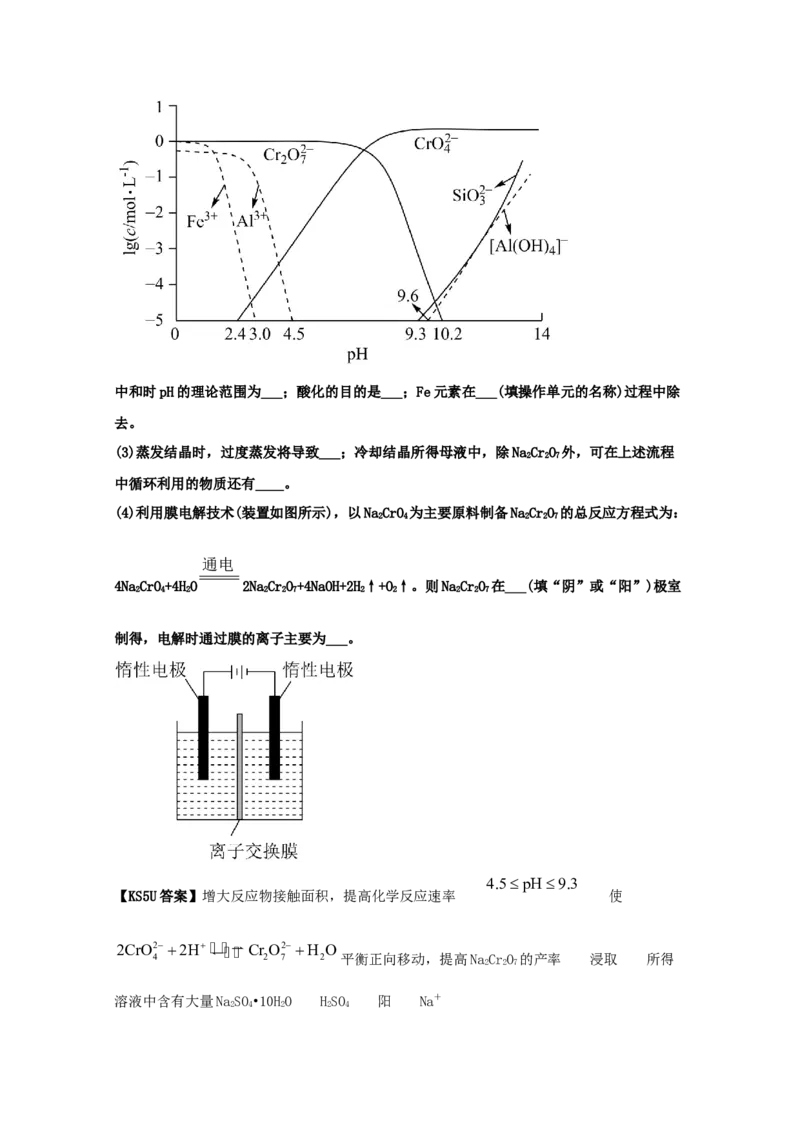
(2)矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图所示。当溶液中可溶组分浓
度c≤1.0×10-5mol•L-1时,可认为已除尽。中和时pH的理论范围为___;酸化的目的是___;Fe元素在___(填操作单元的名称)过程中除
去。
(3)蒸发结晶时,过度蒸发将导致___;冷却结晶所得母液中,除NaCrO 外,可在上述流程
2 2 7
中循环利用的物质还有____。
(4)利用膜电解技术(装置如图所示),以NaCrO 为主要原料制备NaCrO 的总反应方程式为:
2 4 2 2 7
通电
4NaCrO+4HO 2NaCrO+4NaOH+2H↑+O↑。则NaCrO 在___(填“阴”或“阳”)极室
2 4 2 2 2 7 2 2 2 2 7
制得,电解时通过膜的离子主要为___。
4.5pH9.3
【KS5U答案】增大反应物接触面积,提高化学反应速率 使
2CrO2
4
2H
Cr
2
O
7
2 H
2
O
平衡正向移动,提高NaCrO 的产率 浸取 所得
2 2 7
溶液中含有大量NaSO•10HO HSO 阳 Na+
2 4 2 2 4【分析】
以铬铁矿(FeCrO,含Al、Si氧化物等杂质)为主要原料制备红矾钠(NaCrO•2HO)过程中,
2 4 2 2 7 2
向铬铁矿中加入纯碱和O 进行焙烧,FeCrO 转化为NaCrO,Fe(II)被O 氧化成FeO,Al、
2 2 4 2 4 2 2 3
Si氧化物转化为NaAlO、NaSiO,加入水进行“浸取”,FeO 不溶于水,过滤后向溶液中加
2 2 3 2 3
AlO SiO2
入HSO 调节溶液pH使 2、 3 转化为沉淀过滤除去,再向滤液中加入HSO,将
2 4 2 4
NaCrO 转化为NaCrO,将溶液蒸发结晶将NaSO 除去,所得溶液冷却结晶得到NaCrO•2HO
2 4 2 2 7 2 4 2 2 7 2
晶体,母液中还含有大量HSO。据此解答。
2 4
【KS5U解析】
(1)焙烧时气体与矿料逆流而行,目的是利用热量使O 向上流动,增大固体与气体的接触面
2
积,提高化学反应速率,故答案为:增大反应物接触面积,提高化学反应速率。
AlO SiO2
(2)中和时调节溶液pH目的是将 2、 3 转化为沉淀过滤除去,由图可知,当溶液
SiO2
pH≥4.5时,Al3+除尽,当溶液pH>9.3时,HSiO 会再溶解生成 3 ,因此中和时pH的理
2 3
4.5pH9.3 Cr O2
论范围为 ;将Al元素和Si元素除去后,溶液中Cr元素主要以 2 7 和
CrO2 存在,溶液中存在平衡: 2CrO2 4 2H Cr 2 O 7 2 H 2 O ,降低溶液pH,平衡正
4
向移动,可提高NaCrO 的产率;由上述分析可知,Fe元素在“浸取”操作中除去,故答案
2 2 7
为: 4.5pH9.3 ;使 2CrO2 4 2H Cr 2 O 7 2 H 2 O 平衡正向移动,提高NaCrO 的
2 2 7
产率;浸取。
(3)蒸发结晶时,NaSO 主要以NaSO•10HO存在,NaSO•10HO的溶解度随温度升高先增大
2 4 2 4 2 2 4 2
后减小,若蒸发结晶时,过度蒸发将导致所得溶液中含有大量NaSO•10HO;由上述分析可
2 4 2
知,流程中循环利用的物质除NaCrO 外,还有HSO,故答案为:所得溶液中含有大量
2 2 7 2 4
NaSO•10HO;HSO。
2 4 2 2 4
通电
(4)由4NaCrO+4HO 2NaCrO+4NaOH+2H↑+O↑可知,电解过程中实质是电解水,
2 4 2 2 2 7 2 2
阳极上水失去电子生成H+和O,阴极上H+得到电子生成H,由
2 2
2CrO2 4 2H Cr 2 O 7 2 H 2 O Cr 2 O 7 22CrO2 4 2H Cr 2 O 7 2 H 2 O 可知, Cr 2 O 7 2 在氢离子浓度较大的电极室中制得,即
NaCrO 在阳极室产生;电解过程中,阴极产生氢氧根离子,氢氧化钠在阴极生成,所以为提
2 2 7
高制备NaCrO 的效率,Na+通过离子交换膜移向阴极,故答案为:阳;Na+。
2 2 7
三、原理综合题
11.(2021·湖南高考真题)氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易
储运,可通过下面两种方法由氨气得到氢气。
方法I:氨热分解法制氢气
相关化学键的键能数据
化学键 N N HH NH
键能E/
kJmol-1
946 436.0 390.8
NH N H
一定温度下,利用催化剂将 3分解为 2和 2。回答下列问题:
(1)反应
2NH
3
(g) N
2
(g)3H
2
(g)
ΔH= _______ kJmol1 ;
S 198.9Jmol1K1
(2)已知该反应的 ,在下列哪些温度下反应能自发进行?
_______(填标号)
A.25℃ B.125℃ C.225℃ D.325℃
0.1molNH
(3)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将 3通
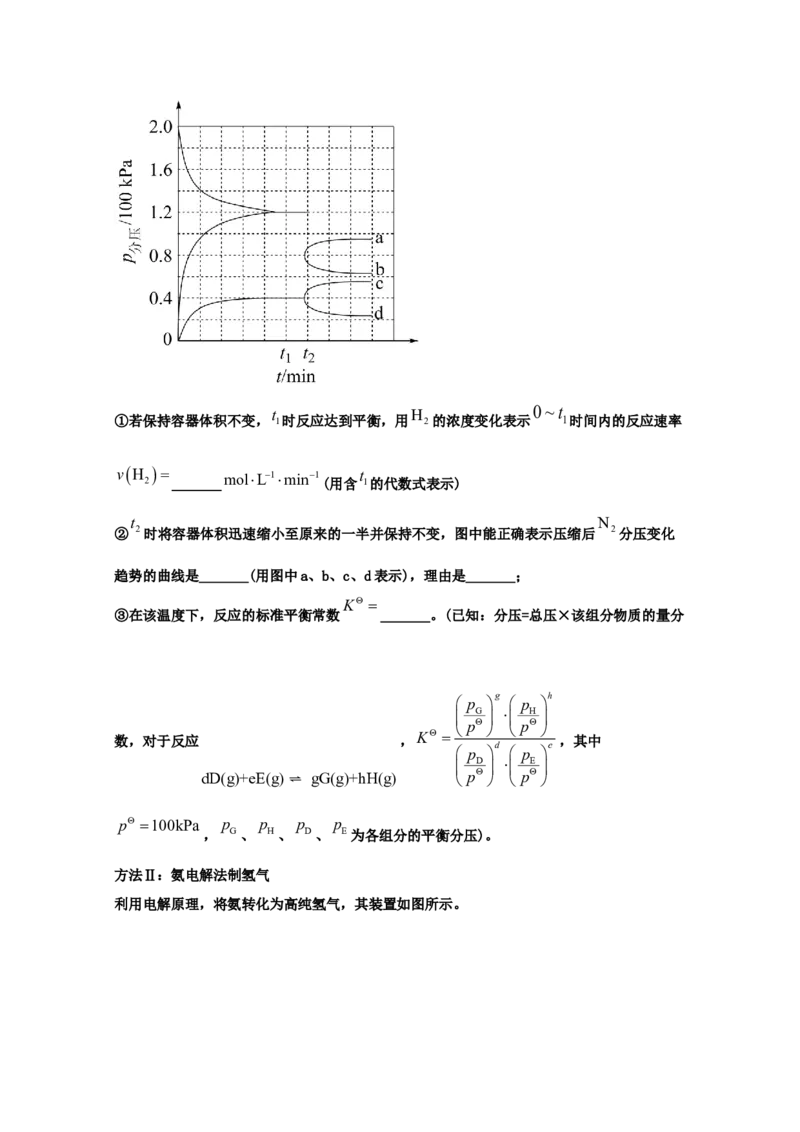
入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线
如图所示。0~t
t H
①若保持容器体积不变, 1时反应达到平衡,用 2的浓度变化表示 1时间内的反应速率
vH
2
_______
molL1min1
(用含
t
1的代数式表示)
t N
② 2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 2分压变化
趋势的曲线是_______(用图中a、b、c、d表示),理由是_______;
K
③在该温度下,反应的标准平衡常数 _______。(已知:分压=总压×该组分物质的量分
g h
p p
G H
p
p
数,对于反应 ,K ,其中
d e
p p
D E
dD(g)+eE(g) gG(g)+hH(g) p p
p 100kPa p p p p
, G 、 H、 D、 E为各组分的平衡分压)。
方法Ⅱ:氨电解法制氢气
利用电解原理,将氨转化为高纯氢气,其装置如图所示。OH
(4)电解过程中 的移动方向为_______(填“从左往右”或“从右往左”);
(5)阳极的电极反应式为_______。
KOH溶液KOH溶液
0.02
【KS5U答案】+90.8 CD t b
1
开始体积减半,N 分压变为原来的2倍,随后由于加压平衡逆向移动,N 分压比原来2
2 2
倍要小 0.48 从右往左 2NH-6e-+6OH-= N+6HO
3 2 2
【KS5U解析】
(1) 根据反应热=反应物的总键能-生成物的总键能,2NH(g) N(g)+3H(g), H=390.8kJ
3 2 2
32 3
mol-1 -(946 kJ mol-1+436.0kJ mol-1 )= +90.8kJ mol-1,故答案为:+90.8;
90.8103J/mol
H
(2)若反应自发进行,则需 H-T S<0,T> =198.9J/molK=456.5K,即温度应高
S
于(456.5-273)℃=183.5℃,CD符合,故答案为:CD;
(3)①设t 时达到平衡,转化的NH 的物质的量为2x,列出三段式:
1 3
2NH g N g 3H g
3 2 2
起始/mol 0.1 0 0
转化/mol 2x x 3x
平衡/mol 0.12x x 3x
0.1 200
根据同温同压下,混合气体的物质的量等于体积之比,0.12x =12012040,解得0.023mol 0.02 0.02
x=0.02mol,υ(H
2
)= 3Lt
1
= t
1
mol
L-1
min-1,故答案为: t
1
;
②t 时将容器体积压缩到原来的一半,开始N 分压变为原来的2倍,随后由于加压平衡逆向
2 2
移动,N 分压比原来2倍要小,故b曲线符合,故答案为:b;开始体积减半,N 分压变为原
2 2
来的2倍,随后由于加压平衡逆向移动,N 分压比原来2倍要小;
2
③由图可知,平衡时,NH、N、H 的分压分别为120 kPa、40 kPa、120 kPa,反应的标准平
3 2 2
0.4(1.2)3
衡常数 K = (1.2)2 =0.48,故答案为:0.48;
(4)由图可知,通NH 的一极氮元素化合价升高,发生氧化反应,为电解池的阳极,则另一电
3
极为阴极,电解过程中OH-移向阳极,则从右往左移动,故答案为:从右往左;
(5)阳极NH 失电子发生氧化反应生成N,结合碱性条件,电极反应式为:2NH-6e-+6OH-=
3 2 3
N+6HO,故答案为:2NH-6e-+6OH-= N+6HO。
2 2 3 2 2
2021年化学高考模拟题
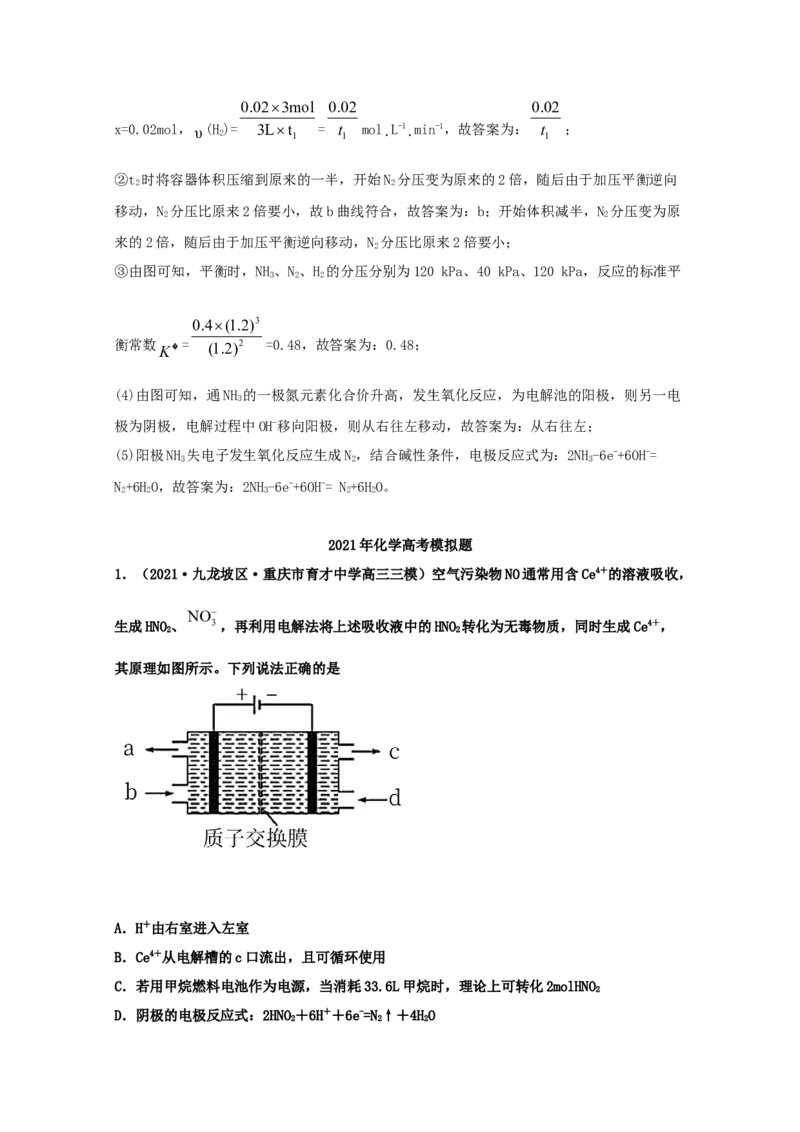
1.(2021·九龙坡区·重庆市育才中学高三三模)空气污染物NO通常用含Ce4+的溶液吸收,
NO
生成HNO、 3,再利用电解法将上述吸收液中的HNO 转化为无毒物质,同时生成Ce4+,
2 2
其原理如图所示。下列说法正确的是
A.H+由右室进入左室
B.Ce4+从电解槽的c口流出,且可循环使用
C.若用甲烷燃料电池作为电源,当消耗33.6L甲烷时,理论上可转化2molHNO
2
D.阴极的电极反应式:2HNO+6H++6e-=N↑+4HO
2 2 2【KS5U答案】D
【分析】
NO
空气污染物NO通常用含Ce4+的溶液吸收,生成HNO、 3,再利用电解法将上述吸收液中
2
的HNO 转化为无毒物质,同时生成Ce4+,电解过程中铈离子在阳极失电子被氧化生成Ce4+,
2
HNO 在阴极得到电子变化为氮气,据此分析解答。
2
【KS5U解析】
A.电解池中阳离子移向阴极,质子交换膜是允许氢离子通过,H+由左室进入右室,故A错误;
B.电解过程中铈离子在阳极失电子被氧化生成Ce4+,Ce4+从电解槽的a口流出,且可循环使
用,故B错误;
CO2-
C.甲烷燃料电池中,在碱性溶液中,甲烷燃料电池的负极反应式为CH-8e-+10OH-═ 3
4
+7HO,故每有1mol甲烷反应,转移电子8mol,阴极的电极反应式:2HNO+6H++6e-
2 2
═N↑+4HO,3CH~8HNO~24e-,当消耗标准状况下33.6L甲烷时,其物质的量=
2 2 4 2
33.6L
22.4L/mol =1.5mol,理论上可转化HNO4mol,故C错误;
2
D.HNO 在阴极上得到电子还原为氮气,电极反应式为2HNO+6H++6e-═N↑+4HO,故D正确;
2 2 2 2
故选D。
2.(2021·南岸区·重庆第二外国语学校高三三模)在日常生活中,我们经常看到铁制品
生锈、铝制品表面出现白斑等众多的金属腐蚀现象。可以通过下列装置所示实验进行探究。
下列说法正确的是A.按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,采用下列方法:用酒精灯加热左
边的具支试管
B.图Ⅲ装置的总反应为4Al+3O+6HO=4Al(OH),生成的Al(OH) 进一步脱水形成白斑
2 2 3 3
C.图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁
D.铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并
在铝箔上发生电极反应:2Cl--2e-=Cl↑
2
【KS5U答案】B
【KS5U解析】
A.具支试管内气体受热压强增大,部分气体溢出,冷却后,气体压强减小,不能更快更清
晰地观察到液柱上升,A错误;
B.正极与负极反应式相加得到图Ⅲ装置的总反应为4Al+3O+6HO=4Al(OH),生成的
2 2 3
Al(OH) 进一步脱水形成白斑,B正确;
3
C.负极材料为铁,正极为碳棒,C错误;
D.铝箔为负极,反应式为:4Al-12e-=4Al3+,碳棒为正极,反应式为:3O+12e-
2
+6HO=12OH-,D错误;
2
答案选B。
3.(2021·重庆市第十一中学校高三二模)我国科学家研发了一种K-CO 二次电池,电池总
2
放电
反应为:4KSn+3CO 2KCO+C+4Sn。下列说法错误的是
2充电 2 3
A.充电时,a电极为阴极
B.充电时,电路中每转移1 mol e-,b电极质量减少12 g
C.放电时,电子由a极经过外电路流向b极
D.放电时,a电极发生的电极反应为:KSn-e-=K++Sn
【KS5U答案】B【分析】
根据电池总反应可知放电时K被氧化,CO 被还原,所以放电时K为负极,反应式为KSn-e-=
2
2-
K++Sn,b为正极吸收CO,反应式为3CO+4e-═2CO3 +C;充电时a为阴极,b为阳极释放
2 2
CO,据此分析解答。
2
【KS5U解析】
A.充电时,K+移向a极,则a电极为阴极,故A正确;
2-
B.充电时,b为阳极,电极反应式为:C+2CO3 -4e-=3CO,每转移4 mol e-,b电极消耗12g
2
C,则转移1 mol e-,b电极质量减少3g,故B错误;
C.放电时,a为负极,b为正极,电子由负极流向正极,则电子由a极经过外电路流向b极,
故C正确;
D.放电时K被氧化,a为负极,电极发生的电极反应为:KSn-e-=K++Sn,故D正确;
故选:B。
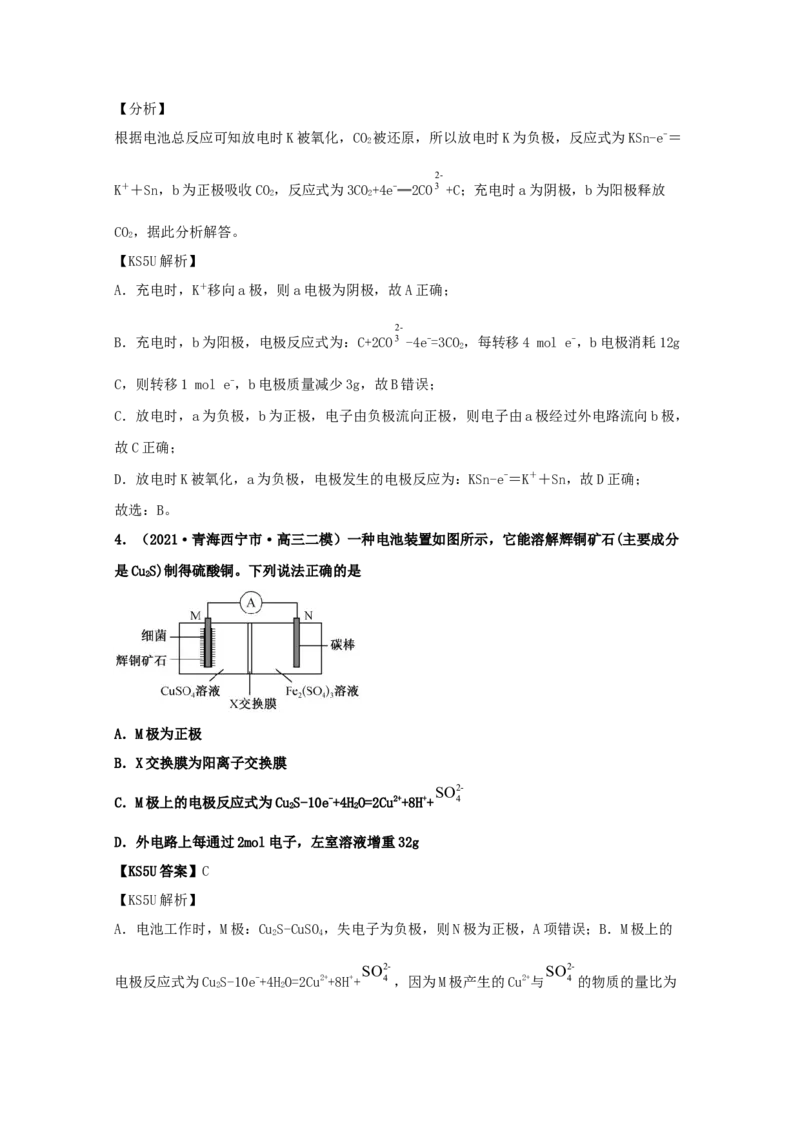
4.(2021·青海西宁市·高三二模)一种电池装置如图所示,它能溶解辉铜矿石(主要成分
是CuS)制得硫酸铜。下列说法正确的是
2
A.M极为正极
B.X交换膜为阳离子交换膜
SO2-
C.M极上的电极反应式为CuS-10e-+4HO=2Cu2++8H++ 4
2 2
D.外电路上每通过2mol电子,左室溶液增重32g
【KS5U答案】C
【KS5U解析】
A.电池工作时,M极:CuS-CuSO,失电子为负极,则N极为正极,A项错误;B.M极上的
2 4
SO2- SO2-
电极反应式为CuS-10e-+4HO=2Cu2++8H++ 4 ,因为M极产生的Cu2+与 4 的物质的量比为
2 2SO2-
2:1,故右室中 4 需通过X交换膜进人左室,则X交换膜是阴离子交换膜,B项错误;
SO2-
C.M极上的电极反应式为CuS-10e-+4HO=2Cu2++8H++ 4 ,C项正确;
2 2
D.因为外电路上每通过2 mol电子,左室溶液中除了有0.2 mol CuS溶解,还有右室中
2
SO2-
的 4 通过X交换膜进入左室,故增重超过32 g,D项错误;
答案选C。
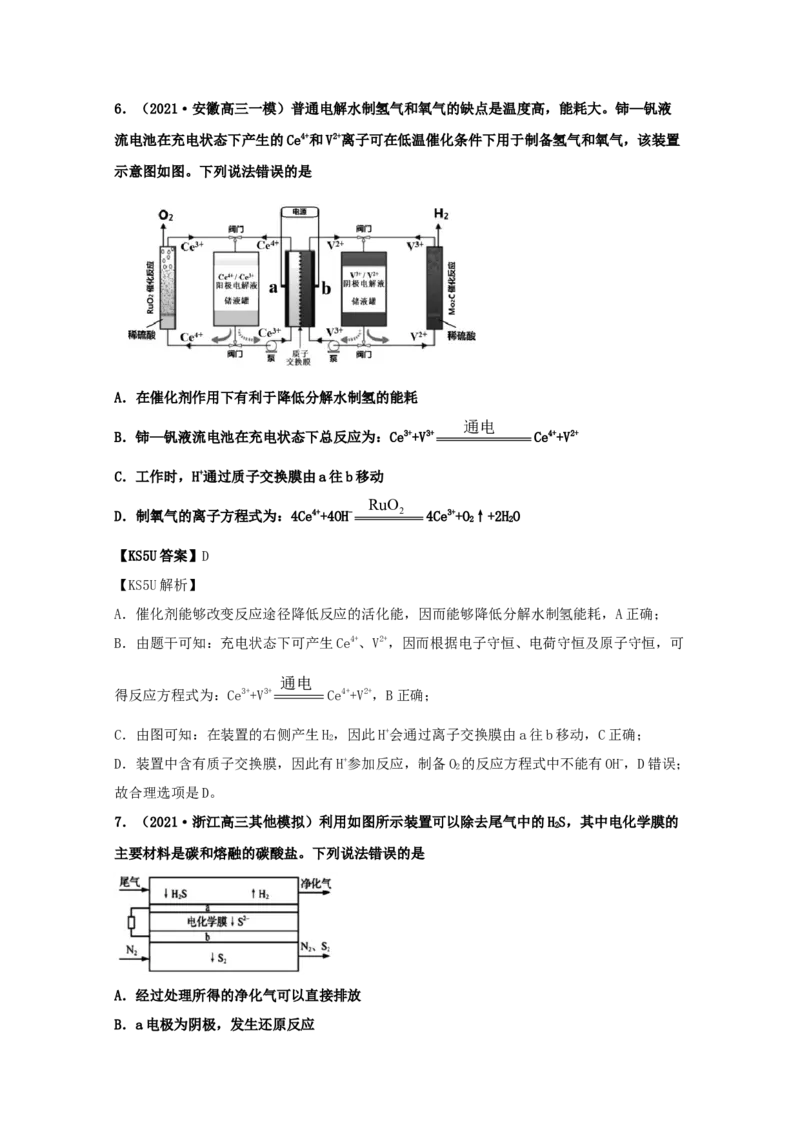
5.(2021·青海高三三模)生物电化学系统还原CO 是另一种产生甲烷的方法,装置如图所
2
示,下列说法正确的是
A.电极A为阴极
B.此交换膜为阴离子交换膜
C.电极A中消耗1 mol CHCOO-时,产生8 mol H+
3
D.电极B电极反应式为:CO+8H++8e-=CH+2HO
2 4 2
【KS5U答案】D
【分析】
电极A为阳极,电极方程式:CHCOO-+2HO-8e-=2CO+7H+,电极B为阴极,电极B电极反应式为:
3 2 2
CO+8H++8e-=CH+2HO,由此解答。
2 4 2
【KS5U解析】
A. 二氧化碳中碳化合价降低变为甲烷,在电解池阴极上发生反应,电极B为阴极,电极A
为阳极,故A错误;
B. 电极A上产生的氢离子向电极B移动,此交换膜为阳离子交换膜,故B错误;
C. 由电极方程式:CHCOO-+2HO-8e-=2CO+7H+,电极A中消耗1 mol CHCOO-时,产生7mol H
3 2 2 3
+,故C错误;
D. 碳由+4价降为-4价,电极B电极反应式为:CO+8H++8e-=CH+2HO,故D正确;
2 4 2
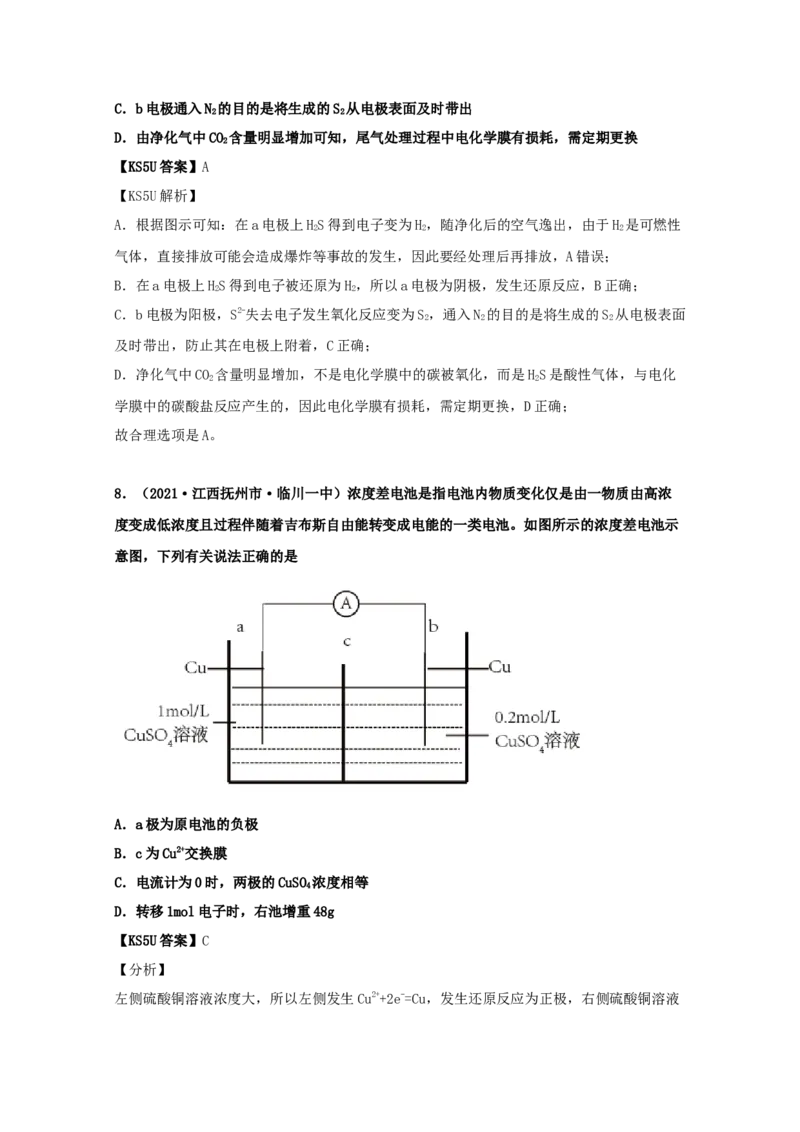
故选D。6.(2021·安徽高三一模)普通电解水制氢气和氧气的缺点是温度高,能耗大。铈—钒液
流电池在充电状态下产生的Ce4+和V2+离子可在低温催化条件下用于制备氢气和氧气,该装置
示意图如图。下列说法错误的是
A.在催化剂作用下有利于降低分解水制氢的能耗
通电
B.铈—钒液流电池在充电状态下总反应为:Ce3++V3+ Ce4++V2+
C.工作时,H+通过质子交换膜由a往b移动
RuO
D.制氧气的离子方程式为:4Ce4++4OH- 2 4Ce3++O↑+2HO
2 2
【KS5U答案】D
【KS5U解析】
A.催化剂能够改变反应途径降低反应的活化能,因而能够降低分解水制氢能耗,A正确;
B.由题干可知:充电状态下可产生Ce4+、V2+,因而根据电子守恒、电荷守恒及原子守恒,可
通电
得反应方程式为:Ce3++V3+ Ce4++V2+,B正确;
C.由图可知:在装置的右侧产生H,因此H+会通过离子交换膜由a往b移动,C正确;
2
D.装置中含有质子交换膜,因此有H+参加反应,制备O 的反应方程式中不能有OH-,D错误;
2
故合理选项是D。
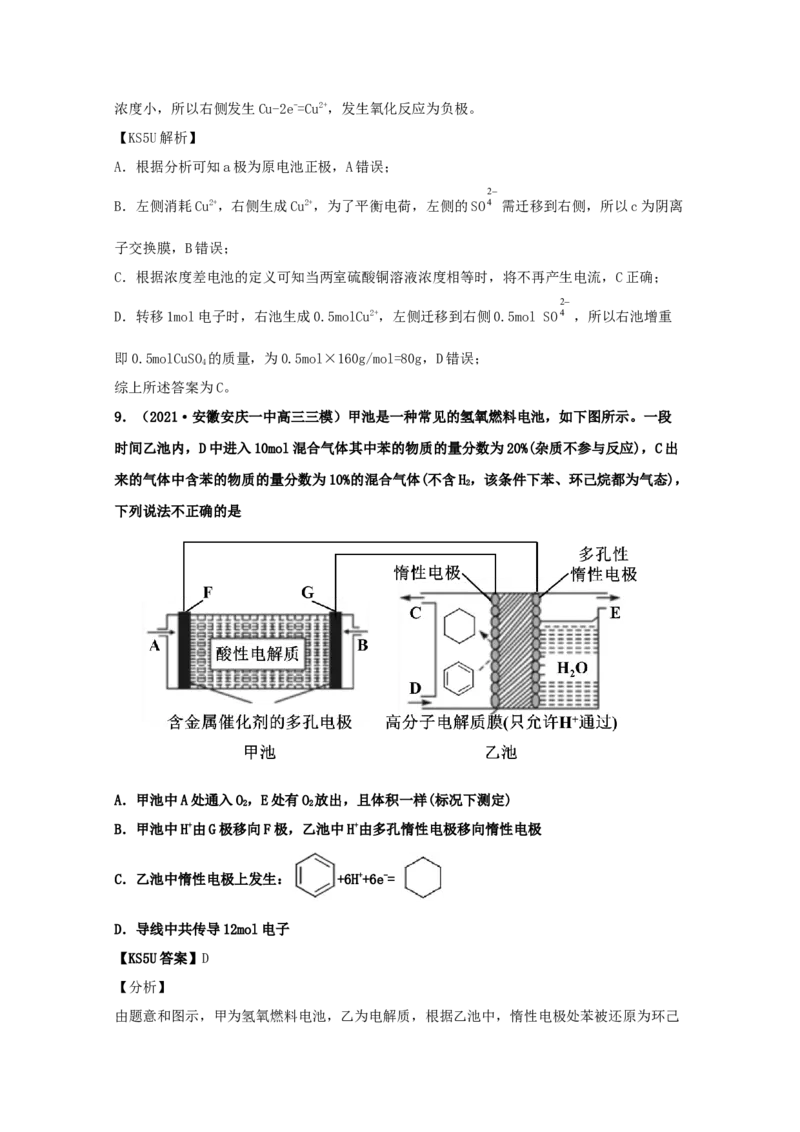
7.(2021·浙江高三其他模拟)利用如图所示装置可以除去尾气中的HS,其中电化学膜的
2
主要材料是碳和熔融的碳酸盐。下列说法错误的是
A.经过处理所得的净化气可以直接排放
B.a电极为阴极,发生还原反应C.b电极通入N 的目的是将生成的S 从电极表面及时带出
2 2
D.由净化气中CO 含量明显增加可知,尾气处理过程中电化学膜有损耗,需定期更换
2
【KS5U答案】A
【KS5U解析】
A.根据图示可知:在a电极上HS得到电子变为H,随净化后的空气逸出,由于H 是可燃性
2 2 2
气体,直接排放可能会造成爆炸等事故的发生,因此要经处理后再排放,A错误;
B.在a电极上HS得到电子被还原为H,所以a电极为阴极,发生还原反应,B正确;
2 2
C.b电极为阳极,S2-失去电子发生氧化反应变为S,通入N 的目的是将生成的S 从电极表面
2 2 2
及时带出,防止其在电极上附着,C正确;
D.净化气中CO 含量明显增加,不是电化学膜中的碳被氧化,而是HS是酸性气体,与电化
2 2
学膜中的碳酸盐反应产生的,因此电化学膜有损耗,需定期更换,D正确;
故合理选项是A。
8.(2021·江西抚州市·临川一中)浓度差电池是指电池内物质变化仅是由一物质由高浓
度变成低浓度且过程伴随着吉布斯自由能转变成电能的一类电池。如图所示的浓度差电池示
意图,下列有关说法正确的是
A.a极为原电池的负极
B.c为Cu2+交换膜
C.电流计为0时,两极的CuSO 浓度相等
4
D.转移1mol电子时,右池增重48g
【KS5U答案】C
【分析】
左侧硫酸铜溶液浓度大,所以左侧发生Cu2++2e-=Cu,发生还原反应为正极,右侧硫酸铜溶液浓度小,所以右侧发生Cu-2e-=Cu2+,发生氧化反应为负极。
【KS5U解析】
A.根据分析可知a极为原电池正极,A错误;
2
B.左侧消耗Cu2+,右侧生成Cu2+,为了平衡电荷,左侧的SO4 需迁移到右侧,所以c为阴离
子交换膜,B错误;
C.根据浓度差电池的定义可知当两室硫酸铜溶液浓度相等时,将不再产生电流,C正确;
2
D.转移1mol电子时,右池生成0.5molCu2+,左侧迁移到右侧0.5mol SO4 ,所以右池增重
即0.5molCuSO 的质量,为0.5mol×160g/mol=80g,D错误;
4
综上所述答案为C。
9.(2021·安徽安庆一中高三三模)甲池是一种常见的氢氧燃料电池,如下图所示。一段
时间乙池内,D中进入10mol混合气体其中苯的物质的量分数为20%(杂质不参与反应),C出
来的气体中含苯的物质的量分数为10%的混合气体(不含H,该条件下苯、环己烷都为气态),
2
下列说法不正确的是
A.甲池中A处通入O,E处有O 放出,且体积一样(标况下测定)
2 2
B.甲池中H+由G极移向F极,乙池中H+由多孔惰性电极移向惰性电极
C.乙池中惰性电极上发生: +6H++6e-=
D.导线中共传导12mol电子
【KS5U答案】D
【分析】
由题意和图示,甲为氢氧燃料电池,乙为电解质,根据乙池中,惰性电极处苯被还原为环己烷,故惰性电极发生还原反应为阴极,多孔性惰性电极为阳极,则G电极与阴极相连,为原
电池负极,F为正极,故甲池中F为正极,A处通入氧气,G为负极,B处通入氢气。
【KS5U解析】
A.由分析,A处通入O,E处为电解池阳极产物,阳极是水放电生成氢气和H+,由于电子转
2
移守恒,故两处的氧气的物质的量相同,体积相同,A正确;
B.原电池中阳离子向正极移动,F极为正极,故甲池中H+由G极移向F极,电解池中,阳离
子向阴极移动,惰性电极为阴极,故乙池中H+由多孔惰性电极移向惰性电极,B正确;
C.乙池中,惰性电极处苯得到电子,被还原为环己烷,电极方程式为: +6H++6e-=
,C正确;
D.10mol含20%苯的混合气体,经过电解生成10mol含苯10%的混合气体,则被还原分苯的
物质的量为10mol(20%-10%)=1mol,由电极方程式得转移电子的物质的量为6mol,D错误;
故选D。
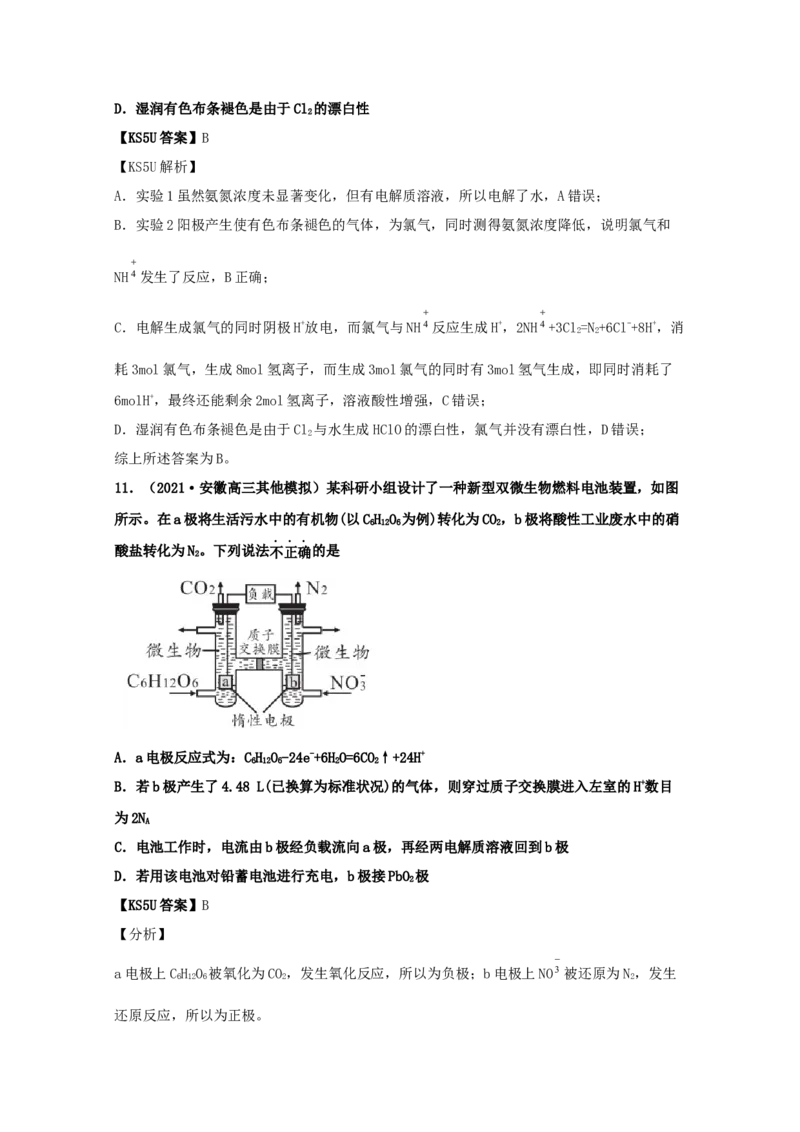
10.(2021·河南新乡市·新乡县一中高三其他模拟)某课外小组同学为探究氨氮废水的处
理方法,以0.005mol/L(NH)SO 溶液模拟氨氮废水,设计了以下实验
4 2 4
实验步骤 实验现象
一段时间后,检测阳极附近溶液
1.如图装置进行电解
中氨氮浓度并未显著变化
阳极产生使湿润有色布条褪色的
2.在氨氮废水中加入NaCl溶
气体,一段时间后,氨氮检测浓
液,进行电解
度明显降低
有关叙述正确的是
A.实验1由于氨氮浓度未显著变化,装置未发生电解反应
+
B.实验2中的氨氮浓度降低是由于生成的氯气氧化了NH4
C.氨氮浓度降低时溶液酸性减弱D.湿润有色布条褪色是由于Cl 的漂白性
2
【KS5U答案】B
【KS5U解析】
A.实验1虽然氨氮浓度未显著变化,但有电解质溶液,所以电解了水,A错误;
B.实验2阳极产生使有色布条褪色的气体,为氯气,同时测得氨氮浓度降低,说明氯气和
+
NH4发生了反应,B正确;
+ +
C.电解生成氯气的同时阴极H+放电,而氯气与NH4反应生成H+,2NH4+3Cl=N+6Cl-+8H+,消
2 2
耗3mol氯气,生成8mol氢离子,而生成3mol氯气的同时有3mol氢气生成,即同时消耗了
6molH+,最终还能剩余2mol氢离子,溶液酸性增强,C错误;
D.湿润有色布条褪色是由于Cl 与水生成HClO的漂白性,氯气并没有漂白性,D错误;
2
综上所述答案为B。
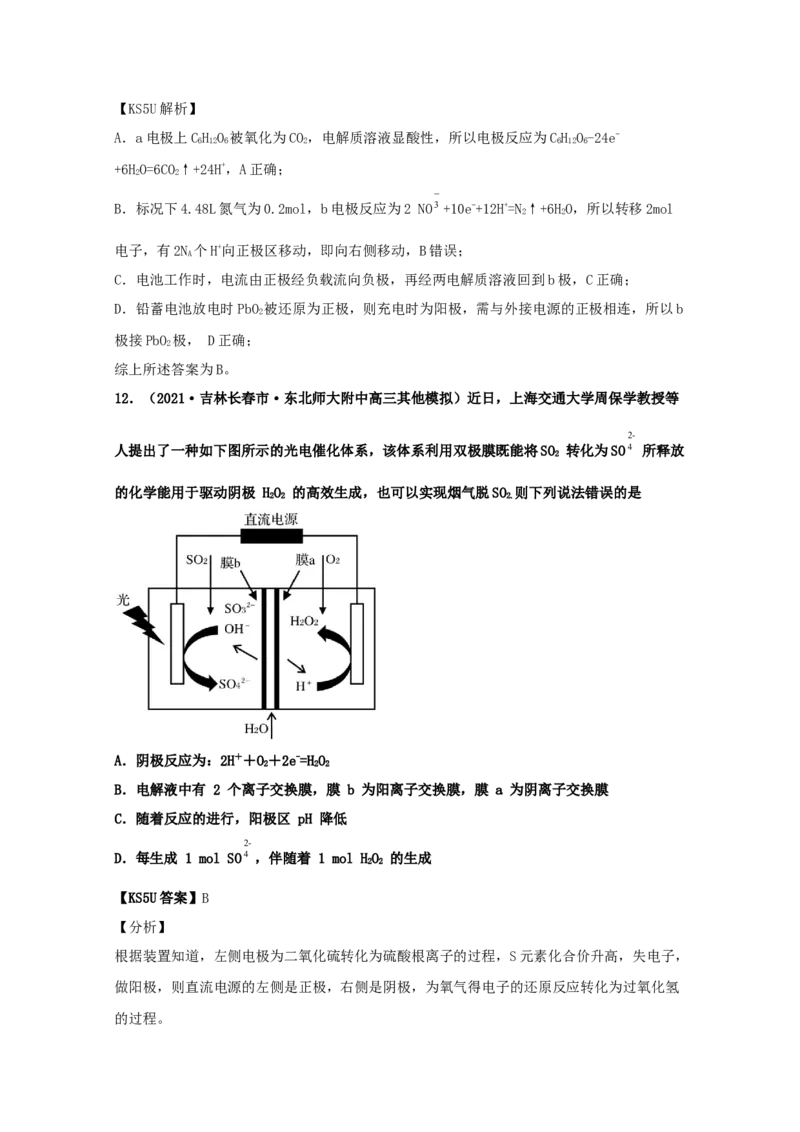
11.(2021·安徽高三其他模拟)某科研小组设计了一种新型双微生物燃料电池装置,如图
所示。在a极将生活污水中的有机物(以CH O 为例)转化为CO,b极将酸性工业废水中的硝
6 12 6 2
酸盐转化为N。下列说法不正确的是
2
A.a电极反应式为:CH O-24e-+6HO=6CO↑+24H+
6 12 6 2 2
B.若b极产生了4.48 L(已换算为标准状况)的气体,则穿过质子交换膜进入左室的H+数目
为2N
A
C.电池工作时,电流由b极经负载流向a极,再经两电解质溶液回到b极
D.若用该电池对铅蓄电池进行充电,b极接PbO 极
2
【KS5U答案】B
【分析】
a电极上CH O 被氧化为CO,发生氧化反应,所以为负极;b电极上NO3 被还原为N,发生
6 12 6 2 2
还原反应,所以为正极。【KS5U解析】
A.a电极上CH O 被氧化为CO,电解质溶液显酸性,所以电极反应为CH O-24e-
6 12 6 2 6 12 6
+6HO=6CO↑+24H+,A正确;
2 2
B.标况下4.48L氮气为0.2mol,b电极反应为2 NO3 +10e-+12H+=N↑+6HO,所以转移2mol
2 2
电子,有2N 个H+向正极区移动,即向右侧移动,B错误;
A
C.电池工作时,电流由正极经负载流向负极,再经两电解质溶液回到b极,C正确;
D.铅蓄电池放电时PbO 被还原为正极,则充电时为阳极,需与外接电源的正极相连,所以b
2
极接PbO 极, D正确;
2
综上所述答案为B。
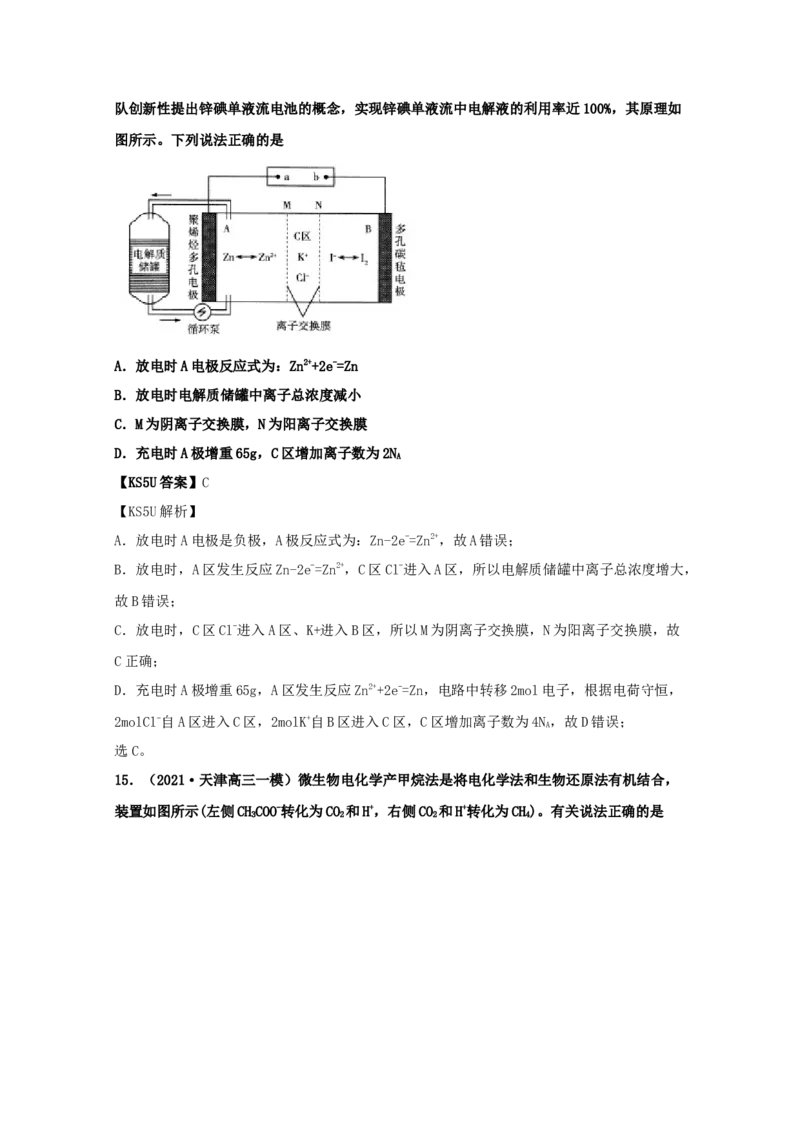
12.(2021·吉林长春市·东北师大附中高三其他模拟)近日,上海交通大学周保学教授等
2-
人提出了一种如下图所示的光电催化体系,该体系利用双极膜既能将SO 转化为SO4 所释放
2
的化学能用于驱动阴极 HO 的高效生成,也可以实现烟气脱SO 则下列说法错误的是
2 2 2.
A.阴极反应为:2H++O+2e-=HO
2 2 2
B.电解液中有 2 个离子交换膜,膜 b 为阳离子交换膜,膜 a 为阴离子交换膜
C.随着反应的进行,阳极区 pH 降低
2-
D.每生成 1 mol SO4 ,伴随着 1 mol HO 的生成
2 2
【KS5U答案】B
【分析】
根据装置知道,左侧电极为二氧化硫转化为硫酸根离子的过程,S元素化合价升高,失电子,
做阳极,则直流电源的左侧是正极,右侧是阴极,为氧气得电子的还原反应转化为过氧化氢
的过程。【KS5U解析】
A.右侧是阴极,为氧气得电子的还原反应转化为过氧化氢的过程,阴极反应为:2H++O+
2
2e-=HO,故A正确;
2 2
B.根据装置知道,氢氧根离子靠近阳极的交换膜进入阳极参加反应,应该为阴离子交换膜;
氢离子通过靠近阴极的交换膜进入阴极参加反应,应该为阳离子交换膜,故B错误;
C.根据装置知道,左侧电极为二氧化硫转化为硫酸根离子的过程,氢氧根离子被消耗,碱
性减弱,pH降低,故C正确;
D.二氧化硫转化为硫酸根离子,每生成1mol硫酸根离子,伴随2mol电子转移,根据电子守
恒,得到的过氧化氢是1mol,故D正确;
故选B。
13.(2021·阜新市第二高级中学高三其他模拟)科学家利用电化学装置实现了CH 和CO 的
4 2
耦合转化,原理如图。下列说法错误的是
A.电极A的电极反应式为:CO+2e-=CO+O2-
2
B.该装置工作时,固体电解质中O2-向电极A移动
C.若一定条件下生成的乙烯和乙烷的体积比为3:1,则消耗的CH 和CO 的体积比为8:7
4 2
D.电催化CO 被还原为CO可以改善温室效应,提供工业原料
2
【KS5U答案】B
【KS5U解析】
A.根据图示可知:在阴极(A电极)反应式为:CO+2e-=CO+O2-,A正确;
2
B.该装置工作时,固体电解质中阴离子O2-向正电荷较多的阳极B电极定向移动,B错误;
C.阳极乙烯和乙烷的体积比为3:1,则B电极反应式为:8CH+7O-14e-=3CH+CH+7HO,结
4 2 2 4 2 6 2
合阴极电极反应式,可得总反应为8CH+7CO=3CH+CH+CO+7HO。可见反应时消耗的相同外
4 2 2 4 2 6 2
界条件下CH 和CO 的体积比为8:7,C正确;
4 2
D.电催化CO 被还原为CO,能够降低空气中CO 的浓度,因此可有效改善温室效应,转化的
2 2
CO可作为化工原料,D正确;
故合理选项是B。
14.(2021·黑龙江哈尔滨市·哈尔滨三中高三其他模拟)中国科学院大连化物所的研究团队创新性提出锌碘单液流电池的概念,实现锌碘单液流中电解液的利用率近100%,其原理如
图所示。下列说法正确的是
A.放电时A电极反应式为:Zn2++2e-=Zn
B.放电时电解质储罐中离子总浓度减小
C.M为阴离子交换膜,N为阳离子交换膜
D.充电时A极增重65g,C区增加离子数为2N
A
【KS5U答案】C
【KS5U解析】
A.放电时A电极是负极,A极反应式为:Zn-2e-=Zn2+,故A错误;
B.放电时,A区发生反应Zn-2e-=Zn2+,C区Cl-进入A区,所以电解质储罐中离子总浓度增大,
故B错误;
C.放电时,C区Cl-进入A区、K+进入B区,所以M为阴离子交换膜,N为阳离子交换膜,故
C正确;
D.充电时A极增重65g,A区发生反应Zn2++2e-=Zn,电路中转移2mol电子,根据电荷守恒,
2molCl-自A区进入C区,2molK+自B区进入C区,C区增加离子数为4N,故D错误;
A
选C。
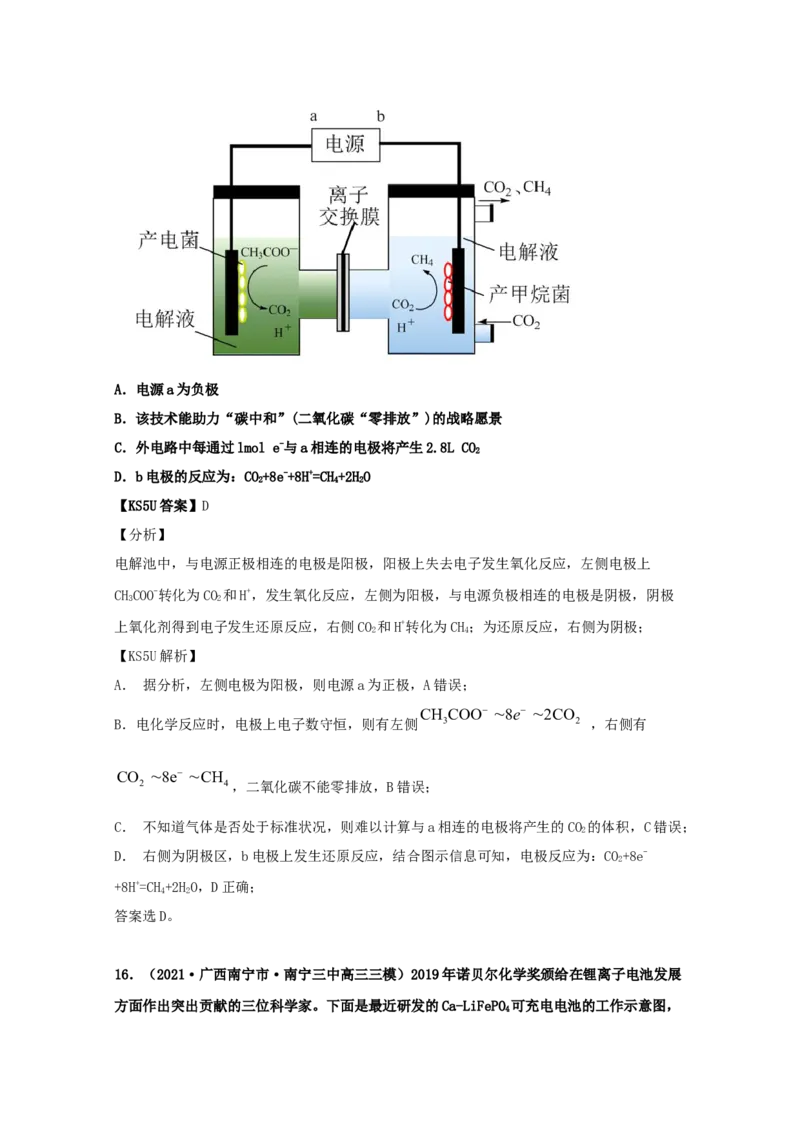
15.(2021·天津高三一模)微生物电化学产甲烷法是将电化学法和生物还原法有机结合,
装置如图所示(左侧CHCOO-转化为CO 和H+,右侧CO 和H+转化为CH)。有关说法正确的是
3 2 2 4A.电源a为负极
B.该技术能助力“碳中和”(二氧化碳“零排放”)的战略愿景
C.外电路中每通过lmol e-与a相连的电极将产生2.8L CO
2
D.b电极的反应为:CO+8e-+8H+=CH+2HO
2 4 2
【KS5U答案】D
【分析】
电解池中,与电源正极相连的电极是阳极,阳极上失去电子发生氧化反应,左侧电极上
CHCOO-转化为CO 和H+,发生氧化反应,左侧为阳极,与电源负极相连的电极是阴极,阴极
3 2
上氧化剂得到电子发生还原反应,右侧CO 和H+转化为CH;为还原反应,右侧为阴极;
2 4
【KS5U解析】
A. 据分析,左侧电极为阳极,则电源a为正极,A错误;
CH COO 8e 2CO
B.电化学反应时,电极上电子数守恒,则有左侧 3 2 ,右侧有
CO 8e CH
2 4,二氧化碳不能零排放,B错误;
C. 不知道气体是否处于标准状况,则难以计算与a相连的电极将产生的CO 的体积,C错误;
2
D. 右侧为阴极区,b电极上发生还原反应,结合图示信息可知,电极反应为:CO+8e-
2
+8H+=CH+2HO,D正确;
4 2
答案选D。
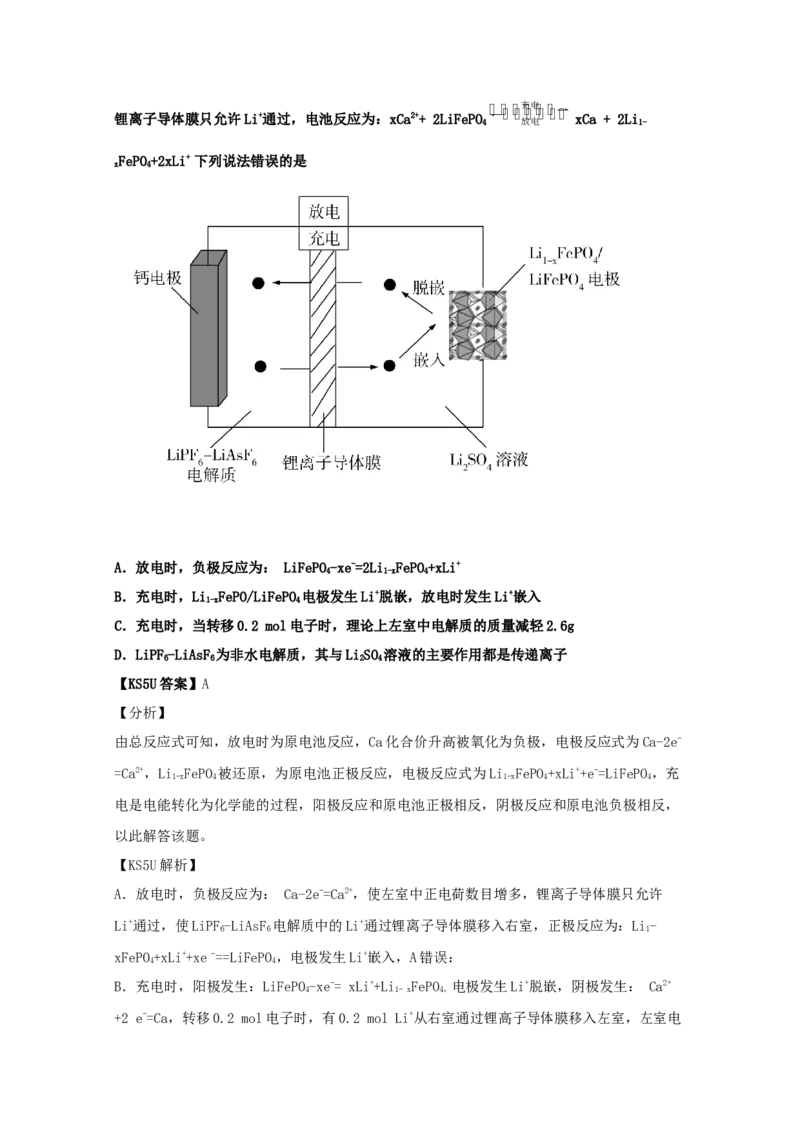
16.(2021·广西南宁市·南宁三中高三三模)2019年诺贝尔化学奖颁给在锂离子电池发展
方面作出突出贡献的三位科学家。下面是最近研发的Ca-LiFePO 可充电电池的工作示意图,
4锂离子导体膜只允许Li+通过,电池反应为:xCa2++ 2LiFePO 充 电 xCa + 2Li
4 放电 1-
FePO+2xLi+下列说法错误的是
x 4
A.放电时,负极反应为: LiFePO-xe-=2Li FePO+xLi+
4 1-x 4
B.充电时,Li FePO/LiFePO 电极发生Li+脱嵌,放电时发生Li+嵌入
1-x 4
C.充电时,当转移0.2 mol电子时,理论上左室中电解质的质量减轻2.6g
D.LiPF-LiAsF 为非水电解质,其与LiSO 溶液的主要作用都是传递离子
6 6 2 4
【KS5U答案】A
【分析】
由总反应式可知,放电时为原电池反应,Ca化合价升高被氧化为负极,电极反应式为Ca-2e-
=Ca2+,Li FePO 被还原,为原电池正极反应,电极反应式为Li FePO+xLi++e-=LiFePO,充
1-x 4 1-x 4 4
电是电能转化为化学能的过程,阳极反应和原电池正极相反,阴极反应和原电池负极相反,
以此解答该题。
【KS5U解析】
A.放电时,负极反应为: Ca-2e-=Ca2+,使左室中正电荷数目增多,锂离子导体膜只允许
Li+通过,使LiPF-LiAsF 电解质中的Li+通过锂离子导体膜移入右室,正极反应为:Li-
6 6 1
xFePO+xLi++xe -==LiFePO,电极发生Li+嵌入,A错误:
4 4
B.充电时,阳极发生:LiFePO-xe-= xLi++Li FePO 电极发生Li+脱嵌,阴极发生: Ca2+
4 1- x 4,
+2 e-=Ca,转移0.2 mol电子时,有0.2 mol Li+从右室通过锂高子导体膜移入左室,左室电解质中有0.1 mol Ca2+得电子生成Ca沉积在钙电极上,故左室中电解质的质量减轻40×0.1g
-7×0.2 g=2.6g,B正确:
C.由B选项分析,可知当转移0.2 mol电子时,理论上左室中电解质的质量减轻2.6g,C正
确;
D.钙与水能够剧烈反应,所以,左室中的LiPF-LiAsF电解质一定为非水电解质,LiSO 溶
6 2 4
液为右室中的电解质溶液,它们的主要作用都是传递离子,形成电流,构成闭合回路,D正
确。
故选:A。
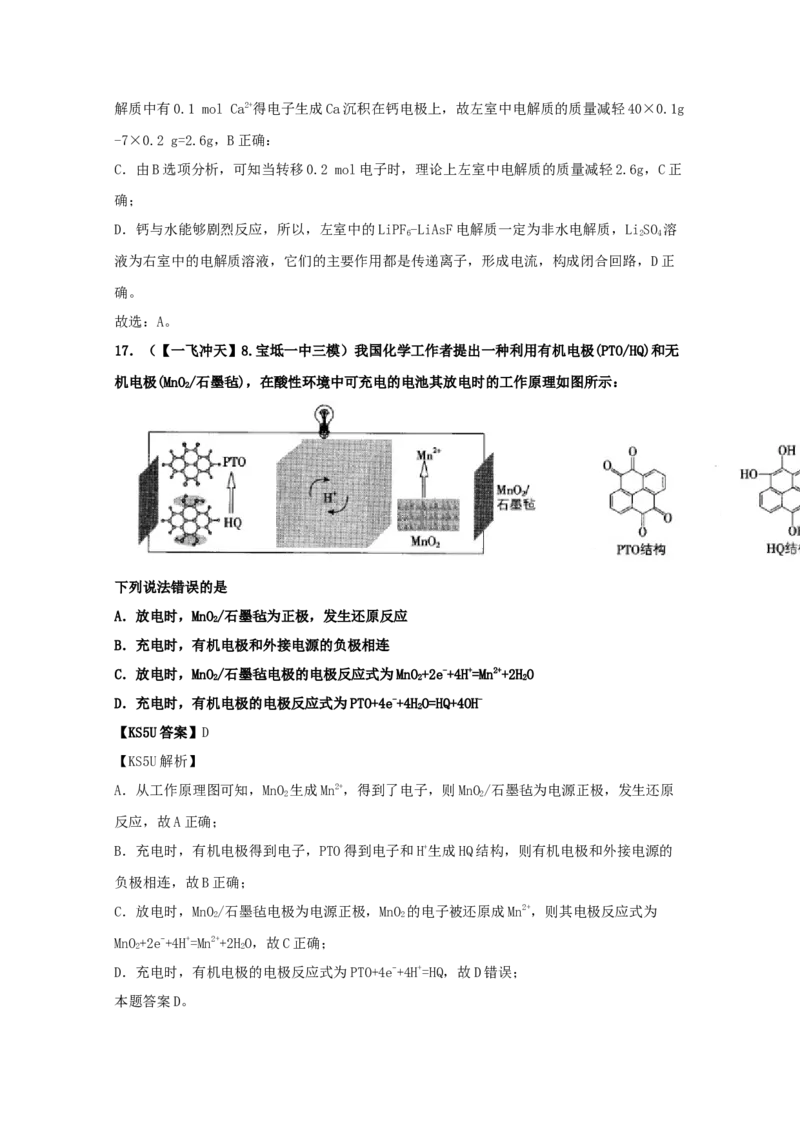
17.(【一飞冲天】8.宝坻一中三模)我国化学工作者提出一种利用有机电极(PTO/HQ)和无
机电极(MnO/石墨毡),在酸性环境中可充电的电池其放电时的工作原理如图所示:
2
下列说法错误的是
A.放电时,MnO/石墨毡为正极,发生还原反应
2
B.充电时,有机电极和外接电源的负极相连
C.放电时,MnO/石墨毡电极的电极反应式为MnO+2e-+4H+=Mn2++2HO
2 2 2
D.充电时,有机电极的电极反应式为PTO+4e-+4HO=HQ+4OH-
2
【KS5U答案】D
【KS5U解析】
A.从工作原理图可知,MnO 生成Mn2+,得到了电子,则MnO/石墨毡为电源正极,发生还原
2 2
反应,故A正确;
B.充电时,有机电极得到电子,PTO得到电子和H+生成HQ结构,则有机电极和外接电源的
负极相连,故B正确;
C.放电时,MnO/石墨毡电极为电源正极,MnO 的电子被还原成Mn2+,则其电极反应式为
2 2
MnO+2e-+4H+=Mn2++2HO,故C正确;
2 2
D.充电时,有机电极的电极反应式为PTO+4e-+4H+=HQ,故D错误;
本题答案D。
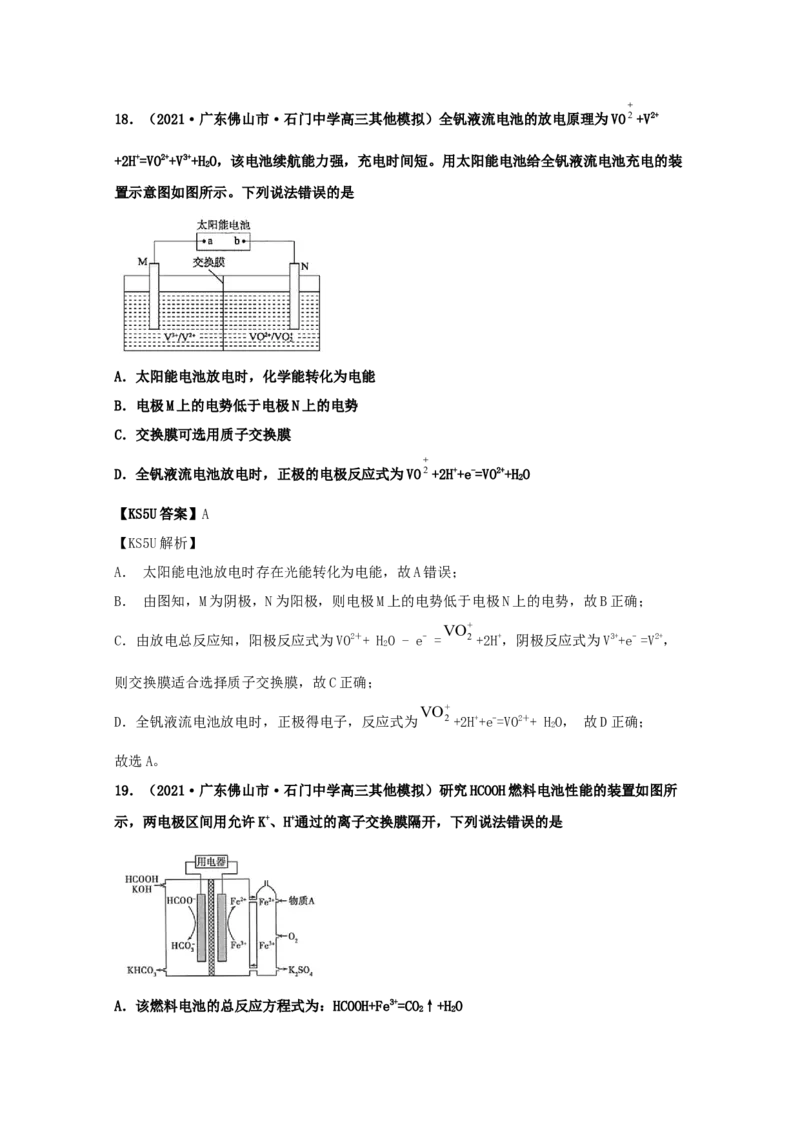
18.(2021·广东佛山市·石门中学高三其他模拟)全钒液流电池的放电原理为VO2+V2+
+2H+=VO2++V3++HO,该电池续航能力强,充电时间短。用太阳能电池给全钒液流电池充电的装
2
置示意图如图所示。下列说法错误的是
A.太阳能电池放电时,化学能转化为电能
B.电极M上的电势低于电极N上的电势
C.交换膜可选用质子交换膜
D.全钒液流电池放电时,正极的电极反应式为VO2+2H++e-=VO2++HO
2
【KS5U答案】A
【KS5U解析】
A. 太阳能电池放电时存在光能转化为电能,故A错误;
B. 由图知,M为阴极,N为阳极,则电极M上的电势低于电极N上的电势,故B正确;
VO+
C.由放电总反应知,阳极反应式为VO2++ HO - e- = 2 +2H+,阴极反应式为V3++e- =V2+,
2
则交换膜适合选择质子交换膜,故C正确;
VO+
D.全钒液流电池放电时,正极得电子,反应式为 2 +2H++e-=VO2++ HO, 故D正确;
2
故选A。
19.(2021·广东佛山市·石门中学高三其他模拟)研究HCOOH燃料电池性能的装置如图所
示,两电极区间用允许K+、H+通过的离子交换膜隔开,下列说法错误的是
A.该燃料电池的总反应方程式为:HCOOH+Fe3+=CO↑+HO
2 2B.放电过程中,K+向右移动
C.放电过程中需要补充的物质A为HSO
2 4
HCO
D.电池负极电极反应式为:HCOO-+2OH--2e-= 3+HO
2
【KS5U答案】A
【KS5U解析】
HCO
A.该装置是燃料电池,因此总方程式为2HCOOH+O+2OH-=2 3+2HO,选项A错误;
2 2
B.根据图示,该燃料电池加入HCOOH的一端为负极,通入O 的一端为正极,因此放电时K+向
2
正极移动,即向右移动,选项B正确;
C.在正极一端发生的反应为O+4Fe2++4H+=4Fe3++2HO,需要消耗H+,且排出KSO,可推出需
2 2 2 4
要补充的物质A为HSO,选项C正确;
2 4
HCO
D.根据图示,负极的电极反应式为:HCOO-+2OH--2e-= 3+HO,选项D正确。
2
答案选A。
20.(2021·天津高三一模)近日,南开大学陈军院士团队以KSn合金为负极,以含羧基多
壁碳纳米管(MWCNTs—COOH)为正极催化剂构建了可充电K—CO 电池(如图所示),电池反应为
2
4KSn+3CO 2
充
放
电
电
2K 2 CO 3 +C+4Sn,其中生成的K 2 CO 3 附着在正极上。该成果对改善环境和缓解
能源问题具有巨大潜力。下列说法正确的是
A.放电时,电子由KSn合金经酯基电解质流向MWCNTs—COOH
B.电池每吸收22.4LCO,电路中转移4mole-
2
C.充电时,阳极电极反应式为:C-4e-+2KCO=3CO↑+4K+
2 3 2
D.为了更好的吸收温室气体CO,可用适当浓度的KOH溶液代替酯基电解质
2【KS5U答案】C
【KS5U解析】
A.放电时,KSn合金作负极,MWCNTs-COOH作正极,在内电路中电流由负极流向正极,选项
A错误;
B.气体未指明状况,无法根据体积确定其物质的量,选项B错误;
C.充电时,阳极发生氧化反应,电极反应为C-4e-+2KCO=3CO↑+4K+,选项C正确;
2 3 2
D.若用KOH溶液代替酯基电解质,则KOH会与正极上的MWCNTs-COOH发生反应,因此不能使
用KOH溶液代替酯基电解质,选项D错误;
答案选C。
21.(2021·天津高三一模)锌电池具有价格便宜、比能量大、可充电等优点。一种新型锌
电池的工作原理如图所示(凝胶中允许离子生成或迁移)。下列说法正确的是
SO2-
A.放电过程中, 4 向a极迁移
B.充电过程中,b电极反应为:Zn2++2e-=Zn
C.充电时,a电极与电源正极相连
D.放电过程中,转移0.4mole-时,a电极消耗0.4molH+
【KS5U答案】C
【KS5U解析】
A.放电过程中,a为正极, b极为负极,溶液中阳离子移向正极,阴离子移向负极,所以放
SO2-
电过程中, 4 向b极迁移,A项错误;ZnOH2
B.充电过程中b电极得到电子发生还原反应,由于在碱性环境中Zn以 形式存在,
4
ZnOH2
则充电过程中, b电极应为: +2e-=Zn+4OH-,B项错误;
4
C.由图示可知,充电时,a电极失电子发生氧化反应,即a电极与电源正极相连,C项正确;
ZnOH2
D.放电过程中b电极为负极,其电极反应式为Zn+4OH--2e-= , a极为正极,则
4
其电极反应式为, MnO+4H++2e-=Mn2+ +2HO,所以放电过程中,转移0.4mole-时,a电极消耗
2 2
0.8molH+,D项错误;
答案选C。
N H
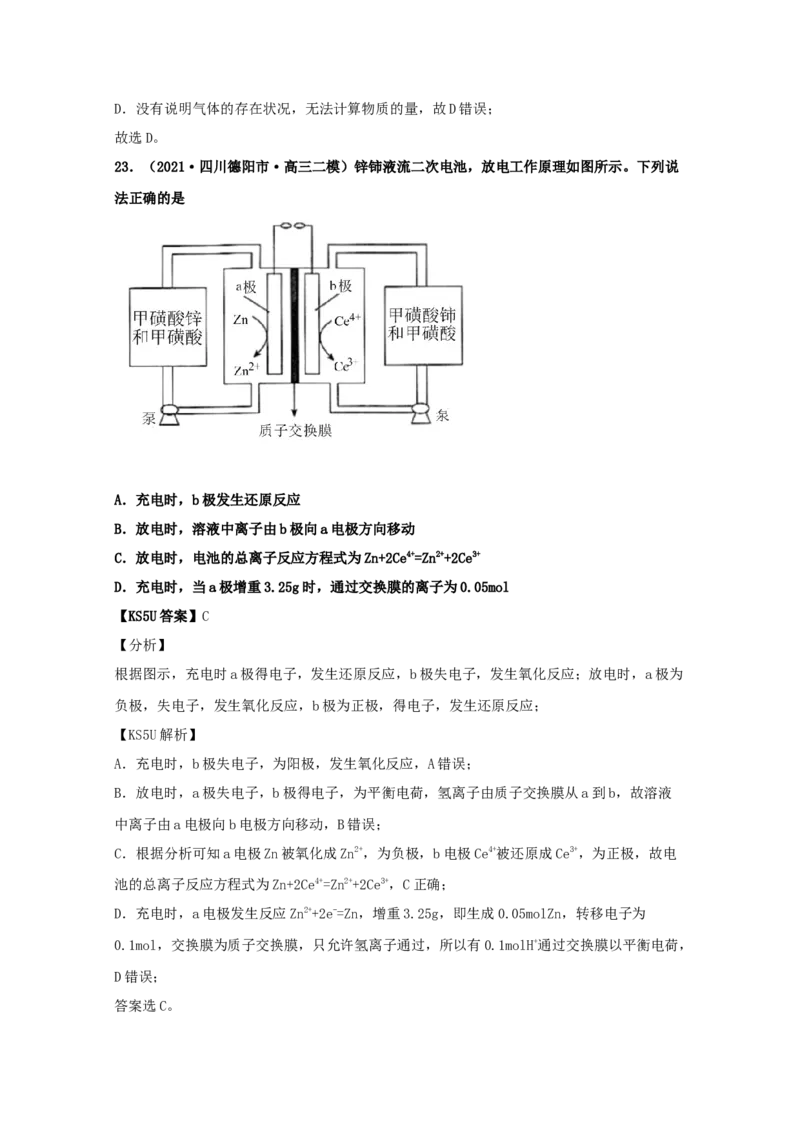
22.(2021·辽宁高三其他模拟)某实验室设计了如图装置制备 2 4。双极膜是阴、阳复
H O
合膜,层间的 2 解离成H和OH 并分别通过阴、阳膜定向移动。下列说法错误的是
Pt
A. 为负极
ClO 2e 2H=Cl H O
B.石墨电极反应式为 2
OH
C.双极膜中产生的 移向Pt电极
11.2L NH 1mol H O
D.每消耗 3时双极膜中消耗 2
【KS5U答案】D
【KS5U解析】
A.Pt电极一侧NH 生成NH,发生了失电子的氧化反应,所以为负极,故A正确;
3 2 4
H ClO
B.双极膜中的 移向正极, 得电子发生还原反应,故B正确;
C.阴离子移向负极,故C正确;D.没有说明气体的存在状况,无法计算物质的量,故D错误;
故选D。
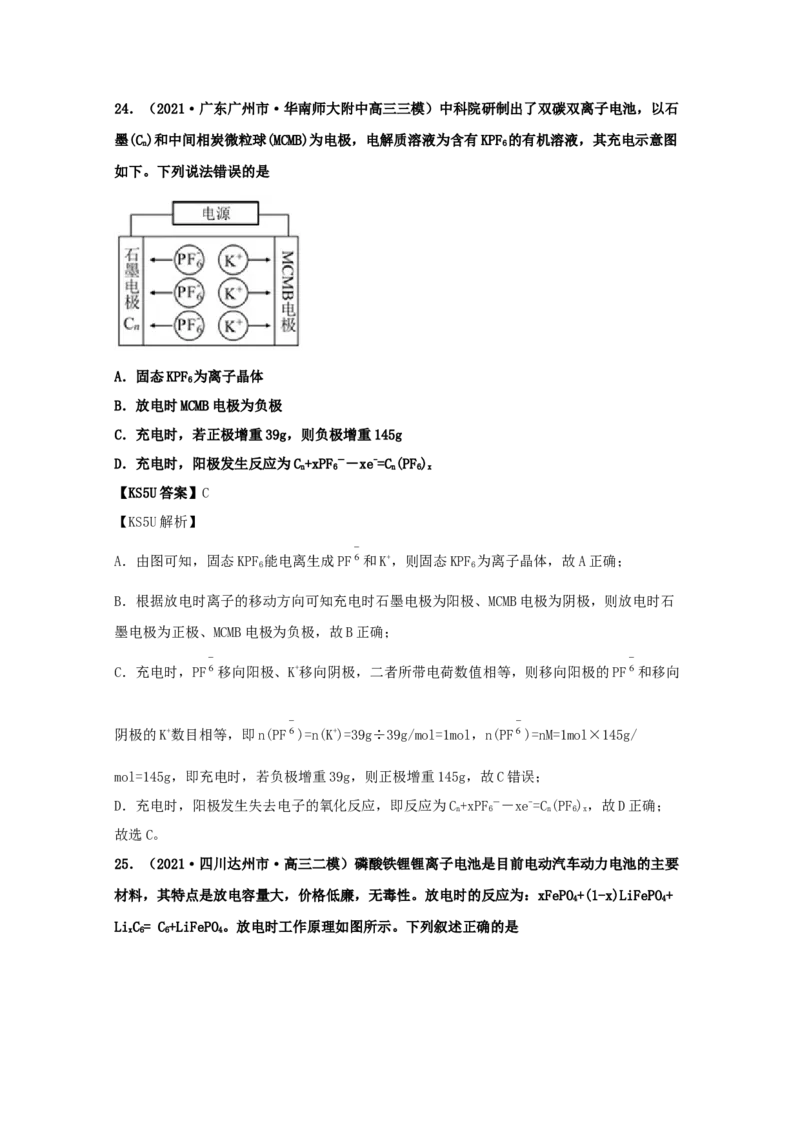
23.(2021·四川德阳市·高三二模)锌铈液流二次电池,放电工作原理如图所示。下列说
法正确的是
A.充电时,b极发生还原反应
B.放电时,溶液中离子由b极向a电极方向移动
C.放电时,电池的总离子反应方程式为Zn+2Ce4+=Zn2++2Ce3+
D.充电时,当a极增重3.25g时,通过交换膜的离子为0.05mol
【KS5U答案】C
【分析】
根据图示,充电时a极得电子,发生还原反应,b极失电子,发生氧化反应;放电时,a极为
负极,失电子,发生氧化反应,b极为正极,得电子,发生还原反应;
【KS5U解析】
A.充电时,b极失电子,为阳极,发生氧化反应,A错误;
B.放电时,a极失电子,b极得电子,为平衡电荷,氢离子由质子交换膜从a到b,故溶液
中离子由a电极向b电极方向移动,B错误;
C.根据分析可知a电极Zn被氧化成Zn2+,为负极,b电极Ce4+被还原成Ce3+,为正极,故电
池的总离子反应方程式为Zn+2Ce4+=Zn2++2Ce3+,C正确;
D.充电时,a电极发生反应Zn2++2e-=Zn,增重3.25g,即生成0.05molZn,转移电子为
0.1mol,交换膜为质子交换膜,只允许氢离子通过,所以有0.1molH+通过交换膜以平衡电荷,
D错误;
答案选C。24.(2021·广东广州市·华南师大附中高三三模)中科院研制出了双碳双离子电池,以石
墨(C)和中间相炭微粒球(MCMB)为电极,电解质溶液为含有KPF 的有机溶液,其充电示意图
n 6
如下。下列说法错误的是
A.固态KPF 为离子晶体
6
B.放电时MCMB电极为负极
C.充电时,若正极增重39g,则负极增重145g
D.充电时,阳极发生反应为C+xPF--xe-=C(PF)
n 6 n 6 x
【KS5U答案】C
【KS5U解析】
A.由图可知,固态KPF 能电离生成PF6和K+,则固态KPF 为离子晶体,故A正确;
6 6
B.根据放电时离子的移动方向可知充电时石墨电极为阳极、MCMB电极为阴极,则放电时石
墨电极为正极、MCMB电极为负极,故B正确;
C.充电时,PF6移向阳极、K+移向阴极,二者所带电荷数值相等,则移向阳极的PF6和移向
阴极的K+数目相等,即n(PF6)=n(K+)=39g÷39g/mol=1mol,n(PF6)=nM=1mol×145g/
mol=145g,即充电时,若负极增重39g,则正极增重145g,故C错误;
D.充电时,阳极发生失去电子的氧化反应,即反应为C+xPF--xe-=C(PF),故D正确;
n 6 n 6 x
故选C。
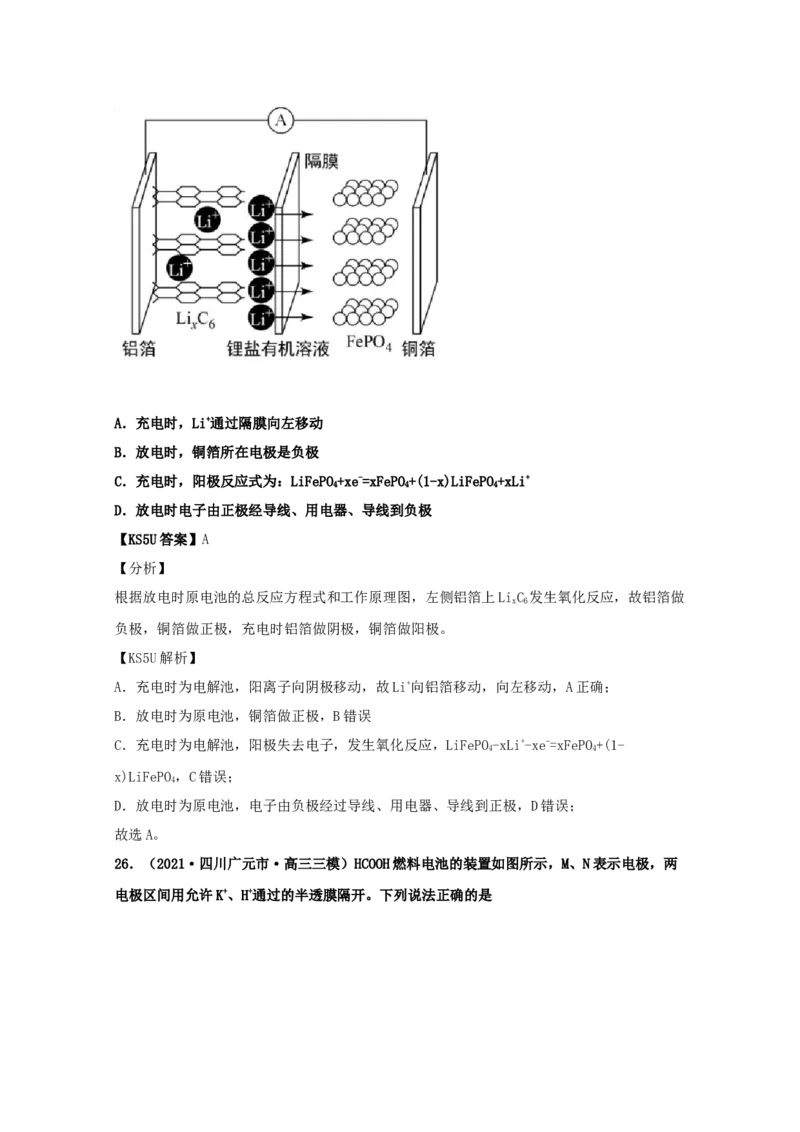
25.(2021·四川达州市·高三二模)磷酸铁锂锂离子电池是目前电动汽车动力电池的主要
材料,其特点是放电容量大,价格低廉,无毒性。放电时的反应为:xFePO+(1-x)LiFePO+
4 4
LiC= C+LiFePO。放电时工作原理如图所示。下列叙述正确的是
x 6 6 4A.充电时,Li+通过隔膜向左移动
B.放电时,铜箔所在电极是负极
C.充电时,阳极反应式为:LiFePO+xe-=xFePO+(1-x)LiFePO+xLi+
4 4 4
D.放电时电子由正极经导线、用电器、导线到负极
【KS5U答案】A
【分析】
根据放电时原电池的总反应方程式和工作原理图,左侧铝箔上LiC 发生氧化反应,故铝箔做
x 6
负极,铜箔做正极,充电时铝箔做阴极,铜箔做阳极。
【KS5U解析】
A.充电时为电解池,阳离子向阴极移动,故Li+向铝箔移动,向左移动,A正确;
B.放电时为原电池,铜箔做正极,B错误
C.充电时为电解池,阳极失去电子,发生氧化反应,LiFePO-xLi+-xe-=xFePO+(1-
4 4
x)LiFePO,C错误;
4
D.放电时为原电池,电子由负极经过导线、用电器、导线到正极,D错误;
故选A。
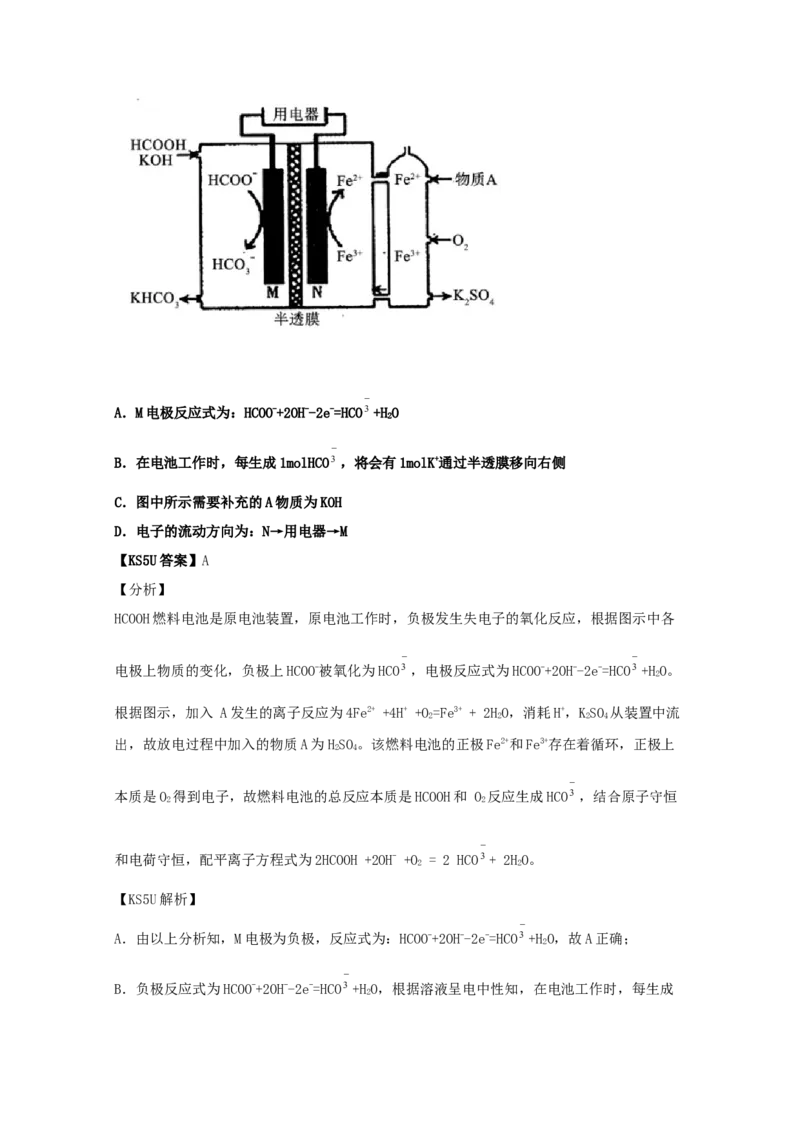
26.(2021·四川广元市·高三三模)HCOOH燃料电池的装置如图所示,M、N表示电极,两
电极区间用允许K+、H+通过的半透膜隔开。下列说法正确的是
A.M电极反应式为:HCOO-+2OH--2e-=HCO3 +HO
2
B.在电池工作时,每生成1molHCO3 ,将会有1molK+通过半透膜移向右侧
C.图中所示需要补充的A物质为KOH
D.电子的流动方向为:N→用电器→M
【KS5U答案】A
【分析】
HCOOH燃料电池是原电池装置,原电池工作时,负极发生失电子的氧化反应,根据图示中各
电极上物质的变化,负极上HCOO-被氧化为HCO3 ,电极反应式为HCOO-+2OH--2e-=HCO3 +HO。
2
根据图示,加入 A发生的离子反应为4Fe2+ +4H+ +O=Fe3+ + 2HO,消耗H+,KSO 从装置中流
2 2 2 4
出,故放电过程中加入的物质A为HSO。该燃料电池的正极Fe2+和Fe3+存在着循环,正极上
2 4
本质是O 得到电子,故燃料电池的总反应本质是HCOOH和 O 反应生成HCO3 ,结合原子守恒
2 2
和电荷守恒,配平离子方程式为2HCOOH +2OH- +O = 2 HCO3 + 2HO。
2 2
【KS5U解析】
A.由以上分析知,M电极为负极,反应式为:HCOO-+2OH--2e-=HCO3 +HO,故A正确;
2
B.负极反应式为HCOO-+2OH--2e-=HCO3 +HO,根据溶液呈电中性知,在电池工作时,每生成
2
1molHCO3 ,将会有2molK+通过半透膜移向右侧,故B错误;
C.由以上分析知,图中所示需要补充的A物质为HSO,故C错误;
2 4
D.原电池中电子从负极经导线流向正极,故电子的流动方向为:M→用电器→N,故D错误;
故选A。
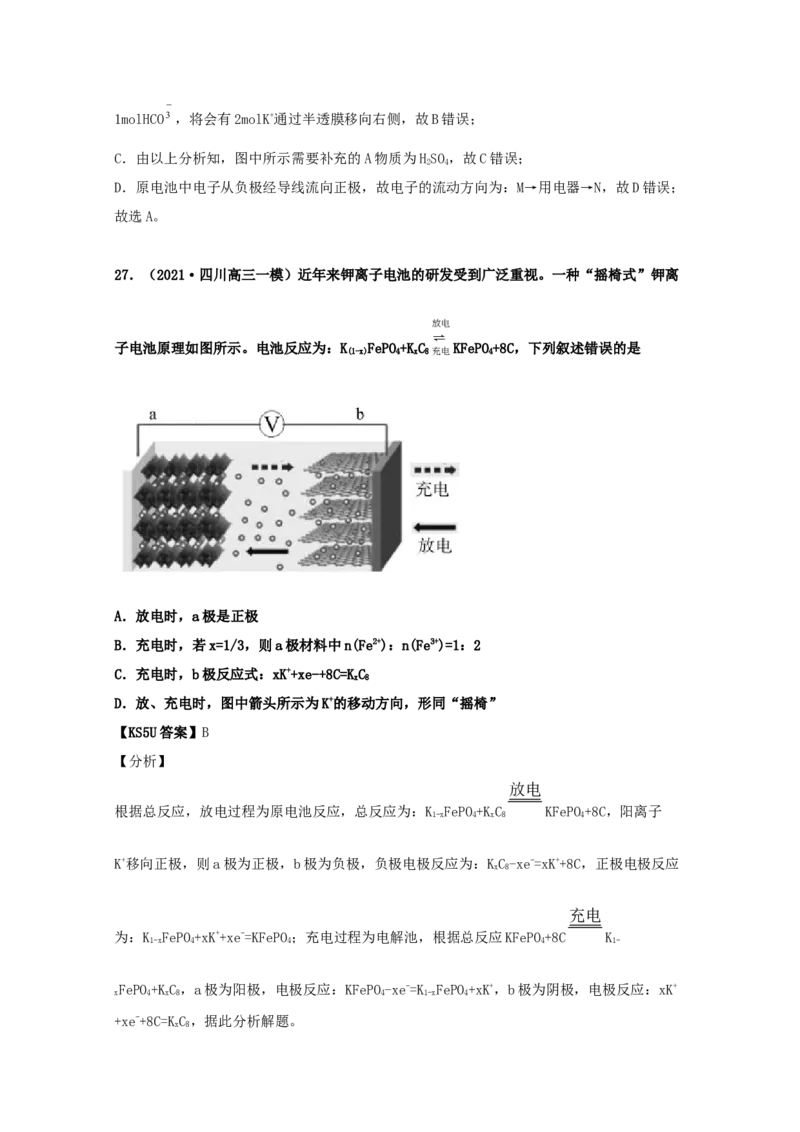
27.(2021·四川高三一模)近年来钾离子电池的研发受到广泛重视。一种“摇椅式”钾离
放电
子电池原理如图所示。电池反应为:K FePO+KC KFePO+8C,下列叙述错误的是
(1-x) 4 x 8充电 4
A.放电时,a极是正极
B.充电时,若x=1/3,则a极材料中n(Fe2+):n(Fe3+)=1:2
C.充电时,b极反应式:xK++xe-+8C=KC
x 8
D.放、充电时,图中箭头所示为K+的移动方向,形同“摇椅”
【KS5U答案】B
【分析】
放电
根据总反应,放电过程为原电池反应,总反应为:K FePO+KC KFePO+8C,阳离子
1-x 4 x 8 4
K+移向正极,则a极为正极,b极为负极,负极电极反应为:KC-xe-=xK++8C,正极电极反应
x 8
充电
为:K FePO+xK++xe-=KFePO;充电过程为电解池,根据总反应KFePO+8C K
1-x 4 4 4 1-
FePO+KC,a极为阳极,电极反应:KFePO-xe-=K FePO+xK+,b极为阴极,电极反应:xK+
x 4 x 8 4 1-x 4
+xe-+8C=KC,据此分析解题。
x 8【KS5U解析】
A.放电时为原电池反应,阳离子K+脱离负极表面进入电解质溶液中,移向正极,则a极为正
极,A正确;
1
B.充电时为电解池,若x=3,根据化合价的代数和为0,设Fe2+的物质的量为a,Fe3+的物
1
质的量为b个,则a+b=1,根据化合价的代数和为0,正化合价之和为(1-3)+2a+3a,PO3-的
4
1 2 1
负化合价为-3价,即(1-3)+2a+3a+(-3)=0,解得a=3 ,b=3,所以K FePO 中的n(Fe2+):
1-x 4
n(Fe3+)=2:1,B错误;
C.由分析得出充电时,b极反应式为:xK++xe-+8C=KC,C正确;
x 8
D.放电过程为原电池反应,阳离子K+移向正极,充电过程为电解池,阳离子K+移向阴极,则
图中箭头所示为K+的移动方向,形同“摇椅”,D正确。
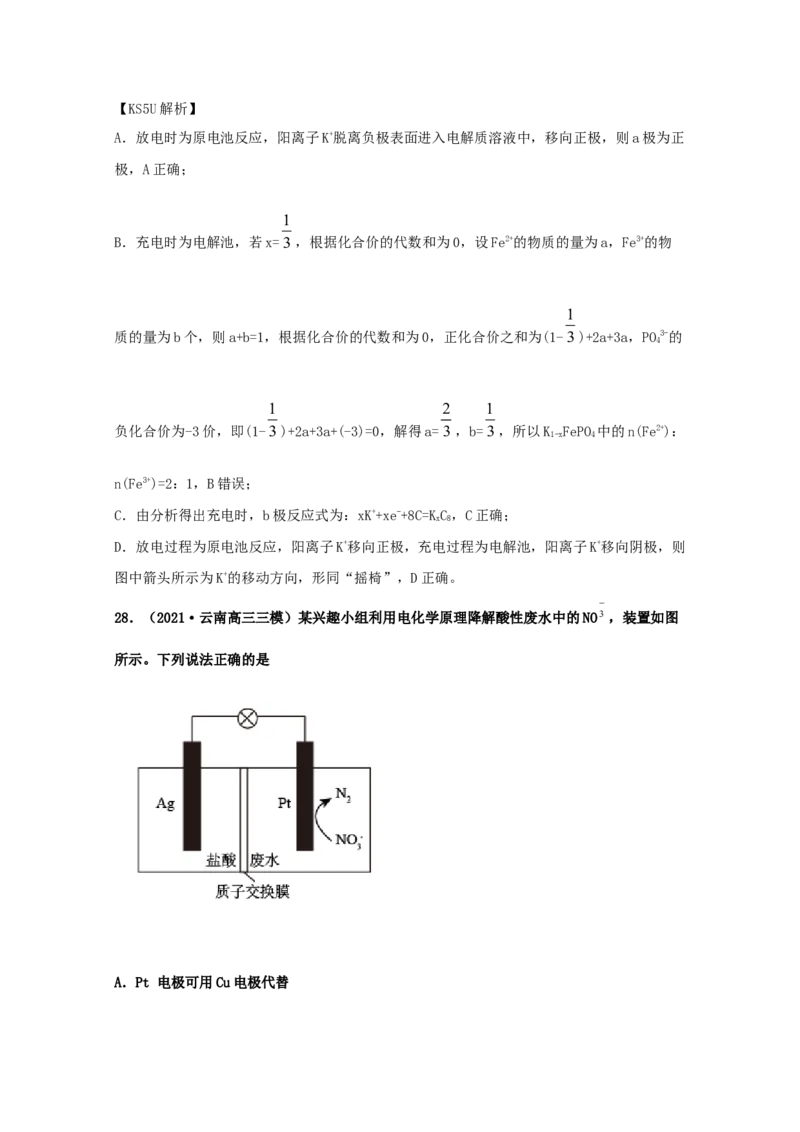
28.(2021·云南高三三模)某兴趣小组利用电化学原理降解酸性废水中的NO3 ,装置如图
所示。下列说法正确的是
A.Pt 电极可用Cu电极代替
B.负极反应式为: 2NO3 +10e- +12H+=N+6HO
2 2
C.溶液中电子通过质子交换膜由Ag电极向Pt电极移动
D.若外电路转移lmol电子,则膜两侧电解液质量共减少38.3g
【KS5U答案】D
【分析】
-
由装置示意图中可知Pt电极上NO3转化为N,发生还原反应,故Pt电极为正极,则Ag电极
2
为负极,发生的电极反应为:Cl-+Ag-e-=AgCl↓,据此分析解题。
【KS5U解析】
-
A. 由于Cu比Ag活泼,故Pt电极不可用Cu电极代替,否则Cu直接与酸性条件下的NO3反应,
不构成原电池,A错误;
B. 根据原电池中负极发生氧化反应,正极发生还原反应,故负极反应式为:Cl-+Ag-e-
=AgCl↓,而 2NO3 +10e- +12H+=N+6HO是正极反应式,B错误;
2 2
C. 由分析可知,Pt电极是正极,Ag为负极,故溶液中H+通过质子交换膜由Ag电极向Pt电
极移动,电子只能在导线上定向移动而不能通过溶液,C错误;
D. 根据电池的总反应可知,10Ag +10Cl-+12H++2NO3 =10AgCl↓+N+6HO,转移10mol电子两
2 2
极质量减少:(10×35.5+28)g,故若外电路转移lmol电子,则膜两侧电解液质量共减少
38.3g,D正确;
故答案为:D。
二、多选题
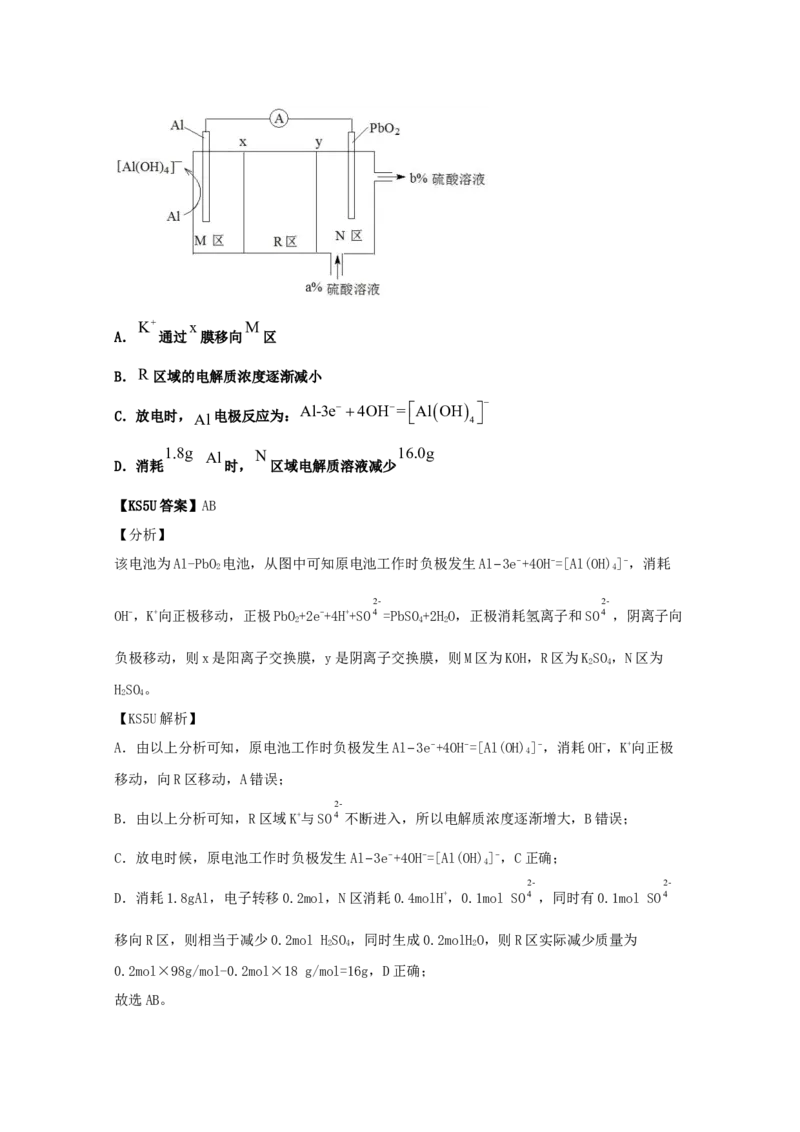
AlPbO K SO
29.(2021·全国高三零模)科学家最近发明了一种 2电池,电解质为 2 4、
H 2 SO 4、 KOH ,通过 x 和 y 两种离子交换膜将电解质溶液隔开,形成 M 、 R 、 N 三个电
a b
解质溶液区域( ),结构示意图如图所示。下列说法不正确的是K x M
A. 通过 膜移向 区
B.R 区域的电解质浓度逐渐减小
Al-3e 4OH=AlOH
C.放电时,Al电极反应为:
4
1.8g Al N 16.0g
D.消耗 时, 区域电解质溶液减少
【KS5U答案】AB
【分析】
该电池为Al-PbO 电池,从图中可知原电池工作时负极发生Al−3e−+4OH−=[Al(OH)]−,消耗
2 4
2- 2-
OH-,K+向正极移动,正极PbO+2e-+4H++SO4 =PbSO+2HO,正极消耗氢离子和SO4 ,阴离子向
2 4 2
负极移动,则x是阳离子交换膜,y是阴离子交换膜,则M区为KOH,R区为KSO,N区为
2 4
HSO。
2 4
【KS5U解析】
A.由以上分析可知,原电池工作时负极发生Al−3e−+4OH−=[Al(OH)]−,消耗OH-,K+向正极
4
移动,向R区移动,A错误;
2-
B.由以上分析可知,R区域K+与SO4 不断进入,所以电解质浓度逐渐增大,B错误;
C.放电时候,原电池工作时负极发生Al−3e−+4OH−=[Al(OH)]−,C正确;
4
2- 2-
D.消耗1.8gAl,电子转移0.2mol,N区消耗0.4molH+,0.1mol SO4 ,同时有0.1mol SO4
移向R区,则相当于减少0.2mol HSO,同时生成0.2molHO,则R区实际减少质量为
2 4 2
0.2mol×98g/mol-0.2mol×18 g/mol=16g,D正确;
故选AB。三、工业流程题
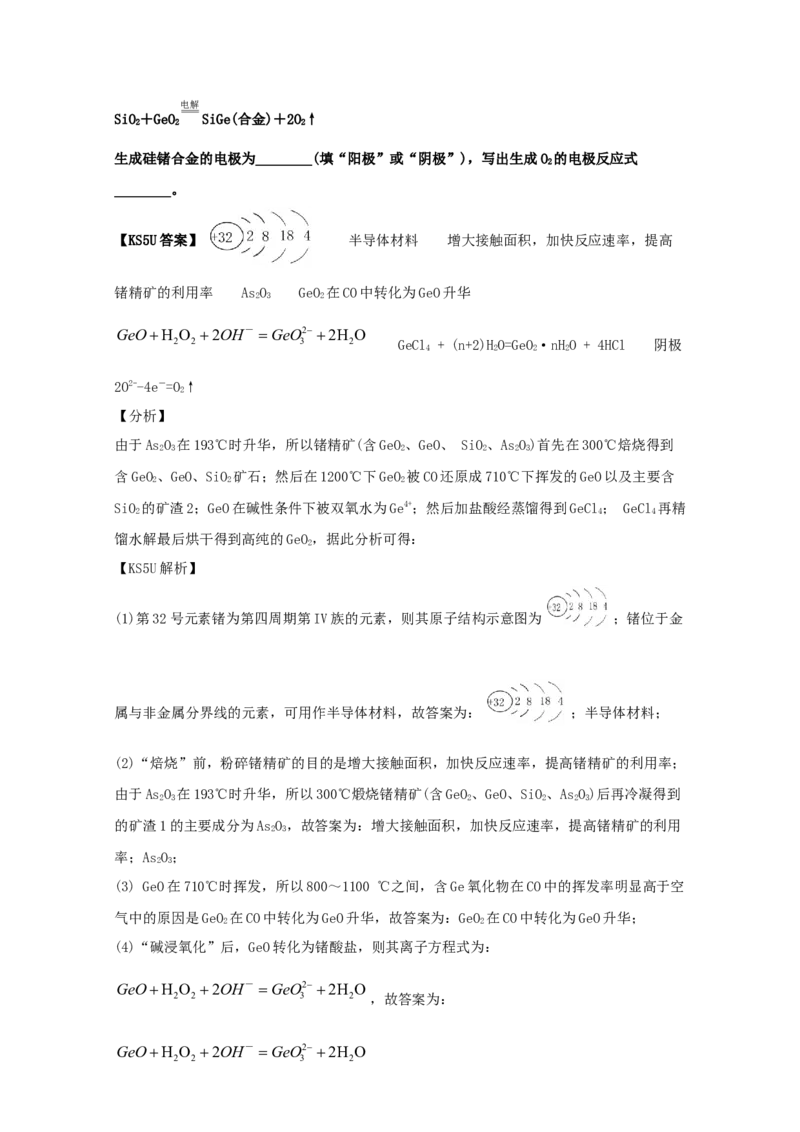
30.(2021·重庆市第十一中学校高三二模)锗属于稀有分散元素,一种以锗精矿(含GeO、
2
GeO、SiO、AsO)制备高纯二氧化锗的工艺流程如下:
2 2 3
下列数据是对应物质的熔点:
物质 GeO GeO SiO AsO
2 2 2 3
熔点/℃ 1115 710(升华) 1723 193(升华)
(1)第32号元素锗的原子结构示意图________,根据锗在元素周期表中的位置写出单质锗的
一种用途________。
(2)“焙烧”前,粉碎锗精矿的目的是________。矿渣1的主要成分是________。
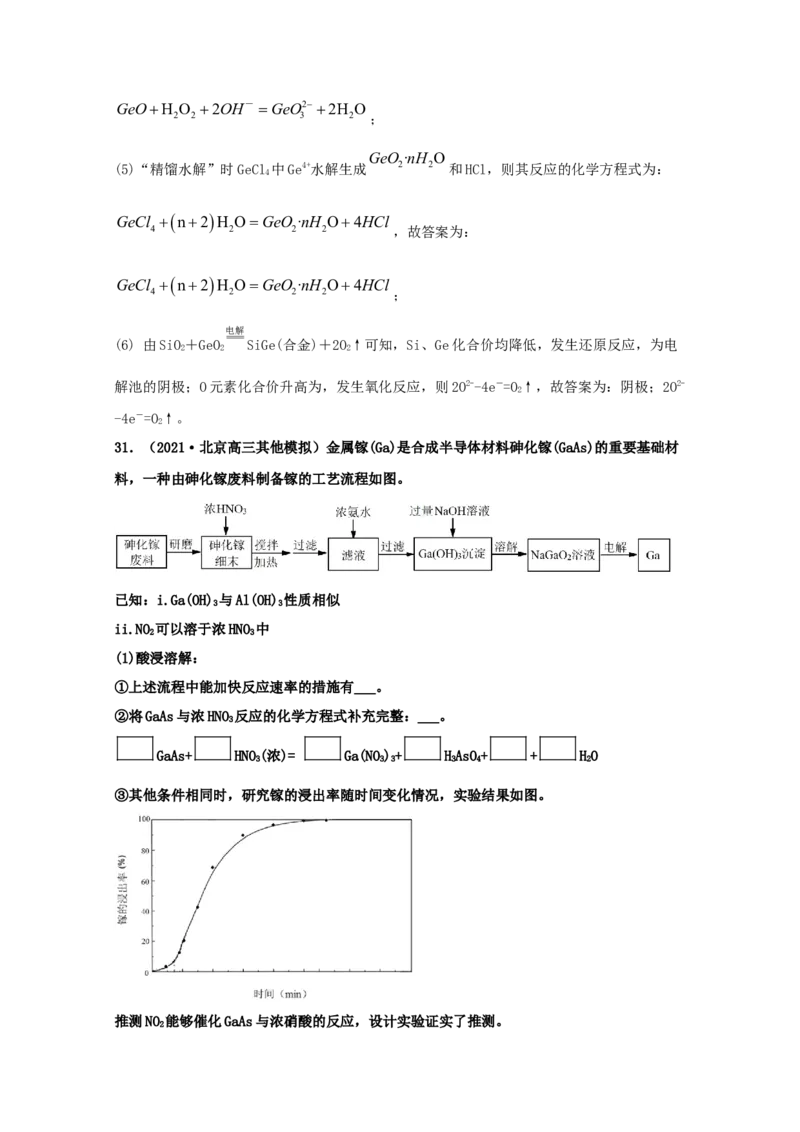
(3)“还原焙烧”中,含Ge氧化物在不同气氛中的挥发情况如图。800~1100℃之间,含Ge
氧化物在CO中的挥发率明显高于空气中的原因是________。
(4)“碱浸氧化”后,GeO转化为锗酸盐,请写出反应的离子方程式________。
(5)“精馏水解”发生反应的化学方程式________。
(6)在氯化物熔盐中,电解SiO 和GeO 的混合物,可制得硅锗合金。反应原理如下:
2 2电解
SiO+GeO SiGe(合金)+2O↑
2 2 2
生成硅锗合金的电极为________(填“阳极”或“阴极”),写出生成O 的电极反应式
2
________。
【KS5U答案】 半导体材料 增大接触面积,加快反应速率,提高
锗精矿的利用率 AsO GeO 在CO中转化为GeO升华
2 3 2
GeOH O 2OH- GeO2 2H O
2 2 3 2 GeCl + (n+2)HO=GeO·nHO + 4HCl 阴极
4 2 2 2
2O2--4e-=O↑
2
【分析】
由于AsO 在193℃时升华,所以锗精矿(含GeO、GeO、 SiO、AsO)首先在300℃焙烧得到
2 3 2 2 2 3
含GeO、GeO、SiO 矿石;然后在1200℃下GeO 被CO还原成710℃下挥发的GeO以及主要含
2 2 2
SiO 的矿渣2;GeO在碱性条件下被双氧水为Ge4+;然后加盐酸经蒸馏得到GeCl; GeCl 再精
2 4 4
馏水解最后烘干得到高纯的GeO,据此分析可得:
2
【KS5U解析】
(1)第32号元素锗为第四周期第IV族的元素,则其原子结构示意图为 ;锗位于金
属与非金属分界线的元素,可用作半导体材料,故答案为: ;半导体材料;
(2)“焙烧”前,粉碎锗精矿的目的是增大接触面积,加快反应速率,提高锗精矿的利用率;
由于AsO 在193℃时升华,所以300℃煅烧锗精矿(含GeO、GeO、SiO、AsO)后再冷凝得到
2 3 2 2 2 3
的矿渣1的主要成分为AsO,故答案为:增大接触面积,加快反应速率,提高锗精矿的利用
2 3
率;AsO;
2 3
(3) GeO在710℃时挥发,所以800~1100 ℃之间,含Ge氧化物在CO中的挥发率明显高于空
气中的原因是GeO 在CO中转化为GeO升华,故答案为:GeO 在CO中转化为GeO升华;
2 2
(4)“碱浸氧化”后,GeO转化为锗酸盐,则其离子方程式为:
GeOH O 2OH- GeO2 2H O
2 2 3 2 ,故答案为:
GeOH O 2OH- GeO2 2H O
2 2 3 2GeOH O 2OH- GeO2 2H O
2 2 3 2 ;
GeO ·nH O
(5)“精馏水解”时GeCl 中Ge4+水解生成 2 2 和HCl,则其反应的化学方程式为:
4
GeCl n2H OGeO ·nH O4HCl
4 2 2 2 ,故答案为:
GeCl n2H OGeO ·nH O4HCl
4 2 2 2 ;
电解
(6) 由SiO+GeO SiGe(合金)+2O↑可知,Si、Ge化合价均降低,发生还原反应,为电
2 2 2
解池的阴极;O元素化合价升高为,发生氧化反应,则2O2--4e-=O↑,故答案为:阴极;2O2-
2
-4e-=O↑。
2
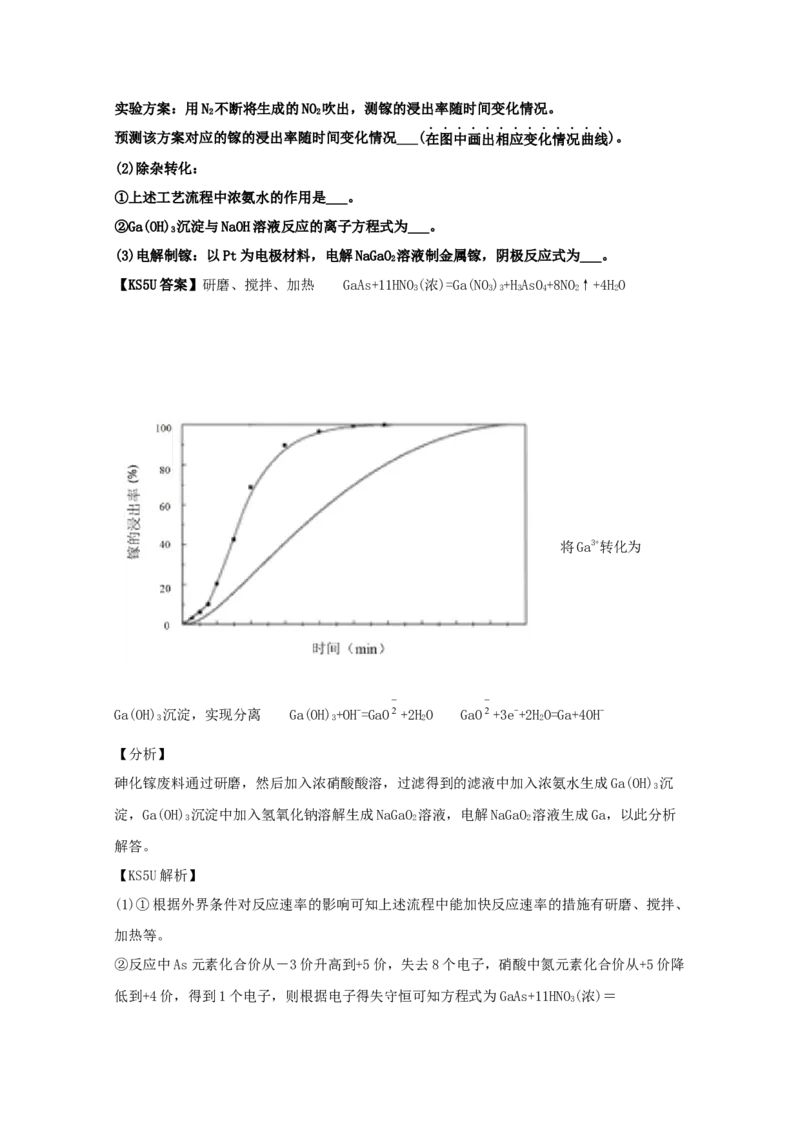
31.(2021·北京高三其他模拟)金属镓(Ga)是合成半导体材料砷化镓(GaAs)的重要基础材
料,一种由砷化镓废料制备镓的工艺流程如图。
已知:i.Ga(OH) 与Al(OH) 性质相似
3 3
ii.NO 可以溶于浓HNO 中
2 3
(1)酸浸溶解:
①上述流程中能加快反应速率的措施有___。
②将GaAs与浓HNO 反应的化学方程式补充完整:___。
3
GaAs+ HNO(浓)= Ga(NO)+ HAsO+ + HO
3 3 3 3 4 2
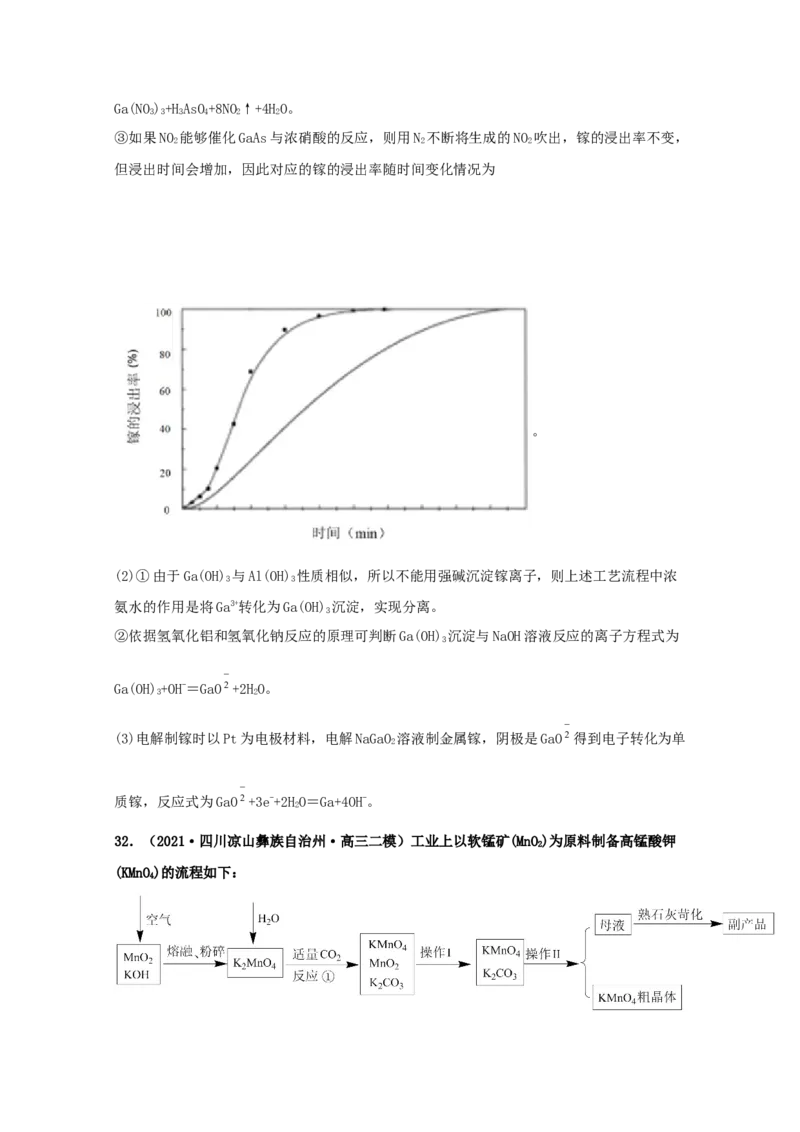
③其他条件相同时,研究镓的浸出率随时间变化情况,实验结果如图。
推测NO 能够催化GaAs与浓硝酸的反应,设计实验证实了推测。
2实验方案:用N 不断将生成的NO 吹出,测镓的浸出率随时间变化情况。
2 2
预测该方案对应的镓的浸出率随时间变化情况___(在图中画出相应变化情况曲线)。
(2)除杂转化:
①上述工艺流程中浓氨水的作用是___。
②Ga(OH) 沉淀与NaOH溶液反应的离子方程式为___。
3
(3)电解制镓:以Pt为电极材料,电解NaGaO 溶液制金属镓,阴极反应式为___。
2
【KS5U答案】研磨、搅拌、加热 GaAs+11HNO(浓)=Ga(NO)+HAsO+8NO↑+4HO
3 3 3 3 4 2 2
将Ga3+转化为
Ga(OH) 沉淀,实现分离 Ga(OH)+OH-=GaO2+2HO GaO2+3e-+2HO=Ga+4OH-
3 3 2 2
【分析】
砷化镓废料通过研磨,然后加入浓硝酸酸溶,过滤得到的滤液中加入浓氨水生成Ga(OH) 沉
3
淀,Ga(OH) 沉淀中加入氢氧化钠溶解生成NaGaO 溶液,电解NaGaO 溶液生成Ga,以此分析
3 2 2
解答。
【KS5U解析】
(1)①根据外界条件对反应速率的影响可知上述流程中能加快反应速率的措施有研磨、搅拌、
加热等。
②反应中As元素化合价从-3价升高到+5价,失去8个电子,硝酸中氮元素化合价从+5价降
低到+4价,得到1个电子,则根据电子得失守恒可知方程式为GaAs+11HNO(浓)=
3Ga(NO)+HAsO+8NO↑+4HO。
3 3 3 4 2 2
③如果NO 能够催化GaAs与浓硝酸的反应,则用N 不断将生成的NO 吹出,镓的浸出率不变,
2 2 2
但浸出时间会增加,因此对应的镓的浸出率随时间变化情况为
。
(2)①由于Ga(OH) 与Al(OH) 性质相似,所以不能用强碱沉淀镓离子,则上述工艺流程中浓
3 3
氨水的作用是将Ga3+转化为Ga(OH) 沉淀,实现分离。
3
②依据氢氧化铝和氢氧化钠反应的原理可判断Ga(OH) 沉淀与NaOH溶液反应的离子方程式为
3
Ga(OH)+OH-=GaO2+2HO。
3 2
(3)电解制镓时以Pt为电极材料,电解NaGaO 溶液制金属镓,阴极是GaO2得到电子转化为单
2
质镓,反应式为GaO2+3e-+2HO=Ga+4OH-。
2
32.(2021·四川凉山彝族自治州·高三二模)工业上以软锰矿(MnO)为原料制备高锰酸钾
2
(KMnO)的流程如下:
4回答下列问题:
(1)写出MnO、KOH与空气共熔发生反应的化学方程式_______。
2
(2)反应①中氧化产物与还原产物的物质的量之比为_______。假设无其他副反应发生,该步
反应KMnO 的最大理论转化率为_______%(保留一位小数)。
2 4
(3)操作I为_______。
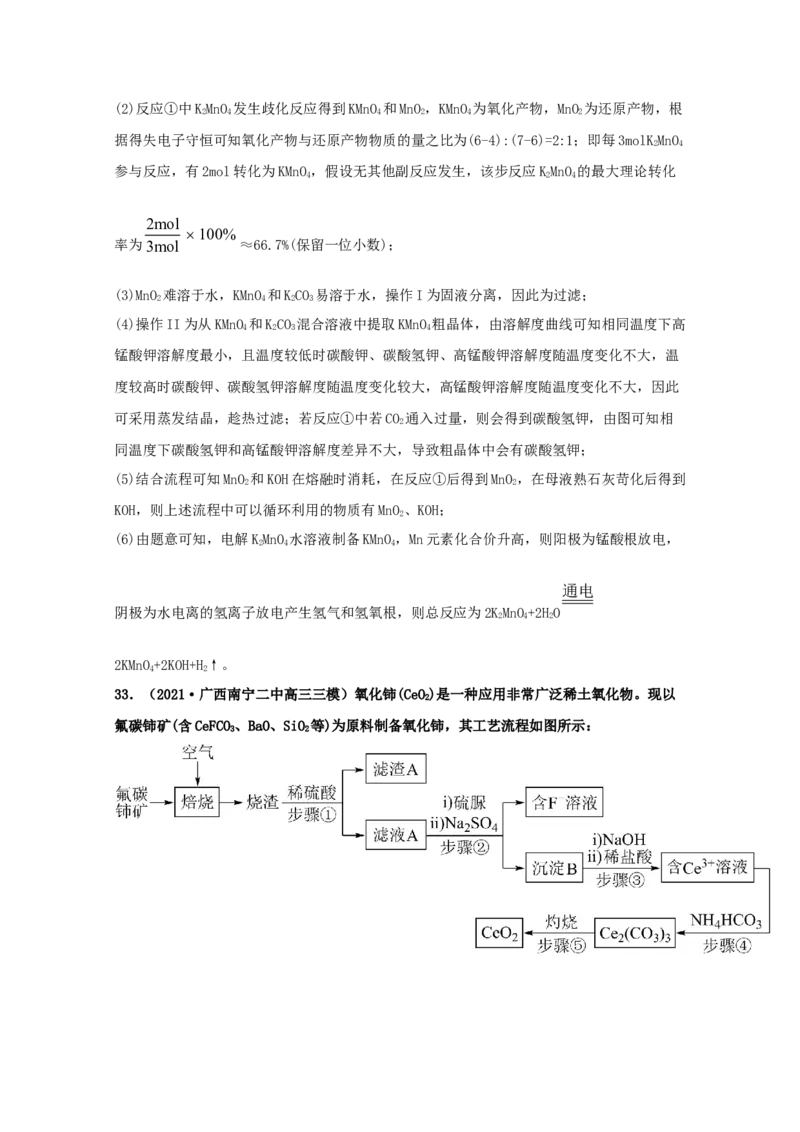
(4)已知有关物质在不同温度(单位:℃)下的溶解度(单位:g/100g水中)如下图:
据图推断操作II最好采用____。反应①中若CO 通入过量造成的影响是____。
2
(5)上述流程中可以循环利用的物质有_______。
(6)由于直接歧化制备高锰酸钾的产率不高,且后续分离纯化步骤较多,目前工业上较多采
用电解KMnO 水溶液法制备,试写出该电解过程总反应的化学方程式_______。
2 4
熔融
【KS5U答案】2MnO+4KOH+O 2KMnO+2HO 2:1 66.7 过滤 蒸发结晶,趁热
2 2 2 4 2
通电
过滤 粗晶体中会有碳酸氢钾 MnO、KOH 2KMnO+2HO 2KMnO+2KOH+H↑
2 2 4 2 4 2
【分析】
二氧化锰、KOH在空气中熔融制得锰酸钾,加水、通入适量二氧化碳,锰酸钾发生歧化反应
得到高锰酸钾、二氧化锰、碳酸钾,过滤除去二氧化锰,得到高锰酸钾、碳酸钾混合溶液,
再经蒸发结晶,趁热过滤等得到高锰酸钾粗品。
【KS5U解析】
(1)由流程可知MnO、KOH与空气共熔得到锰酸钾,结合原子守恒可知产物还有水和,发生反
2
熔融
应的化学方程式为2MnO+4KOH+O 2KMnO+2HO;
2 2 2 4 2(2)反应①中KMnO 发生歧化反应得到KMnO 和MnO,KMnO 为氧化产物,MnO 为还原产物,根
2 4 4 2 4 2
据得失电子守恒可知氧化产物与还原产物物质的量之比为(6-4):(7-6)=2:1;即每3molKMnO
2 4
参与反应,有2mol转化为KMnO,假设无其他副反应发生,该步反应KMnO 的最大理论转化
4 2 4
2mol
100%
率为3mol ≈66.7%(保留一位小数);
(3)MnO 难溶于水,KMnO 和KCO 易溶于水,操作I为固液分离,因此为过滤;
2 4 2 3
(4)操作II为从KMnO 和KCO 混合溶液中提取KMnO 粗晶体,由溶解度曲线可知相同温度下高
4 2 3 4
锰酸钾溶解度最小,且温度较低时碳酸钾、碳酸氢钾、高锰酸钾溶解度随温度变化不大,温
度较高时碳酸钾、碳酸氢钾溶解度随温度变化较大,高锰酸钾溶解度随温度变化不大,因此
可采用蒸发结晶,趁热过滤;若反应①中若CO 通入过量,则会得到碳酸氢钾,由图可知相
2
同温度下碳酸氢钾和高锰酸钾溶解度差异不大,导致粗晶体中会有碳酸氢钾;
(5)结合流程可知MnO 和KOH在熔融时消耗,在反应①后得到MnO,在母液熟石灰苛化后得到
2 2
KOH,则上述流程中可以循环利用的物质有MnO、KOH;
2
(6)由题意可知,电解KMnO 水溶液制备KMnO,Mn元素化合价升高,则阳极为锰酸根放电,
2 4 4
通电
阴极为水电离的氢离子放电产生氢气和氢氧根,则总反应为2KMnO+2HO
2 4 2
2KMnO+2KOH+H↑。
4 2
33.(2021·广西南宁二中高三三模)氧化铈(CeO)是一种应用非常广泛稀土氧化物。现以
2
氟碳铈矿(含CeFCO、BaO、SiO 等)为原料制备氧化铈,其工艺流程如图所示:
3 22-
已知:①Ce3+易和SO4 形成复盐沉淀:Ce(SO)+NaSO+nHO=Ce(SO)·NaSO·nHO↓(复盐
2 4 3 2 4 2 2 4 3 2 4 2
沉淀);
②硫脲:(分子式为SCNH),具有还原性,酸性条件下易被氧化为(SCNH);
2 4 2 3 2
③Ce3+在空气中易被氧化为Ce4+;
回答下列问题:
(1)焙烧时,为了提高焙烧效率,可采取的措施有_______(任写一条)。
(2)滤渣A的主要成分是_______、_______。
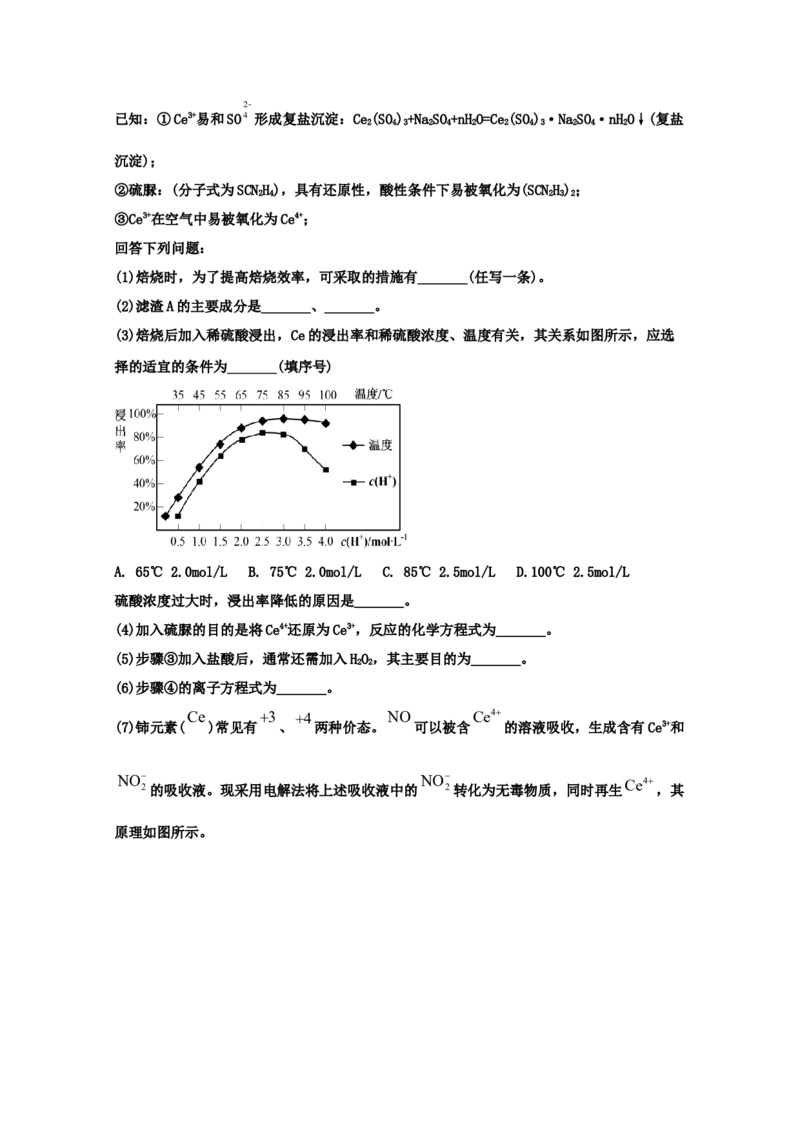
(3)焙烧后加入稀硫酸浸出,Ce的浸出率和稀硫酸浓度、温度有关,其关系如图所示,应选
择的适宜的条件为_______(填序号)
A. 65℃ 2.0mol/L B. 75℃ 2.0mol/L C. 85℃ 2.5mol/L D.100℃ 2.5mol/L
硫酸浓度过大时,浸出率降低的原因是_______。
(4)加入硫脲的目的是将Ce4+还原为Ce3+,反应的化学方程式为_______。
(5)步骤③加入盐酸后,通常还需加入HO,其主要目的为_______。
2 2
(6)步骤④的离子方程式为_______。
Ce 3 4 NO Ce4
(7)铈元素( )常见有 、 两种价态。 可以被含 的溶液吸收,生成含有Ce3+和
NO NO
Ce4
2的吸收液。现采用电解法将上述吸收液中的 2转化为无毒物质,同时再生 ,其
原理如图所示。Ce4
① 从电解槽的_______(填字母代号)口流出。
②写出阴极的电极反应式:_______。
【KS5U答案】粉碎氟碳铈矿以增大接触面积或延长焙烧时间 BaSO SiO C 硫
4 2
2
酸浓度过大时,溶液中c(SO4 )增大,易和稀土离子形成复盐沉淀而使浸出率降低
2Ce(SO)+2SCNH=Ce(SO)+(SCNH)+HSO 防止Ce3+被氧化 2Ce3++6HCO3
4 2 2 4 2 4 3 2 3 2 2 4
2NO 8H 6e=N 4H O
=Ce(CO)↓+3CO↑+3HO a 2 2 2
2 3 3 2 2
【分析】
氟碳铈矿含CeFCO、BaO、SiO 等,在空气中焙烧,Ce3+在空气中氧化为Ce4+,用硫酸浸取,
3 2
Ce4+进入溶液,SiO 不反应,BaO与硫酸反应生成BaSO 沉淀,过滤分离,滤渣A为SiO、
2 4 2
BaSO。滤液A中加入硫脲将Ce4+还原为Ce3+,Ce(SO) 与NaSO 形成复盐沉淀
4 2 4 3 2 4
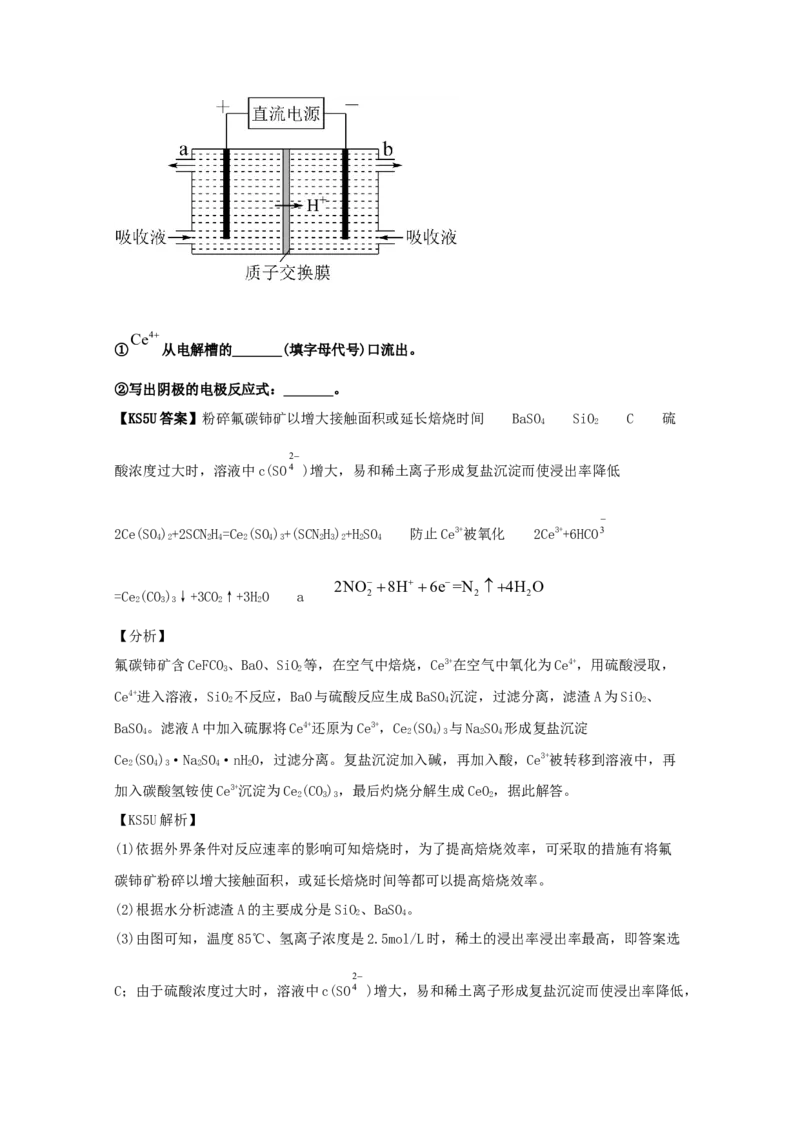
Ce(SO)·NaSO·nHO,过滤分离。复盐沉淀加入碱,再加入酸,Ce3+被转移到溶液中,再
2 4 3 2 4 2
加入碳酸氢铵使Ce3+沉淀为Ce(CO),最后灼烧分解生成CeO,据此解答。
2 3 3 2
【KS5U解析】
(1)依据外界条件对反应速率的影响可知焙烧时,为了提高焙烧效率,可采取的措施有将氟
碳铈矿粉碎以增大接触面积,或延长焙烧时间等都可以提高焙烧效率。
(2)根据水分析滤渣A的主要成分是SiO、BaSO。
2 4
(3)由图可知,温度85℃、氢离子浓度是2.5mol/L时,稀土的浸出率浸出率最高,即答案选
2
C;由于硫酸浓度过大时,溶液中c(SO4 )增大,易和稀土离子形成复盐沉淀而使浸出率降低,所以硫酸浓度过大时,浸出率降低。
(4)加入硫脲的目的是将Ce4+还原为Ce3+,该反应的化学方程式为
2Ce(SO)+2SCNH=Ce(SO)+(SCNH)+HSO。
4 2 2 4 2 4 3 2 3 2 2 4
(5)Ce3+在空气中易被氧化为Ce4+,过氧化氢具有还原性,步骤③加入盐酸后,通常还需加入
HO,其主要目的为了防止Ce3+被氧化。
2 2
(6)步骤④是碳酸氢铵提供碳酸根与Ce3+结合生成为(Ce(CO),产生的氢离子又与碳酸氢根
2 3 3
反应生成二氧化碳与水,反应离子方程式为2Ce3++6HCO3 =Ce(CO)↓+3CO↑+3HO。
2 3 3 2 2
Ce4
(7)①Ce3+转化为 相应失去电子,即在阳极放电,所以从电解槽的a口流出。
NO
②阴极是 2得到电子转化为无毒物质氮气,电极反应式为
2NO 8H 6e=N 4H O
2 2 2 。
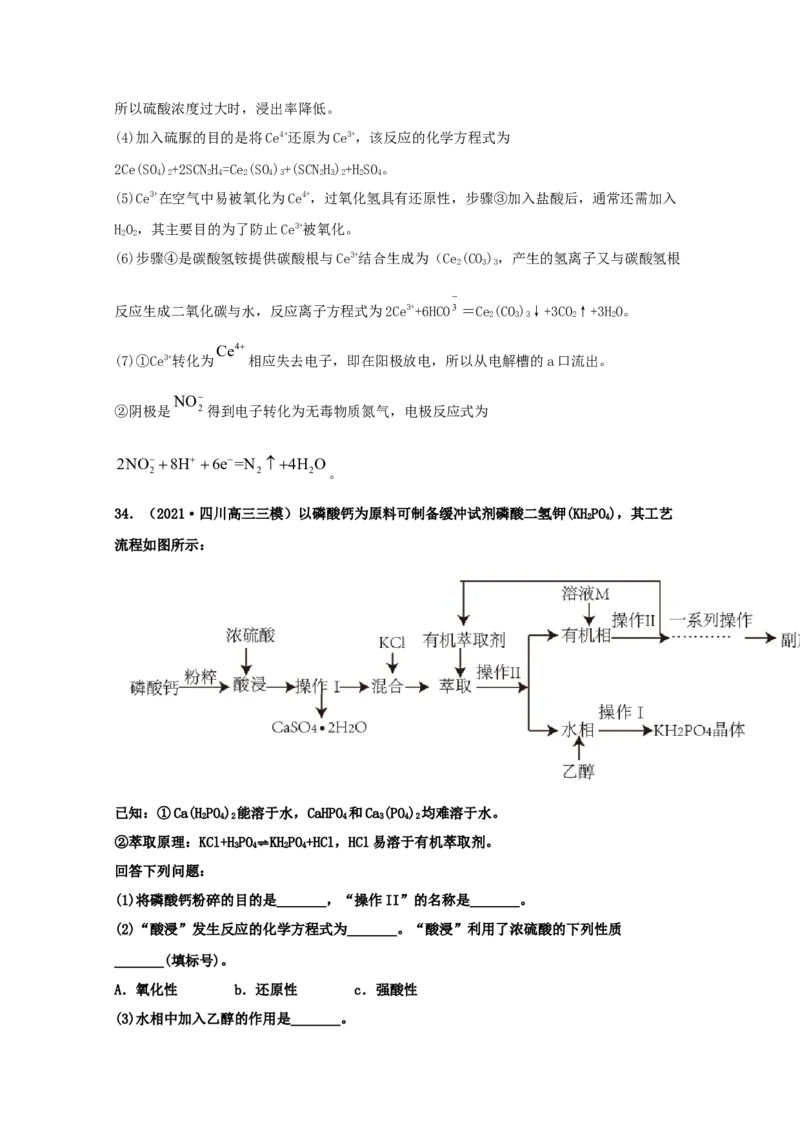
34.(2021·四川高三三模)以磷酸钙为原料可制备缓冲试剂磷酸二氢钾(KHPO),其工艺
2 4
流程如图所示:
已知:①Ca(HPO) 能溶于水,CaHPO 和Ca(PO) 均难溶于水。
2 4 2 4 3 4 2
②萃取原理:KCl+HPO KHPO+HCl,HCl易溶于有机萃取剂。
3 4 2 4
回答下列问题:
(1)将磷酸钙粉碎的目的是_______,“操作II”的名称是_______。
(2)“酸浸”发生反应的化学方程式为_______。“酸浸”利用了浓硫酸的下列性质
_______(填标号)。
A.氧化性 b.还原性 c.强酸性
(3)水相中加入乙醇的作用是_______。(4)副产品N作肥料可使作物枝繁叶茂,提高产量,则溶液M是_______(填名称)。
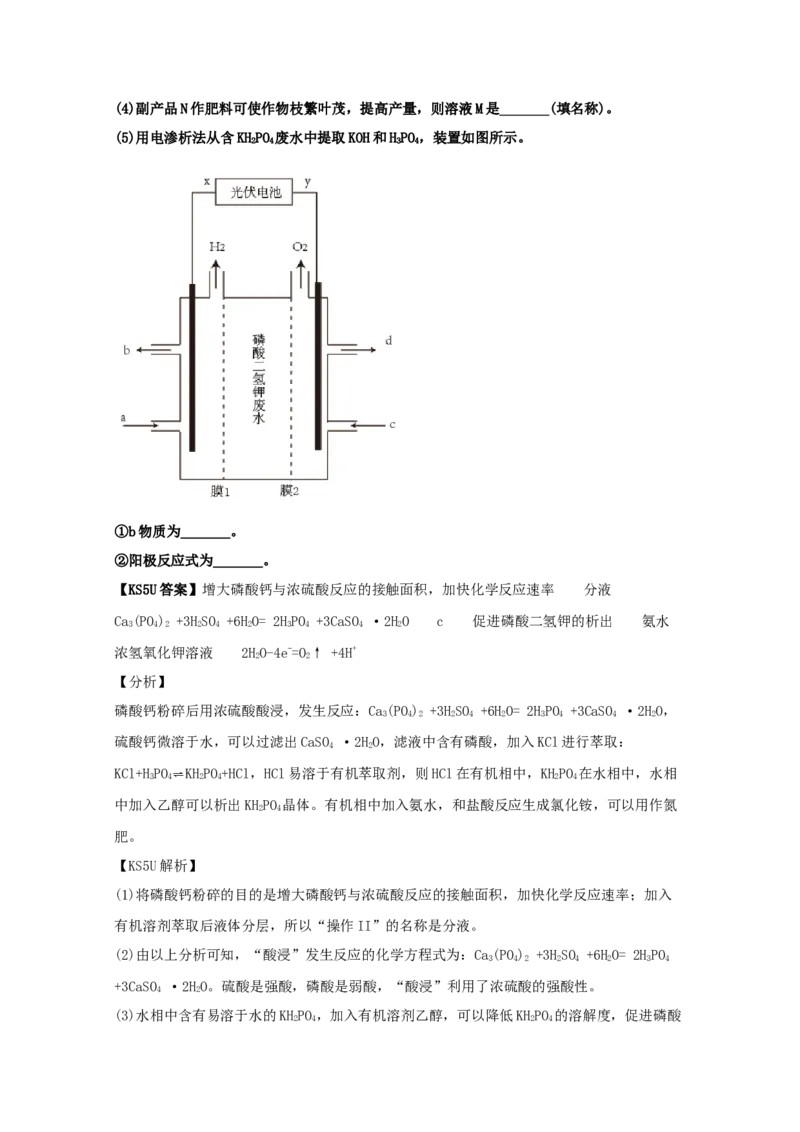
(5)用电渗析法从含KHPO 废水中提取KOH和HPO,装置如图所示。
2 4 3 4
①b物质为_______。
②阳极反应式为_______。
【KS5U答案】增大磷酸钙与浓硫酸反应的接触面积,加快化学反应速率 分液
Ca(PO) +3HSO +6HO= 2HPO +3CaSO ·2HO c 促进磷酸二氢钾的析出 氨水
3 4 2 2 4 2 3 4 4 2
浓氢氧化钾溶液 2HO-4e-=O↑ +4H+
2 2
【分析】
磷酸钙粉碎后用浓硫酸酸浸,发生反应:Ca(PO) +3HSO +6HO= 2HPO +3CaSO ·2HO,
3 4 2 2 4 2 3 4 4 2
硫酸钙微溶于水,可以过滤出CaSO ·2HO,滤液中含有磷酸,加入KCl进行萃取:
4 2
KCl+HPO KHPO+HCl,HCl易溶于有机萃取剂,则HCl在有机相中,KHPO 在水相中,水相
3 4 2 4 2 4
中加入乙醇可以析出KHPO 晶体。有机相中加入氨水,和盐酸反应生成氯化铵,可以用作氮
2 4
肥。
【KS5U解析】
(1)将磷酸钙粉碎的目的是增大磷酸钙与浓硫酸反应的接触面积,加快化学反应速率;加入
有机溶剂萃取后液体分层,所以“操作II”的名称是分液。
(2)由以上分析可知,“酸浸”发生反应的化学方程式为:Ca(PO) +3HSO +6HO= 2HPO
3 4 2 2 4 2 3 4
+3CaSO ·2HO。硫酸是强酸,磷酸是弱酸,“酸浸”利用了浓硫酸的强酸性。
4 2
(3)水相中含有易溶于水的KHPO,加入有机溶剂乙醇,可以降低KHPO 的溶解度,促进磷酸
2 4 2 4二氢钾的析出。
(4)氮肥可以使作物枝繁叶茂,在有机相中有HCl,所以加入的溶液M是氨水,和盐酸反应生
成氯化铵,可以做氮肥。
(5)用电渗析法从含KHPO 废水中提取KOH和HPO,装置如图所示。x为阴极,溶液中水电离
2 4 3 4
出来的H+得到电子生成氢气,同时促进水电离产生更多的OH-,为了增强溶液的导电性,同时
不引入新杂质,加入的a为稀KOH溶液,从b口流出的是浓KOH溶液。y为阳极,溶液中的水
电离出来的OH-失去电子生成氧气,电极反应式为:2HO-4e-=O↑ +4H+。
2 2
四、原理综合题
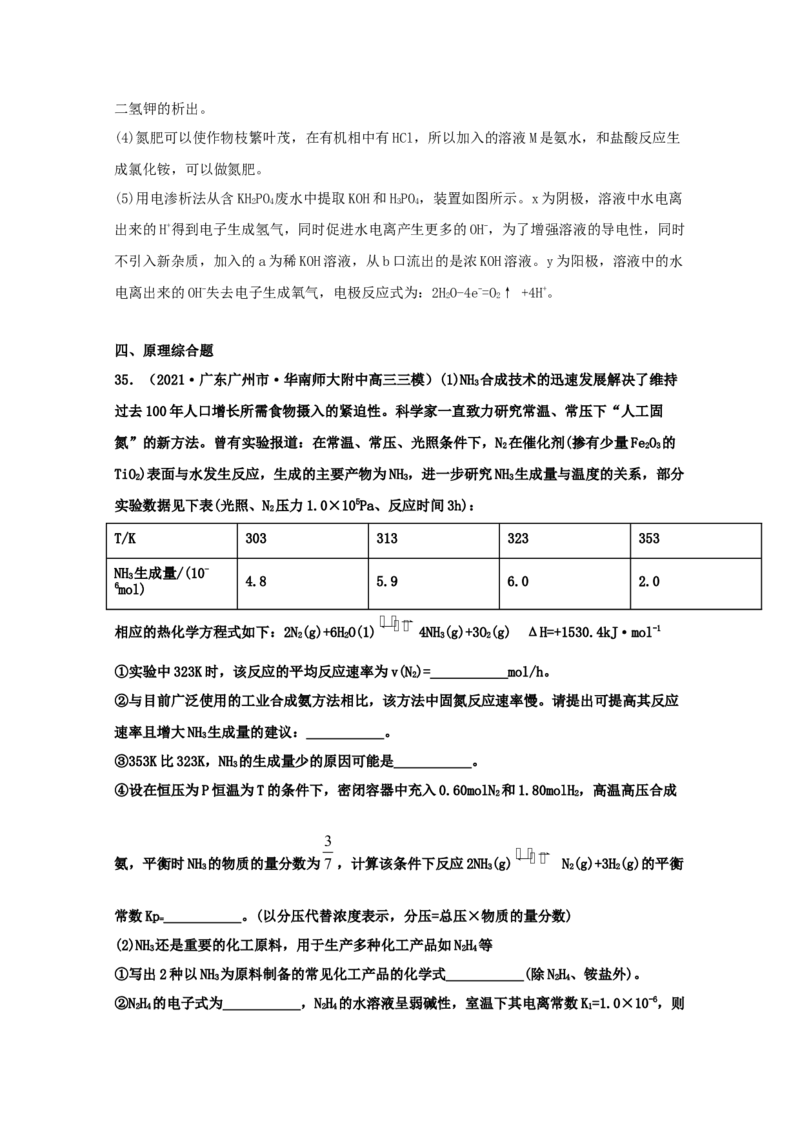
35.(2021·广东广州市·华南师大附中高三三模)(1)NH 合成技术的迅速发展解决了维持
3
过去100年人口增长所需食物摄入的紧迫性。科学家一直致力研究常温、常压下“人工固
氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N 在催化剂(掺有少量FeO 的
2 2 3
TiO)表面与水发生反应,生成的主要产物为NH,进一步研究NH 生成量与温度的关系,部分
2 3 3
实验数据见下表(光照、N 压力1.0×105Pa、反应时间3h):
2
T/K 303 313 323 353
NH 生成量/(10-
3 4.8 5.9 6.0 2.0
6mol)
相应的热化学方程式如下:2N(g)+6HO(1)
4NH(g)+3O(g) ΔH=+1530.4kJ·mol-1
2 2 3 2
①实验中323K时,该反应的平均反应速率为v(N)=___________mol/h。
2
②与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢。请提出可提高其反应
速率且增大NH 生成量的建议:___________。
3
③353K比323K,NH 的生成量少的原因可能是___________。
3
④设在恒压为P恒温为T的条件下,密闭容器中充入0.60molN 和1.80molH,高温高压合成
2 2
3
氨,平衡时NH 的物质的量分数为7 ,计算该条件下反应2NH(g)
N(g)+3H(g)的平衡
3 3 2 2
常数Kp___________。(以分压代替浓度表示,分压=总压×物质的量分数)
=
(2)NH 还是重要的化工原料,用于生产多种化工产品如NH 等
3 2 4
①写出2种以NH 为原料制备的常见化工产品的化学式___________(除NH、铵盐外)。
3 2 4
②NH 的电子式为___________,NH 的水溶液呈弱碱性,室温下其电离常数K=1.0×10-6,则
2 4 2 4 10.01mol·L-1NH 水溶液的pH=___________(忽略NH 的二级电离和HO的电离)。
2 4 2 4 2
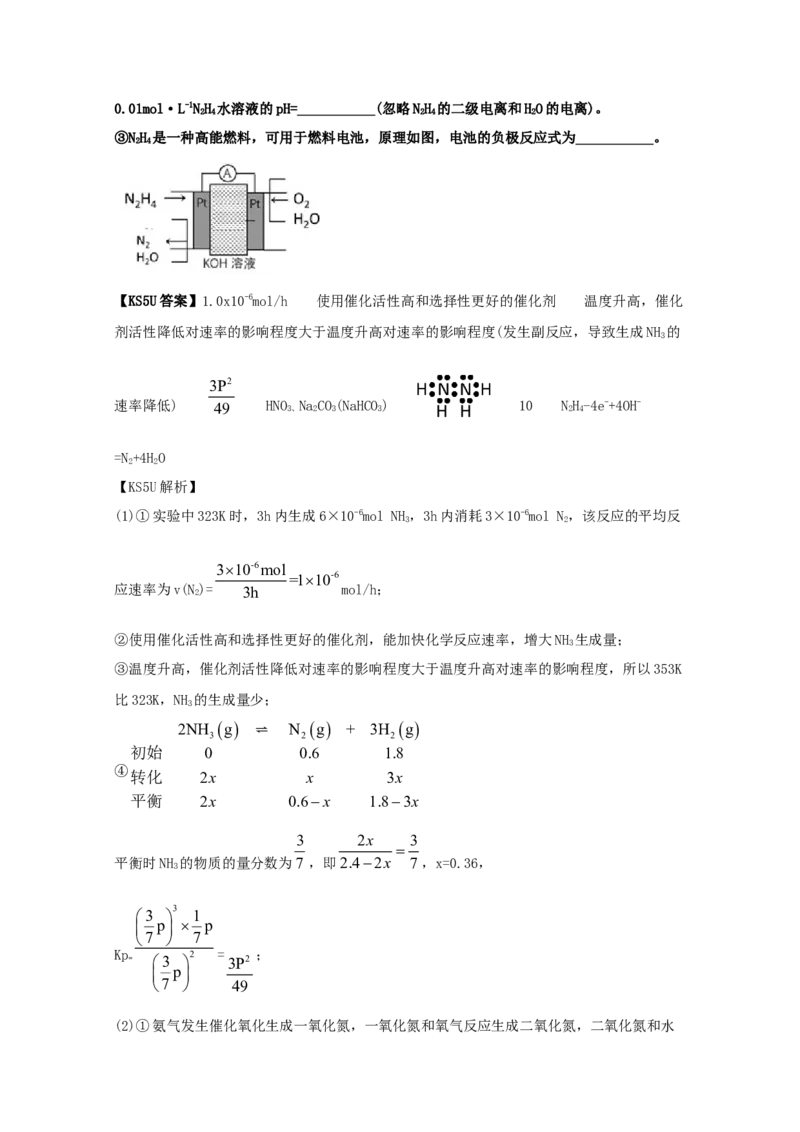
③NH 是一种高能燃料,可用于燃料电池,原理如图,电池的负极反应式为___________。
2 4
【KS5U答案】1.0x10-6mol/h 使用催化活性高和选择性更好的催化剂 温度升高,催化
剂活性降低对速率的影响程度大于温度升高对速率的影响程度(发生副反应,导致生成NH 的
3
3P2
速率降低) 49 HNO 3、 Na 2 CO 3 (NaHCO 3 ) 10 N 2 H 4 -4e-+4OH-
=N+4HO
2 2
【KS5U解析】
(1)①实验中323K时,3h内生成6×10-6mol NH,3h内消耗3×10-6mol N,该反应的平均反
3 2
310-6mol
=110-6
应速率为v(N 2 )= 3h mol/h;
②使用催化活性高和选择性更好的催化剂,能加快化学反应速率,增大NH 生成量;
3
③温度升高,催化剂活性降低对速率的影响程度大于温度升高对速率的影响程度,所以353K
比323K,NH 的生成量少;
3
2NH g N g + 3H g
3 2 2
初始 0 0.6 1.8
④
转化 2x x 3x
平衡 2x 0.6x 1.83x
3 2x 3
平衡时NH 的物质的量分数为7 ,即2.42x 7,x=0.36,
3
3
3 1
p p
7 7
Kp = 3 2 = 3P2 ;
p
7 49
(2)①氨气发生催化氧化生成一氧化氮,一氧化氮和氧气反应生成二氧化氮,二氧化氮和水反应生成硝酸;氨气、饱和食盐水、二氧化碳反应生成碳酸氢钠,以NH 为原料可以制备
3
HNO,NaCO(NaHCO);
3 2 3 3
②NH 的电子式为 ,NH 的水溶液呈弱碱性,室温下其电离常数K=1.0×10-6,
2 4 2 4 1
c2 OH
0.01mol·L-1NH 水溶液中, 1106 ,c OH 1104,
2 4 0.01
1014
c H 1010
104 ,则0.01mol·L-1N
2
H
4
水溶液的pH=10。
③由图示可知,电池的负极NH 失电子生成N 和水,反应式为NH-4e-+4OH-=N+4HO。
2 4 2 2 4 2 2