文档内容
备战2025年高考化学【二轮·突破提升】专题复习讲义
专题23 水溶液中的离子反应与平衡
讲义包含四部分:把握命题方向►精选高考真题►高效解题策略►各地最新模拟
水溶液中的离子反应与平衡在高考卷中主要以选择题形式出现,综合性较强,以相关图像为信息载
体,考查离子平衡、曲线含义的判断、平衡常数的计算、离子数量关系、溶液酸碱性判断及变化等知识。
总体来说,历年高考中电解质溶液试题具有一定的难度。其考查的主要内容有:
(1)弱电解质的电离平衡及图像分析;
(2)水的电离平衡及图像分析、混合溶液酸碱性的判断;
(3)盐类的水解平衡及图像分析;
(4)电解质溶液中离子浓度大小的比较(三大守恒关系的应用);
(5)沉淀的溶解平衡及转化。
预计2025年高考中,“四大常数”(水的离子积常数、电离常数、水解常数、溶度积常数)的计算及应
用、中和滴定的迁移应用、离子浓度大小的比较、沉淀溶解平衡仍会成为考查的重点,难度以偏难为主,
以选择题、图像题的形式呈现。在化工流程题中考查溶度积(Ksp)的计算及应用,在化学反应原理综合题中
考查电离常数、水解常数等的计算及应用等。
1.(2024·广西·高考真题)常温下,用 溶液分别滴定下列两种混合溶液:
Ⅰ.20.00mL浓度均为 和 溶液
Ⅱ.20.00mL浓度均为 和 溶液
两种混合溶液的滴定曲线如图。已知 ,下列说法正确的是
A.Ⅰ对应的滴定曲线为N线
B. 点水电离出的 数量级为C. 时,Ⅱ中
D. 时,Ⅰ中 之和小于Ⅱ中 之和
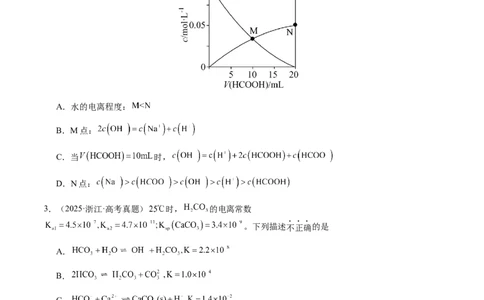
2.(2024·湖南·高考真题)常温下 ,向 溶液中缓慢滴入相
同浓度的 溶液,混合溶液中某两种离子的浓度随加入 溶液体积的变化关系如图所示,下
列说法错误的是
A.水的电离程度:
B.M点:
C.当 时,
D.N点:
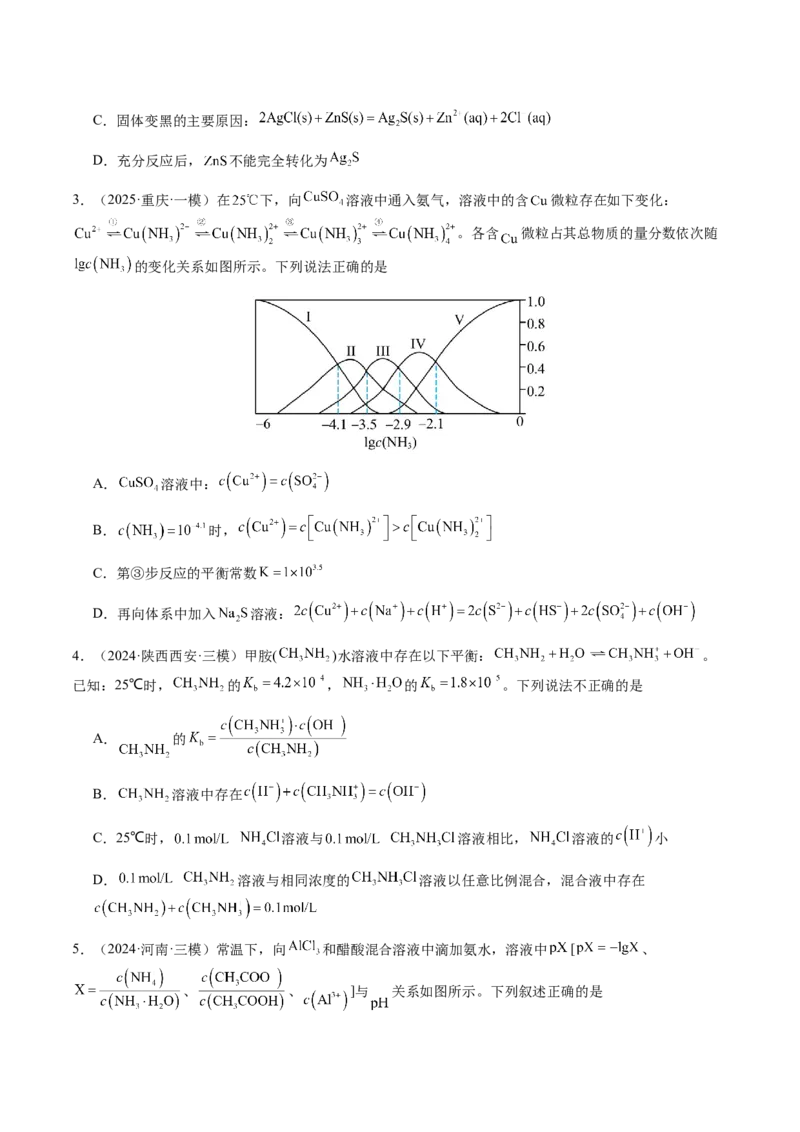
3.(2025·浙江·高考真题) 时, 的电离常数
。下列描述不正确的是
A.
B.
C.
D. 溶液中, ,则
4.(2024·天津·高考真题)甲胺 水溶液中存在以下平衡: 。
已知: 时, 的 , 的 。下列说法错误的是
A. 的B. 溶液中存在
C. 时, 溶液与 溶液相比, 溶液中的 小
D. 溶液与相同浓度的 溶液以任意比例混合,混合液中存在
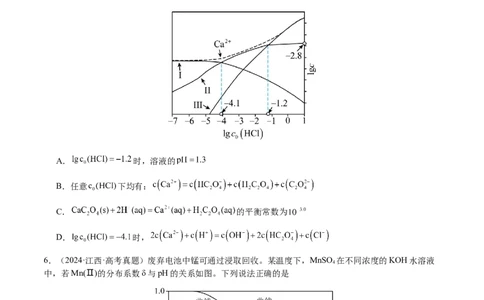
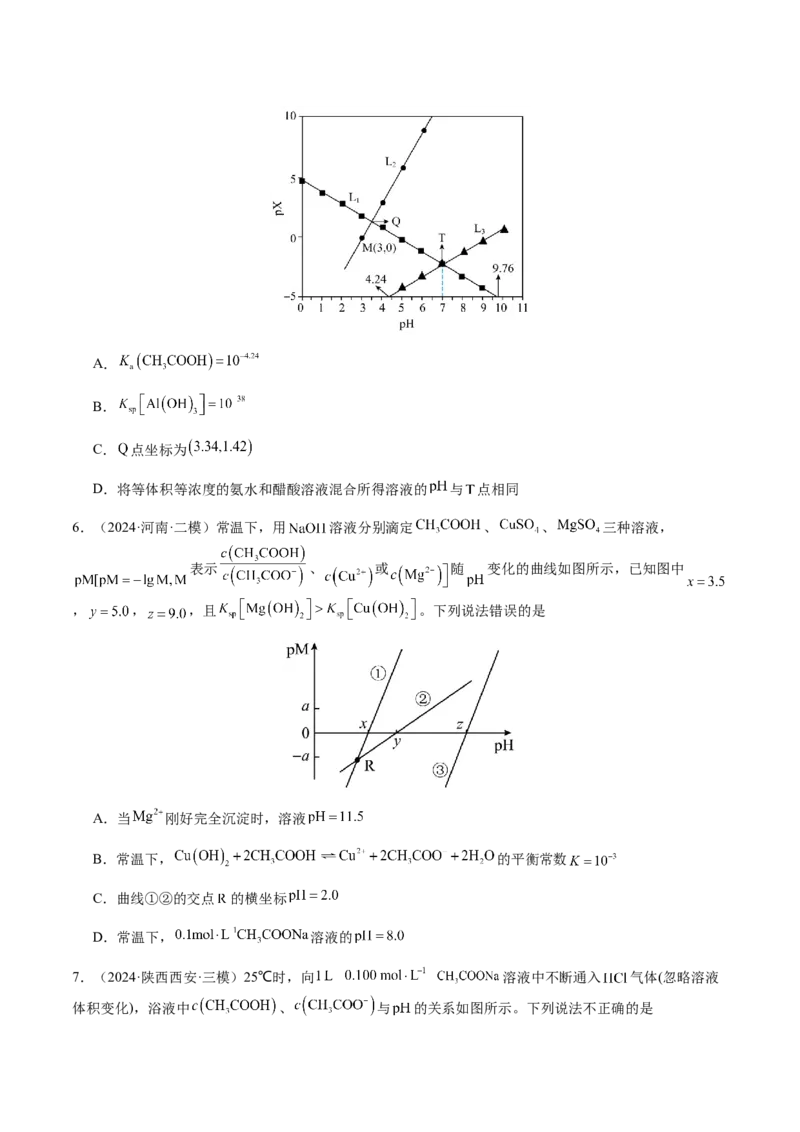
5.(2024·福建·高考真题)将草酸钙固体溶于不同初始浓度 的盐酸中,平衡时部分组分的
关系如图。已知草酸 。下列说法错误的是
A. 时,溶液的
B.任意 下均有:
C. 的平衡常数为
D. 时,
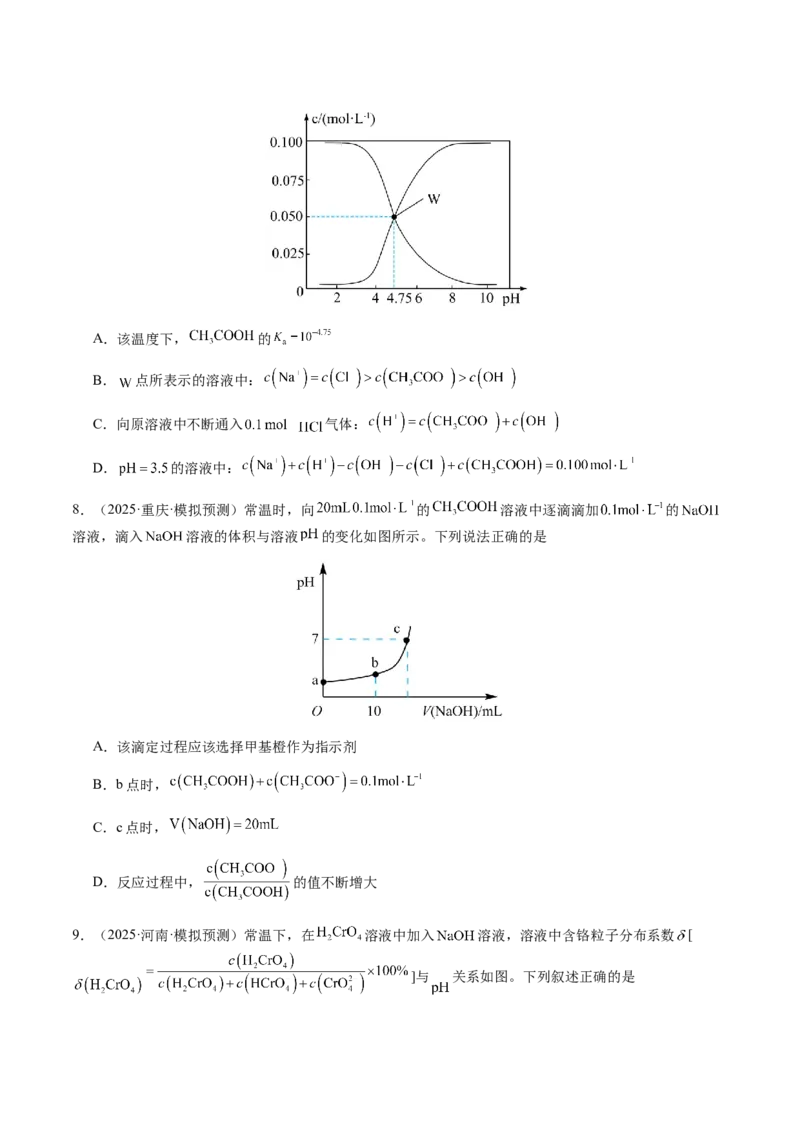
6.(2024·江西·高考真题)废弃电池中锰可通过浸取回收。某温度下,MnSO 在不同浓度的KOH水溶液
4
中,若Mn(Ⅱ)的分布系数δ与pH的关系如图。下列说法正确的是已知:Mn(OH) 难溶于水,具有两性;δ(MnOH+)=
2
;
A.曲线z为δ(MnOH+)
B.O点,
C.P点,c(Mn2+)<c(K+)
D.Q点,c( )=2c(MnOH+)+2c( )
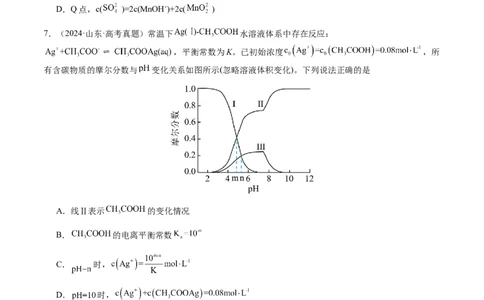
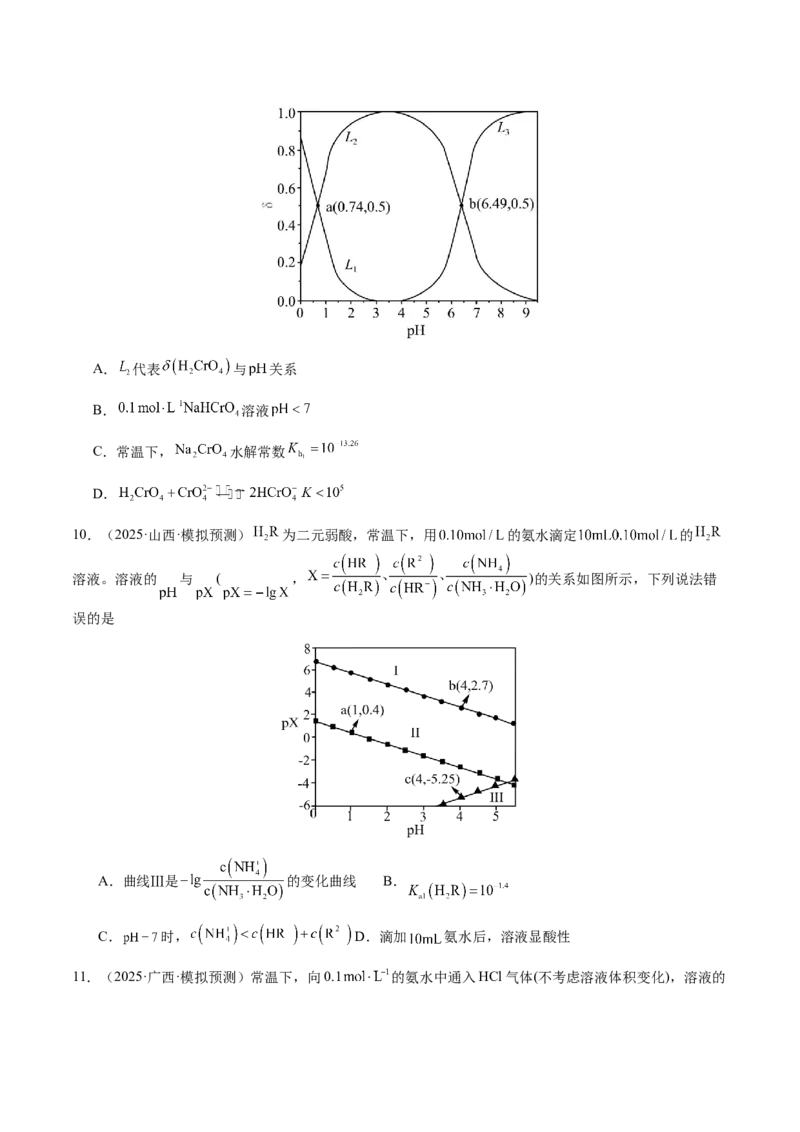
7.(2024·山东·高考真题)常温下 水溶液体系中存在反应:
,平衡常数为K。已初始浓度 ,所
有含碳物质的摩尔分数与 变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
A.线Ⅱ表示 的变化情况
B. 的电离平衡常数
C. 时,
D. 时,
8.(2024·浙江·高考真题)常温下、将等体积、浓度均为 溶液与新制 溶液混合,
出现白色浑浊;再滴加过量的 溶液,振荡,出现白色沉淀。
已知: ,
下列说法不正确的是
A. 溶液中存在B.将 溶液稀释到 , 几乎不变
C. 溶液与 溶液混合后出现的白色浑浊不含有
D.存在反应 是出现白色沉淀的主要原因
9.(2023·辽宁·高考真题)某废水处理过程中始终保持HS饱和,即 ,通过调节pH使
2
和 形成硫化物而分离,体系中 与 关系如下图所示,c为 和 的浓度,
单位为 。已知 ,下列说法正确的是
A. B.③为 与 的关系曲线
C. D.
10.(2024·江苏·高考真题)室温下,通过下列实验探究 的性质。已知 ,
。
实验1:将 气体通入水中,测得溶液 。
实验2:将 气体通入 溶液中,当溶液 时停止通气。
实验3:将 气体通入 酸性 溶液中,当溶液恰好褪色时停止通气。
下列说法正确的是
A.实验1所得溶液中:
B.实验2所得溶液中:
C.实验2所得溶液经蒸干、灼烧制得 固体
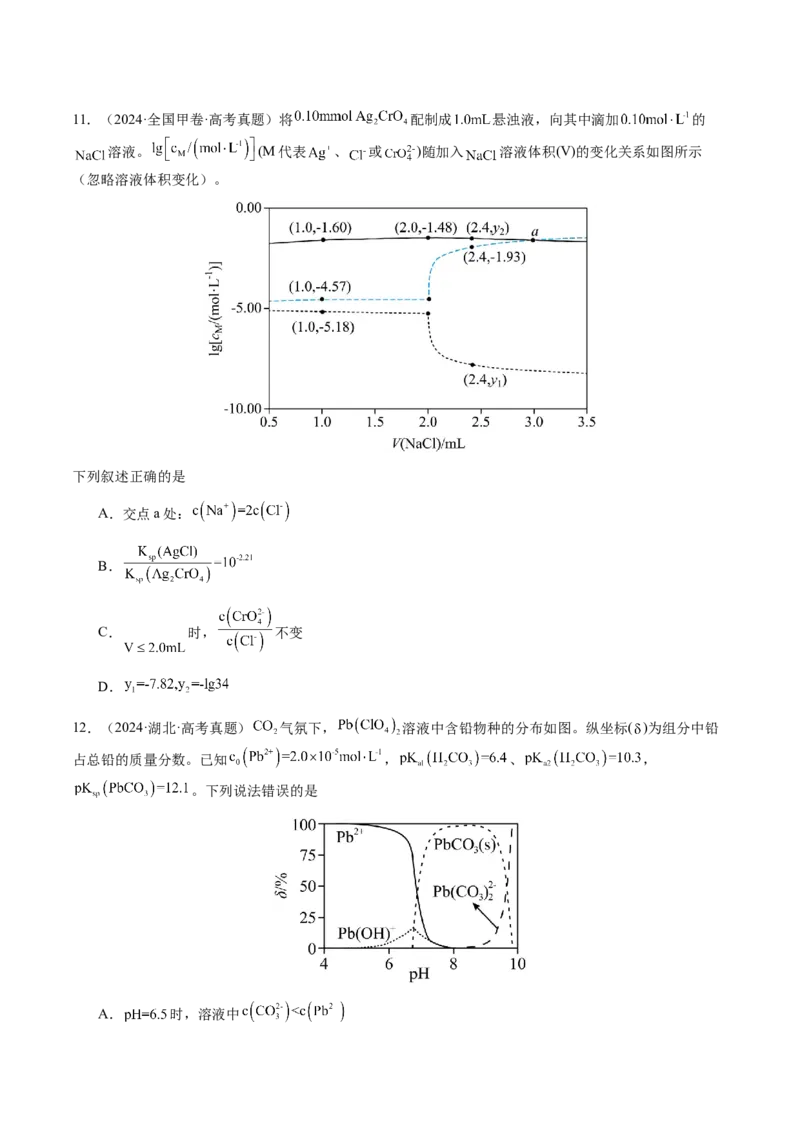
D.实验3所得溶液中:11.(2024·全国甲卷·高考真题)将 配制成 悬浊液,向其中滴加 的
溶液。 (M代表 、 或 )随加入 溶液体积(V)的变化关系如图所示
(忽略溶液体积变化)。
下列叙述正确的是
A.交点a处:
B.
C. 时, 不变
D.
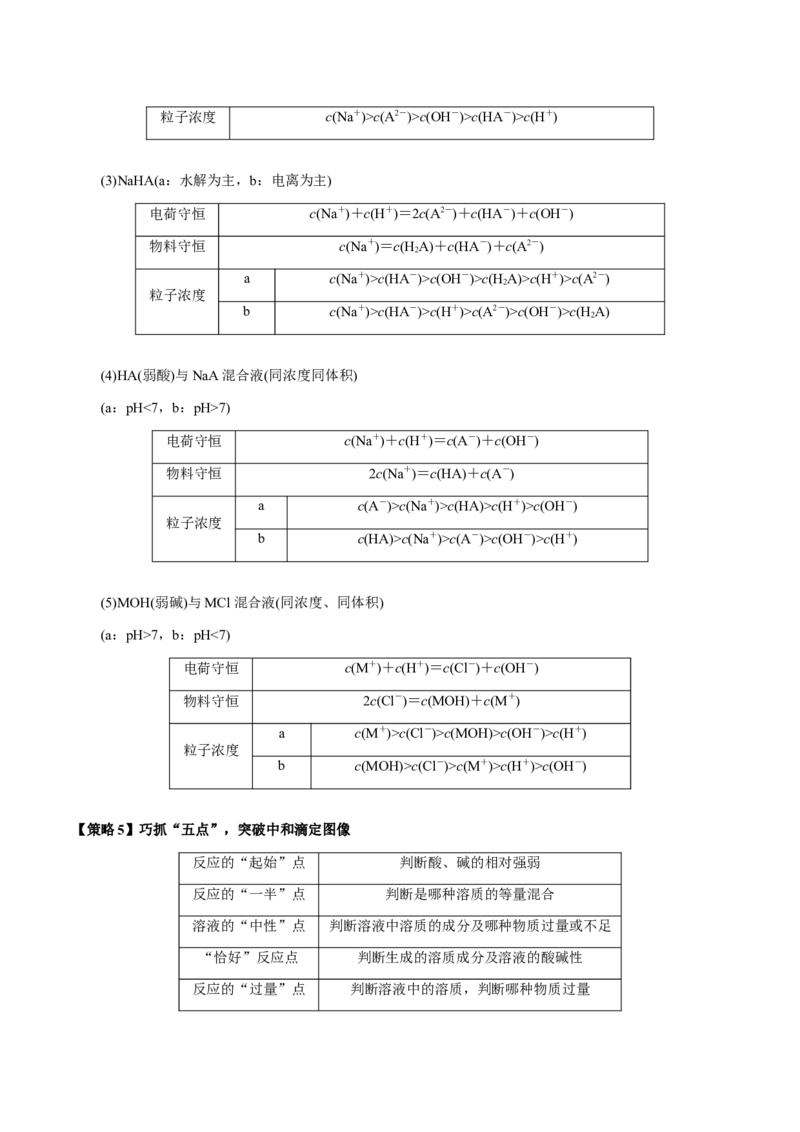
12.(2024·湖北·高考真题) 气氛下, 溶液中含铅物种的分布如图。纵坐标( )为组分中铅
占总铅的质量分数。已知 , 、 ,
。下列说法错误的是
A. 时,溶液中B. 时,
C. 时,
D. 时,溶液中加入少量 , 会溶解
13.(2024·安徽·高考真题)环境保护工程师研究利用 、 和 处理水样中的 。已知
时, 饱和溶液浓度约为 , , , ,
。下列说法错误的是
A. 溶液中:
B. 溶液中:
C.向 的溶液中加入 ,可使
D.向 的溶液中通入 气体至饱和,所得溶液中:
14.(2024·吉林·高考真题) 下, 、 和 的沉淀溶解平衡曲线如下图所示。某实验
小组以 为指示剂,用 标准溶液分别滴定含 水样、含 水样。
已知:① 为砖红色沉淀;
②相同条件下 溶解度大于 ;
③ 时, , 。
pAg=-lg[c(Ag+)/(mol·L-1)]
pX=-lg[c(Xn-)/(mol·L-1)](X代表Cl-、Br-或CrO )
下列说法错误的是
A.曲线②为 沉淀溶解平衡曲线B.反应 的平衡常数
C.滴定 时,理论上混合液中指示剂浓度不宜超过
D.滴定 达终点时,溶液中
15.(2024·上海·高考真题)已知:
①
②
③
(1)以下能判断总反应达到平衡状态的是_______。
A.钙离子浓度保持不变 B. 保持不变
C. D.
(2) 增大有利于珊瑚的形成,请解释原因 。
(3)已知 的 ,
为 。当 时,开始产生 沉淀。
【策略1】理解溶液中四大平衡的概念、影响因素及应用1.弱电解质的电离平衡——“四条件”对弱电解质电离的影响
条件改变 对电离平衡的影响 微粒浓度影响结果 电离程度 电离常数
弱酸的H+、酸根离子浓度减小,OH
加水 正向移动 -浓度增大;弱碱的OH-、金属离子 增大 不变
浓
(或NH)浓度减小,H+浓度增大
度
弱电解质相应离子和弱电解质浓度均
加弱电解质 正向移动 减小 不变
增大
弱电解质分子浓度减小;弱电解质相
加热 正向移动 增大 增大
应离子浓度增大
弱电解质浓度增大,“同离子”浓度
同离子效应 逆向移动 减小 不变
增大,其他离子浓度减小
加入与弱电解质 参与反应的离子浓度减小,其他离子
正向移动 增大 不变
反应的物质 浓度增大
2.影响水电离的因素及溶液的酸碱性
(1)影响水电离的因素(2)溶液的酸碱性及pH
①溶液酸碱性与pH:在任何温度下的中性溶液中,c(H+)=c(OH-)=,常温下中性溶液的pH=7,温
度升高时,中性溶液的pH<7。
②溶液pH的计算方法
解答有关pH的计算时,首先要注意温度,明确是25℃还是非25℃,然后判断溶液的酸碱性,再根据
“酸按酸”,“碱按碱”的原则进行计算。
若溶液为酸性,先求c(H+),再求pH;
若溶液为碱性,先求c(OH-),再由c(H+)=求c(H+),最后求pH。
3.盐类的水解及其应用
(1)盐类水解的规律
①组成盐的弱碱阳离子水解使溶液显酸性,组成盐的弱酸根离子水解使溶液显碱性。
②盐对应的酸(或碱)越弱,水解程度越大,溶液碱性(或酸性)越强。
③多元弱酸的酸根离子比酸式酸根离子的水解程度大得多。如相同浓度时,CO比HCO的水解程度
大。
④水解程度:相互促进水解的盐>单水解的盐>相互抑制水解的盐。如 NH 的水解程度:
(NH )CO>(NH)SO >(NH)Fe(SO )。
4 2 3 4 2 4 4 2 4 2
(2)溶液酸碱性的判断方法
①电离能力大于水解能力,如 CHCOOH 的电离程度大于 CHCOO-的水解程度,所以等浓度的
3 3
CHCOOH与CHCOONa溶液等体积混合后溶液显酸性;同理NH ·H O的电离程度大于NH的水解程度,
3 3 3 2
等浓度的NH ·H O和NH Cl溶液等体积混合后溶液显碱性。
3 2 4
②水解能力大于电离能力,如HClO的电离程度小于ClO-水解程度,所以等浓度的HClO与NaClO溶
液等体积混合后溶液显碱性。
③酸式盐溶液的酸碱性主要取决于酸式酸根的电离能力和水解能力哪一个更强。如在 NaHCO 溶液
3
中,HCO的水解程度大于电离程度,故溶液显碱性;而在NaHSO 溶液中,HSO的电离程度大于水解程
3
度,故溶液显酸性。
4.沉淀溶解平衡及其应用
一般情况下,升高温度能促进沉淀的溶解;稀释使沉淀溶解平衡向右移动,稀释后重新达到平衡时各
离子浓度保持不变。对于确定的物质来说,K 只与温度有关;温度相同时,组成形式相同的物质,K 较
sp sp
大者溶解度较大。(1)沉淀的生成或溶解的判断:若体系内Q=K ,体系处于溶解平衡状态;Q>K ,体系内会有沉淀析
c sp c sp
出;QK 者先
c sp
形成沉淀。
(3)沉淀的转化与K 大小间的关系:组成形式相同的难溶物质,K 较大的沉淀易转化为K 较小的沉
sp sp sp
淀,但当二者K 相差不大时,反过来也可转化。
sp
【策略2】掌握溶液中各类平衡常数的计算方法及关系
(1)电离度(α)与电离平衡常数(K 、K )之间的关系
a b
①一元弱酸(以CHCOOH为例)
3
设常温下,浓度为c mol·L-1的醋酸的电离度为α
CHCOOH CHCOO-+H+
3 3
起始(mol·L-1) c 0 0
转化(mol·L-1) c·α c·α c·α
平衡(mol·L-1) c-cα≈c c·α c·α
K==cα2、α=,c(H+)=cα=。
a
②一元弱碱(如NH ·H O,电离常数为K )
3 2 b
同理可得:K =cα2,c(OH-)=cα=。
b
(2)水解常数(K )与电离常数的定量关系
h
(1)强碱弱酸盐:K =
h
如:CHCOONa:CHCOO-+HO CHCOOH+OH-
3 3 2 3
(2)强酸弱碱盐:K =
h
如:NH Cl:NH ++HO NH ·H O+H+
4 4 2 3 2
(3)多元弱酸强碱盐:
NaCO: CO+HO HCO+OH- ,
2 3 2HCO-+HO HCO+OH-
3 2 2 3
即K ·K =K ,K ·K =K 。
a1 h2 w a2 h1 w
可以用电离平衡常数与水解常数的大小关系判断弱酸的酸式盐溶液的酸碱性,以HCO为例,已知:
K =:
a1
电离方程式:HCO H++CO K =
a2
水解方程式:HCO+HO HCO+OH- K ==,
2 2 3 h2
只需比较K 和K =的大小即可判断弱酸的酸式盐溶液的酸碱性。
a2 h2
①如一定浓度的NaHCO 溶液,K (H CO)=4.4×10-7,K (H CO)=5.6×10-11,K ==≈2.27×10-8>
3 a1 2 3 a2 2 3 h
K ,HCO的水解程度大于其电离程度,溶液呈碱性,c(OH-)>c(H+),c(H CO)>c(CO)。
a2 2 3
②又如一定浓度的NaHSO 溶液,K (H SO )=1.54×10-2,K (H SO )=1.2×10-7,K ==≈6.5×10-13
3 a1 2 3 a2 2 3 h
<K ,HSO的水解程度小于其电离程度,溶液呈酸性,c(H+)>c(OH-),c(SO)>c(H SO )。
a2 2 3
③再如一定浓度的CHCOONH 溶液,由于K(CHCOOH)=1.75×10-5≈K (NH ·H O)=1.71×10-5,则
3 4 a 3 b 3 2
CHCOO-与NH的水解常数近似相等,二者水解程度相同,CHCOONH 溶液呈中性,c(CHCOO-)=
3 3 4 3
c(NH)。
【策略3】溶度积(K )的有关计算
sp
1、已知溶度积,求溶液中的某种离子的浓度。
①AgCl、AgBr、AgI等1:1型:如K =a的饱和AgCl溶液中c(Ag+)= mol·L-1。
sp
【例】以AgCl(s) Ag+(aq)+Cl-(aq)为例,K (AgCl)=1.8×10-10
SP
设AgCl的饱和溶液的浓度为x mol·L-1
AgCl(s) Ag+(aq) + Cl-(aq)
1 1 1
x mol·L-1 x mol·L-1 x mol·L-1
则:K =c(Ag+)·c(Cl-)=x2, =1.34×10-5 mol·L-1
sp
②类型不同的难溶电解质的溶度积大小不能直接反映出它们的溶解度大小,因为它们溶度积与溶解度的关
系式是不同的。
【例】以Ag CrO(s) 2Ag+(aq)+CrO2-(aq)为例,K (Ag CrO)=9.0×10-12
2 4 4 SP 2 4
设Ag CrO 的饱和溶液的浓度为y mol·L-1
2 4
Ag CrO(s) 2Ag+(aq) + CrO2-(aq)
2 4 4
1 2 1y mol·L-1 2y mol·L-1 ymol·L-1
则:K =c2(Ag+)·c(CrO2-)=(2y)2·y=4y3, =1.3×10-4 mol·L-1
SP 4
【例】以Fe(OH) (S) Fe3+(aq)+3OH-(aq)为例,K (Fe(OH) )=4.0×10-38
3 SP 3
设Fe(OH) 的饱和溶液的浓度为z mol·L-1
3
Fe(OH) (s) Fe3+(aq) + 3OH-(aq)
3
1 1 3
z mol·L-1 z mol·L-1 3z mol·L-1
则:K =c(Fe3+)·c3(OH-)=z·(3z)3=27z4, =2.0×10-10 mol·L-1
SP
2、已知溶度积、溶液中某离子的浓度,求溶液中另一种离子的浓度。
如某温度下AgCl的K =a,在0.1 mol·L-1的NaCl溶液中加入过量的AgCl固体,达到平衡后c(Ag+)
sp
= =10a mol·L-1
3、计算反应的平衡常数,,并判断沉淀转化的程度。
如反应Cu2+(aq)+MnS(s) CuS(s)+Mn2+(aq),K (MnS)=c(Mn2+)·c(S2-),K (CuS)=c(Cu2+)·c(S2
sp sp
-),平衡常数K==。
4、求解开始沉淀和沉淀完全时的pH。
如判断M(OH) (s) Mn+(aq)+nOH-(aq)开始沉淀与沉淀完全时的pH。
n
①开始沉淀时pH的求法:c(OH-)=,c(H+)=,从而确定pH。
②沉淀完全时pH的求法:当Mn+的浓度小于或等于1.0×10-5 mol·L-1时,认为该离子已经沉淀完
全,c(OH-)= mol·L-1,结合K 求出c(H+),从而确定pH。
w
注意:有关K 的计算往往与pH的计算结合,要注意pH与c(OH-)关系的转换;难溶电解质的悬浊液
sp
即其沉淀溶解平衡状态,满足相应的K 。
sp
5、判断沉淀的生成或沉淀是否完全
①把离子浓度数据代入K 表达式得Q,若Q>K ,则有沉淀生成;若Qc(H PO -)>c(HPO 2-)>c(PO 3-)。
3 4 2 4 4 4
(2)电离能力大于水解能力,如:CHCOOH的电离程度大于CHCOO-的水解程度,所以等浓度的
3 3
CHCOOH与CHCOONa溶液等体积混合后溶液显酸性;同理NH ·H O的电离程度大于NH +的水解程
3 3 3 2 4
度,等浓度的NH ·H O和NH Cl溶液等体积混合后溶液显碱性。
3 2 4
例如,等物质的量浓度的NH Cl与NH ·H
O混合溶液中:c(NH+
)>c(Cl-)>c(OH-)>c(H+);
4 3 2 4
等物质的量浓度的CHCOONa与CHCOOH混合溶液中:c(CHCOO-)>c(Na+)>c(H+)>c(OH-)。
3 3 3
(3)水解能力大于电离能力,如:HClO的电离程度小于ClO-水解程度,所以等浓度的HClO与NaClO
溶液等体积混合后溶液显碱性。
例如,在0.1 mol·L-1的NaCN和0.1 mol·L-1的HCN混合溶液中:c(Na+)>c(CN-)>c(OH-)>c(H+)。
(4)多元弱酸的酸式盐溶液的酸碱性主要取决于酸式酸根的电离能力和水解能力哪一个更强。如在
NaHCO 溶液中,HCO—的水解大于电离,故溶液显碱性;而在NaHSO 溶液中,HSO—的电离大于水解,
3 3 3 3
故溶液显酸性。
如HCO -以水解为主,0.1 mol·L-1 NaHCO 溶液中:c(Na+)>c(HCO -)>c(OH-)>c(H+)>c(CO2-);
3 3 3 3
而HSO -以电离为主,0.1 mol·L-1 NaHSO 溶液中:c(Na+)>c(HSO -)>c(H+)>c(SO 2-)>c(OH-)。
3 3 3 3
(5)对于多元弱酸的正盐溶液,根据弱酸根离子的分步水解分析。
例如,0.1 mol·L-1 Na CO 溶液中电离过程有NaCO=2Na++ CO 2-,HO OH-+H+;水解过程有
2 3 2 3 3 2
CO2-+H O HCO -+OH-,HCO -+H O HCO+OH-。故溶液中存在的离子有Na+、CO2-、OH-、
3 2 3 3 2 2 3 3
HCO -、H+,因此溶液中各离子浓度的大小顺序为c(Na+)>c(CO2-)>c(OH-)>c(HCO -)>c(H+)。
3 3 3
(6)不同溶液中同一离子浓度的大小比较,要考虑溶液中其他离子对该离子的影响。如在0.10 mol·L-1
的①NH HSO 、②NH Cl、③CHCOONH、④(NH )SO 溶液中,c(NH +)的大小顺序为④>①>②>③。
4 4 4 3 4 4 2 4 4
4.突破溶液中粒子浓度的“五模板”
(1)MCl(强酸弱碱盐)溶液
电荷守恒 c(M+)+c(H+)=c(Cl-)+c(OH-)
物料守恒 c(M+)+c(MOH)=c(Cl-)
粒子浓度 c(Cl-)>c(M+)>c(H+)>c(MOH)>c(OH-)
(2)Na A(强碱弱酸盐)溶液
2
电荷守恒 c(Na+)+c(H+)=2c(A2-)+c(HA-)+c(OH-)
物料守恒 c(Na+)=2[c(H A)+c(HA-)+c(A2-)]
2粒子浓度 c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+)
(3)NaHA(a:水解为主,b:电离为主)
电荷守恒 c(Na+)+c(H+)=2c(A2-)+c(HA-)+c(OH-)
物料守恒 c(Na+)=c(H A)+c(HA-)+c(A2-)
2
a c(Na+)>c(HA-)>c(OH-)>c(H A)>c(H+)>c(A2-)
2
粒子浓度
b c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)>c(H A)
2
(4)HA(弱酸)与NaA混合液(同浓度同体积)
(a:pH<7,b:pH>7)
电荷守恒 c(Na+)+c(H+)=c(A-)+c(OH-)
物料守恒 2c(Na+)=c(HA)+c(A-)
a c(A-)>c(Na+)>c(HA)>c(H+)>c(OH-)
粒子浓度
b c(HA)>c(Na+)>c(A-)>c(OH-)>c(H+)
(5)MOH(弱碱)与MCl混合液(同浓度、同体积)
(a:pH>7,b:pH<7)
电荷守恒 c(M+)+c(H+)=c(Cl-)+c(OH-)
物料守恒 2c(Cl-)=c(MOH)+c(M+)
a c(M+)>c(Cl-)>c(MOH)>c(OH-)>c(H+)
粒子浓度
b c(MOH)>c(Cl-)>c(M+)>c(H+)>c(OH-)
【策略5】巧抓“五点”,突破中和滴定图像
反应的“起始”点 判断酸、碱的相对强弱
反应的“一半”点 判断是哪种溶质的等量混合
溶液的“中性”点 判断溶液中溶质的成分及哪种物质过量或不足
“恰好”反应点 判断生成的溶质成分及溶液的酸碱性
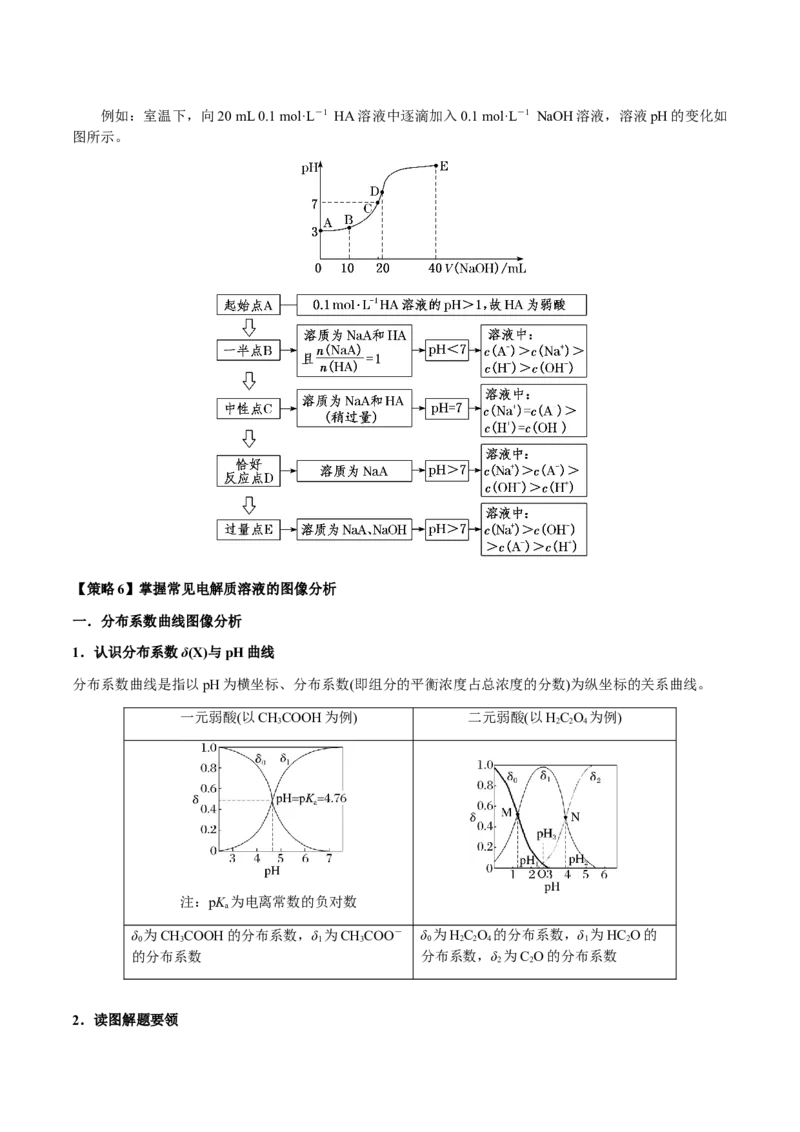
反应的“过量”点 判断溶液中的溶质,判断哪种物质过量例如:室温下,向20 mL 0.1 mol·L-1 HA溶液中逐滴加入0.1 mol·L-1 NaOH溶液,溶液pH的变化如
图所示。
【策略6】掌握常见电解质溶液的图像分析
一.分布系数曲线图像分析
1.认识分布系数δ(X)与pH曲线
分布系数曲线是指以pH为横坐标、分布系数(即组分的平衡浓度占总浓度的分数)为纵坐标的关系曲线。
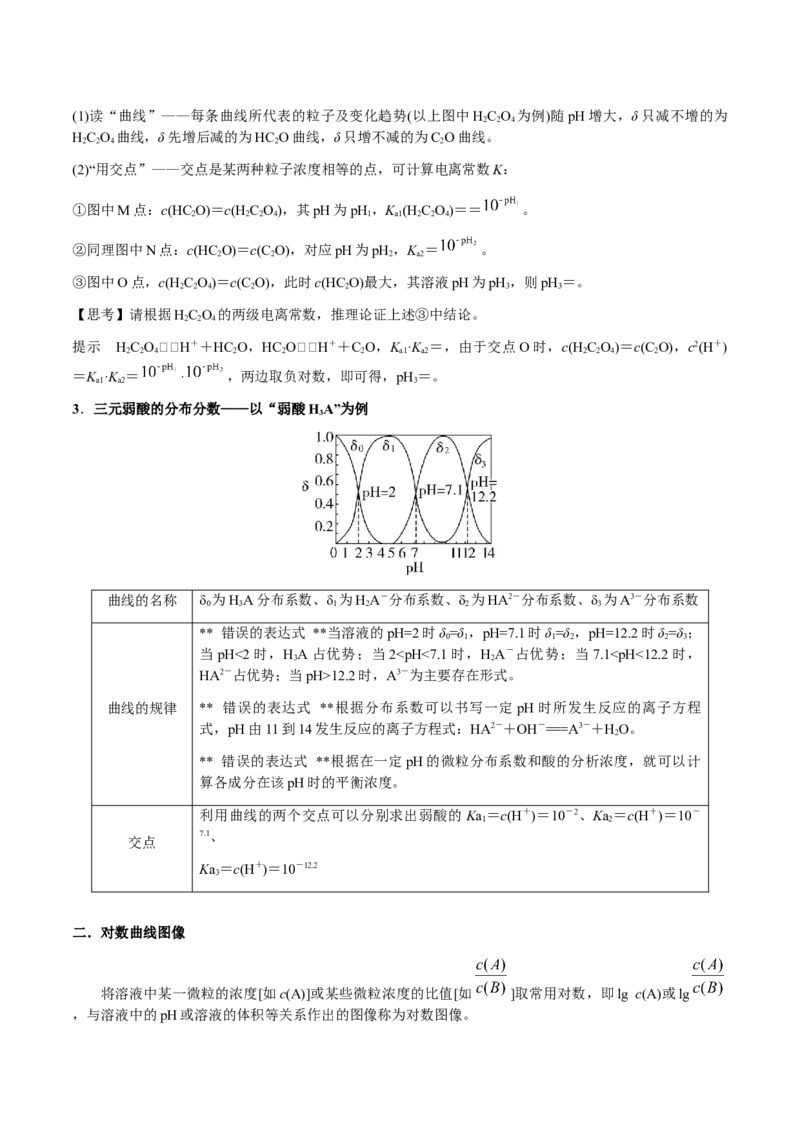
一元弱酸(以CHCOOH为例) 二元弱酸(以HC O 为例)
3 2 2 4
注:pK 为电离常数的负对数
a
δ 为CHCOOH的分布系数,δ 为CHCOO- δ 为HC O 的分布系数,δ 为HC O的
0 3 1 3 0 2 2 4 1 2
的分布系数 分布系数,δ 为C O的分布系数
2 2
2.读图解题要领(1)读“曲线”——每条曲线所代表的粒子及变化趋势(以上图中HC O 为例)随pH增大,δ只减不增的为
2 2 4
HC O 曲线,δ先增后减的为HC O曲线,δ只增不减的为C O曲线。
2 2 4 2 2
(2)“用交点”——交点是某两种粒子浓度相等的点,可计算电离常数K:
①图中M点:c(HC O)=c(H C O),其pH为pH,K (H C O)== 。
2 2 2 4 1 a1 2 2 4
②同理图中N点:c(HC O)=c(C O),对应pH为pH,K = 。
2 2 2 a2
③图中O点,c(H C O)=c(C O),此时c(HC O)最大,其溶液pH为pH,则pH=。
2 2 4 2 2 3 3
【思考】请根据HC O 的两级电离常数,推理论证上述③中结论。
2 2 4
提示 HC OH++HC O,HC OH++C O,K ·K =,由于交点O时,c(H C O)=c(C O),c2(H+)
2 2 4 2 2 2 a1 a2 2 2 4 2
=K ·K = · ,两边取负对数,即可得,pH=。
a1 a2 3
3.三元弱酸的分布分数——以“弱酸HA”为例
3
曲线的名称 δ 为HA分布系数、δ 为HA-分布系数、δ 为HA2-分布系数、δ 为A3-分布系数
0 3 1 2 2 3
** 错误的表达式 **当溶液的pH=2时δ=δ ,pH=7.1时δ=δ ,pH=12.2时δ=δ ;
0 1 1 2 2 3
当pH<2时,HA占优势;当212.2时,A3-为主要存在形式。
曲线的规律 ** 错误的表达式 **根据分布系数可以书写一定pH时所发生反应的离子方程
式,pH由11到14发生反应的离子方程式:HA2-+OH-===A3-+HO。
2
** 错误的表达式 **根据在一定pH的微粒分布系数和酸的分析浓度,就可以计
算各成分在该pH时的平衡浓度。
利用曲线的两个交点可以分别求出弱酸的 Ka =c(H+)=10-2、Ka =c(H+)=10-
1 2
7.1、
交点
Ka=c(H+)=10-12.2
3
二.对数曲线图像
将溶液中某一微粒的浓度[如c(A)]或某些微粒浓度的比值[如 ]取常用对数,即lg c(A)或lg
,与溶液中的pH或溶液的体积等关系作出的图像称为对数图像。1.常考对数图像的类型
图像种类 具体类型 含义 变化规律
生成物与反应物离子
对数 lg 浓度比的常用对数 lg 越大,反应向正反应方向进行的程度越大
图像
H+与OH-浓度比的常
AG=lg 用对数 AG越大,酸性越强,中性时, =1,AG=0
pH=-lg c(H+) H+浓度的常用负对数 pH越大,c(H+)越小,溶液的碱性越强
C离子浓度的常用负
负对数 pC= -lg c(C) pC越大,c(C)越小
对数
图像
生成物与反应物离子
-lg 浓度比的常用负对数 -lg 越大,反应向正反应方向进行的程度越小
2.破解对数图像的数据
(1)运算法则:lg ab=lg a+lg b、lg=lg a-lg b、lg 1=0。
(2)运算突破点:如lg =0的点有c(A)=c(B);lg c(D)=0的点有c(D)=1 mol·L-1。
3.破解对数图像的步骤
(1)识图像:观察横坐标、纵坐标的含义,看清每条曲线代表的粒子种类以及曲线的变化趋势,计算电
离常数时应利用两种粒子浓度相等的点,如lg =0。
①若c(A)=1,则lg c(A)=0;若c(A)=c(B),则lg =0
②若c(A)>1,则lg c(A)取正值;且c(A)越大lg c(A)越大
图像中数据的含义
若c(A)>c(B),则lg 取正值,且 越大lg 越大
③若c(A)<1,则lg c(A)取负值,且c(A)越大lg c(A)越小
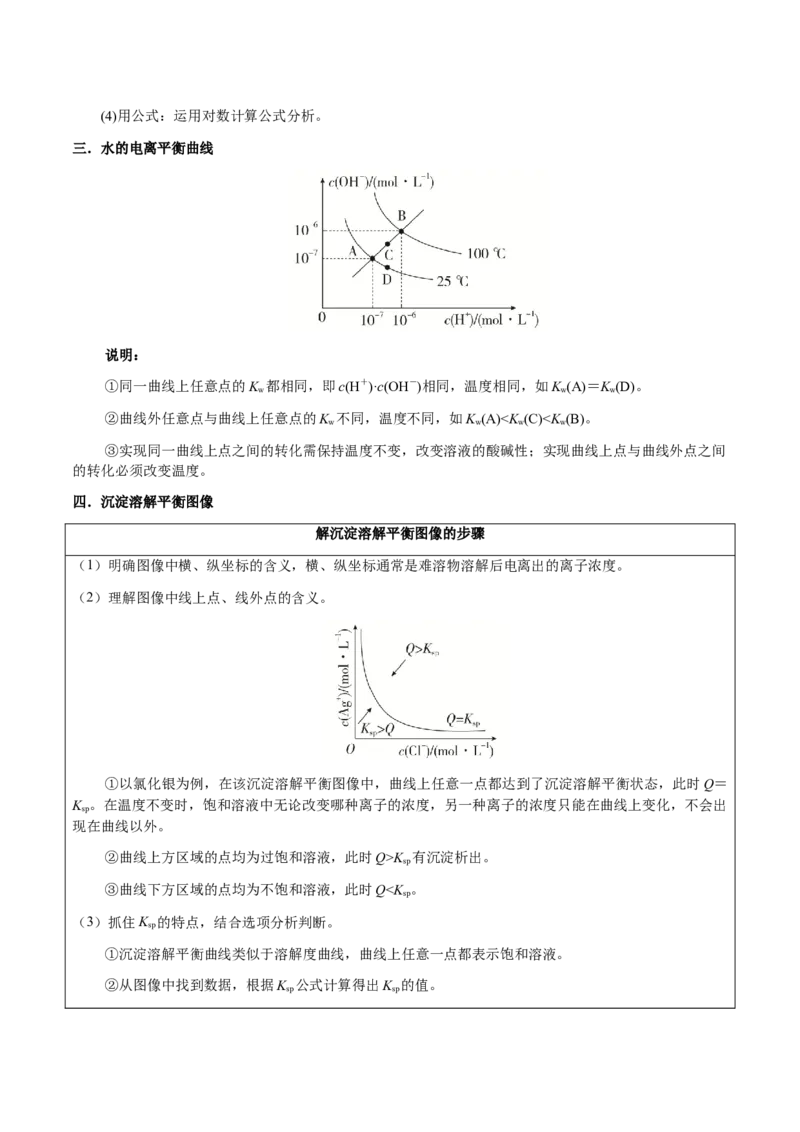
若c(A)K 有沉淀析出。
sp
③曲线下方区域的点均为不饱和溶液,此时QK 。
sp
(4)升高温度,直线向左下方平移。【例2】直线型(pM为阳离子浓度的负对数,pR为阴离子浓度的负对数)
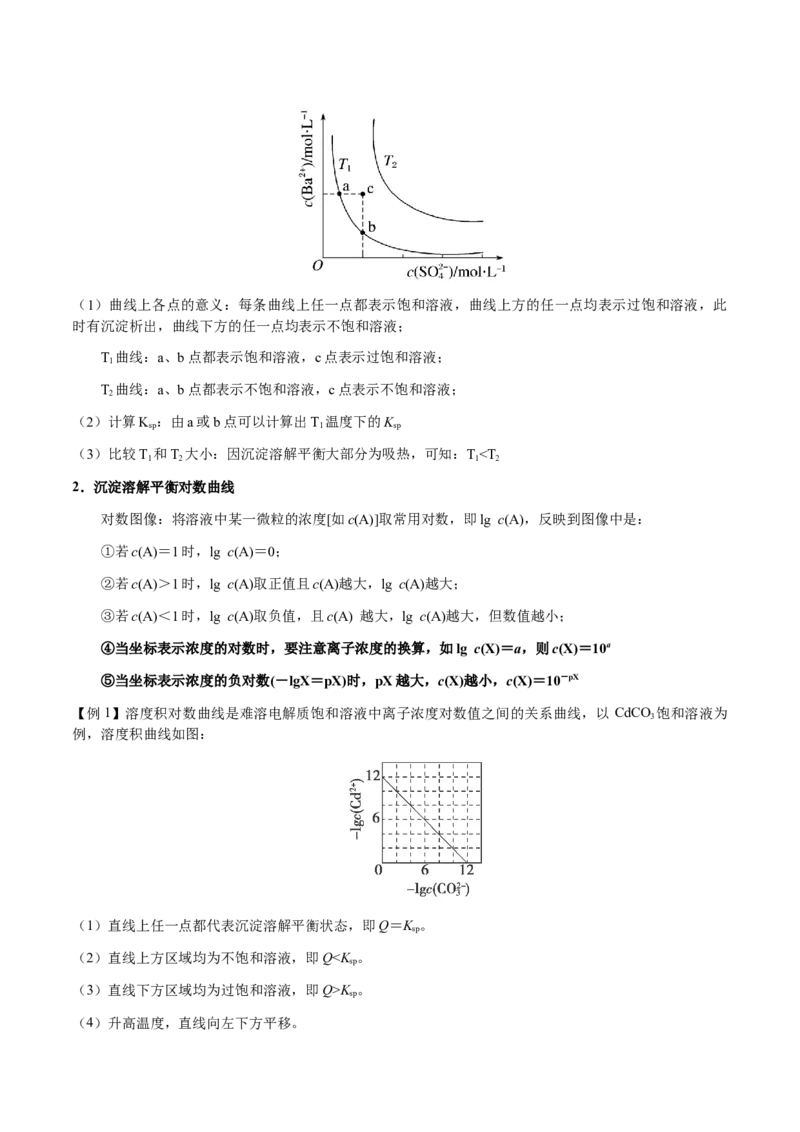
①直线AB上的点:c(M2+)=c(R2-)。
②溶度积K :CaSO>CaCO >MnCO。
sp 4 3 3
③X点:对CaCO 要析出沉淀;对CaSO 是不饱和溶液,能继续溶解CaSO。
3 4 4
④Y点:c(SO)>c(Ca2+),二者的离子积等于10-5。
⑤Z点:c(CO)K (CuS)
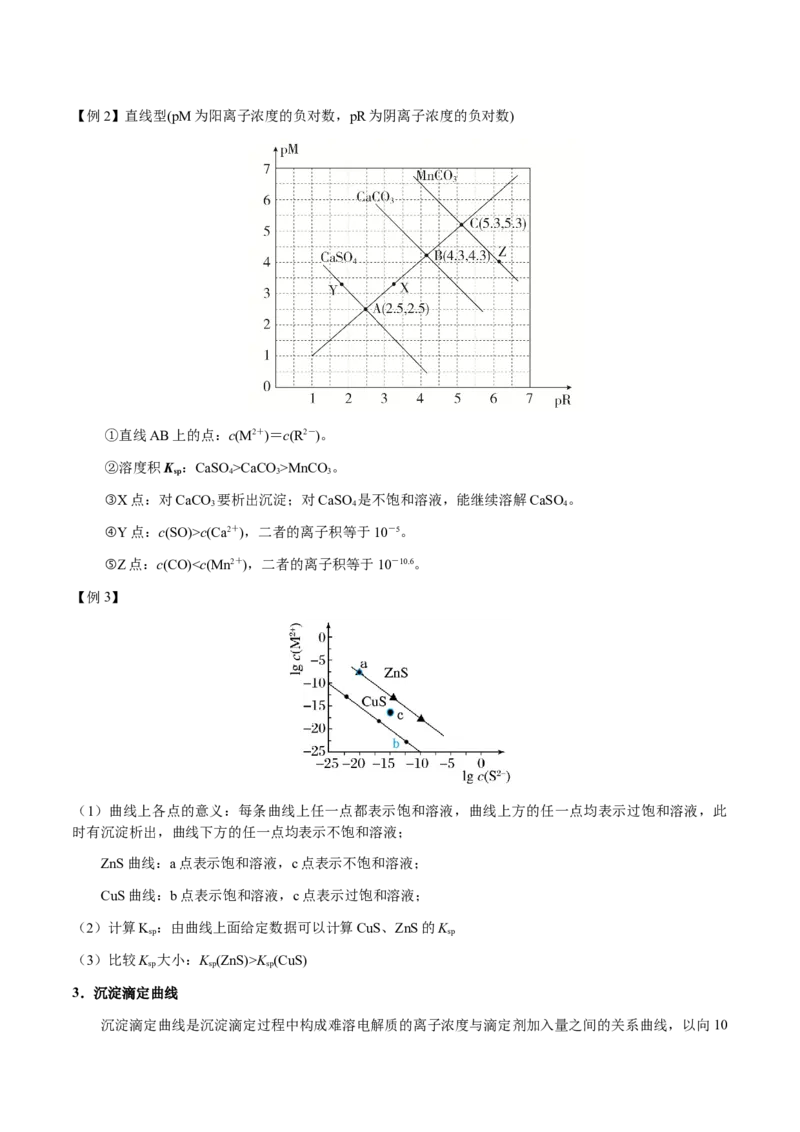
sp sp sp
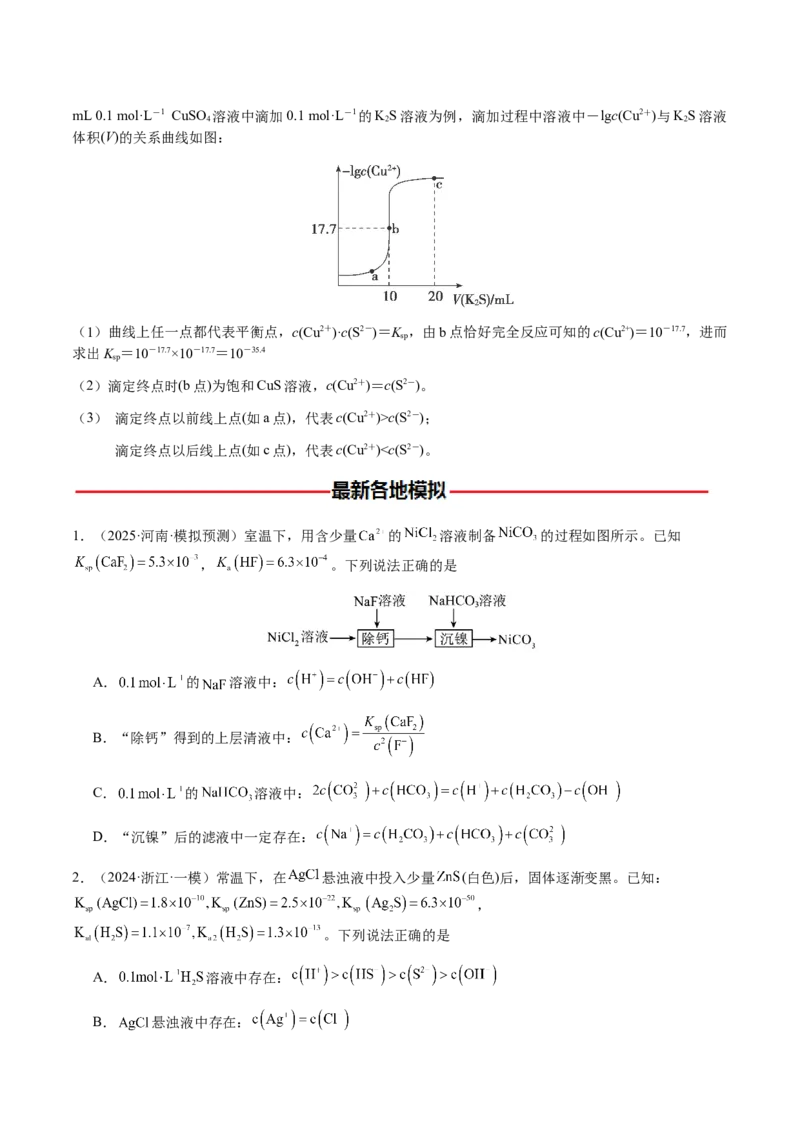
3.沉淀滴定曲线
沉淀滴定曲线是沉淀滴定过程中构成难溶电解质的离子浓度与滴定剂加入量之间的关系曲线,以向10mL 0.1 mol·L-1 CuSO 溶液中滴加0.1 mol·L-1的KS溶液为例,滴加过程中溶液中-lgc(Cu2+)与KS溶液
4 2 2
体积(V)的关系曲线如图:
(1)曲线上任一点都代表平衡点,c(Cu2+)·c(S2-)=K ,由b点恰好完全反应可知的c(Cu2+)=10-17.7,进而
sp
求出K =10-17.7×10-17.7=10-35.4
sp
(2)滴定终点时(b点)为饱和CuS溶液,c(Cu2+)=c(S2-)。
(3) 滴定终点以前线上点(如a点),代表c(Cu2+)>c(S2-);
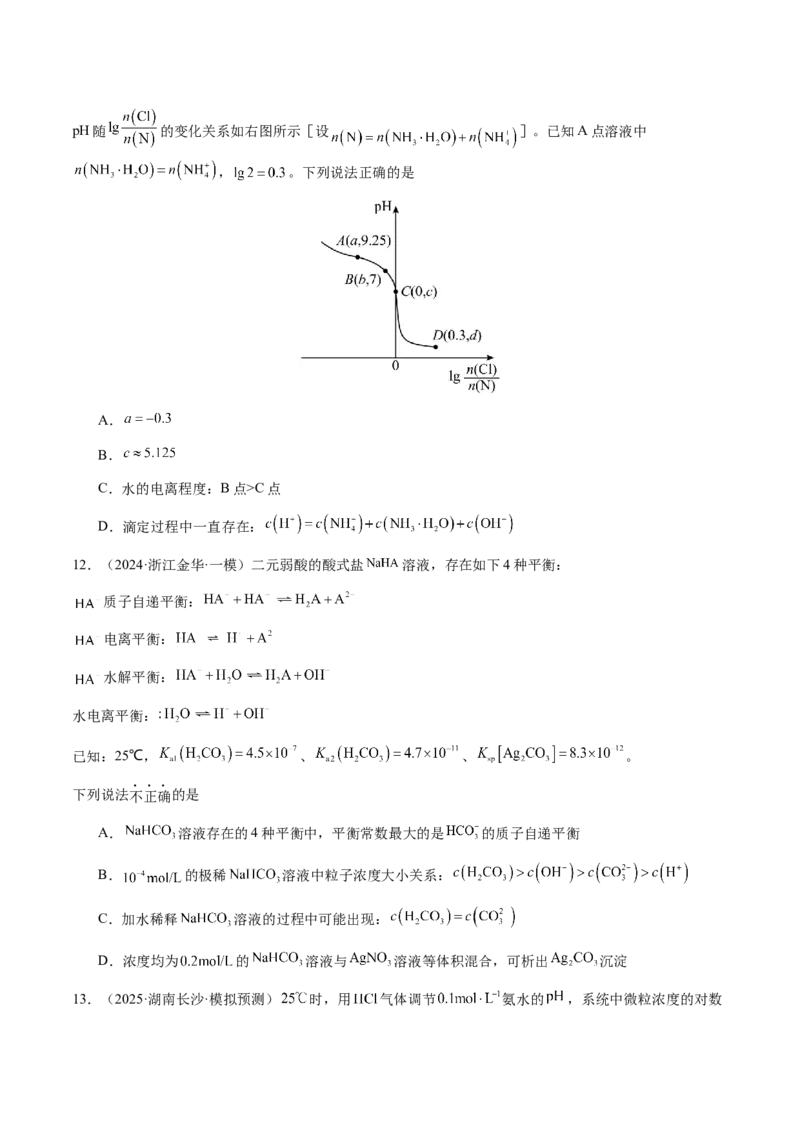
滴定终点以后线上点(如c点),代表c(Cu2+)C点
D.滴定过程中一直存在:
12.(2024·浙江金华·一模)二元弱酸的酸式盐 溶液,存在如下4种平衡:
质子自递平衡:
电离平衡:
水解平衡:
水电离平衡:
已知:25℃, 、 、 。
下列说法不正确的是
A. 溶液存在的4种平衡中,平衡常数最大的是 的质子自递平衡
B. 的极稀 溶液中粒子浓度大小关系:
C.加水稀释 溶液的过程中可能出现:
D.浓度均为 的 溶液与 溶液等体积混合,可析出 沉淀
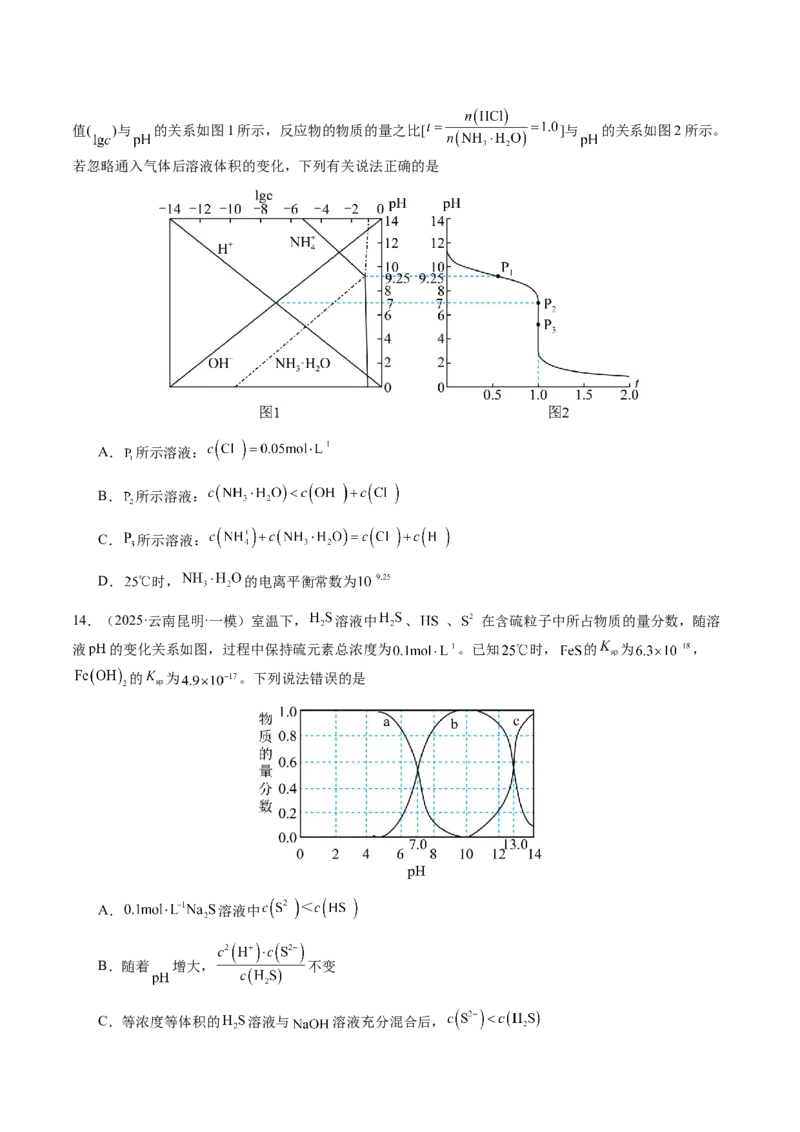
13.(2025·湖南长沙·模拟预测) 时,用 气体调节 氨水的 ,系统中微粒浓度的对数值( )与 的关系如图1所示,反应物的物质的量之比[ ]与 的关系如图2所示。
若忽略通入气体后溶液体积的变化,下列有关说法正确的是
A. 所示溶液:
B. 所示溶液:
C. 所示溶液:
D. 时, 的电离平衡常数为
14.(2025·云南昆明·一模)室温下, 溶液中 、 、 在含硫粒子中所占物质的量分数,随溶
液 的变化关系如图,过程中保持硫元素总浓度为 。已知 时, 的 为 ,
的 为 。下列说法错误的是
A. 溶液中
B.随着 增大, 不变
C.等浓度等体积的 溶液与 溶液充分混合后,D. 时,向溶液中滴入少量 溶液,先产生 沉淀
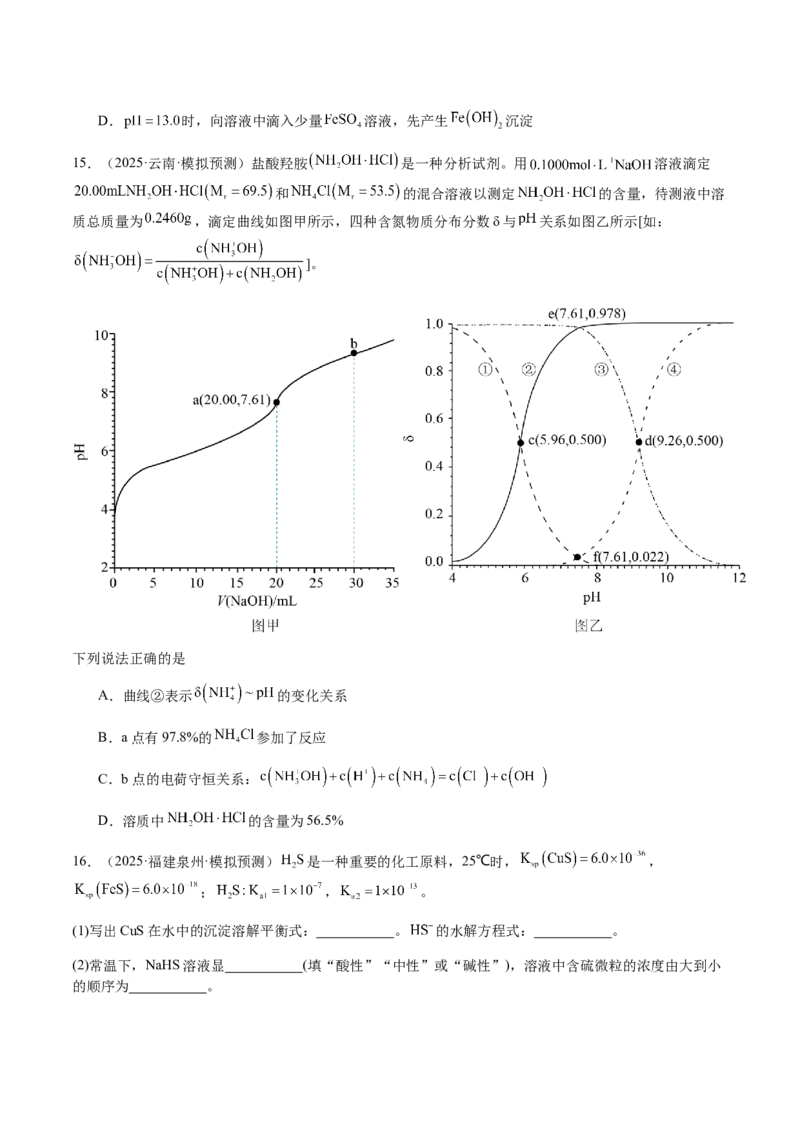
15.(2025·云南·模拟预测)盐酸羟胺 是一种分析试剂。用 溶液滴定
和 的混合溶液以测定 的含量,待测液中溶
质总质量为 ,滴定曲线如图甲所示,四种含氮物质分布分数δ与 关系如图乙所示[如:
]。
下列说法正确的是
A.曲线②表示 的变化关系
B.a点有97.8%的 参加了反应
C.b点的电荷守恒关系:
D.溶质中 的含量为56.5%
16.(2025·福建泉州·模拟预测) 是一种重要的化工原料,25℃时, ,
; , 。
(1)写出CuS在水中的沉淀溶解平衡式: 。 的水解方程式: 。
(2)常温下,NaHS溶液显 (填“酸性”“中性”或“碱性”),溶液中含硫微粒的浓度由大到小
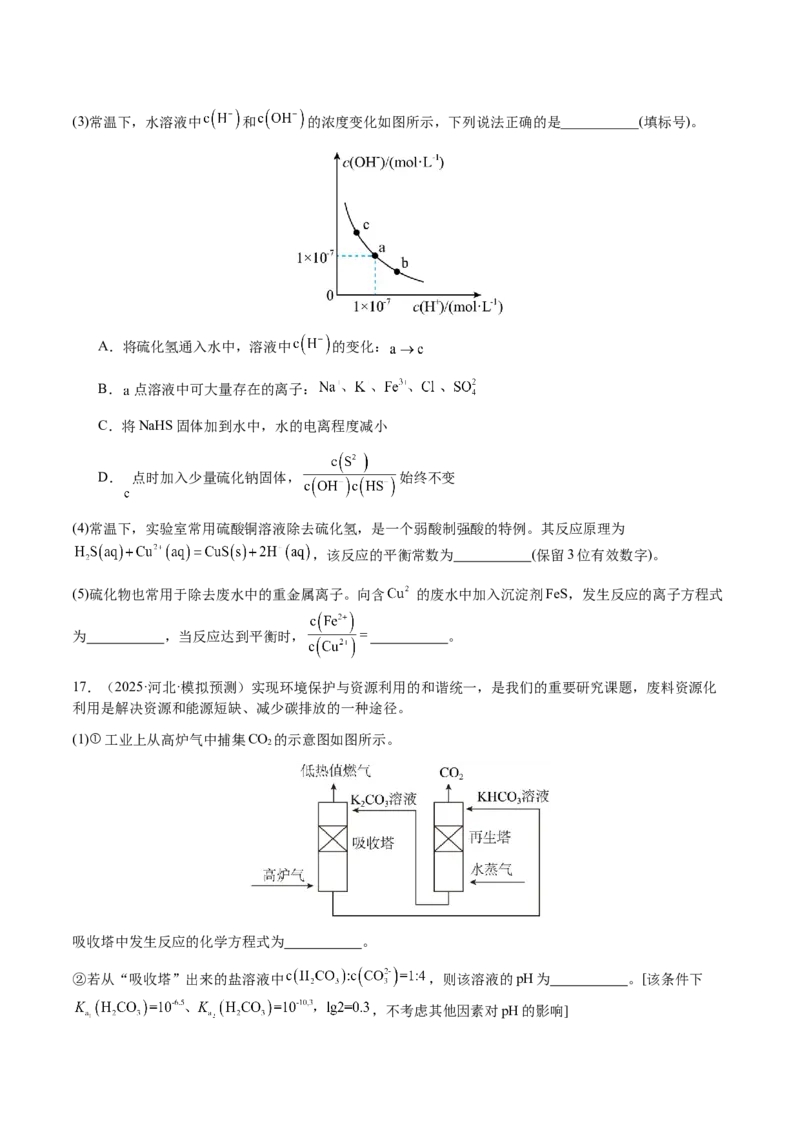
的顺序为 。(3)常温下,水溶液中 和 的浓度变化如图所示,下列说法正确的是___________(填标号)。
A.将硫化氢通入水中,溶液中 的变化:
B. 点溶液中可大量存在的离子:
C.将NaHS固体加到水中,水的电离程度减小
D. 点时加入少量硫化钠固体, 始终不变
(4)常温下,实验室常用硫酸铜溶液除去硫化氢,是一个弱酸制强酸的特例。其反应原理为
,该反应的平衡常数为 (保留3位有效数字)。
(5)硫化物也常用于除去废水中的重金属离子。向含 的废水中加入沉淀剂FeS,发生反应的离子方程式
为 ,当反应达到平衡时, 。
17.(2025·河北·模拟预测)实现环境保护与资源利用的和谐统一,是我们的重要研究课题,废料资源化
利用是解决资源和能源短缺、减少碳排放的一种途径。
(1)①工业上从高炉气中捕集CO 的示意图如图所示。
2
吸收塔中发生反应的化学方程式为 。
②若从“吸收塔”出来的盐溶液中 ,则该溶液的pH为 。[该条件下
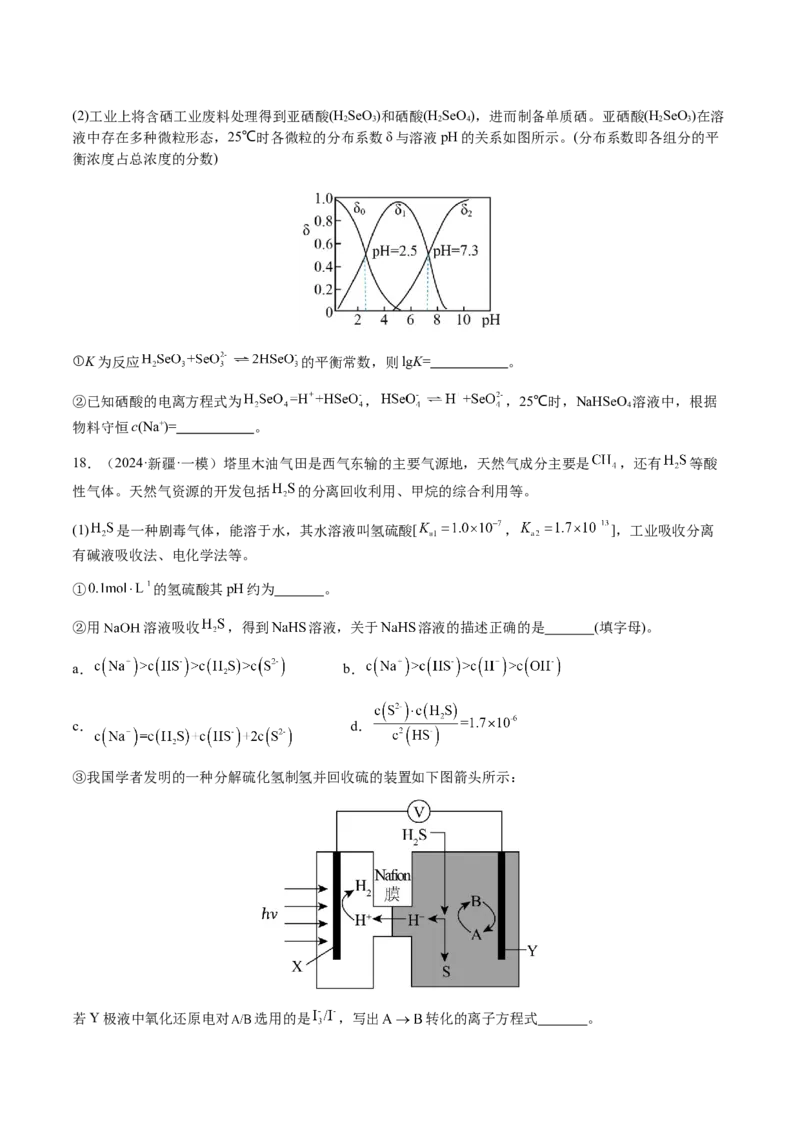
,不考虑其他因素对pH的影响](2)工业上将含硒工业废料处理得到亚硒酸(H SeO)和硒酸(H SeO),进而制备单质硒。亚硒酸(H SeO)在溶
2 3 2 4 2 3
液中存在多种微粒形态,25℃时各微粒的分布系数δ与溶液pH的关系如图所示。(分布系数即各组分的平
衡浓度占总浓度的分数)
①K为反应 的平衡常数,则lgK= 。
②已知硒酸的电离方程式为 , ,25℃时,NaHSeO 溶液中,根据
4
物料守恒c(Na+)= 。
18.(2024·新疆·一模)塔里木油气田是西气东输的主要气源地,天然气成分主要是 ,还有 等酸
性气体。天然气资源的开发包括 的分离回收利用、甲烷的综合利用等。
(1) 是一种剧毒气体,能溶于水,其水溶液叫氢硫酸[ , ],工业吸收分离
有碱液吸收法、电化学法等。
① 的氢硫酸其pH约为 。
②用 溶液吸收 ,得到 溶液,关于 溶液的描述正确的是 (填字母)。
a. b.
c. d.
③我国学者发明的一种分解硫化氢制氢并回收硫的装置如下图箭头所示:
若Y极液中氧化还原电对 选用的是 ,写出 转化的离子方程式 。19.(2025·广东·模拟预测) 能与 生成 ,常用于自然界中提取银或废液中回收银。
(1)已知Ag在第五周期,与Cu同族, 的价层电子排布式为 。 中 原子提供
孤电子对。
(2)向AgCl悬浊液中加入少量NaCN粉末,沉淀会逐渐溶解。此过程也可以表示为
,则此反应的 。
已知:
(3)常温下,向含有 溶液中加入 ,生成黑色沉淀,存在以下平衡:
ⅰ. ;
ⅱ. 。
①下列说法正确的是 (填标号)。
A.加入 时,反应ⅰ的平衡逆向移动,其平衡常数 减小
B.随着 增大, 减小
C.溶液中存在
D.加水稀释,反应ⅱ的平衡正向移动, 增大
②反应 (用 、 表示)。
(4)由于 有剧毒,生产中常改用 提取 。
已知: ;
。
向 溶液中加入 固体,得到澄清溶液(溶液体积不变),溶液中 、 、的物质的量分数 随 的变化如图所示。
已知:溶液中 。
①曲线 (填标号)表示 的变化。
②m点 约为 。
20.(2024·上海·三模)有机酸种类繁多。下表是一些有机酸的电离平衡常数 。
有机酸
;
电离平衡常数
(1)分析乙酸的官能团结构,可以使用以下仪器分析手段___________(不定项)。
A.原子吸收光谱 B.红外光谱 C.质谱 D.射线衍射
(2) 与少量 溶液反应的化学方程式是: 。
(3) 的电离平衡常数可能是___________。
A. B. C. D.
(4) 时,相同 的两种一元弱酸 与 溶液分别加水稀释,溶液 随溶液体积变
化的曲线如图所示。下列说法正确的是___________(不定项)。A.a点的 大于b点的
B.a点溶液的导电性小于b点溶液
C.同浓度的 与 溶液中, 大于
D. 是
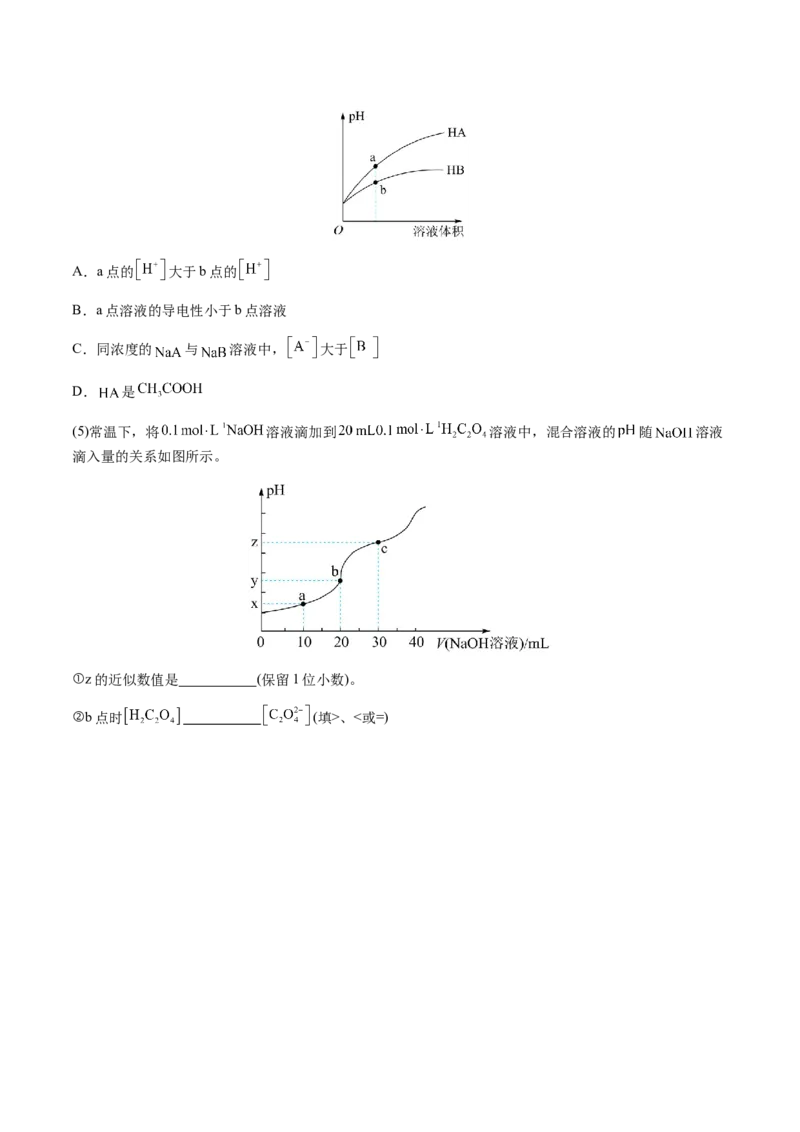
(5)常温下,将 溶液滴加到 溶液中,混合溶液的 随 溶液
滴入量的关系如图所示。
①z的近似数值是 (保留1位小数)。
②b点时 (填>、<或=)