文档内容
第2课时 共价晶体
发 展 目 标 体 系 构 建
1.借助共价晶体模型认识共价晶体的结构特点。
2.能够从化学键的特征,分析理解共价晶体的物理特性。
一、共价晶体的结构和性质
1.共价晶体的结构特点
(1)构成粒子及作用力
共价晶体
(2)空间结构:整块晶体是一个三维的共价键网状结构,不存在单个的小分子,是一个“巨分
子”。
2.共价晶体与物质的类别
物质种类 实例
某些非金属单质 晶体硼、晶体硅、晶体锗、金刚石等
某些非金属化合物 碳化硅(SiC)、氮化硅(Si N )、氮化硼(BN)等
3 4
某些氧化物 二氧化硅(SiO )等
2
3.共价晶体的熔、沸点
(1)共价晶体由于原子间以较强的共价键相结合,熔化时必需破坏共价键,而破坏它们需要很高
的温度,所以共价晶体具有很高的熔点。
(2)结构相似的共价晶体,原子半径越小,键长越短,键能越大,晶体的熔点越高。
微点拨:含有共价键的晶体都是共价晶体吗?
提示:共价晶体中都有共价键,但含有共价键的不一定是共价晶体。如 CO 、H O等分子晶体
2 2
中也含有共价键。
二、典型的共价晶体
1.金刚石
(1)碳原子采取 sp 3 杂化,C—C—C夹角为 109°28 ′ 。
(2)每个碳原子与周围紧邻的4 个碳原子以共价键结合成正四面体结构,向空间伸展形成空间网
状结构。
(3)最小碳环由6 个碳原子组成,且最小环上有 4个碳原子在同一平面内;每个碳原子被 12个六元环共用。
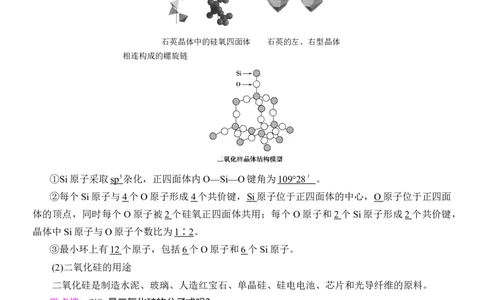
2.二氧化硅晶体
(1)二氧化硅的结构
二氧化硅是自然界含量最高的固态二元氧化物,有多种结构,最常见的是低温石英(αSiO )。低
2
温石英的结构中有顶角相连的硅氧四面体形成螺旋上升的长链,没有封闭的环状结构,这一结构
决定了它具有手性。
石英晶体中的硅氧四面体 石英的左、右型晶体
相连构成的螺旋链
①Si原子采取 sp 3 杂化,正四面体内O—Si—O键角为 109°28 ′ 。
②每个Si原子与4 个O原子形成4 个共价键,Si 原子位于正四面体的中心,O 原子位于正四面
体的顶点,同时每个O原子被2 个硅氧正四面体共用;每个 O原子和2 个Si原子形成2 个共价键,
晶体中Si原子与O原子个数比为 1 ∶ 2 。
③最小环上有12 个原子,包括6 个O原子和6 个Si原子。
(2)二氧化硅的用途
二氧化硅是制造水泥、玻璃、人造红宝石、单晶硅、硅电电池、芯片和光导纤维的原料。
微点拨:SiO 是二氧化硅的分子式吗?
2
提示:二氧化硅为共价晶体,晶体中不存在单个分子,其化学式为 Si与O的最简个数比,而
不是分子式。
1.判断正误(对的在括号内打“√”,错的在括号内打“×”。)
(1)凡是由原子构成的晶体都是共价晶体 (×)
(2)CO 和SiO 中化学键类型相同,晶体类型也相同 (×)
2 2
(3)1 mol SiO 晶体中含4 mol Si—O键 (×)
2
(4)由于共价键的键能远大于分子间作用力,故共价晶体的熔点比分子晶体高2.下列有关共价晶体的叙述错误的是( )
A.共价晶体中,只存在共价键
B.共价晶体具有空间网状结构
C.共价晶体中不存在独立的分子
D.共价晶体熔化时不破坏共价键
D [A项,共价晶体中原子之间通过共价键相连;B项,共价晶体是相邻原子之间通过共价键
结合而成的空间网状结构;C项,共价晶体是由原子以共价键相结合形成的,不存在独立的分子;
D项,共价晶体中原子是通过共价键连接的,熔化时需要破坏共价键。]
3.有下列物质:①水晶 ②冰醋酸 ③氧化钙 ④白磷 ⑤晶体氩 ⑥氢氧化钠 ⑦铝 ⑧
金刚石 ⑨过氧化钠 ⑩碳化钙 ⑪碳化硅 ⑫干冰 ⑬过氧化氢。
根据要求填空:
(1)属于共价晶体的化合物是________(填序号,下同)。
(2)直接由原子构成的晶体是________。
(3)直接由原子构成的分子晶体是________。
(4)由极性分子构成的晶体是________,属于分子晶体的单质是________。
[解析] 属于共价晶体的是金刚石、碳化硅和水晶;属于分子晶体的有晶体氩(无化学键)、白
磷(非极性分子)、干冰(由极性键构成的非极性分子)、过氧化氢和冰醋酸(由极性键和非极性键构成
的极性分子)。
[答案] (1)①⑪ (2)①⑤⑧⑪ (3)⑤ (4)②⑬ ④⑤
共价晶体与分子晶体的比较
科学研究揭示,30亿年前,在地壳下200 km左右的地幔中处在高温、高压岩浆中的碳元素,
逐渐形成了具有正四面体结构的金刚石。火山爆发时,金刚石夹在岩浆中上升到接近地表时冷却,
形成含有少量金刚石的原生矿床。金刚石具有诸多不同凡响的优良性质:熔点高(3 350 ℃),不导
电,硬度极高。而干冰容易气化,碘晶体容易升华。
(1)分子晶体和共价晶体的构成粒子相同吗?
提示:不同。分子晶体为分子,共价晶体为原子。
(2)分子晶体和共价晶体受热熔化时克服粒子间作用力相同吗?
提示:不同,前者为分子间作用力,后者为共价键。
1.共价晶体与分子晶体的结构特征
(1)共价晶体的结构特征在共价晶体中,各原子均以共价键结合,因为共价键有方向性和饱和性,所以中心原子周围
的原子数目是有限的,原子不采取密堆积方式。
(2)分子晶体的结构特征
①分子间不存在氢键的分子晶体,由于范德华力没有方向性和饱和性,所以分子尽可能采取密
堆积方式。
②分子间存在氢键的分子晶体,由于氢键具有方向性和饱和性,所以分子不能采取密堆积方式。
2.共价晶体与分子晶体熔、沸点高低的比较
(1)晶体类型不同:共价晶体>分子晶体
理由:共价晶体的熔、沸点与共价键有关,分子晶体的熔、沸点与分子间作用力有关。共价
键的作用力远大于分子间作用力。
(2)晶体类型相同
①共价晶体
一般来说,对结构相似的共价晶体来说,键长越短,键能越大,晶体的熔、沸点越高。例如:
金刚石>二氧化硅>碳化硅>晶体硅。
②分子晶体
a.若分子间有氢键,则分子间作用力比结构相似的同类晶体大,故熔、沸点较高。如 HF>
HI;NH >PH ;H O>H Te。
3 3 2 2
b.组成和结构相似的分子晶体,一般相对分子质量越大,范德华力越大,熔、沸点越高。如
I >Br >Cl >F ;SnH >GeH >SiH >CH 。
2 2 2 2 4 4 4 4
c.组成和结构不相似的物质(相对分子质量接近),分子的极性越大,范德华力越大,熔、沸点
越高。如CO>N 。
2
d.同类别的同分异构体,支链越多,熔、沸点越低。如正戊烷>异戊烷>新戊烷。
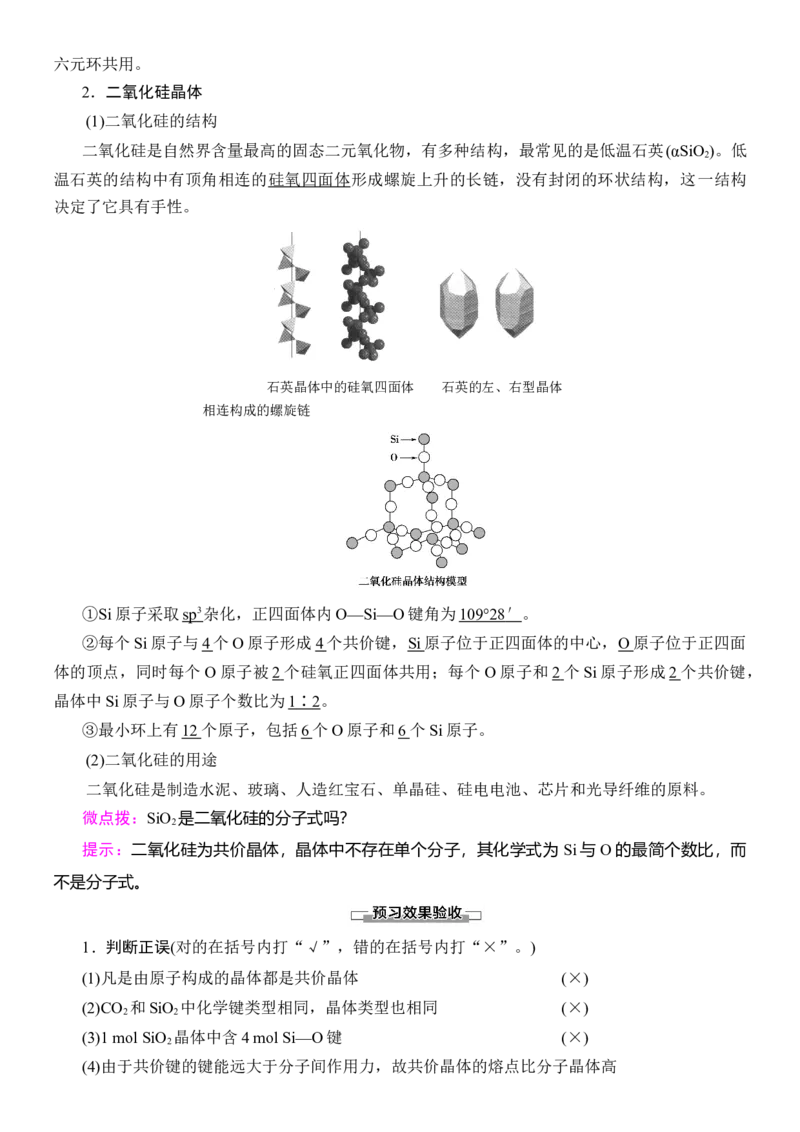
1.下表是某些共价晶体的熔点和硬度,分析表中的数据,判断下列叙述正确的是( )
共价晶体 金刚石 氮化硼 碳化硅 石英 硅 锗
熔点/℃ 3 900 3 000 2 700 1 710 1 410 1 211
硬度 10 9.5 9.5 7 6.5 6.0
① 构成共价晶体的原子种类越多,晶体的熔点越高
②构成共价晶体的原子间的共价键的键能越大,晶体的熔点越高
③构成共价晶体的原子半径越大,晶体的硬度越大
④构成共价晶体的原子半径越小,晶体的硬度越大
A.①② B.③④ C.①③ D.②④
D [共价晶体的熔、沸点和硬度等物理性质取决于晶体内的共价键,构成共价晶体的原子半径
越小,键长越短,键能越大,对应共价晶体的熔、沸点越高,硬度越大。]
2.下列晶体性质的比较中不正确的是( )A.熔点:金刚石>碳化硅>晶体硅
B.沸点:NH >PH
3 3
C.硬度:白磷>冰>二氧化硅
D.熔点:SiI >SiBr >SiCl
4 4 4
C [A项中三种物质都是共价晶体,因原子半径 r(C)C—Si>Si—Si。键能越大,共价晶体的熔点越高,A项正确;因为NH 分子间存在
3
氢键,所以NH 的沸点大于PH 的沸点,B项正确;二氧化硅是共价晶体,硬度很大,白磷和冰都
3 3
是分子晶体,硬度较小,C项错误;四卤化硅为分子晶体,它们的组成和结构相似,分子间不存在
氢键,故相对分子质量越大,熔点越高,D项正确。]
比较共价晶体和分子晶体熔点高低的基本思路
认识典型共价晶体的结构
(1)分析金刚石、二氧化硅的晶体结构模型,判断共价晶体的化学式是否可以代表其分子式?
提示:不能。因为共价晶体是一个三维的网状结构,无小分子存在。
(2)以金刚石为例,说明共价晶体的微观结构与分子晶体有哪些不同?
提示:①构成粒子不同,共价晶体中只存在原子,没有小分子。②相互作用不同,共价晶体中
存在的是共价键。
(3)分析二氧化硅晶体结构模型,判断晶体中最小的环有多少个原子?1 mol SiO 中含有多少摩
2
尔Si—O键?
提示:SiO 晶体中最小环上有12个原子。1 mol SiO 中含有4 mol Si—O。
2 2
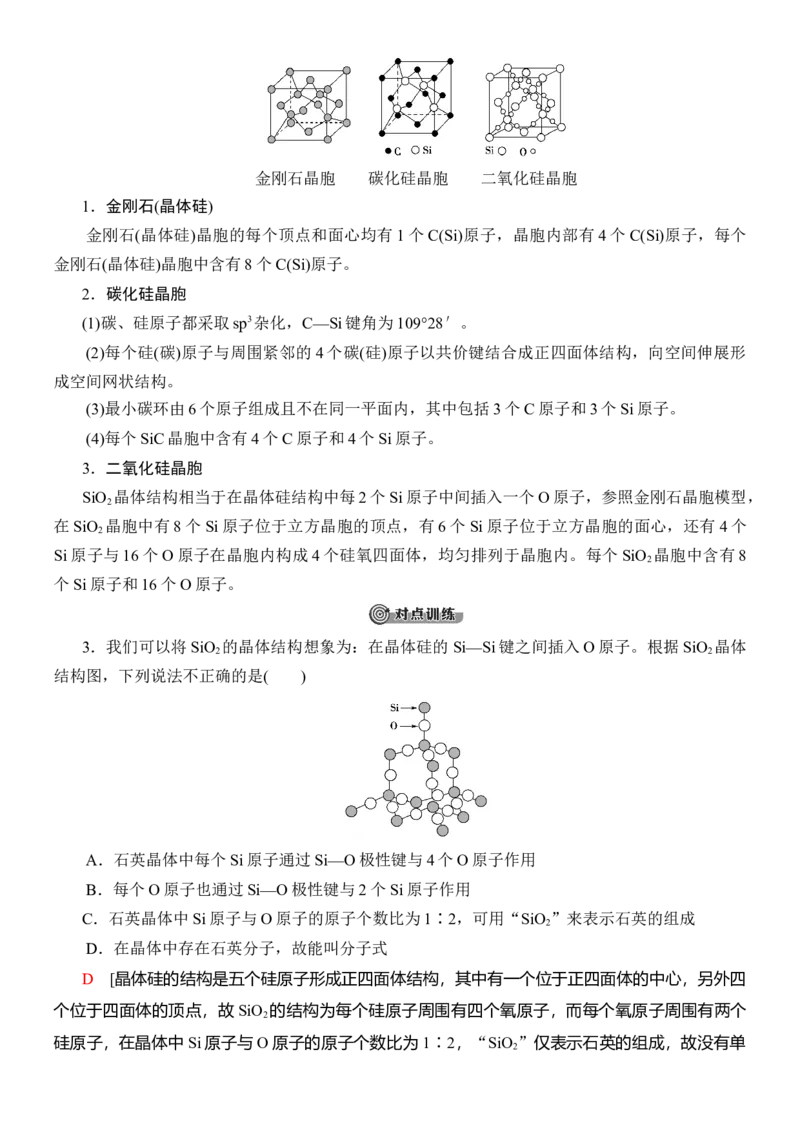
金刚石(晶体硅)、碳化硅、二氧化硅的晶胞金刚石晶胞 碳化硅晶胞 二氧化硅晶胞
1.金刚石(晶体硅)
金刚石(晶体硅)晶胞的每个顶点和面心均有1个C(Si)原子,晶胞内部有4个C(Si)原子,每个
金刚石(晶体硅)晶胞中含有8个C(Si)原子。
2.碳化硅晶胞
(1)碳、硅原子都采取sp3杂化,C—Si键角为109°28′。
(2)每个硅(碳)原子与周围紧邻的4个碳(硅)原子以共价键结合成正四面体结构,向空间伸展形
成空间网状结构。
(3)最小碳环由6个原子组成且不在同一平面内,其中包括3个C原子和3个Si原子。
(4)每个SiC晶胞中含有4个C原子和4个Si原子。
3.二氧化硅晶胞
SiO 晶体结构相当于在晶体硅结构中每2个Si原子中间插入一个O原子,参照金刚石晶胞模型,
2
在SiO 晶胞中有8个Si原子位于立方晶胞的顶点,有6个Si原子位于立方晶胞的面心,还有4个
2
Si原子与16个O原子在晶胞内构成4个硅氧四面体,均匀排列于晶胞内。每个SiO 晶胞中含有8
2
个Si原子和16个O原子。
3.我们可以将SiO 的晶体结构想象为:在晶体硅的Si—Si键之间插入O原子。根据SiO 晶体
2 2
结构图,下列说法不正确的是( )
A.石英晶体中每个Si原子通过Si—O极性键与4个O原子作用
B.每个O原子也通过Si—O极性键与2个Si原子作用
C.石英晶体中Si原子与O原子的原子个数比为1∶2,可用“SiO ”来表示石英的组成
2
D.在晶体中存在石英分子,故能叫分子式
D [晶体硅的结构是五个硅原子形成正四面体结构,其中有一个位于正四面体的中心,另外四
个位于四面体的顶点,故SiO 的结构为每个硅原子周围有四个氧原子,而每个氧原子周围有两个
2
硅原子,在晶体中Si原子与O原子的原子个数比为1∶2,“SiO ”仅表示石英的组成,故没有单
2个的SiO 分子。]
2
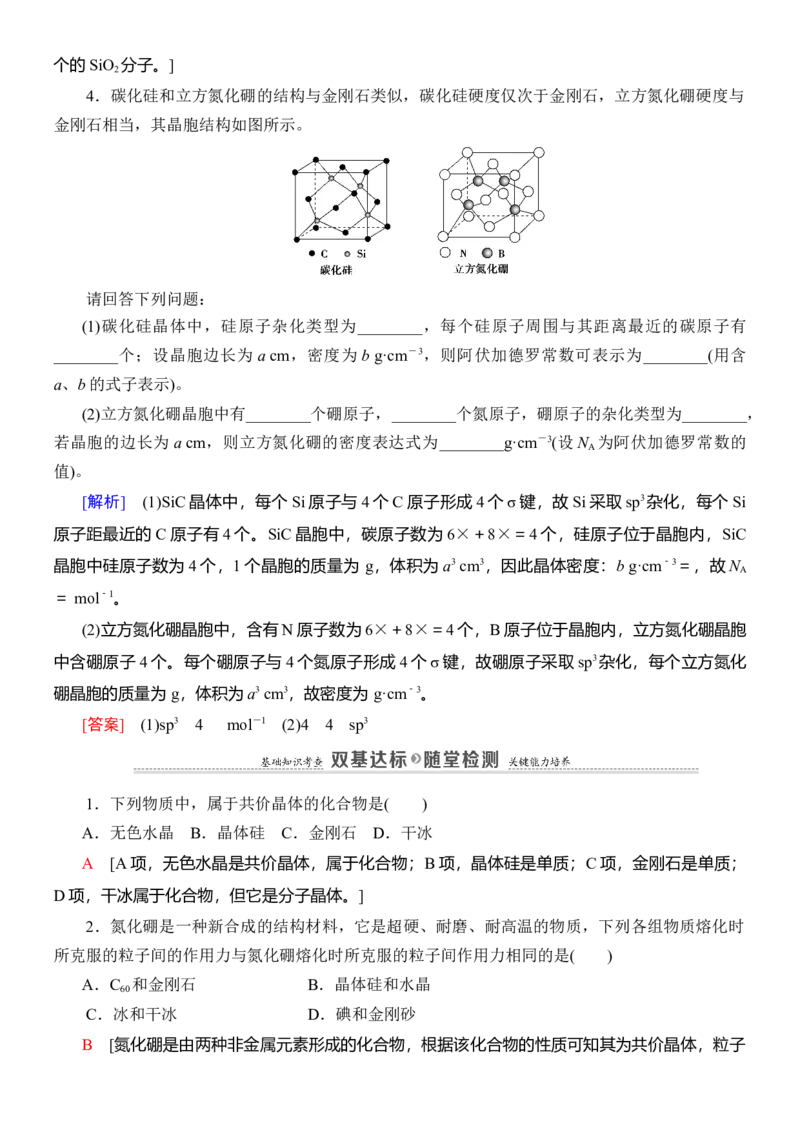
4.碳化硅和立方氮化硼的结构与金刚石类似,碳化硅硬度仅次于金刚石,立方氮化硼硬度与
金刚石相当,其晶胞结构如图所示。
请回答下列问题:
(1)碳化硅晶体中,硅原子杂化类型为________,每个硅原子周围与其距离最近的碳原子有
________个;设晶胞边长为 a cm,密度为 b g·cm-3,则阿伏加德罗常数可表示为________(用含
a、b的式子表示)。
(2)立方氮化硼晶胞中有________个硼原子,________个氮原子,硼原子的杂化类型为________,
若晶胞的边长为 a cm,则立方氮化硼的密度表达式为________g·cm-3(设N 为阿伏加德罗常数的
A
值)。
[解析] (1)SiC晶体中,每个Si原子与4个C原子形成4个σ键,故Si采取sp3杂化,每个Si
原子距最近的C原子有4个。SiC晶胞中,碳原子数为 6×+8×=4个,硅原子位于晶胞内,SiC
晶胞中硅原子数为4个,1个晶胞的质量为 g,体积为a3 cm3,因此晶体密度:b g·cm-3=,故N
A
= mol-1。
(2)立方氮化硼晶胞中,含有N原子数为6×+8×=4个,B原子位于晶胞内,立方氮化硼晶胞
中含硼原子4个。每个硼原子与4个氮原子形成4个σ键,故硼原子采取sp3杂化,每个立方氮化
硼晶胞的质量为 g,体积为a3 cm3,故密度为 g·cm-3。
[答案] (1)sp3 4 mol-1 (2)4 4 sp3
1.下列物质中,属于共价晶体的化合物是( )
A.无色水晶 B.晶体硅 C.金刚石 D.干冰
A [A项,无色水晶是共价晶体,属于化合物;B项,晶体硅是单质;C项,金刚石是单质;
D项,干冰属于化合物,但它是分子晶体。]
2.氮化硼是一种新合成的结构材料,它是超硬、耐磨、耐高温的物质,下列各组物质熔化时
所克服的粒子间的作用力与氮化硼熔化时所克服的粒子间作用力相同的是( )
A.C 和金刚石 B.晶体硅和水晶
60
C.冰和干冰 D.碘和金刚砂
B [氮化硼是由两种非金属元素形成的化合物,根据该化合物的性质可知其为共价晶体,粒子间作用力为共价键。C 和金刚石熔化时分别克服的是分子间作用力和共价键,A项错误;冰和干
60
冰熔化时均克服的是分子间作用力,C项错误;碘和金刚砂熔化时分别克服的是分子间作用力和共
价键,D项错误。]
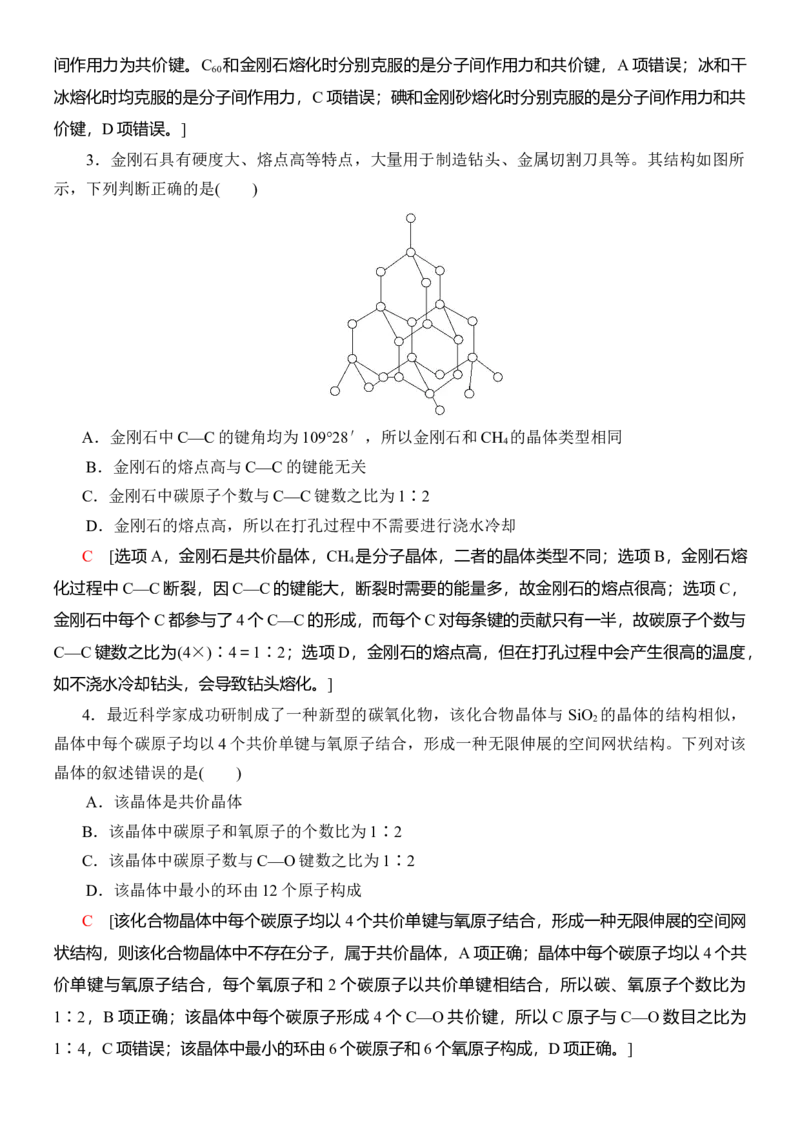
3.金刚石具有硬度大、熔点高等特点,大量用于制造钻头、金属切割刀具等。其结构如图所
示,下列判断正确的是( )
A.金刚石中C—C的键角均为109°28′,所以金刚石和CH 的晶体类型相同
4
B.金刚石的熔点高与C—C的键能无关
C.金刚石中碳原子个数与C—C键数之比为1∶2
D.金刚石的熔点高,所以在打孔过程中不需要进行浇水冷却
C [选项A,金刚石是共价晶体,CH 是分子晶体,二者的晶体类型不同;选项B,金刚石熔
4
化过程中C—C断裂,因C—C的键能大,断裂时需要的能量多,故金刚石的熔点很高;选项 C,
金刚石中每个C都参与了4个C—C的形成,而每个C对每条键的贡献只有一半,故碳原子个数与
C—C键数之比为(4×)∶4=1∶2;选项D,金刚石的熔点高,但在打孔过程中会产生很高的温度,
如不浇水冷却钻头,会导致钻头熔化。]
4.最近科学家成功研制成了一种新型的碳氧化物,该化合物晶体与 SiO 的晶体的结构相似,
2
晶体中每个碳原子均以4个共价单键与氧原子结合,形成一种无限伸展的空间网状结构。下列对该
晶体的叙述错误的是( )
A.该晶体是共价晶体
B.该晶体中碳原子和氧原子的个数比为1∶2
C.该晶体中碳原子数与C—O键数之比为1∶2
D.该晶体中最小的环由12个原子构成
C [该化合物晶体中每个碳原子均以4个共价单键与氧原子结合,形成一种无限伸展的空间网
状结构,则该化合物晶体中不存在分子,属于共价晶体,A项正确;晶体中每个碳原子均以4个共
价单键与氧原子结合,每个氧原子和 2个碳原子以共价单键相结合,所以碳、氧原子个数比为
1∶2,B项正确;该晶体中每个碳原子形成 4个C—O共价键,所以 C原子与C—O数目之比为
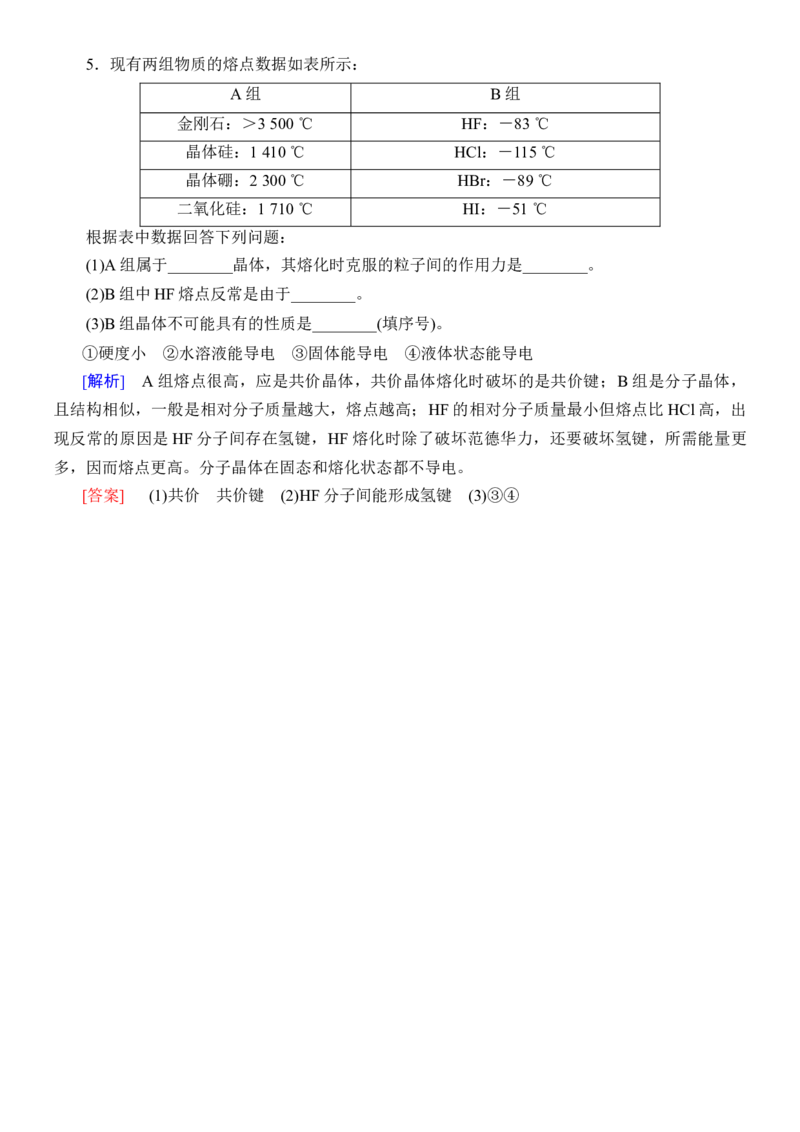
1∶4,C项错误;该晶体中最小的环由6个碳原子和6个氧原子构成,D项正确。]5.现有两组物质的熔点数据如表所示:
A组 B组
金刚石:>3 500 ℃ HF:-83 ℃
晶体硅:1 410 ℃ HCl:-115 ℃
晶体硼:2 300 ℃ HBr:-89 ℃
二氧化硅:1 710 ℃ HI:-51 ℃
根据表中数据回答下列问题:
(1)A组属于________晶体,其熔化时克服的粒子间的作用力是________。
(2)B组中HF熔点反常是由于________。
(3)B组晶体不可能具有的性质是________(填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④液体状态能导电
[解析] A组熔点很高,应是共价晶体,共价晶体熔化时破坏的是共价键;B组是分子晶体,
且结构相似,一般是相对分子质量越大,熔点越高;HF的相对分子质量最小但熔点比HCl高,出
现反常的原因是HF分子间存在氢键,HF熔化时除了破坏范德华力,还要破坏氢键,所需能量更
多,因而熔点更高。分子晶体在固态和熔化状态都不导电。
[答案] (1)共价 共价键 (2)HF分子间能形成氢键 (3)③④