文档内容
第二节 分子晶体与共价晶体
第1课时 分子晶体
发 展 目 标 体 系 构 建
1.借助分子晶体模型认识分子晶体的结构特点。
2.能够从范德华力、氢键的特征,分析理解分子晶体
的物理特性。
一、分子晶体及其结构特点
1.概念
只含分子的晶体。
2.粒子间的作用
分子晶体中相邻的分子间以分子间作用力相互吸引。
3.常见分子晶体及物质类别
物质种类 实例
所有非金属氢化物 H O、NH 、CH 等
2 3 4
部分非金属单质 卤素(X )、O 、N 、白磷(P )、硫(S )等
2 2 2 4 8
部分非金属氧化物 CO 、P O 、SO 、SO 等
2 4 10 2 3
几乎所有的酸 HNO 、H SO 、H PO 、H SiO 等
3 2 4 3 4 2 3
绝大多数有机物 苯、乙醇、乙酸、乙酸乙酯等
4.分子晶体的常见堆积方式
分子间作用力 堆积方式 实例
分子采用密堆积,
范德华力 如C 、干冰、I 、O
60 2 2
每个分子周围有12 个紧邻的分子
分子不采用密堆积,
范德华力、氢键 如HF、NH 、冰
3
每个分子周围紧邻的分子少于12个
二、两种典型的分子晶体的组成和结构
1.冰(1)水分子之间的主要作用力是氢键,当然也存在范德华力。
(2)氢键有方向性,它的存在迫使在四面体中心的每个水分子与四面体顶角方向的4 个相邻水分
子互相吸引。
2.干冰
(1)干冰中的CO 分子间只存在范德华力,不存在氢键。
2
(2)①每个晶胞中有4 个CO 分子,12 个原子。
2
②每个CO 分子周围等距离紧邻的CO 分子数为12 个。
2 2
三、分子晶体的物理性质
1.物理特性
(1)分子晶体的熔、沸点较低,密度较小,硬度较小,较易熔化和挥发。
(2)一般是绝缘体,熔融状态也不导电。
(3)溶解性符合“相似相溶规律”。
2.分子晶体熔、沸点高低的比较规律
(1)分子晶体中分子间作用力越大,物质熔、沸点越高,反之越低。
(2)具有氢键的分子晶体,熔、沸点反常高。
1.判断正误(对的在括号内打“√”,错的在括号内打“×”。)
(1)分子晶体中只存在分子间作用力 (×)
(2)分子晶体熔化时共价键断裂 (×)
(3)分子晶体中氢键越强,分子越稳定 (×)
(4)分子晶体中一定含有分子间作用力,不一定含有化学键 (√)
2.下列各组物质各自形成晶体,均属于分子晶体的化合物是( )
A.NH 、P 、C H B.PCl 、CO 、H SO
3 4 10 8 3 2 2 4
C.SO 、SiO 、P O D.CCl 、H O、Na O
2 2 2 5 4 2 2 2
B [A中,P (白磷)为单质,不是化合物;C中,SiO 为共价晶体;D中,Na O 是离子化合物、
4 2 2 2离子晶体。]
3.(1)CO 能与金属 Fe 形成 Fe(CO) ,该化合物熔点为 253 K,沸点为 376 K,其固体属于
5
________晶体。
(2)F 与其他卤素单质反应可以形成卤素互化物,如 ClF 、BrF ,常温下它们都是易挥发的液体。
2 3 3
ClF 的熔、沸点比BrF 的________(填“高”或“低”)。
3 3
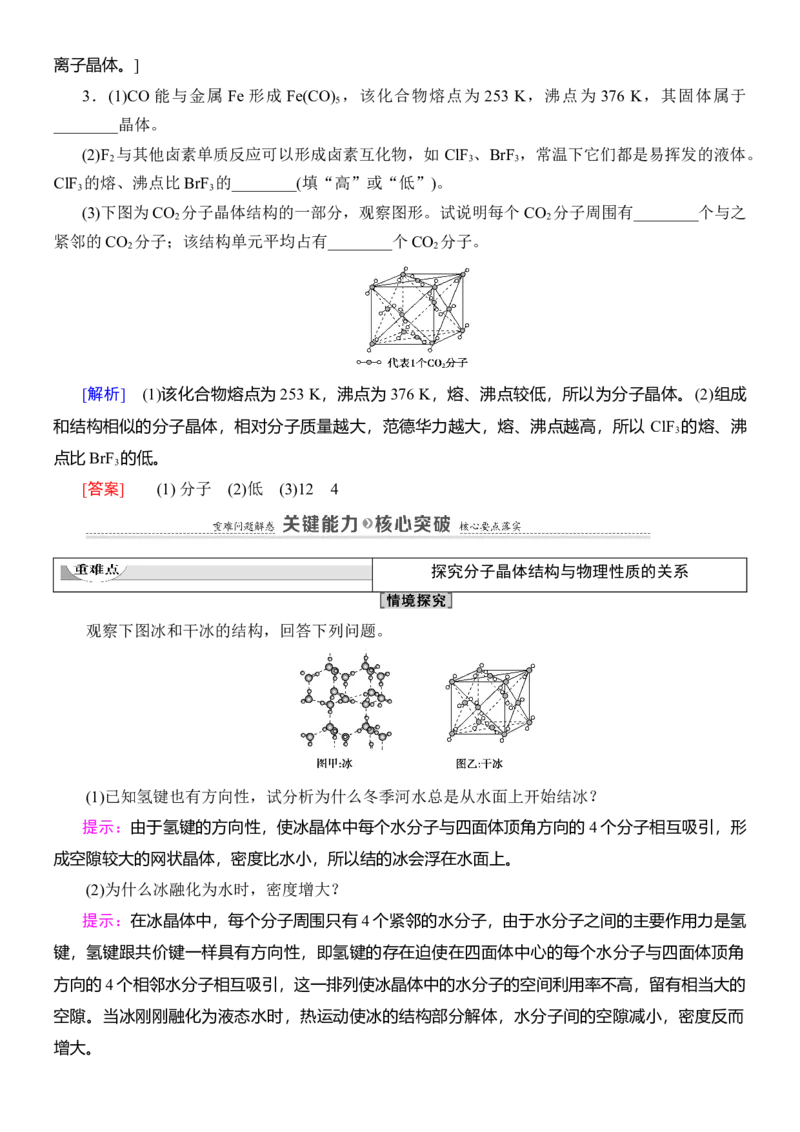
(3)下图为CO 分子晶体结构的一部分,观察图形。试说明每个 CO 分子周围有________个与之
2 2
紧邻的CO 分子;该结构单元平均占有________个CO 分子。
2 2
[解析] (1)该化合物熔点为253 K,沸点为376 K,熔、沸点较低,所以为分子晶体。(2)组成
和结构相似的分子晶体,相对分子质量越大,范德华力越大,熔、沸点越高,所以 ClF 的熔、沸
3
点比BrF 的低。
3
[答案] (1) 分子 (2)低 (3)12 4
探究分子晶体结构与物理性质的关系
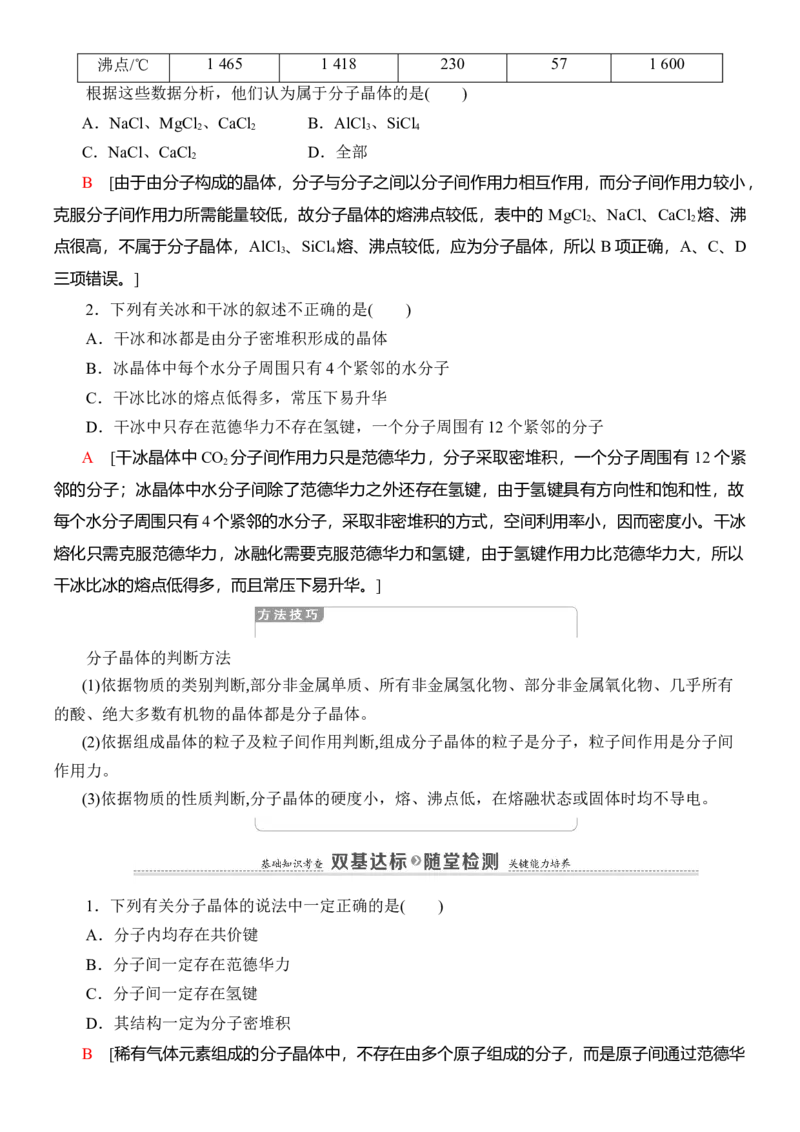
观察下图冰和干冰的结构,回答下列问题。
(1)已知氢键也有方向性,试分析为什么冬季河水总是从水面上开始结冰?
提示:由于氢键的方向性,使冰晶体中每个水分子与四面体顶角方向的4个分子相互吸引,形
成空隙较大的网状晶体,密度比水小,所以结的冰会浮在水面上。
(2)为什么冰融化为水时,密度增大?
提示:在冰晶体中,每个分子周围只有4个紧邻的水分子,由于水分子之间的主要作用力是氢
键,氢键跟共价键一样具有方向性,即氢键的存在迫使在四面体中心的每个水分子与四面体顶角
方向的4个相邻水分子相互吸引,这一排列使冰晶体中的水分子的空间利用率不高,留有相当大的
空隙。当冰刚刚融化为液态水时,热运动使冰的结构部分解体,水分子间的空隙减小,密度反而
增大。(3)为什么干冰的熔沸点比冰低而密度却比冰大?
提示:由于冰中除了范德华力外还有氢键作用,破坏分子间作用力较难,所以熔沸点比干冰高。
由于水分子间氢键的方向性,导致冰晶体不具有分子密堆积特征,晶体中有相当大的空隙,所以
相同状况下冰体积较大。由于CO 分子的相对分子质量>H O分子的相对分子质量,所以干冰的密
2 2
度大。
(4)干冰升华过程中破坏共价键吗?
提示:干冰升华的过程中破坏分子间作用力,不破坏共价键。
1.分子晶体的物理性质
(1)分子晶体具有较低的熔、沸点和较小的硬度。分子晶体熔化时要破坏分子间作用力,由
于分子间作用力很弱,所以分子晶体的熔、沸点一般较低,部分分子晶体易升华(如干冰、碘、红
磷、萘等),且硬度较小。
(2)分子晶体不导电。分子晶体在固态和熔融状态下均不存在自由移动的离子或自由电子,因
而分子晶体在固态和熔融状态下都不能导电。有些分子晶体的水溶液能导电,如HI、乙酸等。
(3)分子晶体的溶解性一般符合“相似相溶”规律,即极性分子易溶于极性溶剂,非极性分子易
溶于非极性溶剂。
如:H O是极性溶剂,SO 、H S、HBr等都是极性分子,它们在水中的溶解度比 N 、O 、CH
2 2 2 2 2 4
等非极性分子在水中的溶解度大。苯、CCl 是非极性溶剂,则Br 、I 等非极性分子易溶于其中,
4 2 2
而水则不溶于苯和CCl 中。
4
2.分子晶体熔、沸点比较规律
(1)少数主要以氢键作用形成的分子晶体,比一般的分子晶体的熔、沸点高,如含有 H—F、H
—O、H—N等共价键的分子间可以形成氢键,所以 HF、H O、NH 、醇、羧酸等物质的熔、沸点
2 3
相对较高。
(2)组成与结构相似,分子之间不含氢键而只利用范德华力形成的分子晶体,随着相对分子质量
的增大,物质的熔、沸点逐渐升高。例如,常温下Cl 呈气态,Br 呈液态,而I 呈固态;CO 呈气
2 2 2 2
态,CS 呈液态。
2
(3)相对分子质量相等或相近的极性分子构成的分子晶体,其熔、沸点一般比非极性分子构成的
分子晶体的熔、沸点高,如CO的熔、沸点比N 的熔、沸点高。
2
(4)有机物中组成和结构相似且不存在氢键的同分异构体,相对分子质量相同,一般支链越多
分子间的相互作用力越弱,熔、沸点越低,如熔、沸点:正戊烷>异戊烷>新戊烷。
1.某化学兴趣小组在学习分子晶体后,查阅了几种氯化物的熔、沸点,记录如下:
NaCl MgCl AlCl SiCl CaCl
2 3 4 2
熔点/℃ 801 712 190 -68 782沸点/℃ 1 465 1 418 230 57 1 600
根据这些数据分析,他们认为属于分子晶体的是( )
A.NaCl、MgCl 、CaCl B.AlCl 、SiCl
2 2 3 4
C.NaCl、CaCl D.全部
2
B [由于由分子构成的晶体,分子与分子之间以分子间作用力相互作用,而分子间作用力较小,
克服分子间作用力所需能量较低,故分子晶体的熔沸点较低,表中的 MgCl 、NaCl、CaCl 熔、沸
2 2
点很高,不属于分子晶体,AlCl 、SiCl 熔、沸点较低,应为分子晶体,所以 B项正确,A、C、D
3 4
三项错误。]
2.下列有关冰和干冰的叙述不正确的是( )
A.干冰和冰都是由分子密堆积形成的晶体
B.冰晶体中每个水分子周围只有4个紧邻的水分子
C.干冰比冰的熔点低得多,常压下易升华
D.干冰中只存在范德华力不存在氢键,一个分子周围有12个紧邻的分子
A [干冰晶体中CO 分子间作用力只是范德华力,分子采取密堆积,一个分子周围有 12个紧
2
邻的分子;冰晶体中水分子间除了范德华力之外还存在氢键,由于氢键具有方向性和饱和性,故
每个水分子周围只有4个紧邻的水分子,采取非密堆积的方式,空间利用率小,因而密度小。干冰
熔化只需克服范德华力,冰融化需要克服范德华力和氢键,由于氢键作用力比范德华力大,所以
干冰比冰的熔点低得多,而且常压下易升华。]
分子晶体的判断方法
1依据物质的类别判断,部分非金属单质、所有非金属氢化物、部分非金属氧化物、几乎所有
的酸、绝大多数有机物的晶体都是分子晶体。
2依据组成晶体的粒子及粒子间作用判断,组成分子晶体的粒子是分子,粒子间作用是分子间
作用力。
3依据物质的性质判断,分子晶体的硬度小,熔、沸点低,在熔融状态或固体时均不导电。
1.下列有关分子晶体的说法中一定正确的是( )
A.分子内均存在共价键
B.分子间一定存在范德华力
C.分子间一定存在氢键
D.其结构一定为分子密堆积
B [稀有气体元素组成的分子晶体中,不存在由多个原子组成的分子,而是原子间通过范德华力结合成晶体,所以不存在任何化学键,A错误;分子间作用力包括范德华力和氢键,范德华力存
在于所有的分子晶体中,而氢键只存在于含有与电负性较强的 N、O、F原子结合的氢原子的分子
之间或者分子之内,B正确,C错误;只存在范德华力的分子晶体才采取分子密堆积的方式,D错
误。]
2.HF分子晶体、NH 分子晶体与冰的结构极为相似,在HF分子晶体中,与F原子距离最近
3
的HF分子有( )
A.3个 B.4个 C.5个 D.12个
B [根据HF分子晶体与冰结构相似可知,每个HF分子周围有4个HF分子与之最近,构成四
面体,故B项正确。]
3.下列物质按熔、沸点由高到低顺序排列,正确的一组是( )
A.HF、HCl、HBr、HI
B.F 、Cl 、Br 、I
2 2 2 2
C.H O、H S、H Se、H Te
2 2 2 2
D.CI 、CBr 、CCl 、CF
4 4 4 4
D [对结构和组成相似的分子晶体,其熔、沸点随着相对分子质量的增大而升高,但 HF、
H O 分子之间都存在氢键,熔、沸点反常。所以 A 中应为 HF>HI>HBr>HCl;B 中应为
2
I >Br >Cl >F ;C中应为H O>H Te>H Se>H S;只有D正确。]
2 2 2 2 2 2 2 2
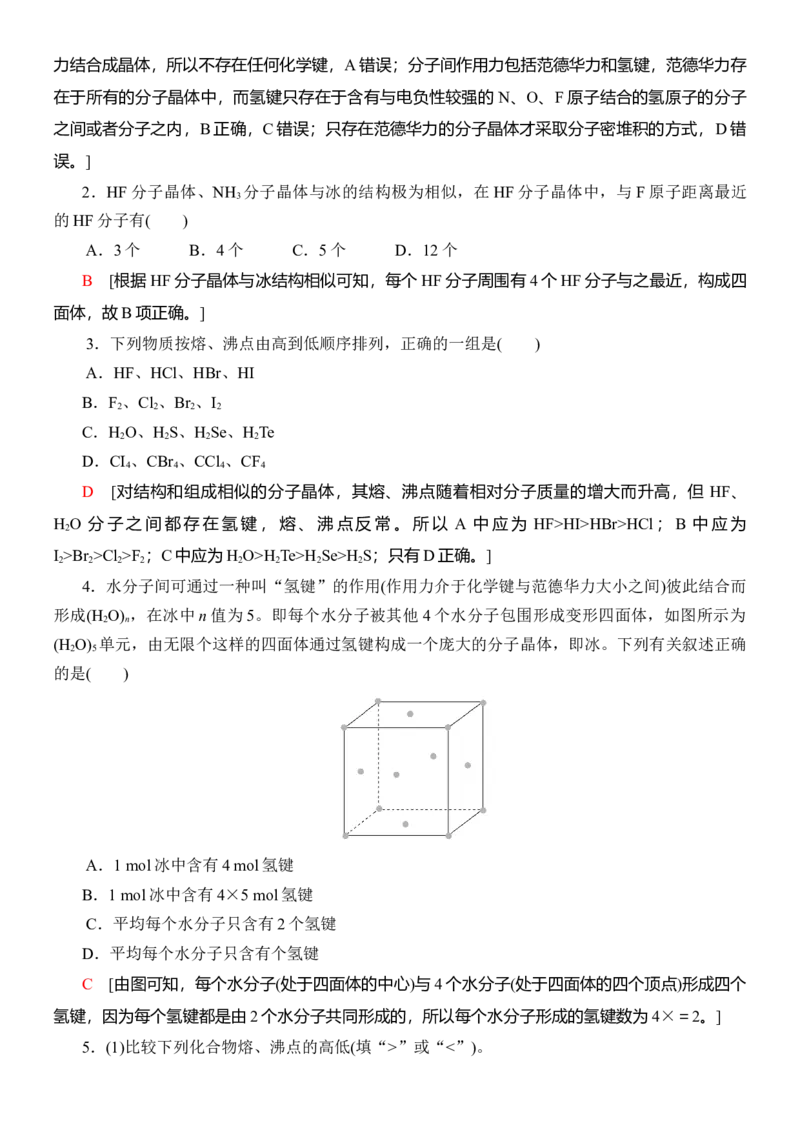
4.水分子间可通过一种叫“氢键”的作用(作用力介于化学键与范德华力大小之间)彼此结合而
形成(H O) ,在冰中n值为5。即每个水分子被其他 4个水分子包围形成变形四面体,如图所示为
2 n
(H O) 单元,由无限个这样的四面体通过氢键构成一个庞大的分子晶体,即冰。下列有关叙述正确
2 5
的是( )
A.1 mol冰中含有4 mol氢键
B.1 mol冰中含有4×5 mol氢键
C.平均每个水分子只含有2个氢键
D.平均每个水分子只含有个氢键
C [由图可知,每个水分子(处于四面体的中心)与4个水分子(处于四面体的四个顶点)形成四个
氢键,因为每个氢键都是由2个水分子共同形成的,所以每个水分子形成的氢键数为4×=2。]
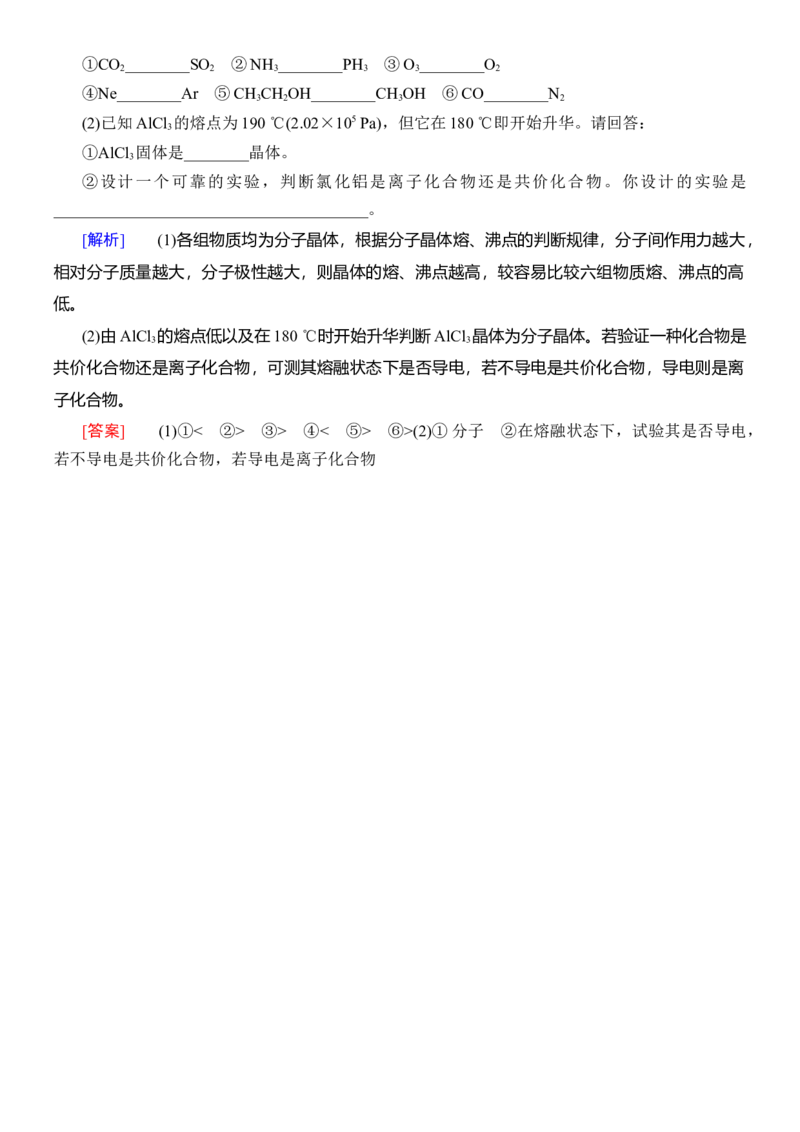
5.(1)比较下列化合物熔、沸点的高低(填“>”或“<”)。①CO ________SO ②NH ________PH ③O ________O
2 2 3 3 3 2
④Ne________Ar ⑤CH CH OH________CH OH ⑥CO________N
3 2 3 2
(2)已知AlCl 的熔点为190 ℃(2.02×105 Pa),但它在180 ℃即开始升华。请回答:
3
①AlCl 固体是________晶体。
3
②设计一个可靠的实验,判断氯化铝是离子化合物还是共价化合物。你设计的实验是
_______________________________________。
[解析] (1)各组物质均为分子晶体,根据分子晶体熔、沸点的判断规律,分子间作用力越大,
相对分子质量越大,分子极性越大,则晶体的熔、沸点越高,较容易比较六组物质熔、沸点的高
低。
(2)由AlCl 的熔点低以及在180 ℃时开始升华判断AlCl 晶体为分子晶体。若验证一种化合物是
3 3
共价化合物还是离子化合物,可测其熔融状态下是否导电,若不导电是共价化合物,导电则是离
子化合物。
[答案] (1)①< ②> ③> ④< ⑤> ⑥>(2)①分子 ②在熔融状态下,试验其是否导电,
若不导电是共价化合物,若导电是离子化合物