文档内容
第二章 第一节 共价键
发 展 目 标 体 系 构 建
1.能从微观角度分析形成共价键的粒子、类型,能辨识
物质中含有的共价键的类型及成键方式,了解键能、
键长及键角对物质性质的影响。
2.理解共价键中σ键和π键的区别,建立判断σ键和π
键的思维模型,熟练判断分子中σ键和π键的存在及
个数。
一、共价键
1.共价键的概念和特征
原子间通过共用电子对所形成的相互作用。
微点拨:共价键的方向性决定了分子的立体构型,并不是所有共价键都具有方向性,如两个 s
电子形成共价键时就没有方向性。
2.共价键的类型(按成键原子的原子轨道重叠方式分类)
(1)σ键
形成 由成键原子的s轨道或p轨道重叠形成
s-s型
类
s-p型
型
p-p型
以形成化学键的两原子核的连线为轴做旋转操作,共价键的电子云的图形不
特征
变,这种特征称为轴对称
(2)π键
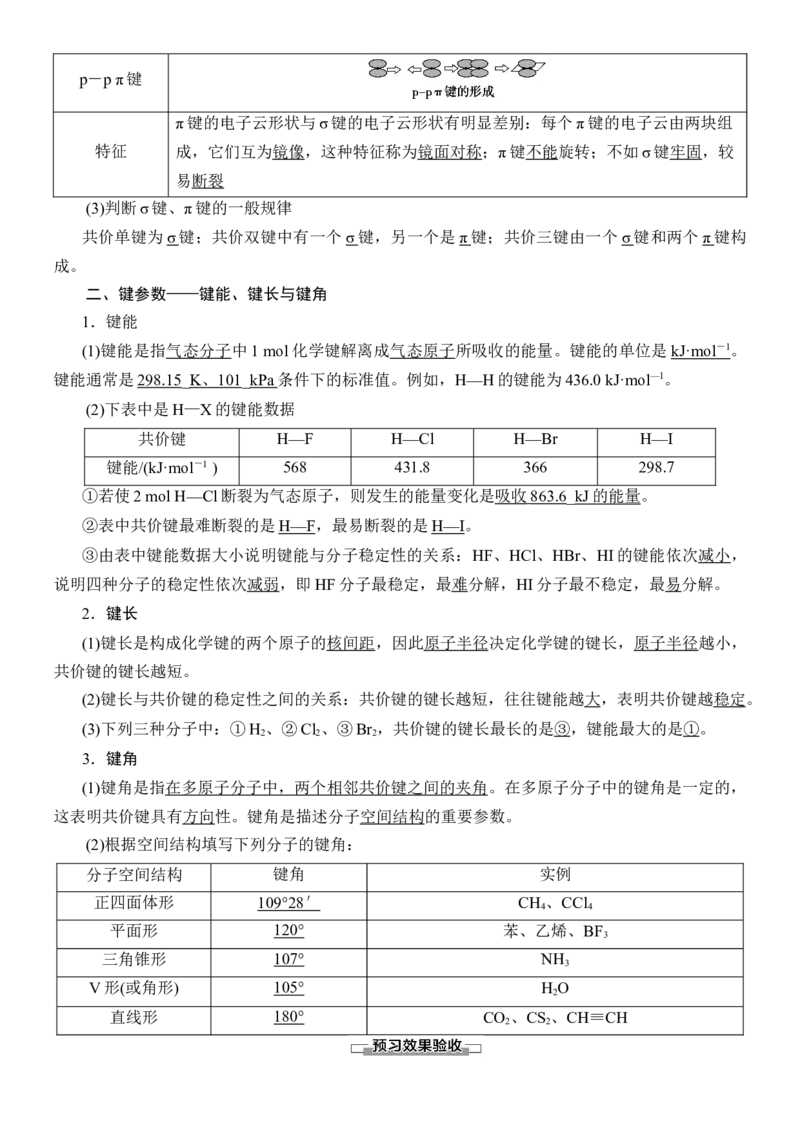
形成 由两个原子的p轨道“肩并肩”重叠形成p-p π键
π键的电子云形状与σ键的电子云形状有明显差别:每个π键的电子云由两块组
特征 成,它们互为镜像,这种特征称为镜面对称;π键不能旋转;不如σ键牢固,较
易断裂
(3)判断σ键、π键的一般规律
共价单键为σ 键;共价双键中有一个σ 键,另一个是π 键;共价三键由一个σ 键和两个π 键构
成。
二、键参数——键能、键长与键角
1.键能
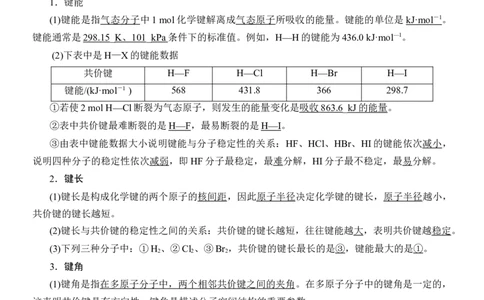
(1)键能是指气态分子中1 mol化学键解离成气态原子所吸收的能量。键能的单位是 kJ·mol - 1 。
键能通常是298.15_ K 、 101 _kPa 条件下的标准值。例如,H—H的键能为436.0 kJ·mol—1。
(2)下表中是H—X的键能数据
共价键 H—F H—Cl H—Br H—I
键能/(kJ·mol-1 ) 568 431.8 366 298.7
①若使2 mol H—Cl断裂为气态原子,则发生的能量变化是 吸收 863. 6_ kJ 的能量 。
②表中共价键最难断裂的是H—F,最易断裂的是H—I。
③由表中键能数据大小说明键能与分子稳定性的关系:HF、HCl、HBr、HI的键能依次减小,
说明四种分子的稳定性依次减弱,即HF分子最稳定,最难分解,HI分子最不稳定,最易分解。
2.键长
(1)键长是构成化学键的两个原子的核间距,因此原子半径决定化学键的键长,原子半径越小,
共价键的键长越短。
(2)键长与共价键的稳定性之间的关系:共价键的键长越短,往往键能越大,表明共价键越稳定。
(3)下列三种分子中:①H 、②Cl 、③Br ,共价键的键长最长的是③,键能最大的是①。
2 2 2
3.键角
(1)键角是指在多原子分子中,两个相邻共价键之间的夹角。在多原子分子中的键角是一定的,
这表明共价键具有方向性。键角是描述分子空间结构的重要参数。
(2)根据空间结构填写下列分子的键角:
分子空间结构 键角 实例
正四面体形 109°28 ′ CH 、CCl
4 4
平面形 120° 苯、乙烯、BF
3
三角锥形 107° NH
3
V形(或角形) 105° H O
2
直线形 180° CO 、CS 、CH≡CH
2 21.判断正误(对的在括号内打“√”,错的在括号内打“×”。)
(1)只有非金属原子之间才能形成共价键 (×)
(2)两个原子之间形成共价键时,至少有一个σ键 (√)
(3)σ键和π键都只能存在于共价化合物中 (×)
(4)双原子分子中,键长越短,分子越牢固 (√)
2.原子间形成分子时,决定各原子相互结合的数量关系的是( )
A.共价键的方向性
B.共价键的饱和性
C.形成共价键原子的大小
D.共价键的稳定性
B [共价键的饱和性决定各原子相互结合的数量关系。]
3.有以下物质:
①HF,②Cl ,③H O,④N ,⑤C H ,⑥C H ,⑦H ,
2 2 2 2 4 2 6 2
⑧H O ,⑨HCN(H—C≡N)。
2 2
(1)只有σ键的是________________(填序号,下同);既有σ键又有π键的是________。
(2)含有由两个原子的s轨道重叠形成的σ键的是___________。
(3)含有由一个原子的s轨道与另一个原子的p轨道重叠形成的σ键的是________。
(4)含有由一个原子的p轨道与另一个原子的p轨道重叠形成的σ键的是________。
[解析] (1)单键只有σ键,双键或三键才含有π键,故只有σ键的是①②③⑥⑦⑧;既有σ键
又有π键的是④⑤⑨。
(2)H原子只有s轨道,题给物质中含有由两个原子的s轨道重叠形成的σ键的只有H 。
2
(3)含有由一个原子的s轨道与另一个原子的p轨道重叠形成的σ键的有①③⑤⑥⑧⑨。
(4)含有由一个原子的p轨道与另一个原子的p轨道重叠形成的σ键,说明构成这种σ键的原子
中一定没有H原子,故正确答案为②④⑤⑥⑧⑨。
[答案] (1)①②③⑥⑦⑧ ④⑤⑨ (2)⑦ (3)①③⑤⑥⑧⑨ (4)②④⑤⑥⑧⑨
σ键与π键的比较
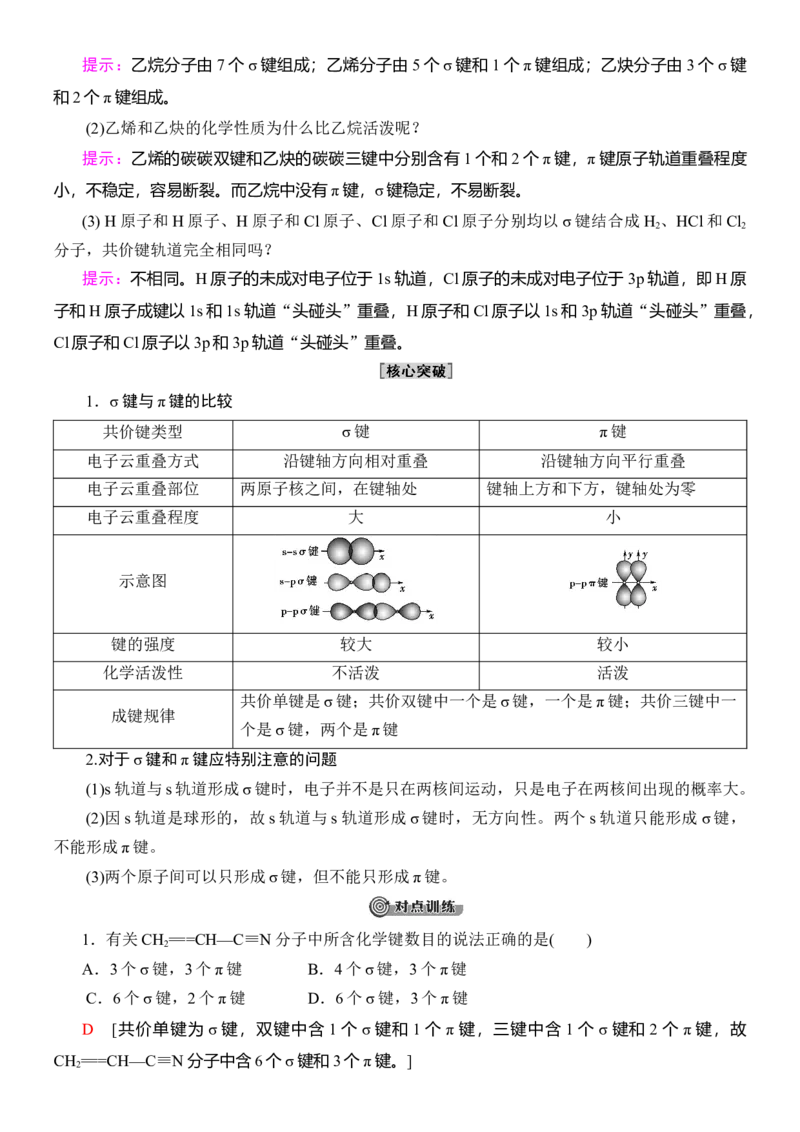
观察下图乙烷、乙烯和乙炔分子的结构回答:
(1)乙烷、乙烯和乙炔分子中的共价键分别由几个σ键和几个π键组成?提示:乙烷分子由7个σ键组成;乙烯分子由5个σ键和1个π键组成;乙炔分子由3个σ键
和2个π键组成。
(2)乙烯和乙炔的化学性质为什么比乙烷活泼呢?
提示:乙烯的碳碳双键和乙炔的碳碳三键中分别含有1个和2个π键,π键原子轨道重叠程度
小,不稳定,容易断裂。而乙烷中没有π键,σ键稳定,不易断裂。
(3) H原子和H原子、H原子和Cl原子、Cl原子和Cl原子分别均以σ键结合成H 、HCl和Cl
2 2
分子,共价键轨道完全相同吗?
提示:不相同。H原子的未成对电子位于1s轨道,Cl原子的未成对电子位于3p轨道,即H原
子和H原子成键以1s和1s轨道“头碰头”重叠,H原子和Cl原子以1s和3p轨道“头碰头”重叠,
Cl原子和Cl原子以3p和3p轨道“头碰头”重叠。
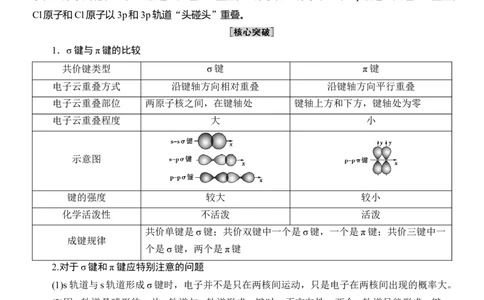
1.σ键与π键的比较
共价键类型 σ键 π键
电子云重叠方式 沿键轴方向相对重叠 沿键轴方向平行重叠
电子云重叠部位 两原子核之间,在键轴处 键轴上方和下方,键轴处为零
电子云重叠程度 大 小
示意图
键的强度 较大 较小
化学活泼性 不活泼 活泼
共价单键是σ键;共价双键中一个是σ键,一个是π键;共价三键中一
成键规律
个是σ键,两个是π键
2.对于σ键和π键应特别注意的问题
(1)s轨道与s轨道形成σ键时,电子并不是只在两核间运动,只是电子在两核间出现的概率大。
(2)因s轨道是球形的,故s轨道与s轨道形成σ键时,无方向性。两个 s轨道只能形成σ键,
不能形成π键。
(3)两个原子间可以只形成σ键,但不能只形成π键。
1.有关CH ===CH—C≡N分子中所含化学键数目的说法正确的是( )
2
A.3个σ键,3个π键 B.4个σ键,3个π键
C.6个σ键,2个π键 D.6个σ键,3个π键
D [共价单键为 σ 键,双键中含 1 个 σ 键和 1 个 π 键,三键中含 1 个 σ 键和 2 个 π 键,故
CH ===CH—C≡N分子中含6个σ键和3个π键。]
22.关于σ键和π键的比较,下列说法不正确的是( )
A.σ键是轴对称的,π键是镜面对称的
B.σ键是“头碰头”式重叠,π键是“肩并肩”式重叠
C.σ键不能断裂,π键容易断裂
D.氢原子只能形成σ键,氧原子可以形成σ键和π键
C [σ键较稳定,不易断裂,而不是不能断裂。]
分子中σ键与π键的判断方法
根据成键原子的价电子数来判断能形成几个共用电子对。如果只有一个共用电子对,则该
共价键一定是σ键;如果形成多个共用电子对时,则先形成1个σ键,另外的原子轨道形成π键。
键参数的应用
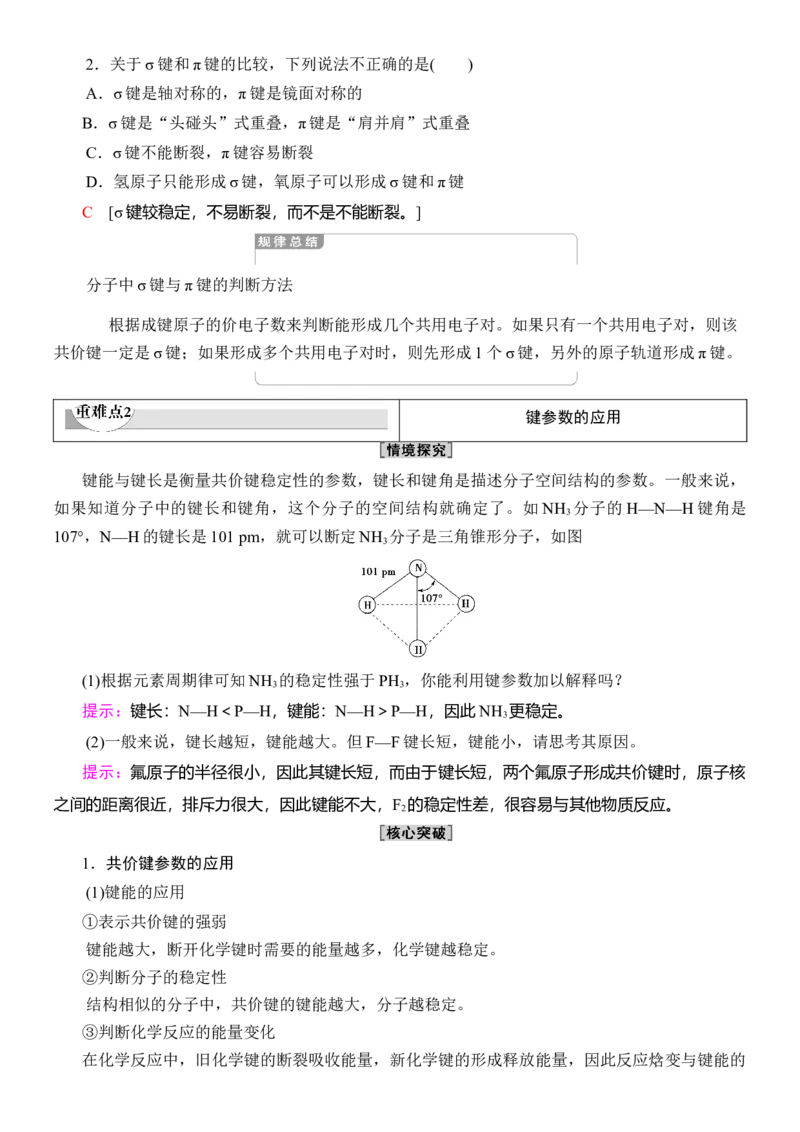
键能与键长是衡量共价键稳定性的参数,键长和键角是描述分子空间结构的参数。一般来说,
如果知道分子中的键长和键角,这个分子的空间结构就确定了。如NH 分子的H—N—H键角是
3
107°,N—H的键长是101 pm,就可以断定NH 分子是三角锥形分子,如图
3
(1)根据元素周期律可知NH 的稳定性强于PH ,你能利用键参数加以解释吗?
3 3
提示:键长:N—H<P—H,键能:N—H>P—H,因此NH 更稳定。
3
(2)一般来说,键长越短,键能越大。但F—F键长短,键能小,请思考其原因。
提示:氟原子的半径很小,因此其键长短,而由于键长短,两个氟原子形成共价键时,原子核
之间的距离很近,排斥力很大,因此键能不大,F 的稳定性差,很容易与其他物质反应。
2
1.共价键参数的应用
(1)键能的应用
①表示共价键的强弱
键能越大,断开化学键时需要的能量越多,化学键越稳定。
②判断分子的稳定性
结构相似的分子中,共价键的键能越大,分子越稳定。
③判断化学反应的能量变化
在化学反应中,旧化学键的断裂吸收能量,新化学键的形成释放能量,因此反应焓变与键能的关系为ΔH=反应物键能总和-生成物键能总和;ΔH<0时,为放热反应;ΔH>0时,为吸热反应。
(2)键长的应用
①一般键长越短,键能越大,共价键越稳定,分子越稳定。
②键长的比较方法
a.根据原子半径比较,同类型的共价键,成键原子的原子半径越小,键长越短。
b.根据共用电子对数比较,相同的两个原子间形成共价键时,单键键长>双键键长>三键键
长。
(3)键角的应用
①键长和键角决定分子的空间结构
②常见分子的键角与分子空间结构
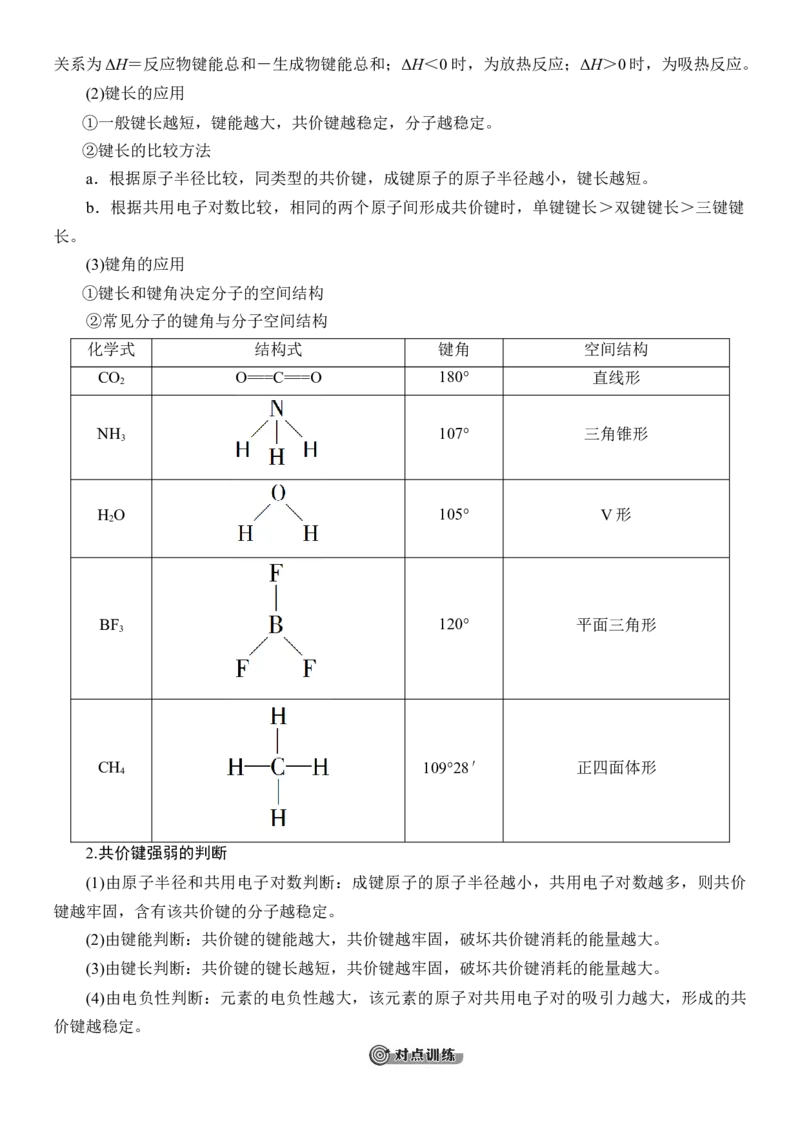
化学式 结构式 键角 空间结构
CO O===C===O 180° 直线形
2
NH 107° 三角锥形
3
H O 105° V形
2
BF 120° 平面三角形
3
CH 109°28′ 正四面体形
4
2.共价键强弱的判断
(1)由原子半径和共用电子对数判断:成键原子的原子半径越小,共用电子对数越多,则共价
键越牢固,含有该共价键的分子越稳定。
(2)由键能判断:共价键的键能越大,共价键越牢固,破坏共价键消耗的能量越大。
(3)由键长判断:共价键的键长越短,共价键越牢固,破坏共价键消耗的能量越大。
(4)由电负性判断:元素的电负性越大,该元素的原子对共用电子对的吸引力越大,形成的共
价键越稳定。3.下列说法正确的是( )
A.分子的结构是由键角决定的
B.共价键的键能越大,共价键越牢固,由该键形成的分子越稳定
C.CF 、CCl 、CBr 、CI 中C—X(X=F、Cl、Br、I)的键长、键角均相等
4 4 4 4
D.H O分子中两个O—H的键角为180°
2
B [分子的结构是由键角、键长共同决定的,A项错误;由于F、Cl、Br、I的原子半径不同,
故C—X(X=F、Cl、Br、I)键的键长不相等,C项错误;H O分子中两个O—H的键角为105°,D
2
项错误。]
4.下列事实不能用键能的大小来解释的是( )
A.氮元素的电负性较大,但N 的化学性质很稳定
2
B.稀有气体一般难发生反应
C.HF、HCl、HBr、HI的稳定性逐渐减弱
D.HF比H O稳定
2
B [由于N 分子中存在三键,键能很大,破坏共价键需要很大的能量,所以 N 的化学性质很
2 2
稳定;稀有气体都为单原子分子,没有化学键;卤族元素从 F到I,原子半径逐渐增大,其氢化物
中化学键的键长逐渐变长,键能逐渐变小,所以稳定性:HF>HCl>HBr>HI;由于H—F的键能
大于H—O,所以稳定性:HF>H O。]
2
由分子构成的物质,其熔、沸点与共价键的键能和键长无关。而分子的稳定性,由键长和键
能决定。
1.下列不属于共价键成键因素的是( )
A.共用电子对在两原子核之间高概率出现
B.共用的电子必须配对
C.成键后体系能量降低,趋于稳定
D.两原子核体积大小要适中
D [共价键的成因和本质是,当成键原子相互靠近时,原子轨道发生重叠,自旋方向相反的未
成对电子形成共用电子对,两原子核间的电子云密度增加,体系的能量降低。]
2.下列分子中的σ键是由一个原子的s轨道和另一个原子的p轨道以“头碰头”方式重叠构建
而成的是( )
A.H B.HCl C.Cl D.N
2 2 2
B [H 中的σ键是ss σ键,Cl 、N 中的σ键都是pp σ键。]
2 2 23.下列说法正确的是( )
A.若把H S分子写成H S分子,违背了共价键的饱和性
2 3
B.基态C原子有两个未成对电子,所以只能形成两个共价键
C.所有共价键都有方向性
D.两个原子轨道发生重叠后,两核间的电子不仅仅在两核之间,而是绕两个原子核运动
A [如在形成CH 分子的过程中,碳原子 2s轨道中的1个电子被激发到2p轨道中,此时碳原
4
子有4个未成对电子,形成4个共价键,B错误;H 分子中的s轨道成键时,因s轨道为球形,故
2
H 分子中的H—H共价键无方向性,C错误;两个原子轨道重叠后,电子在核间出现的概率增大,
2
但不是绕两个原子核运动,D错误。]
4.下列说法中正确的是( )
A.双原子分子中化学键键能越大,分子越稳定
B.双原子分子中化学键键长越长,分子越稳定
C.双原子分子中化学键键角越大,分子越稳定
D.在双键中,σ键的键能要小于π键
A [共价键键能越大、键长越短,分子越稳定,A正确,B错误;在双原子分子中没有键角,
且分子稳定性与键角无关,C错误;一般σ键的重叠程度大于π键,σ键的键能大于π键,D错
误。]
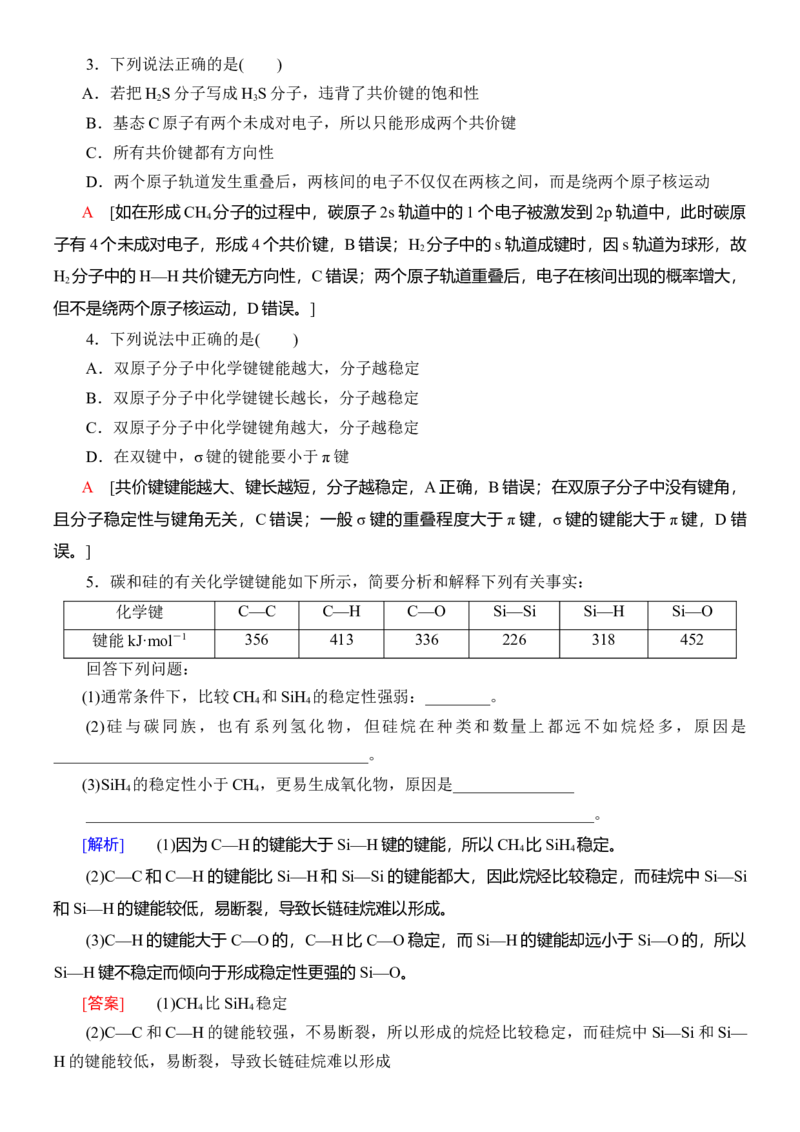
5.碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
化学键 C—C C—H C—O Si—Si Si—H Si—O
键能kJ·mol-1 356 413 336 226 318 452
回答下列问题:
(1)通常条件下,比较CH 和SiH 的稳定性强弱:________。
4 4
(2)硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是
_______________________________________。
(3)SiH 的稳定性小于CH ,更易生成氧化物,原因是_______________
4 4
_______________________________________________________________。
[解析] (1)因为C—H的键能大于Si—H键的键能,所以CH 比SiH 稳定。
4 4
(2)C—C和C—H的键能比Si—H和Si—Si的键能都大,因此烷烃比较稳定,而硅烷中Si—Si
和Si—H的键能较低,易断裂,导致长链硅烷难以形成。
(3)C—H的键能大于C—O的,C—H比C—O稳定,而Si—H的键能却远小于Si—O的,所以
Si—H键不稳定而倾向于形成稳定性更强的Si—O。
[答案] (1)CH 比SiH 稳定
4 4
(2)C—C和C—H的键能较强,不易断裂,所以形成的烷烃比较稳定,而硅烷中Si—Si和Si—
H的键能较低,易断裂,导致长链硅烷难以形成(3)C—H的键能大于C—O,C—H比C—O稳定,而Si—H的键能却远小于Si—O,所以Si—
H不稳定而倾向于形成稳定性更强的Si—O