文档内容
第 2 课时 杂化轨道理论简介
发 展 目 标 体 系 构 建
1. 知道杂化轨道理论的基本内容。
2.能根据杂化轨道理论确定简单分子的空间结构。
1.用杂化轨道理论解释甲烷分子的形成
在形成CH 分子时,碳原子的一个2s 轨道和三个2p 轨道发生混杂,形成4个能量相等的 sp 3 杂
4
化轨道。4个 sp 3 杂化轨道分别与4个H原子的1s轨道重叠形成4个C—Hσ 键,所以4个C—H键
是等同的。
2.杂化轨道的形成及其特点
3.杂化轨道类型及其空间结构
(1)sp3杂化轨道
sp3杂化轨道是由1 个s轨道和3 个p轨道杂化形成的。sp3杂化轨道间的夹角是109°28′,空间
结构为正四面体形(如下图所示)。(2)sp2杂化轨道
sp2杂化轨道是由1 个s轨道和2 个p轨道杂化而成的。sp2杂化轨道间的夹角是120°,呈平面三
角形(如下图所示)。
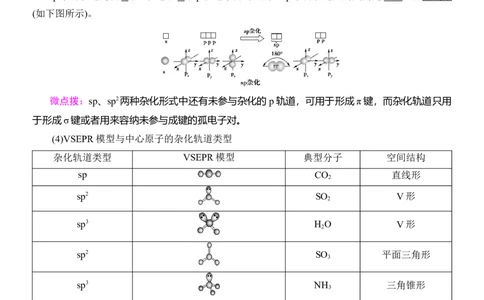
(3)sp杂化轨道
sp杂化轨道是由1 个s轨道和1 个p轨道杂化而成的。sp杂化轨道间的夹角是180°,呈直线形
(如下图所示)。
微点拨:sp、sp2两种杂化形式中还有未参与杂化的 p轨道,可用于形成π键,而杂化轨道只用
于形成σ键或者用来容纳未参与成键的孤电子对。
(4)VSEPR模型与中心原子的杂化轨道类型
杂化轨道类型 VSEPR模型 典型分子 空间结构
sp CO 直线形
2
sp2 SO V形
2
sp3 H O V形
2
sp2 SO 平面三角形
3
sp3 NH 三角锥形
3
sp3 CH 正四面体形
4
1.判断正误(对的在括号内打“√”,错的在括号内打“×”。)
(1)杂化轨道与参与杂化的原子轨道的数目相同,但能量不同。 (√)
(2)杂化轨道间的夹角与分子内的键角不一定相同。 (√)
(3)凡是中心原子采取sp3杂化轨道成键的分子其空间结构都是正四面体形。
(4)凡AB 型的共价化合物,其中心原子A均采用sp3杂化轨道成键。
3
(×)2.能正确表示CH 中碳原子的成键方式的示意图为( )
4
D [碳原子的2s轨道与2p轨道形成4个等性的杂化轨道,因此碳原子 4个价电子分占在4个
sp3杂化轨道上,且自旋状态相同。]
3.ClO-、ClO、ClO、ClO中,中心原子Cl都是以sp3杂化轨道方式与O原子成键,则ClO-
的空间结构是________;ClO的空间结构是________;ClO的空间结构是________;ClO的空间结
构是________。
[解析] ClO-的组成决定其空间结构为直线形。其他 3种离子的中心原子的杂化方式都为 sp3
杂化,从离子的组成上看其空间结构依次类似于H O、NH 、CH (或NH)。
2 3 4
[答案] 直线形 V形 三角锥形 正四面体形
杂化类型及分子空间结构的判断
在形成多原子分子时,中心原子价电子层上的某些能量相近的原子轨道发生混杂,重新组合成
一组新的轨道的过程,叫做轨道的杂化。双原子分子中,不存在杂化过程。例如 sp杂化、sp2杂化
的过程如下:
(1)观察上述杂化过程,分析原子轨道杂化后,数量和能量有什么变化?
提示:杂化轨道与参与杂化的原子轨道数目相同,但能量不同。s轨道与p轨道的能量不同,
杂化后,形成的一组杂化轨道能量相同。(2)2s轨道与3p轨道能否形成sp2杂化轨道?
提示:不能。只有能量相近的原子轨道才能形成杂化轨道。2s与3p不在同一能级,能量相差
较大。
(3)用杂化轨道理论解释NH 、H O的空间结构?
3 2
提示:NH 分子中N原子的价电子排布式为2s22p3。1个2s轨道和3个2p经杂化后形成4个sp3
3
杂化轨道,其中3个杂化轨道中各有1个未成对电子,分别与H原子的1s轨道形成共价键,另1
个杂化轨道中是成对电子,不与H原子形成共价键,sp3杂化轨道为正四面体形,但由于孤电子对
的排斥作用,使3个N—H的键角变小,成为三角锥形的空间结构。H O分子中O原子的价电子排
2
布式为2s22p4。1个2s轨道和3个2p轨道经杂化后形成4个sp3杂化轨道,其中2个杂化轨道中各
有1个未成对电子,分别与 H原子的1s轨道形成共价键,另2个杂化轨道是成对电子,不与 H原
子形成共价键,sp3杂化轨道为正四面体形,但由于2对孤电子对的排斥作用,使2个O—H的键角
变得更小,成为V形的空间结构。
(4)CH 、NH 、H O中心原子的杂化类型都为sp3,键角为什么依次减小?从杂化轨道理论的角
4 3 2
度比较键角大小时有什么方法?
提示:CH 、NH 、H O中心原子都采取sp3杂化,中心原子的孤电子对数依次为0个、1个、2
4 3 2
个。由于孤电子对对共用电子对的排斥作用使键角变小,孤电子对数越多排斥作用越大,键角越
小。比较键角时,先看中心原子杂化类型,杂化类型不同时:一般键角按 sp、sp2、sp3顺序依次减
小;杂化类型相同时,中心原子孤电子对数越多,键角越小。
1.杂化轨道理论要点
(1)只有能量相近的原子轨道才能杂化。
(2)杂化轨道数目和参与杂化的原子轨道数目相等,杂化轨道能量相同。
(3)杂化改变原有轨道的形状和伸展方向,使原子形成的共价键更牢固。
(4)杂化轨道为使相互间的排斥力最小,故在空间取最大夹角分布,不同的杂化轨道伸展方向
不同。
(5)杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对。
(6)未参与杂化的p轨道可用于形成π键。
2.中心原子轨道杂化类型的判断
(1)利用价层电子对互斥理论、杂化轨道理论判断分子构型的思路:
价层电子对――→杂化轨道数――→杂化类型――→杂化轨道构型。
(2)根据杂化轨道之间的夹角判断:若杂化轨道之间的夹角为 109°28′,则中心原子发生sp3杂
化;若杂化轨道之间的夹角为 120°,则中心原子发生sp2杂化;若杂化轨道之间的夹角为 180°,则
中心原子发生sp杂化。(3)有机物中碳原子杂化类型的判断:饱和碳原子采取 sp3杂化,连接双键的碳原子采取sp2杂化,
连接三键的碳原子采取sp杂化。
1.下列分子中中心原子的杂化方式和分子的空间结构均正确的是( )
A.C H :sp2、直线形 B.SO:sp3、三角锥形
2 2
C.H O+:sp3、V形 D.BF :sp2、平面三角形
3 3
D [乙炔的结构式为H—C≡C—H,每个碳原子价层电子对个数是2且不含孤电子对,所以C
原子采用sp杂化,为直线形结构;SO中硫原子的价层电子对数=4,孤电子对数为0,采取sp3杂
化,为正四面体形;H O+中氧原子的价层电子对数=3+1=4,所以中心原子原子轨道为 sp3杂化,
3
该离子中含有一个孤电子对,所以其空间结构为三角锥形;BF 分子中硼原子价层电子对数=3+0
3
=3,杂化轨道数为3,孤电子对数为0,所以其空间结构为平面三角形。]
2.下列说法中正确的是( )
A.NCl 分子呈三角锥形,这是氮原子采取sp2杂化的结果
3
B.sp3杂化轨道是由任意的1个s轨道和3个p轨道混合形成的4个sp3杂化轨道
C.中心原子采取sp3杂化的分子,其空间结构可能是四面体形或三角锥形或V形
D.AB 型的分子空间结构必为平面三角形
3
C [NCl 分子中心氮原子上的价层电子对数=σ键电子对数+孤电子对数=3+=4,因此NCl
3 3
分子中氮原子以sp3杂化,选项A错误;sp3杂化轨道是原子最外电子层上的s轨道和3个p轨道
“混杂”起来,形成能量相等、成分相同的4个轨道,选项B错误;一般中心原子采取sp3杂化的
分子所得到的空间结构为四面体形,如甲烷分子,但如果有杂化轨道被中心原子上的孤电子对占
据,则空间结构发生变化,如NH 、PCl 分子是三角锥形,选项D错误,选项C正确。 ]
3 3
3.计算下列各粒子中心原子的杂化轨道数、判断中心原子的杂化轨道类型、写出 VSEPR模
型名称。
[答案] (1)2 sp 直线形 (2)4 sp3 正四面体形 (3)4 sp3 四面体形 (4)4 sp3 四面
体形 (5)3 sp2 平面三角形1.下列关于杂化轨道的说法错误的是( )
A.并不是所有的原子轨道都参与杂化
B.同一原子中能量相近的原子轨道参与杂化
C.杂化轨道能量集中,有利于牢固成键
D.杂化轨道都用来成键
D [参与杂化的原子轨道,其能量不能相差太大,如 1s与2s、2p的能量相差太大,不能形成
杂化轨道,即只有能量相近的原子轨道才能参与杂化,故A、B正确;杂化轨道的电子云一头大一
头小,成键时利用大的一头,可使电子云的重叠程度更大,形成牢固的化学键,故 C项正确;并
不是所有的杂化轨道中都成键,也可以容纳孤电子对(如NH 、H O的形成),故D项错误。]
3 2
2.三氯化磷分子中的中心原子以sp3杂化,下列有关叙述正确的是( )
①3个P—Cl键长、键角均相等
②空间结构为平面三角形
③空间结构为正四面体形
④空间结构为三角锥形
A.①② B.②③
C.③④ D.①④
D [PCl 中P原子采取sp3杂化,有一对孤电子对,结构类似于NH 分子,3个P—Cl键长、键
3 3
角均相等,空间结构为三角锥形。]
3.有关乙炔分子中的化学键描述不正确的是( )
A.两个碳原子采用sp杂化方式
B.两个碳原子采用sp2杂化方式
C.每个碳原子都有两个未杂化的2p轨道形成π键
D.两个碳原子形成两个π键
B [乙炔中每个碳原子价层电子对数是2且不含孤电子对,所以碳原子采用sp杂化,A正确,
B错误;每个碳原子中两个未杂化的2p轨道肩并肩重叠形成π键,C正确;两个碳原子之间形成1
个σ键2个π键,D正确。]
4.下列关于原子轨道的说法正确的是( )
A.杂化轨道形成共价键时,只能形成σ键不能形成π键
B.凡AB 型的共价化合物,其中心原子A均采用sp3杂化轨道成键
3
C.凡是中心原子采取sp3杂化轨道成键的分子,其空间结构都是正四面体形
D.CH 分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合起来而形成的
4
A [AB 型的共价化合物,A原子可能采取sp2杂化或sp3杂化,B错误;中心原子采取sp3杂化,
3
轨道形状是正四面体,但如果中心原子还有孤电子对,分子的空间结构则不是正四面体,C错误;
CH 分子中的sp3杂化轨道是C原子的一个2s轨道与三个2p轨道杂化而成的,D错误。]
45.根据杂化轨道理论可以判断分子的空间结构,试根据相关知识填空:
(1)AsCl 分子的空间结构为________,其中As的杂化轨道类型为________。
3
(2)CS 分子中C原子的杂化轨道类型是________。
2
(3)CH COOH中C原子轨道杂化类型为________。
3
[解析] (1)AsCl 中As元素价电子对数为4,As的杂化方式为sp3杂化,AsCl 分子的空间结
3 3
构为三角锥形。(2)CS 的结构式为S===C===S,C原子形成2个双键,无孤电子对,所以为sp杂
2
化。(3)CH COOH的结构式为 ,分子中甲基上的碳原子采用sp3杂化,羧基中碳原
3
子采用sp2杂化。
[答案] (1)三角锥形 sp3 (2)sp (3)sp3、sp2