文档内容
微专题 3 四类典型晶体的比较
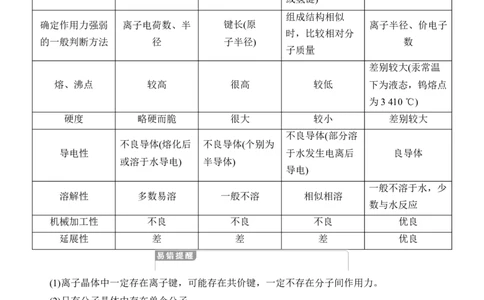
1.四类典型晶体的比较
类型
离子晶体 共价晶体 分子晶体 金属晶体
项目
金属阳离子和自由
构成晶体的粒子 阴、阳离子 原子 分子
电子
分子间作用力(范
粒子间的作用 离子键 共价键 德华力 金属键
或氢键)
组成结构相似
确定作用力强弱 离子电荷数、半 键长(原 离子半径、价电子
时,比较相对分
的一般判断方法 径 子半径) 数
子质量
差别较大(汞常温
熔、沸点 较高 很高 较低 下为液态,钨熔点
为3 410 ℃)
硬度 略硬而脆 很大 较小 差别较大
不良导体(部分溶
不良导体(熔化后 不良导体(个别为
导电性 于水发生电离后 良导体
或溶于水导电) 半导体)
导电)
一般不溶于水,少
溶解性 多数易溶 一般不溶 相似相溶
数与水反应
机械加工性 不良 不良 不良 优良
延展性 差 差 差 优良
1离子晶体中一定存在离子键,可能存在共价键,一定不存在分子间作用力。
2只有分子晶体中存在单个分子。
3某些离子晶体的熔点高于某些共价晶体的熔点。如MgO2 852 ℃>SiO 1 710 ℃。
2
4某些分子晶体的熔点高于某些金属晶体的熔点。如碱金属熔点较低。
5个别金属的熔点高于某些共价晶体的熔点。如钨3 410 ℃>SiO 1 710 ℃。
2
6合金的熔点一般低于成分金属的熔点。
2.晶体熔、沸点高低的比较方法
(1)不同类型晶体熔、沸点的比较:
①不同类型晶体的熔、沸点高低一般规律:共价晶体>离子晶体>分子晶体。②金属晶体的熔、沸点差别很大,如钨、铂等熔、沸点很高,汞、铯等熔、沸点很低。
(2)同种类型晶体熔、沸点的比较:
①共价晶体
原子半径越小→键长越短→键能越大→熔、沸点越高。如熔点:金刚石>硅晶体。
②离子晶体
一般地说,阴、阳离子的电荷数越多,离子半径越小,则离子间的作用力就越强,其离子晶
体的熔、沸点就越高。如熔点:MgO>NaCl>CsCl。
③分子晶体
a.分子间作用力越大,物质的熔、沸点越高;具有氢键的分子晶体熔、沸点反常得高。如沸
点:H O>H Te>H Se>H S。
2 2 2 2
b.组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越高。如熔、沸点:SnH >
4
GeH >SiH >CH 。
4 4 4
c.组成和结构不相似的物质(相对分子质量接近),分子的极性越大,其熔、沸点越高。如熔、
沸点:CO>N ,CH OH>CH CH 。
2 3 3 3
④金属晶体
金属离子半径越小,离子电荷数越多,其金属键越强,金属熔、沸点就越高。如熔、沸点:
Na<Mg<Al。
1.下列各组物质中,化学键类型相同、晶体类型也相同的是( )
A.CaCl 和NaOH B.碘、氖
2
C.CO 和H O D.CCl 和KCl
2 2 4
C [A项都是离子晶体,CaCl 只有离子键,NaOH既有离子键又有共价键;B项都是分子晶体,
2
碘分子中有共价键,氖分子中无化学键;C项都是分子晶体,只有极性共价键;D项CCl 是分子
4
晶体,含有共价键,KCl是离子晶体,含有离子键。]
2.下列说法中正确的是( )
A.固态时能导电的物质一定是金属晶体
B.熔融状态能导电的晶体一定是离子晶体
C.水溶液能导电的晶体一定是离子晶体
D.固态不导电而熔融态导电的晶体一定是离子晶体
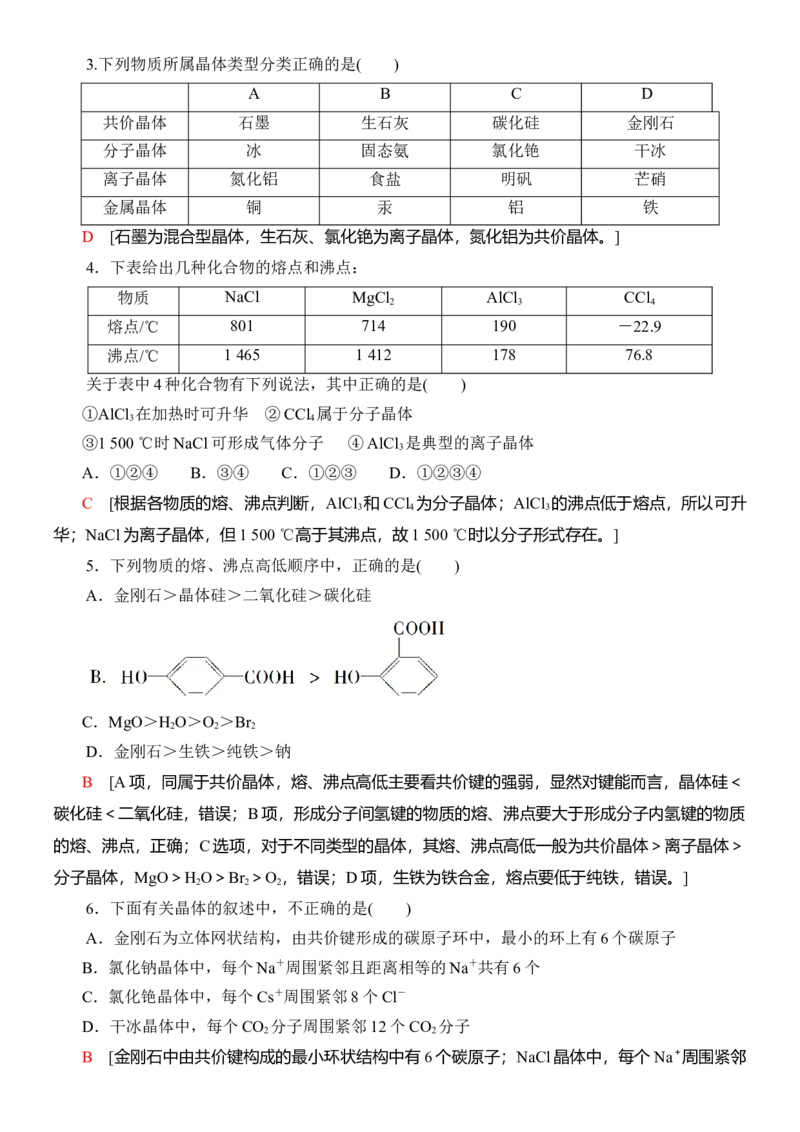
D [四种晶体在不同状态下的导电性区别如下:
分子晶体 共价晶体 金属晶体 离子晶体
固态 不导电 不导电(晶体硅导电) 导电 不导电
熔融状态 不导电 不导电 导电 可导电
水溶液 有的可导电 - - 可导电3.下列物质所属晶体类型分类正确的是( )
A B C D
共价晶体 石墨 生石灰 碳化硅 金刚石
分子晶体 冰 固态氨 氯化铯 干冰
离子晶体 氮化铝 食盐 明矾 芒硝
金属晶体 铜 汞 铝 铁
D [石墨为混合型晶体,生石灰、氯化铯为离子晶体,氮化铝为共价晶体。]
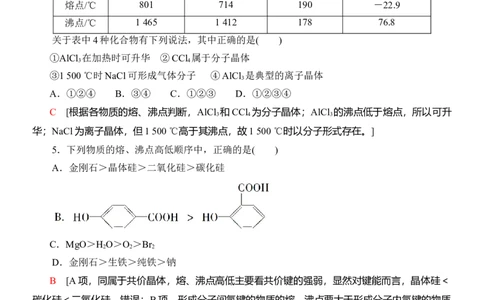
4.下表给出几种化合物的熔点和沸点:
物质 NaCl MgCl AlCl CCl
2 3 4
熔点/℃ 801 714 190 -22.9
沸点/℃ 1 465 1 412 178 76.8
关于表中4种化合物有下列说法,其中正确的是( )
①AlCl 在加热时可升华 ②CCl 属于分子晶体
3 4
③1 500 ℃时NaCl可形成气体分子 ④AlCl 是典型的离子晶体
3
A.①②④ B.③④ C.①②③ D.①②③④
C [根据各物质的熔、沸点判断,AlCl 和CCl 为分子晶体;AlCl 的沸点低于熔点,所以可升
3 4 3
华;NaCl为离子晶体,但1 500 ℃高于其沸点,故1 500 ℃时以分子形式存在。]
5.下列物质的熔、沸点高低顺序中,正确的是( )
A.金刚石>晶体硅>二氧化硅>碳化硅
C.MgO>H O>O >Br
2 2 2
D.金刚石>生铁>纯铁>钠
B [A项,同属于共价晶体,熔、沸点高低主要看共价键的强弱,显然对键能而言,晶体硅<
碳化硅<二氧化硅,错误;B项,形成分子间氢键的物质的熔、沸点要大于形成分子内氢键的物质
的熔、沸点,正确;C选项,对于不同类型的晶体,其熔、沸点高低一般为共价晶体>离子晶体>
分子晶体,MgO>H O>Br >O ,错误;D项,生铁为铁合金,熔点要低于纯铁,错误。]
2 2 2
6.下面有关晶体的叙述中,不正确的是( )
A.金刚石为立体网状结构,由共价键形成的碳原子环中,最小的环上有6个碳原子
B.氯化钠晶体中,每个Na+周围紧邻且距离相等的Na+共有6个
C.氯化铯晶体中,每个Cs+周围紧邻8个Cl-
D.干冰晶体中,每个CO 分子周围紧邻12个CO 分子
2 2
B [金刚石中由共价键构成的最小环状结构中有6个碳原子;NaCl晶体中,每个Na+周围紧邻6个Cl-,每个Na+周围紧邻12个Na+;氯化铯晶体中,每个Cs+周围紧邻8个Cl-,每个Cs+周围
紧邻6个Cs+;干冰晶体中,每个CO 分子周围紧邻12个CO 分子。]
2 2
7.KO 的晶体结构与NaCl相似,KO 可以看作是Na+的位置用K+代替,Cl-的位置用O代替,
2 2
则下列对于KO 晶体结构的描述正确的是( )
2
A.与K+距离相等且最近的O2-共有8个
B.与K+距离相等且最近的O2-构成的多面体是正八面体
C.与K+距离相等且最近的K+有8个
D.一个KO 晶胞中的K+和O粒子数均为8
2
B [K+位于晶胞棱心,与K+距离相等且最近的O2-位于顶点和面心,共有6个,故A错误;
与K+距离相等且最近的O2-共有6个,构成正八面体,K+位于正八面体中心,故B正确;K+位于
晶胞棱心,则被横平面、竖平面和正平面共有,且每一个平面有4个K+距离最近,共4×3=12个,
故C错误;K+位于晶胞棱心和体心,数目为 12×1/4+1=4,O2-位于顶点和面心,数目为8×1/8
+6×1/2=4,即一个KO 晶胞中摊得的K+和O2-粒子数均为4个,故D错误。]
2
8.分析下列物质的物理性质,判断其晶体类型:
(1)碳化铝,黄色晶体,熔点2 200 ℃,熔融状态下不导电________。
(2)溴化铝,无色晶体,熔点98 ℃,熔融状态下不导电________。
(3)五氟化钒,无色晶体,熔点19.5 ℃,易溶于乙醇、氯仿、丙酮等________。
(4)溴化钾,无色晶体,熔融时或溶于水中能导电________。
[解析] 晶体的熔点高低、熔融态能否导电及溶解性等性质相结合,是判断晶体类型的重要依
据。共价晶体和离子晶体的熔点都很高或较高,两者最大的差异是熔融态的导电性不同。一般共
价晶体熔融态不导电,离子晶体熔融时或水溶液都能导电。共价晶体和分子晶体的区别则主要在
于熔、沸点有很大差异。一般共价晶体和分子晶体熔融状态时都不能导电。另外易溶于一些有机
溶剂往往也是分子晶体的特征之一。
[答案] (1)共价晶体 (2)分子晶体 (3)分子晶体 (4)离子晶体