文档内容
专题一 能力提升检测卷
(本卷共20小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5 K 39
Ca 40 Fe 56 Cu 64
第I卷 (选择题共50分)
一、选择题:本题共10个小题,每小题3分,共30分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.下列分散系能产生丁达尔效应的是
A.KCl溶液 B.酒精溶液 C.熔融硝酸钾 D.氢氧化铁胶体
【答案】D
【解析】分散系溶液、浊液中不能产生丁达尔效应,而胶体可以产生丁达尔效应,KCl溶液、酒精溶
液均为溶液分散系,不能产生丁达尔效应,熔融硝酸钾属于纯净物,不能产生丁达尔效应,氢氧化铁胶体
属于胶体分散系,能够产生丁达尔效应,故答案为D。
2.虎年春晚一段舞蹈诗剧《只此青绿》生动还原了北宋名画《千里江山图》,此画用到了一种矿物
颜料——石青 。以下关于石青的说法错误的是
A.属于盐 B.可溶于水
C.在常温下较稳定 D.与盐酸反应后的溶液呈蓝色
【答案】B
【解析】石青的化学式为 ,属于碱式盐,A正确; 中,CuCO 和
3
Cu(OH) 均难溶于水,B错误;石青 能够一直保存下来,说明该物质在常温下较稳定,
2C正确;石青与盐酸反应的方程式为: +6HCl=3CuCl +4H O+2CO↑,得到的溶液为
2 2 2
CuCl 溶液,呈蓝色,D正确;答案选B。
2
3.湖南民俗文化源远流长,下列民俗文化作品在制作过程中涉及化学变化的是
A.玉和酿醋 B.望城剪纸 C.欣康木雕 D.长沙花鼓
【答案】A
【解析】酿醋过程涉及淀粉水解、葡萄糖发酵、氧化等化学变化,A项正确;望城剪纸是纸张的形状
发生变化,没有生成新物质,不属于化学变化,B项错误;欣康木雕没有生成新物质,不属于化学变化,
C项错误;长沙花鼓未涉及新物质生成,不属于化学变化,D项错误;故选A。
4.分类是一种重要的学习方法。物质的分类如图所示,下列说法中正确的是
A.图甲所示的分类方法属于树状分类法
B.酸性氧化物一定是非金属氧化物
C.Fe(OH) 胶体属于碱
3
D.甲图中“……”包含混合物
【答案】A
【解析】由题干信息可知,图甲所示的分类方法属于树状分类法,A正确;酸性氧化物不一定是非金
属氧化物,如MnO 是金属氧化物,属于酸性氧化物,B错误;Fe(OH) 胶体是混合物,而酸、碱、盐均属
2 7 3
于纯净物,属于化合物,故Fe(OH) 胶体不属于碱,C错误;化合物是指含有两种或两种以上元素的纯净
3
物,故甲图中“……”不包含混合物,D错误;故答案为A。
5.2021年新冠肺炎疫情夺走了至少330万人的生命,化学在攻克这一世界难题中功不可没,“新型
冠状病毒”由蛋白质外壳和单链核酸组成,直径为60-140 nm,怕酒精,不耐高温。下列说法不正确的是A.“新型冠状病毒”扩散到空气中不可能形成胶体
B.“新型冠状病毒”扩散到空气中形成的分散系可能具有一定的稳定性
C.蛋白质、酒精属于有机物
D.减少外出、勤通风可有效预防“新型冠状病毒”感染
【答案】A
【解析】胶体是分散质粒子大小在 1nm~100nm 的分散系;“新型冠状病毒”由蛋白质外壳和单链核
酸组成,直径为60-140 nm,扩散到空气中可能形成胶体,A错误;由A分析可知,“新型冠状病毒”扩
散到空气中形成的分散系为胶体,具有一定的稳定性,B正确;蛋白质、酒精都是含碳元素的化合物,属
于有机物,C正确;减少外出、勤通风,减少人员聚集,增加空气的流动,可有效预防“新型冠状病毒”
感染,D正确;故选A。
6.下列澄清溶液中,一定能大量共存的离子组是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
【答案】A
【解析】各个离子之间互不反应,能共存,故A正确; 、 、 发生氧化还原反应,不能大
量共存,故B错误; 与 生成BaSO 沉淀而不能大量共存,故C错误; 、 反应而不能大
4
量共存,故D错误;故选A。
7.下列离子方程式书写不正确的是
A.铁与硫酸铜溶液反应:
B.氢氧化钠溶液与稀盐酸反应:
C.铁与稀硫酸反应:
D.氯化钡溶液与稀硫酸反应:
【答案】C
【解析】因为在金属的活泼性顺序排列表中Fe的活泼性强于Cu,因此Fe可以从硫酸铜溶液中置换出
Cu单质,Fe变为+2价,铜由+2价变为单质铜,故A正确;氢氧化钠和盐酸的反应为酸碱中和反应,反应中氢氧化钠的OH-与盐酸的H+结合生成HO,故B正确;铁与稀盐酸反应是生成的为Fe2+,正确的离子方
2
程式为:Fe+2H+=Fe2++H ↑,故C错误;氯化钡溶液与稀硫酸反应;Ba2+和SO 2-结合生成BaSO 沉淀,离子
2 4 4
方程式正确,故D正确;故选C。
8.某溶液中大量存在5种离子:NO 、SO 、Al3+、H+、M,其物质的量之比为n(NO )∶n(SO
)∶n(Al3+)∶n(H+)∶n(M)=2∶3∶1∶3∶1,则M可能为
A.Ba2+ B.Na+ C.Mg2+ D.Cl-
【答案】C
【解析】n(NO )∶n(SO )∶n(Al3+)∶n(H+)∶n(M)=2∶3∶1∶3∶1,可设n(NO )、n(SO )、n(Al3+)、n(H+)、n(M)
分别为2mol、3mol、1mol、3mol、1mol,根据电荷守恒可知:3n(Al3+)+n(H+)=6mol<n(NO )+2n(SO
)=8mol,故M为阳离子,且M所带的电荷数为:8-6=2,说明M为带有2个正电荷的离子,又因为钡离子
和硫酸根离子不能大量共存,所以选项中只有Mg2+符合。故选C。
9.将100 mL0.1 mol· L-1Hg(NO) 溶液和100 mL 0. 2 mol· L-1 KI溶液混合,恰好完全反应,有红色沉
3 2
淀M生成,过滤后向滤液中加入淀粉溶液,溶液变蓝,测得纯净物M的物质的量为0.005 mol。下列推断
正确的是
A.上述反应是非氧化还原反应
B.M的化学式为HgI
2
C.上述反应生成了I
2
D.参加反应的KI全部作还原剂
【答案】C
【解析】向滤液中加入淀粉溶液,溶液变蓝,说明生成物有I,I元素的化合价由-1价升高至0价,涉
2
及元素化合价的变化,因此上述反应是氧化还原反应,A错误;根据题干信息,100 mL0.1 mol·
L-1Hg(NO) 溶液和100 mL 0. 2 mol· L-1 KI溶液混合,恰好完全反应,生成0.005molM,根据氧化还原反应
3 2
得失电子守恒可得,M的化学式为HgI,B错误;向滤液中加入淀粉溶液,溶液变蓝,说明生成物有I,C
2
正确;产物为HgI和I,说明KI中部分I的化合价未发生改变,因此参加反应的KI没有全部作还原剂,D
2
错误;答案选C。
10.水合肼(N H·H O)的性质类似氨水。利用水合肼处理铜氨{[Cu(NH )]2+}废液回收铜粉的实验流程
2 4 2 3 4
如图:下列说法错误的是
A.上述三步反应过程均为氧化还原反应
B.反应1的目的是制备NaClO
C.合成水合肼的反应中每消耗1molCO(NH ) 转移电子数为N
2 2 A
D.反应2完成后要用到过滤操作
【答案】C
【解析】NaOH稀溶液与Cl 在一定温度下反应生成NaClO、NaCl和HO,向反应后的混合液中加入
2 2
CO(NH),NaClO与CO(NH) 反应合成(N H•H O),同时有NaCl和NaCO 生成,发生反应为
2 2 2 2 2 4 2 2 3
CO(NH)+ClO-+2OH-=N H•H O+Cl-+CO ;向反应后的溶液中继续加入铜氨溶液发生反应2[Cu(NH )]2+
2 2 2 4 2 3 4
+N H•H O+4OH- 2Cu↓+N ↑+8NH↑+5H O,有Cu析出,经过滤得到铜粉,以此分析解答。
2 4 2 2 3 2
第一步反应中Cl元素发生变化,第二步反应中Cl、N元素化合价发生变化,第三步反应中Cu、N元素化
合价发生变化,所以上述三步反应过程均为氧化还原反应,故A正确;合成水合肼时需要用到NaClO,则
反应1的目的是用氢氧化钠溶液与氯气反应制备NaClO,故B正确;NaClO与CO(NH) 反应合成水合肼的
2 2
过程中,N元素化合价由-3升高至-2,化合价升高1价,消耗1molCO(NH ) 时需要转移2mol电子,转移
2 2
电子数为2N ,故C错误;反应2为2[Cu(NH )]2++N H•H O+4OH- 2Cu↓+N ↑+8NH↑+5H O,有Cu析
A 3 4 2 4 2 2 3 2
出,通过过滤操作得到铜粉,故D正确;故选C。
二、选择题:本题共5个小题,每小题4分,共20分。在每小题给出的四个选项中,只有一项或两项
是符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只
选一个且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
11.下列关于某无色溶液中离子检验的操作、现象与结论对应正确的是
检验操作 现象 结论
A 加入盐酸酸化的氯化钡 产生白色沉淀 一定有SO 2-
4
B 加入酚酞溶液 溶液显红色 一定有
C 加入足量稀盐酸 产生无色气体 一定有CO2-
3D 加入硝酸银 产生白色沉淀 一定有
【答案】B
【解析】加入盐酸酸化的氯化钡,能产生白色沉淀的是SO ,也可能有 ,白色沉淀为BaSO 或者
4
AgCl,A项错误;加入酚酞溶液溶液变红色的是碱性溶液,则一定有 ,B项正确;加入稀盐酸能产生
无色气体的离子 或 ,产生的气体为CO,C项错误;加入硝酸银产生白色沉淀的离子为 、
2
SO ,白色沉淀为AgCl、Ag SO ,D项错误;答案选B。
2 4
12.下列指定反应的离子方程式书写正确的是
A.硫化氢气体通入氯化铁溶液:2Fe3++S2-=S↓+2Fe2+
B.向碳酸氢铵溶液中加入足量石灰水:Ca2++HCO +OH-=CaCO ↓+H O
3 2
C.向稀硝酸中加入过量铁粉:Fe+NO +4H+=Fe3++NO↑+2HO
2
D.用氨水吸收少量SO :2NH •H O+SO =2NH +SO +H O
2 3 2 2 2
【答案】D
【解析】硫化氢和氯化铁反应生成硫、氯化亚铁和氯化氢,硫化氢应该写成化学式,反应的离子方程
式为:2Fe3++H S=S↓+2Fe2++2H+,A错误;向碳酸氢铵溶液中加入足量石灰水,反应生成碳酸钙沉淀、一
2
水合氨和水,反应的离子方程式应为:NH +Ca2++HCO +2OH-=CaCO ↓+H O+NH ·H O,B错误;过量铁
3 2 3 2
粉和稀硝酸反应生成硝酸亚铁、一氧化氮和水,反应的离子方程式为:3Fe+2NO +8H+=3Fe2+
+2NO↑+4HO,C错误;少量SO 和氨水反应生成亚硫酸铵和水,反应的离子方程式应为:
2 2
2NH ·H O+SO =2NH +SO +H O,D正确;故选D。
3 2 2 2
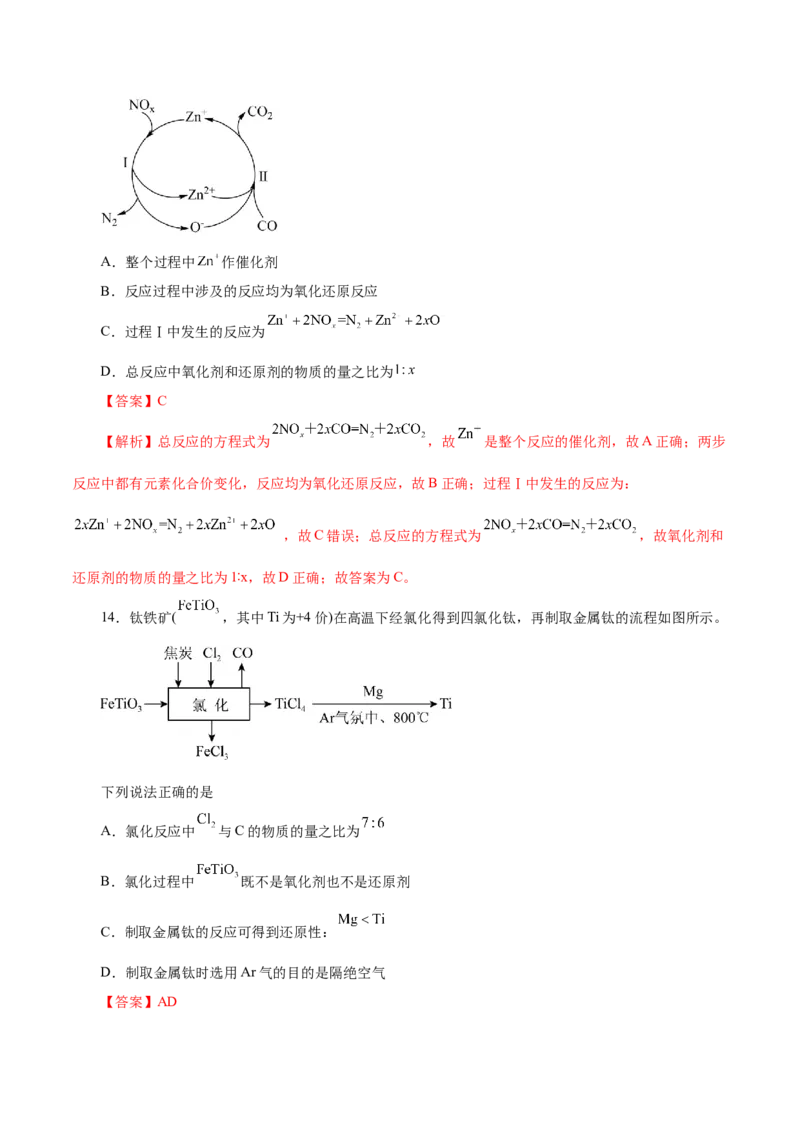
13.用 方法可将汽车尾气中的 和 转化为无污染的气体,下列说法错误的是A.整个过程中 作催化剂
B.反应过程中涉及的反应均为氧化还原反应
C.过程Ⅰ中发生的反应为
D.总反应中氧化剂和还原剂的物质的量之比为
【答案】C
【解析】总反应的方程式为 ,故 是整个反应的催化剂,故A正确;两步
反应中都有元素化合价变化,反应均为氧化还原反应,故B正确;过程Ⅰ中发生的反应为:
,故C错误;总反应的方程式为 ,故氧化剂和
还原剂的物质的量之比为1∶x,故D正确;故答案为C。
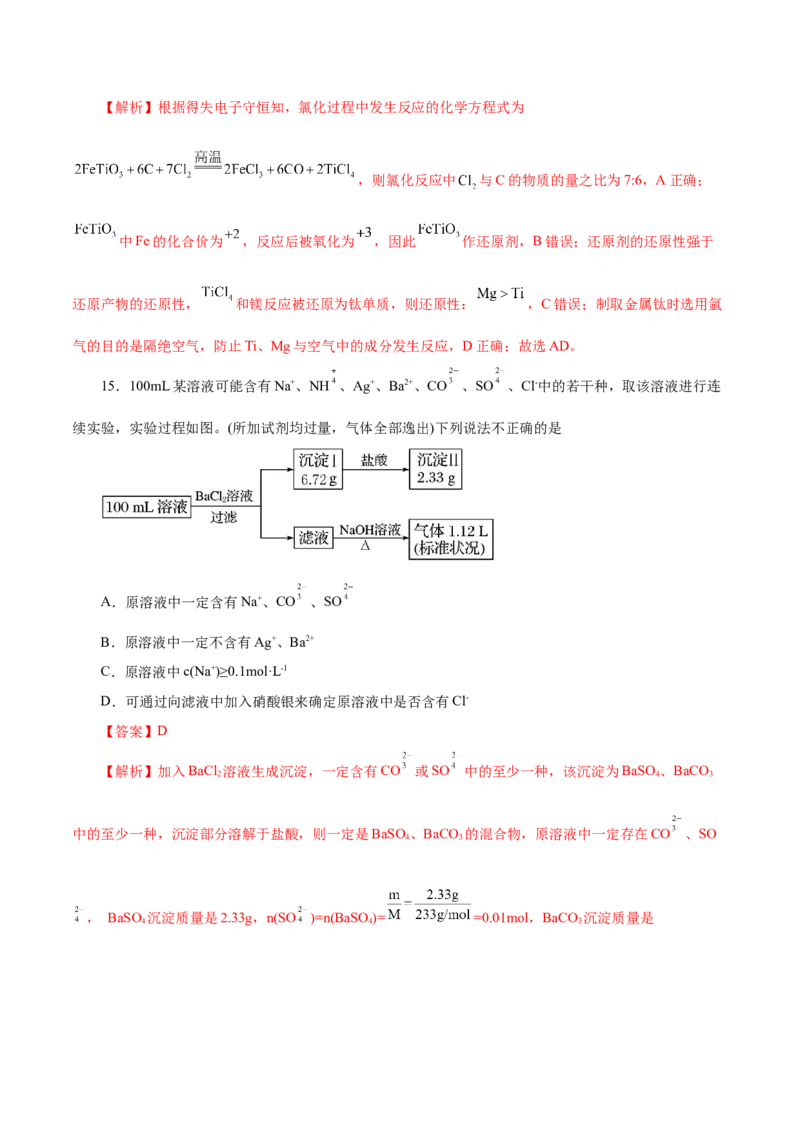
14.钛铁矿( ,其中Ti为+4价)在高温下经氯化得到四氯化钛,再制取金属钛的流程如图所示。
下列说法正确的是
A.氯化反应中 与C的物质的量之比为
B.氯化过程中 既不是氧化剂也不是还原剂
C.制取金属钛的反应可得到还原性:
D.制取金属钛时选用Ar气的目的是隔绝空气
【答案】AD【解析】根据得失电子守恒知,氯化过程中发生反应的化学方程式为
,则氯化反应中 与C的物质的量之比为7:6,A正确;
中Fe的化合价为 ,反应后被氧化为 ,因此 作还原剂,B错误;还原剂的还原性强于
还原产物的还原性, 和镁反应被还原为钛单质,则还原性: ,C错误;制取金属钛时选用氩
气的目的是隔绝空气,防止Ti、Mg与空气中的成分发生反应,D正确;故选AD。
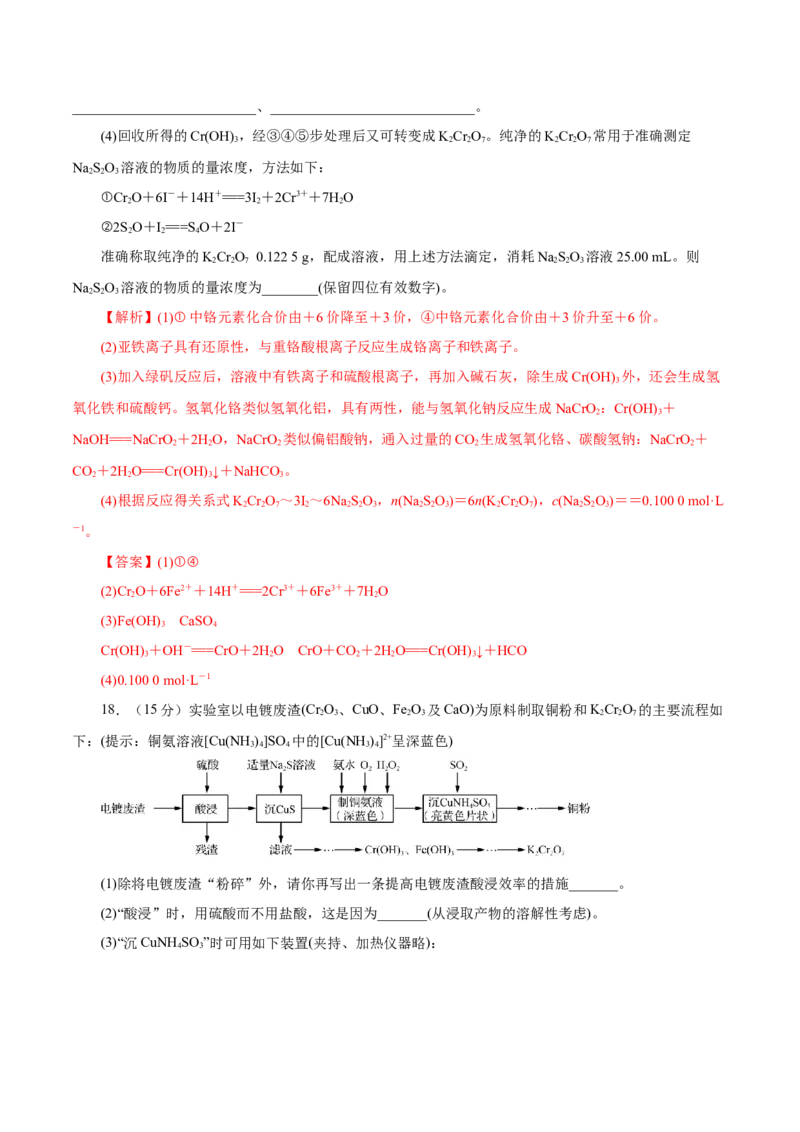
15.100mL某溶液可能含有Na+、NH 、Ag+、Ba2+、CO 、SO 、Cl-中的若干种,取该溶液进行连
续实验,实验过程如图。(所加试剂均过量,气体全部逸出)下列说法不正确的是
A.原溶液中一定含有Na+、CO 、SO
B.原溶液中一定不含有Ag+、Ba2+
C.原溶液中c(Na+)≥0.1mol·L-1
D.可通过向滤液中加入硝酸银来确定原溶液中是否含有Cl-
【答案】D
【解析】加入BaCl 溶液生成沉淀,一定含有CO 或SO 中的至少一种,该沉淀为BaSO、BaCO
2 4 3
中的至少一种,沉淀部分溶解于盐酸,则一定是BaSO、BaCO 的混合物,原溶液中一定存在CO 、SO
4 3
, BaSO 沉淀质量是2.33g,n(SO )=n(BaSO )= =0.01mol,BaCO 沉淀质量是
4 4 36.27g-2.33g=3.94g,n(CO )=n(BaCO )= =0.02mol,CO 和Ag+、Ba2+不共存,原溶液中一定
3
不存在Ag+、Ba2+;所得到的滤液中加入氢氧化钠,加热生成的气体为NH ,原溶液中一定含有NH ,
3
n(NH )=n(NH )= =0.05mol;正电荷量为0.05mol,负电荷量为
3
0.01mol×2+0.02mol×2=0.06mol>0.05mol,根据电荷守恒可知,一定含有Na+,可能含有Cl-,据此分析解
答。
由分析可知,原溶液中一定含有Na+、CO 、SO ,A正确;CO 和Ag+、Ba2+不共存,原溶液中一定不
存在Ag+、Ba2+,B正确;正电荷量为0.05mol,负电荷量为0.01mol×2+0.02mol×2=0.06mol>0.05mol,根据
电荷守恒可知,一定含有Na+,n(Na+)≥0.01mol,100mL原溶液中c(Na+)≥ 0.1mol·L-1,C正
确;
由于加入BaCl 溶液引入Cl-,则通过向滤液中加入硝酸银不能确定原溶液中是否含有Cl-,D错误;故选
2
D。
第II卷 (非选择题共50分)
三、非选择题:本题共4个小题,共50分。
16.(10分)Ⅰ.为探究NH HCO 和NaOH的反应,设计实验方案如下:向含0.1 mol NH HCO 的溶
4 3 4 3
液中加入0.1 mol NaOH,反应完全后,滴加氯化钙稀溶液。
(1)若有沉淀,则NH HCO 与NaOH的反应可能为_______________________________ (写离子方程
4 3
式)。
(2)若无沉淀,则NH HCO 与NaOH的反应可能为________________________________ (写离子方程
4 3
式)。
Ⅱ.Ba(OH) 溶液与NaHSO 溶液的反应:
2 4
(1)当反应后的溶液呈碱性时,反应离子方程式:_________________________________。
(2)当n[Ba(OH) ]∶n(NaHSO)=1∶2时反应的离子方程式:_______________________。
2 4
Ⅲ.按要求完成下列离子方程式。
(1)生物硝化法:在富氧条件下,通过硝酸盐菌的作用,将氨氮(以NH表示,下同)氧化成硝酸盐,其反应的离子方程式为_________________________________________________。
(2)将过碳酸钠(2Na CO·3H O)溶于水配成溶液,加入适量稀硫酸,再加入足量KI,充分反应后加入
2 3 2 2
少量淀粉试剂,溶液呈蓝色,其反应的离子方程式为____________________。
【解析】Ⅰ.NHHCO 电离出的HCO、NH都能与OH-反应,滴加少量的氢氧化钠,反应完全后,滴
4 3
加氯化钙稀溶液,有沉淀生成,说明是HCO与OH-反应生成碳酸根离子,反应离子方程式为HCO+OH-
===CO+HO;没有沉淀生成,说明NH与OH-反应生成一水合氨,反应离子方程式为NH+OH-
2
===NH·H O。
3 2
Ⅱ.Ba(OH) 溶液与NaHSO 溶液反应,反应后的溶液呈碱性,说明Ba(OH) 溶液过量,反应离子方程
2 4 2
式为Ba2++OH-+SO+H+===BaSO ↓+HO;当n[Ba(OH) ]∶n(NaHSO)=1∶2时,生成硫酸钡、水的物质的
4 2 2 4
量之比为1∶2,反应离子方程式为Ba2++2OH-+SO+2H+===BaSO ↓+2HO。
4 2
Ⅲ.(1)在富氧条件下,通过硝酸盐菌的作用, NH被氧气氧化为NO,反应离子方程式为NH+
2O=====NO+HO+2H+;(2)加入足量KI,充分反应后加入少量淀粉试剂,溶液呈蓝色,说明I-被过氧
2 2
化氢氧化为碘单质,反应离子方程式为HO+2I-+2H+===I +2HO。
2 2 2 2
【答案】Ⅰ.(1)HCO+OH-===CO+HO
2
(2)NH+OH-===NH·H O
3 2
Ⅱ.(1)Ba2++OH-+SO+H+===BaSO ↓+HO
4 2
(2)Ba2++2OH-+SO+2H+===BaSO ↓+2HO
4 2
Ⅲ.(1)NH+2O=====NO+HO+2H+
2 2
(2)H O+2I-+2H+===I +2HO
2 2 2 2
17.(10分)铬及其化合物常被应用于冶金、化工、电镀、制药等行业,但使用后的废水因其中含高
价铬的化合物而毒性很强,必须进行处理。工业上往往采取下列循环工艺防止铬的污染:
(1)上述各步反应中属于氧化还原反应的是________(填序号)。
(2)第①步,含Cr O的废水在酸性条件下用绿矾(FeSO ·7H O)处理,写出并配平反应的离子方程式:
2 4 2
_________________________________________________________________。
(3)第②步,向上述反应后的溶液中加入适量的碱石灰,使铬离子转变为Cr(OH) 沉淀。处理后,沉淀
3
物中除了Cr(OH) 外,还有________、________(写化学式)。已知Cr(OH) 性质类似Al(OH) ,是既能与强
3 3 3
酸反应又能与强碱反应的两性物质,写出从该沉淀物中分离出Cr(OH) 的离子方程式:
3__________________________、_____________________________。
(4)回收所得的Cr(OH) ,经③④⑤步处理后又可转变成KCr O。纯净的KCr O 常用于准确测定
3 2 2 7 2 2 7
NaSO 溶液的物质的量浓度,方法如下:
2 2 3
①Cr O+6I-+14H+===3I +2Cr3++7HO
2 2 2
②2S O+I===S O+2I-
2 2 4
准确称取纯净的KCr O 0.122 5 g,配成溶液,用上述方法滴定,消耗NaSO 溶液25.00 mL。则
2 2 7 2 2 3
NaSO 溶液的物质的量浓度为________(保留四位有效数字)。
2 2 3
【解析】(1)①中铬元素化合价由+6价降至+3价,④中铬元素化合价由+3价升至+6价。
(2)亚铁离子具有还原性,与重铬酸根离子反应生成铬离子和铁离子。
(3)加入绿矾反应后,溶液中有铁离子和硫酸根离子,再加入碱石灰,除生成Cr(OH) 外,还会生成氢
3
氧化铁和硫酸钙。氢氧化铬类似氢氧化铝,具有两性,能与氢氧化钠反应生成NaCrO :Cr(OH) +
2 3
NaOH===NaCrO+2HO,NaCrO 类似偏铝酸钠,通入过量的CO 生成氢氧化铬、碳酸氢钠:NaCrO +
2 2 2 2 2
CO+2HO===Cr(OH) ↓+NaHCO 。
2 2 3 3
(4)根据反应得关系式KCr O~3I~6NaSO,n(Na SO)=6n(K Cr O),c(Na SO)==0.100 0 mol·L
2 2 7 2 2 2 3 2 2 3 2 2 7 2 2 3
-1。
【答案】(1)①④
(2)Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
(3)Fe(OH) CaSO
3 4
Cr(OH) +OH-===CrO+2HO CrO+CO+2HO===Cr(OH) ↓+HCO
3 2 2 2 3
(4)0.100 0 mol·L-1
18.(15分)实验室以电镀废渣(CrO、CuO、Fe O 及CaO)为原料制取铜粉和KCr O 的主要流程如
2 3 2 3 2 2 7
下:(提示:铜氨溶液[Cu(NH )]SO 中的[Cu(NH )]2+呈深蓝色)
3 4 4 3 4
(1)除将电镀废渣“粉碎”外,请你再写出一条提高电镀废渣酸浸效率的措施_______。
(2)“酸浸”时,用硫酸而不用盐酸,这是因为_______(从浸取产物的溶解性考虑)。
(3)“沉CuNH SO ”时可用如下装置(夹持、加热仪器略):
4 3①制取SO 的化学方程式为_______。
2
②“沉CuNH SO ”时,反应的离子方程式:_______。
4 3
③反应完成的实验现象是_______。
(4)提纯“沉CuNH SO ”后的溶液可获得硫酸铵晶体。设计实验证明某晶体是硫酸铵。实验过程:取少
4 3
许晶体溶于水配成溶液,_______。(完成实验过程,试剂任选。)
【答案】(1)升高酸浸温度或适当增大硫酸浓度、搅拌等合理答案
(2)硫酸可将CaO转化为CaSO 渣而除去
4
(3) Cu+2H SO (浓) CuSO +SO↑+2H O 2[Cu(NH )]2+ +3SO +4H O=2CuNH SO ↓+ +6
2 4 4 2 2 3 4 2 2 4 3
上层清液由深蓝色逐渐变为几乎无色
(4)取少许溶液于试管中,加入少许盐酸,无现象后滴加氯化钡溶液,如果产生白色沉淀,证明阴离子
是硫酸根;再取少许溶液于另一只试管中,加入氢氧化钠溶液,加热,用湿润的红色石蕊试纸在管口检
验,如果试纸变蓝,证明阳离子是铵根离子,则该晶体是硫酸铵
【解析】分析流程图,电镀废渣用硫酸酸浸,残渣为与硫酸反应后的难溶物或微溶物,结合电镀废渣
的成分可分析出残渣主要成分。向滤液中加入适量硫化钠溶液,进行沉CuS,可知主要发生Cu2++S2-=CuS↓
的反应,过滤后滤液和滤渣经不同方式处理。滤液中主要含有Fe3+和Cr3+,经一系列处理,将Fe3+和Cr3+转
化为Cr(OH) 和Fe(OH) ,结合题意,根据二者的溶度积的差异,除去Fe(OH) ,Cr(OH) 经过一系列变化最
3 3 3 3
终得到KCr O.向滤渣中加入氨水、O 和HO,制深蓝色的铜氨液,后向铜氨液中加入SO 得到亮黄色
2 2 7 2 2 2 2
片状的沉CuNH SO ,最终经一系列变化得到铜粉,据此进行分析。
4 3
(1)根据外界对反应速率的影响因素可知,升高酸浸温度或适当增大硫酸浓度、搅拌等均可以提高电镀
废渣酸浸效率;
(2)“酸浸”时,用硫酸而不用盐酸,这是因为硫酸可以将氧化钙转化为硫酸钙而除去;
(3)①铜与浓硫酸加热生成二氧化硫、硫酸铜和水,所以化学方程式为:Cu+2H SO (浓)
2 4
CuSO +SO↑+2H O;
4 2 2
②在[Cu(NH )]SO 溶液中,通入SO ,发生氧化还原反应,Cu元素化合价由+2价,得电子变为+1
3 4 4 2价,SO 中S元素化合价由+4价失电子变为+6价,根据得失电子守恒、原子守恒和电荷守恒,离子方程式
2
为:2[Cu(NH )]2+ +3SO +4H O=2CuNH SO ↓+ +6 ;
3 4 2 2 4 3
③[Cu(NH )]SO 溶液呈蓝色,通入SO ,反应生成CuNH SO 和Cu,反应完成的实验现象是上层清液
3 4 4 2 4 3
由深蓝色逐渐变为几乎无色;
(4)该实验的目的是设计实验验证某晶体是硫酸铵,即检验是否含有 和 ,实验操作如下,取少
许溶液于试管中,加入少许盐酸,无现象后滴加氯化钡溶液,如果产生白色沉淀,证明阴离子是硫酸根;
再取少许溶液于另一只试管中,加入氢氧化钠溶液,加热,用湿润的红色石蕊试纸在管口检验,如果试纸
变蓝,证明阳离子是铵根离子,则该晶体是硫酸铵;
19.(15分)工业上以软锰矿(主要成分MnO )为原料,通过液相法生产KMnO 。即在碱性条件下用
2 4
氧气氧化MnO 得到KMnO ,分离后得到的KMnO ,再用惰性材料为电极电解KMnO 溶液得到
2 2 4 2 4 2 4
KMnO ,其生产工艺简略如下:
4
(1)反应器中反应的化学方程式为____________________________________________。
(2)生产过程中最好使用含MnO 80%以上的富矿,因为MnO 含量最低的贫矿中Al、Si的氧化物含量
2 2
较高,会导致KOH消耗量__________(填“偏高”或“偏低”)。
(3)电解槽中总的离子反应方程式为_________________________________________。
(4)在传统工艺中得到KMnO 后,向其中通入适量CO 反应生成黑色固体、KMnO 等,反应的化学方
2 4 2 4
程式为_____________________________________________。上述反应中氧化剂与还原剂的质量比为
____________。与该传统工艺相比,电解法的优势是____________________________________________。
(5)用高锰酸钾测定草酸结晶水合物的纯度:称草酸晶体样品0.500 g溶于水配制成100 mL溶液,取出
20.00 mL用0.020 0 mol·L-1的酸性KMnO 溶液滴定(杂质不反应),至溶液呈浅粉红色且半分钟内不褪去,
4
消耗KMnO 溶液14.80 mL,则该草酸晶体的纯度为__________。(结果保留三位有效数字)(已知该草酸结
4
晶水合物HC O·2H O的相对分子质量为126)
2 2 4 2
【解析】(1)根据题给流程和信息知,反应器中KOH、MnO 和O 反应生成KMnO 和HO,利用化合
2 2 2 4 2
价升降法配平,反应的化学方程式为4KOH+2MnO +O===2K MnO +2HO。(2)若贫矿中Al、Si的氧化
2 2 2 4 2
物含量较高,发生反应:Al O+2KOH===2KAlO+HO、SiO+2KOH===K SiO+HO,会导致KOH消
2 3 2 2 2 2 3 2
耗量偏高。(3)电解锰酸钾溶液制备高锰酸钾,电解槽中阳极发生氧化反应,MnO失电子转化为MnO,电极反应式为2MnO-2e-===2MnO,阴极发生还原反应,电极反应式为2HO+2e-===H ↑+2OH-,两式相
2 2
加得总的离子反应方程式为2MnO+2HO=====2MnO+2OH-+H↑。(4)向KMnO 溶液中通入适量CO,
2 2 2 4 2
二者反应生成黑色固体二氧化锰、KMnO ,利用化合价升降法配平,该反应的化学方程式为3KMnO +
4 2 4
2CO===2KMnO +MnO +2KCO。上述反应中3 mol K MnO 中有1 mol锰元素化合价由+6价降为+4价
2 4 2 2 3 2 4
生成二氧化锰,作氧化剂,有2 mol锰元素化合价由+6价升高到+7价生成高锰酸钾,作还原剂,氧化剂
与还原剂的质量比为1∶2。KMnO 的转化率为66.7%,与该传统工艺相比,电解法的优势是产率更高、
2 4
KOH循环利用。(5)酸性高锰酸钾溶液与草酸反应的离子方程式是6H++2MnO+5HC O===2Mn2++8HO
2 2 4 2
+10CO↑,则样品中草酸晶体的物质的量为n(H C O·2H O)=5×14.8×10-3×0.02× mol=3.7×10-3 mol,草
2 2 2 4 2
酸晶体的质量为3.7×10-3 mol×126 g·mol-1=0.466 2 g,则该草酸晶体的纯度为×100%≈93.2%。
【答案】(1)4KOH+2MnO +O===2K MnO +2HO
2 2 2 4 2
(2)偏高
(3)2MnO+2HO=====2MnO+2OH-+H↑
2 2
(4)3K MnO +2CO===2KMnO +MnO +2KCO 1∶2 产率更高、KOH循环利用 (5)93.2%
2 4 2 4 2 2 3