文档内容
2025新教材化学高考第一轮
专题七 原子结构 元素周期律
1.下列化学用语或图示表达错误的是( )
A.反-2-丁烯的球棍模型:
B.MgCl 的形成过程:
2
C.基态碘原子的简化电子排布式:[Kr]5s25p5
D.基态氮原子的轨道表示式:
2.1828年人类首次使用无机物氰酸铵(NH CNO,可由氯化铵和氰酸银反应制得)人工合成
4
了尿素[CO(NH ) ],揭开了人工合成有机物的序幕。下列说法正确的是( )
2 2
A.已知氰酸银微溶于水,使用氰酸银悬浊液制备氰酸铵的离子方程式为Ag++Cl- AgCl↓
B.尿素的组成元素的第一电离能由大到小的顺序为O>N>C>H
C.简单离子的半径由大到小的顺序为O2->N3->H->H+
D.氰酸铵转化为尿素,反应前后碳元素的化合价没有改变
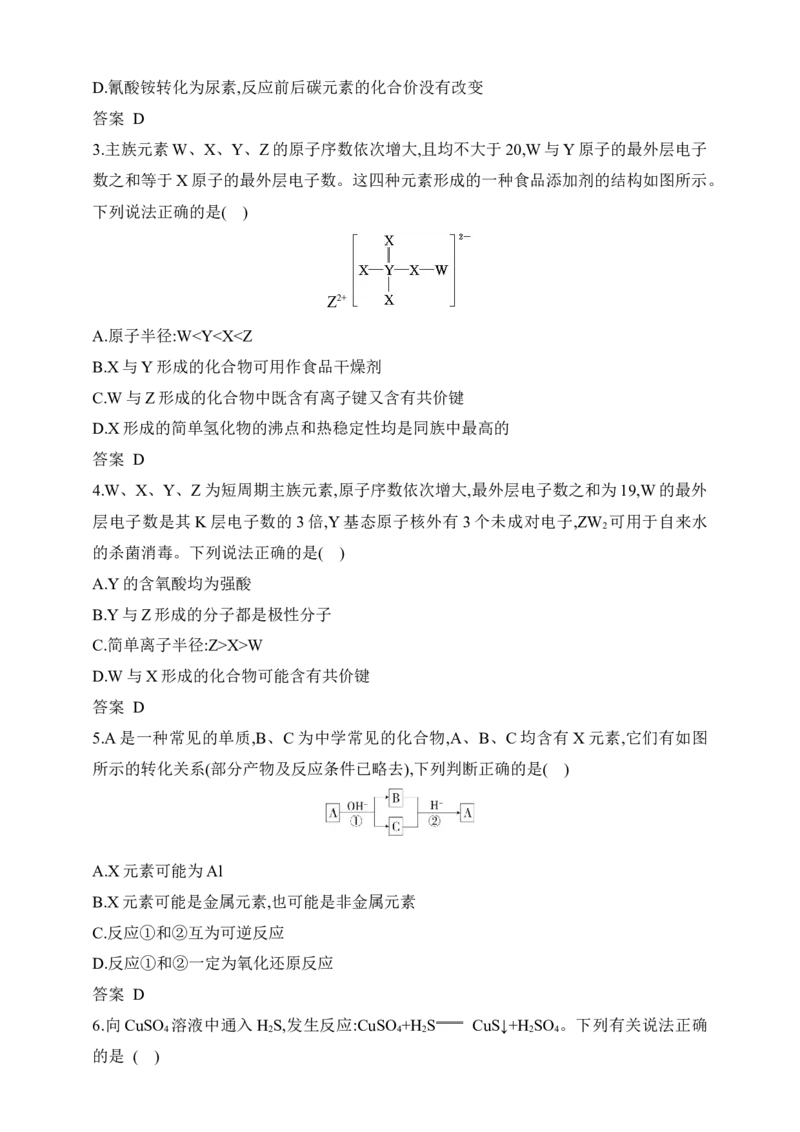
3.主族元素W、X、Y、Z的原子序数依次增大,且均不大于20,W与Y原子的最外层电子
数之和等于X原子的最外层电子数。这四种元素形成的一种食品添加剂的结构如图所示。
下列说法正确的是( )
Z2+
A.原子半径:WX>W
D.W与X形成的化合物可能含有共价键
5.A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有X元素,它们有如图
所示的转化关系(部分产物及反应条件已略去),下列判断正确的是( )
A.X元素可能为Al
B.X元素可能是金属元素,也可能是非金属元素
C.反应①和②互为可逆反应
D.反应①和②一定为氧化还原反应
6.向CuSO 溶液中通入H S,发生反应:CuSO +H S CuS↓+H SO 。下列有关说法正确
4 2 4 2 2 4
的是 ( )
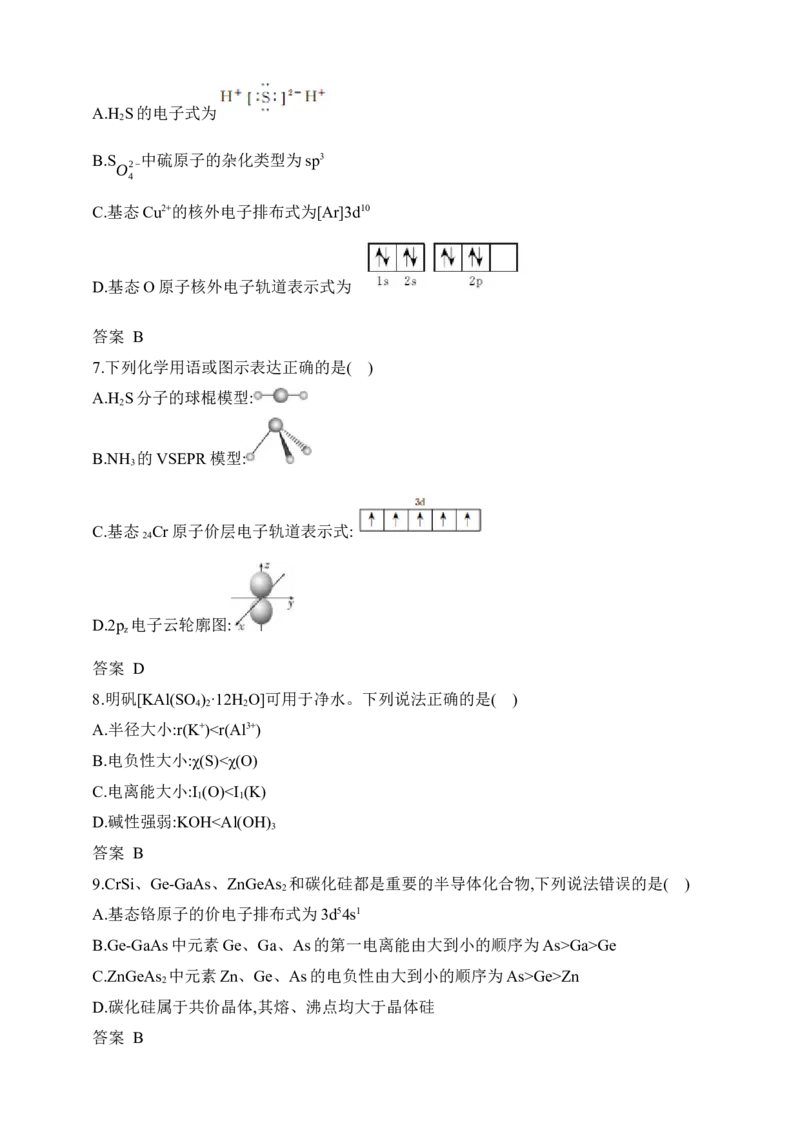
A.H S的电子式为
2
B.S 中硫原子的杂化类型为sp3
O2−
4
C.基态Cu2+的核外电子排布式为[Ar]3d10
D.基态O原子核外电子轨道表示式为
7.下列化学用语或图示表达正确的是( )
A.H S分子的球棍模型:
2
B.NH 的VSEPR模型:
3
C.基态 Cr原子价层电子轨道表示式:
24
D.2p 电子云轮廓图:
z
8.明矾[KAl(SO ) ·12H O]可用于净水。下列说法正确的是( )
4 2 2
A.半径大小:r(K+)Ga>Ge
C.ZnGeAs 中元素Zn、Ge、As的电负性由大到小的顺序为As>Ge>Zn
2
D.碳化硅属于共价晶体,其熔、沸点均大于晶体硅
10.X、Y、Z、W是原子序数依次增大的短周期元素。X和Y基态原子的s能级电子总
数均等于其p能级电子总数,Z原子的最外层电子数是Y原子最外层电子数的2倍,W和
X位于同一主族。下列说法正确的是( )
A.第一电离能:I (X)W
C.原子半径:r(W)>r(Y)>r(X)
D.简单气态氢化物的热稳定性:X>Z
11.下列化学用语不正确的是( )
A.中子数为2的氢核素:3H
B.用电子式表示H O的形成过程:
2
C.基态铬原子的价电子排布式:3d44s2
O2−
D.C 3 的空间结构模型:
12.某食品添加剂的主要成分为 WZ(RY ) ·12X Y。已知X、Y、Z、R、W为原子序数依
4 2 2
次增大的前20号元素,X、Z的周期序数等于主族序数,Y和R位于同主族,基态X、W原
子最外层电子排布式为ns1。下列叙述正确的是( )
A.原子半径:W>R>Z>Y>X
B.电负性:Y>R>X>Z>W
C.常温下,Z、W单质都能与水发生置换反应
D.R的最高价氧化物对应水化物一定有强氧化性
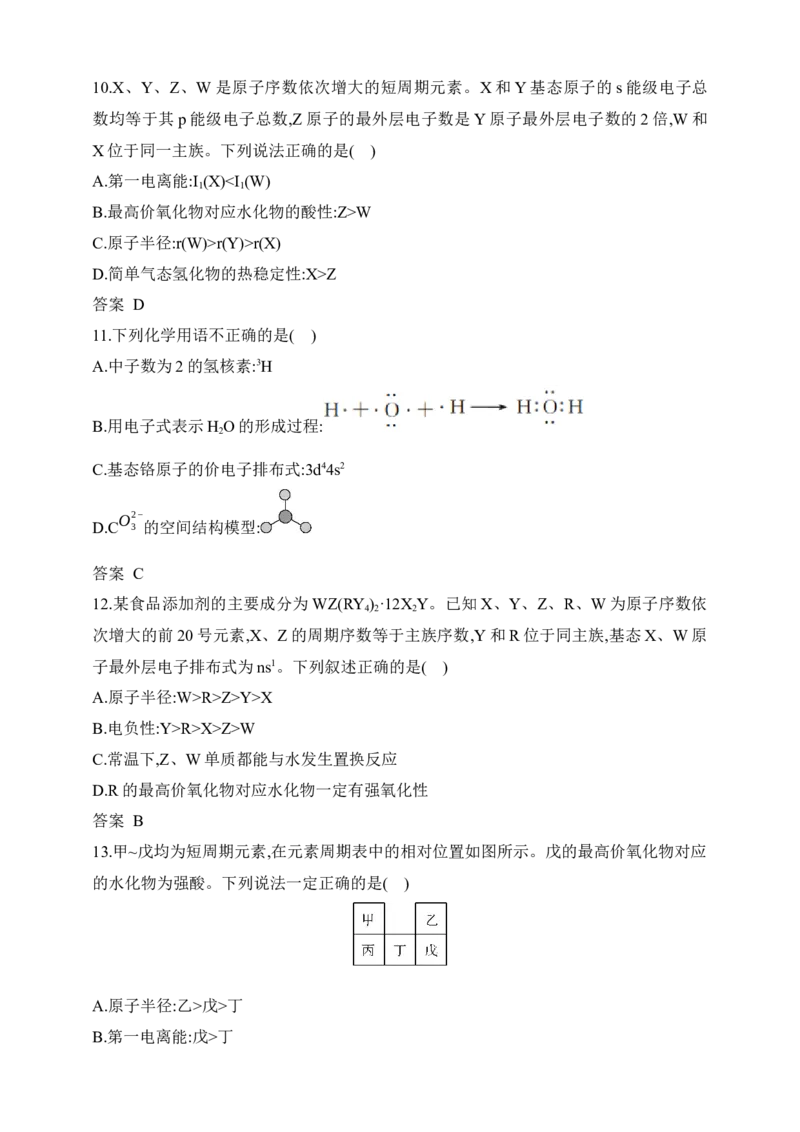
13.甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应
的水化物为强酸。下列说法一定正确的是( )A.原子半径:乙>戊>丁
B.第一电离能:戊>丁
C.甲的氢化物遇湿润的红色石蕊试纸变蓝
D.丙的最高价氧化物对应的水化物能与强碱反应
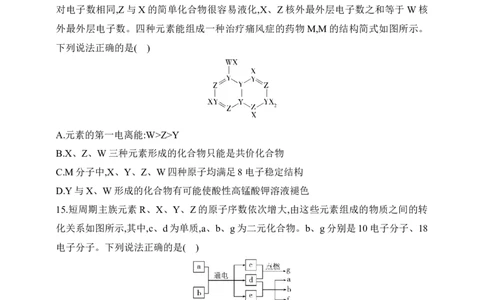
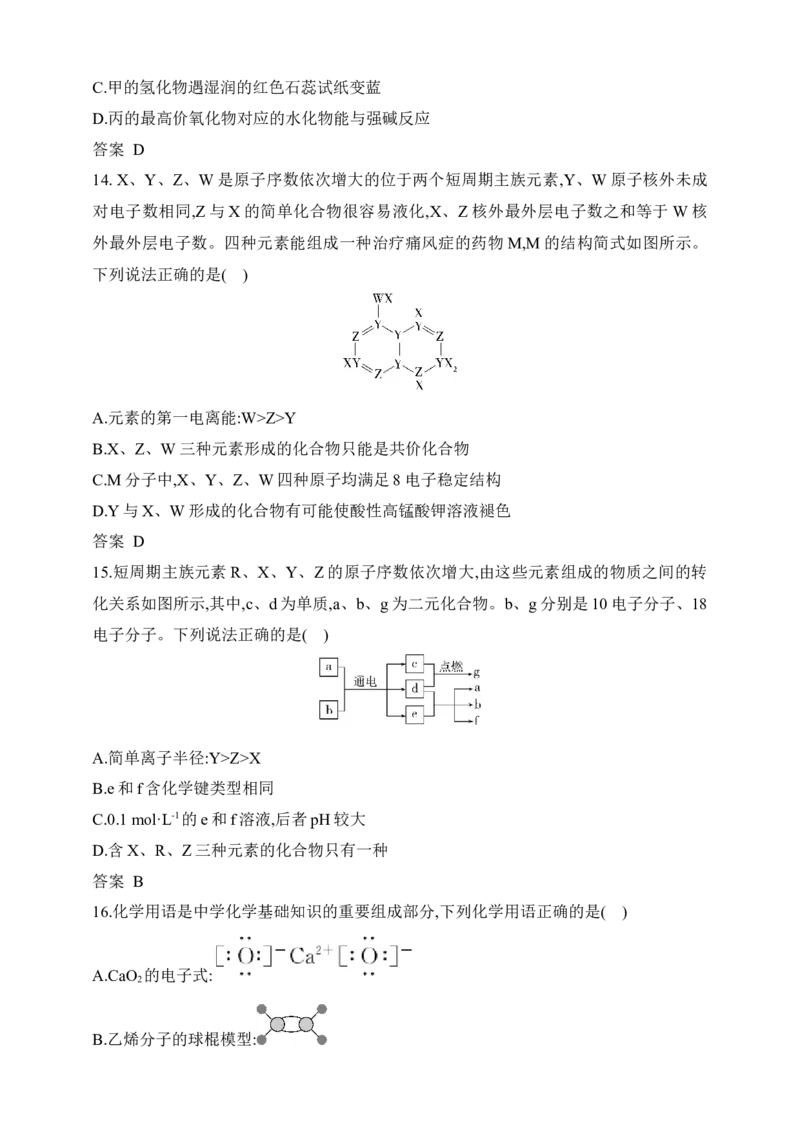
14. X、Y、Z、W是原子序数依次增大的位于两个短周期主族元素,Y、W原子核外未成
对电子数相同,Z与X的简单化合物很容易液化,X、Z核外最外层电子数之和等于 W核
外最外层电子数。四种元素能组成一种治疗痛风症的药物M,M的结构简式如图所示。
下列说法正确的是( )
A.元素的第一电离能:W>Z>Y
B.X、Z、W三种元素形成的化合物只能是共价化合物
C.M分子中,X、Y、Z、W四种原子均满足8电子稳定结构
D.Y与X、W形成的化合物有可能使酸性高锰酸钾溶液褪色
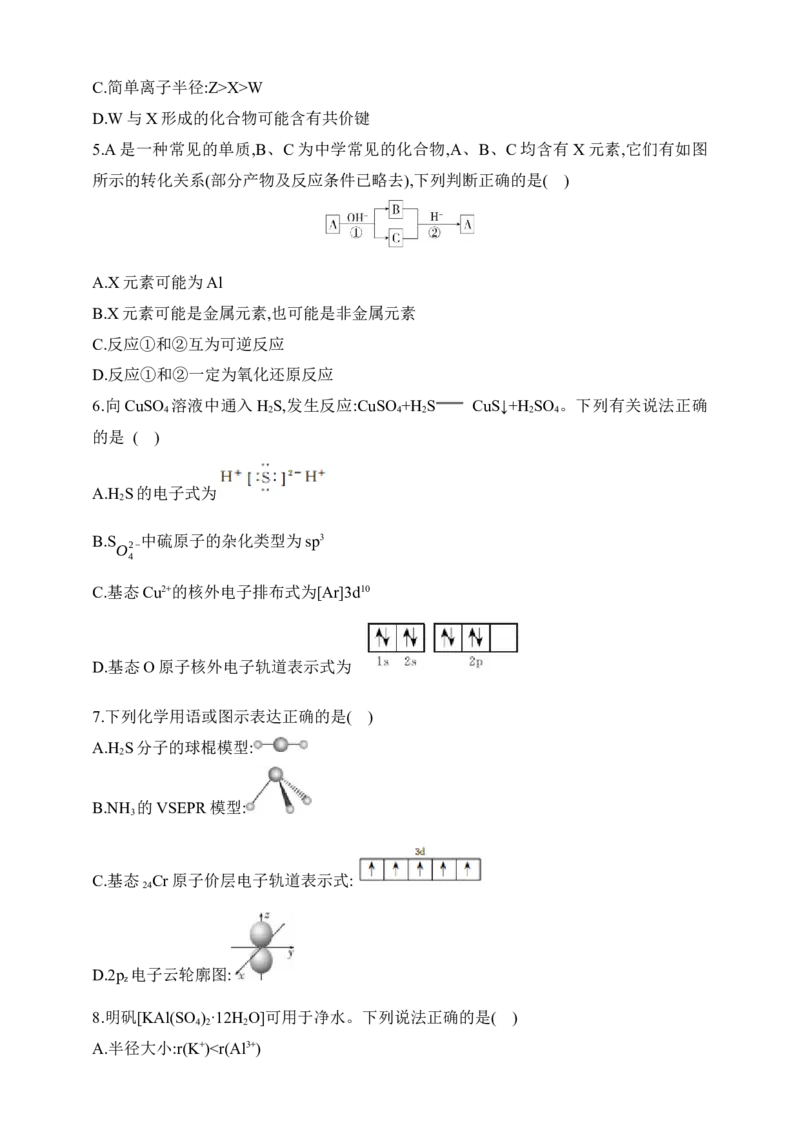
15.短周期主族元素R、X、Y、Z的原子序数依次增大,由这些元素组成的物质之间的转
化关系如图所示,其中,c、d为单质,a、b、g为二元化合物。b、g分别是10电子分子、18
电子分子。下列说法正确的是( )
A.简单离子半径:Y>Z>X
B.e和f含化学键类型相同
C.0.1 mol·L-1的e和f溶液,后者pH较大
D.含X、R、Z三种元素的化合物只有一种
16.化学用语是中学化学基础知识的重要组成部分,下列化学用语正确的是( )
A.CaO 的电子式:
2B.乙烯分子的球棍模型:
C.37Cl-的结构示意图:
D. Na CO 溶液显碱性的原因:C +2H O H CO +2OH-
2 3 O2− 2 2 3
3
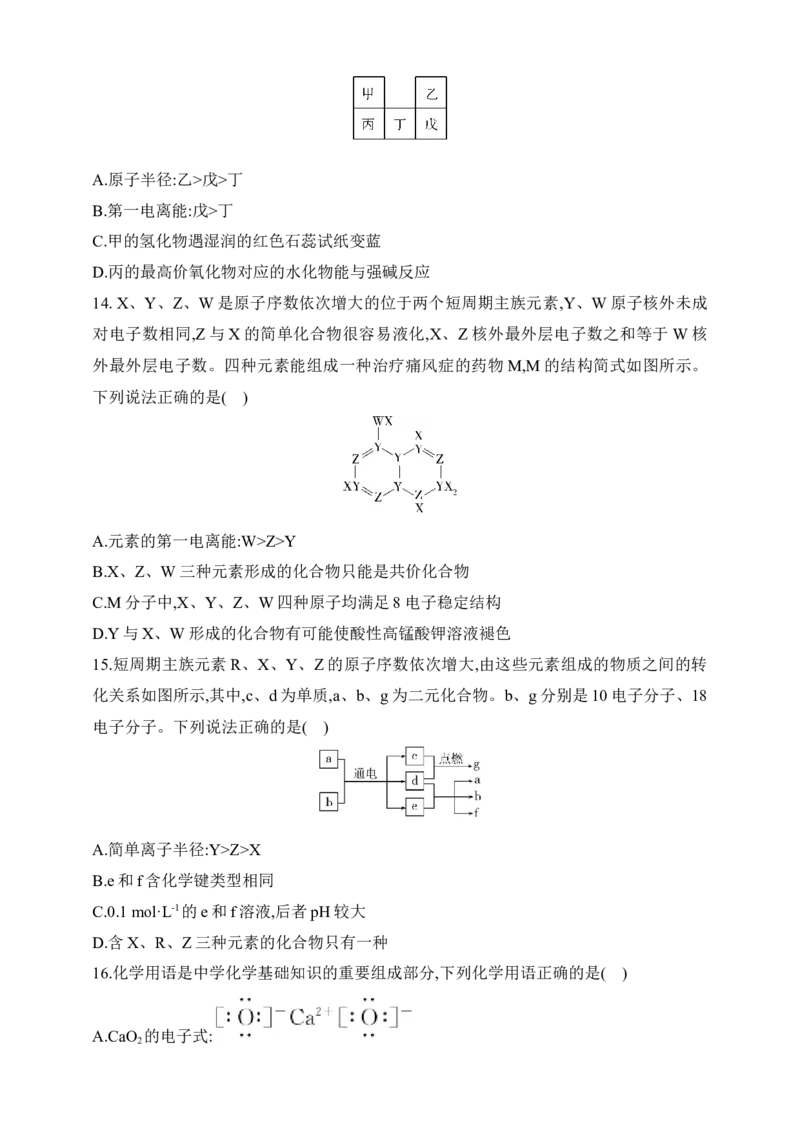
17.2022年12月,首架国产大飞机C919正式交付,国之重器,世界瞩目。铼(Re)是生产飞机
发动机叶片必不可少的材料。X、Y、Z、Q、W是原子序数依次增大且位于不同主族的
短周期元素,其中X、Y、Z三种元素可与铼元素组成一种化合物(结构如图),该化合物与
X的单质反应可得到铼。Q是地壳中含量最丰富的金属元素,Z与W形成的化合物为共
价晶体。下列说法正确的是 ( )
A.第一电离能:Z>Y>W>Q
B.图中的阳离子存在三个共价键和一个配位键,四个键的性质不同
C.熔点:W晶体大于W、Y形成的晶体
D.Q的最高价氧化物对应水化物可以和强碱反应
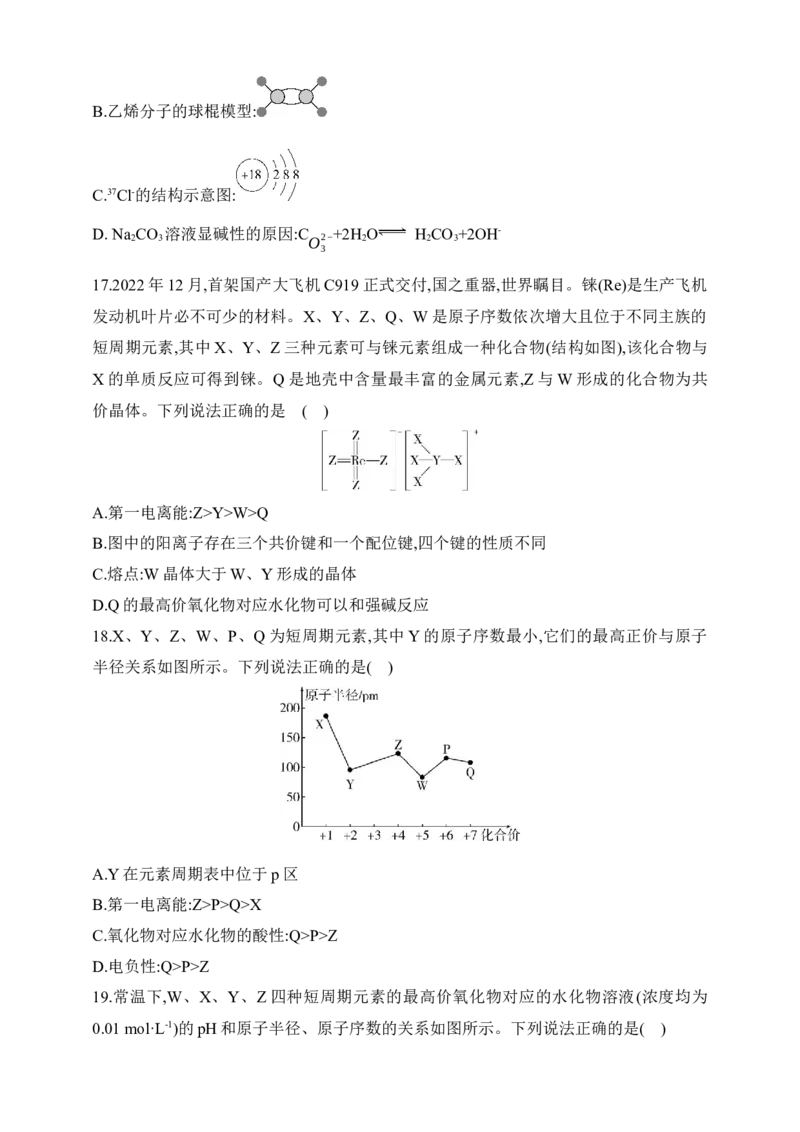
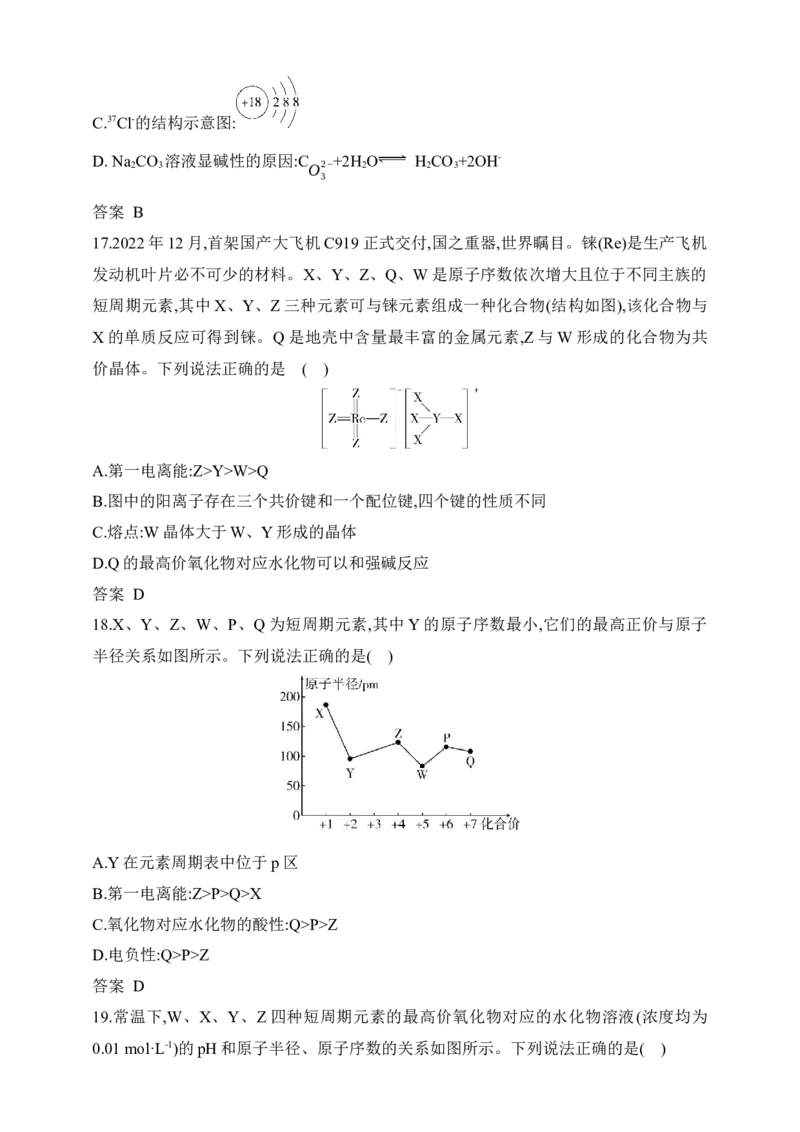
18.X、Y、Z、W、P、Q为短周期元素,其中Y的原子序数最小,它们的最高正价与原子
半径关系如图所示。下列说法正确的是( )
A.Y在元素周期表中位于p区
B.第一电离能:Z>P>Q>X
C.氧化物对应水化物的酸性:Q>P>Z
D.电负性:Q>P>Z
19.常温下,W、X、Y、Z四种短周期元素的最高价氧化物对应的水化物溶液(浓度均为
0.01 mol·L-1)的pH和原子半径、原子序数的关系如图所示。下列说法正确的是( )A.第一电离能:Z>Y>X
B.X Y 含有极性共价键和非极性共价键
2 2
C.工业上通过电解XZ的水溶液来制取X的单质
D.Z的单质具有强氧化性和漂白性
专题七 原子结构 元素周期律
1.下列化学用语或图示表达错误的是( )
A.反-2-丁烯的球棍模型:
B.MgCl 的形成过程:
2
C.基态碘原子的简化电子排布式:[Kr]5s25p5
D.基态氮原子的轨道表示式:
答案 C
2.1828年人类首次使用无机物氰酸铵(NH CNO,可由氯化铵和氰酸银反应制得)人工合成
4
了尿素[CO(NH ) ],揭开了人工合成有机物的序幕。下列说法正确的是( )
2 2
A.已知氰酸银微溶于水,使用氰酸银悬浊液制备氰酸铵的离子方程式为Ag++Cl- AgCl↓
B.尿素的组成元素的第一电离能由大到小的顺序为O>N>C>H
C.简单离子的半径由大到小的顺序为O2->N3->H->H+D.氰酸铵转化为尿素,反应前后碳元素的化合价没有改变
答案 D
3.主族元素W、X、Y、Z的原子序数依次增大,且均不大于20,W与Y原子的最外层电子
数之和等于X原子的最外层电子数。这四种元素形成的一种食品添加剂的结构如图所示。
下列说法正确的是( )
Z2+
A.原子半径:WX>W
D.W与X形成的化合物可能含有共价键
答案 D
5.A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有X元素,它们有如图
所示的转化关系(部分产物及反应条件已略去),下列判断正确的是( )
A.X元素可能为Al
B.X元素可能是金属元素,也可能是非金属元素
C.反应①和②互为可逆反应
D.反应①和②一定为氧化还原反应
答案 D
6.向CuSO 溶液中通入H S,发生反应:CuSO +H S CuS↓+H SO 。下列有关说法正确
4 2 4 2 2 4
的是 ( )A.H S的电子式为
2
B.S 中硫原子的杂化类型为sp3
O2−
4
C.基态Cu2+的核外电子排布式为[Ar]3d10
D.基态O原子核外电子轨道表示式为
答案 B
7.下列化学用语或图示表达正确的是( )
A.H S分子的球棍模型:
2
B.NH 的VSEPR模型:
3
C.基态 Cr原子价层电子轨道表示式:
24
D.2p 电子云轮廓图:
z
答案 D
8.明矾[KAl(SO ) ·12H O]可用于净水。下列说法正确的是( )
4 2 2
A.半径大小:r(K+)Ga>Ge
C.ZnGeAs 中元素Zn、Ge、As的电负性由大到小的顺序为As>Ge>Zn
2
D.碳化硅属于共价晶体,其熔、沸点均大于晶体硅
答案 B10.X、Y、Z、W是原子序数依次增大的短周期元素。X和Y基态原子的s能级电子总
数均等于其p能级电子总数,Z原子的最外层电子数是Y原子最外层电子数的2倍,W和
X位于同一主族。下列说法正确的是( )
A.第一电离能:I (X)W
C.原子半径:r(W)>r(Y)>r(X)
D.简单气态氢化物的热稳定性:X>Z
答案 D
11.下列化学用语不正确的是( )
A.中子数为2的氢核素:3H
B.用电子式表示H O的形成过程:
2
C.基态铬原子的价电子排布式:3d44s2
O2−
D.C 3 的空间结构模型:
答案 C
12.某食品添加剂的主要成分为 WZ(RY ) ·12X Y。已知X、Y、Z、R、W为原子序数依
4 2 2
次增大的前20号元素,X、Z的周期序数等于主族序数,Y和R位于同主族,基态X、W原
子最外层电子排布式为ns1。下列叙述正确的是( )
A.原子半径:W>R>Z>Y>X
B.电负性:Y>R>X>Z>W
C.常温下,Z、W单质都能与水发生置换反应
D.R的最高价氧化物对应水化物一定有强氧化性
答案 B
13.甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应
的水化物为强酸。下列说法一定正确的是( )
A.原子半径:乙>戊>丁
B.第一电离能:戊>丁C.甲的氢化物遇湿润的红色石蕊试纸变蓝
D.丙的最高价氧化物对应的水化物能与强碱反应
答案 D
14. X、Y、Z、W是原子序数依次增大的位于两个短周期主族元素,Y、W原子核外未成
对电子数相同,Z与X的简单化合物很容易液化,X、Z核外最外层电子数之和等于 W核
外最外层电子数。四种元素能组成一种治疗痛风症的药物M,M的结构简式如图所示。
下列说法正确的是( )
A.元素的第一电离能:W>Z>Y
B.X、Z、W三种元素形成的化合物只能是共价化合物
C.M分子中,X、Y、Z、W四种原子均满足8电子稳定结构
D.Y与X、W形成的化合物有可能使酸性高锰酸钾溶液褪色
答案 D
15.短周期主族元素R、X、Y、Z的原子序数依次增大,由这些元素组成的物质之间的转
化关系如图所示,其中,c、d为单质,a、b、g为二元化合物。b、g分别是10电子分子、18
电子分子。下列说法正确的是( )
A.简单离子半径:Y>Z>X
B.e和f含化学键类型相同
C.0.1 mol·L-1的e和f溶液,后者pH较大
D.含X、R、Z三种元素的化合物只有一种
答案 B
16.化学用语是中学化学基础知识的重要组成部分,下列化学用语正确的是( )
A.CaO 的电子式:
2
B.乙烯分子的球棍模型:C.37Cl-的结构示意图:
D. Na CO 溶液显碱性的原因:C +2H O H CO +2OH-
2 3 O2− 2 2 3
3
答案 B
17.2022年12月,首架国产大飞机C919正式交付,国之重器,世界瞩目。铼(Re)是生产飞机
发动机叶片必不可少的材料。X、Y、Z、Q、W是原子序数依次增大且位于不同主族的
短周期元素,其中X、Y、Z三种元素可与铼元素组成一种化合物(结构如图),该化合物与
X的单质反应可得到铼。Q是地壳中含量最丰富的金属元素,Z与W形成的化合物为共
价晶体。下列说法正确的是 ( )
A.第一电离能:Z>Y>W>Q
B.图中的阳离子存在三个共价键和一个配位键,四个键的性质不同
C.熔点:W晶体大于W、Y形成的晶体
D.Q的最高价氧化物对应水化物可以和强碱反应
答案 D
18.X、Y、Z、W、P、Q为短周期元素,其中Y的原子序数最小,它们的最高正价与原子
半径关系如图所示。下列说法正确的是( )
A.Y在元素周期表中位于p区
B.第一电离能:Z>P>Q>X
C.氧化物对应水化物的酸性:Q>P>Z
D.电负性:Q>P>Z
答案 D
19.常温下,W、X、Y、Z四种短周期元素的最高价氧化物对应的水化物溶液(浓度均为
0.01 mol·L-1)的pH和原子半径、原子序数的关系如图所示。下列说法正确的是( )A.第一电离能:Z>Y>X
B.X Y 含有极性共价键和非极性共价键
2 2
C.工业上通过电解XZ的水溶液来制取X的单质
D.Z的单质具有强氧化性和漂白性
答案 A