文档内容
综合大题中气体体积、固体质量的测定
1.气体体积的测量
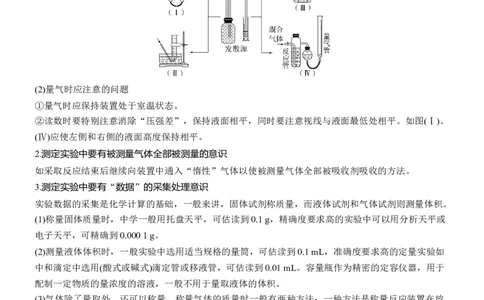
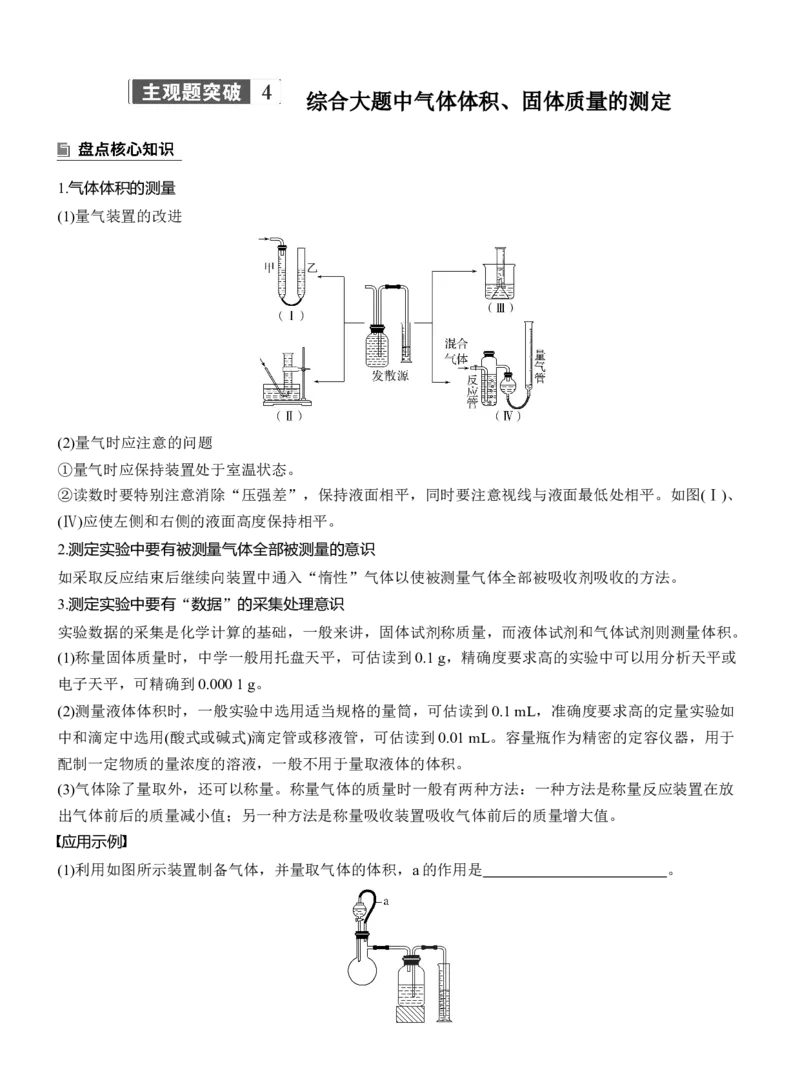
(1)量气装置的改进
(2)量气时应注意的问题
①量气时应保持装置处于室温状态。
②读数时要特别注意消除“压强差”,保持液面相平,同时要注意视线与液面最低处相平。如图(Ⅰ)、
(Ⅳ)应使左侧和右侧的液面高度保持相平。
2.测定实验中要有被测量气体全部被测量的意识
如采取反应结束后继续向装置中通入“惰性”气体以使被测量气体全部被吸收剂吸收的方法。
3.测定实验中要有“数据”的采集处理意识
实验数据的采集是化学计算的基础,一般来讲,固体试剂称质量,而液体试剂和气体试剂则测量体积。
(1)称量固体质量时,中学一般用托盘天平,可估读到0.1 g,精确度要求高的实验中可以用分析天平或
电子天平,可精确到0.000 1 g。
(2)测量液体体积时,一般实验中选用适当规格的量筒,可估读到0.1 mL,准确度要求高的定量实验如
中和滴定中选用(酸式或碱式)滴定管或移液管,可估读到0.01 mL。容量瓶作为精密的定容仪器,用于
配制一定物质的量浓度的溶液,一般不用于量取液体的体积。
(3)气体除了量取外,还可以称量。称量气体的质量时一般有两种方法:一种方法是称量反应装置在放
出气体前后的质量减小值;另一种方法是称量吸收装置吸收气体前后的质量增大值。
应用示例
(1)利用如图所示装置制备气体,并量取气体的体积,a的作用是 。(2)如图所示,用量筒量取气体体积时,应怎样操作才能读出气体的体积?
。
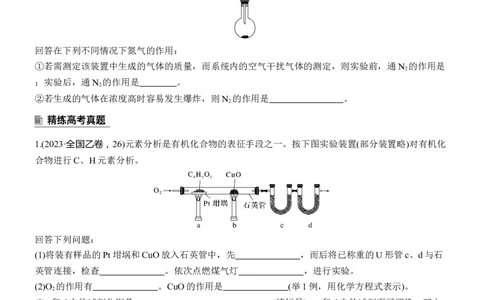
(3)实验中为了排尽空气、充分吸收某种气体、降低某种气体的浓度,常用性质稳定的气体——氮气作
载气。
回答在下列不同情况下氮气的作用:
①若需测定该装置中生成的气体的质量,而系统内的空气干扰气体的测定,则实验前,通N 的作用是
2
;实验后,通N 的作用是 。
2
②若生成的气体在浓度高时容易发生爆炸,则N 的作用是 。
2
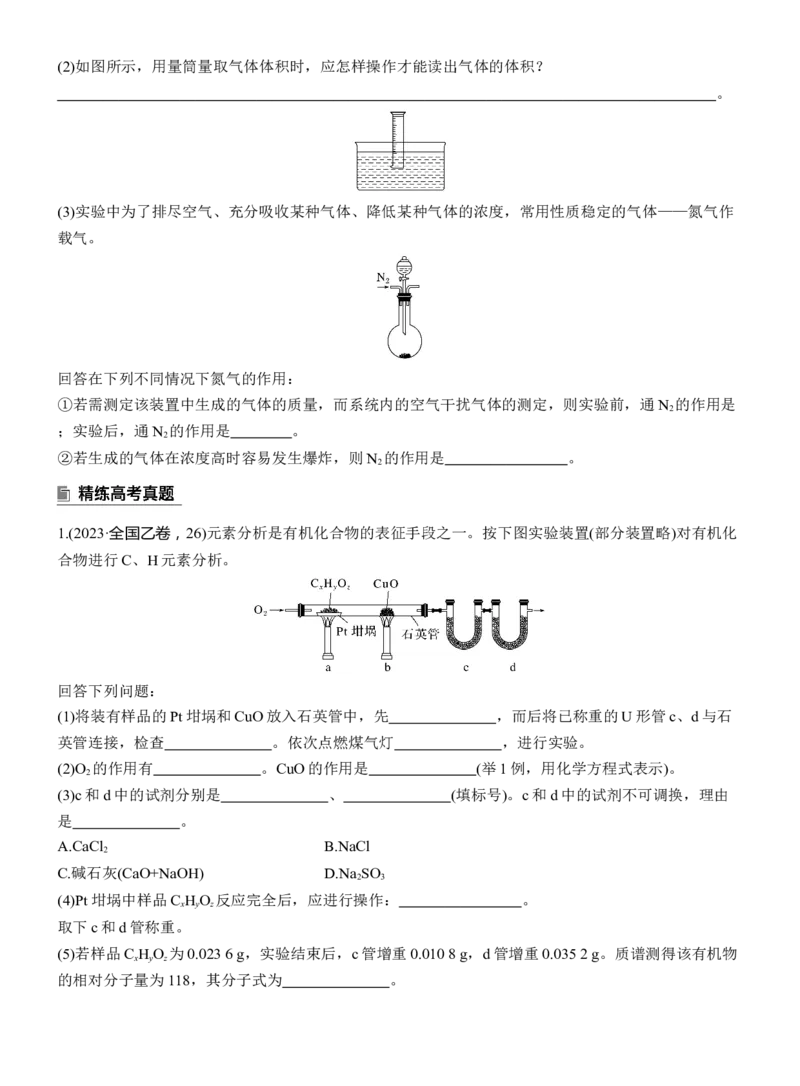
1.(2023·全国乙卷,26)元素分析是有机化合物的表征手段之一。按下图实验装置(部分装置略)对有机化
合物进行C、H元素分析。
回答下列问题:
(1)将装有样品的Pt坩埚和CuO放入石英管中,先 ,而后将已称重的U形管c、d与石
英管连接,检查 。依次点燃煤气灯 ,进行实验。
(2)O 的作用有 。CuO的作用是 (举1例,用化学方程式表示)。
2
(3)c和d中的试剂分别是 、 (填标号)。c和d中的试剂不可调换,理由
是 。
A.CaCl B.NaCl
2
C.碱石灰(CaO+NaOH) D.Na SO
2 3
(4)Pt坩埚中样品CHO 反应完全后,应进行操作: 。
x y z
取下c和d管称重。
(5)若样品CHO 为0.023 6 g,实验结束后,c管增重0.010 8 g,d管增重0.035 2 g。质谱测得该有机物
x y z
的相对分子量为118,其分子式为 。2.(2021·全国甲卷,27)胆矾(CuSO ·5H O)易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的
4 2
CuO(杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题:
(1)制备胆矾时,用到的实验仪器除量筒、酒精灯、玻璃棒、漏斗外,还必须使用的仪器有
(填字母)。
A.烧杯 B.容量瓶
C.蒸发皿 D.移液管
(2)将CuO加入到适量的稀硫酸中,加热,其主要反应的化学方程式为 ,与直接用废
铜和浓硫酸反应相比,该方法的优点是 。
(3)待CuO完全反应后停止加热,边搅拌边加入适量H O ,冷却后用NH ·H O调pH为3.5~4,再煮沸
2 2 3 2
10 min,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、 、乙醇洗涤、
,得到胆矾。其中,控制溶液pH为3.5~4的目的是 ,煮沸10 min的作用是
。
(4)结晶水测定:称量干燥坩埚的质量为m ,加入胆矾后总质量为m ,将坩埚加热至胆矾全部变为白色,
1 2
置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为m 。根据实验数据,胆矾分子中结
3
晶水的个数为 (写表达式)。
(5)下列操作中,会导致结晶水数目测定值偏高的是 (填标号)。
①胆矾未充分干燥
②坩埚未置于干燥器中冷却
③加热时有少量胆矾迸溅出来答案精析
盘点核心知识
应用示例
(1)平衡气压,使分液漏斗中的液体顺利滴下;可以消除由于液体滴入而使气体体积增大的影响
(2)应将量筒慢慢地向下移动,当量筒中的液面和水槽中的液面相平时再读数
(3)①将空气排尽 使生成的气体被指定装置充分吸收
②稀释气体,控制易爆炸气体的浓度
精练高考真题
1.(1)通入一定量的O 装置气密性 b、a (2)排出装置中的空气,氧化有机物,将生成的CO 和H O完全
2 2 2
赶入U形管中 CO+CuO Cu+CO (3)A C 碱石灰可以同时吸收水蒸气和二氧化碳 (4)熄灭a处煤
2
气灯,继续通入一定量的O ,熄灭b处煤气灯,冷却至室温,停止通O (5)C H O
2 2 4 6 4
解析 (1)实验前,应先通入一定量的O 排尽石英管中的空气,保证没有其他产物生成,而后将U形管c、
2
d与石英管连接,检查装置气密性,随后先点燃b处酒精灯后点燃a处酒精灯,保证当a处发生反应时产生
的CO能被CuO氧化生成CO 。(2)有机物氧化不充分时会生成CO,而CuO可将CO氧化为CO ,反应的
2 2
化学方程式为CO+CuO Cu+CO 。(3)有机物燃烧后生成的CO 和H O分别用碱石灰和无水CaCl 吸收,
2 2 2 2
其中c管装有无水CaCl ,d管装有碱石灰,二者不可调换,因为碱石灰能同时吸收水蒸气和二氧化碳,影
2
2×0.010 8 g 0.035 2 g
响最后分子式的确定。(5)n(H)= =0.001 2 mol;n(C)= =0.000 8 mol;n(O)=
18 g·mol-1 44 g·mol-1
(0.023 6-0.001 2×1-0.000 8×12)g
=0.000 8 mol;该有机物中C、H、O三种元素的原子个数比为
16 g·mol-1
0.000 8∶0.001 2∶0.000 8=2∶3∶2;质谱测得该有机物的相对分子量为118,则其分子式为C H O 。
4 6 4
2.(1)AC (2)CuO+H SO CuSO +H O 不会产生二氧化硫且产生等量胆矾消耗硫酸少(硫酸利用率高)
2 4 4 2
80(m -m )
(3)过滤 干燥 除尽铁,抑制硫酸铜水解 破坏氢氧化铁胶体,易于过滤 (4) 2 3 (5)①③
9(m -m )
3 1
解析 (1)制备胆矾时,根据题干信息可知,需进行溶解、过滤、结晶操作,用到的实验仪器除量筒、酒精
灯、玻璃棒、漏斗外,还必须使用的仪器有烧杯和蒸发皿。
(2)直接用废铜和浓硫酸反应生成硫酸铜、二氧化硫和水,与这种方法相比,将CuO加入到适量的稀硫酸
中,加热制备胆矾的实验方案具有的优点是不会产生二氧化硫且产生等量胆矾消耗硫酸少(硫酸利用率高)。
(3)CuO中含氧化铁杂质,溶于硫酸后会形成铁离子,为使铁元素以氢氧化铁形式沉淀完全,需控制溶液
pH为3.5~4,同时酸性环境还可抑制铜离子发生水解;操作过程中可能会生成氢氧化铁胶体,所以煮沸10
min的目的是破坏氢氧化铁胶体,使其沉淀,易于过滤。m -m m -m
(4)水的质量是(m -m ),所以胆矾(CuSO ·nH O)中n值的表达式为 2 3∶ 3 1=n∶1,解得n=
2 3 4 2 18 160
80(m -m )
2 3
。
9(m -m )
3 1
80(m -m )
2 3
(5)①胆矾未充分干燥,导致所测m 偏大,根据n= 可知,最终会导致结晶水数目测定值偏高,
2 9(m -m )
3 1
符合题意;②坩埚未置于干燥器中冷却,部分白色硫酸铜会与空气中水蒸气结合重新生成胆矾,导致所测
80(m -m )
2 3
m 偏大,根据n= 可知,最终会导致结晶水数目测定值偏低,不符合题意;③加热胆矾晶体时
3 9(m -m )
3 1
80(m -m )
2 3
有晶体从坩埚中溅出,会使m 数值偏小,根据n= 可知,最终会导致结晶水数目测定值偏高,
3 9(m -m )
3 1
符合题意。