文档内容
无机化工微流程
1.题型特点
(1)核心元素转化过程中条件控制、定性及定量关系判断。
(2)过渡金属元素价态变化特点、形成氢氧化物沉淀的条件、形成配合物的性质等。
(3)物质分离提纯中涉及仪器使用、操作注意事项的判断等。
(4)绿色化学思想的考查,主要是废物的再利用、循环物质的判断等。
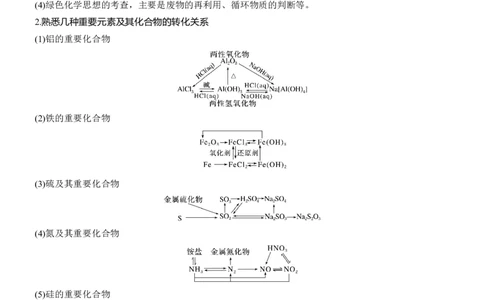
2.熟悉几种重要元素及其化合物的转化关系
(1)铝的重要化合物
(2)铁的重要化合物
(3)硫及其重要化合物
(4)氮及其重要化合物
(5)硅的重要化合物
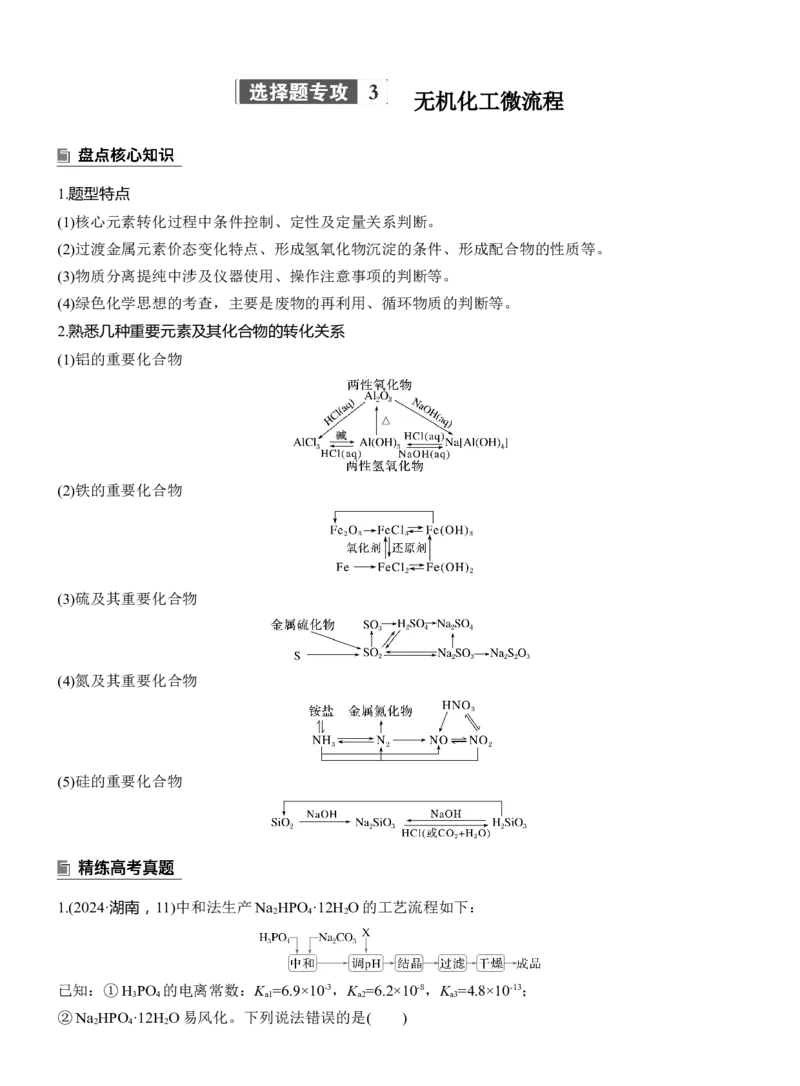
1.(2024·湖南,11)中和法生产Na HPO ·12H O的工艺流程如下:
2 4 2
已知:①H PO 的电离常数:K =6.9×10-3,K =6.2×10-8,K =4.8×10-13;
3 4 a1 a2 a3
②Na HPO ·12H O易风化。下列说法错误的是( )
2 4 2A. “中和”工序若在铁质容器中进行,应先加入Na CO 溶液
2 3
B.“调pH”工序中X为NaOH或H PO
3 4
C.“结晶”工序中溶液显酸性
D.“干燥”工序需在低温下进行
答案 C
解析 铁是较活泼金属,可与H PO 反应生成氢气,故“中和”工序若在铁质容器中进行,应先加入
3 4
Na CO 溶液,A正确;若“中和”工序加入的Na CO 过量,则需要加入酸性物质来调节pH,为了不引入
2 3 2 3
新杂质,可加入H PO ;若“中和”工序加入H PO 过量,则需要加入碱性物质来调节pH,为了不引入新
3 4 3 4
K
杂质,可加入NaOH,B正确;“结晶”工序中的溶液为饱和Na HPO
溶液,HPO2-
的水解常数K =
w
=
2 4 4 h K
a2
1.0×10-14
≈1.6×10-7>K ,Na HPO 的水解程度大于其电离程度,溶液显碱性,C错误;由于
6.2×10-8 a3 2 4
Na HPO ·12H O易风化失去结晶水,故“干燥”工序需要在低温下进行,D正确。
2 4 2
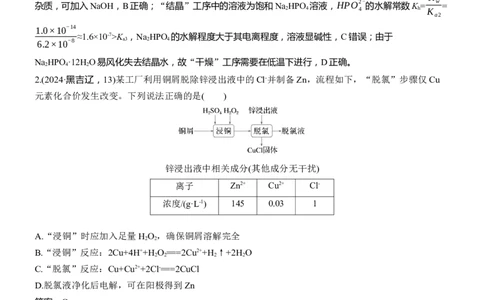
2.(2024·黑吉辽,13)某工厂利用铜屑脱除锌浸出液中的Cl-并制备Zn,流程如下,“脱氯”步骤仅Cu
元素化合价发生改变。下列说法正确的是( )
锌浸出液中相关成分(其他成分无干扰)
离子 Zn2+ Cu2+ Cl-
浓度/(g·L-1) 145 0.03 1
A.“浸铜”时应加入足量H O ,确保铜屑溶解完全
2 2
B.“浸铜”反应:2Cu+4H++H O ===2Cu2++H ↑+2H O
2 2 2 2
C.“脱氯”反应:Cu+Cu2++2Cl-===2CuCl
D.脱氯液净化后电解,可在阳极得到Zn
答案 C
解析 “浸铜”步骤中,铜屑不能溶解完全,Cu在“脱氯”步骤还需要充当还原剂,故A错误;“浸
铜”时,铜屑中加入H SO 和H O 得到Cu2+,反应的离子方程式为Cu+2H++H O ===Cu2++2H O,故B错
2 4 2 2 2 2 2
误;“脱氯”步骤中,“浸铜”后的溶液中加入锌浸出液,仅Cu元素的化合价发生改变,得到CuCl固体,
即Cu的化合价升高,Cu2+的化合价降低,发生归中反应,离子方程式为Cu+Cu2++2Cl-===2CuCl,故C正
确;脱氯液净化后电解,Zn2+应在阴极得到电子变为Zn,故D错误。
3.(2023·湖北,3)工业制备高纯硅的主要过程如下:石英砂 粗硅 SiHCl 高纯硅
3
下列说法错误的是( )
A.制备粗硅的反应方程式为SiO +2C Si+2CO↑
2
B.1 mol Si含Si—Si键的数目约为4×6.02×1023
C.原料气HCl和H 应充分去除水和氧气
2
D.生成SiHCl 的反应为熵减过程
3
答案 B
解析 在晶体硅中,每个Si与其周围的4个Si形成共价键并形成立体空间网状结构,因此,平均每个Si
形成2个共价键, 1 mol Si含Si—Si的数目约为2×6.02×1023,B说法错误;SiHCl 易水解,氢气中混有氧
3
气易爆炸,原料气HCl和H 应充分去除水和氧气 ,C说法正确;Si+3HCl SiHCl +H ,该反应是气
2 3 2
体分子数减少的反应,因此,生成SiHCl 的反应为熵减过程,D说法正确。
3
4.(2023·辽宁,10)某工厂采用如下工艺制备Cr(OH) ,已知焙烧后Cr元素以+6价形式存在,下列说法
3
错误的是( )
A.“焙烧”中产生CO
2
B.滤渣的主要成分为Fe(OH)
2
C.滤液①中Cr元素的主要存在形式为CrO2-
4
D.淀粉水解液中的葡萄糖起还原作用
答案 B
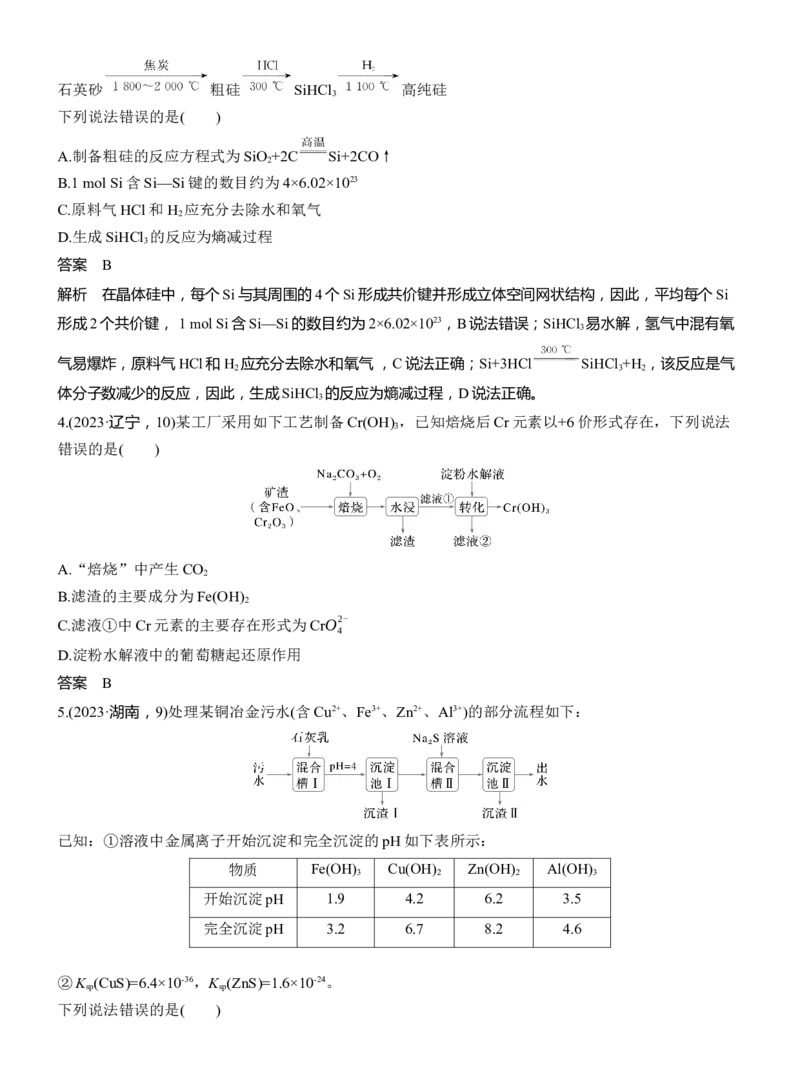
5.(2023·湖南,9)处理某铜冶金污水(含Cu2+、Fe3+、Zn2+、Al3+)的部分流程如下:
已知:①溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
物质 Fe(OH) Cu(OH) Zn(OH) Al(OH)
3 2 2 3
开始沉淀pH 1.9 4.2 6.2 3.5
完全沉淀pH 3.2 6.7 8.2 4.6
②K (CuS)=6.4×10-36,K (ZnS)=1.6×10-24。
sp sp
下列说法错误的是( )A.“沉渣Ⅰ”中含有Fe(OH) 和Al(OH)
3 3
B.Na S溶液呈碱性,其主要原因是S2-+H O HS-+OH-
2 2
c(Cu2+
)
C.“沉淀池Ⅱ”中,当Cu2+和Zn2+完全沉淀时,溶液中 =4.0×10-12
c(Zn2+
)
D.“出水”经阴离子交换树脂软化处理后,可用作工业冷却循环用水
答案 D
解析 当pH=1.9时氢氧化铁开始沉淀,当pH=3.5时氢氧化铝开始沉淀,当pH=4时,则会生成氢氧化铝
和氢氧化铁,即“沉渣Ⅰ”中含有Fe(OH) 和Al(OH) ,A正确;硫化钠溶液中的硫离子可以水解,产生氢
3 3
氧根离子,使溶液显碱性,其第一步水解的离子方程式为S2-+H O HS-+OH-,B正确;当铜离子和锌离
2
c(Cu2+ ) c(Cu2+ )·c(S2- ) K (CuS)
sp
子完全沉淀时,则硫化铜和硫化锌都达到了沉淀溶解平衡,则 = = =
c(Zn2+ ) c(Zn2+ )·c(S2- ) K (ZnS)
sp
6.4×10-36
=4.0×10-12,C正确;“出水”中除含有阴离子外,还含有大量的Na+、Ca2+等,故只经阴离子交
1.6×10-24
换树脂软化处理后,不可用作工业冷却循环用水,D错误。
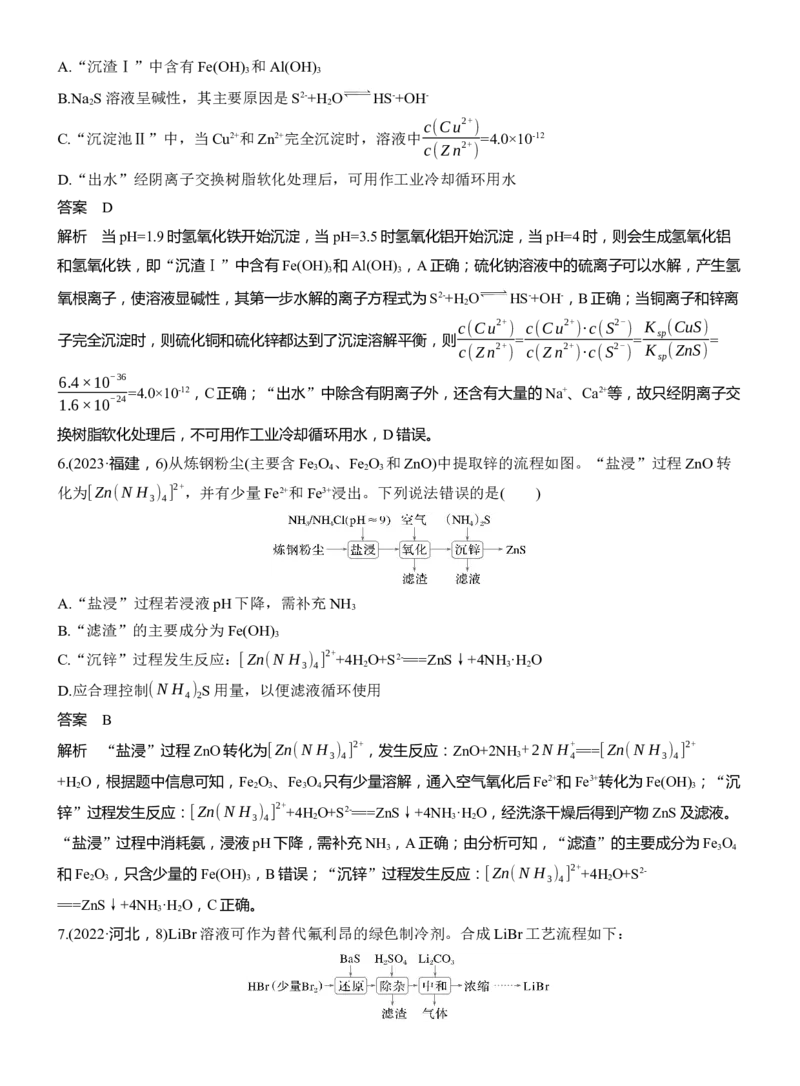
6.(2023·福建,6)从炼钢粉尘(主要含Fe O 、Fe O 和ZnO)中提取锌的流程如图。“盐浸”过程ZnO转
3 4 2 3
化为[Zn(N H ) ] 2+ ,并有少量Fe2+和Fe3+浸出。下列说法错误的是( )
3 4
A.“盐浸”过程若浸液pH下降,需补充NH
3
B.“滤渣”的主要成分为Fe(OH)
3
C.“沉锌”过程发生反应:[Zn(N H ) ] 2+ +4H O+S2-===ZnS↓+4NH ·H O
3 4 2 3 2
D.应合理控制(N H ) S用量,以便滤液循环使用
4 2
答案 B
解析 “盐浸”过程ZnO转化为[Zn(N H ) ] 2+ ,发生反应:ZnO+2NH +2N H+ ===[Zn(N H ) ] 2+
3 4 3 4 3 4
+H O,根据题中信息可知,Fe O 、Fe O 只有少量溶解,通入空气氧化后Fe2+和Fe3+转化为Fe(OH) ;“沉
2 2 3 3 4 3
锌”过程发生反应:[Zn(N H ) ] 2+ +4H O+S2-===ZnS↓+4NH ·H O,经洗涤干燥后得到产物ZnS及滤液。
3 4 2 3 2
“盐浸”过程中消耗氨,浸液pH下降,需补充NH ,A正确;由分析可知,“滤渣”的主要成分为Fe O
3 3 4
和Fe O ,只含少量的Fe(OH) ,B错误;“沉锌”过程发生反应:[Zn(N H ) ] 2+ +4H O+S2-
2 3 3 3 4 2
===ZnS↓+4NH ·H O,C正确。
3 2
7.(2022·河北,8)LiBr溶液可作为替代氟利昂的绿色制冷剂。合成LiBr工艺流程如下:下列说法错误的是( )
A.还原工序逸出的Br 用NaOH溶液吸收,吸收液直接返回还原工序
2
B.除杂工序中产生的滤渣可用煤油进行组分分离
C.中和工序中的化学反应为Li CO +2HBr===CO ↑+2LiBr+H O
2 3 2 2
D.参与反应的n(Br )∶n(BaS)∶n(H SO )为1∶1∶1
2 2 4
答案 A
解析 由流程可知,氢溴酸中含有少量的溴,加入硫化钡将溴还原生成溴化钡和硫,再加入硫酸除杂,得
到的滤渣为硫酸钡和硫;加入碳酸锂进行中和,得到的溴化锂溶液经浓缩等操作后得到产品溴化锂。还原
工序逸出的Br 用NaOH溶液吸收,吸收液中含有溴化钠和次溴酸钠等物质,若直接返回还原工序,则产
2
品中会有一定量的溴化钠,导致产品的纯度降低,A错误;除杂工序中产生的滤渣为硫酸钡和硫,硫可溶
于煤油,而硫酸钡不溶于煤油,因此可用煤油进行组分分离,B正确;中和工序中,碳酸锂和氢溴酸发生
反应生成溴化锂、二氧化碳和水,C正确;根据得失电子守恒可知,溴和硫化钡反应时物质的量之比为
1∶1;根据硫酸钡的化学组成及钡元素守恒可知,n(BaS)∶n(H SO )为1∶1,因此,参与反应的
2 4
n(Br )∶n(BaS)∶n(H SO )为1∶1∶1,D正确。
2 2 4
题型突破练 [分值:50 分]
(选择题1~5题,每小题3分,6~12题,每小题5分,共50分)
1.(2024·贵州省六校联盟高三联考)多晶硅生产工艺流程如图所示。下列说法错误的是( )
A.粗硅粉碎的目的是增大接触面积,加快反应速率
B.该流程中可以循环使用的物质是HCl、H
2
C.为提高还原时SiHCl 的转化率,可采取的措施为增大SiHCl 浓度
3 3
D.SiCl 与上述流程中的单质发生化合反应,可以制得SiHCl ,其化学方程式为3SiCl +Si+2H ===4SiHCl
4 3 4 2 3
答案 C
解析 增大SiHCl 的浓度,可增大转化速率,但不能提高还原时SiHCl 的转化率,C错误;结合流程,对
3 3
比SiHCl 和SiCl ,可知SiCl 与上述流程中的单质H 、Cl 发生化合反应生成SiHCl ,化学方程式为
3 4 4 2 2 3
3SiCl +Si+2H ===4SiHCl ,D正确。
4 2 3
2.(2024·长沙高三新高考适应性考试)《自然·天文学》发表的一篇研究论文称在金星大气中探测到一个只属
于磷化氢(PH )的特征光谱。磷化氢是一种无色、剧毒、易燃的强还原性气体,制备的流程如图所示:
3下列说法正确的是( )
A.通过晶体的X射线衍射实验获得P 分子中∠P—P—P键角为109°28'
4
B.1 mol P 与足量浓NaOH溶液反应,氧化剂和还原剂的物质的量之比为1∶3
4
C.次磷酸的分子式为H PO ,属于三元弱酸
3 2
D.含Ca P 等杂质的电石制得的乙炔中混有PH ,可用高锰酸钾除去乙炔中的PH
3 2 3 3
答案 B
解析 P 分子为正四面体形,∠P—P—P键角为60°,故A错误;P 与足量浓NaOH溶液反应,化学方程
4 4
式为P +3NaOH+3H O PH ↑+3NaH PO ,属于歧化反应,氧化剂和还原剂的物质的量之比为1∶3,故
4 2 3 2 2
B正确;次磷酸的分子式为H PO ,由于与过量浓NaOH溶液反应生成NaH PO ,说明H PO 属于一元酸,
3 2 2 2 3 2
故C错误;高锰酸钾也可氧化乙炔,故D错误。
3.(2024·贵阳高三下学期适应性测试)实验室制备FeCO 的流程如图所示,下列叙述不正确的是( )
3
A.可用KSCN溶液检验FeSO 溶液是否变质
4
B.沉淀时可用冷水浴降温以防止NH HCO 分解
4 3
C.沉淀时的离子方程式:Fe2++HCO-
===FeCO ↓+H+
3 3
D.为了使FeCO 快速干燥,洗涤操作时可用无水乙醇
3
答案 C
解析 亚铁离子变质会生成铁离子,可利用KSCN溶液检验硫酸亚铁溶液是否变质,若溶液变红,则证明
硫酸亚铁溶液已变质,故A正确;NH HCO 受热易分解,所以加NH HCO 溶液生成FeCO 沉淀时,可用
4 3 4 3 3
冷水浴降温以防止NH HCO 分解,故B正确;硫酸亚铁与NH HCO
发生反应的离子方程式为Fe2++2HCO-
4 3 4 3 3
===FeCO ↓+H O+CO ↑,故C错误。
3 2 2
4.用FeCl 溶液腐蚀覆铜板产生的腐蚀废液可回收利用,实验流程如下。下列有关说法错误的是( )
3
A.“氧化”步骤中可用的试剂为氯气
B.“调pH”后,检验Fe3+是否沉淀完全的操作:取少量上层清液于试管中,滴加几滴酸性KMnO 溶液,
4
观察溶液紫红色是否褪去
C.进行“灼烧”操作时用到的仪器主要有坩埚、坩埚钳、泥三角、三脚架和酒精灯D.“步骤X”包含的操作有蒸发浓缩、冷却结晶
答案 B
解析 “氧化”的目的是使Fe2+转化为Fe3+,为防止引入杂质离子,可用的试剂为氯气,A正确;酸性
KMnO 溶液与Fe2+反应,使溶液紫红色褪去,不能用酸性KMnO 溶液检验Fe3+是否存在,B错误;过滤除
4 4
去Fe(OH) 沉淀的滤液中含有CuCl ,加入盐酸酸化,可防止Cu2+水解,然后经蒸发浓缩、冷却结晶、过滤
3 2
就可以获得CuCl ·2H O晶体,D正确。
2 2
5.(2024·湖南常德高三模拟)世界上95%的铝业公司均使用拜耳法(原料为铝土矿,主要成分为Al O ,含少
2 3
量Fe O 、SiO 等)生产Al O ,其工艺流程如下:
2 3 2 2 3
下列说法错误的是( )
A.物质X为Fe O
2 3
B.可用过量CO 代替氢氧化铝晶种
2
C.“缓慢加热”可促使SiO 转化为水合铝硅酸钠
2
D.该流程中可循环利用的物质主要有氢氧化铝晶种
答案 D
解析 氧化铁和氢氧化钠不反应,物质X为Fe O ,A正确;过量CO 能和四羟基合铝酸钠反应生成氢氧
2 3 2
化铝沉淀,可代替氢氧化铝晶种,B正确;“缓慢加热”有利于SiO 和氢氧化钠、氧化铝反应转化为水合
2
铝硅酸钠,C正确;该流程中得到的滤液2中含有氢氧化钠,则可循环利用的物质主要为含氢氧化钠的滤
液,D错误。
6.(2024·合肥第一中学高三第一次教学质量检测)工业上以硫黄或黄铁矿为原料制备硫酸的原理示意图如图。
下列叙述错误的是( )
A.通过量的空气可将硫黄直接转化为SO
3
B.控制温度400~500 ℃可增大催化剂活性
C.吸收剂b可选用98.3%的浓硫酸D.工业上可用氨水处理尾气中的SO
2
答案 A
解析 硫黄和氧气反应只会生成SO ,A错误;选择400~500 ℃是因为V O 作催化剂时在该温度范围内催
2 2 5
化活性较好,B正确;工业制硫酸用98.3%的浓硫酸吸收SO ,不用水吸收,是因为用水会生成酸雾,C正
3
确;氨水作为一种碱性溶液可以和酸性氧化物SO 反应,工业上可用氨水处理尾气中的SO ,D正确。
2 2
7.(2024·河北衡水部分高中高三模拟)某兴趣小组用铝箔制备Al O 、AlCl ·6H O及明矾大晶体,具体流程如
2 3 3 2
图,下列说法错误的是( )
A.步骤Ⅲ,为了得到纯Al O ,需灼烧至恒重
2 3
B.步骤Ⅴ中抽滤所需仪器:布氏漏斗、吸滤瓶、抽气泵等
C.通入HCl的作用是抑制AlCl 水解和增大溶液中Cl-的浓度,有利于AlCl ·6H O结晶
3 3 2
D.步骤Ⅳ的操作是配制高于室温10~20 ℃的明矾饱和溶液,选规则明矾小晶体并悬挂在溶液中央,快速冷
却至室温,得到明矾大晶体
答案 D
解析 为了得到纯Al O ,灼烧至恒重时氢氧化铝完全分解,故A正确;AlCl 水解生成Al(OH) 和HCl,
2 3 3 3
通入HCl的作用是抑制AlCl 水解和增大溶液中Cl-的浓度,有利于AlCl ·6H O结晶,故C正确;步骤Ⅳ的
3 3 2
操作是配制高于室温10~20 ℃的明矾饱和溶液,选规则明矾小晶体并悬挂在溶液中央,自然冷却至室温,
得到明矾大晶体,故D错误。
8.为吸收工业尾气中的NO和SO ,设计如图流程,同时还能获得连二亚硫酸钠(Na S O ,其结晶水合物又
2 2 2 4
称保险粉)和NH NO 产品。
4 3
下列说法不正确的是( )
A.工业尾气中的NO和SO 排放到大气中会形成酸雨
2
B.装置Ⅱ的作用是吸收NO
C.Ce4+从阴极口流出回到装置Ⅱ循环使用
D.装置Ⅳ中氧化1 L 2
mol·L-1NO-
,至少需要标准状况下22.4 L O
2 2答案 C
解析 工业尾气中的NO可与氧气反应生成NO ,NO 与水反应得硝酸,形成硝酸型酸雨,SO 与水反应得
2 2 2
H SO ,H SO
被氧气氧化为硫酸,形成硫酸型酸雨,故A正确;装置Ⅱ中Ce4+将NO氧化为NO- 、NO-
,
2 3 2 3 3 2
故B正确;装置Ⅲ(电解槽)中阳极发生反应:Ce3+-e-===Ce4+,Ce4+从阳极口流出回到装置Ⅱ循环使用,故C
错误;装置Ⅳ中NO- 被氧气氧化为NO- 的离子方程式为2NO-
+O
===2NO- ,n(NO-
)=1 L×2 mol·L-1=2
2 3 2 2 3 2
mol,即消耗1 mol O ,标准状况下体积为22.4 L,故D正确。
2
9.(2024·福建龙岩质量检测)以炼铁厂锌灰(主要成分为ZnO,含少量的CuO、SiO 、Fe O )为原料制备ZnO
2 2 3
的流程如图所示。下列说法正确的是( )
已知:“浸取”工序中ZnO、CuO分别转化为[Zn(NH ) ]2+和[Cu(NH ) ]2+。
3 4 3 4
A.H—N—H键角:[Cu(NH ) ]2+NH ,故A错误;浸取时,SiO 、Fe O 不反应,“滤液①”
3 4 3 2 2 3
中含有金属元素的离子为[Zn(NH ) ]2+、[Cu(NH ) ]2+,加入锌粉发生反应:Zn+[Cu(NH ) ]2+===Cu+
3 4 3 4 3 4
[Zn(NH ) ]2+,因此“滤渣②”的主要成分为Cu和过量的Zn,“滤液②”中含有金属元素的离子为
3 4
[Zn(NH ) ]2+,Zn的相对原子质量大于Cu,金属元素的质量增加,即“滤液①”< “滤液②”,故B错误、
3 4
C正确;煅烧时ZnCO ·Zn(OH) 会分解,Zn为+2价,不会被氧气氧化,因此不需要隔绝空气,故D错误。
3 2
10.(2024·河北雄安新区高三模拟)从废催化剂中回收贵金属和有色金属,不仅所得金属品位高,而且投资少、
效益高。以废锆催化剂(含ZrO 、Y O 及Fe的氧化物)为原料回收氧化锆和氧化钇的部分工艺如下:
2 2 3已知:①ZrO 、Y O 可溶于热的浓硫酸;
2 2 3
②聚乙二醇可与Fe3+形成红褐色配合物,便于“离心萃取”操作进行。
下列说法错误的是( )
A.“焙烧”时,加入硫酸的浓度不宜过小,以将金属氧化物完全转化为硫酸盐进入溶液为宜
B.“离心萃取”前,加入H O 溶液,目的是将可能存在的Fe2+氧化为Fe3+,便于离心分离
2 2
C.“红褐色溶液a”的主要成分为Fe(OH) 胶体,用激光笔照射时会出现丁达尔效应
3
(C O )
D.“煅烧分解”时,化学方程式为Y 2 4 3 Y O +3CO↑+3CO ↑
2 2 3 2
答案 C
解析 根据已知信息①,硫酸浓度不宜太小,太小可能导致ZrO 、Y O 溶解不充分,影响后续回收,A正
2 2 3
确;过氧化氢为氧化剂,将亚铁离子氧化为铁离子,Fe3+与聚乙二醇形成配合物,便于离心分离,B正确;
红褐色溶液a为聚乙二醇与Fe3+形成的配合物,C错误;沉淀转化,说明氢氧化钇转化为草酸钇,草酸钇
(C O )
煅烧分解生成氧化钇:Y 2 4 3 Y O +3CO↑+3CO ↑,D正确。
2 2 3 2
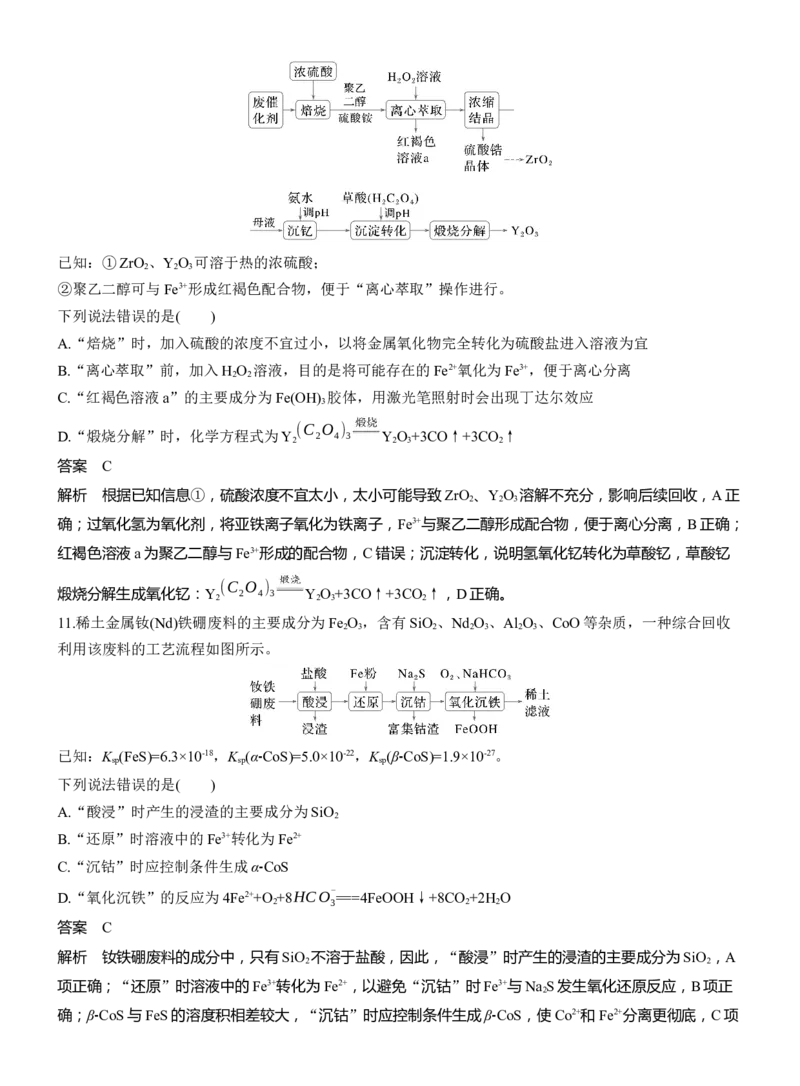
11.稀土金属钕(Nd)铁硼废料的主要成分为Fe O ,含有SiO 、Nd O 、Al O 、CoO等杂质,一种综合回收
2 3 2 2 3 2 3
利用该废料的工艺流程如图所示。
已知:K
sp
(FeS)=6.3×10-18,K
sp
(α⁃CoS)=5.0×10-22,K
sp
(β⁃CoS)=1.9×10-27。
下列说法错误的是( )
A.“酸浸”时产生的浸渣的主要成分为SiO
2
B.“还原”时溶液中的Fe3+转化为Fe2+
C.“沉钴”时应控制条件生成α⁃CoS
D.“氧化沉铁”的反应为4Fe2++O
+8HCO-
===4FeOOH↓+8CO +2H O
2 3 2 2
答案 C
解析 钕铁硼废料的成分中,只有SiO 不溶于盐酸,因此,“酸浸”时产生的浸渣的主要成分为SiO ,A
2 2
项正确;“还原”时溶液中的Fe3+转化为Fe2+,以避免“沉钴”时Fe3+与Na S发生氧化还原反应,B项正
2
确;β⁃CoS与FeS的溶度积相差较大,“沉钴”时应控制条件生成β⁃CoS,使Co2+和Fe2+分离更彻底,C项错误;“氧化沉铁”时,向含有Fe2+的溶液中通入O 并加入NaHCO ,反应生成FeOOH,反应的离子方程
2 3
式为4Fe2++O
+8HCO-
===4FeOOH↓+8CO +2H O,D项正确。
2 3 2 2
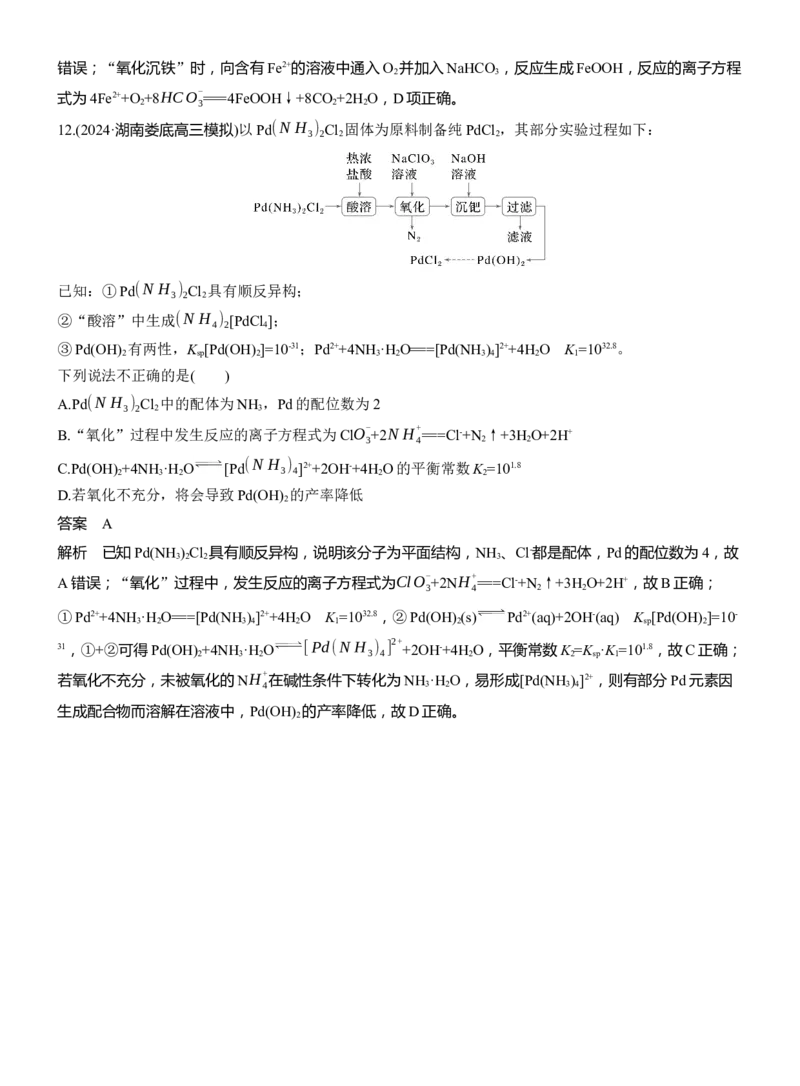
12.(2024·湖南娄底高三模拟)以Pd(N H ) Cl 固体为原料制备纯PdCl ,其部分实验过程如下:
3 2 2 2
已知:①Pd(N H ) Cl 具有顺反异构;
3 2 2
②“酸溶”中生成(N H ) [PdCl ];
4 2 4
③Pd(OH) 有两性,K [Pd(OH) ]=10-31;Pd2++4NH ·H O===[Pd(NH ) ]2++4H O K =1032.8。
2 sp 2 3 2 3 4 2 1
下列说法不正确的是( )
A.Pd(N H ) Cl 中的配体为NH ,Pd的配位数为2
3 2 2 3
B.“氧化”过程中发生反应的离子方程式为ClO- +2N H+ ===Cl-+N ↑+3H O+2H+
3 4 2 2
C.Pd(OH) +4NH ·H O [Pd(N H ) ]2++2OH-+4H O的平衡常数K =101.8
2 3 2 3 4 2 2
D.若氧化不充分,将会导致Pd(OH) 的产率降低
2
答案 A
解析 已知Pd(NH ) Cl 具有顺反异构,说明该分子为平面结构,NH 、Cl-都是配体,Pd的配位数为4,故
3 2 2 3
A错误;“氧化”过程中,发生反应的离子方程式为ClO- +2NH+
===Cl-+N ↑+3H O+2H+,故B正确;
3 4 2 2
①Pd2++4NH ·H O===[Pd(NH ) ]2++4H O K =1032.8,②Pd(OH) (s) Pd2+(aq)+2OH-(aq) K [Pd(OH) ]=10-
3 2 3 4 2 1 2 sp 2
31,①+②可得Pd(OH) +4NH ·H O [Pd(N H ) ] 2+ +2OH-+4H O,平衡常数K =K ·K =101.8,故C正确;
2 3 2 3 4 2 2 sp 1
若氧化不充分,未被氧化的NH+
在碱性条件下转化为NH ·H O,易形成[Pd(NH ) ]2+,则有部分Pd元素因
4 3 2 3 4
生成配合物而溶解在溶液中,Pd(OH) 的产率降低,故D正确。
2