文档内容
专题五 电化学
必备知识 解读
知识点一 原电池
一、原电池工作原理
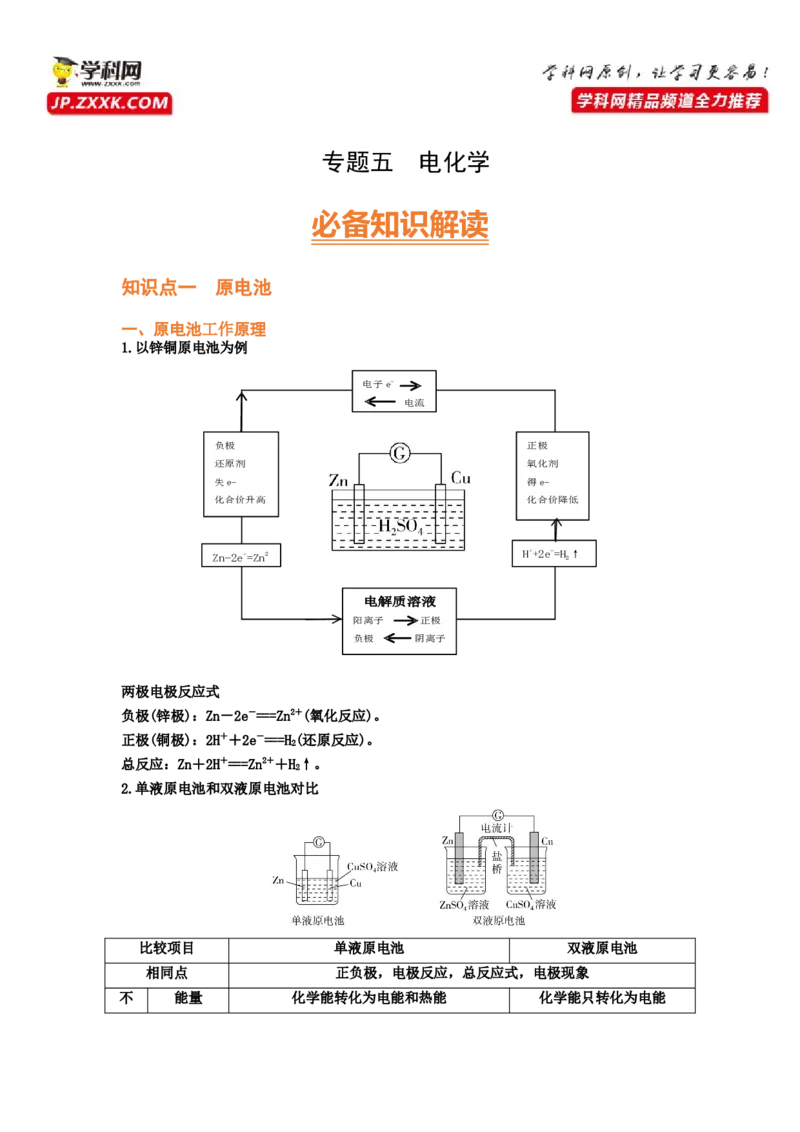
1.以锌铜原电池为例
电子e-
电流
负极 正极
还原剂 氧化剂
失e- 得e-
化合价升高 化合价降低
Zn-2e-=Zn2 H++2e-=H 2 ↑
电解质溶液
阳离子 正极
负极 阴离子
两极电极反应式
负极(锌极):Zn-2e-===Zn2+(氧化反应)。
正极(铜极):2H++2e-===H(还原反应)。
2
总反应:Zn+2H+===Zn2++H↑。
2
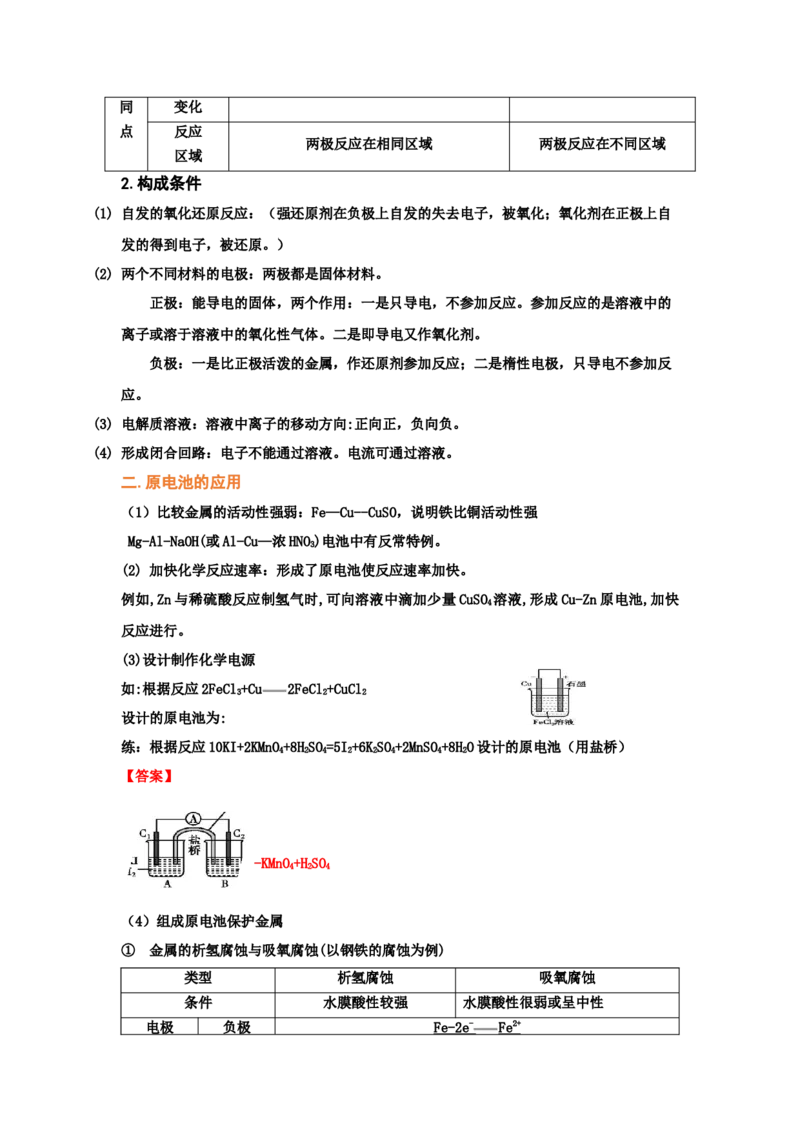
2.单液原电池和双液原电池对比
比较项目 单液原电池 双液原电池
相同点 正负极,电极反应,总反应式,电极现象
不 能量 化学能转化为电能和热能 化学能只转化为电能同 变化
点 反应
两极反应在相同区域 两极反应在不同区域
区域
2.构成条件
(1) 自发的氧化还原反应:(强还原剂在负极上自发的失去电子,被氧化;氧化剂在正极上自
发的得到电子,被还原。)
(2) 两个不同材料的电极:两极都是固体材料。
正极:能导电的固体,两个作用:一是只导电,不参加反应。参加反应的是溶液中的
离子或溶于溶液中的氧化性气体。二是即导电又作氧化剂。
负极:一是比正极活泼的金属,作还原剂参加反应;二是楕性电极,只导电不参加反
应。
(3) 电解质溶液:溶液中离子的移动方向:正向正,负向负。
(4) 形成闭合回路:电子不能通过溶液。电流可通过溶液。
二.原电池的应用
(1)比较金属的活动性强弱:Fe—Cu--CuSO,说明铁比铜活动性强
Mg-Al-NaOH(或Al-Cu—浓HNO)电池中有反常特例。
3
(2) 加快化学反应速率:形成了原电池使反应速率加快。
例如,Zn与稀硫酸反应制氢气时,可向溶液中滴加少量CuSO 溶液,形成Cu-Zn原电池,加快
4
反应进行。
(3)设计制作化学电源
如:根据反应2FeCl+Cu 2FeCl+CuCl
3 2 2
设计的原电池为:
练:根据反应10KI+2KMnO+8HSO=5I+6KSO+2MnSO+8HO设计的原电池(用盐桥)
4 2 4 2 2 4 4 2
【答案】
-KMnO+HSO
4 2 4
(4)组成原电池保护金属
① 金属的析氢腐蚀与吸氧腐蚀(以钢铁的腐蚀为例)
类型 析氢腐蚀 吸氧腐蚀
条件 水膜酸性较强 水膜酸性很弱或呈中性
电极 负极 Fe-2 e - F e 2 +反应
正极 2 H + +2 e - H↑ O+2H O+4 e - 4O H -
2 2 2
总反应式 Fe+2 H + F e 2 + + H↑ 2Fe+O+2HO 2Fe(OH)
2 2 2 2
联系 吸氧腐蚀更普遍
铁锈 4Fe(OH)+O+2HO 4Fe(OH)
2 2 2 3
形成 2Fe(OH) FeO·xHO(铁锈)+(3-x)HO
3 2 3 2 2
② 金属的原电池防护
负极 比被保护金属活泼的金属
牺牲阳极的阴极保护法——原电池原
理
正极 被保护的金属设备
知识点二 电解池
一、电解原理:电解质溶液的导电过程。
构成电解池:(1)要有电源:电势高的电极叫正极,电势低的电极叫负极,电流正极出,
电子负极出。
(2)有两个电极:发生氧化反应的极叫阳极,与电源的正极相连,阳极上的离子失去电
子;发生还原反应的极叫阴极,与电源的负极相连,阴极上的离子得到电子。
(3)有电解质溶液:电子不能通过电解质溶液,要通过离子运动导电。阳离子向阴极移
动,在阴极上得到电子,被还原;阴离子向阳极移动,在阳极上失去电子,被氧化。
电解质溶液导电必然发生氧化还原反应。
二、熟记电解的放电顺序:
阴极:阳离子放电顺序:Ag+>Fe3+>Cu2+>H+(酸)>Pb2+>Sn2+>Fe2+>Zn2+>H+(水)>Al3+>Mg2+
>Na+>Ca2+>K+。
阳极:金属电极>S2->I->Br->Cl->OH->含氧酸根离子(NO、SO、CO)>F-。
应考能力 解 密
一、原电池电极反应的书写
1. 电极反应的最先进书写方法:根据氧化还原反应原理写出电极反应式:
(1) 负极反应:负极上还原剂失去电子。可以是活泼金属或还原性气体。正极反应:正极
上氧化剂得到电子。溶液中的氧化性离子或溶于其中的氧化性气体以及氧化性的金属
氧化物。判断得失电子的物质。
(2)计算得失电子的多少:(高价-低价)×原子个数
(3)用电解质溶液中的离子,如:H+、OH-、O2-、CO2-等使两边电荷平衡。
3(4)用HO、CO 等使两边原子个数平衡。
2 2
例如:当正极上的反应物质是O 时:若电解质溶液为中性或碱性,则水必须写入正极反应
2
式中,O 生成OH-,写为O+2HO+4e-===4OH-;
2 2 2
若电解质溶液为酸性,则 H+必须写入正极反应式中,O 生成水,写为 O +4H++4e-
2 2
===2HO。如果是KCO,正极通CO,则正极反应为:O+4e-+2CO=2CO2-
2 2 3 2 2 2 3
2.几种常见原电池电极反应的书写:
(1)负极参加反应,还原剂失电子,发生氧化反应;正极材料不反应:
如:Al-Mg-NaOH。
负极:Al-3e-+4OH-=AlO-+2HO
2 2
正极:2HO+2e=H↑+2OH-
2 2
总反应:
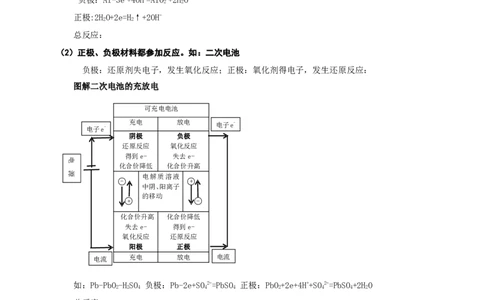
(2)正极、负极材料都参加反应。如:二次电池
负极:还原剂失电子,发生氧化反应;正极:氧化剂得电子,发生还原反应:
图解二次电池的充放电
可充电电池
充电 放电
电子e-
阴极 负极
还原反应 氧化反应
得到e- 失去e-
化合价降低 化合价升高
电解质溶液
○- ○+
中阴、阳离子
的移动
○+ ○-
化合价升高 化合价降低
失去e- 得到e-
氧化反应 还原反应
阳极 正极
电流 充电 放电
电
源
电子e-
电流
如:Pb-PbO-HSO 负极:Pb-2e+SO2-=PbSO 正极:PbO+2e+4H++SO2-=PbSO+2HO
2 2 4 4 4 2 4 4 2
总反应:
(3)负极、正极材料都不参加反应(燃料电池):
如:CH-O-HSO 负极: CH-8e+2HO=CO+8H+ 正极:O+4e+4H+=HO
4 2 2 4 4 2 2 2 2
总反应:
CH-O-NaOH 负极:CH-8e+10OH-=CO2-+7HO 正极:O+4e+2HO=4OH-
4 2 4 3 2 2 2
总反应:
CH-O-KCO 负极:CH-8e+4CO2-=5CO+2HO正极:O+4e+2CO=2CO2-
4 2 2 3 4 3 2 2 2 2 3
总反应:(4)M(Li)、M(H)、C(Li)等物质电极反应的书写:
2 6
M和C 都是吸附Li、H 的材料,化合价为0.
6 2
例:C(Li)-e-=Li++C
6 6
LixCn-xe-==xLi++nC
二、原电池中要牢记重要的五个问题
1.正极电势高,负极电势低,电流:正出负入,电子:负出向正入。
2.电子不通过电解质溶液。电流通过电解质溶液。
3.电解质溶液中,离子流向:正向正,负向负。
4.电解质溶液PH值的变化:正极(阴极)附近PH变大或显碱性,负极(阳极)附近PH变
小或显酸性。
5.充电时,与电源的两极相连:正连正,负连负。
三、电解池的电极反应书写:
1.一看电极材料
若是金属(Au、Pt除外)作阳极,金属一定被氧化(注:Fe生成Fe2+)。
若是惰性电极,则看溶液中存在什么离子,按放电顺序进行放电反应。
2. 二看放电的离子和产生的产物。
3. 介质是否与放电产生的产物发生反应。电解产生的离子(如H+或OH-)能否与溶液中的
某些离子发生反应,如果能发生反应,则这个离子也要与入电极反应。
4. 电荷和原子个数要平衡。
四、电解池楕性电极的电解及其应用
1.楕性电极的电解的电极反应书写
(1)电解水型:
电解质 含氧酸 强碱(如 活泼金属的含氧酸盐
(水溶液) (如HSO) NaOH) (如KNO、NaSO)
2 4 3 2 4
阳极:___________ 阳极:___________ 阳极:___________
电极方程式
阴极:___________ 阴极:___________ 阴极:___________
电解物质 HO
2
总化学方程式
电解质浓度 增大 增大 增大
溶液pH 减小 增大 不变
溶液复原 加______ 加______ 加______
(2)电解电解质型:电解质 无氧酸(如HCl), 不活泼金属的无氧酸盐
(水溶液) 除HF外 (如CuCl),除氟化物外
2
阳极:___________ 阳极:___________
电极方程式 阴极:___________ 阴极:___________
电解物质 酸 盐
总化学方程式 2HCl=====H↑+Cl↑ CuCl=====Cu+Cl↑
2 2 2 2
电解质浓度 减小
溶液pH 增大
溶液复原 通入HCl气体 加________固体
(3)放H 生碱型:
2
电解质(水溶液) 活泼金属的无氧酸盐(如NaCl)
阳极:___________
电极方程式
阴极:___________
电解物质 水和盐
总化学方程式 2NaCl+2HO=====Cl↑+H↑+2NaOH
2 2 2
电解质浓度 生成新电解质
溶液pH 增大
溶液复原 通入HCl气体
(4)放O 生酸型:
2
电解质(水溶液) 不活泼金属的含氧酸盐(如CuSO)
4
阳极:___________
电极方程式
阴极:___________
电解物质 水和盐
总化学方程式 ___________
电解质浓度 生成新电解质
溶液pH 减小
溶液复原 加________或____________
【答案】:①(从上到下,从左到右)2HO-4e-=O↑+4H+ 4H++4e-===2H↑; 4OH--4e-
2 2 2
===O↑+2HO 4HO+4e-=2H↑+4OH-;2HO-4e-=O↑+4H+ 4HO+4e-=2H↑+4OH-
2 2 2 2 2 2 2 2
2HO=====O↑+2H↑ HO HO HO
2 2 2 2 2 2
②2Cl--2e-===Cl↑ 2H++2e-===H↑ 2Cl--2e-===Cl↑
2 2 2
Cu2++2e-===Cu CuCl
2
③2Cl--2e-===Cl↑ 2HO+2e-===H↑+2OH-
2 2 2
④4OH--4e-===2HO+O↑ 2Cu2++4e-===2Cu
2 2
2CuSO+2HO=====2Cu+O↑+2HSO CuO CuCO
4 2 2 2 4 3
练:按要求书写有关的电极反应式及总反应式。
(1)用惰性电极电解AgNO 溶液:
3阳极反应式:___________;
阴极反应式:___________;
总反应离子方程式:___________。
(2)用惰性电极电解MgCl 溶液:(电解产生的OH-与Mg2+不共存)
2
阳极反应式:___________;
阴极反应式:___________;
总反应离子方程式:___________。
【答案】:(1)4OH--4e-===O↑+2HO
2 2
4Ag++4e-===4Ag 4Ag++2HO=====4Ag+O↑+4H+
2 2
(2)2Cl--2e-===Cl↑ 2HO+Mg2++2e-===Mg(OH)↓+H↑
2 2 2 2
Mg2++2Cl-+2HO=====Mg(OH)↓+Cl↑+H↑
2 2 2 2
2.楕性电极的电解应用:
(1).电解饱和食盐水
应用:氯碱工业制烧碱、氯气和氢气。
(2).电冶金
利用电解熔融盐的方法来冶炼活泼金属Na、Ca、Mg、Al等。
(1)冶炼钠:
2NaCl(熔融)=====2Na+Cl↑。
2
电极反应:
【答案】阳极:2Cl--2e-===Cl↑;阴极:2Na++2e-===2Na。
2
(3)冶炼铝:
2AlO(熔融)=====4Al+3O↑。
2 3 2
电极反应:
【答案】阳极:6O2--12e-===3O↑;阴极:4Al3++12e-===4Al。
2
五、非楕性电极的电解及其应用
1..非楕性电极的电解的电极反应书写
例1:用铜作电极电解NaCl溶液:
阳极反应式:___________;
阴极反应式:___________;
总化学方程式:___________。
例2.用铜作电极电解盐酸溶液:
阳极反应式:___________;
阴极反应式:___________;总反应离子方程式:___________。
【答案】1.Cu-2e-===Cu2+ 2HO+2e-===H↑+2OH-
2 2
Cu+2HO=====Cu(OH)↓+H↑
2 2 2
2.Cu-2e-===Cu2+ 2H++2e-===H↑
2
Cu+2H+=====Cu2++H↑
2
5. 非楕性电极的电解应用.
(1)电镀
如图为金属表面镀银的工作示意图,据此回答下列问题:
①镀件作______极,镀层金属银作______极。
②电解质溶液是____________。
③电极反应:
④特点:______极溶解,______极沉积,电镀液的浓度________。
【答案】①阴 阳 ②AgNO 溶液 ④阳 阴 不变
3
阳极:Ag-e-===Ag+
阴极:Ag++e-===Ag
(2)电解精炼铜
①电极材料:阳极为________;阴极为________。
②电解质溶液:含Cu2+的盐溶液。
③电极反应:
【答案】①粗铜 纯铜
阳极:Zn-2e-===Zn2+、Fe-2e-===Fe2+、Ni-2e-===Ni2+、Cu-2e-===Cu2+
阴极:Cu2++2e-===Cu
电解质溶液Cu2+的浓度会减小,要定期补充。
高考实例剖析
高考怎么考《电化学》题,根据高考指挥棒来学习《电化学》题
1
高频考点 原电池原理在选择题中的应用
选择题中的原电池要弄清以下问题
1.原电池电极正负极的判断、发生的反应类型判断、电势高价的判断。
2.电极反应的书写或总反应。
3.放电时,电解质溶液中离子的移动方向
4.放电前后,电极附近PH值的变化5.充电时,原电池的正负极与电源的正负极的连接关系
6.阴离子交接膜和阳离子交接膜的判断
7.简单计算:转移电子数、电极或溶液反应前后质量变化、反应前后两极附近PH等等。
【高考实例一】
例1.(2022·全国高考甲卷)一种水性电解液Zn-MnO 离子选择双隔膜电池如图所示(KOH溶
2
液中,Zn2+以Zn(OH) 存在)。电池放电时,下列叙述错误的是
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO 通过隔膜向Ⅱ区迁移
C. MnO 电极反应:MnO +2e-+4H+=Mn2++2H O
2 2 2
D.电池总反应:Zn+4OH-+MnO +4H+=Zn(OH) +Mn2++2H O
2 2
【答案】A
【解析】根据图示的电池结构和题目所给信息可知,Ⅲ区Zn为电池的负极,电极反应为
Zn-2e-+4OH-=Zn(OH) ,Ⅰ区MnO 为电池的正极,电极反应为MnO +2e-+4H+=Mn2+
2 2
+2H O;电池在工作过程中,由于两个离子选择隔膜没有指明的阳离子隔膜还是阴离
2
子隔膜,故两个离子隔膜均可以通过阴、阳离子,因此可以得到Ⅰ区消耗H+,生成
Mn2+,Ⅱ区的K+向Ⅰ区移动或Ⅰ区的SO 向Ⅱ区移动,Ⅲ区消耗OH-,生成Zn(OH)
,Ⅱ区的SO 向Ⅲ区移动或Ⅲ区的K+向Ⅱ区移动。据此分析答题。
A项:根据分析,Ⅱ区的K+只能向Ⅰ区移动,A错误;B项:根据分析,Ⅰ区的SO 向Ⅱ区移动,B正确;
C项:MnO 电极的电极反应式为MnO +2e-+4H+=Mn2++2H O,C正确;
2 2 2
D项:电池的总反应为Zn+4OH-+MnO +4H+=Zn(OH) +Mn2++2H O,D正确;
2 2
故答案选A。
【考点演练】
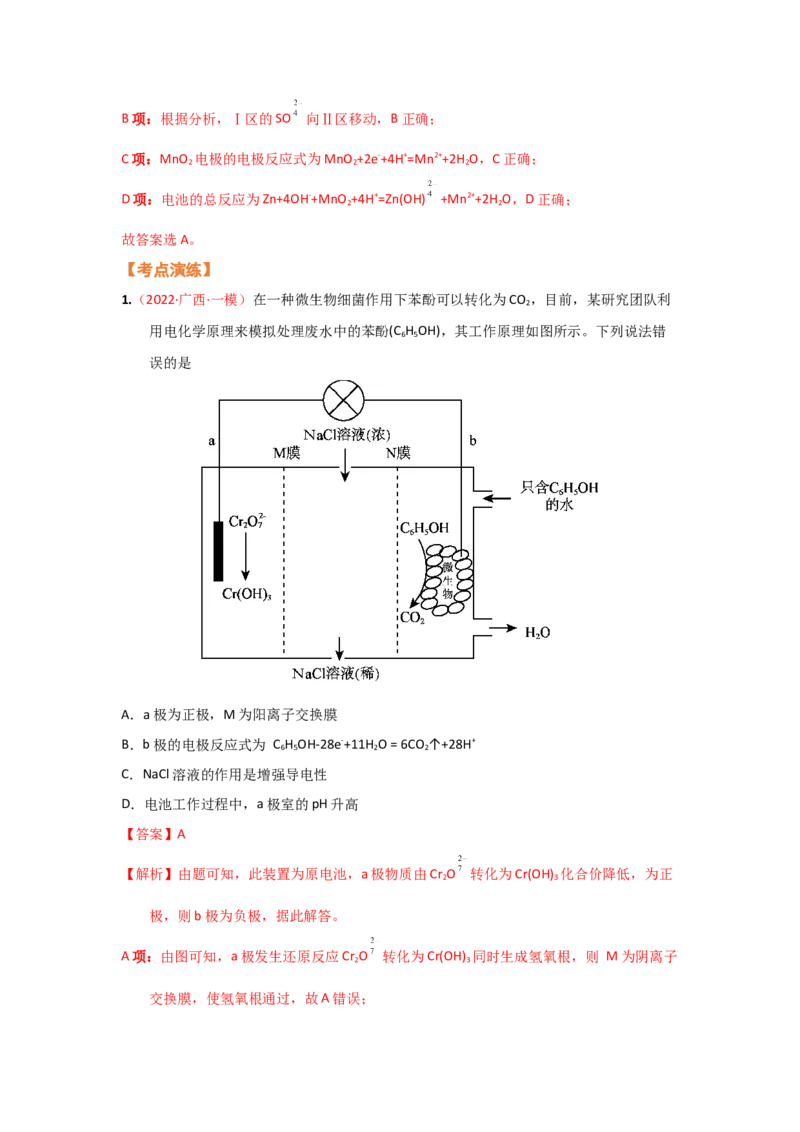
1.(2022·广西·一模)在一种微生物细菌作用下苯酚可以转化为CO ,目前,某研究团队利
2
用电化学原理来模拟处理废水中的苯酚(C H OH),其工作原理如图所示。下列说法错
6 5
误的是
A.a极为正极,M为阳离子交换膜
B.b极的电极反应式为 C H OH-28e-+11H O = 6CO ↑+28H+
6 5 2 2
C.NaCl溶液的作用是增强导电性
D.电池工作过程中,a极室的pH升高
【答案】A
【解析】由题可知,此装置为原电池,a极物质由Cr O 转化为Cr(OH) 化合价降低,为正
2 3
极,则b极为负极,据此解答。
A项:由图可知,a极发生还原反应Cr O 转化为Cr(OH) 同时生成氢氧根,则 M为阴离子
2 3
交换膜,使氢氧根通过,故A错误;B项:b极苯酚发生氧化反应生成CO ,电极反应式为C H OH-28e-+11H O = 6CO ↑+28H+,
2 6 5 2 2
故B正确;
C项:氯化钠溶液的作用是增强溶液导电性,故C正确;
D项:电池工作过程中,a极室发生反应Cr O +6e-+7H O=2Cr(OH) ↓+8OH-,a极室的pH升
2 2 3
高,故D正确;
故答案选A。
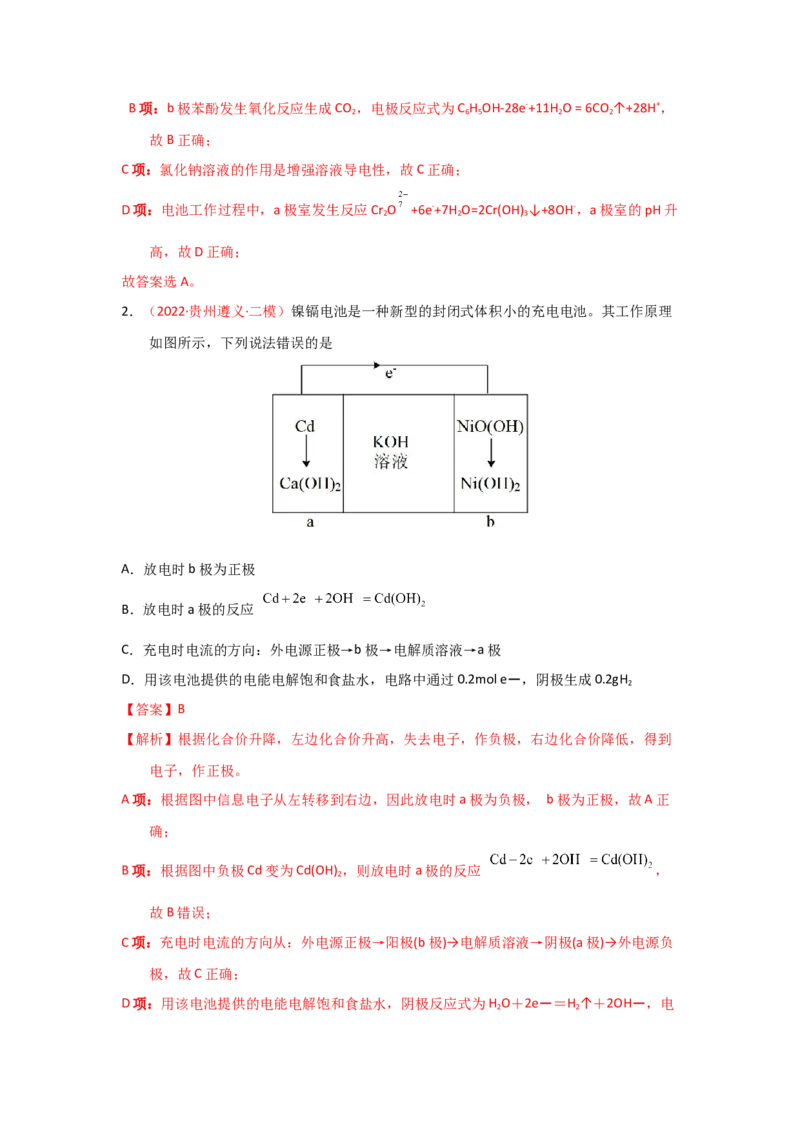
2.(2022·贵州遵义·二模)镍镉电池是一种新型的封闭式体积小的充电电池。其工作原理
如图所示,下列说法错误的是
A.放电时b极为正极
B.放电时a极的反应
C.充电时电流的方向:外电源正极→b极→电解质溶液→a极
D.用该电池提供的电能电解饱和食盐水,电路中通过0.2mol e-,阴极生成0.2gH
2
【答案】B
【解析】根据化合价升降,左边化合价升高,失去电子,作负极,右边化合价降低,得到
电子,作正极。
A项:根据图中信息电子从左转移到右边,因此放电时a极为负极, b极为正极,故A正
确;
B项:根据图中负极Cd变为Cd(OH) ,则放电时a极的反应 ,
2
故B错误;
C项:充电时电流的方向从:外电源正极→阳极(b极)→电解质溶液→阴极(a极)→外电源负
极,故C正确;
D项:用该电池提供的电能电解饱和食盐水,阴极反应式为H O+2e-=H ↑+2OH-,电
2 2路中通过0.2mol e-,则阴极生成氢气物质的量为0.1mol,质量为0.2g,故D正确;
综上所述,答案为B。
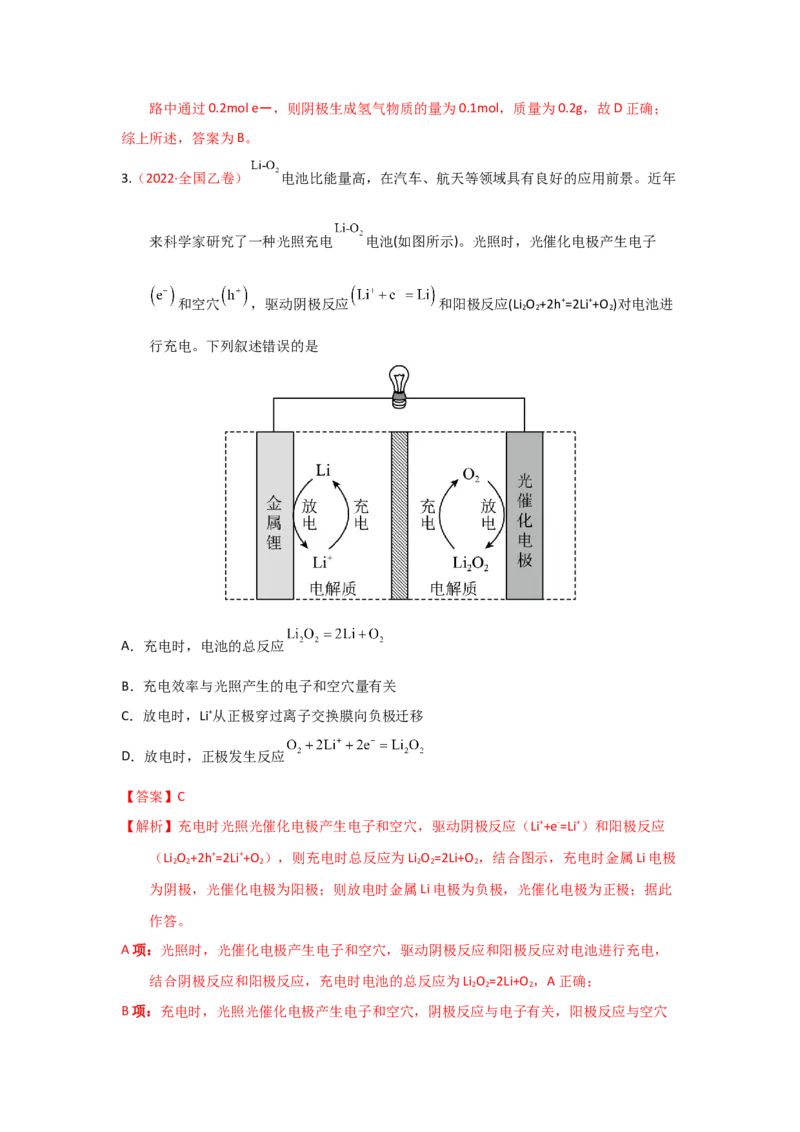
3.(2022·全国乙卷) 电池比能量高,在汽车、航天等领域具有良好的应用前景。近年
来科学家研究了一种光照充电 电池(如图所示)。光照时,光催化电极产生电子
和空穴 ,驱动阴极反应 和阳极反应(Li O +2h+=2Li++O )对电池进
2 2 2
行充电。下列叙述错误的是
A.充电时,电池的总反应
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应
【答案】C
【解析】充电时光照光催化电极产生电子和空穴,驱动阴极反应(Li++e-=Li+)和阳极反应
(Li O +2h+=2Li++O ),则充电时总反应为Li O =2Li+O ,结合图示,充电时金属Li电极
2 2 2 2 2 2
为阴极,光催化电极为阳极;则放电时金属Li电极为负极,光催化电极为正极;据此
作答。
A项:光照时,光催化电极产生电子和空穴,驱动阴极反应和阳极反应对电池进行充电,
结合阴极反应和阳极反应,充电时电池的总反应为Li O =2Li+O ,A正确;
2 2 2
B项:充电时,光照光催化电极产生电子和空穴,阴极反应与电子有关,阳极反应与空穴有关,故充电效率与光照产生的电子和空穴量有关,B正确;
C项:放电时,金属Li电极为负极,光催化电极为正极,Li+从负极穿过离子交换膜向正极
迁移,C错误;
D项:放电时总反应为2Li+O =Li O ,正极反应为O +2Li++2e-=Li O ,D正确;
2 2 2 2 2 2
答案选C。
2
高频考点 电解池在选择题中的应用
1.电极反应的书写或总反应。
2.简单计算:转移电子数、电极或溶液反应前后质量变化、反应前后两极附近PH等等。
3.放电时,电解质溶液中离子的移动方向
【高考实例二】
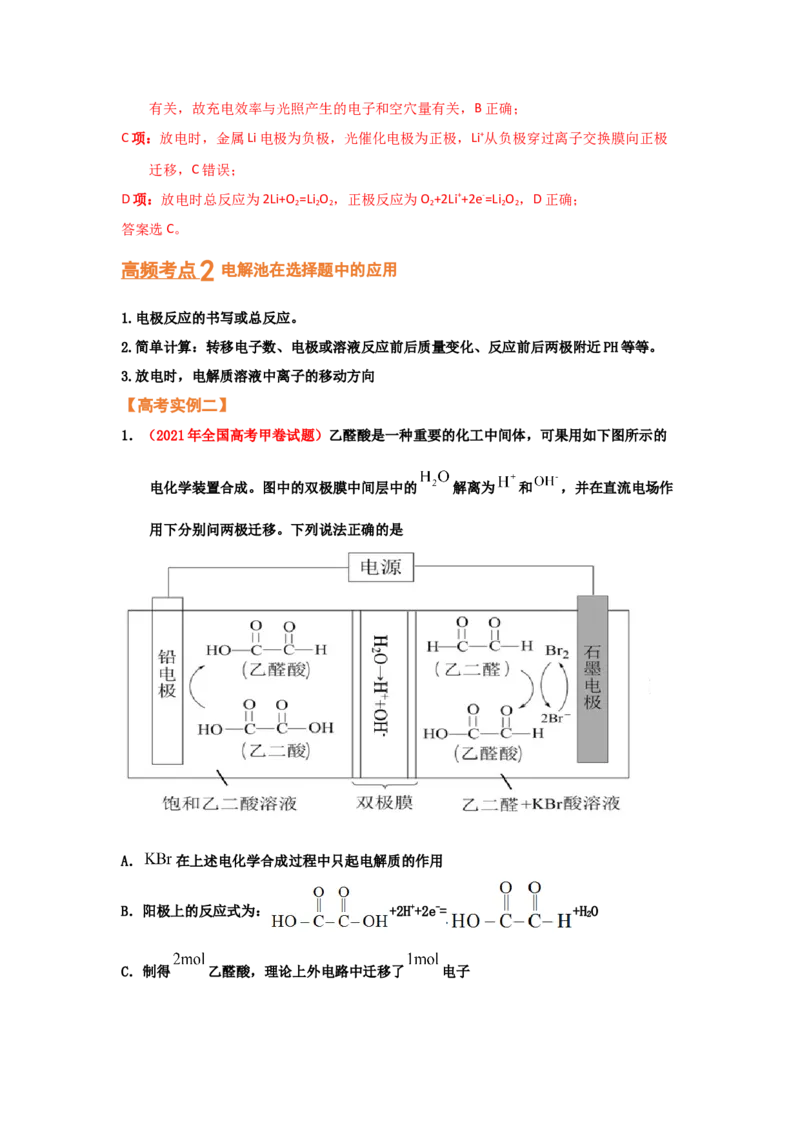
1.(2021年全国高考甲卷试题)乙醛酸是一种重要的化工中间体,可果用如下图所示的
电化学装置合成。图中的双极膜中间层中的 解离为 和 ,并在直流电场作
用下分别问两极迁移。下列说法正确的是
A. 在上述电化学合成过程中只起电解质的作用
B.阳极上的反应式为: +2H++2e-= +HO
2
C.制得 乙醛酸,理论上外电路中迁移了 电子D.双极膜中间层中的 在外电场作用下向铅电极方向迁移
【答案】D
【解析】该装置通电时,乙二酸被还原为乙醛酸,因此铅电极为电解池阴极,石墨电极为
电解池阳极,阳极上Br-被氧化为Br,Br 将乙二醛氧化为乙醛酸,双极膜中间层的
2 2
H+在直流电场作用下移向阴极,OH-移向阳极。
A项:KBr在上述电化学合成过程中除作电解质外,同时还是电解过程中阳极的反应物,生
成的Br 为乙二醛制备乙醛酸的中间产物,故A错误;
2
B项:阳极上为Br-失去电子生成Br,Br 将乙二醛氧化为乙醛酸,故B错误;
2 2
C项:电解过程中阴阳极均生成乙醛酸,1mol乙二酸生成1mol乙醛酸转移电子为2mol,
1mol乙二醛生成1mol乙醛酸转移电子为2mol,根据转移电子守恒可知每生成1mol乙
醛酸转移电子为1mol,因此制得2mol乙醛酸时,理论上外电路中迁移了2mol电子,
故C错误;
D项:由上述分析可知,双极膜中间层的H+在外电场作用下移向阴极,即H+移向铅电极,
故D正确;
综上所述,说法正确的是D项,故答案为D。
【考点演练】
1.(2022·云南曲靖·二模)科学家设计了一种高效、低能耗制备H O 的装置,装置如图所
2 2
示。下列有关说法不正确的是
A.阴极区产生2molOH-时,参加反应的O 在标准状况下的体积为11.2L
2
B.a为电源的正极C.阳极区反应为 −2e-+3OH-=2H O+
2
D.该装置中,离子交换膜为阴离子交换膜
【答案】A
【解析】右边氧气变双氧水,氧化合价降低,说明右边是阴极,则b为负极,a为正极,
左边为阳极。
A项:阴极电极反应式O +2e-+2H O=H O +2OH-,则阴极区产生2molOH-时,参加
2 2 2 2
反应的O 为1mol,在标准状况下的体积为22.4L,故A错误;
2
B项:根据前面分析a为电源的正极,故B正确;
C项:根据前面得到左边是阳极, 被氧化,因此阳极区反应式为
−2e-+3OH-=2H O+ ,故C正确;
2
D项:该装置中,氢氧根在阳极消耗,因此阴极产生的氢氧根要转移到阳极区域,则离子
交换膜为阴离子交换膜,故D正确。
综上所述,答案为A。
2.(2022·广西南宁·二模)KIO 广泛用于化工、医学和生活中,工业上制备KIO 的工作原
3 3
理如图所示,下列说法正确的是
A.a为正极,B极上发生氧化反应
B.电子流向:A→a→b→B
C.X气体是H ,每转移2mole-,可产生22.4LX气体
2D.A极的电极反应式为:I-+6OH--6e-=IO +3H O
2
【答案】D
【解析】根据图示,该装置为电解池,A电极上I-发生失电子的氧化反应生成 ,A电极
为阳极,则a为电源的正极,b为电源的负极,B电极为阴极;据此分析作答。
A项:a为电源的正极,B电极为阴极,B极上发生得电子的还原反应,A错误;
B项:A电极为阳极,a为电源的正极,b为电源的负极,B电极为阴极,电子流向为:
A→a、b→B,电子不通过电源的内电路,B错误;
C项:B极电极反应式为2H O+2e-=H ↑+2OH-,X气体是H ,每转移2mole-生成1molH ,由
2 2 2 2
于H 所处温度和压强未知,不能计算H 的体积,C错误;
2 2
D项:A电极上I-发生失电子的氧化反应生成 ,电极反应式为I-+6OH--6e-= +3H O,D
2
正确;
答案选D。
3.(2022·浙江卷)通过电解废旧锂电池中的 可获得难溶性的 和 ,电
解示意图如下(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液
的体积变化忽略不计)。下列说法不正确的是
A.电极A为阴极,发生还原反应
B.电极B的电极发应:
C.电解一段时间后溶液中 浓度保持不变D.电解结束,可通过调节 除去 ,再加入 溶液以获得
【答案】C
【解析】A项:由电解示意图可知,电极B上Mn2+转化为了MnO ,锰元素化合价升高,失
2
电子,则电极B为阳极,电极A为阴极,得电子,发生还原反应,A正确;
B项:由电解示意图可知,电极B上Mn2+失电子转化为了MnO ,电极反应式为:
2
2H O+Mn2+-2e-=MnO +4H+,B正确;
2 2
C项:电极A为阴极, LiMn O 得电子,电极反应式为:2LiMn O +6e-+16H+=2Li++4Mn2+
2 4 2 4
+8H O,依据得失电子守恒,电解池总反应为:2LiMn O +4H+=2Li++Mn2+
2 2 4
+3MnO +2H O,反应生成了Mn2+,Mn2+浓度增大,C错误;
2 2
D项:电解池总反应为:2LiMn O +4H+=2Li++Mn2++3MnO +2H O,电解结束后,可通过调节
2 4 2 2
溶液pH将锰离子转化为沉淀除去,然后再加入碳酸钠溶液,从而获得碳酸锂,D正
确;
答案选C。