文档内容
沉淀溶解平衡、络合平衡图像的分析应用
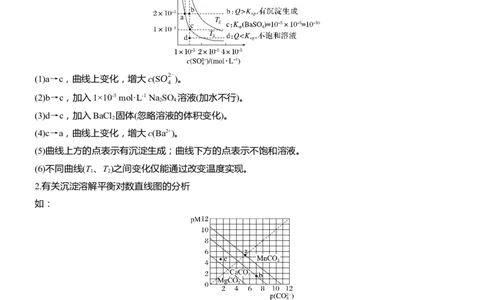
1.有关K 曲线图的分析
sp
如:
(1)a→c,曲线上变化,增大c(SO2-
)。
4
(2)b→c,加入1×10-5 mol·L-1 Na SO 溶液(加水不行)。
2 4
(3)d→c,加入BaCl 固体(忽略溶液的体积变化)。
2
(4)c→a,曲线上变化,增大c(Ba2+)。
(5)曲线上方的点表示有沉淀生成;曲线下方的点表示不饱和溶液。
(6)不同曲线(T 、T )之间变化仅能通过改变温度实现。
1 2
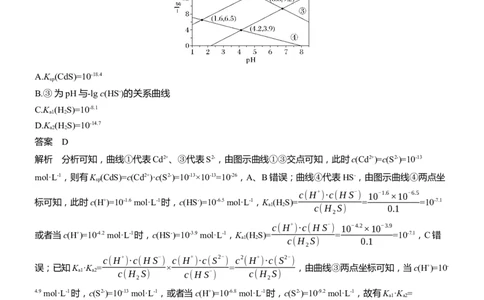
2.有关沉淀溶解平衡对数直线图的分析
如:
已知:pM=-lg
c(M)(M:Mg2+、Ca2+、Mn2+),p(CO2-
)=-lg
c(CO2-
)。
3 3
(1)横坐标数值越大,c(CO2-
)越小。
3
(2)纵坐标数值越大,c(M)越小。
(3)直线上方的点为不饱和溶液。
(4)直线上的点为饱和溶液。
(5)直线下方的点表示有沉淀生成。
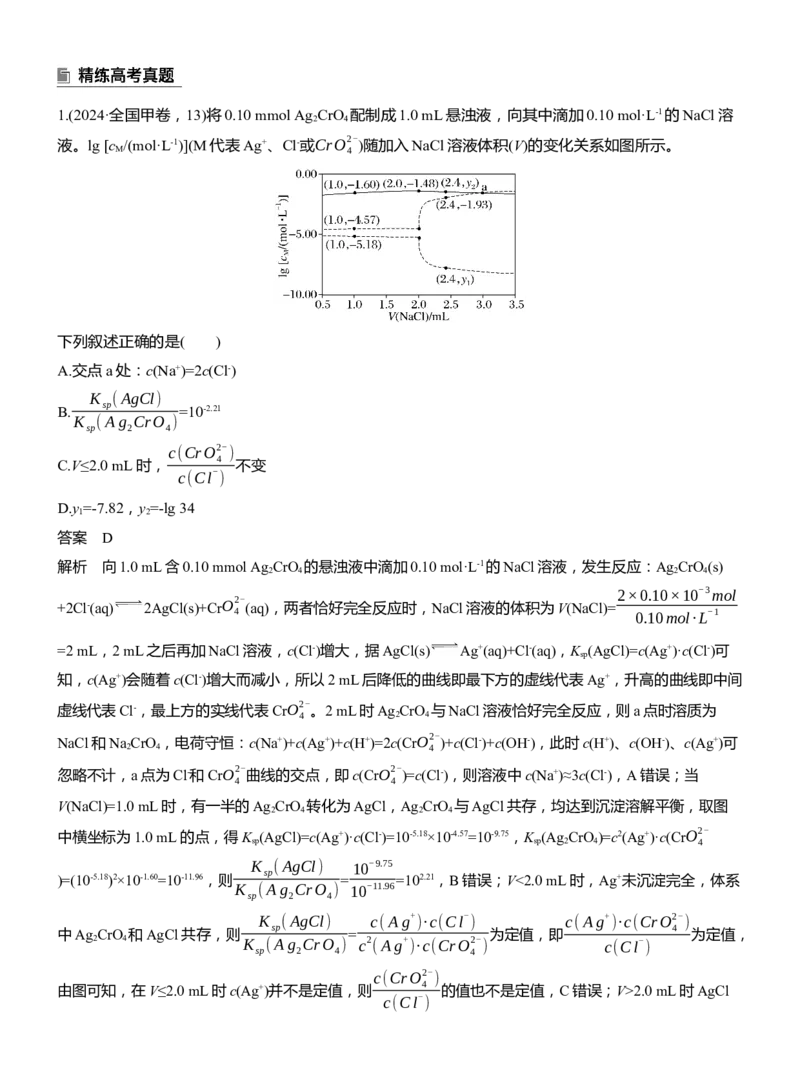
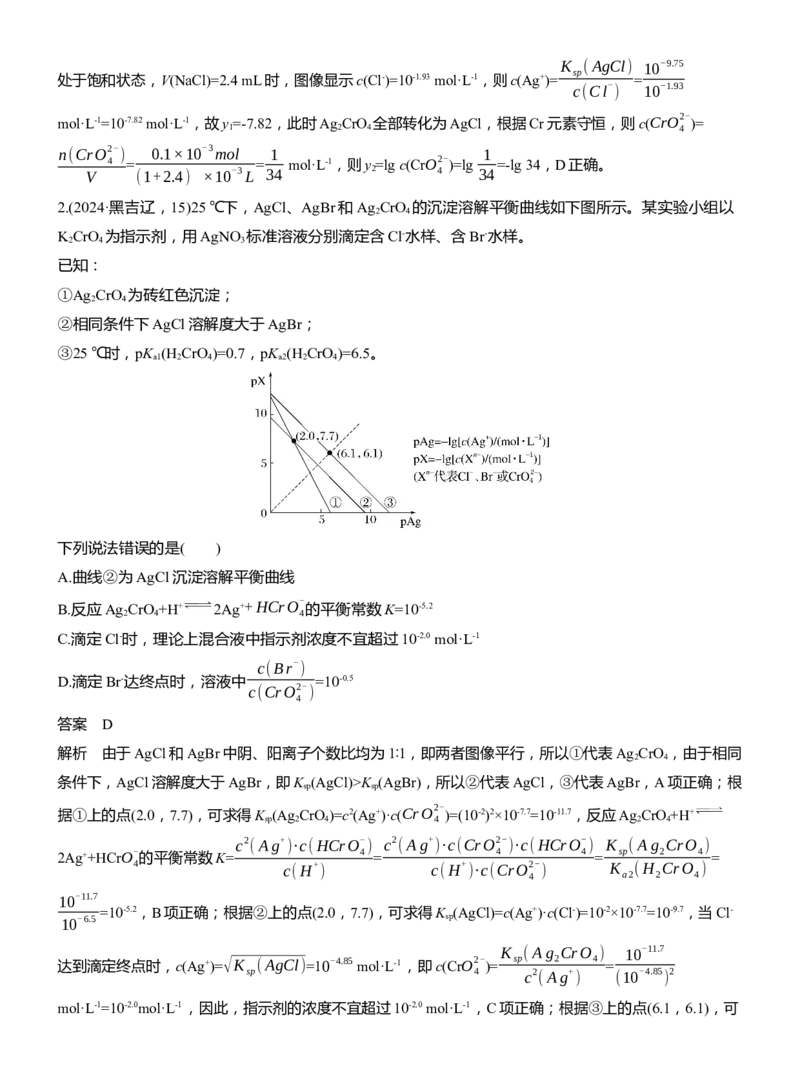
(6)直线上任意点,坐标数值越大,其对应的离子浓度越小。1.(2024·全国甲卷,13)将0.10 mmol Ag CrO 配制成1.0 mL悬浊液,向其中滴加0.10 mol·L-1的NaCl溶
2 4
液。lg [c
/(mol·L-1)](M代表Ag+、Cl-或CrO2-
)随加入NaCl溶液体积(V)的变化关系如图所示。
M 4
下列叙述正确的是( )
A.交点a处:c(Na+)=2c(Cl-)
K (AgCl)
B. sp =10-2.21
K (Ag CrO )
sp 2 4
c(CrO2-
)
4
C.V≤2.0 mL时, 不变
c(Cl-
)
D.y =-7.82,y =-lg 34
1 2
答案 D
解析 向1.0 mL含0.10 mmol Ag CrO 的悬浊液中滴加0.10 mol·L-1的NaCl溶液,发生反应:Ag CrO (s)
2 4 2 4
2×0.10×10-3mol
+2Cl-(aq)
2AgCl(s)+CrO2-
(aq),两者恰好完全反应时,NaCl溶液的体积为V(NaCl)=
4 0.10mol·L-1
=2 mL,2 mL之后再加NaCl溶液,c(Cl-)增大,据AgCl(s) Ag+(aq)+Cl-(aq),K (AgCl)=c(Ag+)·c(Cl-)可
sp
知,c(Ag+)会随着c(Cl-)增大而减小,所以2 mL后降低的曲线即最下方的虚线代表Ag+,升高的曲线即中间
虚线代表Cl-,最上方的实线代表CrO2-
。2 mL时Ag CrO 与NaCl溶液恰好完全反应,则a点时溶质为
4 2 4
NaCl和Na CrO
,电荷守恒:c(Na+)+c(Ag+)+c(H+)=2c(CrO2-
)+c(Cl-)+c(OH-),此时c(H+)、c(OH-)、c(Ag+)可
2 4 4
忽略不计,a点为Cl-和CrO2- 曲线的交点,即c(CrO2-
)=c(Cl-),则溶液中c(Na+)≈3c(Cl-),A错误;当
4 4
V(NaCl)=1.0 mL时,有一半的Ag CrO 转化为AgCl,Ag CrO 与AgCl共存,均达到沉淀溶解平衡,取图
2 4 2 4
中横坐标为1.0 mL的点,得K (AgCl)=c(Ag+)·c(Cl-)=10-5.18×10-4.57=10-9.75,K (Ag CrO
)=c2(Ag+)·c(CrO2-
sp sp 2 4 4
K (AgCl) 10-9.75
sp
)=(10-5.18)2×10-1.60=10-11.96,则 = =102.21,B错误;V<2.0 mL时,Ag+未沉淀完全,体系
K (Ag CrO ) 10-11.96
sp 2 4
K (AgCl) c(Ag+ )·c(Cl- ) c(Ag+ )·c(CrO2- )
sp 4
中Ag CrO 和AgCl共存,则 = 为定值,即 为定值,
2 4 K (Ag CrO ) c2 (Ag+ )·c(CrO2- ) c(Cl- )
sp 2 4 4
c(CrO2-
)
由图可知,在V≤2.0 mL时c(Ag+)并不是定值,则 4 的值也不是定值,C错误;V>2.0 mL时AgCl
c(Cl-
)K (AgCl) 10-9.75
sp
处于饱和状态,V(NaCl)=2.4 mL时,图像显示c(Cl-)=10-1.93 mol·L-1,则c(Ag+)= =
c(Cl-
)
10-1.93
mol·L-1=10-7.82 mol·L-1,故y =-7.82,此时Ag CrO
全部转化为AgCl,根据Cr元素守恒,则c(CrO2-
)=
1 2 4 4
n(CrO2- ) 0.1×10-3mol 1 1
4 = = mol·L-1,则y =lg c(CrO2- )=lg =-lg 34,D正确。
V (1+2.4) ×10-3L 34 2 4 34
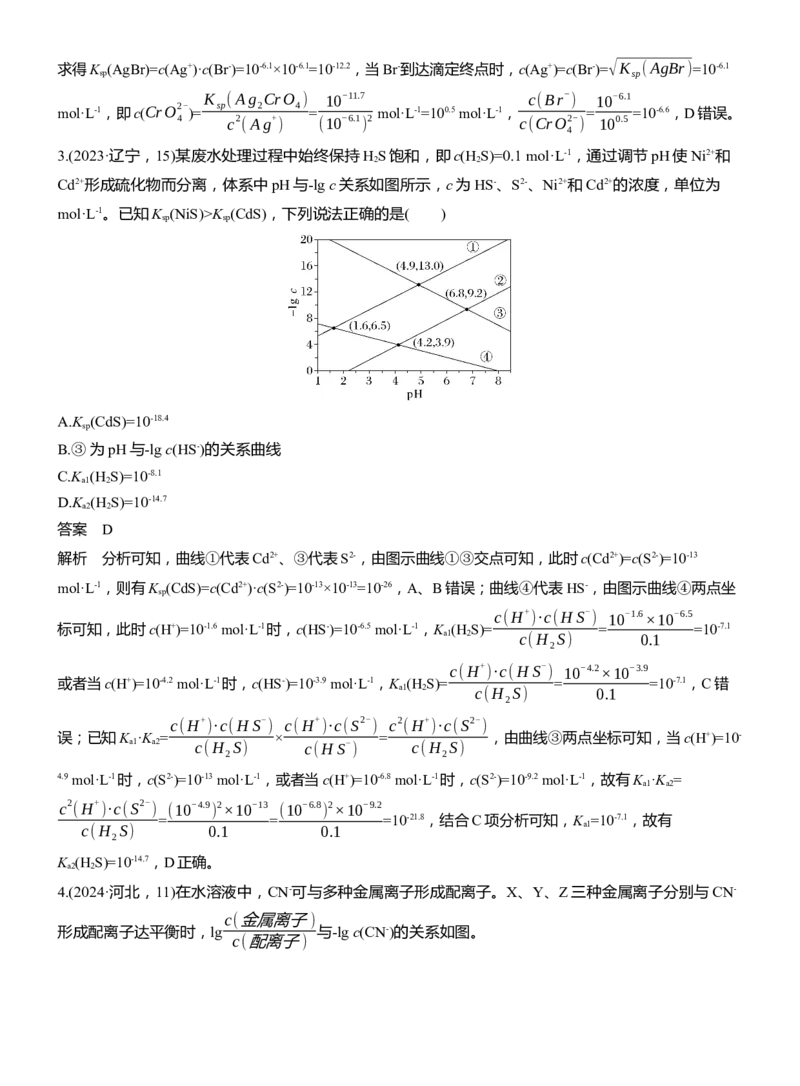
2.(2024·黑吉辽,15)25 ℃下,AgCl、AgBr和Ag CrO 的沉淀溶解平衡曲线如下图所示。某实验小组以
2 4
K CrO 为指示剂,用AgNO 标准溶液分别滴定含Cl-水样、含Br-水样。
2 4 3
已知:
①Ag CrO 为砖红色沉淀;
2 4
②相同条件下AgCl溶解度大于AgBr;
③25 ℃时,pK (H CrO )=0.7,pK (H CrO )=6.5。
a1 2 4 a2 2 4
下列说法错误的是( )
A.曲线②为AgCl沉淀溶解平衡曲线
B.反应Ag CrO +H+
2Ag++HCrO-
的平衡常数K=10-5.2
2 4 4
C.滴定Cl-时,理论上混合液中指示剂浓度不宜超过10-2.0 mol·L-1
c(Br-
)
D.滴定Br-达终点时,溶液中 =10-0.5
c(CrO2-
)
4
答案 D
解析 由于AgCl和AgBr中阴、阳离子个数比均为1∶1,即两者图像平行,所以①代表Ag CrO ,由于相同
2 4
条件下,AgCl溶解度大于AgBr,即K (AgCl)>K (AgBr),所以②代表AgCl,③代表AgBr,A项正确;根
sp sp
据①上的点(2.0,7.7),可求得K (Ag CrO
)=c2(Ag+)·c(CrO2-
)=(10-2)2×10-7.7=10-11.7,反应Ag CrO +H+
sp 2 4 4 2 4
c2 (Ag+ )·c(HCrO- ) c2 (Ag+ )·c(CrO2- )·c(HCrO- ) K (Ag CrO )
2Ag++HCrO- 的平衡常数K= 4 = 4 4 = sp 2 4 =
4 c(H+ ) c(H+ )·c(CrO2- ) K (H CrO )
4 a2 2 4
10-11.7
=10-5.2,B项正确;根据②上的点(2.0,7.7),可求得K (AgCl)=c(Ag+)·c(Cl-)=10-2×10-7.7=10-9.7,当Cl-
10-6.5 sp
K (Ag CrO ) 10-11.7
达到滴定终点时,c(Ag+)=√K (AgCl)=10-4.85 mol·L-1 ,即c(CrO2- )= sp 2 4 =
sp 4 c2 (Ag+
)
(10-4.85
)
2
mol·L-1=10-2.0mol·L-1 ,因此,指示剂的浓度不宜超过10-2.0 mol·L-1 ,C项正确;根据③上的点(6.1,6.1),可求得K (AgBr)=c(Ag+)·c(Br-)=10-6.1×10-6.1=10-12.2,当Br-到达滴定终点时,c(Ag+)=c(Br-)=√K (AgBr)=10-6.1
sp sp
K (Ag CrO ) 10-11.7 c(Br- ) 10-6.1
mol·L-1,即c(CrO2-
)=
sp 2 4
= mol·L-1=100.5 mol·L-1, = =10-6.6,D错误。
4 c2 (Ag+ ) (10-6.1 ) 2 c(CrO2- ) 100.5
4
3.(2023·辽宁,15)某废水处理过程中始终保持H S饱和,即c(H S)=0.1 mol·L-1,通过调节pH使Ni2+和
2 2
Cd2+形成硫化物而分离,体系中pH与-lg c关系如图所示,c为HS-、S2-、Ni2+和Cd2+的浓度,单位为
mol·L-1。已知K (NiS)>K (CdS),下列说法正确的是( )
sp sp
A.K (CdS)=10-18.4
sp
B.③为pH与-lg c(HS-)的关系曲线
C.K (H S)=10-8.1
a1 2
D.K (H S)=10-14.7
a2 2
答案 D
解析 分析可知,曲线①代表Cd2+、③代表S2-,由图示曲线①③交点可知,此时c(Cd2+)=c(S2-)=10-13
mol·L-1,则有K (CdS)=c(Cd2+)·c(S2-)=10-13×10-13=10-26,A、B错误;曲线④代表HS-,由图示曲线④两点坐
sp
c(H+ )·c(HS- ) 10-1.6×10-6.5
标可知,此时c(H+)=10-1.6 mol·L-1时,c(HS-)=10-6.5 mol·L-1,K (H S)= = =10-7.1
a1 2 c(H S) 0.1
2
c(H+ )·c(HS- ) 10-4.2×10-3.9
或者当c(H+)=10-4.2 mol·L-1时,c(HS-)=10-3.9 mol·L-1,K (H S)= = =10-7.1,C错
a1 2 c(H S) 0.1
2
c(H+ )·c(HS-
)
c(H+ )·c(S2-
)
c2 (H+ )·c(S2-
)
误;已知K ·K = × = ,由曲线③两点坐标可知,当c(H+)=10-
a1 a2 c(H S) c(HS- ) c(H S)
2 2
4.9 mol·L-1时,c(S2-)=10-13 mol·L-1,或者当c(H+)=10-6.8 mol·L-1时,c(S2-)=10-9.2 mol·L-1,故有K ·K =
a1 a2
c2 (H+ )·c(S2- ) (10-4.9 ) 2×10-13 (10-6.8 ) 2×10-9.2
= = =10-21.8,结合C项分析可知,K =10-7.1,故有
c(H S) 0.1 0.1 a1
2
K (H S)=10-14.7,D正确。
a2 2
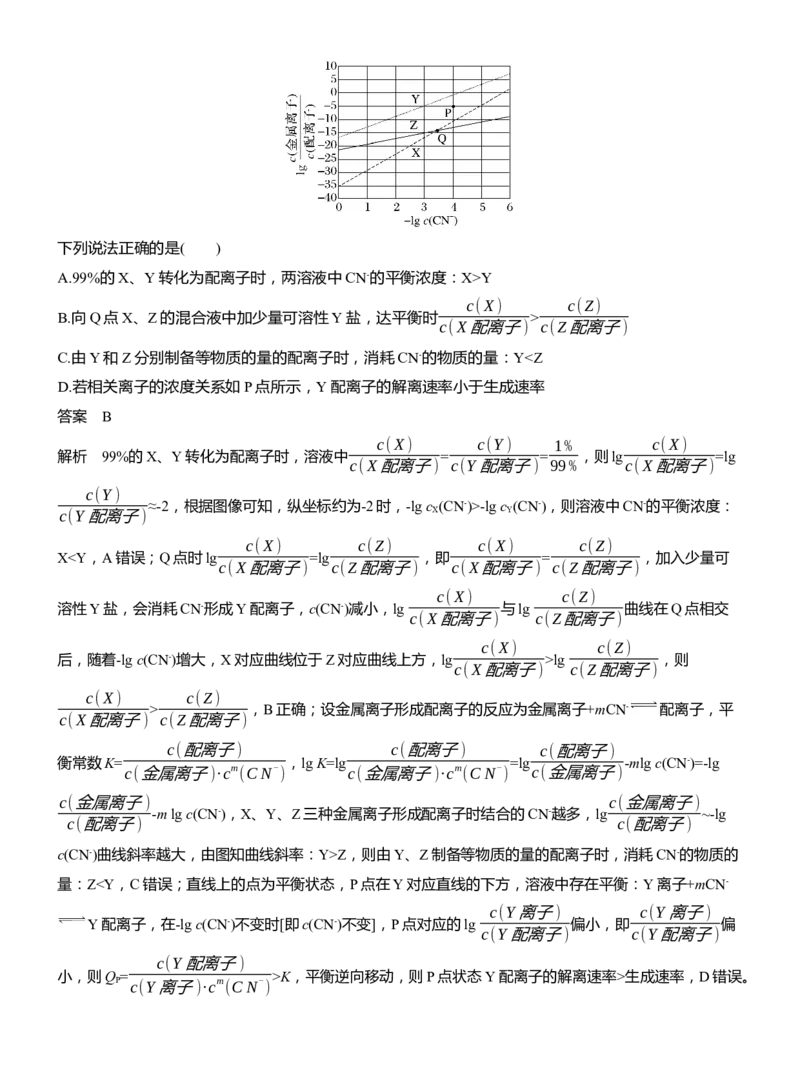
4.(2024·河北,11)在水溶液中,CN-可与多种金属离子形成配离子。X、Y、Z三种金属离子分别与CN-
c(金属离子)
形成配离子达平衡时,lg 与-lg c(CN-)的关系如图。
c(配离子)下列说法正确的是( )
A.99%的X、Y转化为配离子时,两溶液中CN-的平衡浓度:X>Y
c(X) c(Z)
B.向Q点X、Z的混合液中加少量可溶性Y盐,达平衡时 >
c(X配离子) c(Z配离子)
C.由Y和Z分别制备等物质的量的配离子时,消耗CN-的物质的量:Y-lg c (CN-),则溶液中CN-的平衡浓度:
c(Y配离子) X Y
c(X) c(Z) c(X) c(Z)
Xlg ,则
c(X配离子) c(Z配离子)
c(X) c(Z)
> ,B正确;设金属离子形成配离子的反应为金属离子+mCN- 配离子,平
c(X配离子) c(Z配离子)
c(配离子) c(配离子) c(配离子)
衡常数K= ,lg K=lg =lg -mlg c(CN-)=-lg
c(金属离子)·cm (CN- ) c(金属离子)·cm (CN- ) c(金属离子)
c(金属离子) c(金属离子)
-m lg c(CN-),X、Y、Z三种金属离子形成配离子时结合的CN-越多,lg ~-lg
c(配离子) c(配离子)
c(CN-)曲线斜率越大,由图知曲线斜率:Y>Z,则由Y、Z制备等物质的量的配离子时,消耗CN-的物质的
量:ZK,平衡逆向移动,则P点状态Y配离子的解离速率>生成速率,D错误。
P c(Y离子)·cm (CN-
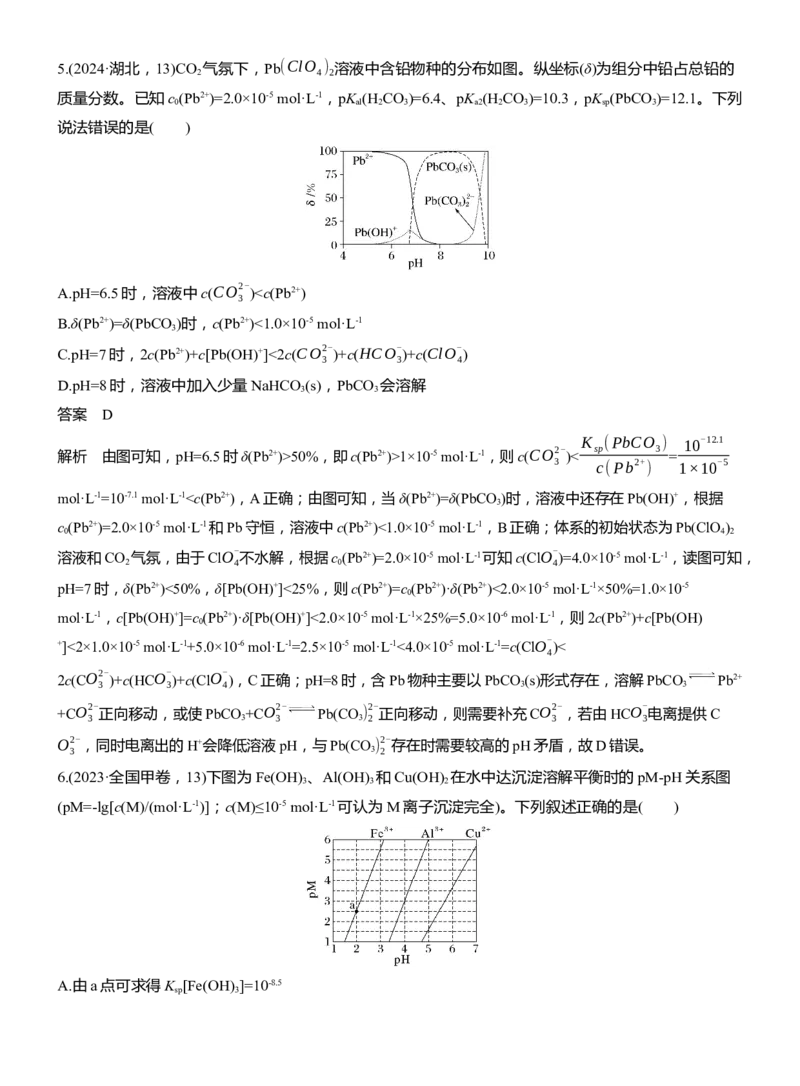
)5.(2024·湖北,13)CO 气氛下,Pb(ClO ) 溶液中含铅物种的分布如图。纵坐标(δ)为组分中铅占总铅的
2 4 2
质量分数。已知c (Pb2+)=2.0×10-5 mol·L-1,pK (H CO )=6.4、pK (H CO )=10.3,pK (PbCO )=12.1。下列
0 al 2 3 a2 2 3 sp 3
说法错误的是( )
A.pH=6.5时,溶液中c(CO2-
)50%,即c(Pb2+)>1×10-5
mol·L-1,则c(CO2-
)<
sp 3
=
3 c(Pb2+
)
1×10-5
mol·L-1=10-7.1 mol·L-110-5 mol·L-1,则
Al3+、Cu2+会同时沉淀,故D错误。
题型突破练 [分值:50 分]
(选择题1~5题,每小题4分,6~11题,每小题5分,共50分)
1.(2024·贵阳模拟)已知:pAg=-lg c(Ag+),常温下向10 mL 0.1 mol·L-1AgNO 溶液中滴加0.1 mol·L-1NaCl溶
3
液的滴定曲线 Ⅰ 如图所示。已知:K (AgCl)>K (AgI)。下列说法正确的是( )
sp sp
A.常温下,K (AgCl)=1.0×10-5.87
sp
B.溶液中水的电离程度:a=cb>c,Ag+促进水的电离,
sp
0.1mol·L-1×5 mL
故溶液中水的电离程度:a>b>c,B错误;c点溶液中c(Cl-)= =0.02 mol·L-1, c(Ag+)=
25 mL
1.0×10-9.74
mol·L-1=5.0×10-8.74 mol·L-1,C正确;K (AgI)c(H+)>c(R2-)
D.直线上任一点均满足c(H+)+2c(Ba2+)=c(OH-)+c(HR-)+2c(R2-)
答案 D
c(Ba2+
)
解析 直线上,lg c(Ba2+)+pH=1,即 =10;难溶物BaR与足量盐酸发生反应:BaR+2H+ Ba2+
c(H+
)
c2 (H+ )·c(R2-
)
+H R,溶液中存在c(Ba2+)≈c(H R),K ·K = ,K (BaR)= c(Ba2+)·c(R2-)=K ·K ×
2 2 a1 a2 c(H R) sp a1 a2
2
c(Ba2+ )·c(H R)
2 =2×10-8×3×10-17×100=6×10-23,A正确;M点,c(H+)=10-0.6 mol·L-1,c(Ba2+)≈c(H R)=100.4
c2 (H+
)
2
K ×c(H R) 2×10-8×100.4
a1 2
mol·L-1,c(HR-)= = =2×10-7 mol·L-1,B正确;溶液中溶质为BaCl 、H R、
c(H+
)
10-0.6 2 2
c2 (H+ )·c(R2-
)
HCl,K ·K = ,N点时,c(H+)=10-0.8 mol·L-1,c(Ba2+)≈c(H R)=100.2 mol·L-1,则c(R2-)=
a1 a2 c(H R) 2
2
c(Ba2+ ) 100.2
×K ·K = ×2×10-8×3×10-17 mol·L-1=6×10-23.2 mol·L-1,c(Cl-)最大,所以N点:
c2 (H+ ) a1 a2 (10-0.8 ) 2
c(Cl-)>c(H+)>c(R2-),C正确;直线上任一点均满足电荷守恒:c(H+)+2c(Ba2+)=c(OH-)+c(HR-)+2c(R2-)+c(Cl-),
所以c(H+)+2c(Ba2+)>c(OH-)+c(HR-)+2c(R2-),D错误。
4.(2024·河北衡水模拟)工业上以SrSO (s)为原料生产SrCO (s),对其工艺条件进行研究。现有含SrCO (s)的
4 3 3
0.1 mol·L-1Na CO 溶液和含SrCO (s)的1.0 mol·L-1Na CO 溶液,以及含SrSO (s)的0.1 mol·L-1Na SO 溶液和
2 3 3 2 3 4 2 4
含SrSO (s)的1.0 mol·L-1Na SO 溶液。在一定pH范围内(固体足量),四种溶液中pM[pM=-lg c(Sr2+)]随pH
4 2 4
的变化关系如图所示。下列说法错误的是( )A.a=6.5
B.由图可知,pH越小,越不利于SrSO 转化为SrCO
4 3
C.曲线①代表含SrCO (s)的1.0 mol·L-1Na CO 溶液的变化曲线
3 2 3
D.将pH=6.8状态下的②、④两物料等体积混合后,溶液中pM等于5.5
答案 D
解析 温度不变时,K (SrCO )和K (SrSO )均不变;Na CO
溶液中存在水解平衡:CO2-
+H O
HCO-
sp 3 sp 4 2 3 3 2 3
+OH-、HCO-
+H O H CO
+OH-,随着pH的增大,溶液中CO2-
的浓度增大,溶液中Sr2+的浓度减小,
3 2 2 3 3
pM增大,pH相同时1.0 mol·L-1 Na CO
溶液中CO2-
的浓度大于0.1 mol·L-1 Na CO
溶液中CO2-
的浓度,故
2 3 3 2 3 3
曲线①代表含SrCO (s)的1.0 mol·L-1 Na CO 溶液的变化曲线,曲线②代表含SrCO (s)的0.1 mol·L-1 Na CO
3 2 3 3 2 3
溶液的变化曲线;Na SO
属于强酸强碱盐,随着pH的增大,溶液中SO2- 的浓度不变,SO2-
浓度越大、
2 4 4 4
Sr2+的浓度越小、pM越大,故曲线③代表含SrSO (s)的1.0 mol·L-1 Na SO 溶液的变化曲线,曲线④代表含
4 2 4
SrSO (s)的0.1 mol·L-1 Na SO 溶液的变化曲线,由曲线④的数据可计算K (SrSO )=10-5.5×0.1=10-6.5。温度不
4 2 4 sp 4
10-6.5
变,K (SrSO )不变,根据分析,曲线③上c(Sr2+)= mol·L-1=10-6.5 mol·L-1,pM=-lg 10-6.5=6.5,即
sp 4 1.0
a=6.5,A项正确;SrSO 转化为SrCO 的反应:SrSO
(s)+CO2-
(aq) SrCO
(s)+SO2-
(aq),溶液pH越小,
4 3 4 3 3 4
CO2-
浓度减小,平衡逆向移动,越不利于SrSO 转化为SrCO ,B项正确;将pH=6.8状态下的②、④两物
3 4 3
料等体积混合后,相当于稀释,瞬间Sr2+的浓度不变,但CO2- 、SO2-
的浓度减小,故固体溶解,Sr2+浓度
3 4
增大,pM减小,即pM<5.5,D项错误。
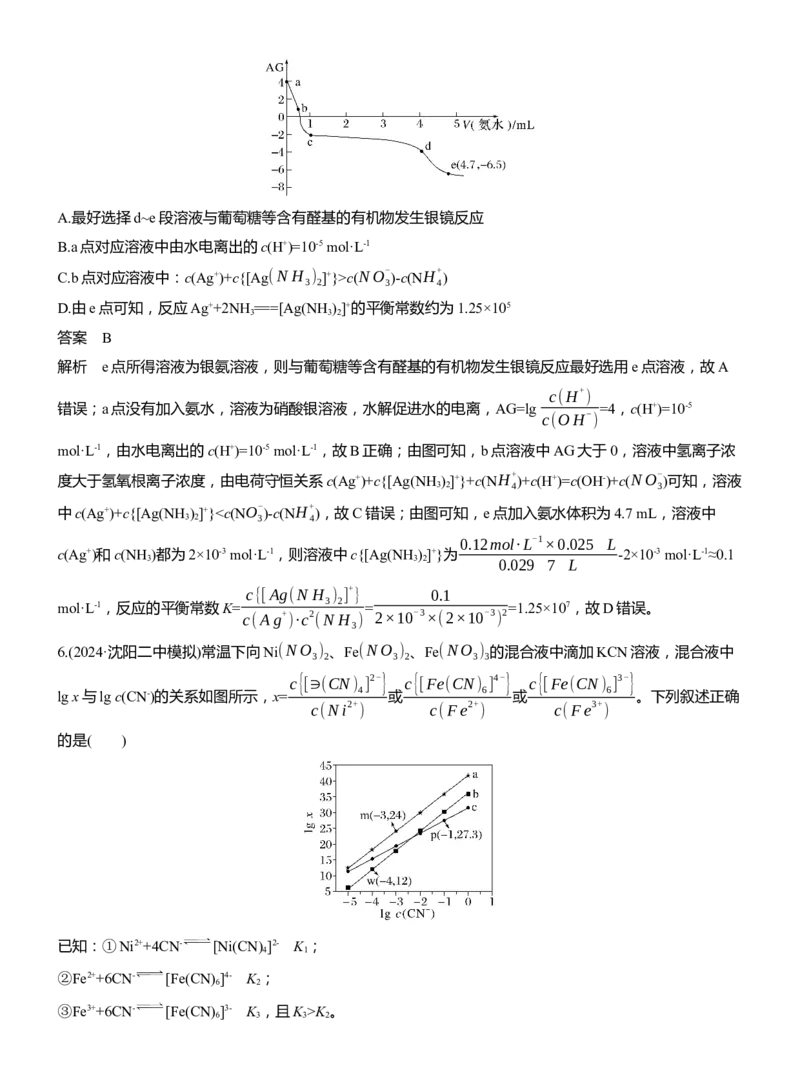
5.(2024·长沙二模)常温下,将一定浓度的氨水逐滴加入25 mL 0.12 mol·L-1AgNO 溶液中,该过程中溶液
3
c(H+
)
AG[AG=lg ]与加入氨水体积V的关系如图所示,已知e点对应的溶液迅速由浑浊变澄清,且此时
c(OH-
)
溶液中的c(Ag+)与c(NH )均约为2×10-3 mol·L-1。下列叙述正确的是( )
3A.最好选择d~e段溶液与葡萄糖等含有醛基的有机物发生银镜反应
B.a点对应溶液中由水电离出的c(H+)=10-5 mol·L-1
C.b点对应溶液中:c(Ag+)+c{[Ag(N H ) ]+}>c(NO- )-c(NH+ )
3 2 3 4
D.由e点可知,反应Ag++2NH ===[Ag(NH ) ]+的平衡常数约为1.25×105
3 3 2
答案 B
解析 e点所得溶液为银氨溶液,则与葡萄糖等含有醛基的有机物发生银镜反应最好选用e点溶液,故A
c(H+
)
错误;a点没有加入氨水,溶液为硝酸银溶液,水解促进水的电离,AG=lg =4,c(H+)=10-5
c(OH-
)
mol·L-1,由水电离出的c(H+)=10-5 mol·L-1,故B正确;由图可知,b点溶液中AG大于0,溶液中氢离子浓
度大于氢氧根离子浓度,由电荷守恒关系c(Ag+)+c{[Ag(NH )
]+}+c(NH+ )+c(H+)=c(OH-)+c(NO-
)可知,溶液
3 2 4 3
中c(Ag+)+c{[Ag(NH )
]+}K 。
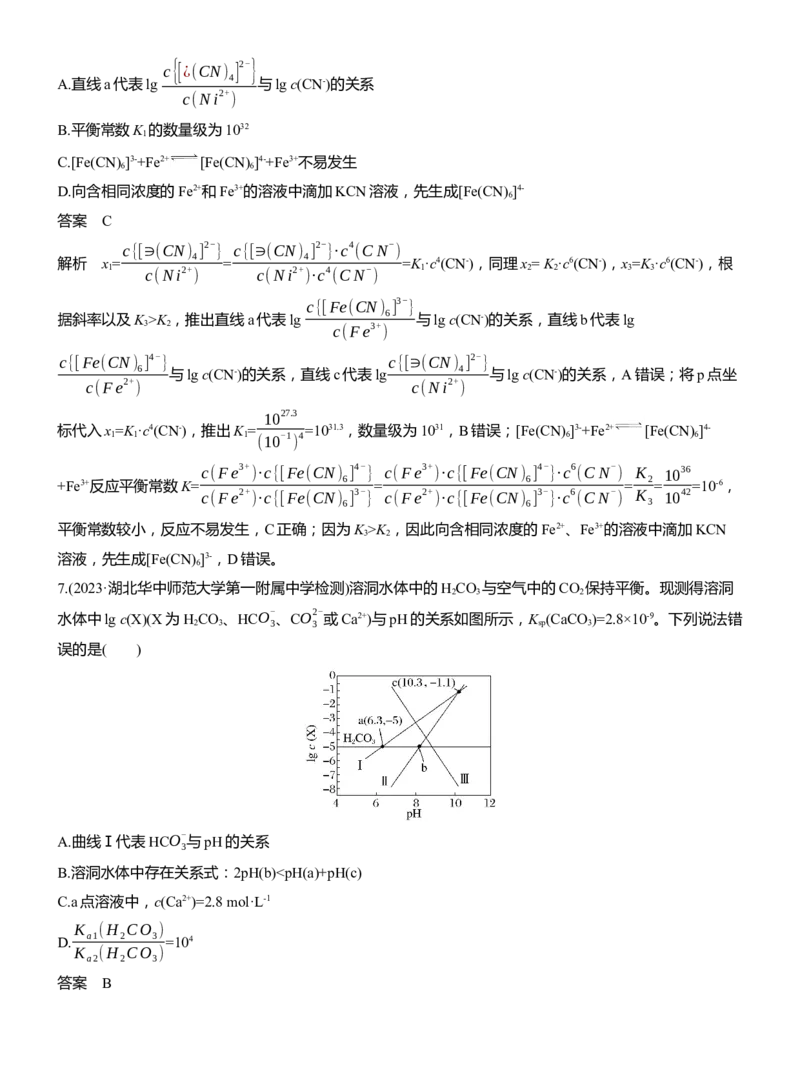
6 3 3 2c{[¿(CN) ] 2-}
A.直线a代表lg 4 与lg c(CN-)的关系
c(Ni2+
)
B.平衡常数K 的数量级为1032
1
C.[Fe(CN) ]3-+Fe2+ [Fe(CN) ]4-+Fe3+不易发生
6 6
D.向含相同浓度的Fe2+和Fe3+的溶液中滴加KCN溶液,先生成[Fe(CN) ]4-
6
答案 C
c{[∋(CN) ] 2- } c{[∋(CN) ] 2- }·c4 (CN- )
解析 x = 4 = 4 =K ·c4(CN-),同理x = K ·c6(CN-),x =K ·c6(CN-),根
1 c(Ni2+
)
c(Ni2+ )·c4 (CN-
)
1 2 2 3 3
c{[Fe(CN) ] 3- }
据斜率以及K >K ,推出直线a代表lg 6 与lg c(CN-)的关系,直线b代表lg
3 2 c(Fe3+
)
c{[Fe(CN) ] 4- } c{[∋(CN) ] 2- }
6 与lg c(CN-)的关系,直线c代表lg 4 与lg c(CN-)的关系,A错误;将p点坐
c(Fe2+
)
c(Ni2+
)
1027.3
标代入x =K ·c4(CN-),推出K = =1031.3,数量级为1031,B错误;[Fe(CN) ]3-+Fe2+ [Fe(CN) ]4-
1 1 1 (10-1
)
4 6 6
c(Fe3+ )·c{[Fe(CN) ] 4- } c(Fe3+ )·c{[Fe(CN) ] 4- }·c6 (CN- ) K 1036
6 6 2
+Fe3+反应平衡常数K= = = = =10-6,
c(Fe2+ )·c{[Fe(CN) ] 3- } c(Fe2+ )·c{[Fe(CN) ] 3- }·c6 (CN- ) K 1042
6 6 3
平衡常数较小,反应不易发生,C正确;因为K >K ,因此向含相同浓度的Fe2+、Fe3+的溶液中滴加KCN
3 2
溶液,先生成[Fe(CN) ]3-,D错误。
6
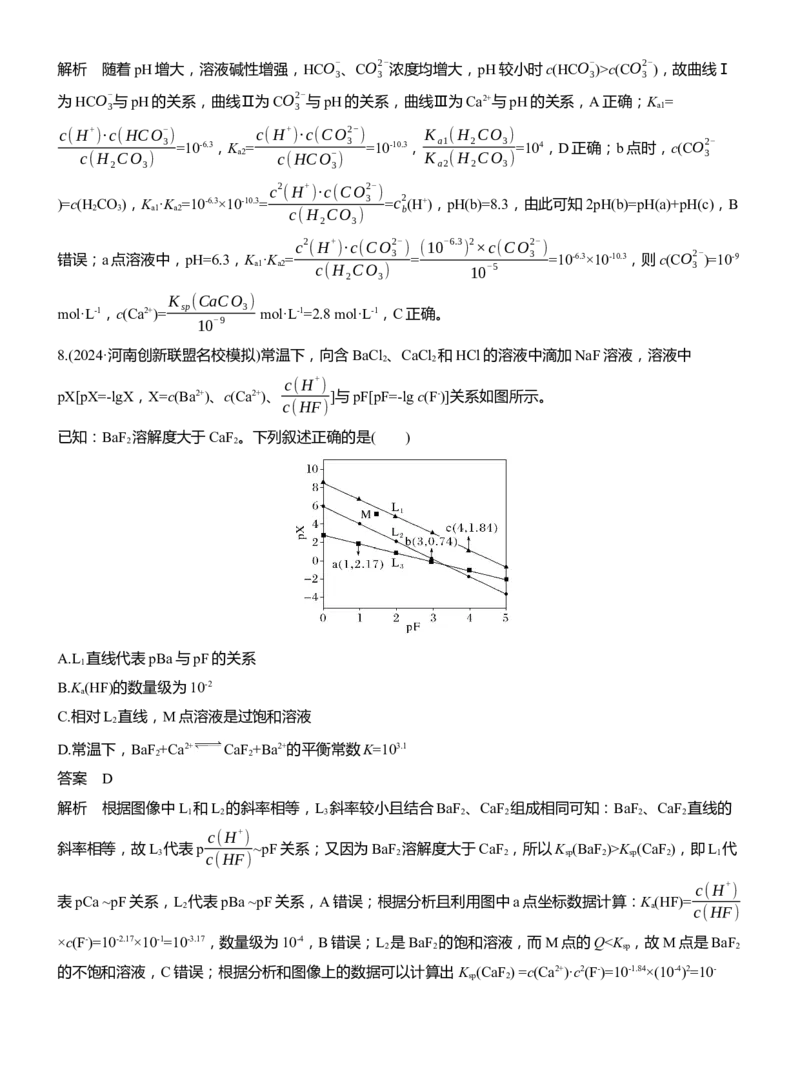
7.(2023·湖北华中师范大学第一附属中学检测)溶洞水体中的H CO 与空气中的CO 保持平衡。现测得溶洞
2 3 2
水体中lg c(X)(X为H CO
、HCO- 、CO2-
或Ca2+)与pH的关系如图所示,K (CaCO )=2.8×10-9。下列说法错
2 3 3 3 sp 3
误的是( )
A.曲线Ⅰ代表HCO-
与pH的关系
3
B.溶洞水体中存在关系式:2pH(b)c(CO2-
),故曲线Ⅰ
3 3 3 3
为HCO- 与pH的关系,曲线Ⅱ为CO2-
与pH的关系,曲线Ⅲ为Ca2+与pH的关系,A正确;K =
3 3 a1
c(H+ )·c(HCO- ) c(H+ )·c(CO2- ) K (H CO )
3 =10-6.3,K = 3 =10-10.3, a1 2 3 =104,D正确;b点时,c(CO2-
c(H CO ) a2 c(HCO- ) K (H CO ) 3
2 3 3 a2 2 3
c2 (H+ )·c(CO2-
)
)=c(H CO ),K ·K =10-6.3×10-10.3= 3 =c2 (H+),pH(b)=8.3,由此可知2pH(b)=pH(a)+pH(c),B
2 3 a1 a2 c(H CO ) b
2 3
c2 (H+ )·c(CO2-
)
(10-6.3
)
2×c(CO2-
)
错误;a点溶液中,pH=6.3,K ·K = 3 = 3 =10-6.3×10-10.3,则c(CO2- )=10-9
a1 a2 c(H CO ) 10-5 3
2 3
K (CaCO )
mol·L-1,c(Ca2+)= sp 3 mol·L-1=2.8 mol·L-1,C正确。
10-9
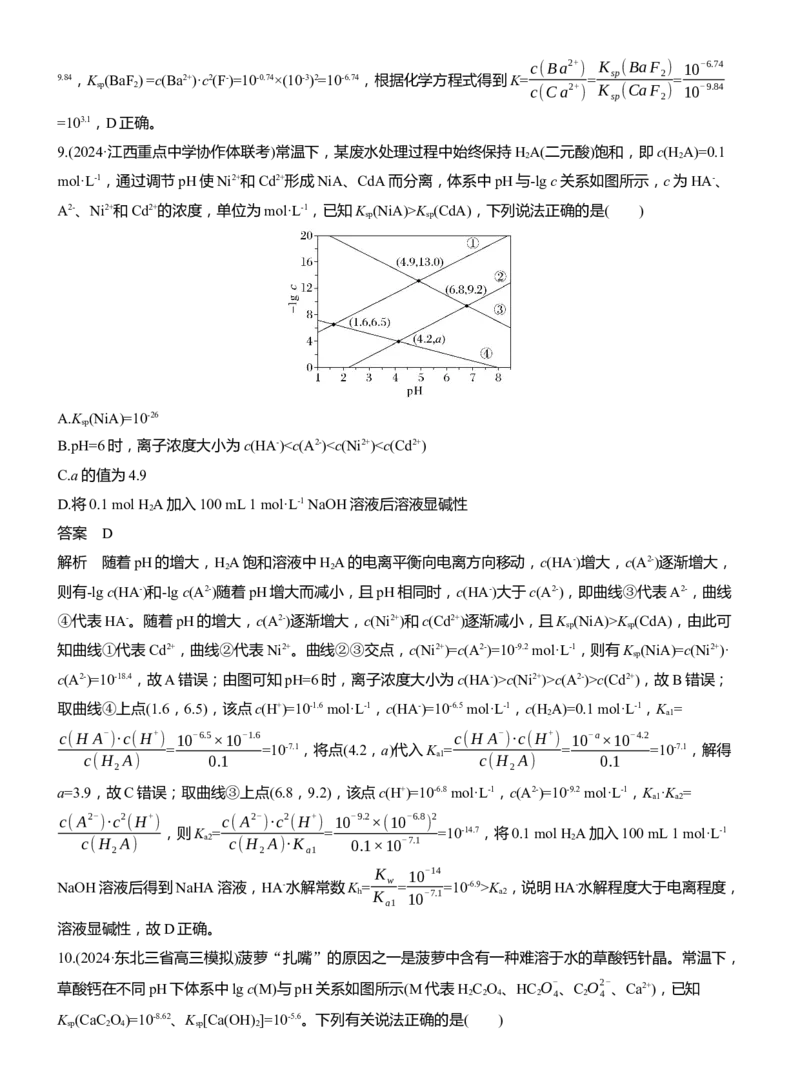
8.(2024·河南创新联盟名校模拟)常温下,向含BaCl 、CaCl 和HCl的溶液中滴加NaF溶液,溶液中
2 2
c(H+
)
pX[pX=-lgX,X=c(Ba2+)、c(Ca2+)、 ]与pF[pF=-lg c(F-)]关系如图所示。
c(HF)
已知:BaF 溶解度大于CaF 。下列叙述正确的是( )
2 2
A.L 直线代表pBa与pF的关系
1
B.K(HF)的数量级为10-2
a
C.相对L 直线,M点溶液是过饱和溶液
2
D.常温下,BaF +Ca2+ CaF +Ba2+的平衡常数K=103.1
2 2
答案 D
解析 根据图像中L 和L 的斜率相等,L 斜率较小且结合BaF 、CaF 组成相同可知:BaF 、CaF 直线的
1 2 3 2 2 2 2
c(H+
)
斜率相等,故L 代表p ~pF关系;又因为BaF 溶解度大于CaF ,所以K (BaF )>K (CaF ),即L 代
3 c(HF) 2 2 sp 2 sp 2 1
c(H+
)
表pCa ~pF关系,L 代表pBa ~pF关系,A错误;根据分析且利用图中a点坐标数据计算:K(HF)=
2 a c(HF)
×c(F-)=10-2.17×10-1=10-3.17,数量级为10-4,B错误;L 是BaF 的饱和溶液,而M点的QK (CdA),下列说法正确的是( )
sp sp
A.K (NiA)=10-26
sp
B.pH=6时,离子浓度大小为c(HA-)K (CdA),由此可
sp sp
知曲线①代表Cd2+,曲线②代表Ni2+。曲线②③交点,c(Ni2+)=c(A2-)=10-9.2 mol·L-1,则有K (NiA)=c(Ni2+)·
sp
c(A2-)=10-18.4,故A错误;由图可知pH=6时,离子浓度大小为c(HA-)>c(Ni2+)>c(A2-)>c(Cd2+),故B错误;
取曲线④上点(1.6,6.5),该点c(H+)=10-1.6 mol·L-1,c(HA-)=10-6.5 mol·L-1,c(H A)=0.1 mol·L-1,K =
2 a1
c(H A- )·c(H+ ) 10-6.5×10-1.6 c(H A- )·c(H+ ) 10-a×10-4.2
= =10-7.1,将点(4.2,a)代入K = = =10-7.1,解得
c(H A) 0.1 a1 c(H A) 0.1
2 2
a=3.9,故C错误;取曲线③上点(6.8,9.2),该点c(H+)=10-6.8 mol·L-1,c(A2-)=10-9.2 mol·L-1,K ·K =
a1 a2
c(A2- )·c2 (H+
)
c(A2- )·c2 (H+
)
10-9.2×(10-6.8
)
2
,则K = = =10-14.7,将0.1 mol H A加入100 mL 1 mol·L-1
c(H A) a2 c(H A)·K 0.1×10-7.1 2
2 2 a1
K 10-14
w
NaOH溶液后得到NaHA溶液,HA-水解常数K = = =10-6.9>K ,说明HA-水解程度大于电离程度,
h K 10-7.1 a2
a1
溶液显碱性,故D正确。
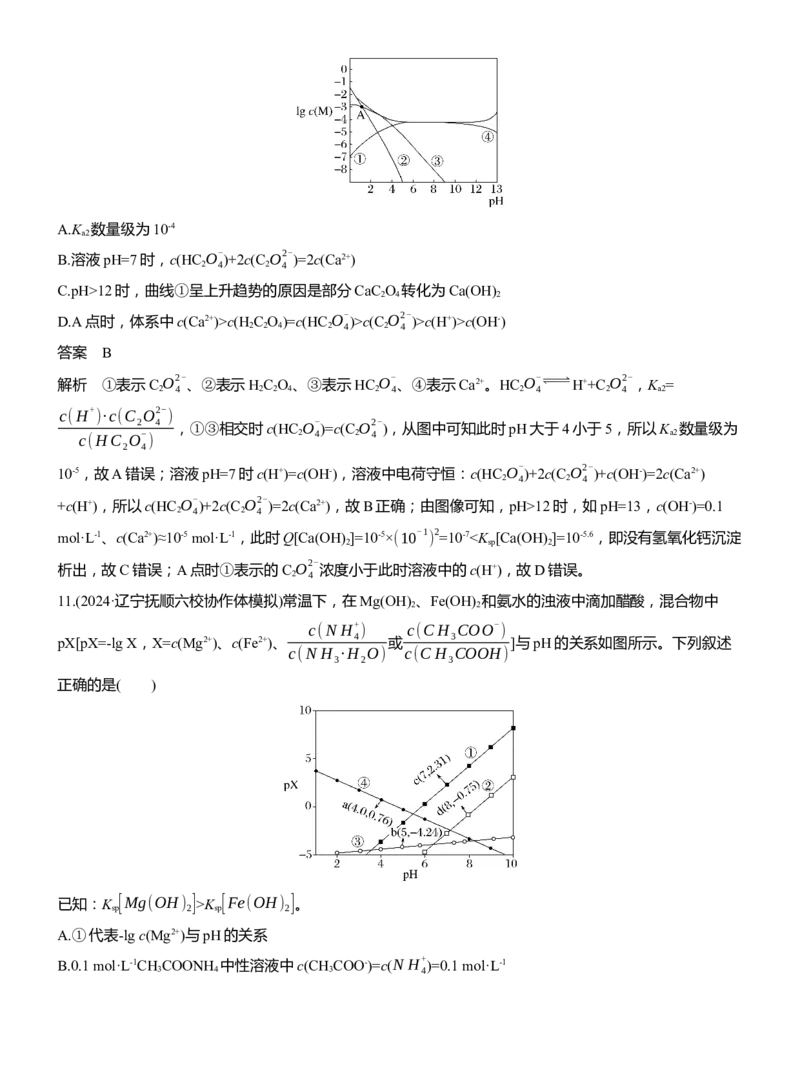
10.(2024·东北三省高三模拟)菠萝“扎嘴”的原因之一是菠萝中含有一种难溶于水的草酸钙针晶。常温下,
草酸钙在不同pH下体系中lg c(M)与pH关系如图所示(M代表H C O 、HC
O-
、C
O2-
、Ca2+),已知
2 2 4 2 4 2 4
K (CaC O )=10-8.62、K [Ca(OH) ]=10-5.6。下列有关说法正确的是( )
sp 2 4 sp 2A.K 数量级为10-4
a2
B.溶液pH=7时,c(HC
O-
)+2c(C
O2-
)=2c(Ca2+)
2 4 2 4
C.pH>12时,曲线①呈上升趋势的原因是部分CaC O 转化为Ca(OH)
2 4 2
D.A点时,体系中c(Ca2+)>c(H C O )=c(HC
O-
)>c(C
O2-
)>c(H+)>c(OH-)
2 2 4 2 4 2 4
答案 B
解析 ①表示C
O2-
、②表示H C O 、③表示HC
O-
、④表示Ca2+。HC
O-
H++C
O2-
,K =
2 4 2 2 4 2 4 2 4 2 4 a2
c(H+ )·c(C O2- )
2 4 ,①③相交时c(HC O- )=c(C O2- ),从图中可知此时pH大于4小于5,所以K 数量级为
c(HC O- ) 2 4 2 4 a2
2 4
10-5,故A错误;溶液pH=7时c(H+)=c(OH-),溶液中电荷守恒:c(HC
O-
)+2c(C
O2-
)+c(OH-)=2c(Ca2+)
2 4 2 4
+c(H+),所以c(HC
O-
)+2c(C
O2-
)=2c(Ca2+),故B正确;由图像可知,pH>12时,如pH=13,c(OH-)=0.1
2 4 2 4
mol·L-1、c(Ca2+)≈10-5 mol·L-1,此时Q[Ca(OH) ]=10-5×(10-1 ) 2=10-7K [Fe(OH) ]。
sp 2 sp 2
A.①代表-lg c(Mg2+)与pH的关系
B.0.1 mol·L-1CH COONH 中性溶液中c(CH COO-)=c(N H+ )=0.1 mol·L-1
3 4 3 4c(M g2+ )
C.在Mg(OH) 和Fe(OH) 的悬浊液中: =105.06
2 2 c(Fe2+
)
D.Mg(OH)
2
+2CH
3
COOH (CH
3
COO)
2
Mg+2H
2
O的平衡常数K为102.17
答案 C
解析 由已知:-lg c(Fe2+)、-lg c(Mg2+)与pH的直线斜率相同,Mg(OH) 溶度积较大,故①代表-lg c(Fe2+)与
2
c(N H+ ) K
pH的关系,②代表-lg c(Mg2+)与pH的关系, 4 = b ,随pH增大,比值减小,
c(N H ·H O) c(OH- )
3 2
c(CH COO- ) K c(CH COO- )
3 = a ,随pH增大,比值增大,因此④代表-lg 3 与pH的关系,③代表-
c(CH COOH) c(H+ ) c(CH COOH)
3 3
c(N H+ )
lg 4 与pH的关系。N H+ 和CH COO-均会水解,因此两者的浓度均小于0.1 mol·L-1,B项错
c(N H ·H O) 4 3
3 2
c(Mg2+ ) 10-11.25
误;由c、d点数据计算知,K [Mg(OH) ]=10-11.25,K [Fe(OH) ]=10-16.31, = =105.06,C项正
sp 2 sp 2 c(Fe2+
)
10-16.31
确;由a点数据计算知,K
a
(CH
3
COOH)=10-4.76,Mg(OH)
2
+2CH
3
COOH (CH
3
COO)
2
Mg+2H
2
O的平衡
K [Mg(OH) ]·K2 (CH COOH) 10-11.25×(10-4.76 ) 2
sp 2 a 3
常数K= = =107.23,D项错误。
K2 10-28
w