文档内容
专题六 化学速率平衡图表分析与数据处理
【考情分析】
从近几年看,化学反应速率和化学平衡的考查,试题的创新性、探究性逐年提升,
如:考查问题多样化的平衡图像问题,通过设计新颖的速率、平衡计算以及通过图
像、表格获取信息、数据等试题在情境上、取材上都有所创新,而且化学反应速率
与化学平衡还与元素化合物知识相互联系,综合考查,并且两者的结合也日趋紧
密。如2015·全国卷Ⅰ·28,2016·全国卷Ⅱ·27,2017·全国卷Ⅰ·28,2018·全国卷
Ⅰ·28,2018·全国卷Ⅱ·27等。
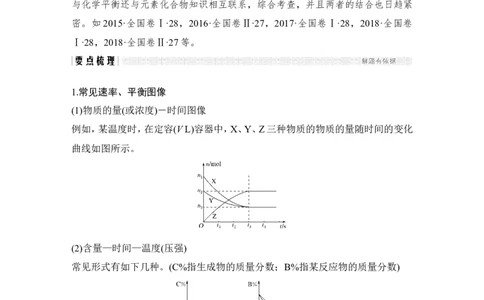
1.常见速率、平衡图像
(1)物质的量(或浓度)-时间图像
例如,某温度时,在定容(V L)容器中,X、Y、Z三种物质的物质的量随时间的变化
曲线如图所示。
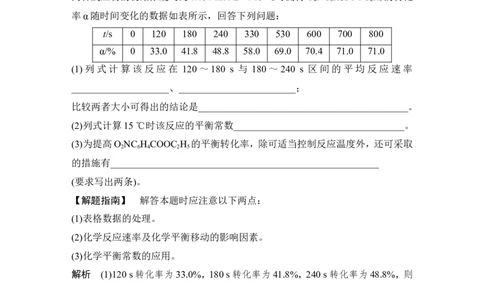
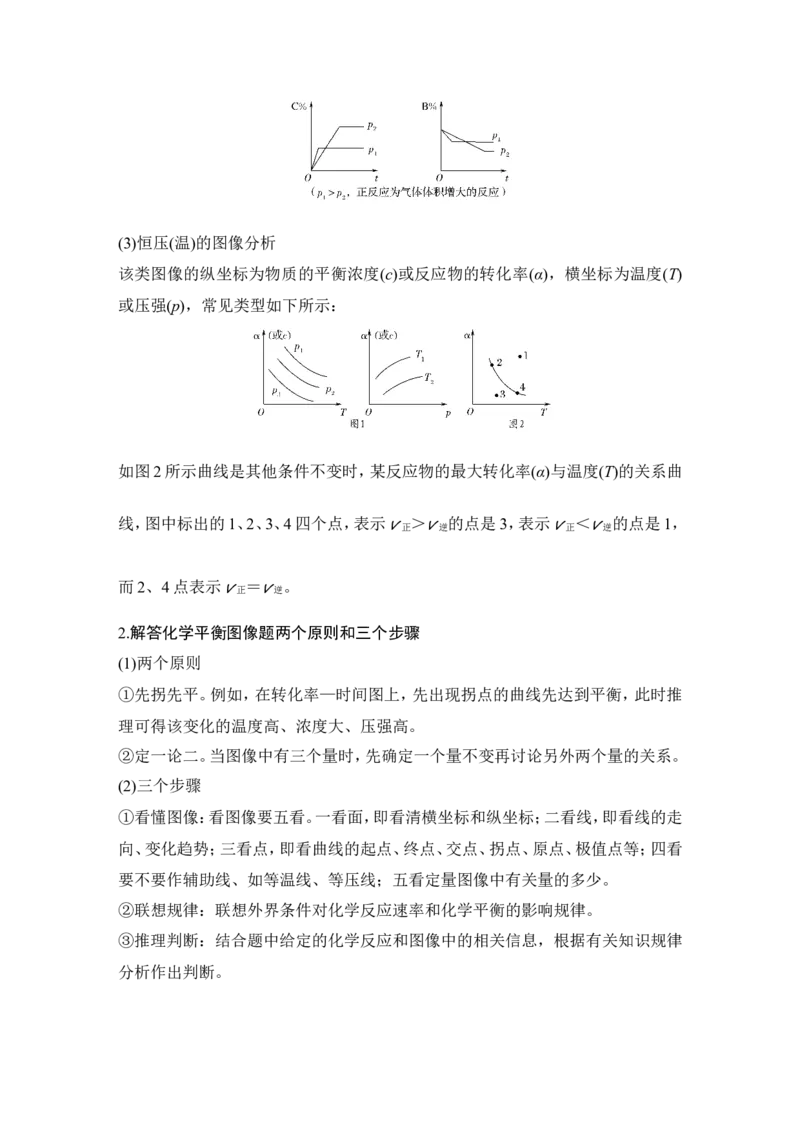
(2)含量—时间—温度(压强)
常见形式有如下几种。(C%指生成物的质量分数;B%指某反应物的质量分数)(3)恒压(温)的图像分析
该类图像的纵坐标为物质的平衡浓度(c)或反应物的转化率(α),横坐标为温度(T)
或压强(p),常见类型如下所示:
如图2所示曲线是其他条件不变时,某反应物的最大转化率(α)与温度(T)的关系曲
线,图中标出的1、2、3、4四个点,表示 > 的点是3,表示 < 的点是1,
v正 v逆 v正 v逆
而2、4点表示 = 。
v正 v逆
2.解答化学平衡图像题两个原则和三个步骤
(1)两个原则
①先拐先平。例如,在转化率—时间图上,先出现拐点的曲线先达到平衡,此时推
理可得该变化的温度高、浓度大、压强高。
②定一论二。当图像中有三个量时,先确定一个量不变再讨论另外两个量的关系。
(2)三个步骤
①看懂图像:看图像要五看。一看面,即看清横坐标和纵坐标;二看线,即看线的走
向、变化趋势;三看点,即看曲线的起点、终点、交点、拐点、原点、极值点等;四看
要不要作辅助线、如等温线、等压线;五看定量图像中有关量的多少。
②联想规律:联想外界条件对化学反应速率和化学平衡的影响规律。
③推理判断:结合题中给定的化学反应和图像中的相关信息,根据有关知识规律
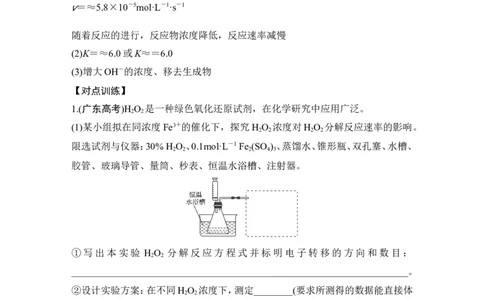
分析作出判断。考点指导1 化学平衡中的表格数据处理
【典例1】 (海南高考)硝基苯甲酸乙酯在OH-存在下发生水解反应:
O NC H COOC H +OH- O NC H COO-+C H OH
2 6 4 2 5 2 6 4 2 5
两种反应物的初始浓度均为0.050 mol·L-1,15 ℃时测得O NC H COOC H 的转化
2 6 4 2 5
率α随时间变化的数据如表所示,回答下列问题:
t/s 0 120 180 240 330 530 600 700 800
α/% 0 33.0 41.8 48.8 58.0 69.0 70.4 71.0 71.0
(1)列式计算该反应在 120~180 s 与 180~240 s 区间的平均反应速率
____________________、________________________;
比较两者大小可得出的结论是___________________________________________。
(2)列式计算15 ℃时该反应的平衡常数___________________________________。
(3)为提高O NC H COOC H 的平衡转化率,除可适当控制反应温度外,还可采取
2 6 4 2 5
的措施有_______________________________________________________
(要求写出两条)。
【解题指南】 解答本题时应注意以下两点:
(1)表格数据的处理。
(2)化学反应速率及化学平衡移动的影响因素。
(3)化学平衡常数的应用。
解析 (1)120 s转化率为33.0%,180 s转化率为41.8%,240 s转化率为48.8%,则
120 ~ 180 s 反 应 速 率 = [0.050 mol·L - 1×(41.8% - 33.0%)]/(180 s - 120
v
s)≈7.3×10-5mol·L-1·s-1,则180~240 s反应速率 =[0.050 mol·L-1×(48.8%-
v
41.8%)]/(240 s-180 s)≈5.8×10-5mol·L-1·s-1,相同时间段内平均速率减小,主要
原因是随着反应进行,反应物浓度逐渐减小,反应速率逐渐减小;
(2)根据表格数据,转化率为71.0%就不再发生变化,即达到化学平衡状态,则化学
平衡常数K==(0.050 mol·L-1×71.0%)2/[0.050 mol·L-1×(1-71.0%)]2=(71/29)2≈6.0;
(3)提高反应物的转化率,是使化学平衡向正反应方向移动,除了控制温度外,根据
化学反应特点(溶液间进行的反应),压强不能改变平衡,因此可以增大另一种反应
物的浓度提高转化率,还可以减少生成物浓度(即移走生成物)增大反应物的转化
率。
答案 (1) ==7.3×10-5mol·L-1·s-1
v
=≈5.8×10-5mol·L-1·s-1
v
随着反应的进行,反应物浓度降低,反应速率减慢
(2)K=≈6.0或K≈=6.0
(3)增大OH-的浓度、移去生成物
【对点训练】
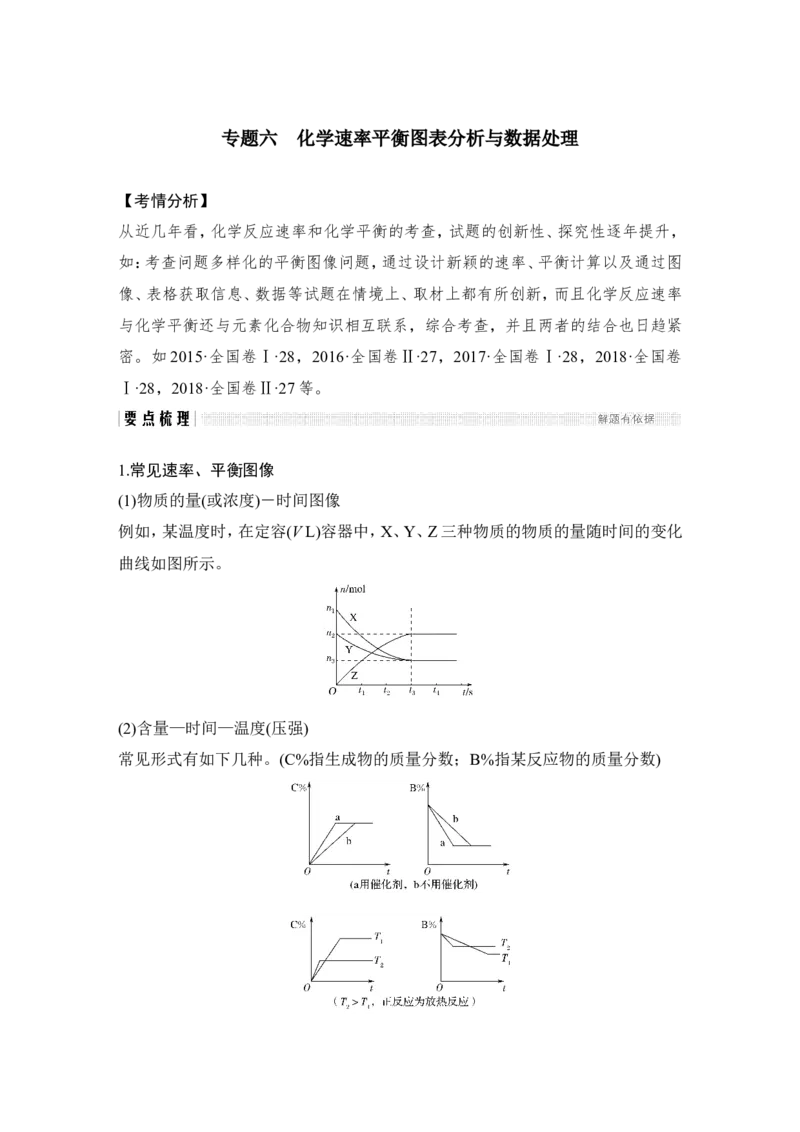
1.(广东高考)H O 是一种绿色氧化还原试剂,在化学研究中应用广泛。
2 2
(1)某小组拟在同浓度Fe3+的催化下,探究H O 浓度对H O 分解反应速率的影响。
2 2 2 2
限选试剂与仪器:30% H O 、0.1mol·L-1 Fe (SO ) 、蒸馏水、锥形瓶、双孔塞、水槽、
2 2 2 4 3
胶管、玻璃导管、量筒、秒表、恒温水浴槽、注射器。
①写出本实验 H O 分解反应方程式并标明电子转移的方向和数目:
2 2
_____________________________________________________________________。
②设计实验方案:在不同H O 浓度下,测定________(要求所测得的数据能直接体
2 2
现反应速率大小)。
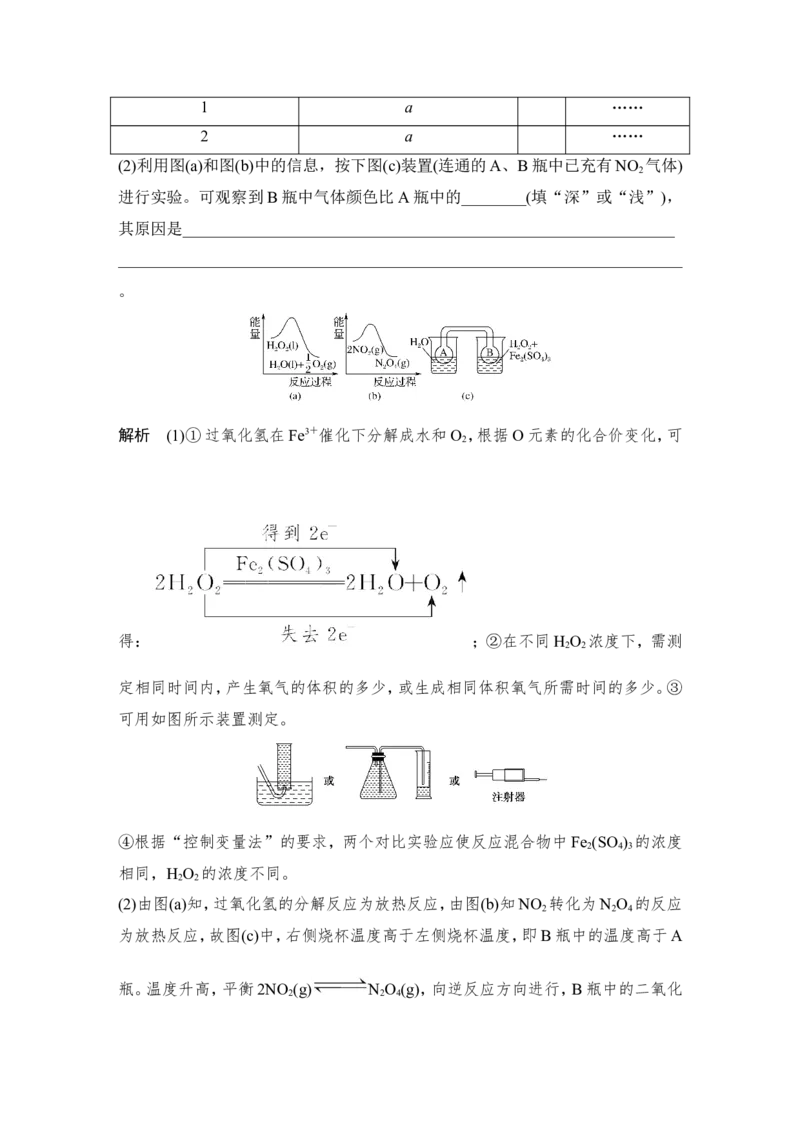
③设计实验装置,完成如图所示的装置示意图。
④参照下表格式,拟定实验表格,完整体现实验方案(列出所选试剂体积、需记录
的待测物理量和所拟定的数据;数据用字母表示)。
物理量
V[0.1 mol·L-1 Fe (SO ) ]/mL ……
2 4 3
实验序号1 a ……
2 a ……
(2)利用图(a)和图(b)中的信息,按下图(c)装置(连通的A、B瓶中已充有NO 气体)
2
进行实验。可观察到B瓶中气体颜色比A瓶中的________(填“深”或“浅”),
其原因是_____________________________________________________________
______________________________________________________________________
。
解析 (1)①过氧化氢在Fe3+催化下分解成水和O ,根据O元素的化合价变化,可
2
得: ;②在不同H O 浓度下,需测
2 2
定相同时间内,产生氧气的体积的多少,或生成相同体积氧气所需时间的多少。③
可用如图所示装置测定。
④根据“控制变量法”的要求,两个对比实验应使反应混合物中Fe (SO ) 的浓度
2 4 3
相同,H O 的浓度不同。
2 2
(2)由图(a)知,过氧化氢的分解反应为放热反应,由图(b)知NO 转化为N O 的反应
2 2 4
为放热反应,故图(c)中,右侧烧杯温度高于左侧烧杯温度,即B瓶中的温度高于A
瓶。温度升高,平衡2NO (g) N O (g),向逆反应方向进行,B瓶中的二氧化
2 2 4氮浓度增大,颜色比A瓶颜色深。
答案 (1)①
②生成相同体积的氧气所需的时间(或相同时间内,生成氧气的体积)
③
④
V(H O )/mL V(H O)/mL V(O ) mL t/s
2 2 2 2
1 b 2b e d
2 2b b e f
或
V(H O )/mL V(H O)/mL t/s V(O ) mL
2 2 2 2
1 b 2b e d
2 2b b e f
(2)深 因为过氧化氢分解是放热反应,2NO (g) N O (g)也是放热反应,所
2 2 4
以B瓶温度高于A瓶,温度升高,平衡逆向移动,二氧化氮浓度增大,颜色加深考
点指导2 速率、平衡图像分析
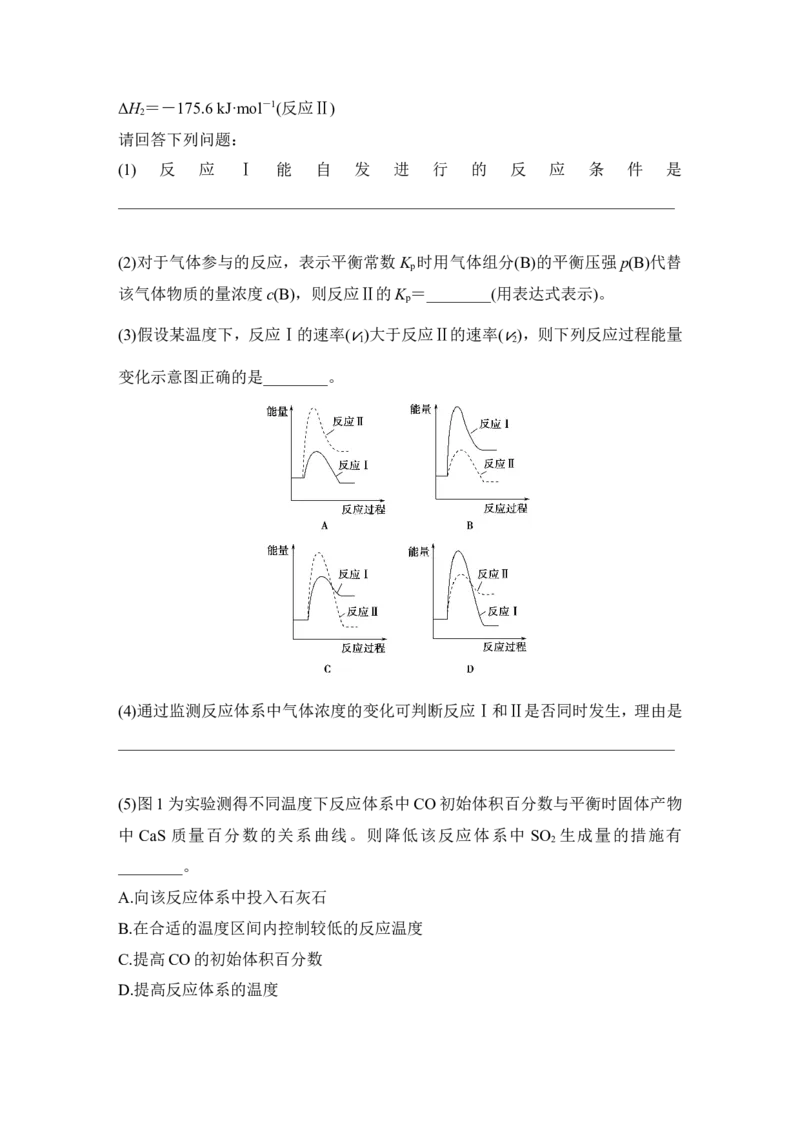
【典例2】 (浙江高考)煤炭燃烧过程中会释放出大量的SO ,严重破坏生态环境。
2
采用一定的脱硫技术可以把硫元素以CaSO 的形式固定,从而降低SO 的排放。
4 2
但是煤炭燃烧过程中产生的CO又会与CaSO 发生化学反应,降低了脱硫效率。相
4
关反应的热化学方程式如下:
CaSO (s)+CO(g) CaO(s)+SO (g)+CO (g)
4 2 2
ΔH =218.4 kJ·mol-1(反应Ⅰ)
1
CaSO (s)+4CO(g) CaS(s)+4CO (g)
4 2ΔH =-175.6 kJ·mol-1(反应Ⅱ)
2
请回答下列问题:
(1) 反 应 Ⅰ 能 自 发 进 行 的 反 应 条 件 是
_____________________________________________________________________
(2)对于气体参与的反应,表示平衡常数 K 时用气体组分(B)的平衡压强p(B)代替
p
该气体物质的量浓度c(B),则反应Ⅱ的K =________(用表达式表示)。
p
(3)假设某温度下,反应Ⅰ的速率( )大于反应Ⅱ的速率( ),则下列反应过程能量
v1 v2
变化示意图正确的是________。
(4)通过监测反应体系中气体浓度的变化可判断反应Ⅰ和Ⅱ是否同时发生,理由是
_____________________________________________________________________
(5)图1为实验测得不同温度下反应体系中CO初始体积百分数与平衡时固体产物
中 CaS 质量百分数的关系曲线。则降低该反应体系中 SO 生成量的措施有
2
________。
A.向该反应体系中投入石灰石
B.在合适的温度区间内控制较低的反应温度
C.提高CO的初始体积百分数
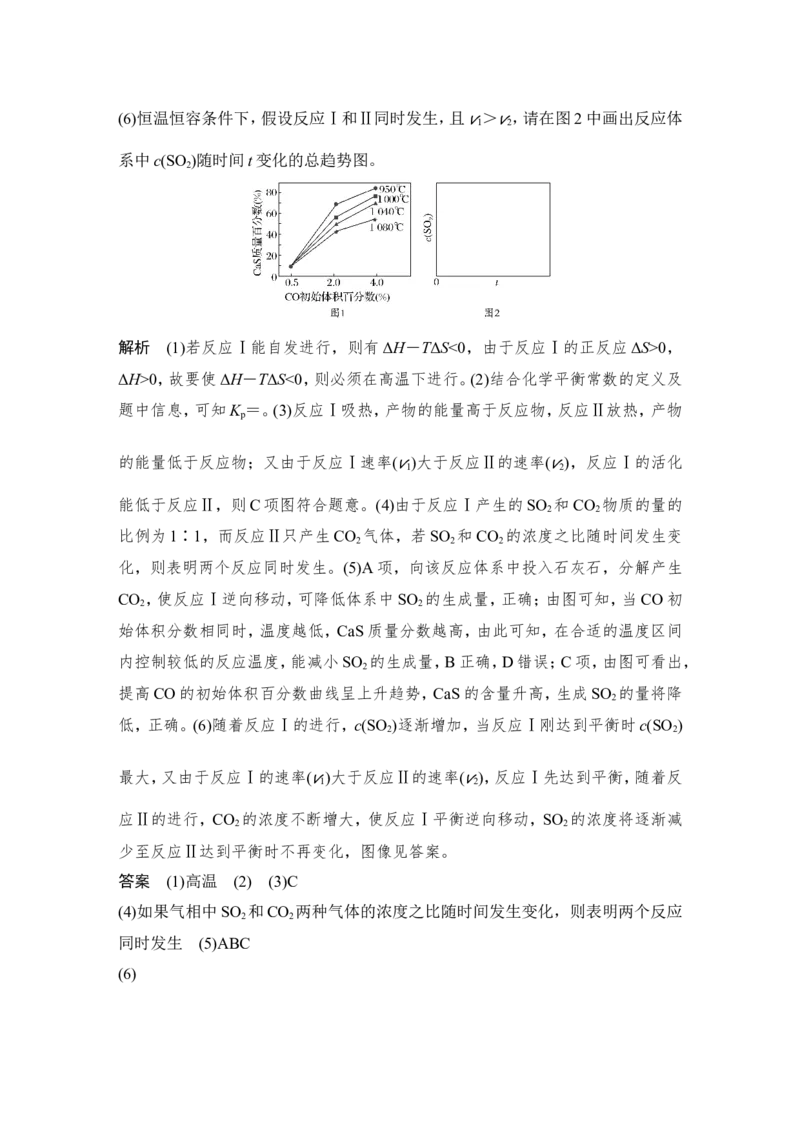
D.提高反应体系的温度(6)恒温恒容条件下,假设反应Ⅰ和Ⅱ同时发生,且 > ,请在图2中画出反应体
v1 v2
系中c(SO )随时间t变化的总趋势图。
2
解析 (1)若反应Ⅰ能自发进行,则有ΔH-TΔS<0,由于反应Ⅰ的正反应ΔS>0,
ΔH>0,故要使ΔH-TΔS<0,则必须在高温下进行。(2)结合化学平衡常数的定义及
题中信息,可知K =。(3)反应Ⅰ吸热,产物的能量高于反应物,反应Ⅱ放热,产物
p
的能量低于反应物;又由于反应Ⅰ速率( )大于反应Ⅱ的速率( ),反应Ⅰ的活化
v1 v2
能低于反应Ⅱ,则C项图符合题意。(4)由于反应Ⅰ产生的SO 和CO 物质的量的
2 2
比例为1∶1,而反应Ⅱ只产生CO 气体,若SO 和CO 的浓度之比随时间发生变
2 2 2
化,则表明两个反应同时发生。(5)A项,向该反应体系中投入石灰石,分解产生
CO ,使反应Ⅰ逆向移动,可降低体系中SO 的生成量,正确;由图可知,当CO初
2 2
始体积分数相同时,温度越低,CaS质量分数越高,由此可知,在合适的温度区间
内控制较低的反应温度,能减小SO 的生成量,B正确,D错误;C项,由图可看出,
2
提高CO的初始体积百分数曲线呈上升趋势,CaS的含量升高,生成SO 的量将降
2
低,正确。(6)随着反应Ⅰ的进行,c(SO )逐渐增加,当反应Ⅰ刚达到平衡时c(SO )
2 2
最大,又由于反应Ⅰ的速率( )大于反应Ⅱ的速率( ),反应Ⅰ先达到平衡,随着反
v1 v2
应Ⅱ的进行,CO 的浓度不断增大,使反应Ⅰ平衡逆向移动,SO 的浓度将逐渐减
2 2
少至反应Ⅱ达到平衡时不再变化,图像见答案。
答案 (1)高温 (2) (3)C
(4)如果气相中SO 和CO 两种气体的浓度之比随时间发生变化,则表明两个反应
2 2
同时发生 (5)ABC
(6)【解题指南】
解答本题时应注意以下四点:
(1)活化能对化学反应速率的影响。
(2)化学平衡常数的多维表示方法
(3)图像的审读及解题信息的获取。
(4)做图能力的训练。
【对点训练】
2.(新课标全国卷)乙醇是重要的有机化工原料,可由乙烯气相直接水合法或间接水
合法生产。回答下列问题:
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C H OSO H),再水解
2 5 3
生 成 乙 醇 。 写 出 相 应 反 应 的 化 学 方 程 式
_____________________________________________________________________。
(2)已知:
甲醇脱水反应
2CH OH(g)===CH OCH (g)+H O(g)ΔH =-23.9 kJ·mol-1
3 3 3 2 1
甲醇制烯烃反应
2CH OH(g)===C H (g)+2H O(g)ΔH =-29.1 kJ·mol-1
3 2 4 2 2
乙醇异构化反应
C H OH(g)===CH OCH (g)ΔH =+50.7 kJ·mol-1
2 5 3 3 3
则乙烯气相直接水合反应C H (g)+H O(g)===C H OH(g)的ΔH=________
2 4 2 2 5
kJ·mol - 1 。 与 间 接 水 合 法 相 比 , 气 相 直 接 水 合 法 的 优 点 是
_____________________________________________________________________。
(3)下图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系 (其中
nH O∶nC H =1∶1)。
2 2 4①列式计算乙烯水合制乙醇反应在图中A点的平衡常数K =________(用平衡分
p
压代替平衡浓度计算,分压=总压×物质的量分数)。
② 图 中 压 强 p 、 p 、 p 、 p 的 大 小 顺 序 为 ______________ , 理 由 是
1 2 3 4
_____________________________________________________________________。
③气相直接水合法常用的工艺条件为:磷酸/硅藻土为催化剂,反应温度290 ℃、压
强6.9 MPa,n(H O)∶n(C H )=0.6∶1。乙烯的转化率为5%。若要进一步提高乙烯
2 2 4
的转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有________、
________。
解析 (1)乙烯与浓硫酸反应生成 C H OSO H,C H OSO H 与水反应生成
2 5 3 2 5 3
CH CH OH,根据原子守恒配平,即可得相应化学方程式:CH ===CH +
3 2 2 2
H SO (浓)―→C H OSO H,C H OSO H+H O―→C H OH+H SO 。
2 4 2 5 3 2 5 3 2 2 5 2 4
(2)2CH OH(g)===CH OCH (g)+H O(g)ΔH =-23.9 kJ·mol-1 ①
3 3 3 2 1
2CH OH(g)===C H (g)+2H O(g)ΔH =-29.1 kJ·mol-1 ②
3 2 4 2 2
C H OH(g)===CH OCH (g)ΔH =+50.7 kJ·mol-1 ③
2 5 3 3 3
根据盖斯定律,由①-②-③得:
C H (g)+H O(g)===C H OH(g)ΔH=-45.5 kJ·mol-1。
2 4 2 2 5
浓硫酸具有强腐蚀性,且浓硫酸与有机物反应常伴有副反应,产生SO 、CO 等气
2 2
体,直接水合反应过程中没有用到浓硫酸,故可有效避免对设备的腐蚀及对环境
的污染。
(3)①设开始充入的原料气中,C H (g)和H O(g)的物质的量均为n。
2 4 2
C H (g)+H O(g)===C H OH(g)
2 4 2 2 5
开始(mol) n n 0
转化(mol) 20%n 20%n 20%n
平衡(mol) 80%n 80%n 20%n
平衡混合气中C H (g)、H O(g)、C H OH(g)的物质的量分数依次为:、、。
2 4 2 2 5
根据题意,将数据代入化学平衡常数表达式,K =。
p②C H (g)+H O(g) C H OH(g)是一个气体体积减小的反应,相同温度下,
2 4 2 2 5
增大压强,平衡向正反应方向移动,C H 的转化率提高,所以p >p >p >p 。
2 4 4 3 2 1
③依据反应特点及平衡移动原理,提高乙烯转化率还可以增大H O与C H 的比例
2 2 4
或将乙醇及时液化分离出去等。
答 案 (1)CH ===CH + H SO ( 浓 )―→C H OSO H , C H OSO H +
2 2 2 4 2 5 3 2 5 3
H O―→C H OH+H SO
2 2 5 2 4
(2)-45.5 污染小,腐蚀性小等
(3)①===0.07(MPa)-1
②p >p >p >p 反应分子数减少,相同温度下,压强升高,乙烯转化率提高
4 3 2 1
③将产物乙醇液化移去 增加nH O∶nC H 比
2 2 4
【课堂总结】
“平衡图像”认知模型构建