文档内容
专题十四 物质结构与性质
考 点 高考年 考频解密 考点分布
2022 年河北卷〔17〕;2022 年山东卷
〔16〕;2022年湖南卷〔18〕;2022年广
物质结构 原子结构与性质〔6次〕,
东卷〔20〕;2022年江苏卷〔14〕;2022
2022 年 分子结构与性质〔8次〕,
与性质 年海南卷〔19〕;2022年北京卷〔15〕;
晶体结构与性质〔8次〕
2022年全国甲卷〔11〕,2022年全国乙卷
〔11〕等
1.物质结构常见考点剖析
(1)以原子或离子结构为主线的考查角度
(2)以分子结构为主线的考查角度(3)以晶体结构为主线的考查角度
2.性质比较及解释类问题模型构建
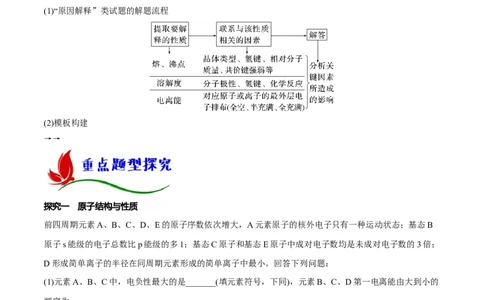
(1)“原因解释”类试题的解题流程
(2)模板构建
→→
探究一 原子结构与性质
前四周期元素A、B、C、D、E的原子序数依次增大,A元素原子的核外电子只有一种运动状态;基态B
原子s能级的电子总数比p能级的多1;基态C原子和基态E原子中成对电子数均是未成对电子数的3倍;
D形成简单离子的半径在同周期元素形成的简单离子中最小。回答下列问题:
(1)元素A、B、C中,电负性最大的是_______(填元素符号,下同),元素B、C、D第一电离能由大到小的
顺序为_______。
(2)与同族其他元素X形成的XA 相比,BA 易液化的原因是_______;BA 分子中键角_______109°28′(填
3 3 3
“>”“<”或“=”),原因是_______。
(3)基态E原子的电子排布式为_______;C、E形成的化合物EC (其中E的化合价为+6)中σ键与π键数目
5
之比为_______。
(4)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞参
数为apm,则晶体的密度为_______g·cm-3(用N 表示阿伏加德罗常数)。
A【变式练习】
1.主族元素N、F、Si、As、Se、Cl、Ti等的某些化合物对工农业生产意义重大,回答下列问题:
(1)Si N 陶瓷是世界上最坚硬的物质之一,具有高强度、低密度、耐高温等性质,其属于_______晶体;高
3 4
纯硅制备过程中会有SiHCl 、SiCl 等中间产物生成。沸点:SiHCl _______ SiCl (填“>”或“<”),SiCl 中
3 4 3 4 4
Si采取的杂化类型为_______。
(2)O、F、Cl电负性由大到小的顺序为_______;OF 分子的空间构型为_______;OF 的熔、沸点低于
2 2
ClO,原因是_______。
2
(3)Se元素基态原子的原子核外电子排布式为_______;As的第一电离能比Se的第一电离能大的原因为
_______。
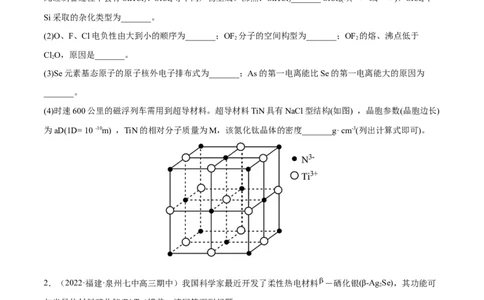
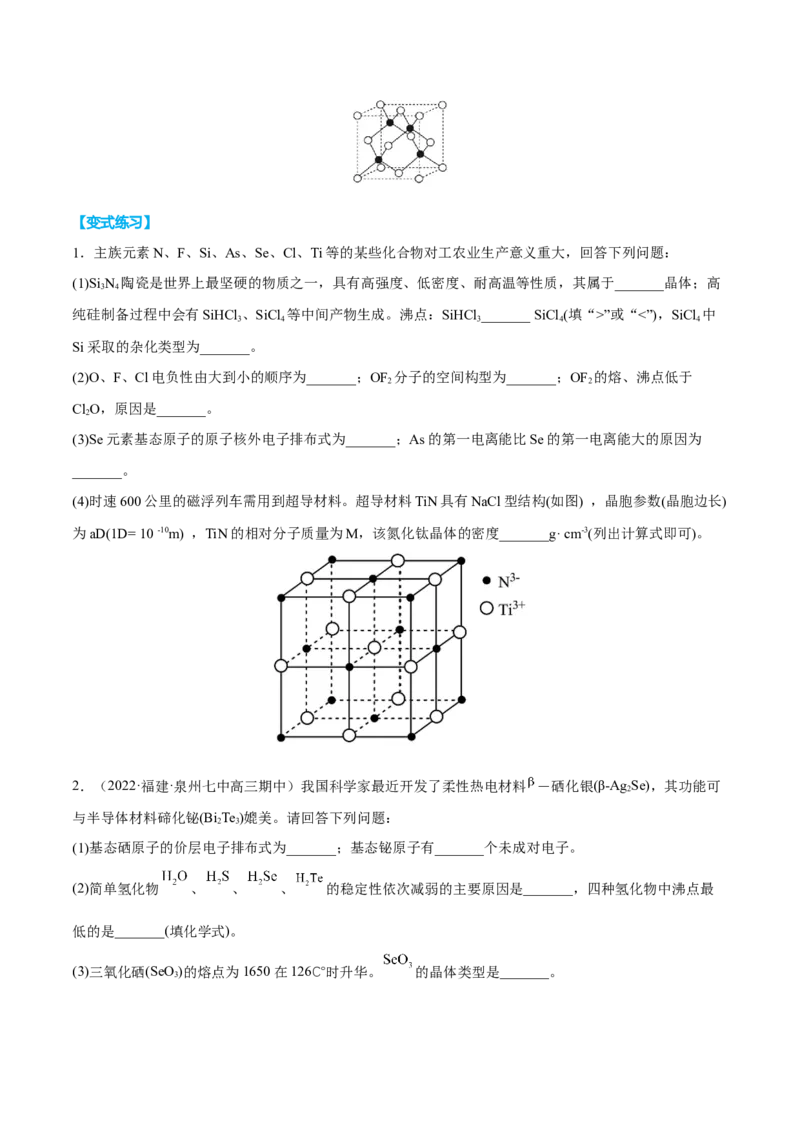
(4)时速600公里的磁浮列车需用到超导材料。超导材料TiN具有NaCl型结构(如图) ,晶胞参数(晶胞边长)
为aD(1D= 10 -10m) ,TiN的相对分子质量为M,该氮化钛晶体的密度_______g· cm-3(列出计算式即可)。
2.(2022·福建·泉州七中高三期中)我国科学家最近开发了柔性热电材料 ―硒化银(β-Ag Se),其功能可
2
与半导体材料碲化铋(Bi Te)媲美。请回答下列问题:
2 3
(1)基态硒原子的价层电子排布式为_______;基态铋原子有_______个未成对电子。
(2)简单氢化物 、 、 、 的稳定性依次减弱的主要原因是_______,四种氢化物中沸点最
低的是_______(填化学式)。
(3)三氧化硒(SeO )的熔点为1650在126℃时升华。 的晶体类型是_______。
3(4)我国科学家利用亚硒酸盐和硫酸盐追踪固氮酶取得新进展。亚硒酸根 的空间构型是_______,碲酸
根 中Te的杂化类型是_______。
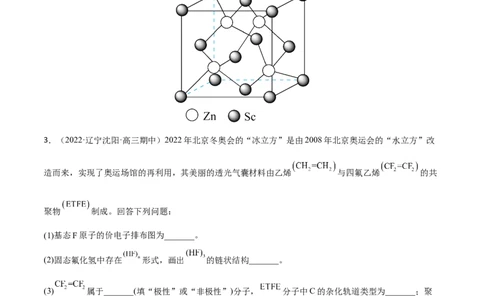
(5)半导体材料硒化锌的晶胞如图所示。已知该晶胞参数为anm,则该晶体密度为_______ (用晶胞参
数a表示)
3.(2022·辽宁沈阳·高三期中)2022年北京冬奥会的“冰立方”是由2008年北京奥运会的“水立方”改
造而来,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯 与四氟乙烯 的共
聚物 制成。回答下列问题:
(1)基态F原子的价电子排布图为_______。
(2)固态氟化氢中存在 形式,画出 的链状结构_______。
(3) 属于_______(填“极性”或“非极性”)分子, 分子中C的杂化轨道类型为_______;聚
四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因:_______。
(4)萤石 是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是_______;若该立方晶
胞参数为 ,正负离子的核间距最小为_______ 。探究二 分子结构与性质
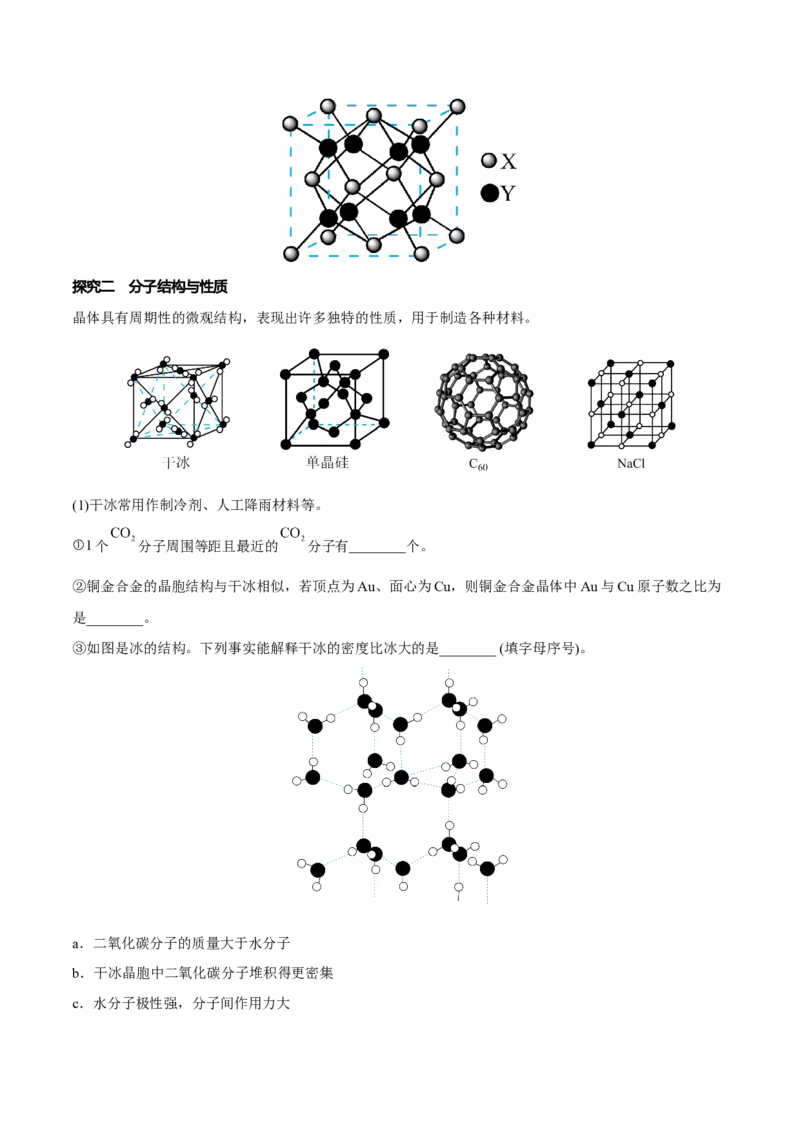
晶体具有周期性的微观结构,表现出许多独特的性质,用于制造各种材料。
(1)干冰常用作制冷剂、人工降雨材料等。
①1个 分子周围等距且最近的 分子有________个。
②铜金合金的晶胞结构与干冰相似,若顶点为Au、面心为Cu,则铜金合金晶体中Au与Cu原子数之比为
是________。
③如图是冰的结构。下列事实能解释干冰的密度比冰大的是________ (填字母序号)。
a.二氧化碳分子的质量大于水分子
b.干冰晶胞中二氧化碳分子堆积得更密集
c.水分子极性强,分子间作用力大d.冰中氢键存在方向性,晶体有较大空隙,空间利用率低
(2)单晶硅等作为制造太阳能电池的材料已得到广泛应用。
①单晶硅中最小的环上有________个Si原子。
②1mol单晶硅中含有________mol Si-Si键。
(3) 是一种碳的单质。
①1个 晶胞中含有________个分子。
②世界上第一辆单分子“纳米小车”的四个轮子是 ,小车运行情况如图所示,从a处化学键的特点说明
其运动原因:________。
(4)NiO晶体与NaCl晶体结构相似。
晶体 离子间距/nm 熔点/℃
NaCl 801
NiO 1960
①NiO的熔点远高于NaCl,结合右表说明理由:________。
②设阿伏加德罗常数的值为 ,距离最近的两个 间距为a pm( ),NiO的摩尔质量为M
,则晶体的密度为________ (列出计算式)。
③晶体普遍存在各种缺陷。某种NiO晶体中存在如右图所示的缺陷:当一个 空缺,会有两个 被两
个 所取代,但晶体仍呈电中性。经测定某氧化镍样品中 与 的离子数之比为6:91。若该晶体的化学式为 ,则x=________。
【变式练习】
1.(2022·辽宁实验中学高三期中)完成下列问题
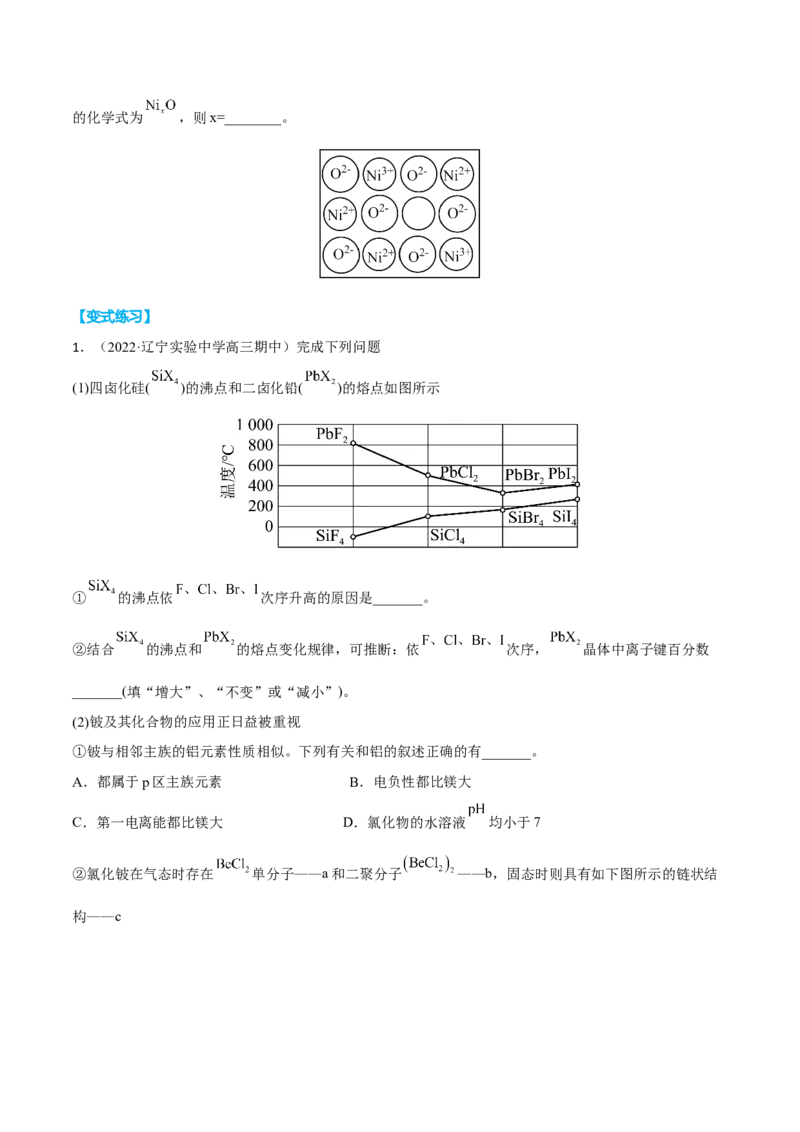
(1)四卤化硅( )的沸点和二卤化铅( )的熔点如图所示
① 的沸点依 次序升高的原因是_______。
②结合 的沸点和 的熔点变化规律,可推断:依 次序, 晶体中离子键百分数
_______(填“增大”、“不变”或“减小”)。
(2)铍及其化合物的应用正日益被重视
①铍与相邻主族的铝元素性质相似。下列有关和铝的叙述正确的有_______。
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.氯化物的水溶液 均小于7
②氯化铍在气态时存在 单分子——a和二聚分子 ——b,固态时则具有如下图所示的链状结
构——ca属于_______(填“极性”或“非极性”)分子,二聚分子 中 原子的杂化方式相同,且所有原子
都在同一平面上,b的结构式为_______。
③ 立方晶胞如下图所示。
阿伏伽德罗常数的数值为 ,若 晶体的密度为 ,则 和 之间最近的距离为_______
。
2.(2022·北京·北师大实验中学高三期中)钛及其化合物被广泛应用于飞机、火箭、卫星、舰艇、医疗以
及石油化工等领域。回答下列问题:
(1)基态Ti原子的核外电子排布式为___________。
(2)钛与卤素形成的化合物TiX 熔点如下表:
4
TiX TiF TiCl TiBr TiI
4 4 4 4 4
熔点/℃ 377 -24 38.3 153
解释TiX 熔点差异的原因___________。
4
(3) TiCl 能与甲胺(CHNH )形成稳定的配合物[TiCl (CHNH )]。
4 3 2 4 3 2 2
①甲胺中N原子的杂化方式为___________。
②CH NH 中H-N-H键角比[TiCl (CHNH )]中H-N-H键角小,从结构角度解释原因___________。
3 2 4 3 2 2
(4)TiO 的化学性质非常稳定,广泛用于涂料、橡胶和造纸等工业。
2
①向TiCl 中加入大量的水,可制得TiO∙xH O,该反应的化学方程式为___________,所得TiO∙xH O经焙
4 2 2 2 2
烧得到TiO。
2
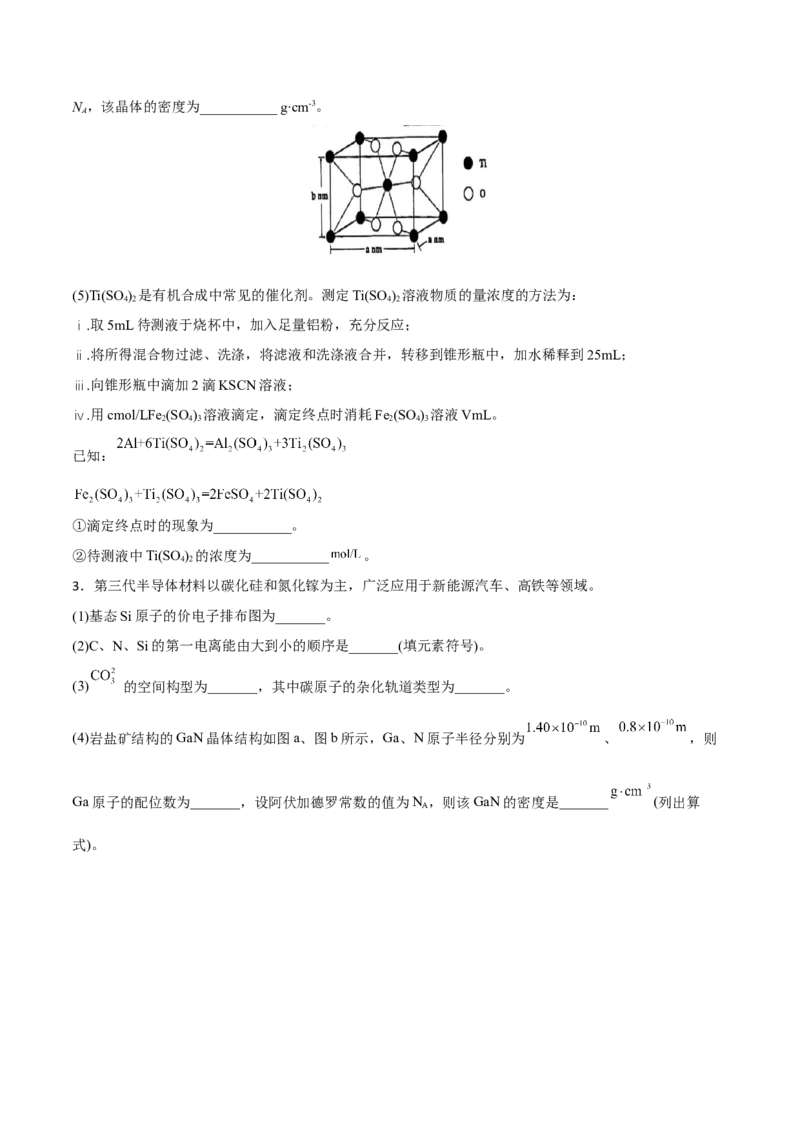
②金红石型TiO 的晶胞为长方体,晶胞参数如图所示。TiO 的摩尔质量为80 g∙mol-1,阿伏加德罗常数为
2 2N ,该晶体的密度为___________ g∙cm-3。
A
(5)Ti(SO ) 是有机合成中常见的催化剂。测定Ti(SO ) 溶液物质的量浓度的方法为:
4 2 4 2
ⅰ.取5mL待测液于烧杯中,加入足量铝粉,充分反应;
ⅱ.将所得混合物过滤、洗涤,将滤液和洗涤液合并,转移到锥形瓶中,加水稀释到25mL;
ⅲ.向锥形瓶中滴加2滴KSCN溶液;
ⅳ.用cmol/LFe (SO ) 溶液滴定,滴定终点时消耗Fe (SO ) 溶液VmL。
2 4 3 2 4 3
已知:
①滴定终点时的现象为___________。
②待测液中Ti(SO ) 的浓度为___________ 。
4 2
3.第三代半导体材料以碳化硅和氮化镓为主,广泛应用于新能源汽车、高铁等领域。
(1)基态Si原子的价电子排布图为_______。
(2)C、N、Si的第一电离能由大到小的顺序是_______(填元素符号)。
(3) 的空间构型为_______,其中碳原子的杂化轨道类型为_______。
(4)岩盐矿结构的GaN晶体结构如图a、图b所示,Ga、N原子半径分别为 、 ,则
Ga原子的配位数为_______,设阿伏加德罗常数的值为N ,则该GaN的密度是_______ (列出算
A
式)。(5)煤的气化是一种重要的制氢途径。在一定温度下:向体积固定的密闭容器中加入足量的 和1mol
,发生下列反应生成水煤气:
Ⅰ.
Ⅱ.
反应平衡时, 的转化率为50%,CO的物质的量为0.1mol。
① _______。
②下列说法正确的是_______。
A.将炭块粉碎,可加快反应速率
B.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
C.混合气体的密度保持不变时,说明反应体系已达到平衡
D.平衡时 的体积分数可能大于
③求反应Ⅱ的平衡常数K=_______。
探究三 晶体结构与性质
(2022·浙江温州·模拟)完成下列问题。
(1)已知气体溶解度(气体压强为 ,温度为293K,在100g水中的溶解度)数据如下表:
气
溶解度/g 分子结构特点
体
乙
0.0062 中心原子 杂化,轨道半径较大,C负电性(δ-)及H正电性(δ+)不明显
烷乙
0.117 中心原子sp杂化,轨道半径较小,C负电性(δ-)及H正电性(δ+)明显
炔
结合上表信息,说明乙烷与乙炔气体的溶解度存在差异的原因:_______。
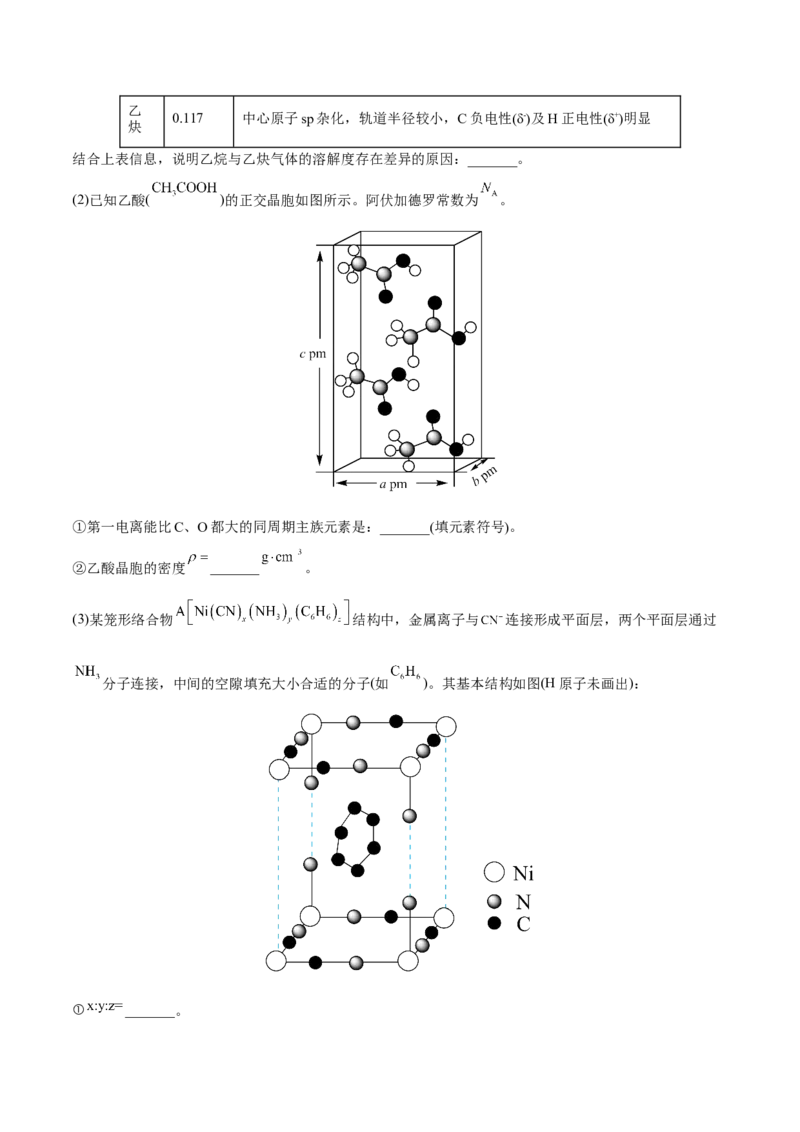
(2)已知乙酸( )的正交晶胞如图所示。阿伏加德罗常数为 。
①第一电离能比C、O都大的同周期主族元素是:_______(填元素符号)。
②乙酸晶胞的密度 _______ 。
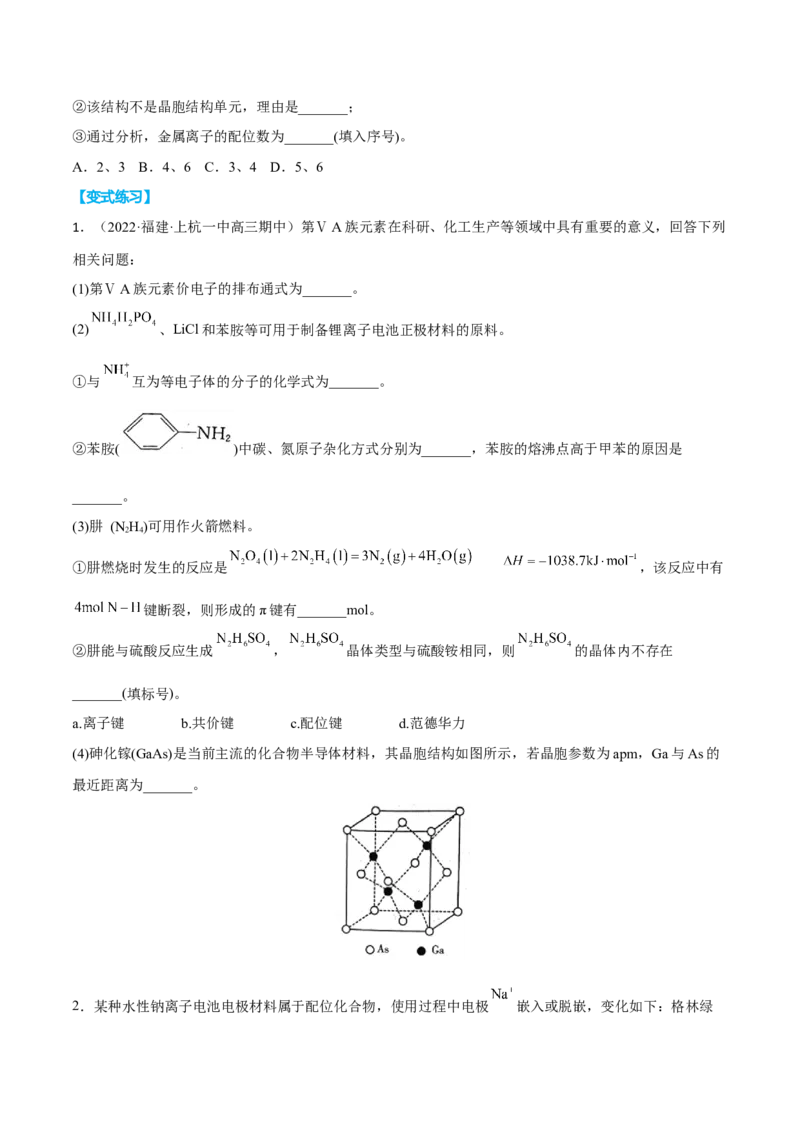
(3)某笼形络合物 结构中,金属离子与 连接形成平面层,两个平面层通过
分子连接,中间的空隙填充大小合适的分子(如 )。其基本结构如图(H原子未画出):
① _______。②该结构不是晶胞结构单元,理由是_______;
③通过分析,金属离子的配位数为_______(填入序号)。
A.2、3 B.4、6 C.3、4 D.5、6
【变式练习】
1.(2022·福建·上杭一中高三期中)第ⅤA族元素在科研、化工生产等领域中具有重要的意义,回答下列
相关问题:
(1)第ⅤA族元素价电子的排布通式为_______。
(2) 、LiCl和苯胺等可用于制备锂离子电池正极材料的原料。
①与 互为等电子体的分子的化学式为_______。
②苯胺( )中碳、氮原子杂化方式分别为_______,苯胺的熔沸点高于甲苯的原因是
_______。
(3)肼 (N H)可用作火箭燃料。
2 4
①肼燃烧时发生的反应是 ,该反应中有
键断裂,则形成的π键有_______mol。
②肼能与硫酸反应生成 , 晶体类型与硫酸铵相同,则 的晶体内不存在
_______(填标号)。
a.离子键 b.共价键 c.配位键 d.范德华力
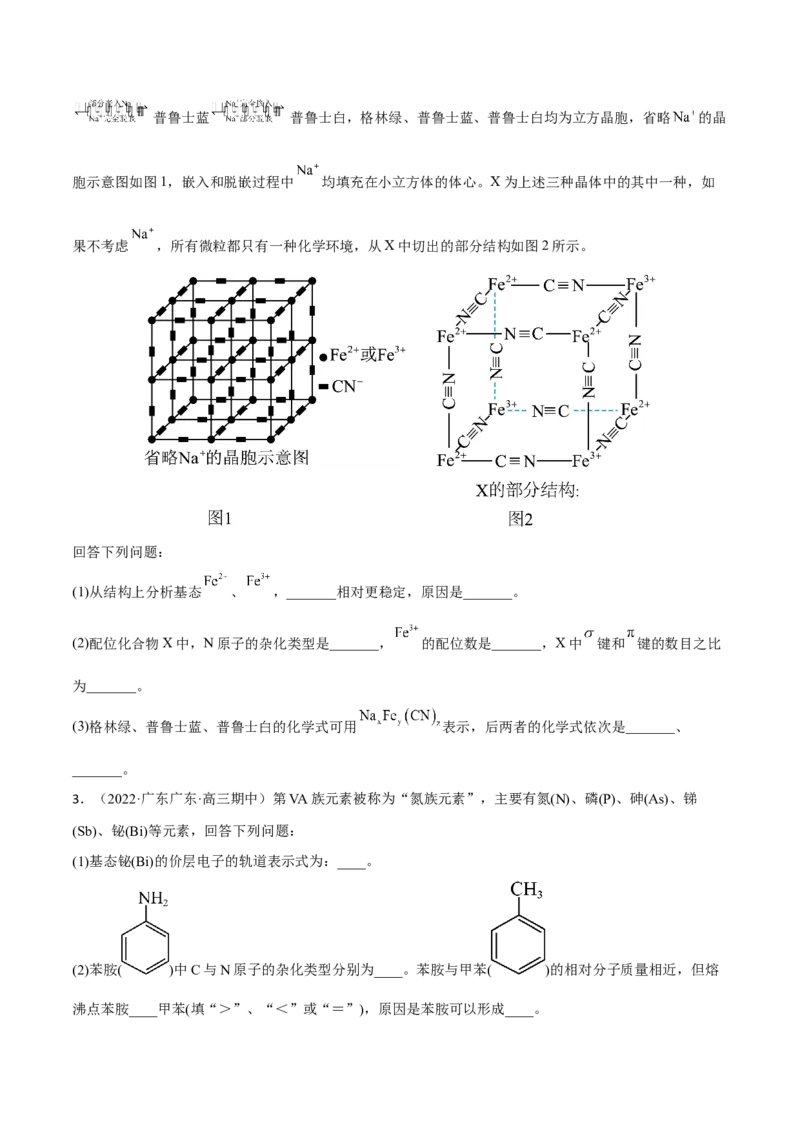
(4)砷化镓(GaAs)是当前主流的化合物半导体材料,其晶胞结构如图所示,若晶胞参数为apm,Ga与As的
最近距离为_______。
2.某种水性钠离子电池电极材料属于配位化合物,使用过程中电极 嵌入或脱嵌,变化如下:格林绿普鲁士蓝 普鲁士白,格林绿、普鲁士蓝、普鲁士白均为立方晶胞,省略 的晶
胞示意图如图1,嵌入和脱嵌过程中 均填充在小立方体的体心。X为上述三种晶体中的其中一种,如
果不考虑 ,所有微粒都只有一种化学环境,从X中切出的部分结构如图2所示。
回答下列问题:
(1)从结构上分析基态 、 ,_______相对更稳定,原因是_______。
(2)配位化合物X中,N原子的杂化类型是_______, 的配位数是_______,X中 键和 键的数目之比
为_______。
(3)格林绿、普鲁士蓝、普鲁士白的化学式可用 表示,后两者的化学式依次是_______、
_______。
3.(2022·广东广东·高三期中)第VA族元素被称为“氮族元素”,主要有氮(N)、磷(P)、砷(As)、锑
(Sb)、铋(Bi)等元素,回答下列问题:
(1)基态铋(Bi)的价层电子的轨道表示式为:____。
(2)苯胺( )中C与N原子的杂化类型分别为____。苯胺与甲苯( )的相对分子质量相近,但熔
沸点苯胺____甲苯(填“>”、“<”或“=”),原因是苯胺可以形成____。(3)磷元素可以形成多种含氧酸,已知次磷酸(H PO )为一元弱酸,其结构式为:____。
3 2
(4)砷(As)与硒(Se)同周期且相邻,比较它们的第一电离能大小____,并说明原因____。
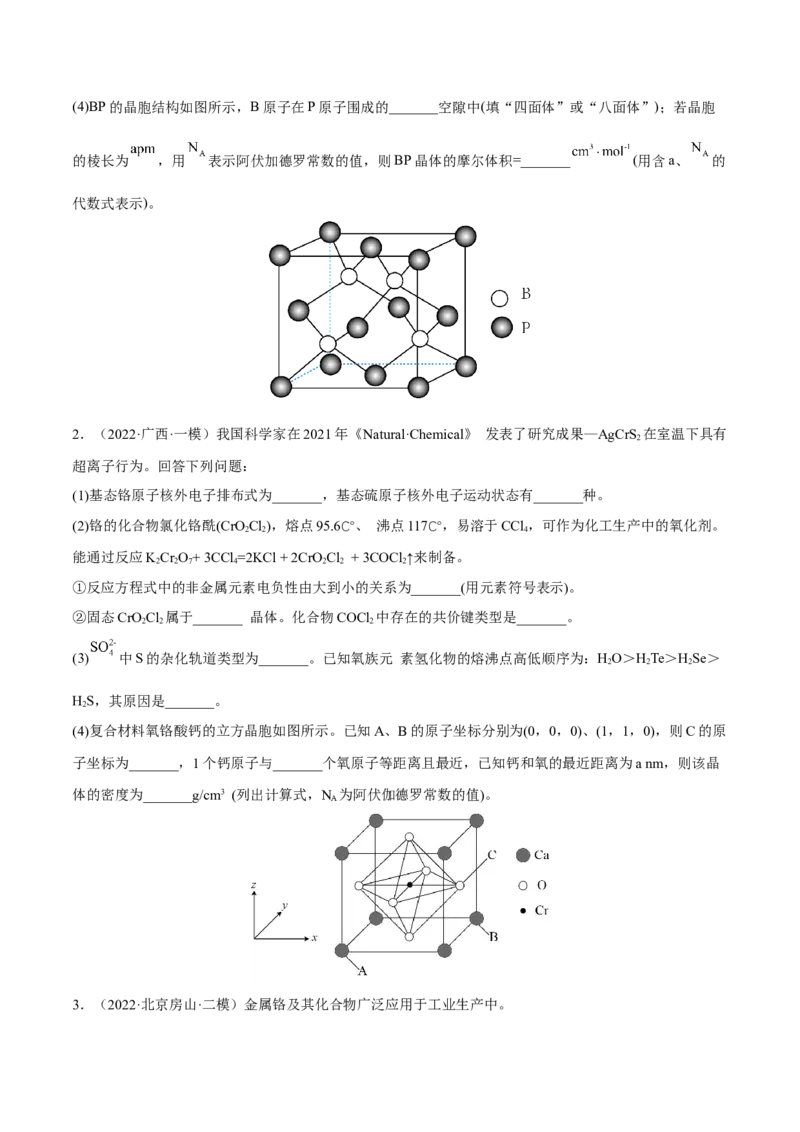
(5)锑酸亚铁晶胞如图所示,其晶胞参数分别为anm、bnm、cnm,α=β=γ=90°。
请写出锑酸亚铁的化学式:____,晶胞内Sb与O的最短距离为____nm(用晶胞参数表示)。
1.(2022·河南·焦作市第一中学模拟)BP晶体超硬、耐磨,是耐高温飞行器的红外增透的理想材料,其
合成途径之一为 。
请回答下列问题:
(1)基态溴原子的核外电子排布式为 _______;基态磷原子中自旋方向相反的电子数目相差_______个。
(2)① 的熔沸点比 的熔沸点高的原因为_______。
②在 分子中,有B的_______杂化轨道与Br的4p轨道形成的_______键(填“σ”或“π”),并且还有
B_______(填“杂化”或“未杂化”)的2p空轨道与Br的4p轨道形成4中心6电子的大π键 。
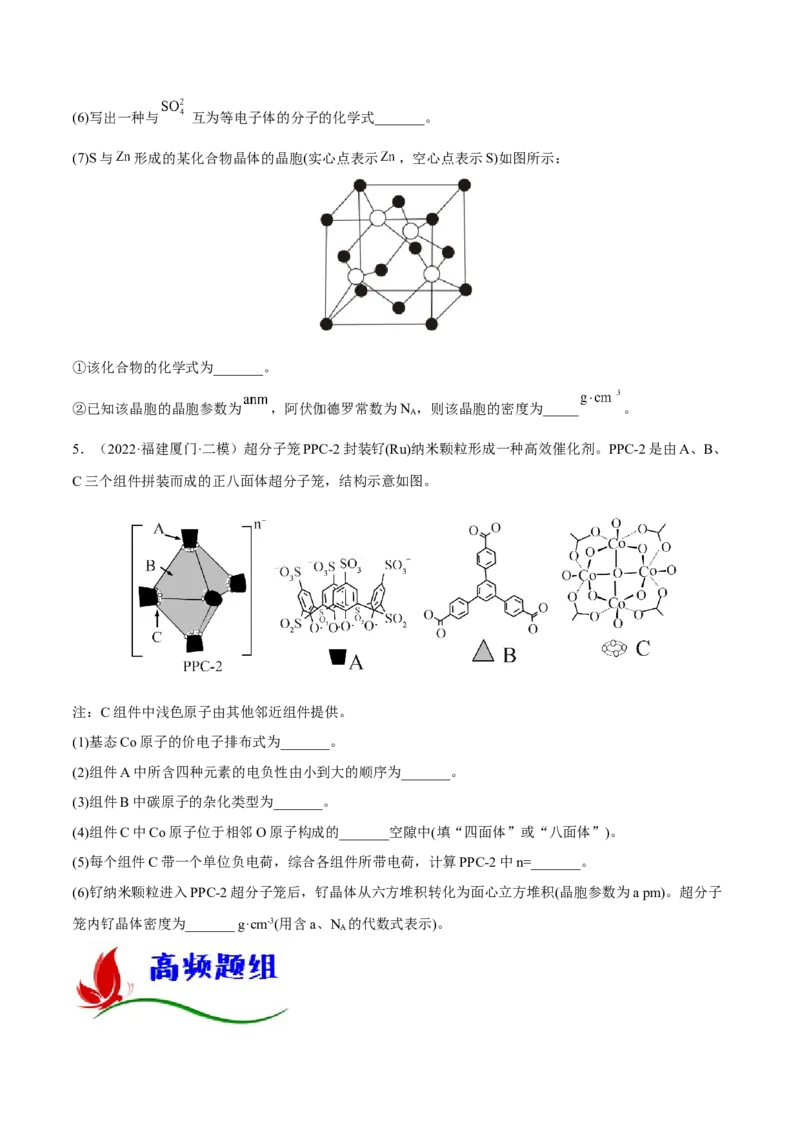
(3) 的空间构型为_______。(4)BP的晶胞结构如图所示,B原子在P原子围成的_______空隙中(填“四面体”或“八面体”);若晶胞
的棱长为 ,用 表示阿伏加德罗常数的值,则BP晶体的摩尔体积=_______ (用含a、 的
代数式表示)。
2.(2022·广西·一模)我国科学家在2021年《Natural·Chemical》 发表了研究成果—AgCrS 在室温下具有
2
超离子行为。回答下列问题:
(1)基态铬原子核外电子排布式为_______,基态硫原子核外电子运动状态有_______种。
(2)铬的化合物氯化铬酰(CrO Cl),熔点95.6℃、 沸点117℃,易溶于CCl ,可作为化工生产中的氧化剂。
2 2 4
能通过反应KCr O+ 3CCl =2KCl + 2CrO Cl + 3COCl ↑来制备。
2 2 7 4 2 2 2
①反应方程式中的非金属元素电负性由大到小的关系为_______(用元素符号表示)。
②固态CrOCl 属于_______ 晶体。化合物COCl 中存在的共价键类型是_______。
2 2 2
(3) 中S的杂化轨道类型为_______。已知氧族元 素氢化物的熔沸点高低顺序为:HO>HTe>HSe>
2 2 2
HS,其原因是_______。
2
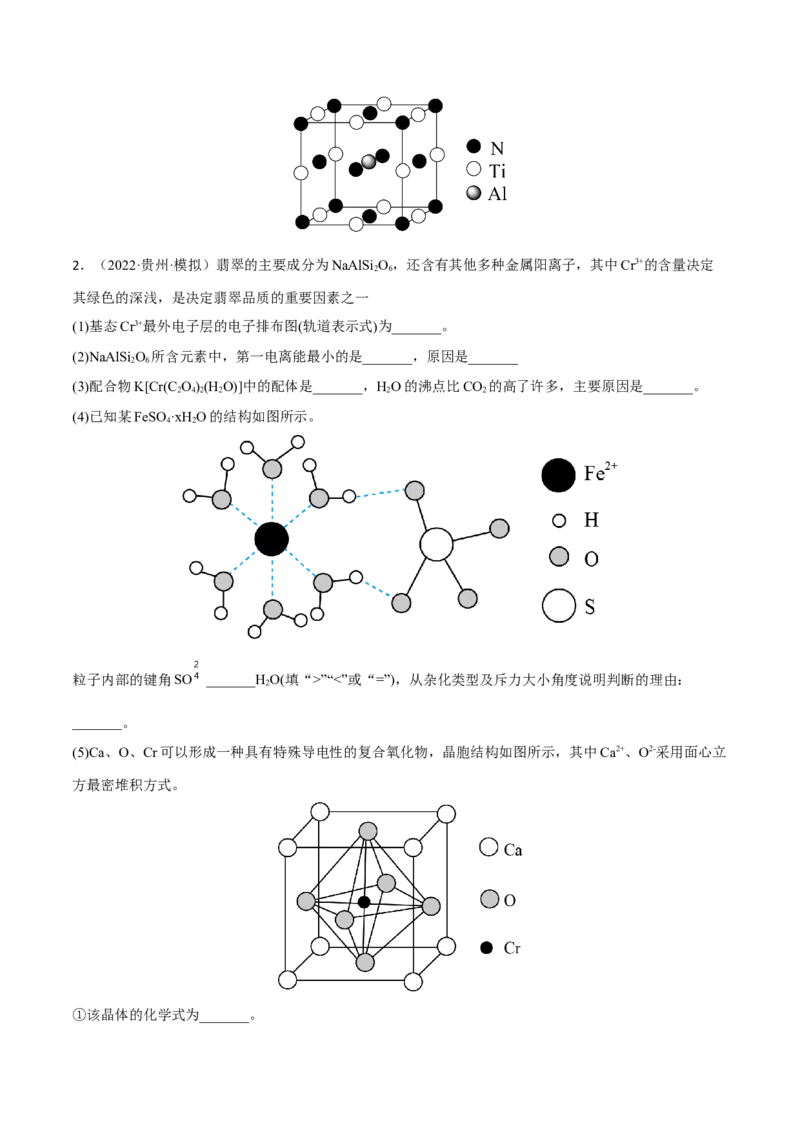
(4)复合材料氧铬酸钙的立方晶胞如图所示。已知A、B的原子坐标分别为(0,0,0)、(1,1,0),则C的原
子坐标为_______,1个钙原子与_______个氧原子等距离且最近,已知钙和氧的最近距离为a nm,则该晶
体的密度为_______g/cm3 (列出计算式,N 为阿伏伽德罗常数的值)。
A
3.(2022·北京房山·二模)金属铬及其化合物广泛应用于工业生产中。(1)烟酸铬是铬的一种化合物,可促进生物体内的蛋白质合成,提高生物体的免疫力,其合成过程如图:
①H、C、N、O的电负性由大到小的顺序是____。
②烟酸中碳原子的杂化方式为____。
(2)基态铬原子的核外电子排布式为____,有____个未成对电子。
(3)铬元素的一种配合物[Cr(H O) Cl]Cl•2H O,配离子中提供孤电子对的原子为____,配位数为____。
2 4 2 2
(4)Cr O 晶体的熔点为2435℃,而CrCl 晶体易升华,其主要原因是____。
2 3 3
(5)铬、钙和氧组成一种特殊的导电材料(复合氧化物),其晶胞如图所示。该晶体的化学式为____。
4.(2022·湖南怀化·一模)制备 的实验操作如下:向盛有硫酸铜水溶液的试管中加
入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂
(如乙醇),将析出深蓝色的晶体。回答以下问题:
(1)“沉淀溶解”时发生反应的离子方程式为_______
(2)基态 价层电子排布式为_______。
(3)N、O、S三种元素的第一电离能由大到小的顺序为_______。
(4)沸点: ,原因为_______。
(5) 含有σ键的数目为_______。(6)写出一种与 互为等电子体的分子的化学式_______。
(7)S与 形成的某化合物晶体的晶胞(实心点表示 ,空心点表示S)如图所示:
①该化合物的化学式为_______。
②已知该晶胞的晶胞参数为 ,阿伏伽德罗常数为N ,则该晶胞的密度为_____ 。
A
5.(2022·福建厦门·二模)超分子笼PPC-2封装钌(Ru)纳米颗粒形成一种高效催化剂。PPC-2是由A、B、
C三个组件拼装而成的正八面体超分子笼,结构示意如图。
注:C组件中浅色原子由其他邻近组件提供。
(1)基态Co原子的价电子排布式为_______。
(2)组件A中所含四种元素的电负性由小到大的顺序为_______。
(3)组件B中碳原子的杂化类型为_______。
(4)组件C中Co原子位于相邻O原子构成的_______空隙中(填“四面体”或“八面体”)。
(5)每个组件C带一个单位负电荷,综合各组件所带电荷,计算PPC-2中n=_______。
(6)钌纳米颗粒进入PPC-2超分子笼后,钌晶体从六方堆积转化为面心立方堆积(晶胞参数为a pm)。超分子
笼内钌晶体密度为_______ g·cm-3(用含a、N 的代数式表示)。
A1.(2022·广西南宁·模拟)软包电池(水系 )具有优异的稳定性,良好的容量保持率,
且成本较低,大规模储能的应用前景广泛。
回答下列问题:
(1)基态 原子核外电子排布式为_______;原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
表示,则与之相反的用 表示,称为电子的自旋磁量子数。对于基态 原子,其核外电子自旋磁量子
数的代数和为_______。
(2) 是锰的一种配合物。配体 与中心原子形成配位键时,提供孤对电子的原子
是_______(填元素符号),其能量最高的电子所在的能级符号为_______,配合物中心原子的配位数是
_______。
(3) 软包电池的关键组件 结构如图所示。
①其中S原子的杂化轨道类型为_______。
② 中存在的作用力为_______(填标号)。
A.金属键 B. 键 C. 键 D.氢键
③ 中第二周期非金属元素的第一电离能由大到小的顺序为_______,原因是_______。
(4) 掺杂的氮化钛晶胞结构如图所示。距离 最近的 有_______个,已知阿伏加德罗常数的值为 ,
若晶体的密度为 ,该晶胞的边长为_______cm(列出算式)。2.(2022·贵州·模拟)翡翠的主要成分为NaAlSi O,还含有其他多种金属阳离子,其中Cr3+的含量决定
2 6
其绿色的深浅,是决定翡翠品质的重要因素之一
(1)基态Cr3+最外电子层的电子排布图(轨道表示式)为_______。
(2)NaAlSi O 所含元素中,第一电离能最小的是_______,原因是_______
2 6
(3)配合物K[Cr(C O)(H O)]中的配体是_______,HO的沸点比CO 的高了许多,主要原因是_______。
2 4 2 2 2 2
(4)已知某FeSO ·xH O的结构如图所示。
4 2
粒子内部的键角SO _______HO(填“>”“<”或“=”),从杂化类型及斥力大小角度说明判断的理由:
2
_______。
(5)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中Ca2+、O2-采用面心立
方最密堆积方式。
①该晶体的化学式为_______。②已知钙离子、氧离子半径分别为100pm、140pm,晶胞中Cr4+位于O2-所形成的正八面体的体心,该正八
面体的边长为_______pm。
3.(2022·四川巴中·模拟)Fe、Ni元素性质非常相似,属于铁系元素,得到广泛应用,请回答下列问题:
(1)Fe元素属于元素周期表的_______ 区(填分区)
(2)基态Ni2+核外电子排布式为________________。
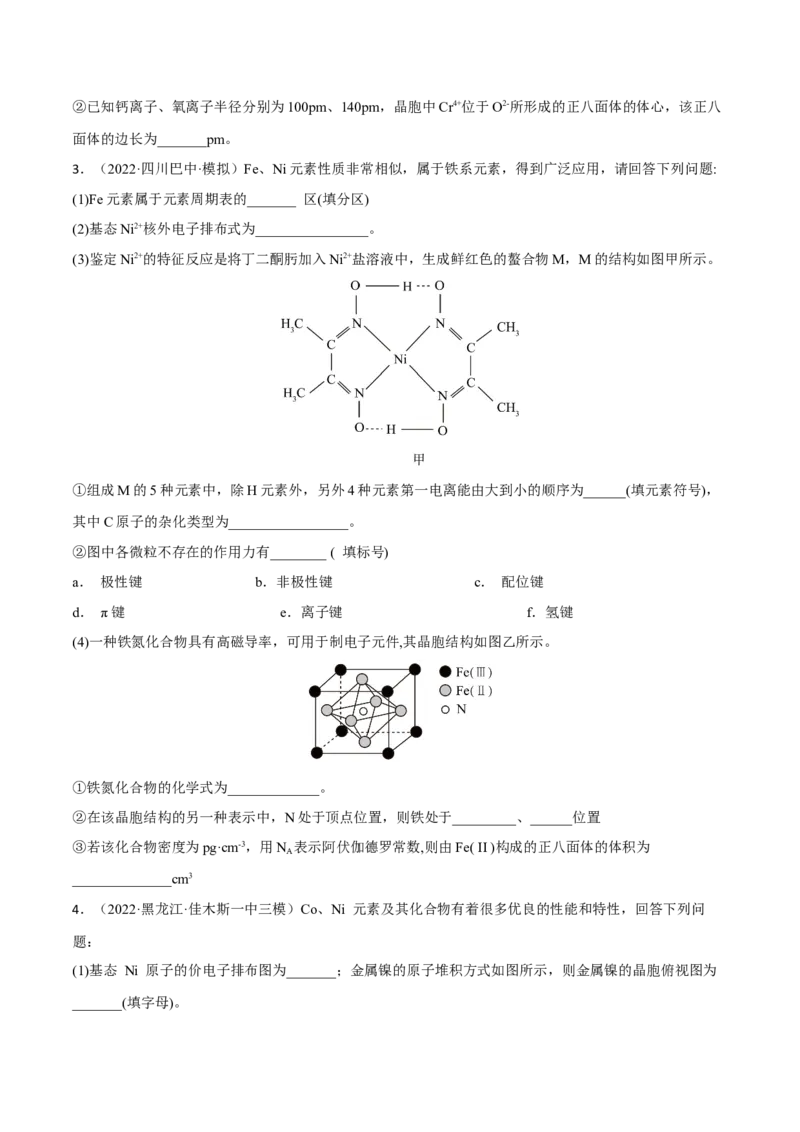
(3)鉴定Ni2+的特征反应是将丁二酮肟加入Ni2+盐溶液中,生成鲜红色的螯合物M,M的结构如图甲所示。
①组成M的5种元素中,除H元素外,另外4种元素第一电离能由大到小的顺序为______(填元素符号),
其中C原子的杂化类型为_________________。
②图中各微粒不存在的作用力有________ ( 填标号)
a. 极性键 b.非极性键 c. 配位键
d. π键 e.离子键 f.氢键
(4)一种铁氮化合物具有高磁导率,可用于制电子元件,其晶胞结构如图乙所示。
①铁氮化合物的化学式为_____________。
②在该晶胞结构的另一种表示中,N处于顶点位置,则铁处于_________、______位置
③若该化合物密度为pg·cm-3,用N 表示阿伏伽德罗常数,则由Fe( II )构成的正八面体的体积为
A
______________cm3
4.(2022·黑龙江·佳木斯一中三模)Co、Ni 元素及其化合物有着很多优良的性能和特性,回答下列问
题:
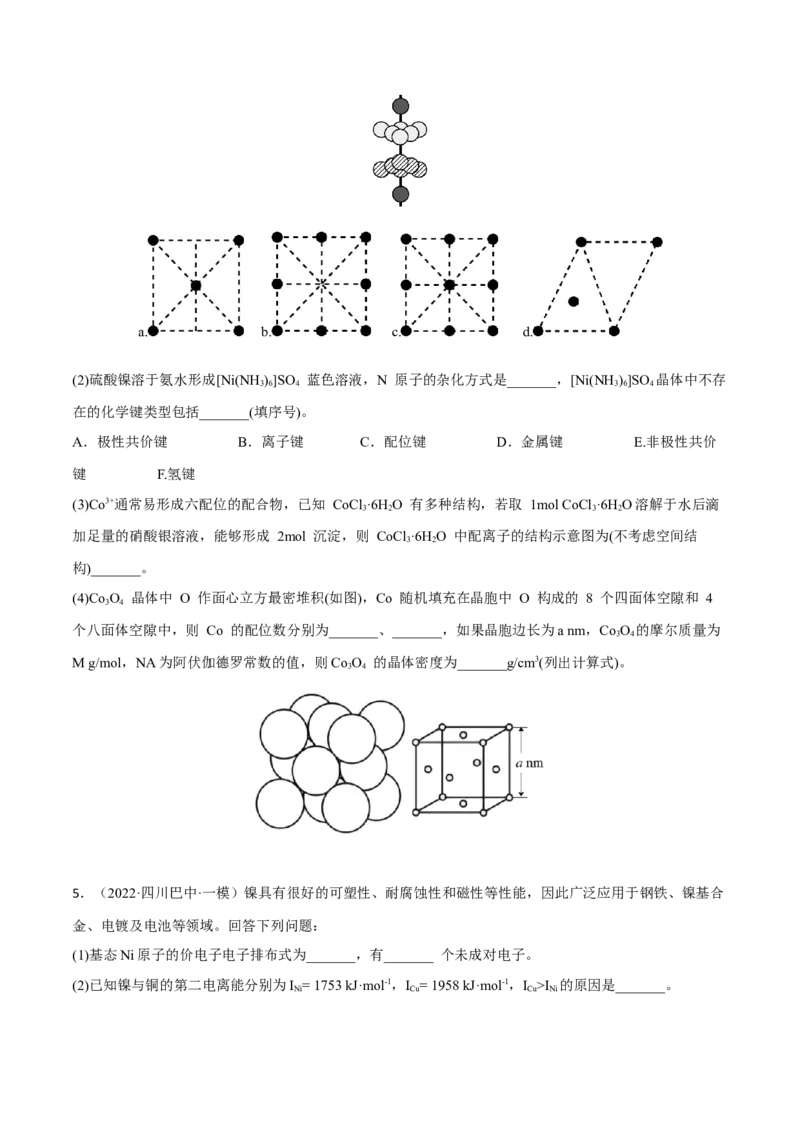
(1)基态 Ni 原子的价电子排布图为_______;金属镍的原子堆积方式如图所示,则金属镍的晶胞俯视图为
_______(填字母)。a. b. c. d.
(2)硫酸镍溶于氨水形成[Ni(NH )]SO 蓝色溶液,N 原子的杂化方式是_______,[Ni(NH )]SO 晶体中不存
3 6 4 3 6 4
在的化学键类型包括_______(填序号)。
A.极性共价键 B.离子键 C.配位键 D.金属键 E.非极性共价
键 F.氢键
(3)Co3+通常易形成六配位的配合物,已知 CoCl ·6H O 有多种结构,若取 1mol CoCl ·6H O溶解于水后滴
3 2 3 2
加足量的硝酸银溶液,能够形成 2mol 沉淀,则 CoCl ·6H O 中配离子的结构示意图为(不考虑空间结
3 2
构)_______。
(4)Co O 晶体中 O 作面心立方最密堆积(如图),Co 随机填充在晶胞中 O 构成的 8 个四面体空隙和 4
3 4
个八面体空隙中,则 Co 的配位数分别为_______、_______,如果晶胞边长为a nm,Co O 的摩尔质量为
3 4
M g/mol,NA为阿伏伽德罗常数的值,则Co O 的晶体密度为_______g/cm3(列出计算式)。
3 4
5.(2022·四川巴中·一模)镍具有很好的可塑性、耐腐蚀性和磁性等性能,因此广泛应用于钢铁、镍基合
金、电镀及电池等领域。回答下列问题:
(1)基态Ni原子的价电子电子排布式为_______,有_______ 个未成对电子。
(2)已知镍与铜的第二电离能分别为I = 1753 kJ·mol-1,I = 1958 kJ·mol-1,I >I 的原因是_______。
Ni Cu Cu Ni(3)Ni2+常与丁二酮肟( )形成图A所示的配合物,图B是硫代氧的结果:
①熔点大小: A_______ B (填“>”或“<”),其原因是_______。
②Ni2+与丁二酮肟之间形成的化学键称为_______。
③B中碳原子的杂化轨道类型是_______。
(4)硫酸镍[NiSO J]常用于有机化学合成中,阴离子的空间构型为_______。
4
(5)NiO,FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO
_______FeO(填“<”或“>”), NiO晶胞中Ni的配位数为_______。
(6)某砷镍合金的密度为ρg·cm-3,其晶胞结构如图所示。As和Ni的原子半径分别为r pm和r pm,阿伏
As Ni
加德罗常数的值为N ,则该晶胞中原子的体积占晶胞体积的百分率为_______。
A
6.(2022·广东惠州·二模)太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工
时,一般掺杂微量的铜、钴、硼、镓、硒等。已知铜的配合物A结构如图。请回答下列问题:(1)基态二价铜离子的核外电子排布式为______,已知高温下Cu O比CuO更稳定,试从核外电子排布角度
2
解释_______。
(2)配体氨基乙酸根(H NCH COO-)受热分解可产生CO 和N,N 中σ键和π键数目之比是_______。
2 2 2 2 2
(3)硫氰酸(H-S-C≡N)的沸点低于异硫氰酸(H-N=C=S)的原因是___________。
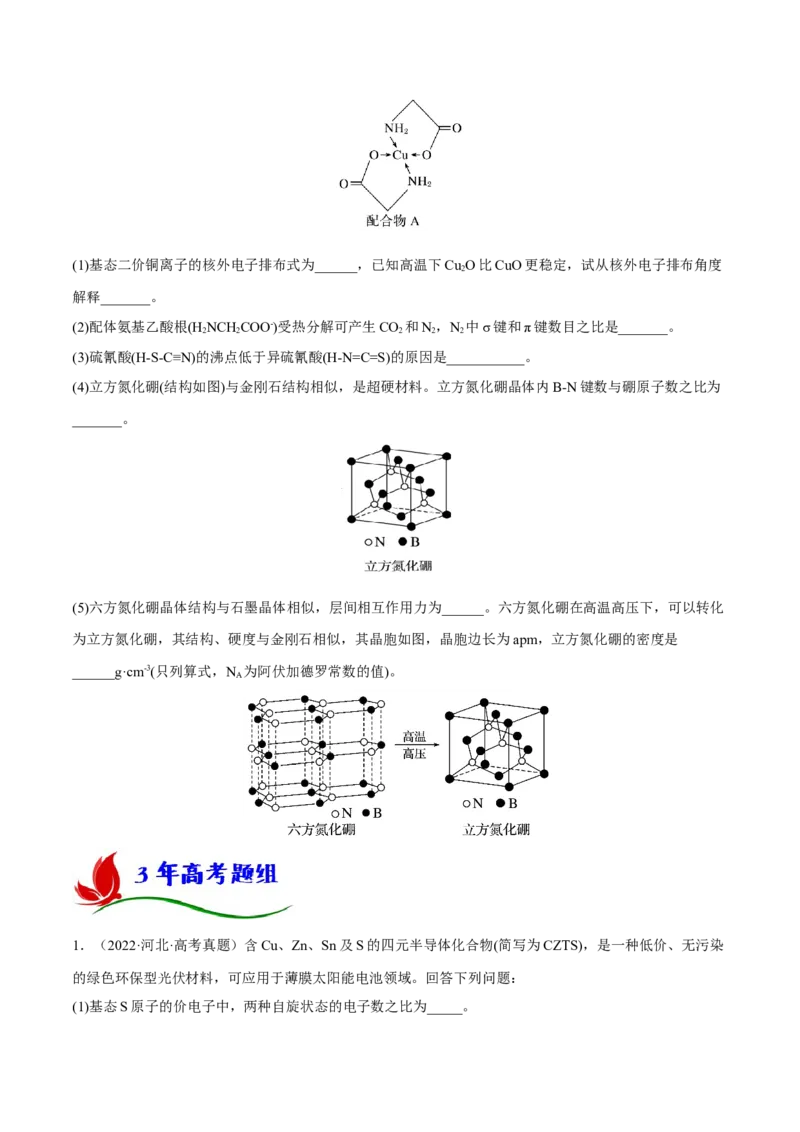
(4)立方氮化硼(结构如图)与金刚石结构相似,是超硬材料。立方氮化硼晶体内B-N键数与硼原子数之比为
_______。
(5)六方氮化硼晶体结构与石墨晶体相似,层间相互作用力为______。六方氮化硼在高温高压下,可以转化
为立方氮化硼,其结构、硬度与金刚石相似,其晶胞如图,晶胞边长为apm,立方氮化硼的密度是
______g·cm-3(只列算式,N 为阿伏加德罗常数的值)。
A
1.(2022·河北·高考真题)含Cu、Zn、Sn及S的四元半导体化合物(简写为CZTS),是一种低价、无污染
的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
(1)基态S原子的价电子中,两种自旋状态的电子数之比为_____。(2)Cu与Zn相比,第二电离能与第一电离能差值更大的是____,原因是_____。
(3)SnCl 的几何构型为____,其中心离子杂化方式为____。
(4)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。下列物质中,属于顺
磁性物质的是____(填标号)。
A.[Cu(NH )]Cl B.[Cu(NH )]SO C.[Zn(NH )]SO D.Na[Zn(OH) ]
3 2 3 4 4 3 4 4 2 4
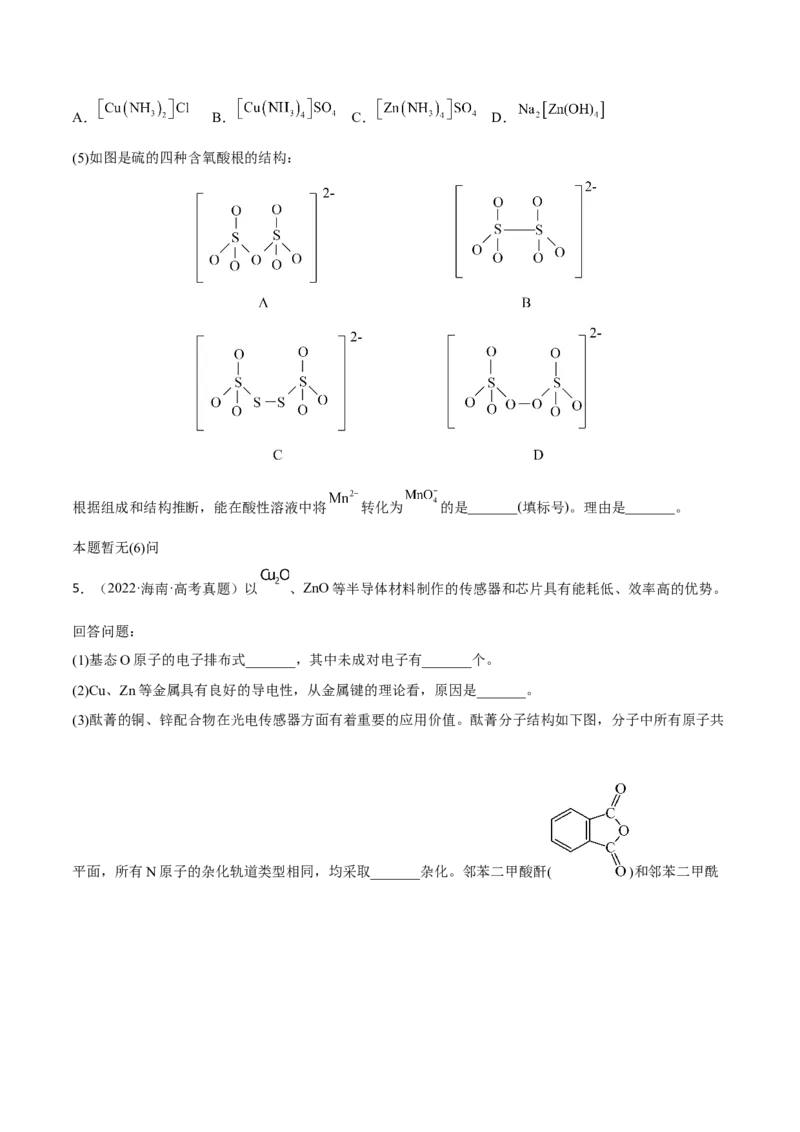
(5)如图是硫的四种含氧酸根的结构:
A. B. C. D.
根据组成和结构推断,能在酸性溶液中将Mn2+转化为MnO 的是____(填标号),理由是____。
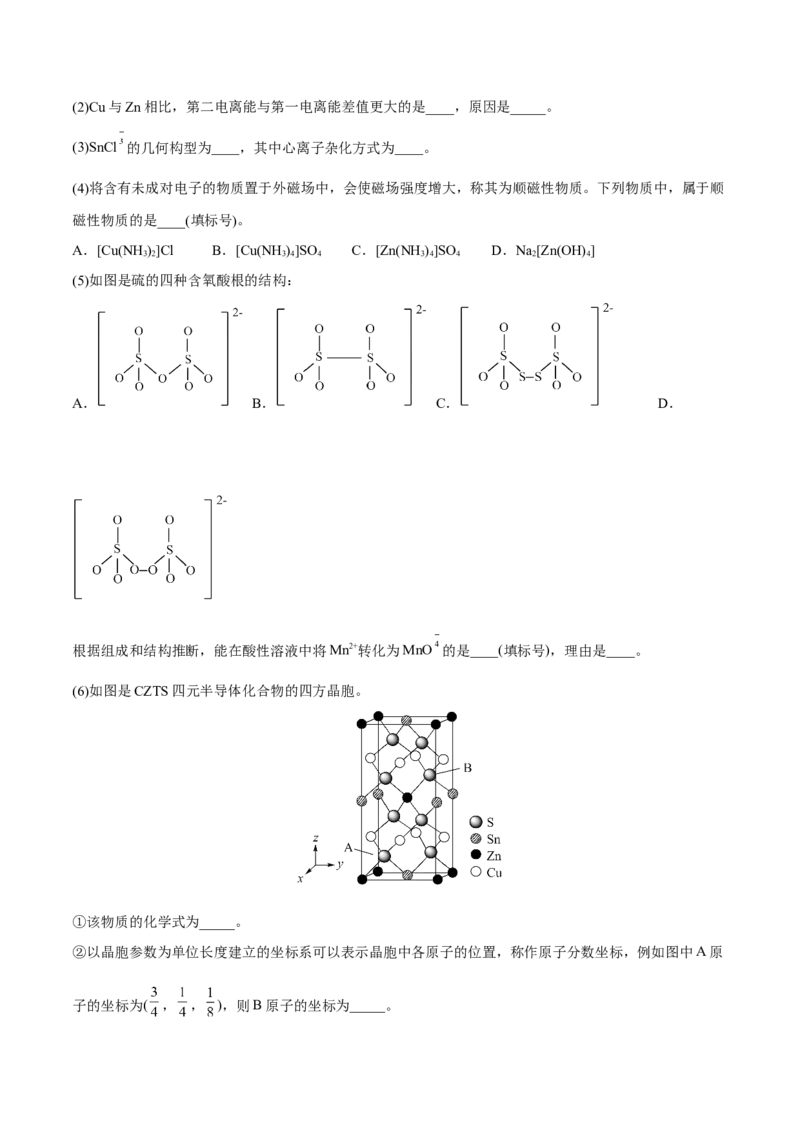
(6)如图是CZTS四元半导体化合物的四方晶胞。
①该物质的化学式为_____。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中A原
子的坐标为( , , ),则B原子的坐标为_____。2.(2022·北京·高考真题)工业中可利用生产钛白的副产物 和硫铁矿 联合制备铁精粉
和硫酸,实现能源及资源的有效利用。
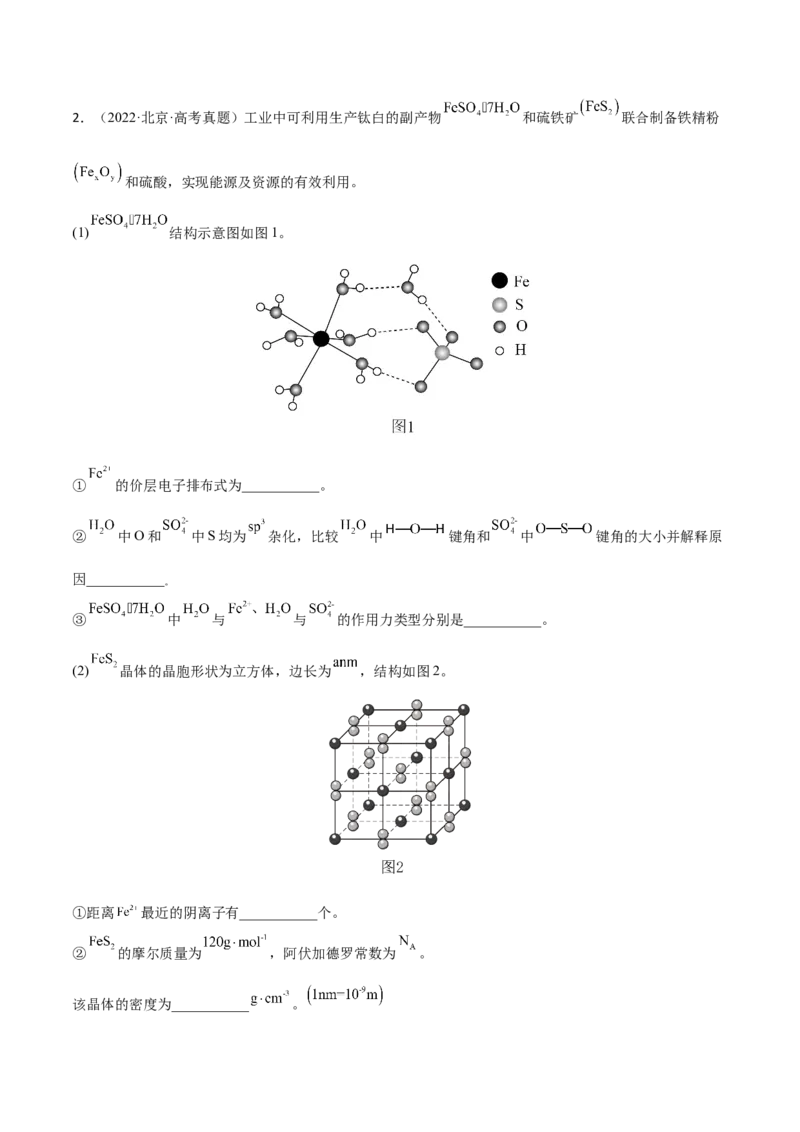
(1) 结构示意图如图1。
① 的价层电子排布式为___________。
② 中O和 中S均为 杂化,比较 中 键角和 中 键角的大小并解释原
因___________
。
③ 中 与 与 的作用力类型分别是___________。
(2) 晶体的晶胞形状为立方体,边长为 ,结构如图2。
①距离 最近的阴离子有___________个。
② 的摩尔质量为 ,阿伏加德罗常数为 。
该晶体的密度为___________ 。(3) 加热脱水后生成 ,再与 在氧气中掺烧可联合制备铁精粉和硫酸。
分解和 在氧气中燃烧的能量示意图如图3。利用 作为 分解的燃料,从能源
及资源利用的角度说明该工艺的优点___________。
3.(2022·江苏·高考真题)硫铁化合物( 、 等)应用广泛。
(1)纳米 可去除水中微量六价铬 。在 的水溶液中,纳米 颗粒表面带正电荷,
主要以 、 、 等形式存在,纳米 去除水中 主要经过“吸附→反应→沉淀”的过
程。
已知: , ; 电离常数分别为 、 。
①在弱碱性溶液中, 与 反应生成 、 和单质S,其离子方程式为_______。
②在弱酸性溶液中,反应 的平衡常数K的数值为_______。
③在 溶液中,pH越大, 去除水中 的速率越慢,原因是_______。
(2) 具有良好半导体性能。 的一种晶体与 晶体的结构相似,该 晶体的一个晶胞中 的数
目为_______,在 晶体中,每个S原子与三个 紧邻,且 间距相等,如图给出了 晶胞中的和位于晶胞体心的 ( 中的 键位于晶胞体对角线上,晶胞中的其他 已省略)。如图中用“-”将
其中一个S原子与紧邻的 连接起来_______。
(3) 、 在空气中易被氧化,将 在空气中氧化,测得氧化过程中剩余固体的质量与起始 的
质量的比值随温度变化的曲线如图所示。 时, 氧化成含有两种元素的固体产物为_______(填化
学式,写出计算过程)。
4.(2022·河北·高考真题)含 及S的四元半导体化合物(简写为 ),是一种低价、无污染
的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
(1)基态S原子的价电子中,两种自旋状态的电子数之比为_______。
(2)Cu与Zn相比,第二电离能与第一电离能差值更大的是_______,原因是_______。
(3) 的几何构型为_______,其中心离子杂化方式为_______。
(4)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列物质中,属于顺
磁性物质的是_______(填标号)。A. B. C. D.
(5)如图是硫的四种含氧酸根的结构:
根据组成和结构推断,能在酸性溶液中将 转化为 的是_______(填标号)。理由是_______。
本题暂无(6)问
5.(2022·海南·高考真题)以 、ZnO等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。
回答问题:
(1)基态O原子的电子排布式_______,其中未成对电子有_______个。
(2)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是_______。
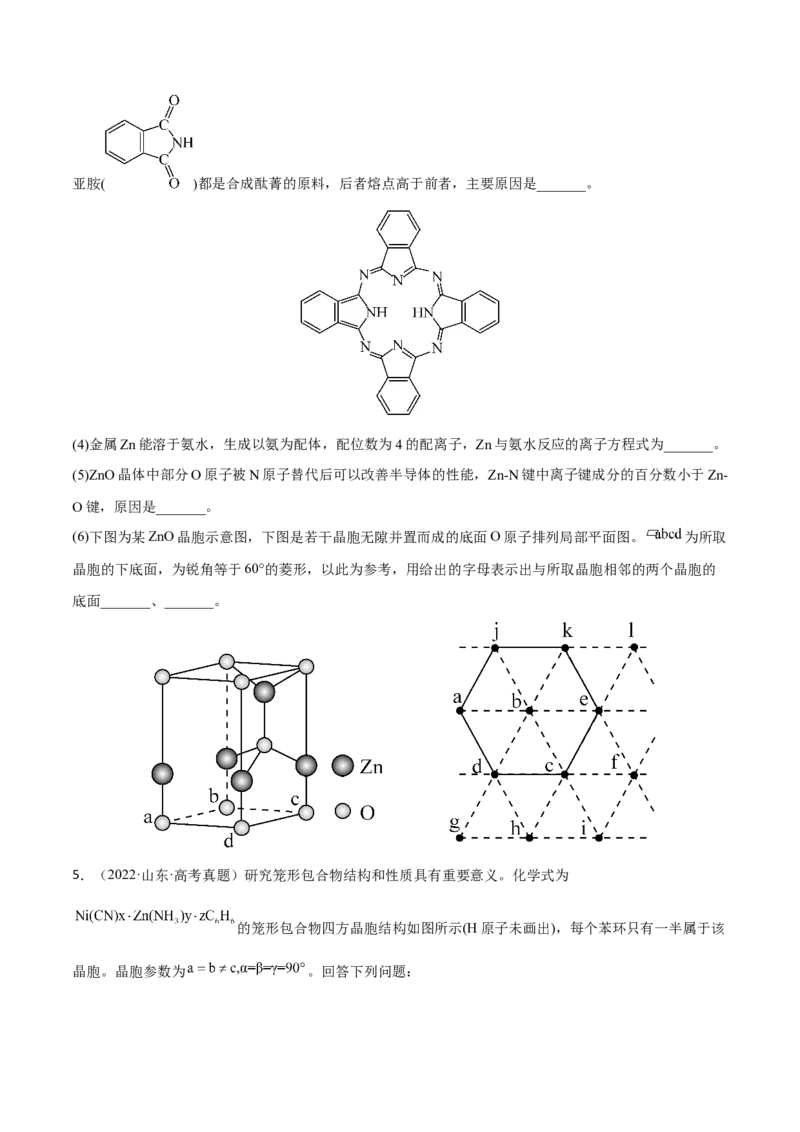
(3)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价值。酞菁分子结构如下图,分子中所有原子共
平面,所有N原子的杂化轨道类型相同,均采取_______杂化。邻苯二甲酸酐( )和邻苯二甲酰亚胺( )都是合成酞菁的原料,后者熔点高于前者,主要原因是_______。
(4)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为_______。
(5)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小于Zn-
O键,原因是_______。
(6)下图为某ZnO晶胞示意图,下图是若干晶胞无隙并置而成的底面O原子排列局部平面图。 为所取
晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母表示出与所取晶胞相邻的两个晶胞的
底面_______、_______。
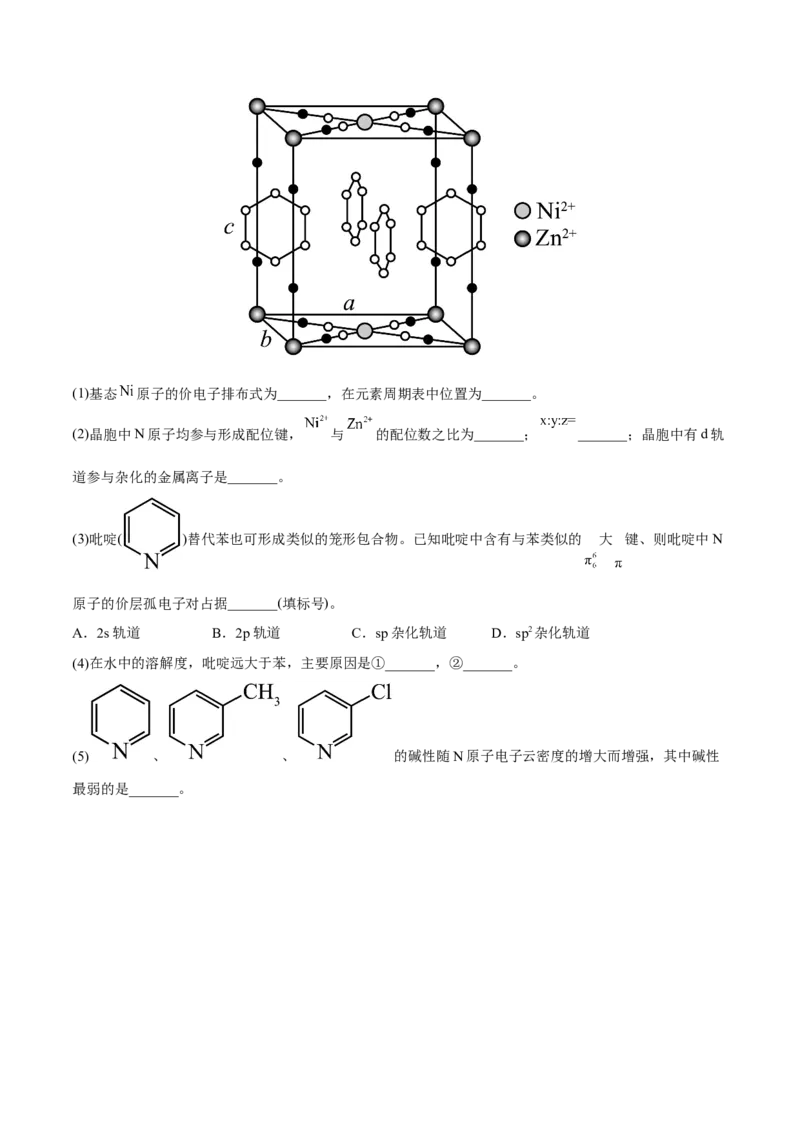
5.(2022·山东·高考真题)研究笼形包合物结构和性质具有重要意义。化学式为
的笼形包合物四方晶胞结构如图所示(H原子未画出),每个苯环只有一半属于该
晶胞。晶胞参数为 。回答下列问题:(1)基态 原子的价电子排布式为_______,在元素周期表中位置为_______。
(2)晶胞中N原子均参与形成配位键, 与 的配位数之比为_______; _______;晶胞中有d轨
道参与杂化的金属离子是_______。
(3)吡啶( )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的 大 键、则吡啶中N
原子的价层孤电子对占据_______(填标号)。
A.2s轨道 B.2p轨道 C.sp杂化轨道 D.sp2杂化轨道
(4)在水中的溶解度,吡啶远大于苯,主要原因是①_______,②_______。
(5) 、 、 的碱性随N原子电子云密度的增大而增强,其中碱性
最弱的是_______。