文档内容
专题突破卷 07 化学反应与能量(一)
——化学反应的热效应 原电池、化学电源
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.(2024·广东揭阳模拟)“蒸汽眼罩”通过发热产生温和蒸汽促进眼部血液微循环,放松眼部肌肉,消解眼
部疲劳。“蒸汽眼罩”由透氧无纺布、铁粉、碳粉、食盐、吸水树脂等组成。下列关于“蒸汽眼罩”的说
法正确的是( )
A.“蒸汽眼罩”工作时利用了原电池原理,发热时负极反应式为Fe-3e-===Fe3+
B.食盐作电解质,起到了导电的作用
C.透氧膜的透氧速率越快越好
D.“蒸汽眼罩”可以反复使用
2.我国力争二氧化碳排放2030年前达到峰值、2060年前实现碳中和。要加快调整优化产业结构、能源结
构,太阳能光催化分解水制氢、太阳能光催化二氧化碳转化为燃料等都是加快推动绿色低碳发展,降低碳
排放强度的有效措施。下列说法错误的是( )
A.太阳能燃料属于一次能源
B.直接电催化CO 制取燃料时,燃料是阴极产物
2
C.用光催化分解水产生的H 是理想的绿色能源
2
D.研发和利用太阳能燃料,有利于经济的可持续发展
3.某学习小组的同学查阅相关资料知氧化性:Cr O>Fe3+,设计了盐桥式的原电池(如图所示)。盐桥中装
2
有琼脂与饱和KSO 溶液。
2 4
下列叙述中正确的是( )
A.甲烧杯的溶液中发生还原反应
B.乙烧杯中发生的电极反应为
2Cr3++7HO-6e-===Cr O+14H+
2 2
C.外电路的电流方向是从b到a
D.电池工作时,盐桥中的SO移向乙烧杯
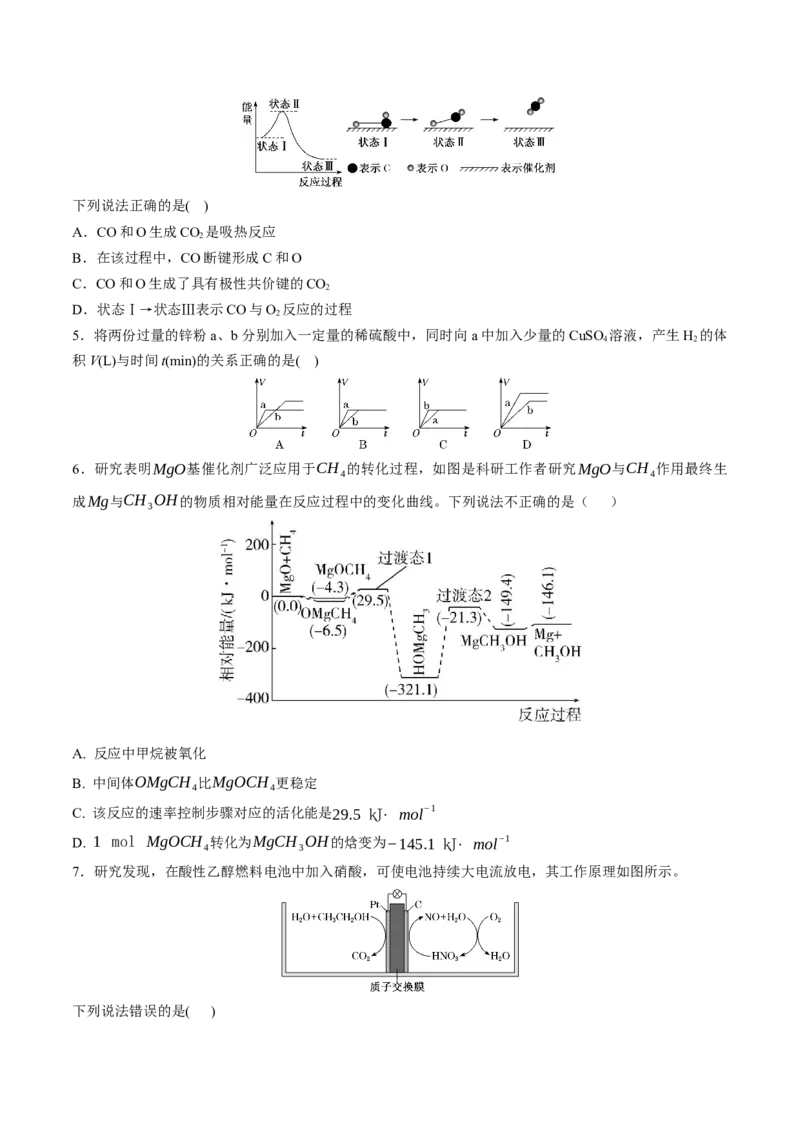
4. 据报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的
示意图如图。下列说法正确的是( )
A.CO和O生成CO 是吸热反应
2
B.在该过程中,CO断键形成C和O
C.CO和O生成了具有极性共价键的CO
2
D.状态Ⅰ→状态Ⅲ表示CO与O 反应的过程
2
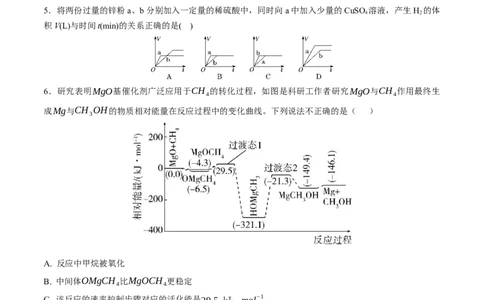
5.将两份过量的锌粉a、b分别加入一定量的稀硫酸中,同时向a中加入少量的CuSO 溶液,产生H 的体
4 2
积V(L)与时间t(min)的关系正确的是( )
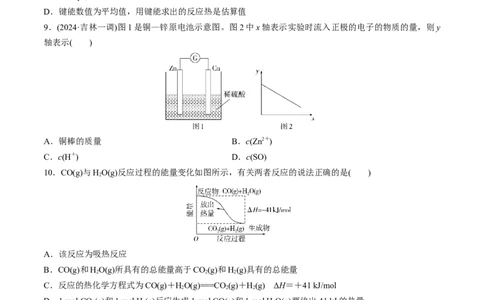
6.研究表明MgO基催化剂广泛应用于CH 的转化过程,如图是科研工作者研究MgO与CH 作用最终生
4 4
成Mg与CH OH的物质相对能量在反应过程中的变化曲线。下列说法不正确的是( )
3
A. 反应中甲烷被氧化
B. 中间体OMgCH 比MgOCH 更稳定
4 4
C. 该反应的速率控制步骤对应的活化能是29.5 kJ⋅ mol−1
D. 1 mol MgOCH 转化为MgCH OH的焓变为−145.1 kJ⋅ mol−1
4 3
7.研究发现,在酸性乙醇燃料电池中加入硝酸,可使电池持续大电流放电,其工作原理如图所示。
下列说法错误的是( )A.加入HNO 降低了正极反应的活化能
3
B.电池工作时正极区溶液的pH增大
C.1 mol CH CHOH被完全氧化时有6 mol O 被还原
3 2 2
D.负极反应为CHCHOH+3HO-12e-===2CO +12H+
3 2 2 2
8.(2024·河南安阳一中月考)下列有关反应热和热化学方程式的描述不正确的是( )
A.已知H+(aq)+OH-(aq)===H O(l) ΔH=-57.3 kJ·mol-1,则稀氨水和稀HSO 溶液完全反应生成1 mol
2 2 4
HO(l)时,放出热量少于57.3 kJ
2
B.热化学方程式各物质前的化学计量数既可以是整数也可以是分数,既表示分子数也表示物质的量
C.101 kpa,20 ℃和25 ℃时,CH 的燃烧热不同
4
D.键能数值为平均值,用键能求出的反应热是估算值
9.(2024·吉林一调)图1是铜—锌原电池示意图。图2中x轴表示实验时流入正极的电子的物质的量,则y
轴表示( )
A.铜棒的质量 B.c(Zn2+)
C.c(H+) D.c(SO)
10.CO(g)与HO(g)反应过程的能量变化如图所示,有关两者反应的说法正确的是( )
2
A.该反应为吸热反应
B.CO(g)和HO(g)所具有的总能量高于CO(g)和H(g)具有的总能量
2 2 2
C.反应的热化学方程式为CO(g)+HO(g)===CO (g)+H(g) ΔH=+41 kJ/mol
2 2 2
D.1 mol CO (g)和1 mol H (g)反应生成1 mol CO(g)和1 mol H O(g)要放出41 kJ的热量
2 2 2
11.一种太阳能电池的工作原理如图所示,电解质为铁氰化钾K[Fe(CN) ]和亚铁氰化钾K[Fe(CN) ]的混合
3 6 4 6
溶液,下列说法不正确的是( )
A.K+移向催化剂b
B.催化剂a电极表面发生的化学反应:[Fe(CN) ]4--e-===[Fe(CN)]3-
6 6C.[Fe(CN) ]3-在催化剂b表面被氧化
6
D.该太阳能电池溶液中的[Fe(CN) ]4-和[Fe(CN) ]3- 浓度基本保持不变
6 6
12.通过以下反应均可获取H。下列有关说法不正确的是( )
2
①太阳光催化分解水制氢:2HO(l)===2H (g)+O(g) ΔH=+571.6 kJ·mol-1
2 2 2 1
②焦炭与水反应制氢:C(s)+HO(g)===CO(g)+H(g) ΔH=+131.3 kJ·mol-1
2 2 2
③甲烷与水反应制氢:CH(g)+HO(g)===CO(g)+3H(g) ΔH=+206.1 kJ·mol-1
4 2 2 3
A.H 的燃烧热为285.8 kJ·mol-1
2
B.反应②中E(反应物键能总和)>E(生成物键能总和)
C.反应C(s)+2H(g)===CH (g)的ΔH=+74.8 kJ·mol-1
2 4
D.2HO(g)===2H (g)+O(g)
2 2 2
ΔH<+571.6 kJ·mol-1
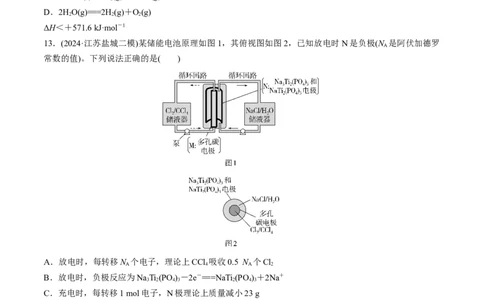
13.(2024·江苏盐城二模)某储能电池原理如图1,其俯视图如图2,已知放电时N是负极(N 是阿伏加德罗
A
常数的值)。下列说法正确的是( )
A.放电时,每转移N 个电子,理论上CCl 吸收0.5 N 个Cl
A 4 A 2
B.放电时,负极反应为NaTi (PO )-2e-===NaTi(PO )+2Na+
3 2 4 3 2 4 3
C.充电时,每转移1 mol电子,N极理论上质量减小23 g
D.充电过程中,右侧储液器中NaCl溶液浓度增大
14.利用微生物可将废水中苯酚的化学能直接转化为电能,装置如图所示。电池工作时,下列说法正确的
是( )A.a极为正极,发生氧化反应
B.b极的电极反应式为2NO+12H+-10e-===N ↑+6HO
2 2
C.中间室的Cl-向左室移动
D.左室消耗苯酚(C HOH)9.4 g时,用电器流过2.4 mol 电子
6 5
15.(2024·江苏盐城质检)甲烷与氯气在光照条件下发生取代反应的部分机理与能量变化如下:
链引发:Cl(g)―→2Cl·(g) ΔH=242.7 kJ/mol
2 1
链增长:部分反应进程与势能变化关系如图(所有物质状态均为气态)
链终止:Cl·(g)+CH·(g)―→CHCl(g) ΔH=-371 kJ/mol
3 3 2
下列说法不正确的是( )
A.Cl 的键能为242.7 kJ/mol
2
B.链增长中反应速率较大的一步的热化学方程式为CH(g)+Cl·(g)―→·CH(g)+HCl(g) ΔH=7.5 kJ/mol
4 3
C.链增长过程中可能产生·CHCl、·CHCl 、·CCl
2 2 3
D.链终止反应的过程中,还可能会生成少量的乙烷
二、非选择题(本题包括4小题,共55分)
16.(10分)某实验小组用0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液进行反应热的测定,实验装
置如图所示。
(1)装置中碎泡沫塑料的作用是______。
(2) 写 出 该 反 应 的 热 化 学 方 程 式 [ 生 成 1 mol H O(l) 时 的 反 应 热 为 - 57.3 kJ·mol - 1] :
2
______________________________________________。
(3)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如表所示。
①请填写表格中的空白:②近似认为0.50 mol·L-1 NaOH溶液和0.50 mol·L-1 硫酸溶液的密度都是1.0 g·mL-1,中和后生成溶液的
比热容c=4.18 J·(g·℃)-1。则生成1 mol H O(l)时的反应热ΔH=_____(取小数点后一位)。
2
③上述实验数值结果与-57.3 kJ·mol-1有偏差,产生偏差的原因不可能是____(填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定HSO 溶液的温度
2 4
17.(16分)低碳经济已成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重要研究
方向。请回答下列问题:
(1)用CO
2
催化加氢可以制取乙烯:CO
2
(g)+3H
2
(g)⇌C
2
H
4
(g)+2H
2
O(g),该反应体系的能量随反应过程的变
化关系如图所示,该反应的ΔH=__________(用含a、b的式子表示)。相关化学键的键能如下表,实验测
得上述反应的ΔH=-152 kJ·mol-1,则表中的x=__________。
化学键 C===O H—H C===C C—H H—O
键能/ (kJ·mol-1) x 436 764 414 464
(2)工业上用CO 和H 反应合成二甲醚。
2 2
已知:CO
2
(g)+3H
2
(g)⇌CH
3
OH(g)+H
2
O(g) ΔH
1
=-53.7 kJ·mol-1
CHOCH (g)+HO(g)===2CH OH(g) ΔH=23.4 kJ·mol-1
3 3 2 3 2
则2CO
2
(g)+6H
2
(g)⇌CH
3
OCH
3
(g)+3H
2
O(g) ΔH
3
=__________kJ·mol-1。
(3)用N 表示阿伏加德罗常数的值,在C H(g)完全燃烧生成CO 和液态水的反应中,每有5N 个电子转移
A 2 2 2 A时,放出650 kJ的热量。C H 的热值为__________kJ·g-1。
2 2
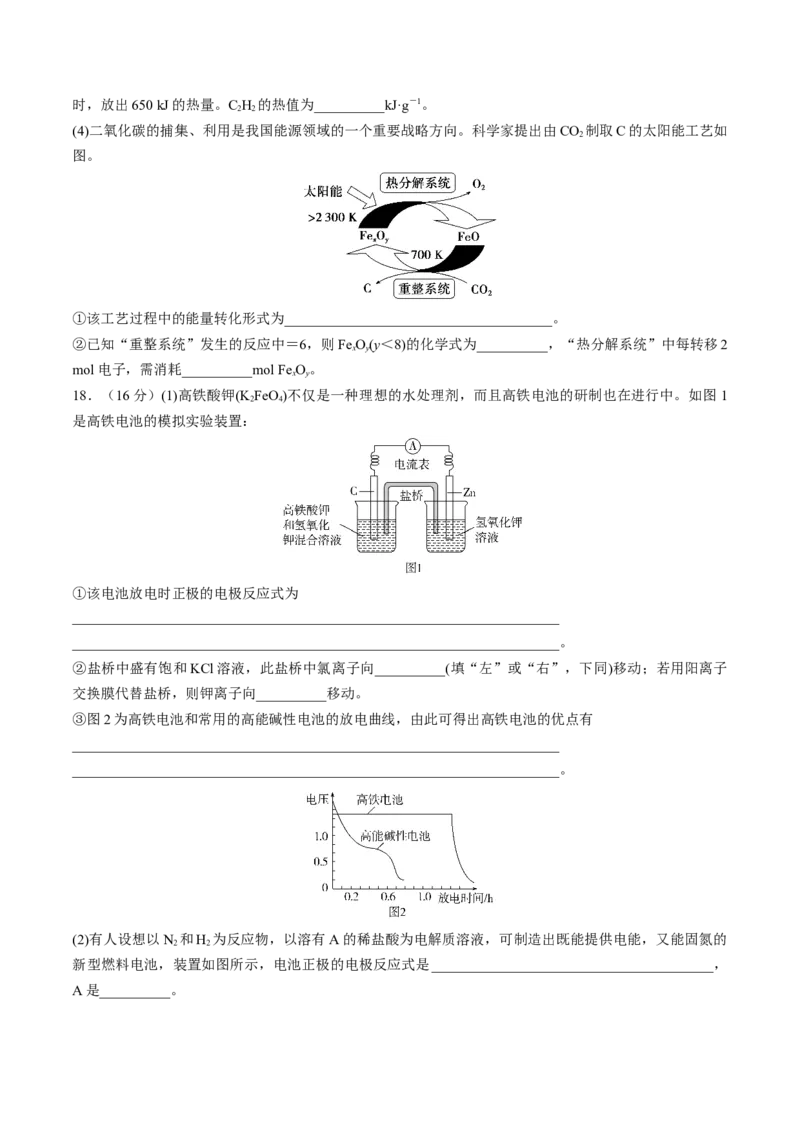
(4)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由CO 制取C的太阳能工艺如
2
图。
①该工艺过程中的能量转化形式为______________________________________。
②已知“重整系统”发生的反应中=6,则FeO(y<8)的化学式为__________,“热分解系统”中每转移2
x y
mol电子,需消耗__________mol FeO。
x y
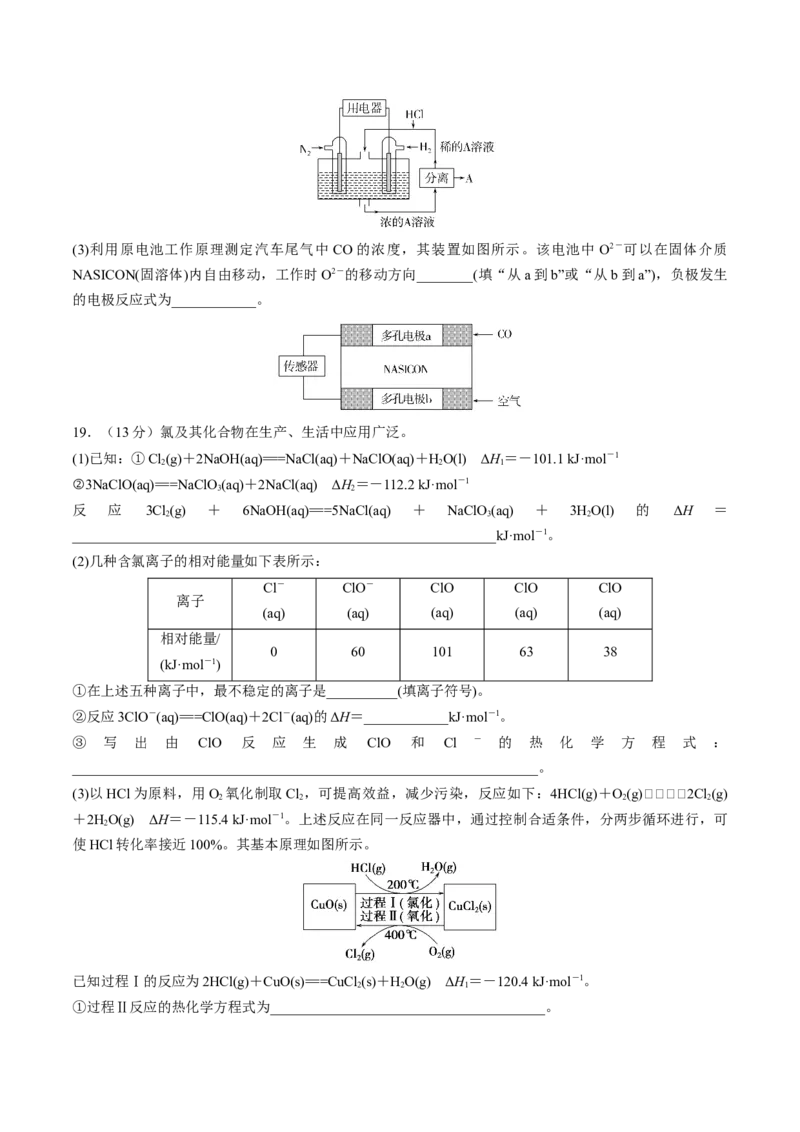
18.(16分)(1)高铁酸钾(K FeO)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图 1
2 4
是高铁电池的模拟实验装置:
①该电池放电时正极的电极反应式为
_____________________________________________________________________
_____________________________________________________________________。
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向__________(填“左”或“右”,下同)移动;若用阳离子
交换膜代替盐桥,则钾离子向__________移动。
③图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有
_____________________________________________________________________
_____________________________________________________________________。
(2)有人设想以N 和H 为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的
2 2
新型燃料电池,装置如图所示,电池正极的电极反应式是________________________________________,
A是__________。(3)利用原电池工作原理测定汽车尾气中 CO的浓度,其装置如图所示。该电池中 O2-可以在固体介质
NASICON(固溶体)内自由移动,工作时O2-的移动方向________(填“从a到b”或“从b到a”),负极发生
的电极反应式为____________。
19.(13分)氯及其化合物在生产、生活中应用广泛。
(1)已知:①Cl(g)+2NaOH(aq)===NaCl(aq)+NaClO(aq)+HO(l) ΔH=-101.1 kJ·mol-1
2 2 1
②3NaClO(aq)===NaClO (aq)+2NaCl(aq) ΔH=-112.2 kJ·mol-1
3 2
反 应 3Cl(g) + 6NaOH(aq)===5NaCl(aq) + NaClO(aq) + 3HO(l) 的 ΔH =
2 3 2
____________________________________________________________kJ·mol-1。
(2)几种含氯离子的相对能量如下表所示:
Cl- ClO- ClO ClO ClO
离子
(aq) (aq) (aq) (aq) (aq)
相对能量/
0 60 101 63 38
(kJ·mol-1)
①在上述五种离子中,最不稳定的离子是__________(填离子符号)。
②反应3ClO-(aq)===ClO(aq)+2Cl-(aq)的ΔH=____________kJ·mol-1。
③ 写 出 由 ClO 反 应 生 成 ClO 和 Cl - 的 热 化 学 方 程 式 :
__________________________________________________________________。
(3)以HCl为原料,用O 氧化制取Cl ,可提高效益,减少污染,反应如下:4HCl(g)+O(g)2Cl(g)
2 2 2 2
+2HO(g) ΔH=-115.4 kJ·mol-1。上述反应在同一反应器中,通过控制合适条件,分两步循环进行,可
2
使HCl转化率接近100%。其基本原理如图所示。
已知过程Ⅰ的反应为2HCl(g)+CuO(s)===CuCl (s)+HO(g) ΔH=-120.4 kJ·mol-1。
2 2 1
①过程Ⅱ反应的热化学方程式为_______________________________________。②过程Ⅰ流出的气体通过稀NaOH溶液(含少量酚酞)进行检测,氯化初期主要为不含HCl的气体,判断氯
化结束时溶液的现象为____________________________________。