文档内容
长沙市市 2023 年新高考考适应性性考试
化化学答案案
一、选择择题:本题共共10小题,每每小题3分,,共30分。在每小题给给出的四个选项中,只有一一项是符
合题题目要求的。
1【答案】B
【解析】
B.生产陶瓷的主要原料是黏黏土,不需要要使用石灰石石,B不正确确;
2【答案】A
【解析】
A.原子符号表表示中,左下角为质子数,,左上角为质质量数,质量量数等于质子子数与中子数数的和,
则原子核内内中子数为200的氯原子质质量数为17++20=37,可表表示为:37Cl,A错误;
17
B.H O分子中中心O原子子价层电子对数是2+ 6-12 =4,O原原子上有2对对孤电子对,故故其分子
2
2
的VSEPR模模型为 ,B正确;
C.CO 分子中C原子与2个O原子形形成4对共用电子对,使分分子中各个原原子都达到最最外层8
2
个电子的稳稳定结构,其其电子式为: ,C正确;;
D.PP-Pπ键的原子子轨道以肩并并肩方式重叠叠形成π键呈呈镜面对称,故故其电子云轮轮廓图为 ,
D正确;
3【答案】B
【解析】
A.氨气的密度度小于空气,收集氨气应用用向下排空气气法,导管要要伸到试管底底部,故A错错误;
B.二氧化硫的密密度大于空气气,可用向上上排空气法收收集,盛有氢氢氧化钠溶液的烧杯可吸收收多余的
二氧化硫,防止污染空空气,烧杯中倒倒置的漏斗可可防倒吸,BB正确;
C.饱和氯化铁铁溶液滴入NaaOH溶液得到的是氢氧化化铁沉淀,CC错误;
D.气体应长进进短出,短进长出的话,气气体会将NaaOH溶液压出出洗气瓶,DD错误。
4【答案】A
【解析】
试题题分析:A.FFe2+能被硝酸酸氧化成Fe3+,,A项正确;B.根据以少少定多的,离离子方程式为为
Ca2++HCCO -+OH-=CaaCO ↓+H O,B项错误;C.AlO -和HHCO -不能共共存,C项错错误;D.离子子方程式
3 3 2 2 3
为:3All3++3SO 2-+3BBa2++6OH-=3BaSO ↓+2AAl(OH) ↓,D项错误误;
4 4 3
5【答案】B
【解析】
根据据题意,结合合物质的结构构可知,X、YY、Z、N、MM分别为H、、C、N、Naa、S元素,因因此电负
性C>H>>Na,A正确确;该物质为为离子化合物,且有氮原子子可以与水形形成氢键,因因此可易溶于于水,B
错误;该该化合物中NN、S原子含有有孤对电子,可以与含有有空轨道的Cu2+、Ag+等形形成配位键,CC正确;
硫酸的浓浓溶液与硫化化氢能发生反反应,D正确确。
化学答答案第1页,共5页6【答案】B
【解析】
亚硝酸根离子与酸发生歧化反应生成二氧化氮、一氧化氮和水,亚硝酸钠既作氧化剂又作还原剂,
B错误。
7【答案】D
【详解】
A.X含碳碳双键和醇羟基,都能使酸性KMnO 溶液褪色,Y含酚羟基,也能使酸性KMnO
4 4
溶液褪色,不能鉴别,故A正确;
B.Y含多个羟基,可与水形成氢键,故B正确;
C.由于单键可旋转,则所有碳原子不一定在同一平面上,故C正确;
D.Z中酚羟基、酯基水解生成的羧基和酚羟基、羧基能和NaOH反应,Z分子中含有5个酚羟
基、1个羧基、1个能水解生成羧基和酚羟基的酯基,所以1molZ最多能消耗8molNaOH,
故D错误;
8【答案】D
【解析】
A.碳酸锌的组成元素中,C与O属于p区元素,Zn属于ds区元素,不属于同区元素,A错;
B.晶体碳化硅为共价晶体,原子之间的作用力为共价键,氧化锌为离子晶体,离子之间的作用
力为离子键,B错误;
C.由两种氧化锌晶体的晶胞结构可以看出,锌原子位于4个氧原子形成的四面体内部,氧原子
位于4个锌原子形成的四面体内部,即锌原子和氧原子的配位数均为4,C错误;
D.图示氧化锌晶体为两种晶体类型不同的离子晶体,锌原子和氧原子都填充在四面体空隙中,
所以两种晶体的空间利用率相同,均为74.05%,故晶胞密度也相同,D正确;
9.【答案】B
【解析】
由图可知,电极a为电解池的阴极,水在阴极得到电子发生还原反应生成氢气和氢氧根离子,
氢氧根离子与进液中亚硫酸氢钠溶液反应生成亚硫酸钠,中间区的进液中的钠离子通过阳离子交换
膜加进入阴极区,电极b为阳极,水在阳极失去电子发生氧化反应生成氧气和氢离子,氢离子通过
阳离子交换膜进入中间区,与再生液中的亚硫酸根离子和亚硫酸氢根离子反应生成亚硫酸。
10【答案】D
【解析】
A.PbSO 与 Na CO 溶液反应生成更难溶的PbCO ,转化后生成的碳酸铅可由酸浸进入溶液中,
4 2 3 3
转化反应的离子方程式:PbSO sCO2aqPbCO sSO2-aq,A错误;
4 3 3 4
B.第一步“溶浸”中PbO 中Pb元素的化合价降低,PbO 做氧化剂,H O 做还原剂,B错误;
2 2 2 2
C. 对于BF 2-离子,其中心原子的杂化方式为sp3
4
D.电解四氟合硼酸铅溶液时,石墨是电解池的阳极,铅是阴极,铅离子在阴极得到电子发生
还原反应生成铅,故D正确;
化学答案第2页,共5页二、选择择题:本题共4小题,每小小题4分,共共16分。在每每小题给出的四四个选项中,有一个或两个个选项符
合题题目要求。全部部选对的得44分,选对但但不全的得2分分,有选错的的得0分。
11.【答案】BD
【解析】
A.该该过程中,88→10为消去去反应,故AA错误;
B. 根据图示,9是主产物、、10、11是副副产物,3、5和8都是反反应的中间体体,故B正确确;
C.根根据题意,发发生反应 ,理论论上1mol
最多能消耗 ,故C错误误;
D.若若原料用 和 ,反应的的主产物是 ,副副产物为 和 故DD正确;
选B。
12【答案案】BC
【解析析】
根据据分析对比,容器Ⅱ的温温度比容器Ⅰ的高,则容器Ⅱ的反应速速率更快,但但10S时生成成的C相
同,则容容器Ⅱ中的反反应一定发生生了逆向移动动,因此,该反应H<0,A错误;10s时,容器器Ⅱ中的
反应一定定处于平衡状状态,C正确;容器III的的压强比容器器Ⅰ的大,则容容器III的反反应速率更快快,但10S
时生成的的C相同,则则容器III中的反应一定发发生了逆向移移动,因此,在容器III中,A、B中中至少有
一种呈非非气态,使反反应物中气体体的化学计量量数小于生成物,加压平衡衡逆移,B正正确;容器ⅡⅡ达到平
衡状态,可列出三段段式
13【答案案】BC
【解析析】
在硝硝酸铁催化下下钠与液氨的的反应来生成成NaNH 和氢氢气,其化学学方程式为:
2
2Na+2NHH =2NaNH ++H ↑,该反反应是放热反反应,为保证液氨处于微沸沸状态,需要要用冷却液控控制一定
3 2 2
的温度。NaNH 易与与水和氧气发发生反应,加加入钠之前处处先通入氨气的目的是排尽尽密闭体系中中空气,
2
A错误;装置B中HHg可防止氧氧气、水进入密闭体系,BB正确;反应应后NaNH 难难溶于液氨中中,可过
2
滤除去液液氨,得到产产品NaNH ,D错误。
2
化学答答案第3页,共5页14【答案】C
【解析】
A.往20.00mL 0.1mol·L−1 HA溶液中滴入0.1mol·L−1 NaOH溶液,发生反应:
NaOH+HA=NaA+H O,体系中−lgc(HA)随溶液pH的增大而增大,−lgc(A−) 随溶液pH的
2
增大而减小,故曲线①表示−lgc(HA)与溶液pH的关系,A错误;
B.a点对应的溶液中存在HA和NaA两种溶质,且二者的物质的量之比为1∶1,该溶液中的
电荷守恒式为c(Na+)+c(H+)=c(A−)+c(OH−),物料守恒式为2c(Na+)=c(A−)+c(HA),联立电
荷守恒式及物料守恒式可得:2c(H+)+c(HA)=2c(OH−)+c(A−),B错误;
C.b点对应的溶液pH=10即c(OH−)>c(H+),此时溶液中的溶质为NaA和NaOH,结合电荷守
恒式可得溶液中:c(Na+)>c(A−),故c(Na+)>c(A−)>c(OH−)>c(H+),C正确;
D.曲线①、曲线②的交点处有−lgc(HA) =−lgc(A−),即c(HA)= c(A−),HA的电离平衡常数
K =c(H+)=10−4.76,其数量级为10−5,D错误;
a
三、非选择题。
15【答案】(共13分)
(1)3d54s2 (2分) +6价(2分)
(2)A(1分)
(3) 使Fe3+转化为Fe(OH) 而除去,不影响Mn2+ (2分)
3
(4) Mn2++2HCO-=MnCO
3
↓+CO
2
↑+H
2
O (2分) 2.2×10-11 (2分)
3
(5) 2Mn2++5S O2+8H
2
O=16H++10SO2-+2MnO- (2分)
2 8 4 4
【解析】
(1)O元素存在-1价,S为主族元素,最高正价不超过最外层电子数,所以为+6价。
(2)固体焙烧应在坩埚中进行;
(3)由图表可知为了使Fe3+转化为Fe(OH) 而除去,而不影响Mn2+,步骤E中调节pH的范围为大
3
于Fe(OH) 的沉淀的pH而小于Mn2+形成沉淀需要的pH
3
(4)在含有Mn2+的溶液中加入NH
4
HCO
3
生成MnCO
3
沉淀,发生反应的离子方程式为Mn2++2HCO-
3
=MnCO
3
↓+CO
2
↑+H
2
O,Mn2+沉淀完全时其浓度为1×10-5mol·L-1,溶液中CO2-的浓度为
3
2.2×10-6mol·L-1,则K (MnCO )=(1×10-5mol·L-1)×(2.2×10-6mol·L-1)=2.2×10-11;
sp 3
(5)Mn从+2价升高为+7价,O从-1价降为-2价,根据电子守恒,再结合电荷守恒和原子守恒得
此反应的离子方程式2Mn2++5S O2+8H
2
O=16H++10SO2-+2MnO- ,故答案为2Mn2++5
2 8 4 4
S O2+8H 2 O=16H++10SO2-+2MnO- 。
2 8 4 4
16.(14 分)
(1)2CO +12e-+9H O=CH CH OH +12OH- (2分)
2 2 3 2
(2)CO *+ H* =HCO *(2分)
2 2
(3)① -122.54(2分) ②反应Ⅲ为吸热反应,当温度超过290℃,反应III占主导因素,CO的选择
性增大得更快,更有利于反应III正向移动,故CO 的转化率随温度升高而增大(2分)
2
1.5(3分) 8.96×10-3(3分)
化学答案第4页,共5页【解析】】
设起起始 CO
2
为为 1mol。CO
22
的起始分压压=41/5=00.8MPa,COO
2
的平衡转化化率 50%,则则转化的
CO 为 00.5mol,二甲甲醚的选择性性为 80%,则则说明有 0..4mol 的 COO 转化为二二甲醚。
2 2
CO
2
的起起始分压为 00.8MPa,达平平衡时分压为 4 0.5//(5-1)=0.55MPa ,
CO
22
(g)+3H
2
((g) CH
3
OH(g)+H
22
O(g) n(减少)
1 3 1 1 2
150% 1
平平衡时 CO
2
的的分压:40.5/(5-1)==0.5MPa,
COO 2 分压的平均均变化速率:(0.8-0.5)/0.2=1.5 MPa/S
COO (g)+3H (gg)CH OHH(g)+H O(gg) 2CH OHH(g)CH OOCH (g)+H O(g)
2 2 3 2 3 3 3 2
起始 1 4 0 0 0.5 0 00.5
转化 0.5 1.55 0.5 0.5 0.580% 0.2 00.2
平衡 0.5 2.55 0.5 0.5 0.1 0.2 00.7
平衡时总物物质的的量=0.5+2.5+0.1+0.2+0.7==4mol
K P =1/42 (0.1/4 0.7/4)/[00.5/4 (22.5/4)3)]=8.96×10-3MMPa—2
17.(144 分)【答案案】
(1)Fee3++3H OFe(OH) +3HH+(2分)
2 3
(2)溶液液中存在平衡衡:[Fe(C O ) ]3- Fe3++3C O 2- ,加入硫酸后,H+与C O 2-结合生成HH C O ,
2 44 3 2 4 2 44 2 2 4
使平衡正向移动动,c(Fe3+)增增大,遇KSSCN溶液变红红。(2分)
(3)B (2 分);Fe3+与 C O 2- 生成稳定的的[Fe(C O ) ]3-,浓度降低,Fe3+的氧氧化性和 C OO 2- 的还
2 4 2 4 3 2 4
原性减弱(2分分)
(4)②中产生大量红红褐色沉淀或或者③中得到到翠绿色溶液液(2分,答答一点即可)
(5)有+4价的碳的的化合物生成成,才能说明 C O 2-被氧化,以上现象象无法判断是是否有+4价的的碳的化
2 4
合物生成,因此此不能说明C O 2-是否被被氧化(2分分) (6))ACD(2分分)
2 4
18.(13分)
(1)甲苯(甲基苯)(1分) 取代代反应 (11分) 酯酯基、醚键(1分)
(2)2(1分)
(3) (2分)
(4) 10 (2分) , (2分分)
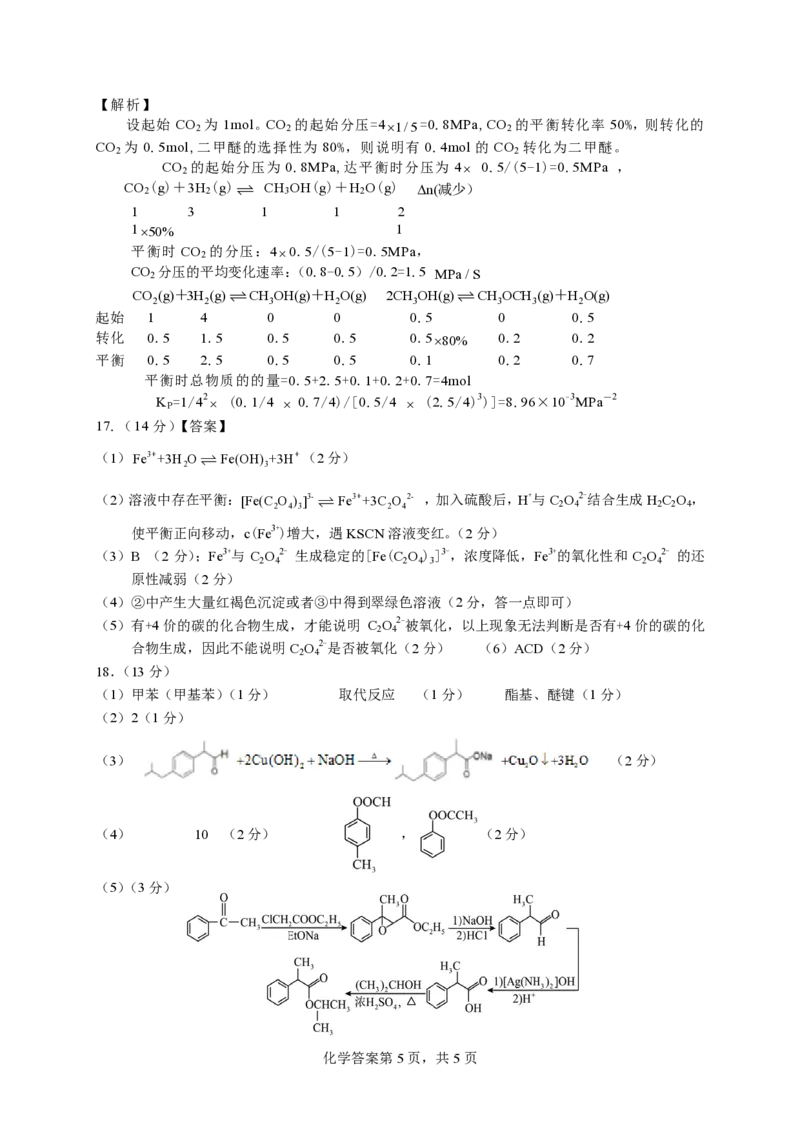
(5)(3分)
化学答答案第5页,共5页