文档内容
微专题09 新情景中氧化还原反应方程式的配平与书写
1.(2022.全国乙卷.高考真题)废旧铅蓄电池的铅膏中主要含有 、 、 和Pb。还有少量
Ba、Fe、Al的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅的回收。
一些难溶电解质的溶度积常数如下表:
难溶电解
质
一定条件下,一些金属氢氧化物沉淀时的 如下表:
金属氢氧化物
开始沉淀的pH 2.3 6.8 3.5 7.2
资料收集整理【淘宝店铺:向阳百分百】 1
学科网(北京)股份有限公司完全沉淀的pH 3.2 8.3 4.6 9.1
回答下列问题:
(1)在“脱硫”中 转化反应的离子方程式为________,用沉淀溶解平衡原理解释选择 的原因
________。
(3)在“酸浸”中,除加入醋酸( ),还要加入 。
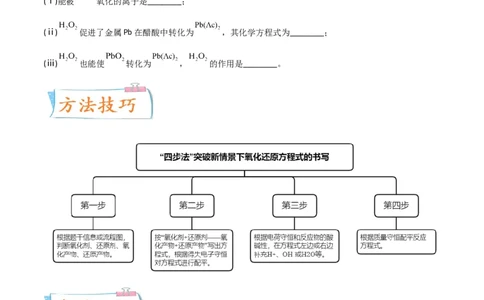
(ⅰ)能被 氧化的离子是________;
(ⅱ) 促进了金属Pb在醋酸中转化为 ,其化学方程式为________;
(ⅲ) 也能使 转化为 , 的作用是________。
一、工艺流程中的氧化还原方程式的书写
【归纳总结】
(1)细读题干寻找提纯对象,结合工艺流程示意图分析被提纯元素的存在形式及杂质的去除情况。
(2)确定未知反应的反应物和生成物,根据题意分析溶液环境,配平氧化还原方程式。
二、实验探究中的氧化还原方程式的书写
资料收集整理【淘宝店铺:向阳百分百】 2
学科网(北京)股份有限公司【归纳总结】
(1)细读题干寻找实验目的,通读题目中从实验步骤中了解操作步骤,结合装置分析实验过程,与实验
目的相对应。
(2)根据题意确定反应物和生成物,结合溶液环境配平方程式,注意质量守恒、电子守恒、电荷守恒。
三、电化学试题中氧化还原反应方程式的书写
【归纳总结】
(1)有关原电池原理的电极方程式的书写,负极失去电子,发生氧化反应;氧化剂在正极上得到电子,
发生还原反应。根据得失电子相等,从而配平电极方程式。
(2)有关电解原理的电极方程式的书写,还原剂在阳极上失去电子,发生氧化反应;氧化剂在阴极上得
到电子,发生还原反应。再根据得失电子相等,从而配平电极反应式。
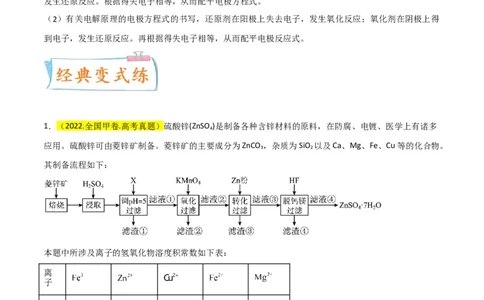
1.(2022.全国甲卷.高考真题)硫酸锌(ZnSO )是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多
4
应用。硫酸锌可由菱锌矿制备。菱锌矿的主要成分为ZnCO ,杂质为SiO 以及Ca、Mg、Fe、Cu等的化合物。
3 2
其制备流程如下:
本题中所涉及离子的氢氧化物溶度积常数如下表:
离
子
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为_______。
(4)向 的滤液①中分批加入适量 溶液充分反应后过滤,滤渣②中有 ,该步反应的离
子方程式为_______。
2.(2022·河北·高考真题)以焙烧黄铁矿 (杂质为石英等)产生的红渣为原料制备铵铁蓝
资料收集整理【淘宝店铺:向阳百分百】 3
学科网(北京)股份有限公司颜料。工艺流程如下:
回答下列问题:
(3)还原工序中,不生成S单质的反应的化学方程式为_______。
(5)沉铁工序产生的白色沉淀 中 的化合价为_______,氧化工序发生反应的离子方程式
为_______。
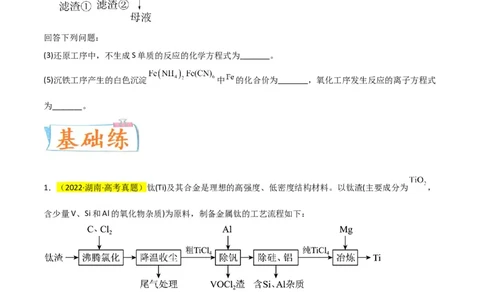
1.(2022·湖南·高考真题)钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为 ,
含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
已知“降温收尘”后,粗 中含有的几种物质的沸点:
物质
沸点/ 136 127 57 180
回答下列问题:
(2) 与C、 ,在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
资料收集整理【淘宝店铺:向阳百分百】 4
学科网(北京)股份有限公司物质
分压
①该温度下, 与C、 反应的总化学方程式为_______;
②随着温度升高,尾气中 的含量升高,原因是_______。
(3)“除钒”过程中的化学方程式为_______;“除硅、铝”过程中,分离 中含 、 杂质的方法是
_______。
2.(2022.辽宁.高考真题)某工厂采用辉铋矿(主要成分为 ,含有 、 杂质)与软锰矿(主要成
分为 )联合焙烧法制各 和 ,工艺流程如下:
已知:①焙烧时过量的 分解为 , 转变为 ;
②金属活动性: ;
③相关金属离子形成氢氧化物的 范围如下:
开始沉淀 完全沉淀
6.5 8.3
1.6 2.8
8.1 10.1
回答下列问题:
(2) 在空气中单独焙烧生成 ,反应的化学方程式为_______。
(5)生成气体A的离子方程式为_______。
3.(2023·全国·高三专题练习)回答下列问题:
资料收集整理【淘宝店铺:向阳百分百】 5
学科网(北京)股份有限公司(1)利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中
(Ⅲ)的处理工艺流程如下:
已知:硫酸浸取液中的金属离子主要是 ,其次是 和 。
① 的作用是将滤液Ⅰ中的 转化为 ,写出此反应的离子方程式:_______。
②写出上述流程中用 进行还原时发生反应的离子方程式:_______。
(2) 常用作陶瓷材料,可由锆英砂(主要成分为 ,也可表示为 ,还含少量
等杂质)通过如下方法制取:
已知: 能与烧碱反应生成可溶于水的 , 与酸反应生成 。
①“熔融”过程中, 发生反应的化学方程式为_______。
②滤渣Ⅲ的成分是 。“调 ”时,所发生反应的离子方程式为_______。滤渣Ⅲ
制备 的方法是_______。
4.(2023·云南·校联考二模)六水合氯化镍(NiCl ·6H O)常用于电镀、陶瓷等工业。某实验室以镍矿渣(主要
2 2
含NiS、CuS、FeS)制备六水合氯化镍晶体,设计流程如图所示:
资料收集整理【淘宝店铺:向阳百分百】 6
学科网(北京)股份有限公司已知: K (NiS)= 1.07×10-21, K (CuS)= 1.27×10-26。
sp sp
回答下列问题:
(1)①写出“酸溶”时,NiS发生反应的离子方程式:_______。
②“酸溶”时,为减少生产过程对大气的污染,通常还需通入过量的_______(填气体名称)。
(3)“除铜”过程发生反应的离子方程式是_______,若要求溶液中Cu2+浓度小于1×10-5mol/L,则应控制溶液
中Ni2+浓度_______。(结果保留两位小数)
5.(2023·海南海口·海南华侨中学校考二模)穿甲弹的弹芯用钨合金制造。工业上以黑钨矿(主要成分是
FeWO 、MnWO ,含少量的Fe O 、SiO )为原料冶炼钨的流程如图所示。
4 4 2 3 2
已知:钨酸H WO 难溶于水。
2 4
回答下列问题:
(1)浸取在加热、通空气条件下进行,FeWO 转化为Na WO 的化学方程式为________________。
4 2 4
6.(2023·安徽淮南·统考一模)锌的用途广泛,主要用于镀锌板及精密铸造等行业。以粗氧化锌(主要成分
为ZnO及少量Fe O 、CuO、MnO、SiO )为原料制备锌的工艺流程如图所示:
2 3 2
已知:①“浸取”时。ZnO、 CuO转化为[ Zn(NH ) ]2+、[Cu(NH ) ]2+进入溶液:
3 4 3 4
②25℃时,Ksp(CuS)=6.4×10-36, Ksp(ZnS)=1.6 ×10-24;
③沉淀除铜标准:溶液中 ≤2.0×10-6
资料收集整理【淘宝店铺:向阳百分百】 7
学科网(北京)股份有限公司回答下列问题:
(2)“氧化除锰”时,H O 将Mn2+转化为难溶的MnO ,该反应的离子方程式为___________。
2 2 2
7.(2023·山西吕梁·统考二模)以萃铜余液为原料制备工业活性氧化锌,其生产工艺流程如图所示:
(1)铜萃余液含硫酸30~60g/L,设计采用过硫酸钠(Na S O )氧化法除锰,写出Mn2+被氧化成MnO 的离子方
2 2 8 2
程式___________ ; 采用石灰石粉中和除去铝和铁,则中和渣中主要成分为___________。
(3)用锌粉除镉(Cd2+ )的离子方程式为___________;沉锌生成碱式碳酸锌[2Zn(OH )·ZnCO ·H O]的化学方程式
2 3 2
为___________。
(5)煅烧炉中发生反应的化学方程式为___________,工艺流程设计中选用高效真空负压内转盘浓缩沉锌后
液一体化设备生产无水___________,蒸发生产过程可实现零排放。
1.(2023·山东潍坊·统考二模)钛及其合金具有密度小、比强度高、耐热、耐低温等特性,是制造飞机、
火箭等的优异材料。工业上以钛铁矿(主要成分为 ,含 的氧化物等杂质)制备钛和
的工艺流程如图:
已知:① 时相关物质的 见下表:
物质
资料收集整理【淘宝店铺:向阳百分百】 8
学科网(北京)股份有限公司②I. ,
Ⅱ. ,
回答下列问题:
(1)“酸浸”时 元素转化为 , 发生反应的离子方程式为___________。
(5)“沉铁”操作单元发生反应的化学方程式为________。
2.(2023·全国·模拟预测) 主要用作颜料、釉料及磁性材料,一种利用含钴催化剂废料(主要含
Co、Fe,还含有少量的CoO、FeO、 、CaO、 )制备氧化钴( )的工艺流程如图所示。
已知:i.黄钠铁矾的化学式为 ;
ii.金属钴与铁具有相似的化学性质;
iii.氧化性 。
回答下列问题:
(3)除铁时先加入NaClO溶液,主要反应的离子方程式为___________,
(5) 在空气中加热煅烧得到 的化学方程式是___________。
3.(2020春·北京海淀·高三人大附中阶段练习)铜银合金在现代工业中有广泛应用。从铜银合金切割废料
(不含其它金属)中回收银并制备铜化工产品的工艺如图。
资料收集整理【淘宝店铺:向阳百分百】 9
学科网(北京)股份有限公司(2)滤渣A溶于稀硝酸时产生无色气体,该反应的离子方程式为___________。
(3)在混料池中,将三种原料按一定的物质的量之比混合均匀,煮沸,过滤。将滤渣B在200℃下翻炒至质
量不再变化,得到固体C.C只含CuO、Al O ,物质的量之比为2:1。在惰性气体保护下,将C在煅烧釜
2 3
中高温灼烧,得到CuAlO 该反应的方程式为___________。
2.
(5)冷却银熔体得到的粗银可使用电解法精炼,精炼池中阳极的电极反应为___________。
4.(2021·广东·高考真题)对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝( )、钼( )、
镍( )等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25℃时, 的 , ; ;
;该工艺中, 时,溶液中 元素以 的形态存在。
(1)“沉钼”中, 为7.0。
①生成 的离子方程式为_______。
5.(2020·全国·高考真题)钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、
镁的铝硅酸盐,以及SiO 、Fe O 。采用以下工艺流程可由黏土钒矿制备NH VO 。
2 3 4 4 3
资料收集整理【淘宝店铺:向阳百分百】 10
学科网(北京)股份有限公司该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Fe3+ Fe2+ Al3+ Mn2+
开始沉淀pH 1.9 7.0 3.0 8.1
完全沉淀pH 3.2 9.0 4.7 10.1
回答下列问题:
(1)“酸浸氧化”中,VO+和VO2+被氧化成 ,同时还有___________离子被氧化。写出VO+转化为 反
应的离子方程式___________。
(2)“沉淀转溶”中, 转化为钒酸盐溶解。滤渣③的主要成分是___________。
6.(2021·海南·高考真题)无水 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废
铁屑(含有少量碳和 杂质)为原料制备无水 。
已知:氯化亚砜( )熔点-101℃,沸点76℃,易水解。
回答问题:
(1)反应 的化学方程式为___________。
资料收集整理【淘宝店铺:向阳百分百】 11
学科网(北京)股份有限公司