文档内容
(新高考)小题必练9:化学能与热能
考查化学反应过程中化学键的断裂和形成过程中的能量变化,吸热反应和放热反应的判
断,能量的转化和利用,热化学方程式的意义,热化学方程式的书写及正误判断;利用盖斯定
律书写热化学方程式和进行反应热计算。
1.【2020年江苏卷】反应 可用于纯硅的制备。下列有关
该反应的说法正确的是( )
A.该反应ΔH>0、ΔS<0
B.该反应的平衡常数
C.高温下反应每生成1mol Si需消耗2×22.4L H
2
D.用E表示键能,该反应ΔH=4E(Si—Cl)+2E(H—H)-4E(H—Cl)
【答案】B
【解析】SiCl 、H、HCl为气体,且反应前气体系数之和小于反应后气体系数之和,因此该
4 2
反应为熵增,即ΔS>0,故A错误;B.根据化学平衡常数的定义,该反应的平衡常数K=
,故 B 正确;C.题中说的是高温,不是标准状况下,因此不能直接用
22.4L·mol−1计算,故C错误;D.ΔH=反应物键能总和-生成物键能总和,即ΔH=4E(Si—Cl)
+2E
(H—H)-4E(H—Cl)-2E(Si—Si),故D错误;答案为B。
【点睛】熵代表的是体系的混乱度,混乱度越大,熵越大。
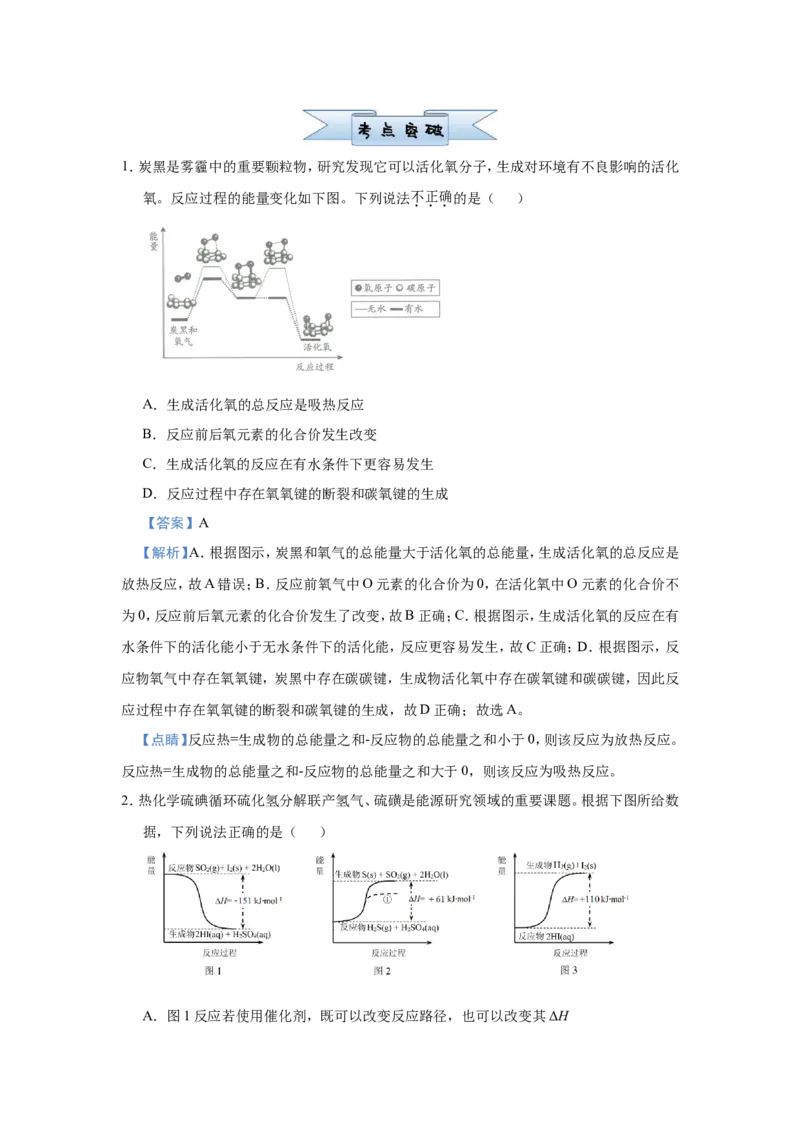
2.【2020年天津卷】理论研究表明,在101kPa和298K下,HCN(g) HNC(g)异构化反应
过程的能量变化如图所示。下列说法错误的是( )A.HCN比HNC稳定
B.该异构化反应的ΔH=+59.3kJ·mol−1
C.正反应的活化能大于逆反应的活化能
D.使用催化剂,可以改变反应的反应热
【答案】D
【解析】A.根据图中信息得到HCN能量比HNC能量低,再根据能量越低越稳定,因此
HCN比HNC稳定,故A正确;B.根据焓变等于生成物总能量减去反应物总能量,因此该异
构化反应的 ,故B正确;C.根据图中信息得出该
反应是吸热反应,因此正反应的活化能大于逆反应的活化能,故C正确;D.使用催化剂,不
能改变反应的反应热,只改变反应路径,反应热只与反应物和生成物的总能量有关,故D错
误。
【点睛】反应热的计算根据图形中给出的数据,套入到反应热等于生成物的总能量之和-
反应物的总能量之和中即可求得。
3.【2020年北京卷】依据图示关系,下列说法不正确的是( )
A.石墨燃烧是放热反应
B.1mol C(石墨)和1mol CO分别在足量O 中燃烧,全部转化为CO,前者放热多
2 2
C.C(石墨)+CO (g)=2CO(g) ΔH=ΔH-ΔH
2 1 2
D.化学反应的ΔH,只与反应体系的始态和终态有关,与反应途径无关
【答案】C
【解析】所有的燃烧都是放热反应,根据图示,C(石墨)+O (g)=CO (g) ΔH=-393.5kJ/mol,
2 2 1ΔH <0,则石墨燃烧是放热反应,故 A正确;B.根据图示,C(石墨)+O (g)=CO (g)
1 2 2
ΔH=-393.5kJ/mol,CO(g)+ O(g)=CO (g) ΔH=-283.0kJ/mol,根据反应可知都是放热反应,
1 2 2 2
1mol C(石墨)和1mol CO分别在足量O 中燃烧,全部转化为CO,1mol C(石墨)放热多,故
2 2
B 正确;根据 B 项分析,① C(石墨)+O (g)=CO (g) ΔH=-393.5kJ/mol,② CO(g)+
2 2 1
O(g)=CO (g) ΔH=-283.0kJ/mol,根据盖斯定律①-②×2可得:C(石墨)+CO (g)=2CO(g)
2 2 2 2
ΔH=ΔH-2ΔH,故C错误;D.根据盖斯定律可知,化学反应的焓变只与反应体系的始态和终
1 2
态有关,与反应途径无关,故D正确;答案选C。
【点睛】盖斯定律的使用时,应注意相应的反应式中系数和反应热应成相同倍数的增减。
4.【2020年浙江选考】在一定温度下,某反应达到了化学平衡,其反应过程对应的能量变化
如图。下列说法正确的是( )
A.E 为逆反应活化能,E为正反应活化能
a
B.该反应为放热反应,ΔH=E’-E
a a
C.所有活化分子的平均能量高于或等于所有分子的平均能量
D.温度升高,逆反应速率加快幅度大于正反应加快幅度,使平衡逆移
【答案】D
【解析】由图可知,反应物的总能量大于生成物的总能量,该反应为放热反应。A项、由图
可知,E 为正反应活化能,E为逆反应活化能,故A错误;B项、由图可知,反应物的总能量大
a
于生成物的总能量,该反应为放热反应,反应热ΔH=-(E’-E),故B错误;C项、在相同温度
a a
下,分子的能量并不完全相同,有些分子的能量高于分子的平均能量,称为活化分子,则所有
活化分子的平均能量高于所有分子的平均能量,故C错误;D项、该反应为放热反应,逆反应
速率加快幅度大于正反应加快幅度,使平衡向吸热的逆反应方向移动,故D正确;故选D。
【点睛】活化分子发生有效碰撞,要求能量高、碰撞方向正确,发生有效碰撞的分子是活化
分子,活化能是活化分子的平均能量与所有分子的平均能量之差是解答关键。1.炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成对环境有不良影响的活化
氧。反应过程的能量变化如下图。下列说法不正确的是( )
A.生成活化氧的总反应是吸热反应
B.反应前后氧元素的化合价发生改变
C.生成活化氧的反应在有水条件下更容易发生
D.反应过程中存在氧氧键的断裂和碳氧键的生成
【答案】A
【解析】A.根据图示,炭黑和氧气的总能量大于活化氧的总能量,生成活化氧的总反应是
放热反应,故A错误;B.反应前氧气中O元素的化合价为0,在活化氧中O元素的化合价不
为0,反应前后氧元素的化合价发生了改变,故B正确;C.根据图示,生成活化氧的反应在有
水条件下的活化能小于无水条件下的活化能,反应更容易发生,故C正确;D.根据图示,反
应物氧气中存在氧氧键,炭黑中存在碳碳键,生成物活化氧中存在碳氧键和碳碳键,因此反
应过程中存在氧氧键的断裂和碳氧键的生成,故D正确;故选A。
【点睛】反应热=生成物的总能量之和-反应物的总能量之和小于0,则该反应为放热反应。
反应热=生成物的总能量之和-反应物的总能量之和大于0,则该反应为吸热反应。
2.热化学硫碘循环硫化氢分解联产氢气、硫磺是能源研究领域的重要课题。根据下图所给数
据,下列说法正确的是( )
A.图1反应若使用催化剂,既可以改变反应路径,也可以改变其ΔHB.图2中若HO的状态为气态,则能量变化曲线可能为①
2
C.图3反应中反应物的总能量比生成物的总能量高
D.由图1、图2和图3可知,HS(g)=H(g)+S(s) ΔH=+20kJ·mol−1
2 2
【答案】D
【解析】催化剂不改变反应热,故A错误;HO(g)的能量高于HO(l)的能量,故B错误;图
2 2
3反应中反应物的总能量比生成物的总能量低,故C错误;D. 由图1:SO (g)+I (s)+2HO(l)
2 2 2
=2HI(aq)+H SO (aq) ΔH=-151kJ·mol−1;由图2:SO (g)+S(s)+2HO(l)=HS(g)+HSO (aq) ΔH
2 4 2 2 2 2 4
=-61kJ·mol−1;由图 3:H(g)+2I (s)=2HI(aq) ΔH=+110kJ·mol−1,根据盖斯定理可知
2 2
HS(g)=H(g)+S(s) ΔH=+20kJ·mol−1,故D正确;故选D。
2 2
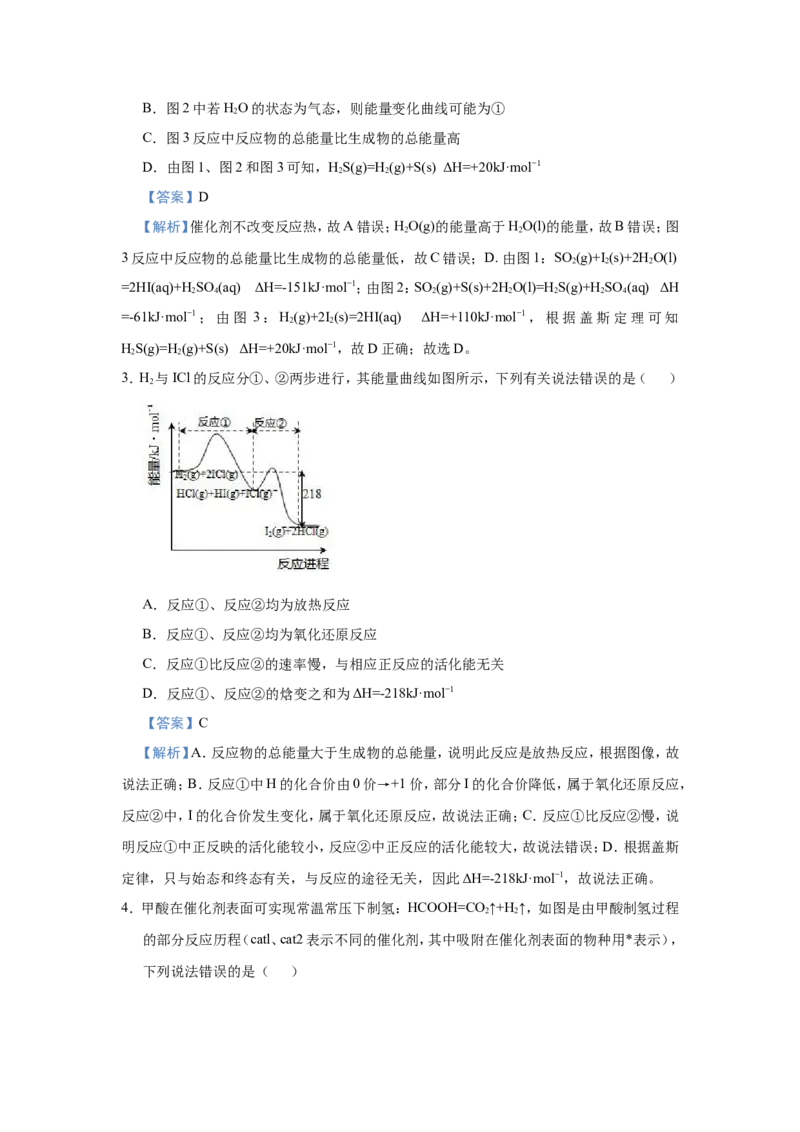
3.H 与ICl的反应分①、②两步进行,其能量曲线如图所示,下列有关说法错误的是( )
2
A.反应①、反应②均为放热反应
B.反应①、反应②均为氧化还原反应
C.反应①比反应②的速率慢,与相应正反应的活化能无关
D.反应①、反应②的焓变之和为ΔH=-218kJ·mol−1
【答案】C
【解析】A.反应物的总能量大于生成物的总能量,说明此反应是放热反应,根据图像,故
说法正确;B.反应①中H的化合价由0价→+1价,部分I的化合价降低,属于氧化还原反应,
反应②中,I的化合价发生变化,属于氧化还原反应,故说法正确;C.反应①比反应②慢,说
明反应①中正反映的活化能较小,反应②中正反应的活化能较大,故说法错误;D.根据盖斯
定律,只与始态和终态有关,与反应的途径无关,因此ΔH=-218kJ·mol−1,故说法正确。
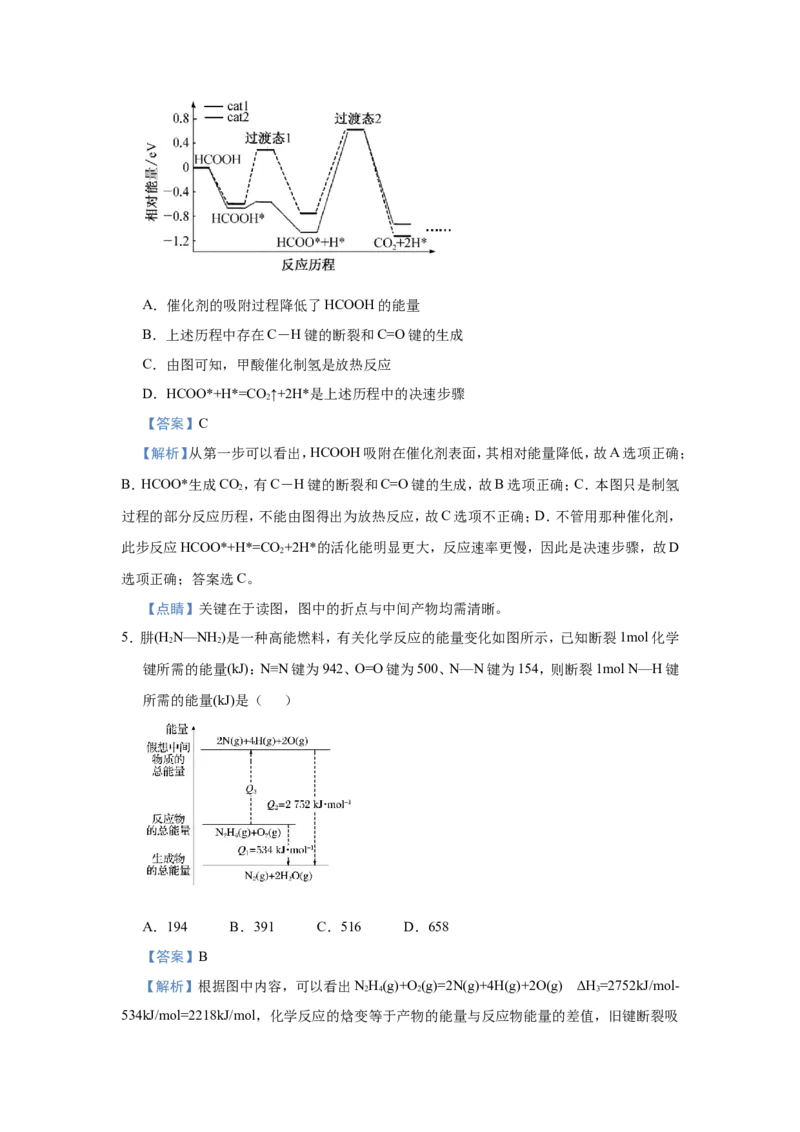
4.甲酸在催化剂表面可实现常温常压下制氢:HCOOH=CO ↑+H ↑,如图是由甲酸制氢过程
2 2
的部分反应历程(catl、cat2表示不同的催化剂,其中吸附在催化剂表面的物种用*表示),
下列说法错误的是( )A.催化剂的吸附过程降低了HCOOH的能量
B.上述历程中存在C-H键的断裂和C=O键的生成
C.由图可知,甲酸催化制氢是放热反应
D.HCOO*+H*=CO ↑+2H*是上述历程中的决速步骤
2
【答案】C
【解析】从第一步可以看出,HCOOH吸附在催化剂表面,其相对能量降低,故A选项正确;
B.HCOO*生成CO,有C-H键的断裂和C=O键的生成,故B选项正确;C.本图只是制氢
2
过程的部分反应历程,不能由图得出为放热反应,故C选项不正确;D.不管用那种催化剂,
此步反应HCOO*+H*=CO +2H*的活化能明显更大,反应速率更慢,因此是决速步骤,故D
2
选项正确;答案选C。
【点睛】关键在于读图,图中的折点与中间产物均需清晰。
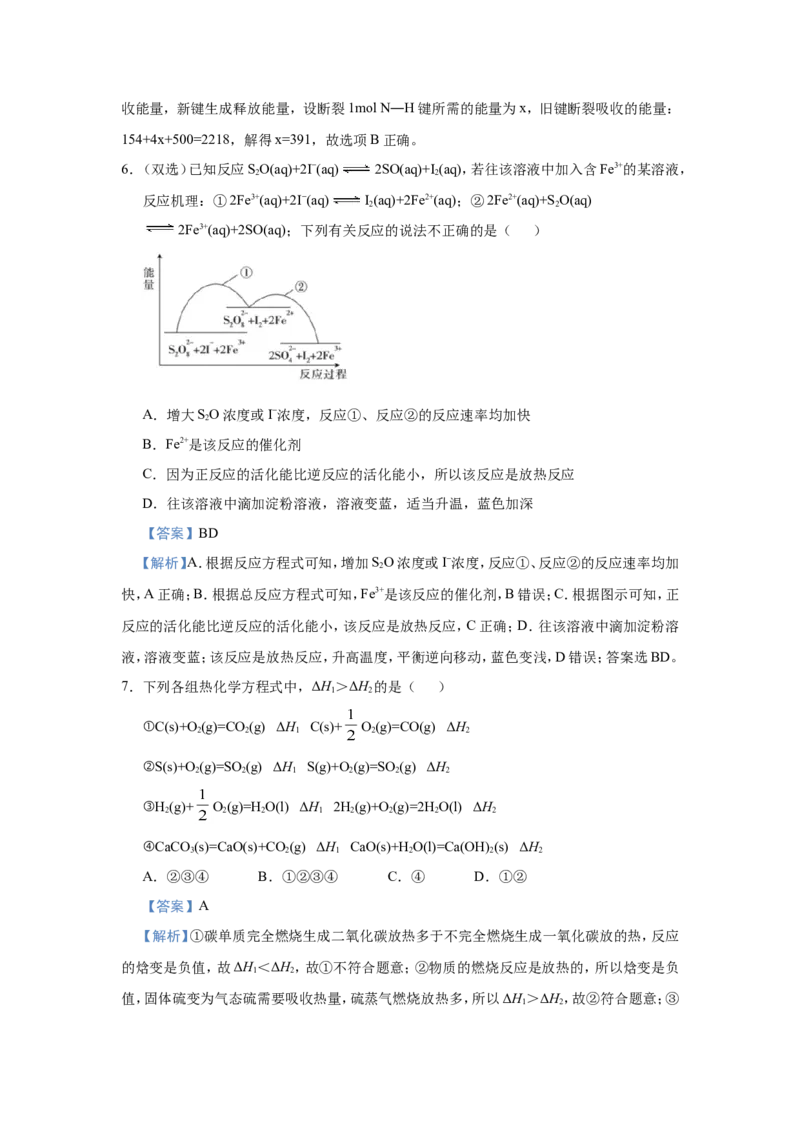
5.肼(H N—NH)是一种高能燃料,有关化学反应的能量变化如图所示,已知断裂1mol化学
2 2
键所需的能量(kJ):N≡N键为942、O=O键为500、N—N键为154,则断裂1mol N—H键
所需的能量(kJ)是( )
A.194 B.391 C.516 D.658
【答案】B
【解析】根据图中内容,可以看出NH(g)+O(g)=2N(g)+4H(g)+2O(g) ΔH=2752kJ/mol-
2 4 2 3
534kJ/mol=2218kJ/mol,化学反应的焓变等于产物的能量与反应物能量的差值,旧键断裂吸收能量,新键生成释放能量,设断裂1mol N―H键所需的能量为x,旧键断裂吸收的能量:
154+4x+500=2218,解得x=391,故选项B正确。
6.(双选)已知反应SO(aq)+2I−(aq) 2SO(aq)+I (aq),若往该溶液中加入含Fe3+的某溶液,
2 2
反应机理:①2Fe3+(aq)+2I−(aq) I(aq)+2Fe2+(aq);②2Fe2+(aq)+S O(aq)
2 2
2Fe3+(aq)+2SO(aq);下列有关反应的说法不正确的是( )
A.增大SO浓度或I−浓度,反应①、反应②的反应速率均加快
2
B.Fe2+是该反应的催化剂
C.因为正反应的活化能比逆反应的活化能小,所以该反应是放热反应
D.往该溶液中滴加淀粉溶液,溶液变蓝,适当升温,蓝色加深
【答案】BD
【解析】A.根据反应方程式可知,增加SO浓度或I−浓度,反应①、反应②的反应速率均加
2
快,A正确;B.根据总反应方程式可知,Fe3+是该反应的催化剂,B错误;C.根据图示可知,正
反应的活化能比逆反应的活化能小,该反应是放热反应,C正确;D.往该溶液中滴加淀粉溶
液,溶液变蓝;该反应是放热反应,升高温度,平衡逆向移动,蓝色变浅,D错误;答案选BD。
7.下列各组热化学方程式中,ΔH>ΔH 的是( )
1 2
①C(s)+O(g)=CO (g) ΔH C(s)+ O(g)=CO(g) ΔH
2 2 1 2 2
②S(s)+O(g)=SO(g) ΔH S(g)+O(g)=SO(g) ΔH
2 2 1 2 2 2
③H(g)+ O(g)=HO(l) ΔH 2H(g)+O(g)=2HO(l) ΔH
2 2 2 1 2 2 2 2
④CaCO(s)=CaO(s)+CO(g) ΔH CaO(s)+HO(l)=Ca(OH) (s) ΔH
3 2 1 2 2 2
A.②③④ B.①②③④ C.④ D.①②
【答案】A
【解析】①碳单质完全燃烧生成二氧化碳放热多于不完全燃烧生成一氧化碳放的热,反应
的焓变是负值,故ΔH<ΔH,故①不符合题意;②物质的燃烧反应是放热的,所以焓变是负
1 2
值,固体硫变为气态硫需要吸收热量,硫蒸气燃烧放热多,所以ΔH>ΔH,故②符合题意;③
1 2化学反应方程式的系数加倍,焓变数值加倍,该化合反应是放热的,所以焓变值是负值,
2ΔH=ΔH,ΔH>ΔH,故③符合题意;④CaCO (s)=CaO(s)+CO (g)反应是吸热反应,ΔH>
1 2 1 2 3 2 1
0;CaO(s)+H O(l)=Ca(OH) (s),反应是放热反应,ΔH<0;前者大于后者,ΔH>ΔH,故④符
2 2 2 1 2
合题意。故选A。
8.下列说法或表示方法正确的是( )
A.由“C(石墨) C(金刚石) ΔH=+1.9kJ/mol”可知金刚石比石墨稳定
B.在101KPa时,1mol碳燃烧所放出的热量为碳的燃烧热
C.相同的条件下,如果1mol氢原子所具有的能量为E,1mol氢分子的能量为E,则2E
1 2 1
﹥E
2
D.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则HSO 和Ca(OH) 反应的中和热为
2 4 2
ΔH=-(2×57.3)kJ/mol
【答案】C
【解析】A.由“C(石墨) C(金刚石) ΔH=+1.9kJ/mol”,金刚石的能量高于石墨,所
以金刚石不如石墨稳定,A不正确;B.在101KPa时,1mol碳完全燃烧放出的热量为碳的燃
烧热;若燃烧不充分,所放出的热量不是碳的燃烧热,B不正确;C.相同的条件下,如果1mol
氢原子所具有的能量为E,1mol氢分子的能量为E,则由氢原子形成氢分子时,形成化学键,
1 2
放出热量,所以2E﹥E,C正确;D.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则HSO
1 2 2 4
和Ca(OH) 反应,由于生成CaSO 也会放出热量,热量数值偏大,所以中和热为 ΔH<-
2 4
(2×57.3)kJ/mol,D不正确;故选C。
9.(双选)固态或气态碘分别与氢气反应的热化学方程式如下:
①H(g)+I (?) 2HI(g) ΔH=-9.48kJ/mol
2 2 1
②H (g)+I (?) 2HI(g) ΔH=+26.48kJ/mol
2 2 2
下列判断正确的是( )
A.反应①中的I 为气态,反应②中的I 为固态
2 2
B.0.1mol H(g)与足量碘充分发生反应①,放出9.48kJ热量
2
C.反应②中,使用适当催化剂,可以减小ΔH
2
D.1mol固态碘完全升华会吸热35.96kJ
【答案】AD
【解析】A.反应①-②得:①I(?) ②I (?) ΔH=-35.96kJ/mol,则反应①中的I 为气态,
2 2 1 2
反应②中的I 为固态,A正确;B.由反应①知,1mol H(g)与1mol I(g)完全反应生成2mol
2 2 2
HI(g),放热9.48kJ,现0.1mol H(g)与足量碘充分发生反应①,则放出的热量小于0.948kJ,B
2不正确;C.反应②中,使用适当催化剂,不能改变反应的热效应,ΔH 不变,C不正确;D.由
2
A中的计算可知,1mol气态碘完全转化为固态碘会放热35.96kJ,则1mol固态碘完全升华会
吸热35.96kJ,D正确;故选AD。
10.(双选)研究表明CO与NO在Fe+作用下发生反应的能量变化及反应历程如图所示,两
2
步反应分别为①NO+Fe+=N +FeO(+ 慢)、②FeO++CO=CO+Fe(+ 快)。下列说法正确的是
2 2 2
( )
A.反应①是氧化还原反应,反应②是非氧化还原反应
B.两步反应均为放热反应,总反应的化学反应速率由反应②决定
C.Fe+使反应的活化能减小,FeO+是中间产物
D.若转移1mol电子,则消耗标况下11.2L N O
2
【答案】CD
【解析】A.反应①NO+Fe+=N +FeO+(慢)中N的化合价由+1价变为0价,Fe的化合价由
2 2
+1价变为+3价,化合价发生改变,反应①是氧化还原反应,同理②FeO++CO=CO +Fe+(快)中
2
Fe元素的化合价由+3价变为+1价,C的化合价由+2价变为+4价,化合价发生改变,故反应
②也是氧化还原反应,A错误;B.由图中可知两步反应的反应物总能量均高于生成物总能量,
故均为放热反应,总反应的化学反应速率是由慢反应决定的,故由反应①决定,B错误;C.由
历程图中可知,Fe+是催化剂,FeO+是中间产物,故Fe+使反应的活化能减小,FeO+是中间产物,
C正确;D.由反应NO+CO=N+CO 可知,反应中转移了2mol电子,故若转移1mol电子,则
2 2 2
消耗0.5mol NO,标准状况下0.5mol NO的体积为11.2L,D正确;答案选CD。
2 2
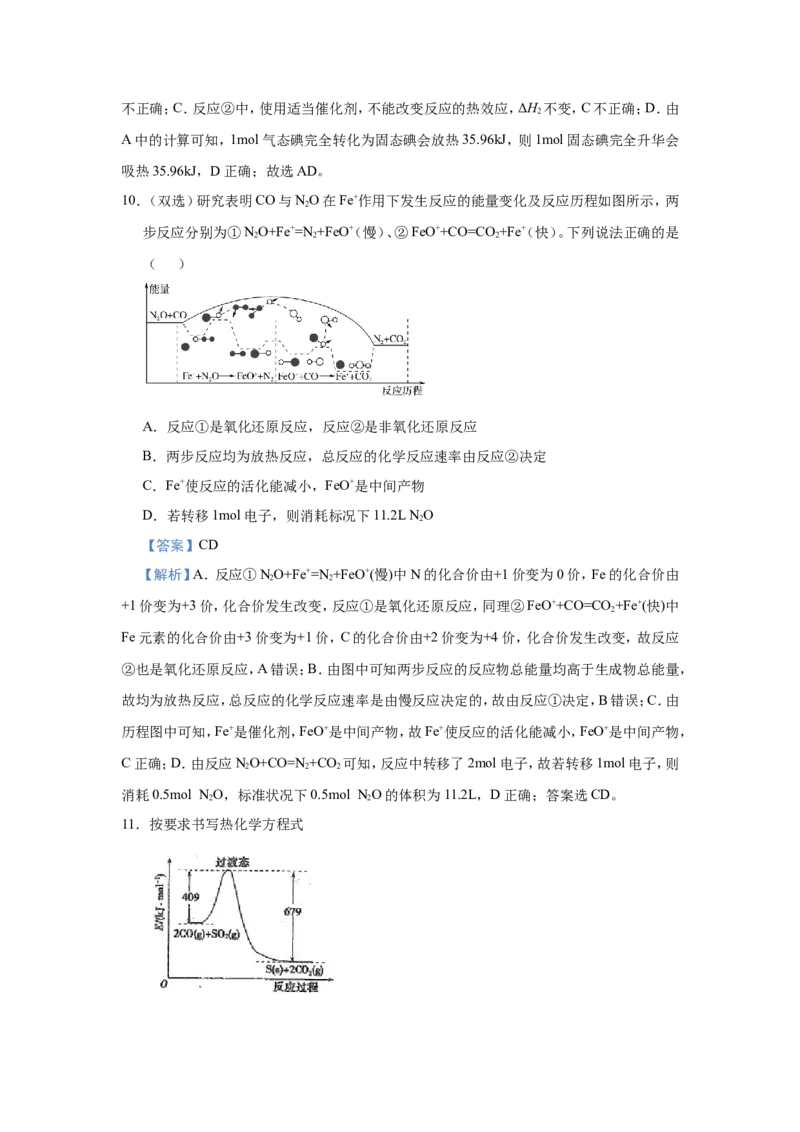
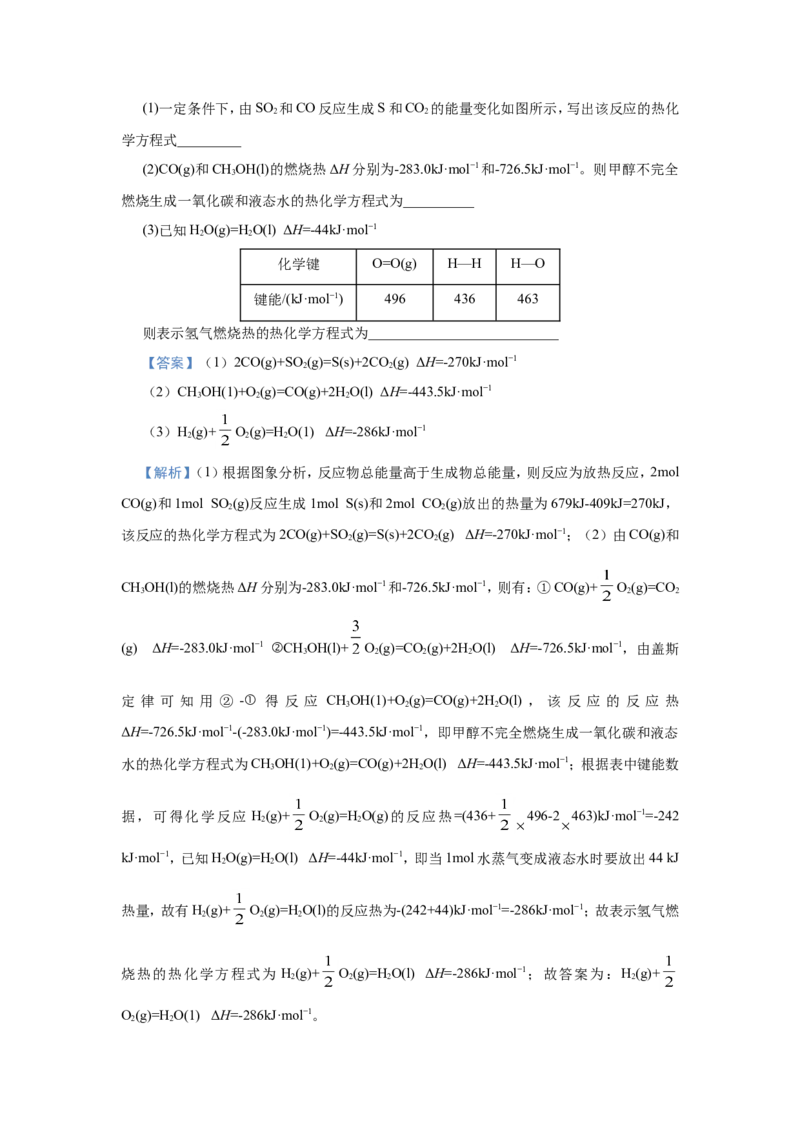
11.按要求书写热化学方程式(1)一定条件下,由SO 和CO反应生成S和CO 的能量变化如图所示,写出该反应的热化
2 2
学方程式_________
(2)CO(g)和CHOH(l)的燃烧热ΔH分别为-283.0kJ·mol−1和-726.5kJ·mol−1。则甲醇不完全
3
燃烧生成一氧化碳和液态水的热化学方程式为__________
(3)已知HO(g)=H O(l) ΔH=-44kJ·mol−1
2 2
化学键 O=O(g) H—H H—O
键能/(kJ·mol−1) 496 436 463
则表示氢气燃烧热的热化学方程式为___________________________
【答案】(1)2CO(g)+SO (g)=S(s)+2CO (g) ΔH=-270kJ·mol−1
2 2
(2)CHOH(1)+O (g)=CO(g)+2HO(l) ΔH=-443.5kJ·mol−1
3 2 2
(3)H(g)+ O(g)=HO(1) ΔH=-286kJ·mol−1
2 2 2
【解析】(1)根据图象分析,反应物总能量高于生成物总能量,则反应为放热反应,2mol
CO(g)和1mol SO (g)反应生成1mol S(s)和2mol CO(g)放出的热量为679kJ-409kJ=270kJ,
2 2
该反应的热化学方程式为2CO(g)+SO (g)=S(s)+2CO (g) ΔH=-270kJ·mol−1;(2)由CO(g)和
2 2
CHOH(l)的燃烧热ΔH分别为-283.0kJ·mol−1和-726.5kJ·mol−1,则有:①CO(g)+ O(g)=CO
3 2 2
(g) ΔH=-283.0kJ·mol−1 ②CH OH(l)+ O(g)=CO (g)+2HO(l) ΔH=-726.5kJ·mol−1,由盖斯
3 2 2 2
定 律 可 知 用 ② -① 得 反 应 CHOH(1)+O (g)=CO(g)+2HO(l) , 该 反 应 的 反 应 热
3 2 2
ΔH=-726.5kJ·mol−1-(-283.0kJ·mol−1)=-443.5kJ·mol−1,即甲醇不完全燃烧生成一氧化碳和液态
水的热化学方程式为CHOH(1)+O (g)=CO(g)+2HO(l) ΔH=-443.5kJ·mol−1;根据表中键能数
3 2 2
据,可得化学反应 H(g)+ O(g)=HO(g)的反应热=(436+ 496-2 463)kJ·mol−1=-242
2 2 2
kJ·mol−1,已知HO(g)=H O(l) ΔH=-44kJ·mol−1,即当1mol水蒸气变成液态水时要放出44 kJ
2 2
热量,故有H(g)+ O(g)=HO(l)的反应热为-(242+44)kJ·mol−1=-286kJ·mol−1;故表示氢气燃
2 2 2
烧热的热化学方程式为 H(g)+ O(g)=HO(l) ΔH=-286kJ·mol−1;故答案为:H(g)+
2 2 2 2
O(g)=HO(1) ΔH=-286kJ·mol−1。
2 212.近期发现,HS是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经
2
信号传递、舒张血管减轻高血压的功能。回答下列问题:
下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。
通过计算,可知系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式分别为________________、
______________,制得等量H 所需能量较少的是_____________。
2
【答案】HO(l)=H(g)+ O(g) ΔH=+286kJ/mol
2 2 2
HS(g)=H(g)+S(s) ΔH=+20kJ/mol 系统(II)
2 2
【 解 析 】 ① HSO (aq)=SO(g)+HO(l)+ O(g) ΔH=+327kJ/mol ②SO (g)+I (s)+
2 4 2 2 2 1 2 2
2HO(l)=2HI(aq)+H SO (aq) ΔH=-151kJ/mol ③2HI(aq)=H (g)+I (s) ΔH=+110 kJ/mol
2 2 4 2 2 2 3
④H S(g)+HSO (aq)=S(s)+SO (g)+2HO(l) ΔH=+61kJ/mol,①+②+③,整理可得系统(I)的热
2 2 4 2 2 4
化学方程式HO(l)=H(g)+ O(g) ΔH=+286kJ/mol;②+③+④,整理可得系统(II)的热化学
2 2 2
方程式HS (g)=H (g)+S(s) ΔH=+20kJ/mol。根据系统I、系统II的热化学方程式可知:每反应
2 2
产生1mol氢气,后者吸收的热量比前者少,所以制取等量的H 所需能量较少的是系统II。
2
13.已知 2mol 氢气燃烧生成液态水时放出 572kJ 的热量,反应方程式是 2H(g)
2
+O(g)=2HO(l)。请回答下列问题:
2 2
(1)①该反应的生成物能量总和________(填“大于”、“小于”或“等于”)反应物能量
总和。②若2mol氢气完全燃烧生成水蒸气,则放出的热量________(填“>”、“<”或“=”)572
kJ。
(2)FeS 焙烧产生的SO 可用于制硫酸。已知25℃、101kPa时:
2 22SO (g)+O(g) 2SO (g) ΔH=-197kJ·mol−1
2 2 3 1
HO(g)=H O(l) ΔH=-44kJ·mol−1
2 2 2
2SO (g)+O(g)+2HO(g)=2H SO (l) ΔH=-545kJ·mol−1
2 2 2 2 4 3
则SO (g)与HO(l)反应的热化学方程式是_________________。
3 2
(3)已知下列反应的热化学方程式:
①6C(s)+5H(g)+3N(g)+9O(g)=2C H(ONO)(l) ΔH
2 2 2 3 5 2 3 1
②2H (g)+O(g)=2HO(g) ΔH
2 2 2 2
③C(s)+O(g)=CO (g) ΔH
2 2 3
则反应4C H(ONO)(l)=12CO (g)+10HO(g)+O(g)+6N(g)的ΔH为________。
3 5 2 3 2 2 2 2
【答案】(1)小于 <
(2)SO (g)+HO(l)=HSO (l) ΔH=-130kJ·mol−1
3 2 2 4
(3)12ΔH+5ΔH-2ΔH
3 2 1
【解析】(1)①氢气燃烧是放热反应,因此该反应的生成物能量总和小于反应物能量总和;
②水蒸气能量高于液态水的能量,因此2mol氢气完全燃烧生成水蒸气放出的热量<572kJ;
(2)已知:① 2SO (g)+O(g) 2SO (g) ΔH=-197kJ·mol−1②H O(g)=HO(l) ΔH=-44
2 2 3 1 2 2 2
kJ·mol−1③2SO(g)+O(g)+2HO(g)=2HSO (l) ΔH=-545kJ·mol−1 则根据盖斯定律可知
2 2 2 2 4 3
即得到 SO (g)与 HO(l)反应的热化学方程式是 SO (g)+HO(l)=HSO (l)
3 2 3 2 2 4
ΔH=-130kJ·mol−1;(3)已知:① 6C(s)+5H(g)+3N(g)+9O(g)=2C H(ONO)(l) ΔH ;
2 2 2 3 5 2 3 1
②2H(g)
2
+O(g)=2HO(g) ΔH③C(s)+O(g)=CO(g) ΔH ,则根据盖斯定律可知③×12+②×5-①×2即
2 2 2 2 2 3
得到反应4C H(ONO)(l)=12CO(g)+10HO(g)+O(g)+6N(g)的ΔH=12ΔH+5ΔH-2ΔH。
3 5 2 3 2 2 2 2 3 2 1
【点睛】掌握利用盖斯定律书写热化学方程式的一般步骤:(1)确定待求的热化学方程式;
(2)找出待求的热化学方程式中各物质出现在已知热化学方程式的位置;(3)根据未知热化
学方程式中各物质的系数和位置的需要对已知热化学方程式进行处理,或调整系数,或调整
反应方向;将新得到的热化学方程式及对应的反应热进行叠加,即可求出待求反应的反应热。