文档内容
培优训练3:化学(离子)方程式的书写
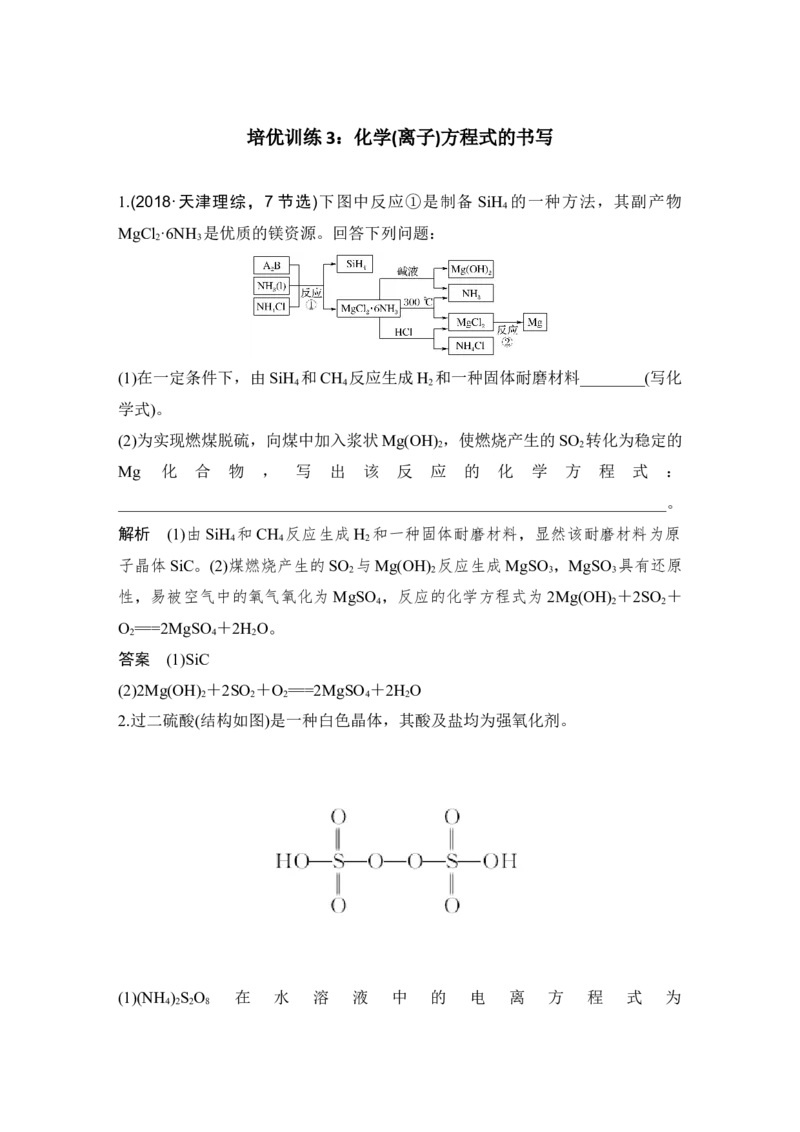
1.(2018·天津理综,7 节选)下图中反应①是制备 SiH 的一种方法,其副产物
4
MgCl ·6NH 是优质的镁资源。回答下列问题:
2 3
(1)在一定条件下,由SiH 和CH 反应生成H 和一种固体耐磨材料________(写化
4 4 2
学式)。
(2)为实现燃煤脱硫,向煤中加入浆状Mg(OH) ,使燃烧产生的SO 转化为稳定的
2 2
Mg 化 合 物 , 写 出 该 反 应 的 化 学 方 程 式 :
____________________________________________________________________。
解析 (1)由SiH 和CH 反应生成H 和一种固体耐磨材料,显然该耐磨材料为原
4 4 2
子晶体SiC。(2)煤燃烧产生的SO 与Mg(OH) 反应生成MgSO ,MgSO 具有还原
2 2 3 3
性,易被空气中的氧气氧化为 MgSO ,反应的化学方程式为2Mg(OH) +2SO +
4 2 2
O ===2MgSO +2H O。
2 4 2
答案 (1)SiC
(2)2Mg(OH) +2SO +O ===2MgSO +2H O
2 2 2 4 2
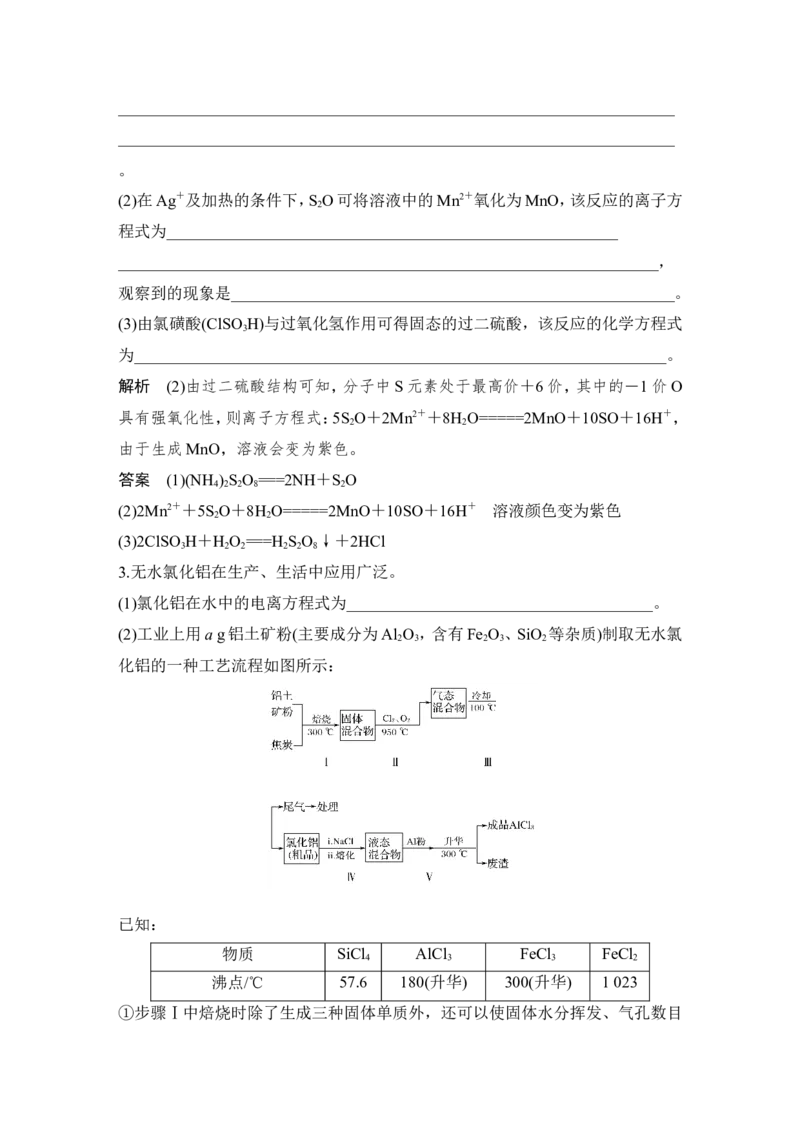
2.过二硫酸(结构如图)是一种白色晶体,其酸及盐均为强氧化剂。
(1)(NH ) S O 在 水 溶 液 中 的 电 离 方 程 式 为
4 2 2 8_____________________________________________________________________
_____________________________________________________________________
。
(2)在Ag+及加热的条件下,S O可将溶液中的Mn2+氧化为MnO,该反应的离子方
2
程式为________________________________________________________
___________________________________________________________________,
观察到的现象是_______________________________________________________。
(3)由氯磺酸(ClSO H)与过氧化氢作用可得固态的过二硫酸,该反应的化学方程式
3
为__________________________________________________________________。
解析 (2)由过二硫酸结构可知,分子中S元素处于最高价+6价,其中的-1价O
具有强氧化性,则离子方程式:5S O+2Mn2++8H O=====2MnO+10SO+16H+,
2 2
由于生成MnO,溶液会变为紫色。
答案 (1)(NH ) S O ===2NH+S O
4 2 2 8 2
(2)2Mn2++5S O+8H O=====2MnO+10SO+16H+ 溶液颜色变为紫色
2 2
(3)2ClSO H+H O ===H S O ↓+2HCl
3 2 2 2 2 8
3.无水氯化铝在生产、生活中应用广泛。
(1)氯化铝在水中的电离方程式为______________________________________。
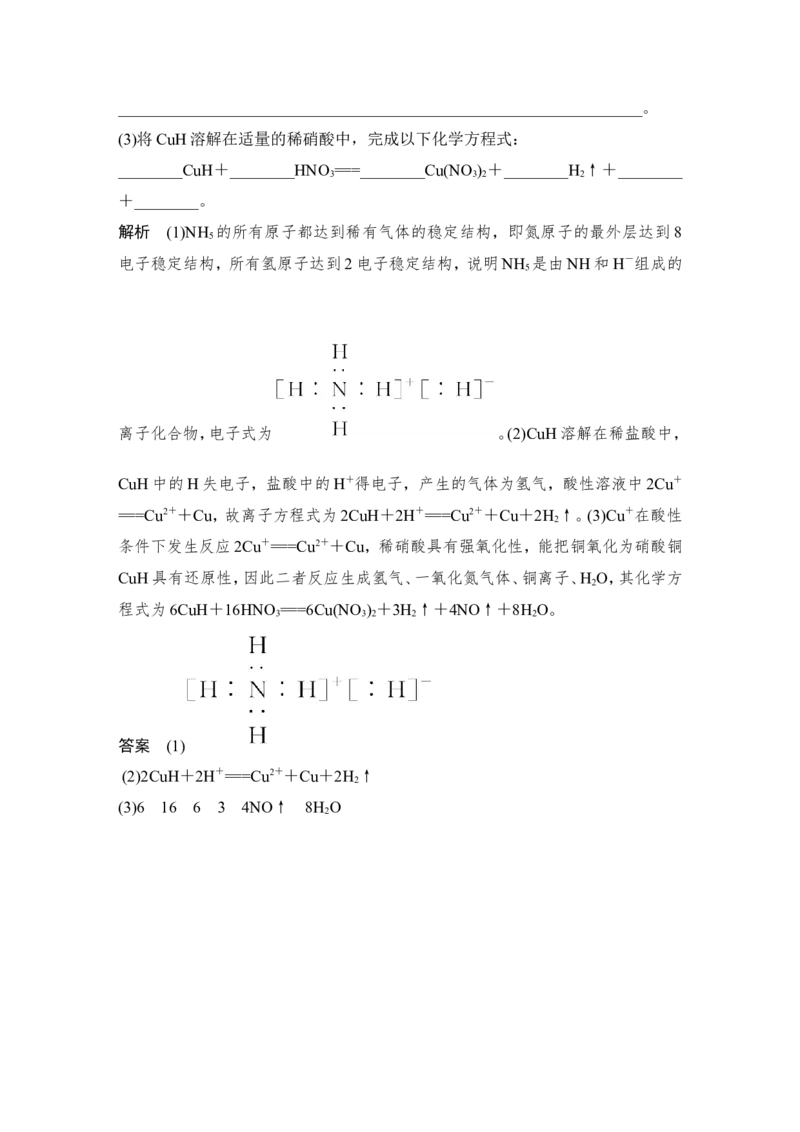
(2)工业上用a g铝土矿粉(主要成分为Al O ,含有Fe O 、SiO 等杂质)制取无水氯
2 3 2 3 2
化铝的一种工艺流程如图所示:
已知:
物质 SiCl AlCl FeCl FeCl
4 3 3 2
沸点/℃ 57.6 180(升华) 300(升华) 1 023
①步骤Ⅰ中焙烧时除了生成三种固体单质外,还可以使固体水分挥发、气孔数目增多,其作用是______________________________________________________(要
求写出两种),
步 骤 Ⅰ 中 生 成 非 金 属 单 质 的 反 应 的 化 学 方 程 式 为
_____________________________________________________________________。
②步骤Ⅲ的尾气经冷却至室温后,用足量的NaOH冷溶液吸收,写出吸收过程中
发生反应的离子方程式___________________________________________
_______________________________________________________________。
解析 (1)AlCl 在水溶液中能完全电离,属于强电解质,电离方程式为
3
AlCl ===Al3++3Cl-。(2)①步骤Ⅰ中焙烧时,固体水分挥发,可以防止后续步骤生
3
成的AlCl 水解;气孔数目增多,可以增大步骤Ⅱ中反应物的接触面积,加快反应
3
速率。由题意知,铝土矿粉中含有SiO 杂质,SiO 与焦炭在高温下反应生成单质
2 2
Si,故步骤Ⅰ中生成非金属单质的反应的化学方程式为 SiO +2C Si+
2
2CO↑。②步骤Ⅲ的尾气经冷却至室温后,主要有Cl 、O 和CO ,用足量的NaOH
2 2 2
冷溶液吸收时,发生反应的离子方程式为Cl +2OH-===Cl-+ClO-+H O和CO
2 2 2
+2OH-===CO+H O。
2
答案 (1)AlCl ===Al3++3Cl-
3
(2)①防止后续步骤生成的AlCl 水解;增大步骤Ⅱ中反应物的接触面积,加快反
3
应速率 SiO +2C=====Si+2CO↑
2
②Cl +2OH-===Cl-+ClO-+H O、CO +2OH-===CO+H O
2 2 2 2
4.高铁酸钾(K FeO )是一种易溶于水,高效的多功能水处理剂。工业上通常先制得
2 4
高铁酸钠,然后在一定温度下,向高铁酸钠溶液中加入KOH至饱和,从而使高铁
酸钾析出。
(1)高铁酸钾中铁元素的化合价为________,推测其具有的化学性质是________。
(2)高铁酸钾与水反应生成O 、Fe(OH) (胶体)和KOH。
2 3
①该反应的离子方程式为__________________________________________。
②高铁酸钾作为水处理剂起到的作用是_______________________________。
(3)①在无水条件下制备高铁酸钠的主要反应为 2FeSO +aNa O ===2Na FeO +
4 2 2 2 4
bX+2Na SO +cO ↑,该反应中物质 X的化学式为________,b与c的关系是
2 4 2
________。②一定温度下,向高铁酸钠溶液中加入 KOH至饱和可析出高铁酸钾,原因是
_____________________________________________________________________
_____________________________________________________________________
。
(4)在碱性条件下,由氯化铁、氯气可制备出高铁酸钾,写出该反应的离子方程式:
______________________________________________________________________
_____________________________________________________________________
。
解析 (1)根据化合物中各元素化合价的代数和为零,可得铁元素的化合价为+6;
高铁酸钾中铁元素处于最高价态,则高铁酸钾具有强氧化性。(2)①高铁酸钾与水
反应生成 O ,同时它本身被还原生成 Fe(OH) ,反应的离子方程式为 4FeO+
2 3
10H O===4Fe(OH) (胶体)+8OH-+3O ↑。②高铁酸钾具有强氧化性,作为水处
2 3 2
理剂能起到杀菌消毒的作用,同时其还原产物为Fe(OH) 胶体,又能起到净水的作
3
用。(3)①根据元素守恒可知,X应是Na O,根据钠元素守恒,有2a=8+2b,根据
2
氧元素守恒有2a=8+b+2c,两式联立,可得b=2c。②一定温度下,向高铁酸钠
溶液中加入KOH至饱和可析出高铁酸钾,原因是该条件下高铁酸钾的溶解度小
于高铁酸钠的溶解度。(4)用氯气在碱性条件下氧化氯化铁可制备高铁酸钾,根据
得失电子守恒、原子守恒及电荷守恒,反应的离子方程式为2Fe3++3Cl +16OH-
2
===2FeO+6Cl-+8H O。
2
答案 (1)+6 强氧化性 (2)①4FeO+10H O===4Fe(OH) (胶体)+8OH-+3O ↑
2 3 2
②杀菌消毒、净水
(3)①Na O b=2c ②相同条件下高铁酸钾的溶解度小于高铁酸钠的溶解度
2
(4)2Fe3++3Cl +16OH-===2FeO+6Cl-+8H O
2 2
5.铜是与人类关系密切的有色金属。已知:常温下,在溶液中Cu2+稳定,Cu+易在
酸性条件下发生反应:2Cu+===Cu2++Cu。大多数+1价铜的化合物是难溶物,如
Cu O、CuI、CuCl、CuH等。一定条件下,在CuSO 中加入NH 反应生成氢化亚铜
2 4 5
(CuH)。
(1)已知NH 是离子化合物且所有原子都达到稀有气体的稳定结构,请写出NH 的
5 5
电子式:______________________________________________________。
(2) 写 出 CuH 在 过 量 稀 盐 酸 中 有 气 体 生 成 的 反 应 的 离 子 方 程 式 :_________________________________________________________________。
(3)将CuH溶解在适量的稀硝酸中,完成以下化学方程式:
________CuH+________HNO ===________Cu(NO ) +________H ↑+________
3 3 2 2
+________。
解析 (1)NH 的所有原子都达到稀有气体的稳定结构,即氮原子的最外层达到 8
5
电子稳定结构,所有氢原子达到2电子稳定结构,说明NH 是由NH和H-组成的
5
离子化合物,电子式为 。(2)CuH溶解在稀盐酸中,
CuH中的H失电子,盐酸中的H+得电子,产生的气体为氢气,酸性溶液中2Cu+
===Cu2++Cu,故离子方程式为2CuH+2H+===Cu2++Cu+2H ↑。(3)Cu+在酸性
2
条件下发生反应2Cu+===Cu2++Cu,稀硝酸具有强氧化性,能把铜氧化为硝酸铜
CuH具有还原性,因此二者反应生成氢气、一氧化氮气体、铜离子、H O,其化学方
2
程式为6CuH+16HNO ===6Cu(NO ) +3H ↑+4NO↑+8H O。
3 3 2 2 2
答案 (1)
(2)2CuH+2H+===Cu2++Cu+2H ↑
2
(3)6 16 6 3 4NO↑ 8H O
2