文档内容
选择题标准练(六)
1.(2024·辽宁沈阳一模)化学与人类生产、生活密切相关,下列说法中错误的是( )
A.歼-20上采用的氮化镓涂层,属于新型金属材料
B.液晶既有液体的流动性,又有类似晶体的各向异性
C.氯化钠不能使蛋白质变性,但可用作食品防腐剂
D.碳酸氢铵、碳酸氢钠可用于制作面包等食品的膨松剂
2.(2024·广西柳州三模)下列有关物质结构和性质的说法错误的是( )
A.CaH 晶体中Ca2+与H-之间的离子键,为强烈相互作用
2
B.依据价层电子对互斥理论预测,CO2-
的空间结构为三角锥形
3
C.液氧和煤油可作为火箭推进剂,液氧分子间靠范德华力凝聚在一起
D.NaCl(800.7 ℃)的熔点远高于SiCl (-68.8 ℃),原因是两者晶体类型不同
4
3.(2024·黑龙江齐齐哈尔一模)名医华佗创制的用于外科手术的麻醉药“麻沸散”中含有东莨菪碱,
其结构简式如图所示。下列关于该物质的说法错误的是 ( )
A.含有3种含氧官能团
B.碳原子的杂化方式有sp2、sp3两种
C.具有碱性,能与强酸反应
D.能发生消去反应、加聚反应
4.(2024·江西景德镇第三次质检)下列方程式能正确表示相应变化的是( )
A.草酸与酸性高锰酸钾溶液反应:2MnO- +16H++5CO2-
2Mn2++10CO ↑+8H O
4 2 4 2 2
B.空气中加热FeO:6FeO+O 2Fe O
2 3 4
C.用铜电极电解饱和食盐水,阳极有白色沉淀生成:Cu-2e-+2Cl- CuCl
2
D.向硝酸银溶液中滴加少量的氨水:Ag++4NH·H O [Ag(NH)]++4H O
3 2 3 4 2
5.(2024·山东临沂二模)噻吩、呋喃、吡咯、咪唑是五元杂环化合物,分子内所有原子共平面,结构简
式如图所示。下列说法错误的是( )
噻吩 呋喃 吡咯 咪唑
A.分子中C、O、N、S的杂化方式均相同
B.水中的溶解度:吡咯>噻吩C.分子中均存在Π6
的大π键
5
D.咪唑中N原子均可与金属离子形成配位键
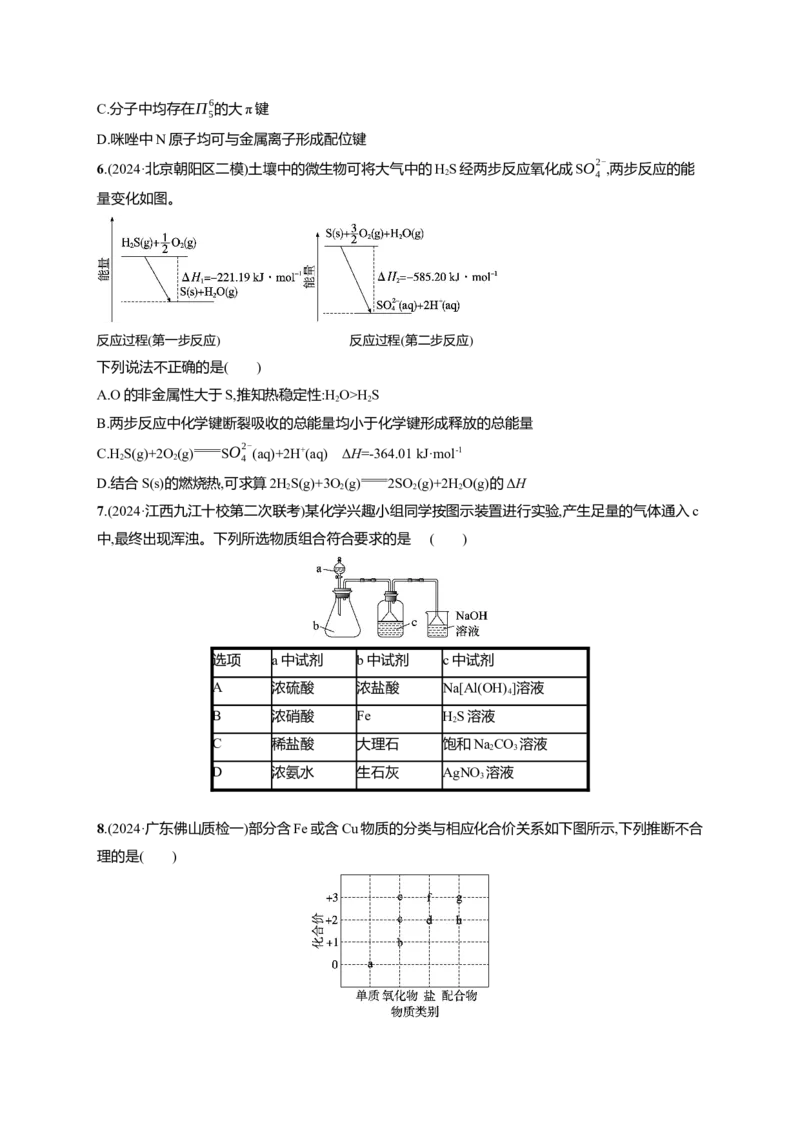
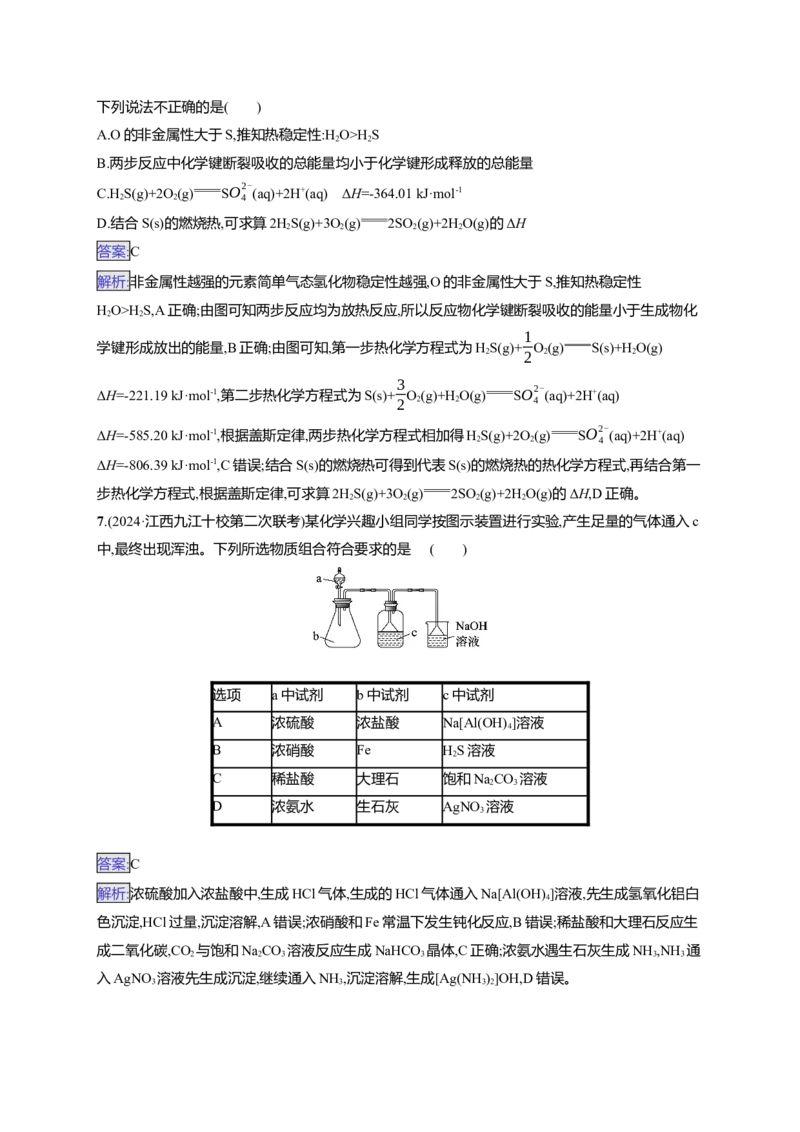
6.(2024·北京朝阳区二模)土壤中的微生物可将大气中的HS经两步反应氧化成SO2-
,两步反应的能
2 4
量变化如图。
反应过程(第一步反应) 反应过程(第二步反应)
下列说法不正确的是( )
A.O的非金属性大于S,推知热稳定性:H O>HS
2 2
B.两步反应中化学键断裂吸收的总能量均小于化学键形成释放的总能量
C.H S(g)+2O(g)
SO2-
(aq)+2H+(aq) ΔH=-364.01 kJ·mol-1
2 2 4
D.结合S(s)的燃烧热,可求算2HS(g)+3O(g) 2SO (g)+2HO(g)的ΔH
2 2 2 2
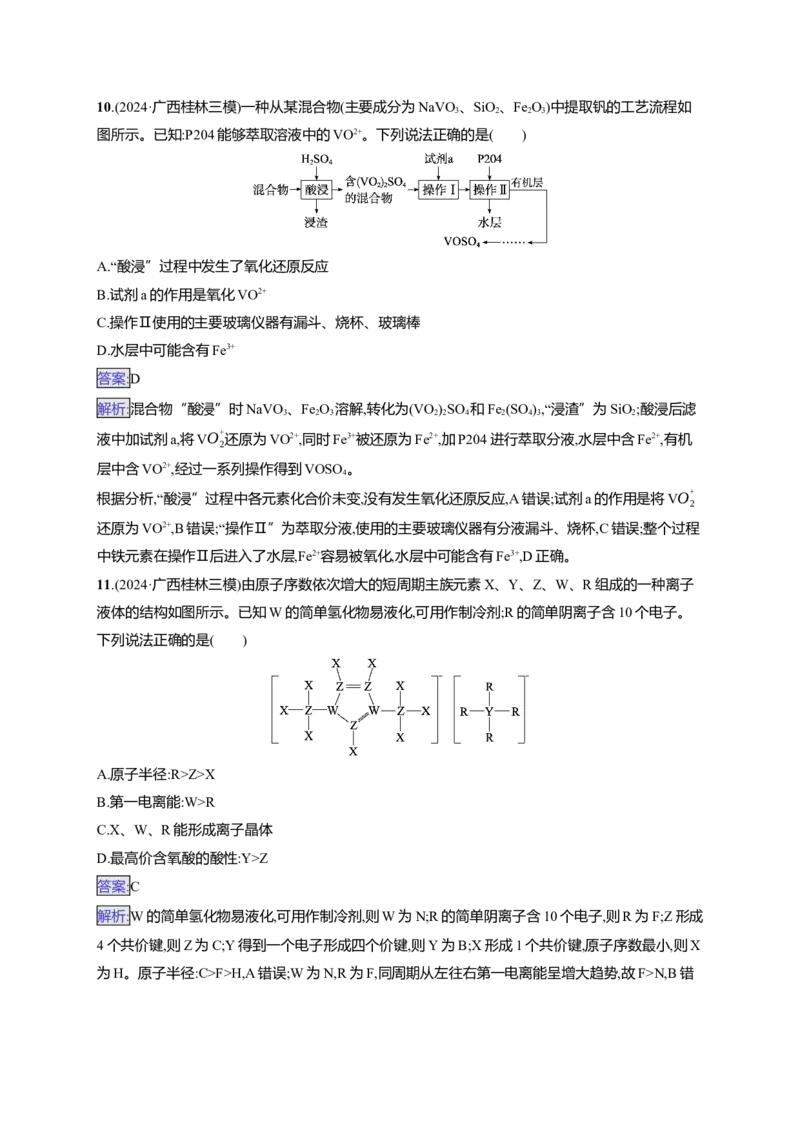
7.(2024·江西九江十校第二次联考)某化学兴趣小组同学按图示装置进行实验,产生足量的气体通入c
中,最终出现浑浊。下列所选物质组合符合要求的是 ( )
选项 a中试剂 b中试剂 c中试剂
A 浓硫酸 浓盐酸 Na[Al(OH)]溶液
4
B 浓硝酸 Fe HS溶液
2
C 稀盐酸 大理石 饱和NaCO 溶液
2 3
D 浓氨水 生石灰 AgNO 溶液
3
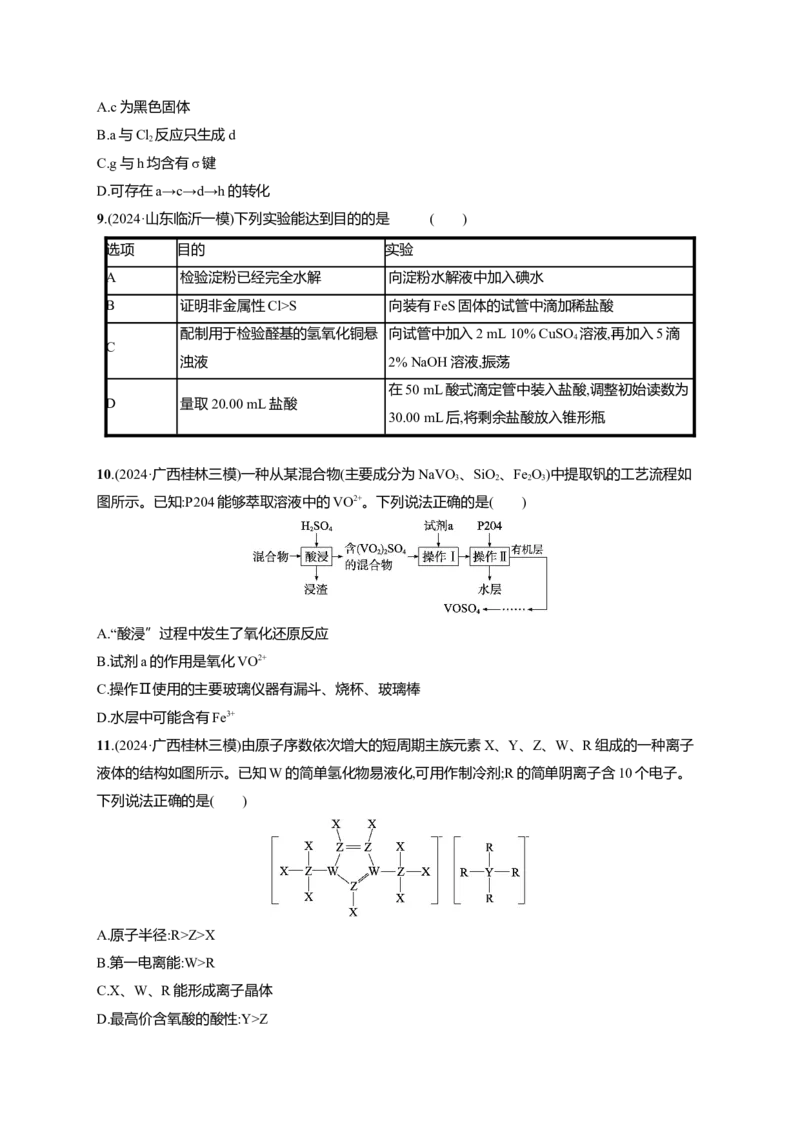
8.(2024·广东佛山质检一)部分含Fe或含Cu物质的分类与相应化合价关系如下图所示,下列推断不合
理的是( )A.c为黑色固体
B.a与Cl 反应只生成d
2
C.g与h均含有σ键
D.可存在a→c→d→h的转化
9.(2024·山东临沂一模)下列实验能达到目的的是 ( )
选项 目的 实验
A 检验淀粉已经完全水解 向淀粉水解液中加入碘水
B 证明非金属性Cl>S 向装有FeS固体的试管中滴加稀盐酸
配制用于检验醛基的氢氧化铜悬 向试管中加入2 mL 10% CuSO 溶液,再加入5滴
4
C
浊液 2% NaOH溶液,振荡
在50 mL酸式滴定管中装入盐酸,调整初始读数为
D 量取20.00 mL盐酸
30.00 mL后,将剩余盐酸放入锥形瓶
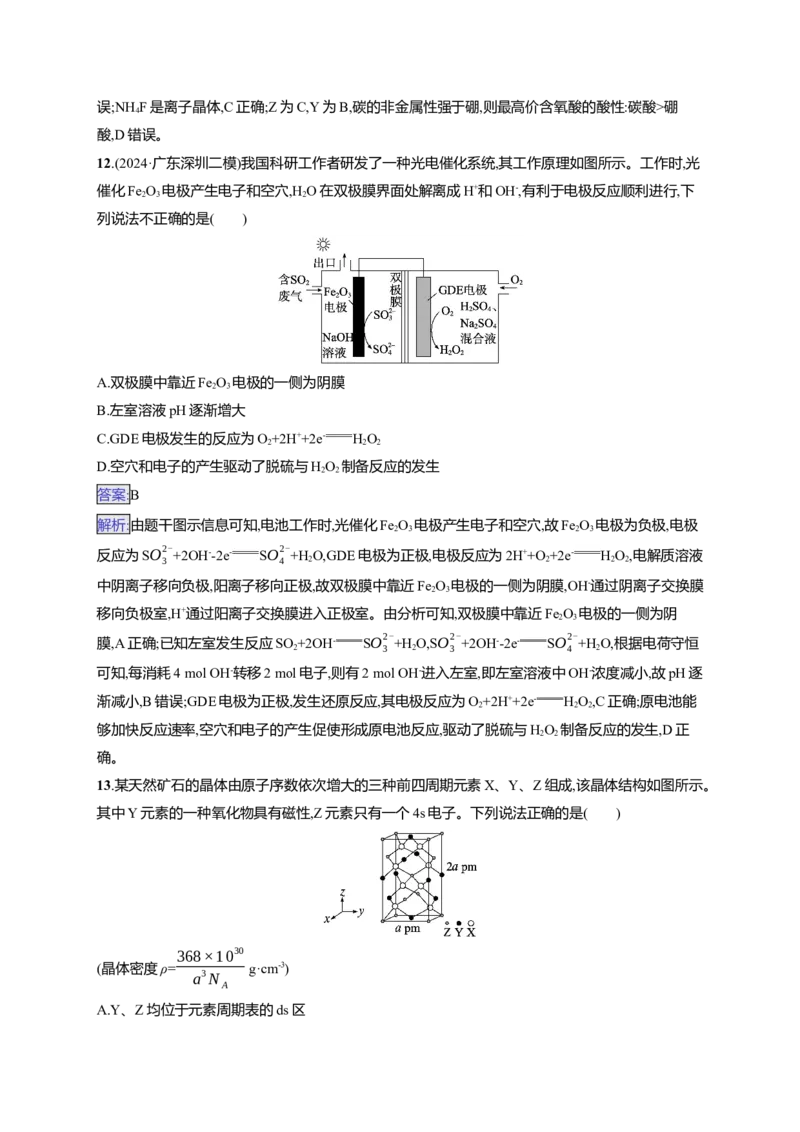
10.(2024·广西桂林三模)一种从某混合物(主要成分为NaVO 、SiO、Fe O)中提取钒的工艺流程如
3 2 2 3
图所示。已知:P204能够萃取溶液中的VO2+。下列说法正确的是( )
A.“酸浸”过程中发生了氧化还原反应
B.试剂a的作用是氧化VO2+
C.操作Ⅱ使用的主要玻璃仪器有漏斗、烧杯、玻璃棒
D.水层中可能含有Fe3+
11.(2024·广西桂林三模)由原子序数依次增大的短周期主族元素X、Y、Z、W、R组成的一种离子
液体的结构如图所示。已知W的简单氢化物易液化,可用作制冷剂;R的简单阴离子含10个电子。
下列说法正确的是( )
A.原子半径:R>Z>X
B.第一电离能:W>R
C.X、W、R能形成离子晶体
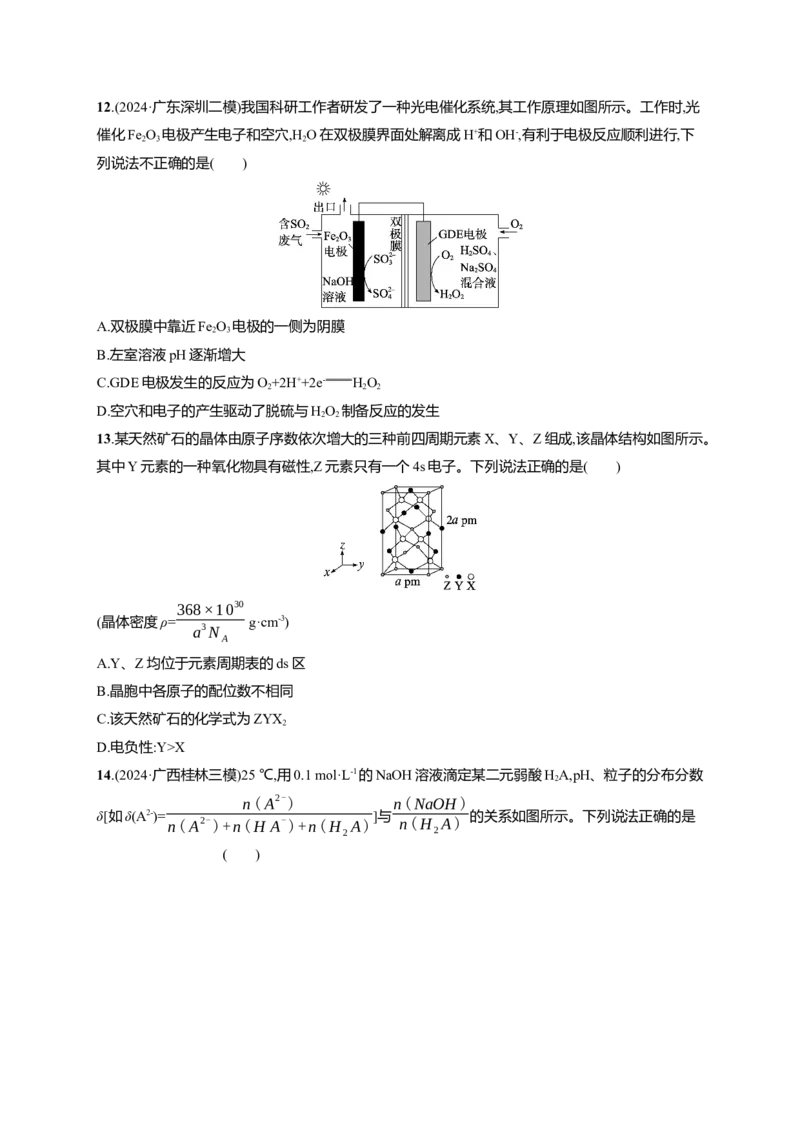
D.最高价含氧酸的酸性:Y>Z12.(2024·广东深圳二模)我国科研工作者研发了一种光电催化系统,其工作原理如图所示。工作时,光
催化Fe O 电极产生电子和空穴,H O在双极膜界面处解离成H+和OH-,有利于电极反应顺利进行,下
2 3 2
列说法不正确的是( )
A.双极膜中靠近Fe O 电极的一侧为阴膜
2 3
B.左室溶液pH逐渐增大
C.GDE电极发生的反应为O+2H++2e- HO
2 2 2
D.空穴和电子的产生驱动了脱硫与HO 制备反应的发生
2 2
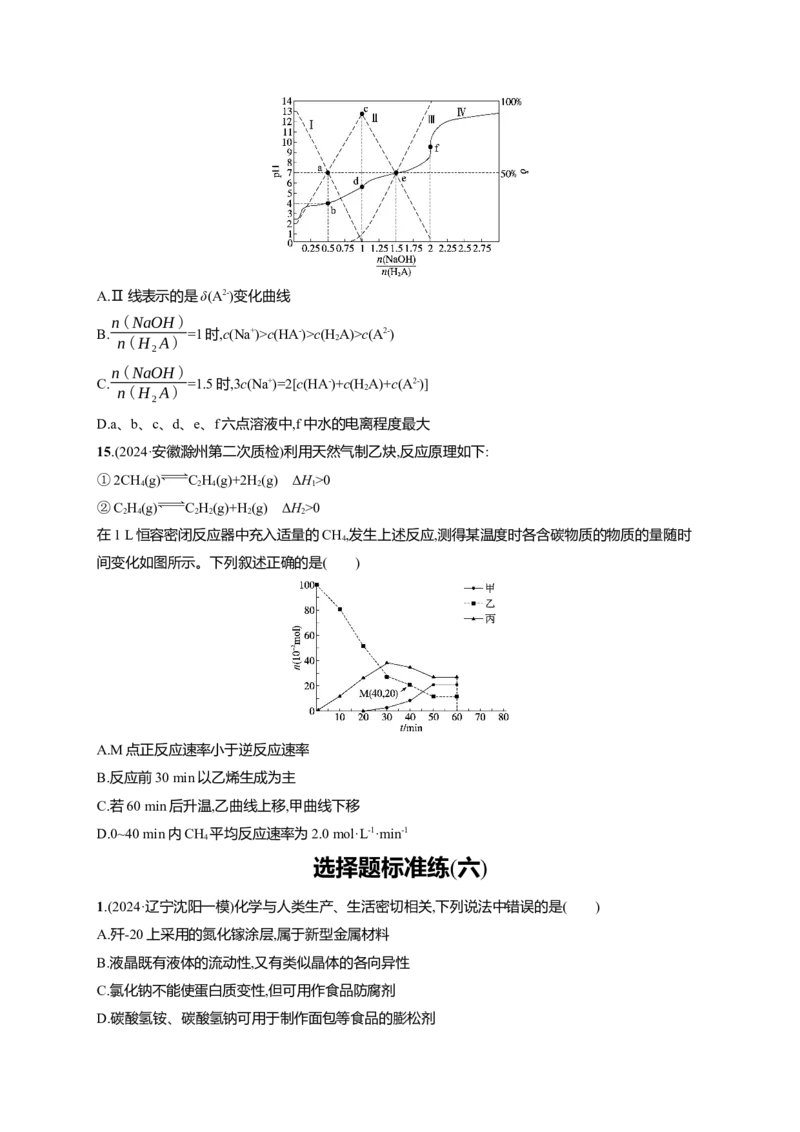
13.某天然矿石的晶体由原子序数依次增大的三种前四周期元素X、Y、Z组成,该晶体结构如图所示。
其中Y元素的一种氧化物具有磁性,Z元素只有一个4s电子。下列说法正确的是( )
368×1030
(晶体密度ρ= g·cm-3)
a3N
A
A.Y、Z均位于元素周期表的ds区
B.晶胞中各原子的配位数不相同
C.该天然矿石的化学式为ZYX
2
D.电负性:Y>X
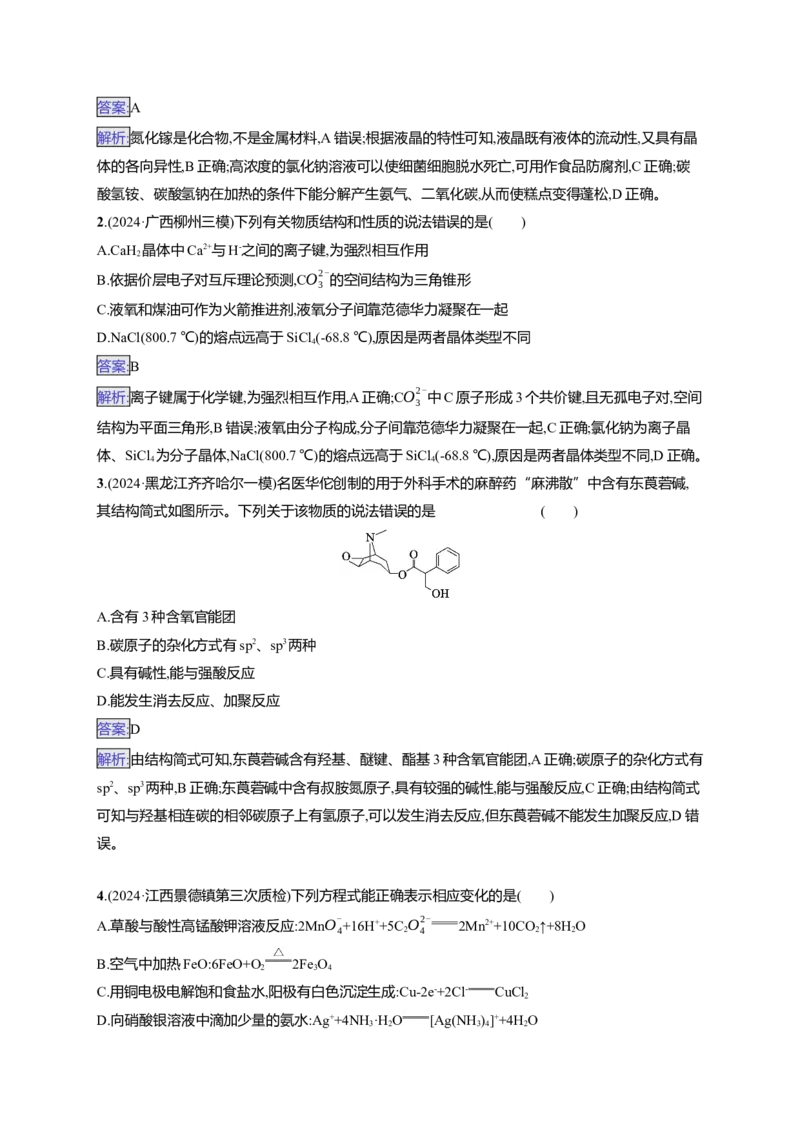
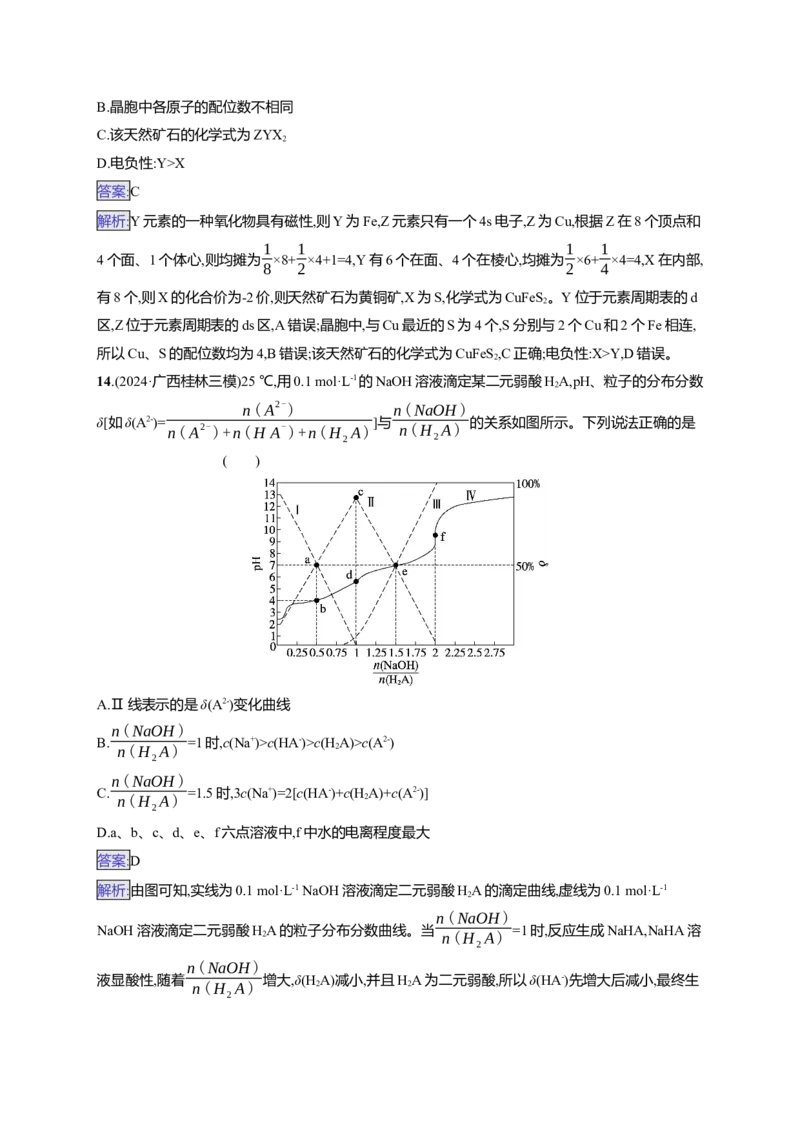
14.(2024·广西桂林三模)25 ℃,用0.1 mol·L-1的NaOH溶液滴定某二元弱酸HA,pH、粒子的分布分数
2
n(A2-) n(NaOH)
δ[如δ(A2-)= ]与 的关系如图所示。下列说法正确的是
n(A2-)+n(H A-)+n(H A) n(H A)
2 2
( )A.Ⅱ线表示的是δ(A2-)变化曲线
n(NaOH)
B. =1时,c(Na+)>c(HA-)>c(H A)>c(A2-)
n(H A) 2
2
n(NaOH)
C. =1.5时,3c(Na+)=2[c(HA-)+c(H A)+c(A2-)]
n(H A) 2
2
D.a、b、c、d、e、f六点溶液中,f中水的电离程度最大
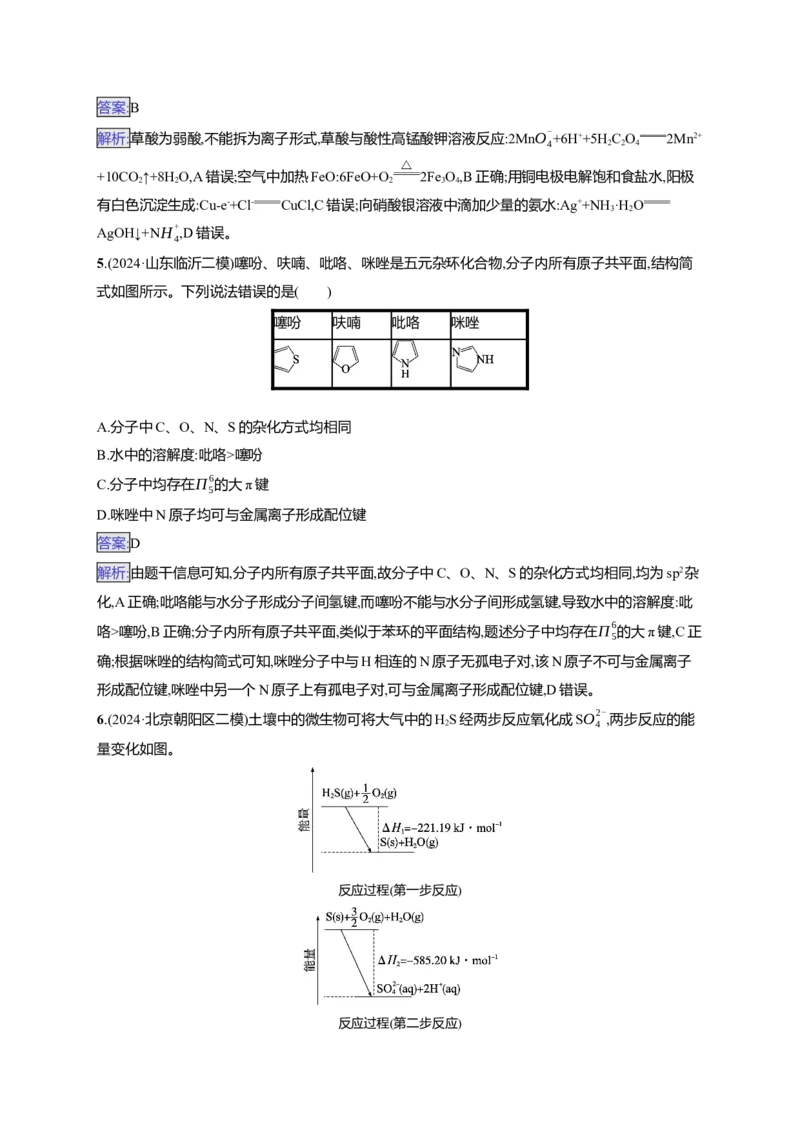
15.(2024·安徽滁州第二次质检)利用天然气制乙炔,反应原理如下:
①2CH(g) C H(g)+2H(g) ΔH>0
4 2 4 2 1
②C H(g) C H(g)+H(g) ΔH>0
2 4 2 2 2 2
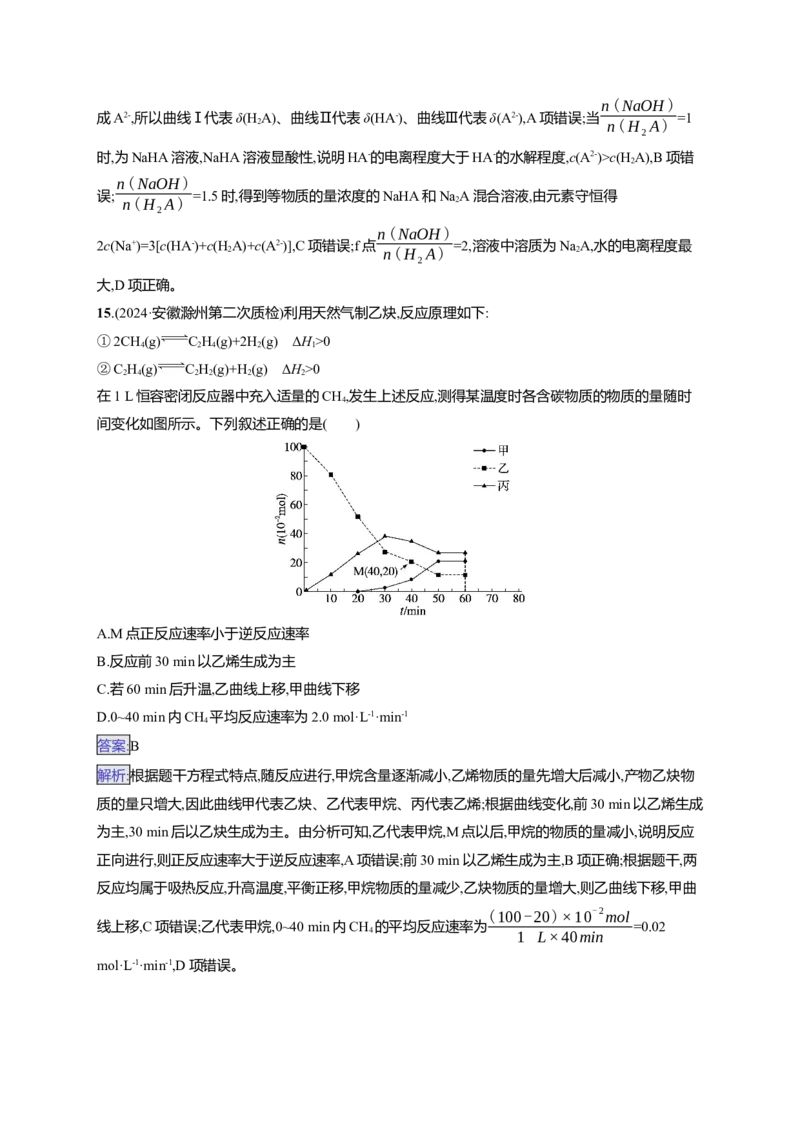
在1 L恒容密闭反应器中充入适量的CH,发生上述反应,测得某温度时各含碳物质的物质的量随时
4
间变化如图所示。下列叙述正确的是( )
A.M点正反应速率小于逆反应速率
B.反应前30 min以乙烯生成为主
C.若60 min后升温,乙曲线上移,甲曲线下移
D.0~40 min内CH 平均反应速率为2.0 mol·L-1·min-1
4
选择题标准练(六)
1.(2024·辽宁沈阳一模)化学与人类生产、生活密切相关,下列说法中错误的是( )
A.歼-20上采用的氮化镓涂层,属于新型金属材料
B.液晶既有液体的流动性,又有类似晶体的各向异性
C.氯化钠不能使蛋白质变性,但可用作食品防腐剂
D.碳酸氢铵、碳酸氢钠可用于制作面包等食品的膨松剂答案:A
解析:氮化镓是化合物,不是金属材料,A错误;根据液晶的特性可知,液晶既有液体的流动性,又具有晶
体的各向异性,B正确;高浓度的氯化钠溶液可以使细菌细胞脱水死亡,可用作食品防腐剂,C正确;碳
酸氢铵、碳酸氢钠在加热的条件下能分解产生氨气、二氧化碳,从而使糕点变得蓬松,D正确。
2.(2024·广西柳州三模)下列有关物质结构和性质的说法错误的是( )
A.CaH 晶体中Ca2+与H-之间的离子键,为强烈相互作用
2
B.依据价层电子对互斥理论预测,CO2-
的空间结构为三角锥形
3
C.液氧和煤油可作为火箭推进剂,液氧分子间靠范德华力凝聚在一起
D.NaCl(800.7 ℃)的熔点远高于SiCl (-68.8 ℃),原因是两者晶体类型不同
4
答案:B
解析:离子键属于化学键,为强烈相互作用,A正确;CO2-
中C原子形成3个共价键,且无孤电子对,空间
3
结构为平面三角形,B错误;液氧由分子构成,分子间靠范德华力凝聚在一起,C正确;氯化钠为离子晶
体、SiCl 为分子晶体,NaCl(800.7 ℃)的熔点远高于SiCl (-68.8 ℃),原因是两者晶体类型不同,D正确。
4 4
3.(2024·黑龙江齐齐哈尔一模)名医华佗创制的用于外科手术的麻醉药“麻沸散”中含有东莨菪碱,
其结构简式如图所示。下列关于该物质的说法错误的是 ( )
A.含有3种含氧官能团
B.碳原子的杂化方式有sp2、sp3两种
C.具有碱性,能与强酸反应
D.能发生消去反应、加聚反应
答案:D
解析:由结构简式可知,东莨菪碱含有羟基、醚键、酯基3种含氧官能团,A正确;碳原子的杂化方式有
sp2、sp3两种,B正确;东莨菪碱中含有叔胺氮原子,具有较强的碱性,能与强酸反应,C正确;由结构简式
可知与羟基相连碳的相邻碳原子上有氢原子,可以发生消去反应,但东莨菪碱不能发生加聚反应,D错
误。
4.(2024·江西景德镇第三次质检)下列方程式能正确表示相应变化的是( )
A.草酸与酸性高锰酸钾溶液反应:2MnO- +16H++5CO2-
2Mn2++10CO ↑+8H O
4 2 4 2 2
B.空气中加热FeO:6FeO+O 2Fe O
2 3 4
C.用铜电极电解饱和食盐水,阳极有白色沉淀生成:Cu-2e-+2Cl- CuCl
2
D.向硝酸银溶液中滴加少量的氨水:Ag++4NH·H O [Ag(NH)]++4H O
3 2 3 4 2答案:B
解析:草酸为弱酸,不能拆为离子形式,草酸与酸性高锰酸钾溶液反应:2MnO-
+6H++5H C O 2Mn2+
4 2 2 4
+10CO ↑+8H O,A错误;空气中加热FeO:6FeO+O 2Fe O,B正确;用铜电极电解饱和食盐水,阳极
2 2 2 3 4
有白色沉淀生成:Cu-e-+Cl- CuCl,C错误;向硝酸银溶液中滴加少量的氨水:Ag++NH·H O
3 2
AgOH↓+NH+
,D错误。
4
5.(2024·山东临沂二模)噻吩、呋喃、吡咯、咪唑是五元杂环化合物,分子内所有原子共平面,结构简
式如图所示。下列说法错误的是( )
噻吩 呋喃 吡咯 咪唑
A.分子中C、O、N、S的杂化方式均相同
B.水中的溶解度:吡咯>噻吩
C.分子中均存在Π6
的大π键
5
D.咪唑中N原子均可与金属离子形成配位键
答案:D
解析:由题干信息可知,分子内所有原子共平面,故分子中C、O、N、S的杂化方式均相同,均为sp2杂
化,A正确;吡咯能与水分子形成分子间氢键,而噻吩不能与水分子间形成氢键,导致水中的溶解度:吡
咯>噻吩,B正确;分子内所有原子共平面,类似于苯环的平面结构,题述分子中均存在Π6
的大π键,C正
5
确;根据咪唑的结构简式可知,咪唑分子中与H相连的N原子无孤电子对,该N原子不可与金属离子
形成配位键,咪唑中另一个N原子上有孤电子对,可与金属离子形成配位键,D错误。
6.(2024·北京朝阳区二模)土壤中的微生物可将大气中的HS经两步反应氧化成SO2-
,两步反应的能
2 4
量变化如图。
反应过程(第一步反应)
反应过程(第二步反应)下列说法不正确的是( )
A.O的非金属性大于S,推知热稳定性:H O>HS
2 2
B.两步反应中化学键断裂吸收的总能量均小于化学键形成释放的总能量
C.H S(g)+2O(g)
SO2-
(aq)+2H+(aq) ΔH=-364.01 kJ·mol-1
2 2 4
D.结合S(s)的燃烧热,可求算2HS(g)+3O(g) 2SO (g)+2HO(g)的ΔH
2 2 2 2
答案:C
解析:非金属性越强的元素简单气态氢化物稳定性越强,O的非金属性大于S,推知热稳定性
HO>HS,A正确;由图可知两步反应均为放热反应,所以反应物化学键断裂吸收的能量小于生成物化
2 2
1
学键形成放出的能量,B正确;由图可知,第一步热化学方程式为HS(g)+ O(g) S(s)+H O(g)
2 2 2 2
3
ΔH=-221.19 kJ·mol-1,第二步热化学方程式为S(s)+ O(g)+HO(g)
SO2-
(aq)+2H+(aq)
2 2 2 4
ΔH=-585.20 kJ·mol-1,根据盖斯定律,两步热化学方程式相加得HS(g)+2O(g)
SO2-
(aq)+2H+(aq)
2 2 4
ΔH=-806.39 kJ·mol-1,C错误;结合S(s)的燃烧热可得到代表S(s)的燃烧热的热化学方程式,再结合第一
步热化学方程式,根据盖斯定律,可求算2HS(g)+3O(g) 2SO (g)+2HO(g)的ΔH,D正确。
2 2 2 2
7.(2024·江西九江十校第二次联考)某化学兴趣小组同学按图示装置进行实验,产生足量的气体通入c
中,最终出现浑浊。下列所选物质组合符合要求的是 ( )
选项 a中试剂 b中试剂 c中试剂
A 浓硫酸 浓盐酸 Na[Al(OH)]溶液
4
B 浓硝酸 Fe HS溶液
2
C 稀盐酸 大理石 饱和NaCO 溶液
2 3
D 浓氨水 生石灰 AgNO 溶液
3
答案:C
解析:浓硫酸加入浓盐酸中,生成HCl气体,生成的HCl气体通入Na[Al(OH)]溶液,先生成氢氧化铝白
4
色沉淀,HCl过量,沉淀溶解,A错误;浓硝酸和Fe常温下发生钝化反应,B错误;稀盐酸和大理石反应生
成二氧化碳,CO 与饱和NaCO 溶液反应生成NaHCO 晶体,C正确;浓氨水遇生石灰生成NH ,NH 通
2 2 3 3 3 3
入AgNO 溶液先生成沉淀,继续通入NH ,沉淀溶解,生成[Ag(NH)]OH,D错误。
3 3 3 28.(2024·广东佛山质检一)部分含Fe或含Cu物质的分类与相应化合价关系如下图所示,下列推断不合
理的是( )
A.c为黑色固体
B.a与Cl 反应只生成d
2
C.g与h均含有σ键
D.可存在a→c→d→h的转化
答案:B
解析:由图可知,a为铁或铜、b为氧化亚铜、c为氧化亚铁或氧化铜、d为亚铁盐或铜盐、e为氧化铁、
f为铁盐、g为+3价铁元素的配合物、h为+2价铁元素或铜元素的配合物。氧化亚铁或氧化铜均为
黑色固体,A正确;铁在氯气中燃烧只能生成氯化铁,不能生成氯化亚铁,B错误;配合物中的配位键都
属于σ键,C正确;铜与氧气共热生成氧化铜,氧化铜溶于酸生成铜盐,铜盐与氨水反应生成四氨合铜离
子,则铜元素中存在a→c→d→h的转化,D正确。
9.(2024·山东临沂一模)下列实验能达到目的的是 ( )
选项 目的 实验
A 检验淀粉已经完全水解 向淀粉水解液中加入碘水
B 证明非金属性Cl>S 向装有FeS固体的试管中滴加稀盐酸
配制用于检验醛基的氢氧化铜悬 向试管中加入2 mL 10% CuSO 溶液,再加入5滴
4
C
浊液 2% NaOH溶液,振荡
在50 mL酸式滴定管中装入盐酸,调整初始读数为
D 量取20.00 mL盐酸
30.00 mL后,将剩余盐酸放入锥形瓶
答案:A
解析:向淀粉水解液中加入碘水,溶液不变蓝色说明淀粉已经完全水解,A正确;元素的非金属性与氢
化物的稳定性有关,与氢化物的酸性无关,向装有硫化亚铁固体的试管中滴加稀盐酸能用于比较盐酸
和氢硫酸的酸性强弱,但不能比较氯元素和硫元素的非金属性强弱,B错误;配制用于检验醛基的氢氧
化铜悬浊液时,应向过量的氢氧化钠溶液中加入硫酸铜溶液,C错误;酸式滴定管的实际容积大于标定
容积,所以量取20.00 mL盐酸时不能将滴定管中的盐酸完全放入锥形瓶中,D错误。10.(2024·广西桂林三模)一种从某混合物(主要成分为NaVO 、SiO、Fe O)中提取钒的工艺流程如
3 2 2 3
图所示。已知:P204能够萃取溶液中的VO2+。下列说法正确的是( )
A.“酸浸”过程中发生了氧化还原反应
B.试剂a的作用是氧化VO2+
C.操作Ⅱ使用的主要玻璃仪器有漏斗、烧杯、玻璃棒
D.水层中可能含有Fe3+
答案:D
解析:混合物“酸浸”时NaVO 、Fe O 溶解,转化为(VO )SO 和Fe (SO ),“浸渣”为SiO;酸浸后滤
3 2 3 2 2 4 2 4 3 2
液中加试剂a,将VO+
还原为VO2+,同时Fe3+被还原为Fe2+,加P204进行萃取分液,水层中含Fe2+,有机
2
层中含VO2+,经过一系列操作得到VOSO。
4
根据分析,“酸浸”过程中各元素化合价未变,没有发生氧化还原反应,A错误;试剂a的作用是将VO+
2
还原为VO2+,B错误;“操作Ⅱ”为萃取分液,使用的主要玻璃仪器有分液漏斗、烧杯,C错误;整个过程
中铁元素在操作Ⅱ后进入了水层,Fe2+容易被氧化,水层中可能含有Fe3+,D正确。
11.(2024·广西桂林三模)由原子序数依次增大的短周期主族元素X、Y、Z、W、R组成的一种离子
液体的结构如图所示。已知W的简单氢化物易液化,可用作制冷剂;R的简单阴离子含10个电子。
下列说法正确的是( )
A.原子半径:R>Z>X
B.第一电离能:W>R
C.X、W、R能形成离子晶体
D.最高价含氧酸的酸性:Y>Z
答案:C
解析:W的简单氢化物易液化,可用作制冷剂,则W为N;R的简单阴离子含10个电子,则R为F;Z形成
4个共价键,则Z为C;Y得到一个电子形成四个价键,则Y为B;X形成1个共价键,原子序数最小,则X
为H。原子半径:C>F>H,A错误;W为N,R为F,同周期从左往右第一电离能呈增大趋势,故F>N,B错误;NHF是离子晶体,C正确;Z为C,Y为B,碳的非金属性强于硼,则最高价含氧酸的酸性:碳酸>硼
4
酸,D错误。
12.(2024·广东深圳二模)我国科研工作者研发了一种光电催化系统,其工作原理如图所示。工作时,光
催化Fe O 电极产生电子和空穴,H O在双极膜界面处解离成H+和OH-,有利于电极反应顺利进行,下
2 3 2
列说法不正确的是( )
A.双极膜中靠近Fe O 电极的一侧为阴膜
2 3
B.左室溶液pH逐渐增大
C.GDE电极发生的反应为O+2H++2e- HO
2 2 2
D.空穴和电子的产生驱动了脱硫与HO 制备反应的发生
2 2
答案:B
解析:由题干图示信息可知,电池工作时,光催化Fe O 电极产生电子和空穴,故Fe O 电极为负极,电极
2 3 2 3
反应为SO2-
+2OH--2e-
SO2-
+H O,GDE电极为正极,电极反应为2H++O +2e- HO,电解质溶液
3 4 2 2 2 2
中阴离子移向负极,阳离子移向正极,故双极膜中靠近Fe O 电极的一侧为阴膜,OH-通过阴离子交换膜
2 3
移向负极室,H+通过阳离子交换膜进入正极室。由分析可知,双极膜中靠近Fe O 电极的一侧为阴
2 3
膜,A正确;已知左室发生反应SO +2OH-
SO2-
+H
O,SO2-
+2OH--2e-
SO2-
+H O,根据电荷守恒
2 3 2 3 4 2
可知,每消耗4 mol OH-转移2 mol电子,则有2 mol OH-进入左室,即左室溶液中OH-浓度减小,故pH逐
渐减小,B错误;GDE电极为正极,发生还原反应,其电极反应为O+2H++2e- HO,C正确;原电池能
2 2 2
够加快反应速率,空穴和电子的产生促使形成原电池反应,驱动了脱硫与HO 制备反应的发生,D正
2 2
确。
13.某天然矿石的晶体由原子序数依次增大的三种前四周期元素X、Y、Z组成,该晶体结构如图所示。
其中Y元素的一种氧化物具有磁性,Z元素只有一个4s电子。下列说法正确的是( )
368×1030
(晶体密度ρ= g·cm-3)
a3N
A
A.Y、Z均位于元素周期表的ds区B.晶胞中各原子的配位数不相同
C.该天然矿石的化学式为ZYX
2
D.电负性:Y>X
答案:C
解析:Y元素的一种氧化物具有磁性,则Y为Fe,Z元素只有一个4s电子,Z为Cu,根据Z在8个顶点和
1 1 1 1
4个面、1个体心,则均摊为 ×8+ ×4+1=4,Y有6个在面、4个在棱心,均摊为 ×6+ ×4=4,X在内部,
8 2 2 4
有8个,则X的化合价为-2价,则天然矿石为黄铜矿,X为S,化学式为CuFeS。Y位于元素周期表的d
2
区,Z位于元素周期表的ds区,A错误;晶胞中,与Cu最近的S为4个,S分别与2个Cu和2个Fe相连,
所以Cu、S的配位数均为4,B错误;该天然矿石的化学式为CuFeS,C正确;电负性:X>Y,D错误。
2
14.(2024·广西桂林三模)25 ℃,用0.1 mol·L-1的NaOH溶液滴定某二元弱酸HA,pH、粒子的分布分数
2
n(A2-) n(NaOH)
δ[如δ(A2-)= ]与 的关系如图所示。下列说法正确的是
n(A2-)+n(H A-)+n(H A) n(H A)
2 2
( )
A.Ⅱ线表示的是δ(A2-)变化曲线
n(NaOH)
B. =1时,c(Na+)>c(HA-)>c(H A)>c(A2-)
n(H A) 2
2
n(NaOH)
C. =1.5时,3c(Na+)=2[c(HA-)+c(H A)+c(A2-)]
n(H A) 2
2
D.a、b、c、d、e、f六点溶液中,f中水的电离程度最大
答案:D
解析:由图可知,实线为0.1 mol·L-1 NaOH溶液滴定二元弱酸HA的滴定曲线,虚线为0.1 mol·L-1
2
n(NaOH)
NaOH溶液滴定二元弱酸HA的粒子分布分数曲线。当 =1时,反应生成NaHA,NaHA溶
2 n(H A)
2
n(NaOH)
液显酸性,随着 增大,δ(H A)减小,并且HA为二元弱酸,所以δ(HA-)先增大后减小,最终生
n(H A) 2 2
2n(NaOH)
成A2-,所以曲线Ⅰ代表δ(H A)、曲线Ⅱ代表δ(HA-)、曲线Ⅲ代表δ(A2-),A项错误;当 =1
2 n(H A)
2
时,为NaHA溶液,NaHA溶液显酸性,说明HA-的电离程度大于HA-的水解程度,c(A2-)>c(H A),B项错
2
n(NaOH)
误; =1.5时,得到等物质的量浓度的NaHA和NaA混合溶液,由元素守恒得
n(H A) 2
2
n(NaOH)
2c(Na+)=3[c(HA-)+c(H A)+c(A2-)],C项错误;f点 =2,溶液中溶质为NaA,水的电离程度最
2 n(H A) 2
2
大,D项正确。
15.(2024·安徽滁州第二次质检)利用天然气制乙炔,反应原理如下:
①2CH(g) C H(g)+2H(g) ΔH>0
4 2 4 2 1
②C H(g) C H(g)+H(g) ΔH>0
2 4 2 2 2 2
在1 L恒容密闭反应器中充入适量的CH,发生上述反应,测得某温度时各含碳物质的物质的量随时
4
间变化如图所示。下列叙述正确的是( )
A.M点正反应速率小于逆反应速率
B.反应前30 min以乙烯生成为主
C.若60 min后升温,乙曲线上移,甲曲线下移
D.0~40 min内CH 平均反应速率为2.0 mol·L-1·min-1
4
答案:B
解析:根据题干方程式特点,随反应进行,甲烷含量逐渐减小,乙烯物质的量先增大后减小,产物乙炔物
质的量只增大,因此曲线甲代表乙炔、乙代表甲烷、丙代表乙烯;根据曲线变化,前30 min以乙烯生成
为主,30 min后以乙炔生成为主。由分析可知,乙代表甲烷,M点以后,甲烷的物质的量减小,说明反应
正向进行,则正反应速率大于逆反应速率,A项错误;前30 min以乙烯生成为主,B项正确;根据题干,两
反应均属于吸热反应,升高温度,平衡正移,甲烷物质的量减少,乙炔物质的量增大,则乙曲线下移,甲曲
(100-20)×10-2mol
线上移,C项错误;乙代表甲烷,0~40 min内CH 的平均反应速率为 =0.02
4 1 L×40min
mol·L-1·min-1,D项错误。