文档内容
热点强化 6 利用溶解度进行物质分离
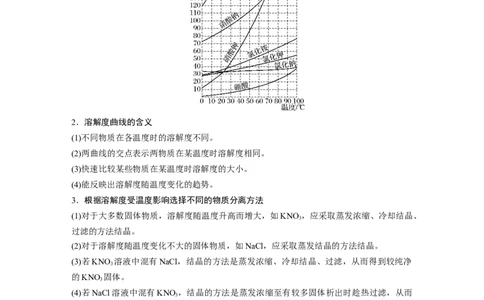
1.常见物质的溶解度曲线
2.溶解度曲线的含义
(1)不同物质在各温度时的溶解度不同。
(2)两曲线的交点表示两物质在某温度时溶解度相同。
(3)快速比较某些物质在某温度时溶解度的大小。
(4)能反映出溶解度随温度变化的趋势。
3.根据溶解度受温度影响选择不同的物质分离方法
(1)对于大多数固体物质,溶解度随温度升高而增大,如KNO ,应采取蒸发浓缩、冷却结晶、
3
过滤的方法结晶。
(2)对于溶解度随温度变化不大的固体物质,如NaCl,应采取蒸发结晶的方法结晶。
(3)若KNO 溶液中混有NaCl,结晶的方法是蒸发浓缩、冷却结晶、过滤,从而得到较纯净
3
的KNO 固体。
3
(4)若NaCl溶液中混有KNO ,结晶的方法是蒸发浓缩至有较多固体析出时趁热过滤,从而
3
得到较纯净的NaCl固体。
(5)带有结晶水的晶体,一般采取蒸发浓缩、冷却结晶的方法。
1.如图是MgSO 、NaCl的溶解度曲线。下列说法正确的是( )
4A.MgSO 的溶解度随温度升高而增大
4
B.NaCl的溶解度比MgSO 的溶解度大
4
C.在t ℃时,MgSO 的饱和溶液通过降温或升温均能析出晶体
2 4
D.把MgSO 饱和溶液的温度从t ℃降至t ℃时,会有晶体析出
4 3 2
2.有关物质的溶解度如图所示。向含NaCr O 的滤液中加入适量KCl,蒸发浓缩,冷却结
2 2 7
晶,过滤得到KCr O 固体。冷却到________(填字母)得到的KCr O 固体产品最多。
2 2 7 2 2 7
A.80 ℃ B.60 ℃ C.40 ℃ D.10 ℃
3.硫酸锰在不同温度下结晶可分别得到MnSO ·7H O、MnSO ·5H O和MnSO ·H O。硫酸
4 2 4 2 4 2
锰在不同温度下的溶解度和该温度范围内析出晶体的组成如图所示。
从过滤所得的滤液中获得较高纯度MnSO ·H O的操作是控制温度在80~90 ℃之间蒸发结
4 2
晶,________,使固体MnSO ·H O与溶液分离,________________、真空干燥。
4 2
4.已知CoCl 的溶解度曲线如图所示。向碱式碳酸钴沉淀中加入足量稀盐酸边加热边搅拌
2
至完全溶解后,需趁热过滤的原因是_______________________________________________
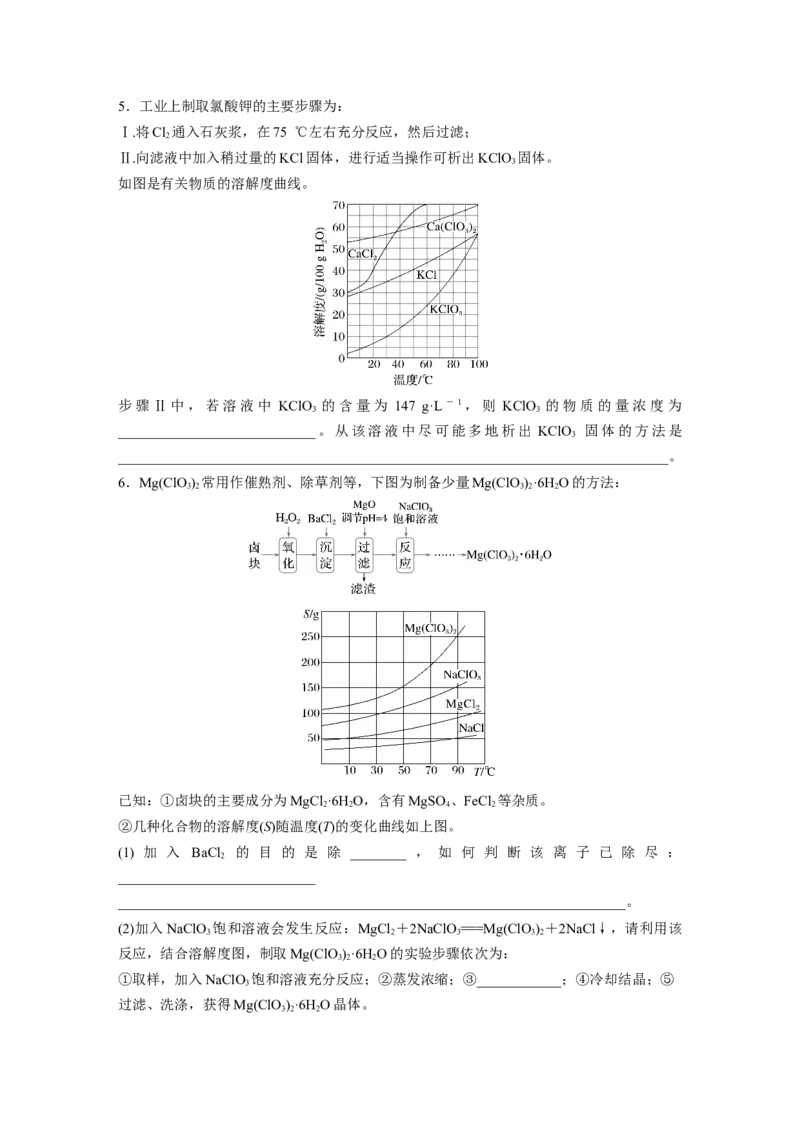
________________________。5.工业上制取氯酸钾的主要步骤为:
Ⅰ.将Cl 通入石灰浆,在75 ℃左右充分反应,然后过滤;
2
Ⅱ.向滤液中加入稍过量的KCl固体,进行适当操作可析出KClO 固体。
3
如图是有关物质的溶解度曲线。
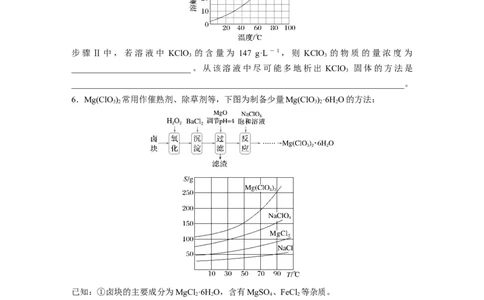
步骤Ⅱ中,若溶液中 KClO 的含量为 147 g·L-1,则 KClO 的物质的量浓度为
3 3
____________________________。从该溶液中尽可能多地析出 KClO 固体的方法是
3
______________________________________________________________________________。
6.Mg(ClO) 常用作催熟剂、除草剂等,下图为制备少量Mg(ClO)·6H O的方法:
3 2 3 2 2
已知:①卤块的主要成分为MgCl ·6H O,含有MgSO 、FeCl 等杂质。
2 2 4 2
②几种化合物的溶解度(S)随温度(T)的变化曲线如上图。
(1) 加 入 BaCl 的 目 的 是 除 ________ , 如 何 判 断 该 离 子 已 除 尽 :
2
____________________________
________________________________________________________________________。
(2)加入NaClO 饱和溶液会发生反应:MgCl +2NaClO===Mg(ClO) +2NaCl↓,请利用该
3 2 3 3 2
反应,结合溶解度图,制取Mg(ClO)·6H O的实验步骤依次为:
3 2 2
①取样,加入NaClO 饱和溶液充分反应;②蒸发浓缩;③____________;④冷却结晶;⑤
3
过滤、洗涤,获得Mg(ClO)·6H O晶体。
3 2 2