文档内容
微专题突破5 无机物的性质、转化与应用一
一、选择题
1.(2024·江苏盐城市高三期中)水是生命之源,寻找火星水冰是“祝融”号火星车的任务之一、
下列关于水的说法正确的是
A.属于两性氧化物 B.既有氧化性又有还原性
C.与HO 互为同素异形体 D.不属于电解质
2 2
2.(2023·扬州调研)氯气及其化合物在生产和生活中具有重要应用。下列有关说法正确的是
A.ClO中氯原子的杂化轨道类型为sp3
B.为了增强KMnO 溶液的氧化性,可选用浓盐酸进行酸化
4
C.氯气有毒,在通风棚中制备氯气可以消除氯气的污染
D.50 mL 12 mol·L-1浓盐酸与足量MnO 共热反应,可生成0.15 mol Cl
2 2
的
3.(2024·南通市如皋2月)下列物质 结构与性质或性质与用途具有对应关系的是
A.N 中化学键非常牢固,可用作保护气
2
B.乙醇易溶于水,可用于消毒杀菌
C.浓硫酸具有强氧化性,可用于与CaF 反应制HF
2
D.SO 是极性分子,可用于漂白纸浆
2
4.(2024·南通市如皋二模)下列化学反应表示正确的是
A.电解饱和食盐水制备Cl 的离子方程式:2Cl-+2H+====Cl↑+H↑
2 2 2
B.将氯水在强光下照射的化学方程式:2HClO====Cl↑+2HO
2 2
C.氨气检验Cl 泄露的化学方程式:3Cl+8NH =N+6NH Cl
2 2 3 2 4
D.Cl 处理含氰碱性废水的离子方程式:5Cl+2CN-+4HO=10Cl-+N↑+2CO↑+8H+
2 2 2 2 2
5.(2022·江苏)我国古代就掌握了青铜(铜-锡合金)的冶炼、加工技术,制造出许多精美的青铜
器;Pb、PbO 是铅蓄电池的电极材料,不同铅化合物一般具有不同颜色,历史上曾广泛用作颜料。下列
2
物质性质与用途具有对应关系的是
A.石墨能导电,可用作润滑剂
B.单晶硅熔点高,可用作半导体材料
C.青铜比纯铜熔点低、硬度大,古代用青铜铸剑
D.含铅化合物颜色丰富,可用作电极材料
6.(2023·海安高级中学高三下学期模拟)下列物质性质与用途具有对应关系的是
A.金属Li密度小,可用作电极材料 B.BeO硬度大,可制作耐高温的坩埚
C.HC O 有还原性,可用作沉淀剂、络合剂 D.聚四氟乙烯耐酸碱腐蚀,可制作滴定管活塞
2 2 4
7.(2024·江苏省盐城阶段练习)物质转化在工业生产中有重要作用。下列说法正确的是
A.工业生产盐酸:H 2 +Cl 2 ======2HCl B.工业生产硫酸:FeS 2O — 2 → —\s\up 4()SO 3 H —— 2 → O\s\up
4()HSO
2 4
C.工业生产硝酸:N 2 点 — 燃 → —\s\up 4()NO 2H —— 2 → O\s\up 4()HNO 3 D.工业冶炼粗硅:SiO 2 +C====Si+微专题突破5 无机物的性质、转化与应用一
CO↑
2
8.(2024·江苏省泰州模拟预测)铁及其化合物的转化具有重要应用。在指定条件下,下列物质间
转化能实现的是
A.Fe 2 O 3 稀 — 盐 — 酸 — \s\up 4()FeCl 3 (aq)蒸 — 发 → —\s\up 4()FeCl 3 (s) B.Fe过 2— 量 — IΔ FeI 2 过 l2 量 — CΔ FeCl 3
C.FeS 2O — 2 → —点 燃 Fe 2 O 3H —— 2 → O\s\up 4()Fe(OH) 3 D.Fe稀 — 盐 — 酸 — \s\up 4()FeCl 2 (aq)S —— O → 2\s\up
4()FeCl (aq)
3
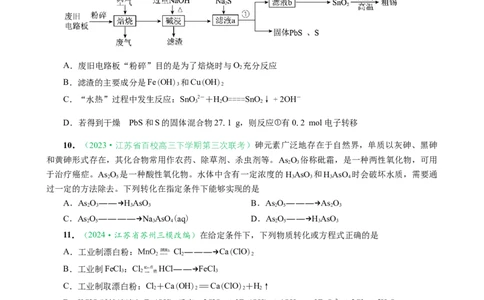
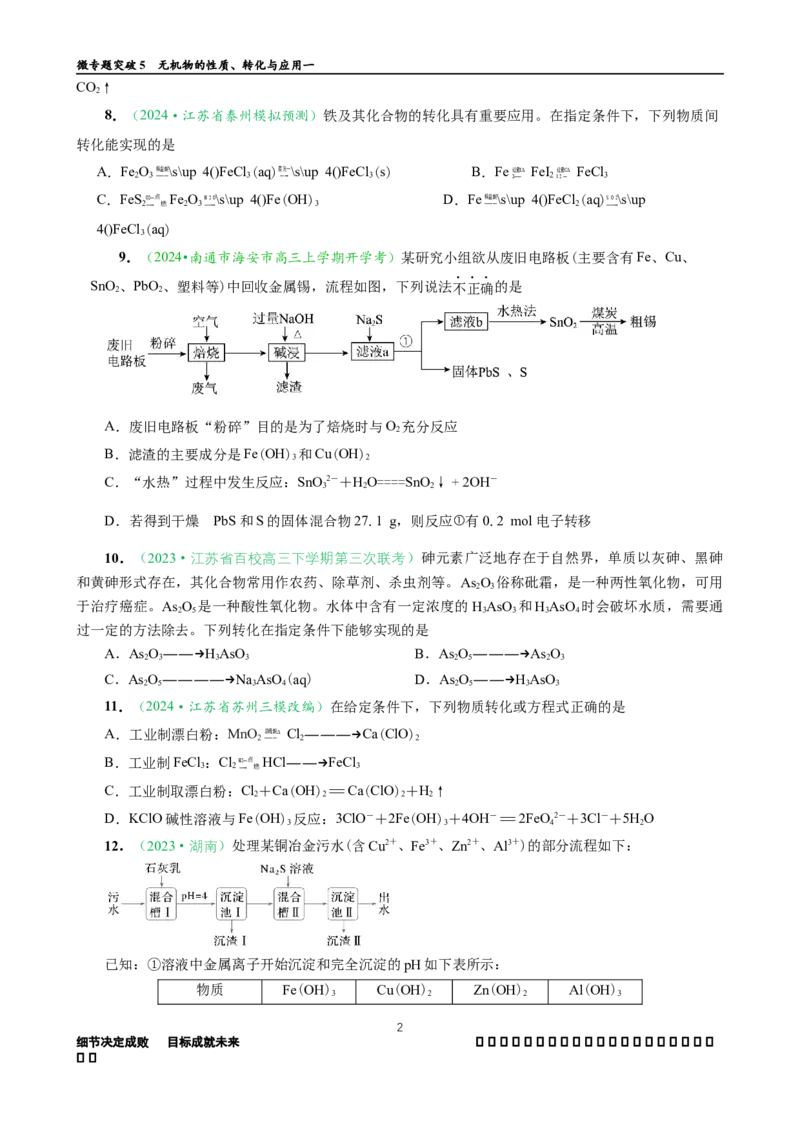
9.(2024•南通市海安市高三上学期开学考)某研究小组欲从废旧电路板(主要含有Fe、Cu、
SnO、PbO 、塑料等)中回收金属锡,流程如图,下列说法不正确的是
2 2
A.废旧电路板“粉碎”目的是为了焙烧时与O 充分反应
2
B.滤渣的主要成分是Fe(OH) 和Cu(OH)
3 2
C.“水热”过程中发生反应:SnO2-+HO====SnO↓+2OH-
3 2 2
的
D.若得到干燥 PbS和S的固体混合物27.1 g,则反应①有0.2 mol电子转移
10.(2023·江苏省百校高三下学期第三次联考)砷元素广泛地存在于自然界,单质以灰砷、黑砷
和黄砷形式存在,其化合物常用作农药、除草剂、杀虫剂等。As O 俗称砒霜,是一种两性氧化物,可用
2 3
于治疗癌症。As O 是一种酸性氧化物。水体中含有一定浓度的 HAsO 和HAsO 时会破坏水质,需要通
2 5 3 3 3 4
过一定的方法除去。下列转化在指定条件下能够实现的是
A.As O――→HAsO B.As O―――→As O
2 3 3 3 2 5 2 3
C.As O――――→NaAsO (aq) D.As O――→HAsO
2 5 3 4 2 5 3 3
11.(2024·江苏省苏州三模改编)在给定条件下,下列物质转化或方程式正确的是
A.工业制漂白粉:MnO 2 浓 — 硫 — 酸 — Δ Cl 2 ―――→Ca(ClO) 2
B.工业制FeCl 3 :Cl 2H — 2 → —点 燃 HCl――→FeCl 3
C.工业制取漂白粉:Cl+Ca(OH)=Ca(ClO)+H↑
2 2 2 2
D.KClO碱性溶液与Fe(OH) 反应:3ClO-+2Fe(OH)+4OH-=2FeO2-+3Cl-+5HO
3 3 4 2
12.(2023·湖南)处理某铜冶金污水(含Cu2+、Fe3+、Zn2+、Al3+)的部分流程如下:
已知:①溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
物质 Fe(OH) Cu(OH) Zn(OH) Al(OH)
3 2 2 3
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找开始沉淀pH 1.9 4.2 6.2 3.5
完全沉淀pH 3.2 6.7 8.2 4.6
②K (CuS)=6.4×10-36,K (ZnS)=1.6×10-24。
sp sp
下列说法错误的是
A.“沉渣Ⅰ”中含有Fe(OH) 和Al(OH)
3 3
B.NaS溶液呈碱性,其主要原因是S2-+HO HS-+OH-
2 2
C.“沉淀池Ⅱ”中,当Cu2+和Zn2+完全沉淀时,溶液中=4.0×10-12
D.“出水”经阴离子交换树脂软化处理后,可用作工业冷却循环用水
13.(2023·南京高三下学期考前模拟)实验室以含锌废液(主要成分为ZnSO ,还含有少量的Fe2
4
+、Mn2+)为原料制备ZnCO ·2Zn(OH) 的实验流程如下:
3 2
下列说法正确的是
A.过二硫酸钠(NaSO)中硫元素的化合价为+7价
2 2 8
B.氧化除锰后的溶液中存在:Na+、Zn2+、Fe2+、SO
C.调节pH时试剂X可以选用Zn、ZnO、ZnCO 等物质
3
D.沉锌时的离子方程式为3Zn2++6HCO=ZnCO ·2Zn(OH)↓+5CO↑+HO
3 2 2 2
14.(2023·苏州上学期期末)含锂物质在能源方面有重要应用。锂在氧气中燃烧与Mg相似,其燃
烧热为299 kJ·mol-1。锂与氮气反应得到的LiN可用作储氨材料。锂-空气电池是一种二次电池,放电
3
时主要产物为LiO ,充电时阴极产物易形成固态枝晶,导致电池短路。目前应用广泛的是锂离子电池,
2 2
例如,磷酸铁锂电池充电时锂离子由 LiFePO 电极迁移至石墨电极形成 LiFePO 的前体 FePO 可由
4 4 4
NH HPO 、FeSO 、HO 在pH=2的条件下反应制得。下列化学反应表示正确的是
4 2 4 4 2 2
的
A.LiN 水解:LiN+3HO=3LiOH+NH ↑
3 3 2 3
B.锂燃烧的热化学方程式:2Li(s)+O(g)=LiO(s) ∆H=299 kJ·mol-1
2 2 2
C.锂-空气电池充电的阳极反应:O2-+2e—=2O2-
2
D.制备FePO 的离子方程式:2HPO -+2Fe2++2OH-+HO=2FePO ↓+4HO
4 2 4 2 2 4 2
15.(2024·浙江省衢州、丽水、湖州三市11月)用钛铁矿(主要成分为FeTiO ,含有少量MgO、
3
SiO 等杂质)制备LiFePO 的工艺流程如图所示:
2 4
已知:钛铁矿经盐酸浸取后钛主要以TiOCl 2-形式存在,K (FePO)=1.0×10-22,
4 sp 4
K [Mg(PO )]=1.0×10-24。下列说法不正确的是
sp 3 4 2
A.滤液①中含有Fe2+、Mg2+微专题突破5 无机物的性质、转化与应用一
B.相同温度下溶解度:Mg(PO )>FePO
3 4 2 4
C.煅烧的主要反应为2FePO+LiCO+HC O====2LiFePO+3CO↑+H O↑
4 2 3 2 2 4 4 2 2
D.为保证水解过滤时能完全除钛,需调pH至溶液呈碱性
二、填空题
16.(2023·苏州上学期期末)NO 燃煤电站产生的主要大气污染物之一。以CuO-CeO 为活性物
x 2
质、γ-Al O 为载体的催化剂,可用于烟气中NO 脱除。
2 3 x
Ⅰ.将吸附有Cu2+、Ce3+的Al(OH) 胶体煅烧可制得CuO-CeO、γ-Al O 催化剂。
3 2 2 3
已知:Al(OH) 胶粒表面带正电荷。
3
(2)将Al(OH) 胶体与CuCl 、CeCl 溶液混合,静置、过滤、洗涤、煅烧制得催化剂。
3 2 3
①与 CuCl 、CeCl 溶液混合前,须在 Al(OH) 胶体中加入一定量 NaOH 溶液的目的是
2 3 3
__________________________________________。
②“煅烧”制得催化剂的过程中固体的质量先减小后增大,固体质量增加的原因是
___________________________________________________。
Ⅱ.将模拟烟气(主要成分为NO、NH 、O)匀速通过装有催化剂的反应管,NH 和NO反应机理可
3 2 3
表示为( 表示吸附态)。
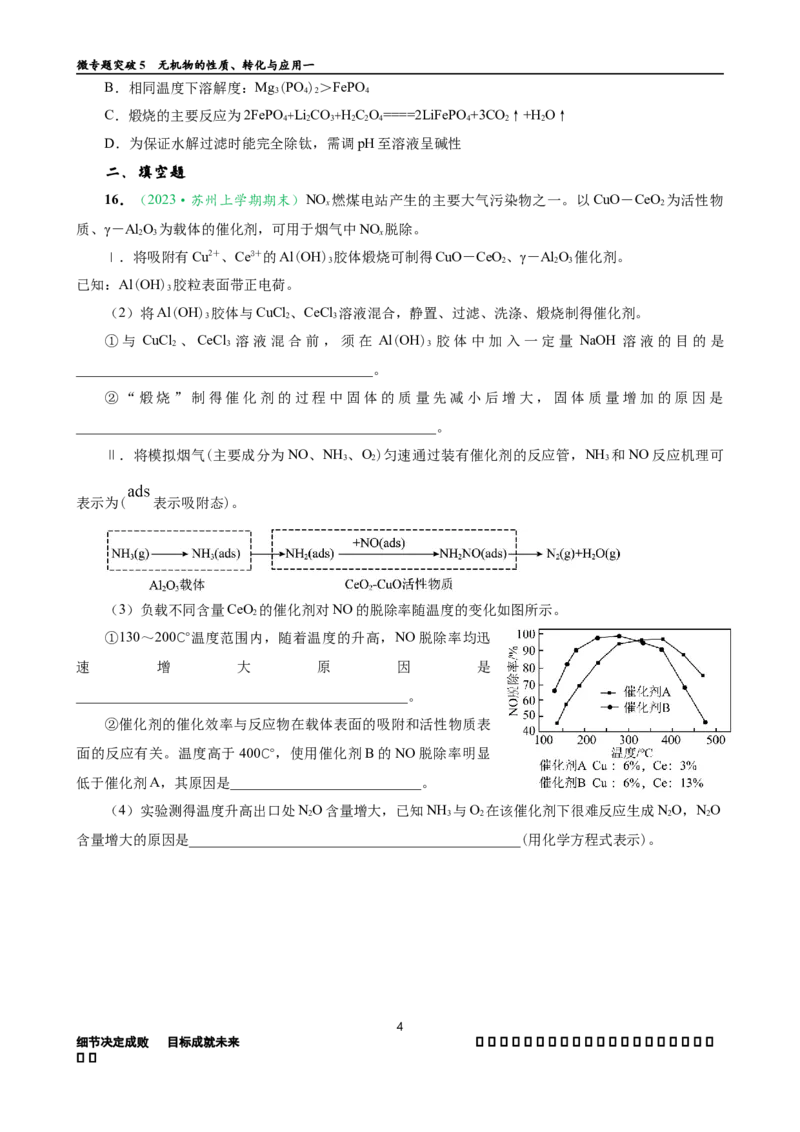
(3)负载不同含量CeO 的催化剂对NO的脱除率随温度的变化如图所示。
2
①130~200℃温度范围内,随着温度的升高,NO脱除率均迅
速 增 大 原 因 是
_______________________________________________。
②催化剂的催化效率与反应物在载体表面的吸附和活性物质表
面的反应有关。温度高于400℃,使用催化剂B的NO脱除率明显
低于催化剂A,其原因是___________________________。
(4)实验测得温度升高出口处NO含量增大,已知NH 与O 在该催化剂下很难反应生成NO,NO
2 3 2 2 2
含量增大的原因是_______________________________________________(用化学方程式表示)。
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找