文档内容
微专题突破6 无机化工流程题透视二
一、选择题
1.(2025·江苏南通市开学考)从炼钢粉尘(主要含Fe O、Fe O 和ZnO)中提取锌的流程如下:
3 4 2 3
“盐浸”过程中ZnO转化为[Zn(NH )]2+,并有少量Fe2+和Fe3+浸出。
3 4
下列说法不正确的是
A.1 mol [Zn(NH )]2+含16 mol σ键
3 4
B.“盐浸”过程中需补充NH ,防止浸液pH下降
3
C.“滤渣”的主要成分为Fe(OH)
3
D.“沉锌”过程中得到的“滤液”可循环利用
【答案】C
【解析】A项,1 mol [Zn(NH )]2+含4 mol Zn-N键和12 mol N-N键,共含16 mol σ键,正确;
3 4
B项,“盐浸”过程中ZnO转化为[Zn(NH )]2+,Zn2+与NH 结合消耗NH ,需补充NH 防止浸液pH下
3 4 3 3 3
降,正确;C项,由题意“盐浸”过程中ZnO转化为[Zn(NH )]2+,并有少量Fe2+和Fe3+浸出,可知
3 4
Fe O 、Fe O 只有少量溶解,故“滤渣”的主要成分是Fe O 、Fe O ,只有少量的Fe(OH) ,错误;D项,
3 4 2 3 3 4 2 3 3
“沉锌”过程中得到的“滤液”中含NH Cl,可循环利用,正确。
4
2.(2025·南通市海安市开学考)碲被誉为“现代工业的维生素”。某科研小组从粗铜精炼的阳极
泥(主要含有Cu Te)中提取粗碲设计工艺流程如图所示。
2
已知:①“焙烧”后,碲主要以TeO 形式存在;②TeO 微溶于水,易溶于强酸和强碱;③HTeO
2 2 6 6
的K =1.0×10-7,氧化性比硫酸强。
a1
下列有关说法正确的是
A.“焙烧”使用的主要仪器有:蒸发皿、酒精灯、玻璃棒
B.“碱溶”后的滤渣中Ag和Au可用稀硝酸分离
C.“氧化”时氧化剂与还原剂的物质的量之比为2∶1
D.“还原”反应的离子方程式为HTeO-+3SO2-+H+=Te↓+3SO 2-+3HO
5 6 3 4 2
【答案】B
【解析】粗铜精炼的阳极泥(主要含有Cu Te),通入氧气焙烧,可生成TeO 和CuO,加入氢氧化钠
2 2
溶液碱浸,生成可溶于水的 NaTeO ,过滤得到的滤渣含有 CuO和不溶的阳极泥,加入双氧水氧化
2 3
NaTeO 生成NaTeO ,经稀硫酸酸化后转化为HTeO ,最后加入亚硫酸钠还原并过滤得到粗碲。
2 3 2 4 6 6
A项,焙烧固体,应用坩埚,且放在泥三角上,另外加热时需要酒精灯,并用玻璃棒搅拌,错误;B
项,“碱浸”后所得的滤渣中含有的Au、Ag,Au不溶于稀硝酸,而Ag溶于稀硝酸,可选择稀硝酸分离,
正确;C项,“氧化”过程中双氧水被还原为水,双氧水中氧元素化合价总降低2价,Te元素化合价由
+4升高至+6,升高2价,因此氧化剂HO 与还原剂TeO2-的物质的量之比为1∶1,错误;D项,还原
2 2 3
反应中HTeO 为弱酸,不能拆分,错误。
6 6
二、填空题
3.循环物质的确定
合成尿素 菱锰矿制备二氧化锰 联合制碱法(侯氏制碱法)微专题突破6 无机化工流程题透视二
流程图
菱锰矿(主要成分为MnCO,还含有FeCO、
3 3
CaCO、SiO、AlO、FeO、MgCO 等杂质)
3 2 2 3 2 3 3
循环物质 ______________ _______ 母液、_______
【答案】N、H 硫酸 CO
2 2 2
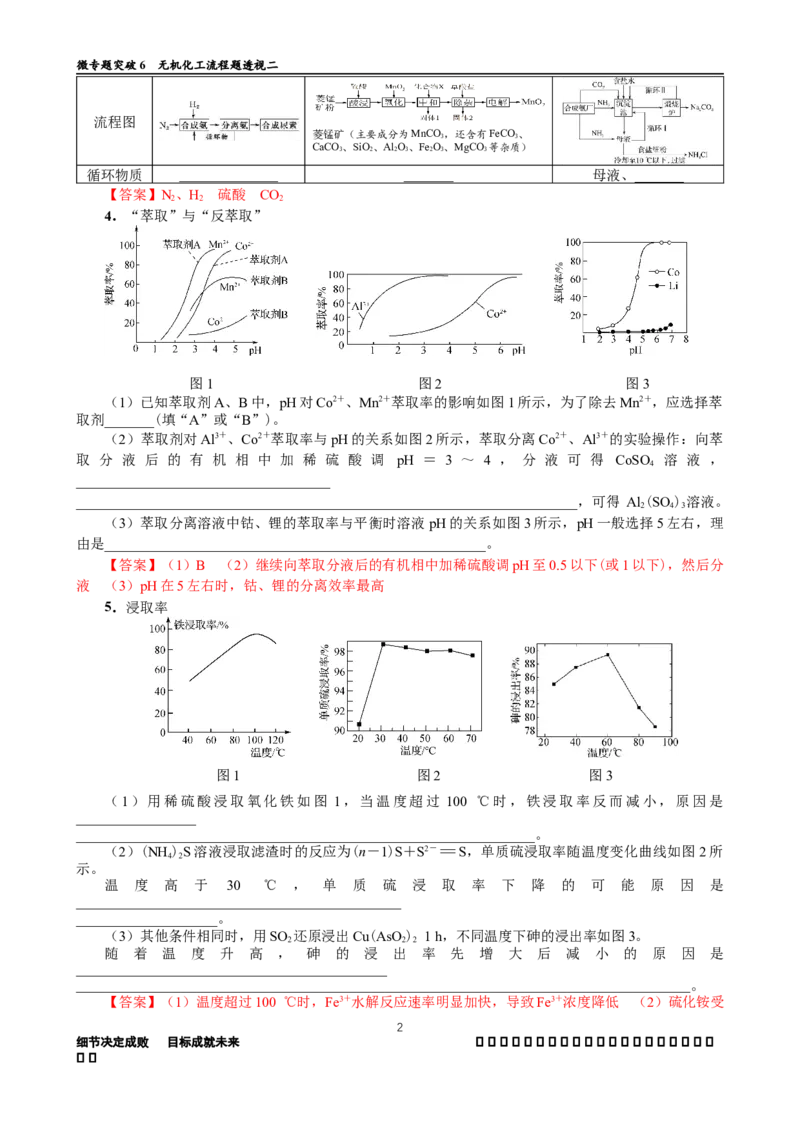
4.“萃取”与“反萃取”
图1 图2 图3
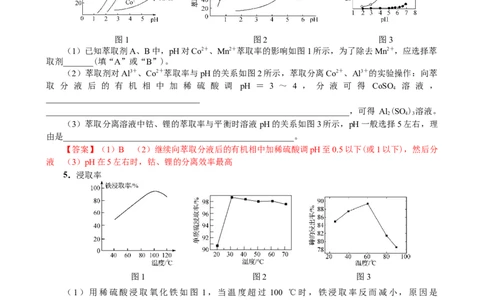
(1)已知萃取剂A、B中,pH对Co2+、Mn2+萃取率的影响如图1所示,为了除去Mn2+,应选择萃
取剂_______(填“A”或“B”)。
(2)萃取剂对Al3+、Co2+萃取率与pH的关系如图2所示,萃取分离Co2+、Al3+的实验操作:向萃
取 分 液 后 的 有 机 相 中 加 稀 硫 酸 调 pH = 3 ~ 4 , 分 液 可 得 CoSO 溶 液 ,
4
____________________________________
_______________________________________________________________________,可得 Al (SO ) 溶液。
2 4 3
(3)萃取分离溶液中钴、锂的萃取率与平衡时溶液 pH的关系如图3所示,pH一般选择5左右,理
由是______________________________________________________。
【答案】(1)B (2)继续向萃取分液后的有机相中加稀硫酸调pH至0.5以下(或1以下),然后分
液 (3)pH在5左右时,钴、锂的分离效率最高
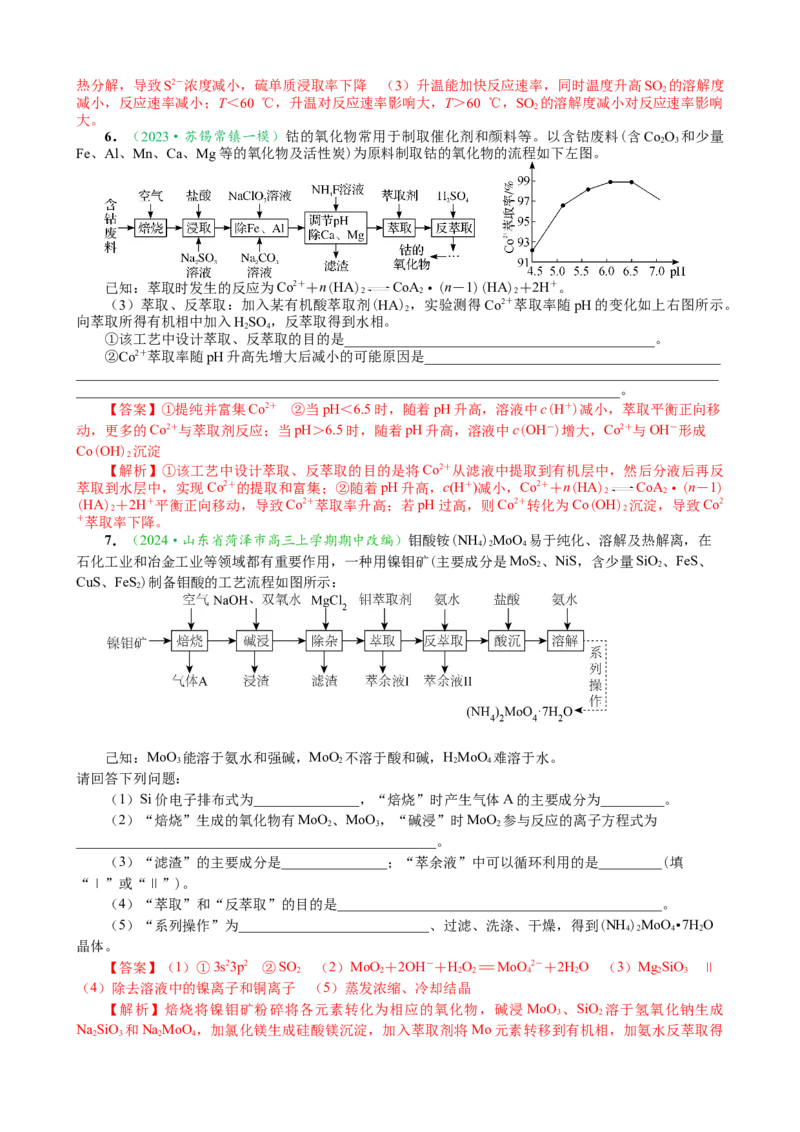
5.浸取率
图1 图2 图3
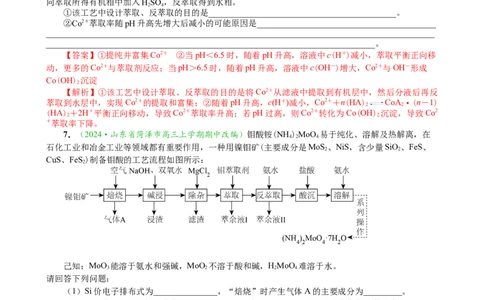
(1)用稀硫酸浸取氧化铁如图 1,当温度超过 100 ℃时,铁浸取率反而减小,原因是
_________________
_________________________________________________________________。
(2)(NH )S溶液浸取滤渣时的反应为(n-1)S+S2-=S,单质硫浸取率随温度变化曲线如图2所
4 2
示。
温 度 高 于 30 ℃ , 单 质 硫 浸 取 率 下 降 的 可 能 原 因 是
______________________________________________
____________________。
(3)其他条件相同时,用SO 还原浸出Cu(AsO ) 1 h,不同温度下砷的浸出率如图3。
2 2 2
随 着 温 度 升 高 , 砷 的 浸 出 率 先 增 大 后 减 小 的 原 因 是
____________________________________________
_______________________________________________________________________________________。
【答案】(1)温度超过100 ℃时,Fe3+水解反应速率明显加快,导致Fe3+浓度降低 (2)硫化铵受
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找热分解,导致S2-浓度减小,硫单质浸取率下降 (3)升温能加快反应速率,同时温度升高SO 的溶解度
2
减小,反应速率减小;T<60 ℃,升温对反应速率影响大,T>60 ℃,SO 的溶解度减小对反应速率影响
2
大。
6.(2023·苏锡常镇一模)钴的氧化物常用于制取催化剂和颜料等。以含钴废料(含Co O 和少量
2 3
Fe、Al、Mn、Ca、Mg等的氧化物及活性炭)为原料制取钴的氧化物的流程如下左图。
已知:萃取时发生的反应为Co2++n(HA) CoA·(n-1)(HA)+2H+。
2 2 2
(3)萃取、反萃取:加入某有机酸萃取剂(HA) ,实验测得Co2+萃取率随pH的变化如上右图所示。
2
向萃取所得有机相中加入HSO ,反萃取得到水相。
2 4
①该工艺中设计萃取、反萃取的目的是____________________________________________。
②Co2+萃取率随pH升高先增大后减小的可能原因是__________________________________________
___________________________________________________________________________________________
_____________________________________________________________________________。
【答案】①提纯并富集Co2+ ②当pH<6.5时,随着pH升高,溶液中c(H+)减小,萃取平衡正向移
动,更多的Co2+与萃取剂反应;当pH>6.5时,随着pH升高,溶液中c(OH-)增大,Co2+与OH-形成
Co(OH) 沉淀
2
【解析】①该工艺中设计萃取、反萃取的目的是将Co2+从滤液中提取到有机层中,然后分液后再反
萃取到水层中,实现Co2+的提取和富集;②随着pH升高,c(H+)减小,Co2++n(HA) CoA·(n-1)
2 2
(HA) +2H+平衡正向移动,导致Co2+萃取率升高;若pH过高,则Co2+转化为Co(OH) 沉淀,导致Co2
2 2
+萃取率下降。
7.(2024·山东省菏泽市高三上学期期中改编)钼酸铵(NH )MoO 易于纯化、溶解及热解离,在
4 2 4
石化工业和冶金工业等领域都有重要作用,一种用镍钼矿(主要成分是MoS、NiS,含少量SiO 、FeS、
2 2
CuS、FeS)制备钼酸的工艺流程如图所示:
2
己知:MoO 能溶于氨水和强碱,MoO 不溶于酸和碱,HMoO 难溶于水。
3 2 2 4
请回答下列问题:
(1)Si价电子排布式为_______________,“焙烧”时产生气体A的主要成分为_________。
(2)“焙烧”生成的氧化物有MoO、MoO,“碱浸”时MoO 参与反应的离子方程式为
2 3 2
___________________________________________________。
(3)“滤渣”的主要成分是_______________;“萃余液”中可以循环利用的是_________(填
“Ⅰ”或“Ⅱ”)。
(4)“萃取”和“反萃取”的目的是______________________________________________。
(5)“系列操作”为___________________________、过滤、洗涤、干燥,得到(NH )MoO•7HO
4 2 4 2
晶体。
【答案】(1)①3s23p2 ②SO (2)MoO+2OH-+HO=MoO2-+2HO (3)MgSiO Ⅱ
2 2 2 2 4 2 2 3
(4)除去溶液中的镍离子和铜离子 (5)蒸发浓缩、冷却结晶
【解析】焙烧将镍钼矿粉碎将各元素转化为相应的氧化物,碱浸MoO 、SiO 溶于氢氧化钠生成
3 2
NaSiO 和NaMoO ,加氯化镁生成硅酸镁沉淀,加入萃取剂将Mo元素转移到有机相,加氨水反萃取得
2 3 2 4微专题突破6 无机化工流程题透视二
到MoO 2-,加盐酸生成HMoO 沉淀,加氨水溶解得到钼酸铵。
4 2 4
(1)Si为14号元素,价电子排布式为3s23p2,“焙烧”时生成硫元素转化为SO ;(2)“焙烧”生
2
成的钼的氧化物有MoO 和MoO 等,已知MoO 不溶于酸和碱,为了提高Mo元素的利用率,将MoO 中
2 3 2 2
+4价Mo氧化为+6价,“碱浸”时MoO 参与反应的离子方程式为MoO +2OH-+HO =MoO2-+
2 2 2 2 4
2HO;(3)根据分析可知加氯化镁为了除去硅元素,生成硅酸镁沉淀,滤渣为MgSiO ;利用有机萃取
2 2 3
剂将钼萃取出来,再利用氨水将钼反萃取至水相,因此“萃余液Ⅰ”是水相,“萃余液Ⅱ”是有机相,
其有机相可再生循环利用,故答案萃余液Ⅱ;(4)由分析可知,加入萃取剂将Mo元素转移到有机相,
加氨水反萃取得到MoO 2-,则萃取和反萃取的目的是除去溶液中的镍离子和铜离子;(5)从溶液到晶
4
体的一系列操作包括:蒸发浓缩、冷却结晶、过滤、洗涤、干燥。
8.(2024·江苏南京市盐城市一模)碲广泛应用于冶金工业。以碲铜废料(主要含Cu Te)为原料
2
回收碲单质的一种工艺流程如下:
已知:K (HC O)=5.0×10-2,K (HC O)=1.5×10-4,K (HTeO )=1.0×10-3,K (CuC O)=
a1 2 2 4 a2 2 2 4 a1 2 3 sp 2 4
2.0×10-8。
(1)“氧化酸浸”得到CuSO 和HTeO ,该反应的化学方程式为
4 2 3
_______________________________________________________________________。
(4)“还原”在50℃条件下进行,HTeO 发生反应的离子方程式为
2 3
____________________________________________。
(5)“还原”时,NaSO 的实际投入量大于理论量,其可能的原因为
2 3
____________________________________________________________________________________。
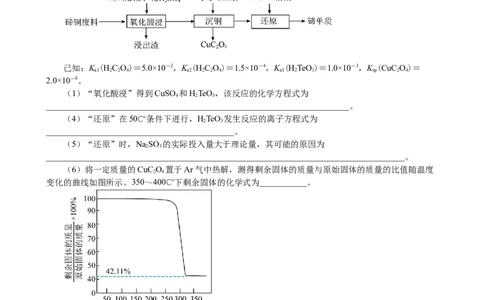
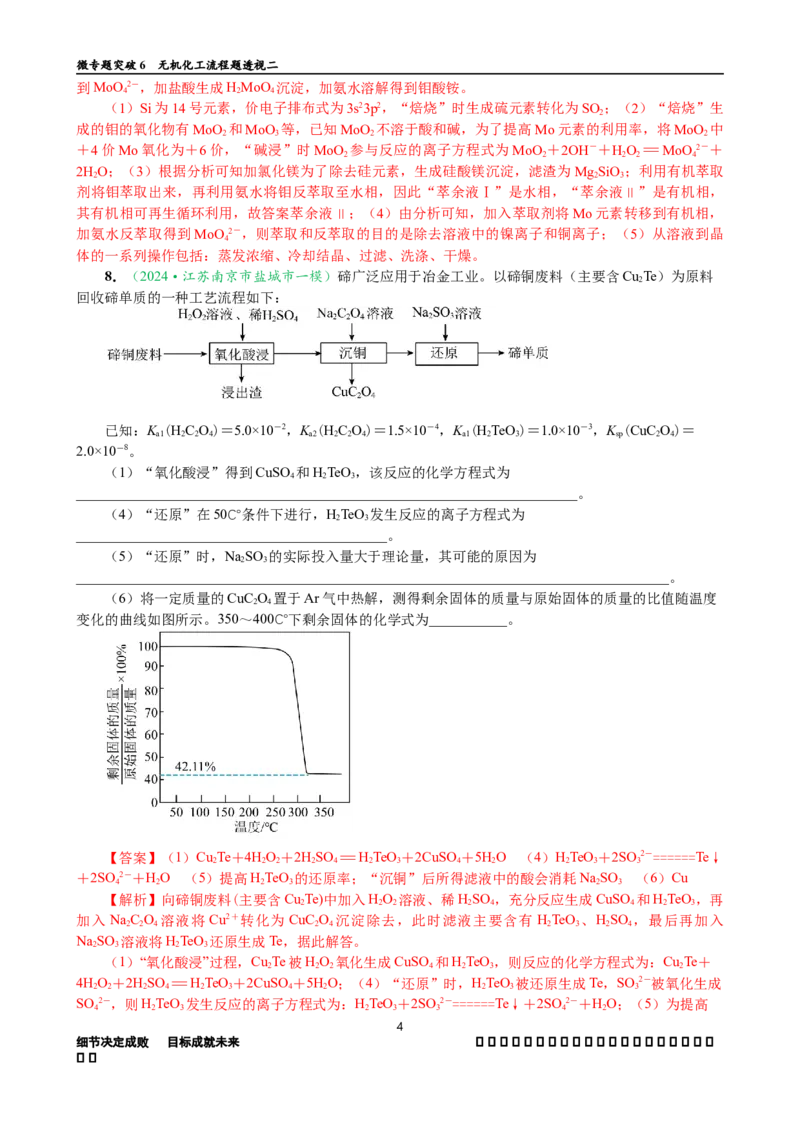
(6)将一定质量的CuC O 置于Ar气中热解,测得剩余固体的质量与原始固体的质量的比值随温度
2 4
变化的曲线如图所示。350~400℃下剩余固体的化学式为___________。
【答案】(1)Cu Te+4HO+2HSO =HTeO+2CuSO +5HO (4)HTeO+2SO2-======Te↓
2 2 2 2 4 2 3 4 2 2 3 3
+2SO 2-+HO (5)提高HTeO 的还原率;“沉铜”后所得滤液中的酸会消耗NaSO (6)Cu
4 2 2 3 2 3
【解析】向碲铜废料(主要含Cu Te)中加入HO 溶液、稀HSO ,充分反应生成CuSO 和HTeO ,再
2 2 2 2 4 4 2 3
加入 NaC O 溶液将Cu2+转化为 CuC O 沉淀除去,此时滤液主要含有 HTeO 、HSO ,最后再加入
2 2 4 2 4 2 3 2 4
NaSO 溶液将HTeO 还原生成Te,据此解答。
2 3 2 3
(1)“氧化酸浸”过程,Cu Te被HO 氧化生成CuSO 和HTeO ,则反应的化学方程式为:Cu Te+
2 2 2 4 2 3 2
4HO+2HSO =HTeO+2CuSO +5HO;(4)“还原”时,HTeO 被还原生成Te,SO2-被氧化生成
2 2 2 4 2 3 4 2 2 3 3
SO 2-,则HTeO 发生反应的离子方程式为:HTeO+2SO2-======Te↓+2SO 2-+HO;(5)为提高
4 2 3 2 3 3 4 2
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找HTeO 的还原率,加入的NaSO 溶液过量;“沉铜”后所得滤液主要含有HTeO 、HSO ,NaSO 会与
2 3 2 3 2 3 2 4 2 3
HSO 反应生成SO 并逸出,则NaSO 的实际投入量大于理论量,其可能的原因为:提高HTeO 的还原
2 4 2 2 3 2 3
率;“沉铜”后所得滤液中的酸会消耗NaSO;(5)由图可知,350~400°C时剩余固体的质量与原始
2 3
固体的质量的比值为42.11%,取1 ml CuC O 其质量为152 g,则剩余固体的摩尔质量为:152
2 4
g×42.11%=64 g,再结合化学反应前后元素种类不变,350~400°C下剩余固体的化学式为Cu。