文档内容
易错专题 12 化学反应速率
聚焦易错点:
►易错点一 化学反应速率影响因素
►易错点二 化学反应速率影响因素的探究
典例精讲
易错点一 化学反应速率的影响因素
【易错典例】
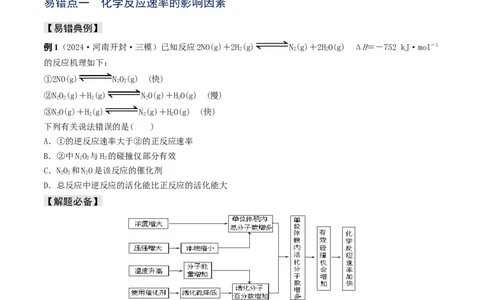
例1(2024·河南开封·三模)已知反应2NO(g)+2H(g) N(g)+2HO(g) ΔH=-752 kJ·mol-1
2 2 2
的反应机理如下:
①2NO(g) NO(g) (快)
2 2
②NO(g)+H(g) NO(g)+HO(g) (慢)
2 2 2 2 2
③NO(g)+H(g) N(g)+HO(g) (快)
2 2 2 2
下列有关说法错误的是( )
A.①的逆反应速率大于②的正反应速率
B.②中NO 与H 的碰撞仅部分有效
2 2 2
C.NO 和NO是该反应的催化剂
2 2 2
D.总反应中逆反应的活化能比正反应的活化能大
【解题必备】
(1)纯液体和固体浓度视为常数,它们的量的改变不会影响化学反应速率。但固体颗粒的大小导致接触面的
大小发生变化,故影响反应速率。
(2)对于固体、液体物质,由于压强改变时对它们的体积影响很小,因而压强对它们浓度的影响可看作不变,
压强对无气体参加的化学反应的速率无影响。
(3)升高温度,不论吸热还是放热反应,也不论正反应速率还是逆反应速率都增大。
(4)用催化剂催化的反应,由于催化剂只有在适宜的温度下活性最大,反应速率才能达到最大,故在许多工
业生产中温度的选择还需考虑催化剂的活性温度范围。【变式突破】
1.(2024·北京朝阳·一模)某同学进行如下实验:
①将H O 溶液与KI溶液混合,产生大量气泡,溶液颜色变黄;
2 2
②将①中的黄色溶液分成两等份,一份加入CCl ,振荡,产生气泡速率明显减小,下层溶液呈紫红色;另
4
一份不加CCl ,振荡,产生气泡速率无明显变化。
4
下列说法不正确的是
A.①中溶液颜色变黄的原因是:H O +2I-=I +2OH-
2 2 2
B.②中下层溶液呈紫红色是因为I 溶于CCl
2 4
C.②中产生气泡速率减小的原因是H O 浓度减小
2 2
D.由该实验可知,I 可以加快H O 分解产生气泡反应速率
2 2 2
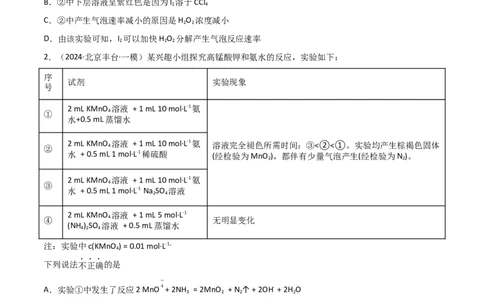
2.(2024·北京丰台·一模)某兴趣小组探究高锰酸钾和氨水的反应,实验如下:
序
试剂 实验现象
号
2 mL KMnO 溶液 + 1 mL 10 mol·L-1氨
① 4
水+0.5 mL蒸馏水
② 2 mL KMnO 4 溶液 + 1 mL 10 mol·L-1氨 溶液完全褪色所需时间:③<②<①。实验均产生棕褐色固体
水 + 0.5 mL 1 mol·L-1稀硫酸 (经检验为MnO ),都伴有少量气泡产生(经检验为N )。
2 2
2 mL KMnO 溶液 + 1 mL 10 mol·L-1氨
③ 4
水 + 0.5 mL 1 mol·L-1 Na SO 溶液
2 4
2 mL KMnO 溶液 + 1 mL 5 mol·L-1
④ 4 无明显变化
(NH ) SO 溶液 + 0.5 mL蒸馏水
4 2 4
注:实验中c(KMnO ) = 0.01 mol·L-1。
4
下列说法不正确的是
A.实验①中发生了反应2 MnO + 2NH = 2MnO + N ↑ + 2OH- + 2H O
3 2 2 2
B.溶液完全褪色所需时间② < ①的主要原因:c(H+)增大,MnO 的氧化性增强
C.对比实验③④可得出,还原性:NH > NH
3
D.在实验④的试剂中,逐滴加入浓NaOH溶液,可观察到溶液褪色
3.(2024·广东佛山·二模)某兴趣小组探究电石与溶液反应的速率并制备乙炔气体。下列说法错误的是
实验 电石质 溶液 现象量/g
1 m 稀食盐水 产气较快,有大量灰白色沉淀和泡沫
2 m 饱和食盐水 产气较慢,有较多灰白色沉淀和泡沫
3 m 稀盐酸
A.灰白色沉淀主要成分为
B.提高NaCl溶液的质量分数能减慢反应速率
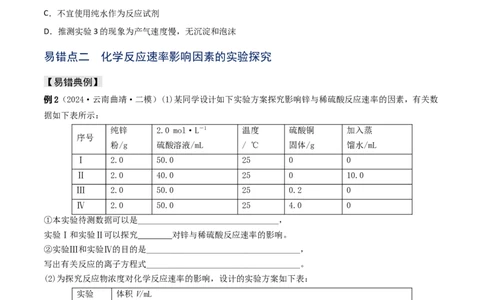
C.不宜使用纯水作为反应试剂
D.推测实验3的现象为产气速度慢,无沉淀和泡沫
易错点二 化学反应速率影响因素的实验探究
【易错典例】
例2(2024·云南曲靖·二模)(1)某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数
据如下表所示:
纯锌 2.0 mol·L-1 温度 硫酸铜 加入蒸
序号
粉/g 硫酸溶液/mL / ℃ 固体/g 馏水/mL
Ⅰ 2.0 50.0 25 0 0
Ⅱ 2.0 40.0 25 0 10.0
Ⅲ 2.0 50.0 25 0.2 0
Ⅳ 2.0 50.0 25 4.0 0
①本实验待测数据可以是_________________________________,
实验Ⅰ和实验Ⅱ可以探究 对锌与稀硫酸反应速率的影响。
②实验Ⅲ和实验Ⅳ的目的是____________________________________,
写出有关反应的离子方程式____________________________________。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验 体积V/mL
序号 KSO 溶液 水 KI溶液 NaSO 溶液 淀粉溶液
2 2 8 2 2 3
① 10.0 0.0 4.0 4.0 2.0
② 9.0 1.0 4.0 4.0 2.0
③ 8.0 V 4.0 4.0 2.0
x
表中V= ,理由是______________________________。
x
【解题必备】
在研究影响化学反应速率和化学平衡的因素时,由于外界影响因素较多,所以搞清某个因素的影响均需控
制其他因素相同或不变时,再进行实验。因此控制变量思想在这部分体现较为充分。控制变量思想是中学化学实验中常用的思想方法,对影响实验结果的因素进行控制,以达到明确各因素在实验中的作用和目的。
尤其是在研究影响化学反应速率和化学平衡的因素时,由于外界影响因素较多,故要弄清某个因素的影响
需控制其他因素相同或不变时再进行实验。在解决这类问题时,要充分挖掘基础知识的内在联系,不被知
识的表面及问题的表象所迷惑,参透问题的本质,准确快速的解决问题。解题的步骤如下:
(1)确定变量:理清影响实验探究结果的所有因素。
(2)定多变一:在探究时,先确定其他的因素不变,只变化一种因素,看这种因素与探究的问题存在怎样
的关系;这样确定一种以后,再确定另一种,通过分析每种因素与所探究问题之间的关系,得出所有影响
因素与所探究问题之间的关系。
(3)数据有效:解答时注意选择数据(或设置实验)要有效,且变量统一,否则无法作出正确判断。
【变式突破】
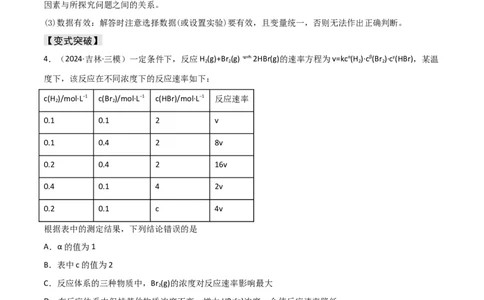
4.(2024·吉林·三模)一定条件下,反应H (g)+Br (g) 2HBr(g)的速率方程为v=kcα(H )·cβ(Br )·cγ(HBr),某温
2 2 2 2
度下,该反应在不同浓度下的反应速率如下:
c(H )/mol·L−1 c(Br )/mol·L−1 c(HBr)/mol·L−1 反应速率
2 2
0.1 0.1 2 v
0.1 0.4 2 8v
0.2 0.4 2 16v
0.4 0.1 4 2v
0.2 0.1 c 4v
根据表中的测定结果,下列结论错误的是
A.α的值为1
B.表中c的值为2
C.反应体系的三种物质中,Br (g)的浓度对反应速率影响最大
2
D.在反应体系中保持其他物质浓度不变,增大HBr(g)浓度,会使反应速率降低
5.(2024·河南焦作·二模)Na S O ·5H O是重要的化工原料,有关制备和应用如下。
2 2 3 2
Ⅰ.制备Na S O ·5H O反应原理:Na SO (aq)+S(s) Na S O (aq)
2 2 3 2 2 3 2 2 3
实验步骤:
①称取15gNa SO 加入圆底烧瓶中,再加入80mL蒸馏水。另取5g研细的硫粉,用3mL乙醇润湿,加入上
2 3
述溶液中。②安装实验装置(如图所示,部分夹持装置略去),水浴加热,微沸60min。回答下列问题:
(1)硫粉在反应前用乙醇润湿的目的是 。
(2)仪器a的作用是 。
(3)产品中除了有未反应的Na SO 外,还可能存在的无机杂质是 ,检验是否存在该杂质的方法是
2 3
。
Ⅱ.分离Na S O ·5H O。已知:Na S O ·5H O于40~45℃熔化,48℃分解;Na S O 易溶于水,不溶于乙醇。
2 2 3 2 2 2 3 2 2 2 3
分离Na S O ·5H O晶体的流程如图所示:
2 2 3 2
回答下列问题:
(4)为减少产品的损失,操作①要 (填操作),其目的是 ;操作②的包括的过程是快速过滤、
洗涤、干燥,其中洗涤操作是用 (填试剂)作洗涤剂。
(5)蒸发浓缩滤液直至溶液呈微黄色浑浊为止,蒸发时要控制温度不宜过高原因 。
Ⅲ.研究外界条件对化学反应速率的影响,设计实验如表(所取溶液体积均为10mL):
实验编
实验温度/℃ c(Na S O )/mol·L-1 c(H SO )/mol·L-1
号 2 2 3 2 4
① 25 0.1 0.1
② 25 0.1 0.2
③ 50 0.2 0.1
④ 50 0.1 0.1
(6)探究浓度对化学反应速率的影响,应选择 (填实验编号)。
(7)探究温度对化学反应速率的影响,应选择 (填实验编号)。6.(2024·吉林延边·一模)叔丁基溴[ ]是重要的化工原料。已知相关物质的沸点如下表所示。
物质 氢溴酸
时 与水共
沸点
沸
回答下列问题:
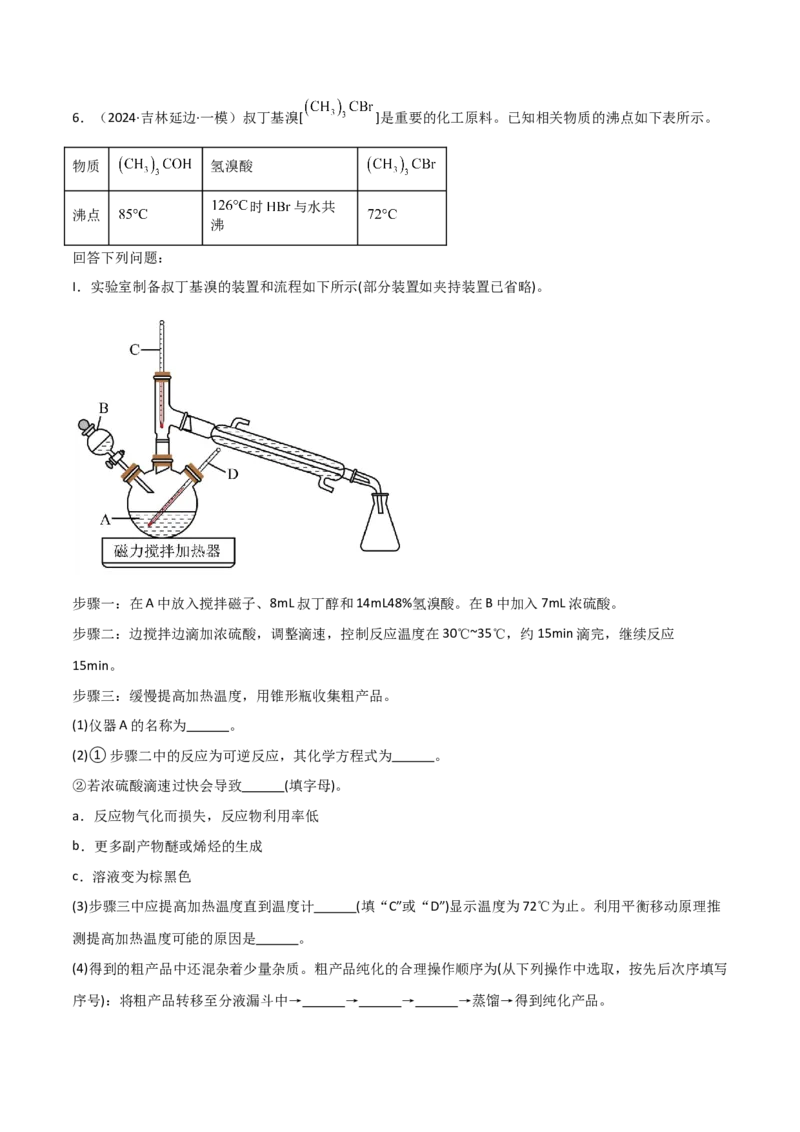
I.实验室制备叔丁基溴的装置和流程如下所示(部分装置如夹持装置已省略)。
步骤一:在A中放入搅拌磁子、8mL叔丁醇和14mL48%氢溴酸。在B中加入7mL浓硫酸。
步骤二:边搅拌边滴加浓硫酸,调整滴速,控制反应温度在30℃~35℃,约15min滴完,继续反应
15min。
步骤三:缓慢提高加热温度,用锥形瓶收集粗产品。
(1)仪器A的名称为 。
(2)①步骤二中的反应为可逆反应,其化学方程式为 。
②若浓硫酸滴速过快会导致 (填字母)。
a.反应物气化而损失,反应物利用率低
b.更多副产物醚或烯烃的生成
c.溶液变为棕黑色
(3)步骤三中应提高加热温度直到温度计 (填“C”或“D”)显示温度为72℃为止。利用平衡移动原理推
测提高加热温度可能的原因是 。
(4)得到的粗产品中还混杂着少量杂质。粗产品纯化的合理操作顺序为(从下列操作中选取,按先后次序填写
序号):将粗产品转移至分液漏斗中→ → → →蒸馏→得到纯化产品。①用 溶液洗涤、分液②用 溶液洗涤、分液③用水洗涤、分液④用碱石灰干燥、过滤
⑤用无水 干燥、过滤
Ⅱ.为探究叔丁基溴水解速率的影响因素,某同学按照下表进行实验,并记录加入的 恰好完全反应
时所需的反应时间。
实验 叔丁基溴的丙 溶液 蒸馏水 酸碱指示 水浴温 反应时
序号 酮溶液 剂/滴 度 间
① 3.0 0.6 16.4 2 25 10
② 3.0 1.2 15.8 2 25 20
③ 1.5 0.6 17.9 2 25 20
④ 1.5 0.6 17.9 2 0 40
(5)对比实验①②,探究影响叔丁基溴水解速率的因素是 ,对比探究实验③④可以得出影响叔丁基溴
水解速率的结论是 。
考点精练
1.(2024·江西萍乡·二模)常温下,向某溶剂(不参与反应)中加入一定量X、Y和M,所得溶液中同时存在
如下平衡:
①
②
③ 。
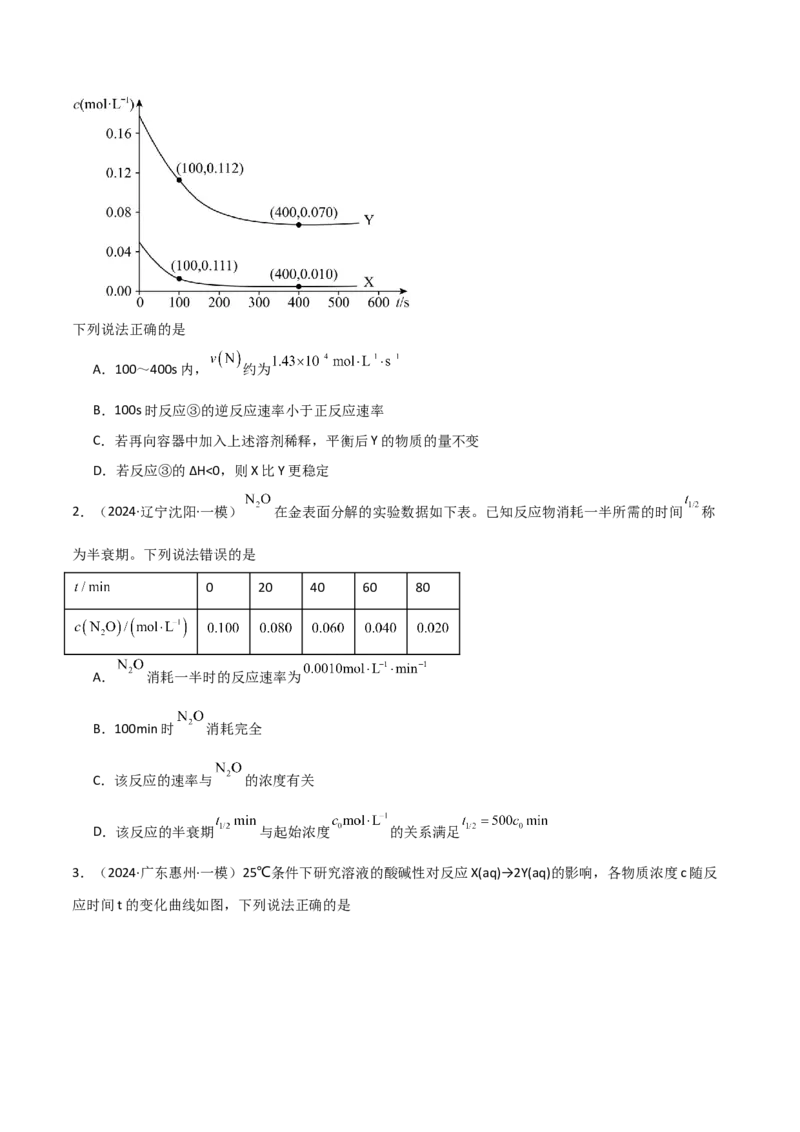
X、Y的物质的量浓度c随时间反应t的变化关系如图所示,400s时反应体系达到平衡状态。下列说法正确的是
A.100~400s内, 约为
B.100s时反应③的逆反应速率小于正反应速率
C.若再向容器中加入上述溶剂稀释,平衡后Y的物质的量不变
D.若反应③的ΔH<0,则X比Y更稳定
2.(2024·辽宁沈阳·一模) 在金表面分解的实验数据如下表。已知反应物消耗一半所需的时间 称
为半衰期。下列说法错误的是
0 20 40 60 80
A. 消耗一半时的反应速率为
B.100min时 消耗完全
C.该反应的速率与 的浓度有关
D.该反应的半衰期 与起始浓度 的关系满足
3.(2024·广东惠州·一模)25℃条件下研究溶液的酸碱性对反应X(aq)→2Y(aq)的影响,各物质浓度c随反
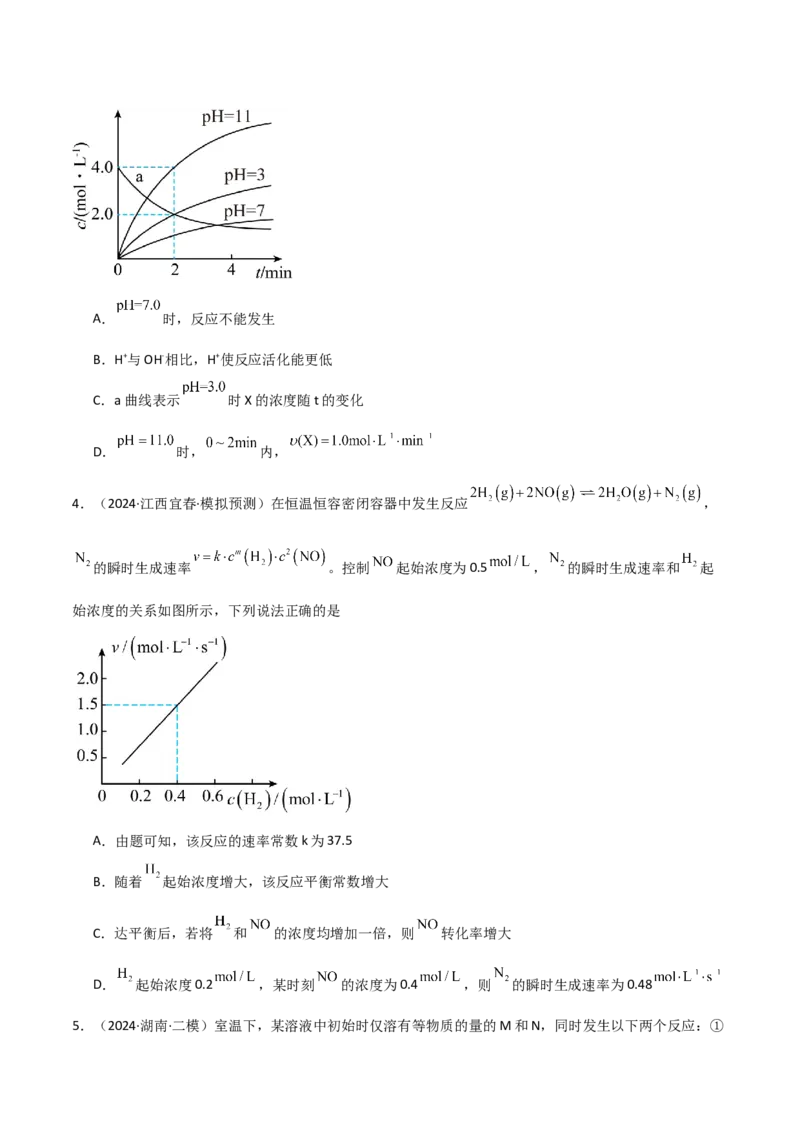
应时间t的变化曲线如图,下列说法正确的是A. 时,反应不能发生
B.H+与OH-相比,H+使反应活化能更低
C.a曲线表示 时X的浓度随t的变化
D. 时, 内,
4.(2024·江西宜春·模拟预测)在恒温恒容密闭容器中发生反应 ,
的瞬时生成速率 。控制 起始浓度为0.5 , 的瞬时生成速率和 起
始浓度的关系如图所示,下列说法正确的是
A.由题可知,该反应的速率常数k为37.5
B.随着 起始浓度增大,该反应平衡常数增大
C.达平衡后,若将 和 的浓度均增加一倍,则 转化率增大
D. 起始浓度0.2 ,某时刻 的浓度为0.4 ,则 的瞬时生成速率为0.48
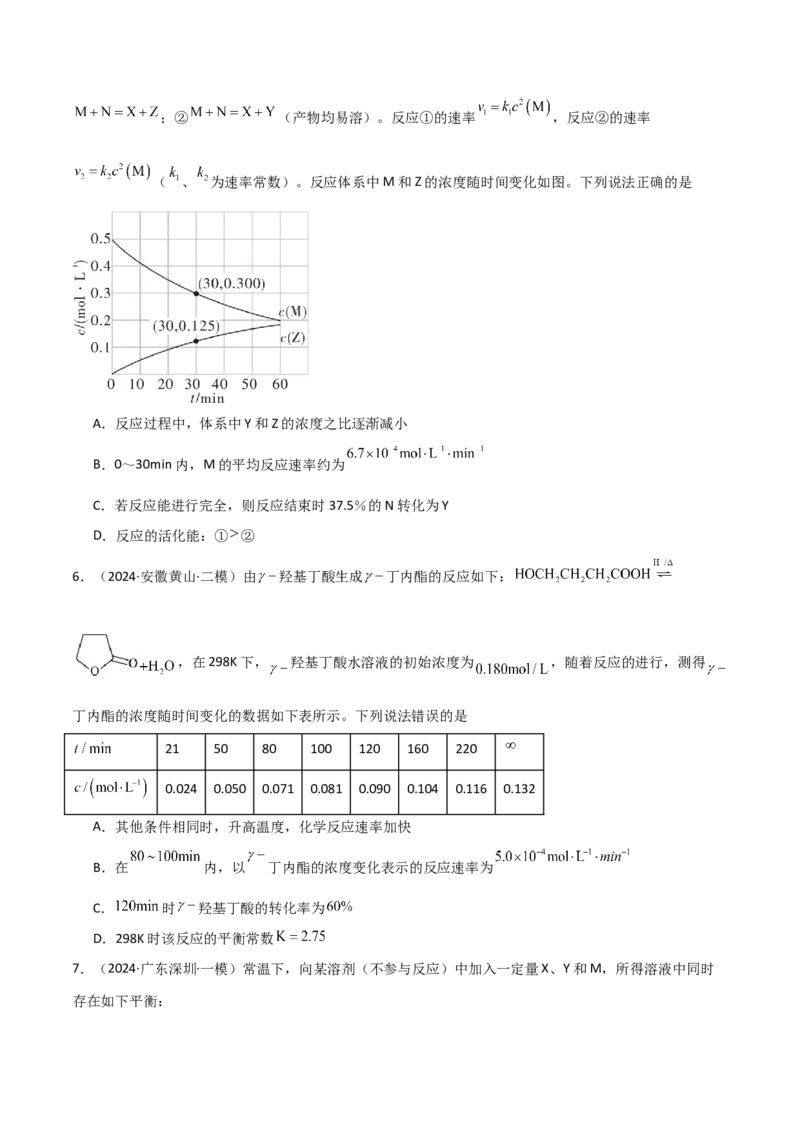
5.(2024·湖南·二模)室温下,某溶液中初始时仅溶有等物质的量的M和N,同时发生以下两个反应:①;② (产物均易溶)。反应①的速率 ,反应②的速率
( 、 为速率常数)。反应体系中M和Z的浓度随时间变化如图。下列说法正确的是
A.反应过程中,体系中Y和Z的浓度之比逐渐减小
B.0~30min内,M的平均反应速率约为
C.若反应能进行完全,则反应结束时37.5%的N转化为Y
D.反应的活化能:① ②
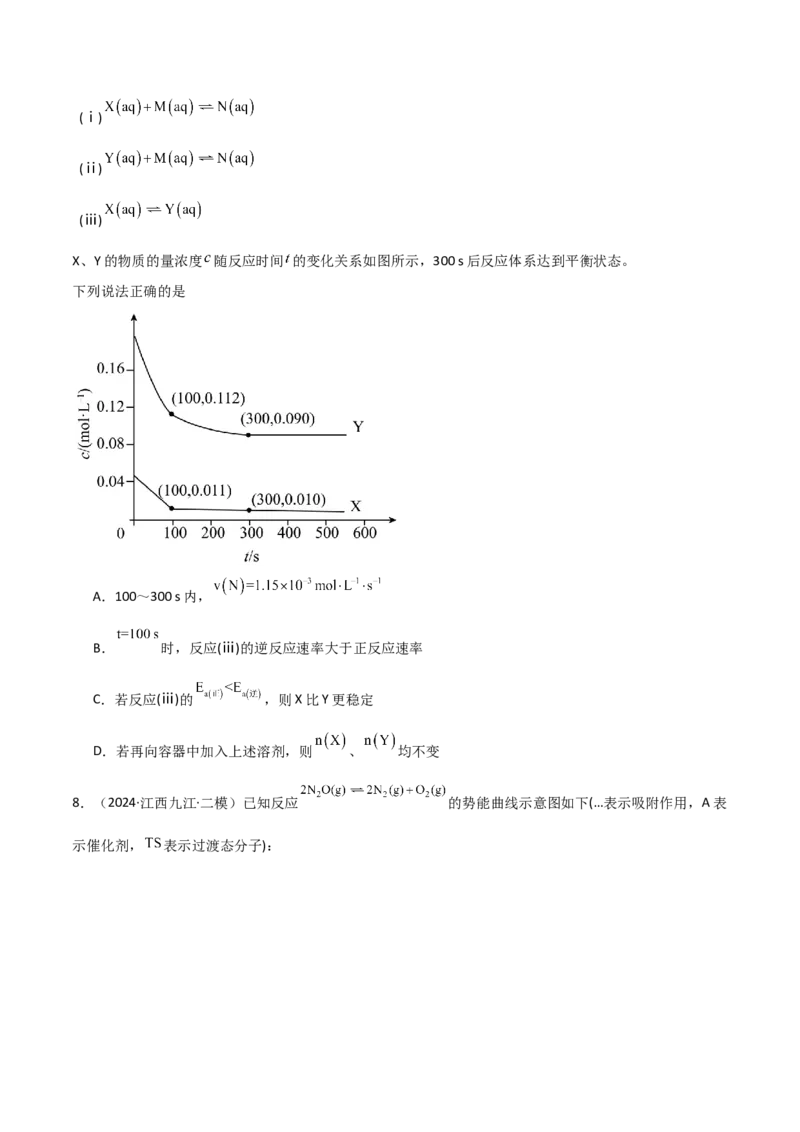
6.(2024·安徽黄山·二模)由 羟基丁酸生成 丁内酯的反应如下:
,在298K下, 羟基丁酸水溶液的初始浓度为 ,随着反应的进行,测得
丁内酯的浓度随时间变化的数据如下表所示。下列说法错误的是
21 50 80 100 120 160 220
0.024 0.050 0.071 0.081 0.090 0.104 0.116 0.132
A.其他条件相同时,升高温度,化学反应速率加快
B.在 内,以 丁内酯的浓度变化表示的反应速率为
C. 时 羟基丁酸的转化率为
D.298K时该反应的平衡常数
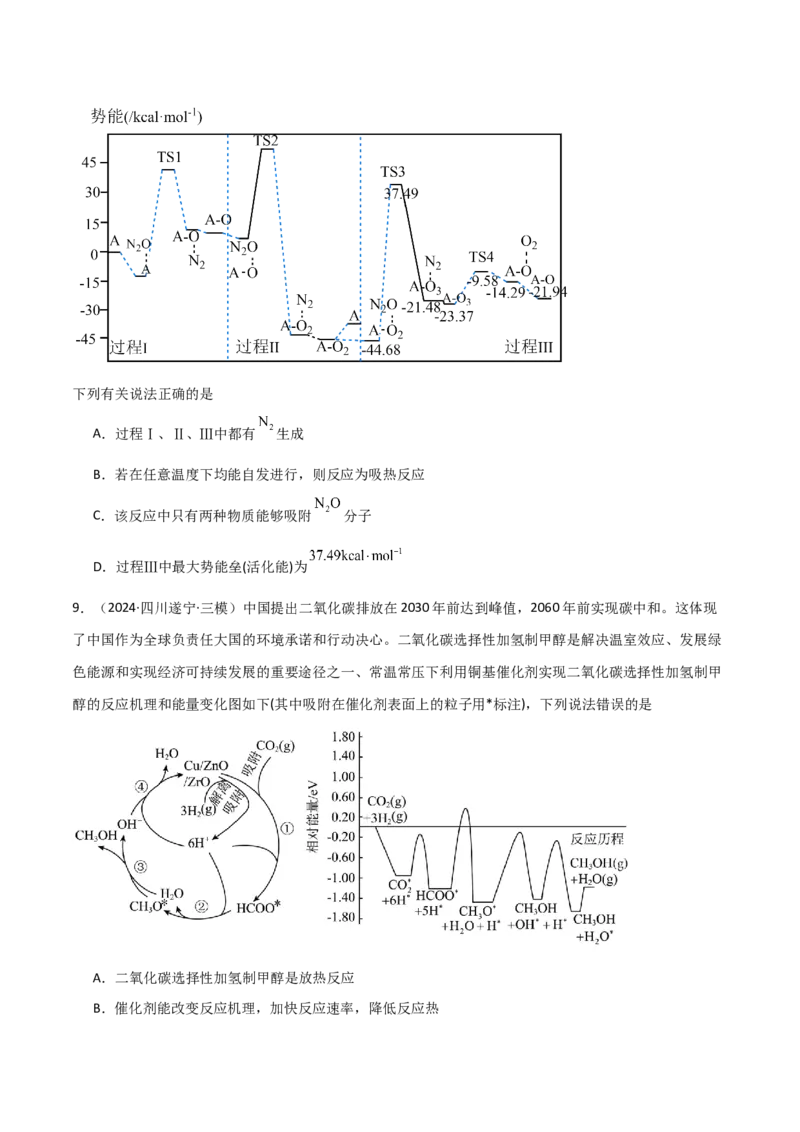
7.(2024·广东深圳·一模)常温下,向某溶剂(不参与反应)中加入一定量X、Y和M,所得溶液中同时
存在如下平衡:(ⅰ)
(ⅱ)
(ⅲ)
X、Y的物质的量浓度 随反应时间 的变化关系如图所示,300 s后反应体系达到平衡状态。
下列说法正确的是
A.100~300 s内,
B. 时,反应(ⅲ)的逆反应速率大于正反应速率
C.若反应(ⅲ)的 ,则X比Y更稳定
D.若再向容器中加入上述溶剂,则 、 均不变
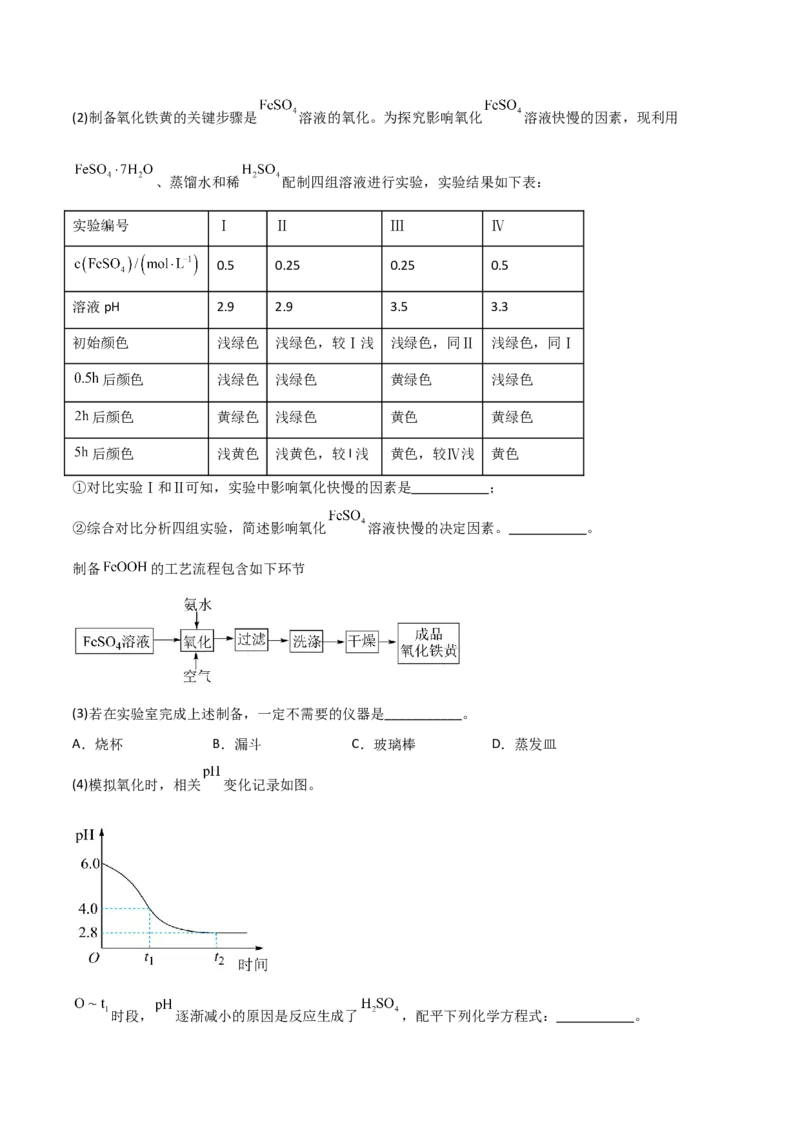
8.(2024·江西九江·二模)已知反应 的势能曲线示意图如下(…表示吸附作用,A表
示催化剂, 表示过渡态分子):下列有关说法正确的是
A.过程Ⅰ、Ⅱ、Ⅲ中都有 生成
B.若在任意温度下均能自发进行,则反应为吸热反应
C.该反应中只有两种物质能够吸附 分子
D.过程Ⅲ中最大势能垒(活化能)为
9.(2024·四川遂宁·三模)中国提出二氧化碳排放在2030年前达到峰值,2060年前实现碳中和。这体现
了中国作为全球负责任大国的环境承诺和行动决心。二氧化碳选择性加氢制甲醇是解决温室效应、发展绿
色能源和实现经济可持续发展的重要途径之一、常温常压下利用铜基催化剂实现二氧化碳选择性加氢制甲
醇的反应机理和能量变化图如下(其中吸附在催化剂表面上的粒子用*标注),下列说法错误的是
A.二氧化碳选择性加氢制甲醇是放热反应
B.催化剂能改变反应机理,加快反应速率,降低反应热C.总反应为CO (g)+3H (g)=CH OH(g)+H O(g)
2 2 3 2
D.该历程的决速步为HCOO*+4H*=CH O*+H O
3 2
10.(2024·河北·模拟预测)在水溶液中进行的反应: ,已
知该反应速率方程为 (k为常数),为探究反应速率(v)与反应物浓度的关系,在
20℃进行实验,所得的数据如下表:
① ② ③ ④ ⑤
0.008 0.008 0.004 0.008 0.008
0.001 0.001 0.001 0.002 0.001
0.10 0.20 0.20 0.10 0.40
v
1
下列结论正确的是
A.反应体系的三种物质中,H+(aq)的浓度对反应速率影响最大
B.速率常数 的数值为0.03
C.a、b、c的值分别为1、5、6
D.实验⑤中,
11.(2023·吉林长春·三模)反应 的速率方程为 (k为速率
常数,其中 , A、R为常数, 为活化能,T为开氏温度,其半衰期反应物消耗一半
所需的时间)为0.8/k。改变反应物浓度时,反应的瞬时速率如表所示。下列说法正确的是
/ 0.25 0.5 1 0.5 1
/ 0.05 0.05 0.1 0.1 0.2
v/ 1.6 3.2 3.2A.
B.
C.升温、加入催化剂,缩小容积(加压),均能使k增大,导致反应的瞬时速率加快
D.在过量的B存在时,A剩余12.5%所需的时间是
12.(2024·辽宁鞍山·二模)丙酮的溴代反应( )的速率方程为:
,其中k为速率常数,与温度有关;“ ”为反应级数。某
温度时,获得如下实验数据:
初始浓度
实验序
溴颜色消失所需时间t/s
号
HCl
① 0.80 0.20 0.0010 200
② 1.60 0.20 0.0010 100
③ 0.80 0.40 0.0010 100
④ 0.80 0.20 0.0020 400
分析该组实验数据所得出的结论错误的是
A.增大 ,能延长溶液颜色消失的时间
B.实验②和③的平均速率相等
C.实验①在200s内的平均速率
D.反应级数为2
13.(2023·上海浦东新·一模)氧化铁黄(化学式为 )是一种黄色颜料,具有非常好的耐光性和耐碱
性,是氧化铁的一水合物。工业上常以绿矾 为原料制备 。
(1)下列关于铁元素的认识正确的是___________。
A.能存在于人体的血红蛋白中 B.是地壳中含量最多的金属元素
C.单质是人类最早使用的金属 D.铁的氧化物都具有致密的结构(2)制备氧化铁黄的关键步骤是 溶液的氧化。为探究影响氧化 溶液快慢的因素,现利用
、蒸馏水和稀 配制四组溶液进行实验,实验结果如下表:
实验编号 Ⅰ Ⅱ Ⅲ Ⅳ
0.5 0.25 0.25 0.5
溶液pH 2.9 2.9 3.5 3.3
初始颜色 浅绿色 浅绿色,较Ⅰ浅 浅绿色,同Ⅱ 浅绿色,同Ⅰ
后颜色 浅绿色 浅绿色 黄绿色 浅绿色
后颜色 黄绿色 浅绿色 黄色 黄绿色
后颜色 浅黄色 浅黄色,较I浅 黄色,较Ⅳ浅 黄色
①对比实验Ⅰ和Ⅱ可知,实验中影响氧化快慢的因素是 ;
②综合对比分析四组实验,简述影响氧化 溶液快慢的决定因素。 。
制备 的工艺流程包含如下环节
(3)若在实验室完成上述制备,一定不需要的仪器是___________。
A.烧杯 B.漏斗 C.玻璃棒 D.蒸发皿
(4)模拟氧化时,相关 变化记录如图。
时段, 逐渐减小的原因是反应生成了 ,配平下列化学方程式: 。________ _______ _______=______ ______
时段,经历的反应为: ,该过程 继续平缓下降的原因可
能是: 。(任写一条)
(5)判断流程中产品是否洗涤干净的方法是: 。
氧化铁黄( )纯度可以通过产品的耗酸量确定,如下图所示。
已知: (配合离子), 不与稀碱液反应。
(6)①在溶液 中滴加 标准溶液时,发生反应的离子方程式为 ;
②若实验时加入了 的 ,消耗 ,设氧化铁黄的式量为 ,则氧化铁黄样品纯度为
;(用含 、 、 、 的代数式表示)
③测定时,若滴入 不足量,会使实验结果 (选填“偏大”、“偏小”或“无影响”)。
14.(23-24高三上·四川雅安·阶段练习)大苏打(Na S O )是一种重要的化工产品,也是实验室常用试剂。
2 2 3
某小组对大苏打展开如下探究。
实验(一):探究大苏打性质。
按如图装置进行实验,记录如下:
实验过程中发现,装置Ⅰ中产生气泡和浅黄色沉淀,试管Ⅱ中红色溶液变为无色,试管Ⅳ中红色溶液逐渐
变为浅红色,最终变为无色。
(1)装Na S O 的仪器名称是 ,其他条件相同时,若拆去热水浴,试管Ⅱ中溶液褪色速率变
2 2 3
(填“快”或“慢”)。
(2)装置Ⅰ中的离子方程式为 。(3)若试管Ⅲ中现象是红色溶液变浅,证明氧化产物为 的试剂是 。由试管Ⅳ中现象可知,电离
常数 (填“>”“<”或“=”) 。
实验(二):探究影响H SO 和Na S O 反应的速率的外界因素。
2 4 2 2 3
编 0.1mol·L-1 Na S O 溶液的体 0.1mol·L-1 H SO 溶液的体 水的体 水浴温 测定变浑浊时
2 2 3 2 4
号 积/mL 积/mL 积/mL 度/℃ 间/s
① 10.0 15.0 0 35
② 10.0 10.0 35
③ 15.0 0 45
(4) 。
(5)实验记录: 。由实验①②得出的结论是 。设计实验①③的目的是 。
实验(三):测定中x的值。
已知新制得的大苏打中往往含有结晶水,化学式可表示为,称取24.8g Na S O ·xH O溶于水配制成100mL溶
2 2 3 2
液,准确量取10.00mL配制的溶液于锥形瓶,滴加0.2mol·L-1碘水至恰好完全反应,消耗25.00mL碘水。提
示: 。
(6)Na S O ·xH O中x为 。
2 2 3 2
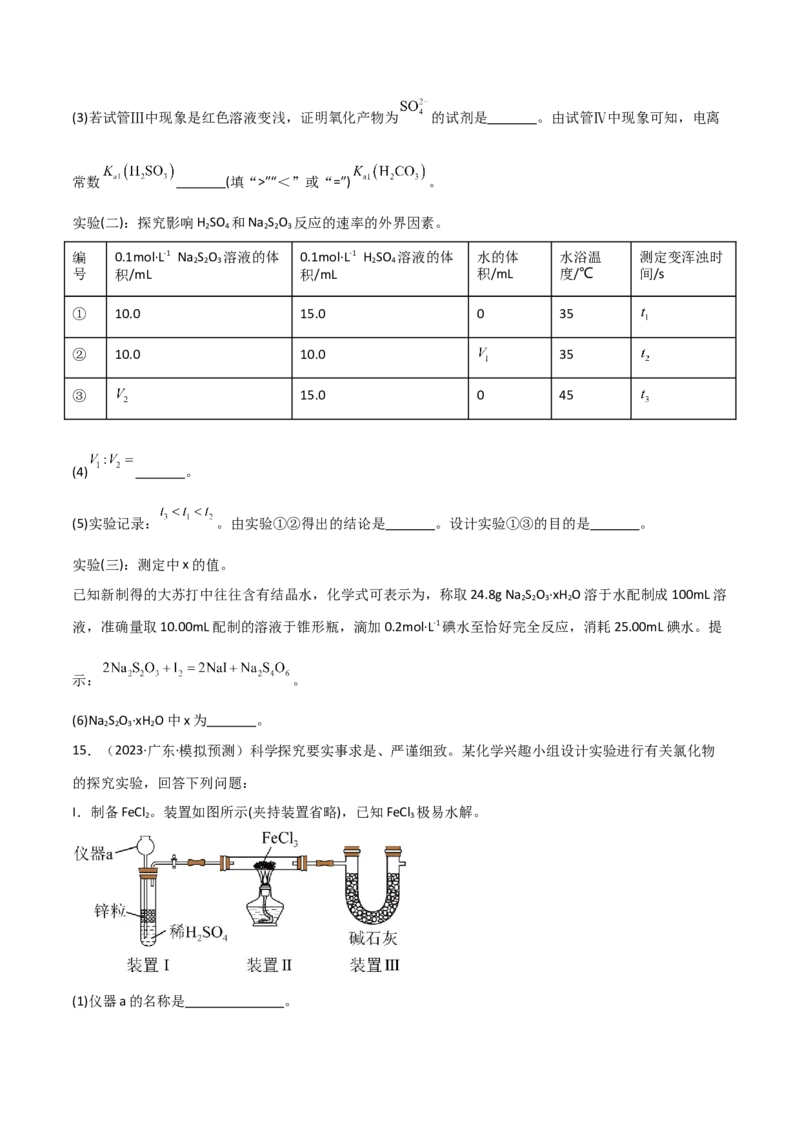
15.(2023·广东·模拟预测)科学探究要实事求是、严谨细致。某化学兴趣小组设计实验进行有关氯化物
的探究实验,回答下列问题:
I.制备FeCl 。装置如图所示(夹持装置省略),已知FeCl 极易水解。
2 3
(1)仪器a的名称是 。(2)装置II中制备FeCl 的化学方程式为 。
2
(3)该装置存在的缺陷是:① ;②缺少氢气的尾气处理装置。
II.利用惰性电极电解0.1 mol•L-1FeCl 溶液,探究外界条件对电极反应(离子放电顺序)的影响。
2
(4)实验数据如表所示:
实验编
电压/V pH 阳极现象 阴极现象
号
1 1.5 5.52 无气泡,滴加KSCN显红色 无气泡,银白色金属析出
2 3.0 5.52 少量气泡,滴加KSCN显红色 无气泡,银白色金属析出
3 4.5 5.52 大量气泡,滴加KSCN显红色 较多气泡,极少量金属析出
4 1.5 1.00 无气泡,滴加KSCN显红色 较多气泡,极少量金属析出
①由实验1、2现象可以得出结论:增大电压, 优先于 放电;
②若由实验1、4现象可以得出结论: 。
II.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
实验编
c(NH Cl)/mol·L-1 温度/℃ 待测物理量 实验目的
号 4
5 0.5 30 a ——
6 1.5 i b 探究浓度对氯化铵水解平衡的影响
7 0.5 35 c ii
8 2.0 40 d 探究温度、浓度同时对氯化铵水解平衡的影响
(5)该实验限选药品和仪器:恒温水浴、pH传感器、烧杯、0.1mol.L-1硝酸银溶液、蒸馏水和各种浓度的
NH Cl溶液。
4
①实验中,“待测物理量”是 ;
②实验目的ii是 ;
③上述表格中,b d(填“>”、“<”或“=”)。
16.(2023·广东·一模)海洋中有丰富的NaCl资源。研究表明,氯离子的侵入是造成钢筋混凝土腐蚀的主
要原因(Na+对腐蚀无影响)。海砂经淡化后,Cl-的含量达到一定标准才能作建筑用砂。某合作学习小组猜测
Cl-会加快金属与盐溶液或酸溶液的反应速率。
(1)工业上通过电解饱和NaCl溶液制Cl 的离子方程式为 。
2
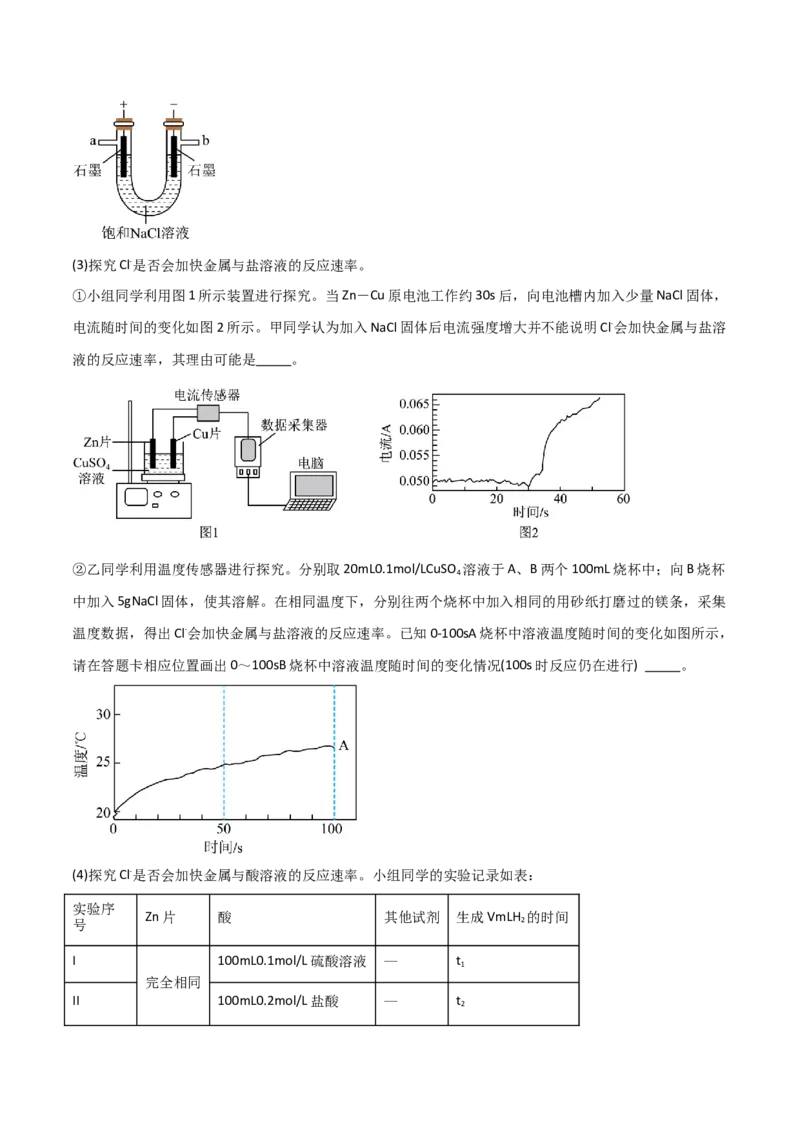
(2)实验室用如图所示装置模拟工业上制Cl 。检验产生的Cl 的操作及现象是 。
2 2(3)探究Cl-是否会加快金属与盐溶液的反应速率。
①小组同学利用图1所示装置进行探究。当Zn-Cu原电池工作约30s后,向电池槽内加入少量NaCl固体,
电流随时间的变化如图2所示。甲同学认为加入NaCl固体后电流强度增大并不能说明Cl-会加快金属与盐溶
液的反应速率,其理由可能是 。
②乙同学利用温度传感器进行探究。分别取20mL0.1mol/LCuSO 溶液于A、B两个100mL烧杯中;向B烧杯
4
中加入5gNaCl固体,使其溶解。在相同温度下,分别往两个烧杯中加入相同的用砂纸打磨过的镁条,采集
温度数据,得出Cl-会加快金属与盐溶液的反应速率。已知0-100sA烧杯中溶液温度随时间的变化如图所示,
请在答题卡相应位置画出0~100sB烧杯中溶液温度随时间的变化情况(100s时反应仍在进行) 。
(4)探究Cl-是否会加快金属与酸溶液的反应速率。小组同学的实验记录如表:
实验序
Zn片 酸 其他试剂 生成VmLH 的时间
号 2
I 100mL0.1mol/L硫酸溶液 — t
1
完全相同
II 100mL0.2mol/L盐酸 — t
2III 100mLamol/L硫酸溶液 少量b t
3
其中,t >t ,t >t 。
1 2 1 3
①由实验I和实验II (填“能”或“不能”)推知Cl-会加快金属与酸溶液的反应速率,理由是 。
②小组同学一致认为,由实验I和实验III可推知Cl-会加快金属与酸溶液的反应速率,则实验III中,a处填
,b处填 。
(5)提出一种合理的降低海砂中Cl-含量的方法: 。