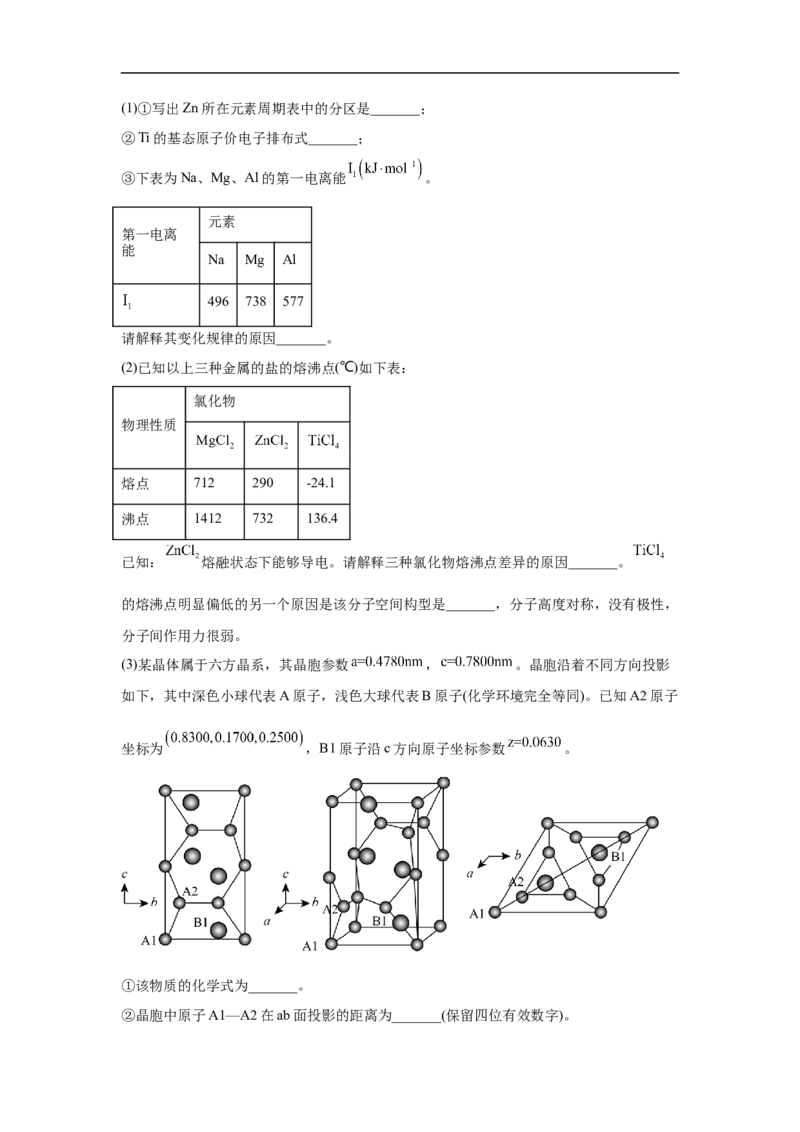文档内容
易错点 13 原子结构与核外电子排布
易错题【01】原子轨道与能级
①第一能层(K)只有s能级,有1个原子轨道;第二能层(L)有s、p两种能级,有4个原子轨
道;第三能层(M)有s、p、d三种能级,有9个原子轨道。
②同一能级的不同原子轨道具有相同的能量(如2p、2p、2p 的能量相同)。
x y z
③不同能层的同种原子轨道具有的能量随能层序数(n)增大而升高,如能量:1s<2s<3s
等。
易错题【02】核外电子排布式
①能量最低原理:在构建基态原子时,电子将尽可能地占据能量最低的原子轨道,使整个
原子的能量最低。“能量最低的原子轨道”指的是电子填入后使整个原子能量达到最低的
轨道。
②洪特规则特例:当能量相同的原子轨道(简并轨道)在全满(p6、d10、f14)、半满(p3、d5、
f7)或全空(p0、d0、f0)状态时,体系较稳定,体系的能量最低。例如, Cr的电子排布式为
24
1s22s22p63s23p63d54s1。
易错题【03】原子核外电子排布的常见错误
(1)在写基态原子的轨道表示式时,常出现以下错误:
① (违反能量最低原理)
② (违反泡利原理)
③ (违反洪特规则)
④ (违反洪特规则)
(2)当出现d轨道时,虽然电子按ns、(n-1)d、np的顺序填充,但在书写电子排布式时,
仍把(n-1)d放在ns前,如Fe:1s22s22p63s23p63d64s2,而失电子时,却先失4s轨道上的电
子,如Fe3+:1s22s22p63s23p63d5。
(3)注意比较原子核外电子排布式、简化电子排布式、价电子排布式的区别与联系。如
Cu的电子排布式:1s22s22p63s23p63d104s1;简化电子排布式:[Ar]3d104s1;价电子排布式:
3d104s1。
易错题【04】核外空间运动状态
(1)判断核外电子的空间运动状态
①判断依据:核外电子的空间运动状态种类数=原子核外电子占据的原子轨道数。
②方法:先写出基态原子(或离子)的核外电子排布式,结合泡利原理和洪特规则,确定价电子轨道表示式,再确定电子占据轨道数,即核外电子的空间运动状态种类。
(2)判断核外电子的运动状态:原子核外不同电子的运动状态不同,故核外电子的运动状
态种类=核外电子总数。
典例分析
例题1、基态Fe原子的价层电子排布式为___________。
(2)基态硫原子价电子排布式为__________。
(3)基态硅原子最外层的电子排布图(轨道表示式)为 。
【解析】(1)基态Fe原子核外有26个电子,核外电子排布式为[Ar]3d64s2,则其价电子层
的电子排式为3d64s2。
(2)基态S原子的核外电子排布式为3s23p4,则基态硫原子的价电子排式为3s23p4。
(3)基态Si原子的价电子层的电子排式为3s23p2,根据泡利原理、洪特规则和能量最低原
理推知,Si的最外层的电子排布图(轨道表示式)为 。
【答案】(1)3d64s2 (2)3s23p4 (3)
例题2、(1)基态F原子核外电子的运动状态有 种。
(2)对于基态Cr原子,下列叙述正确的是_______(填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和
为 。
【解析】(1)基态F原子共有9个核外电子,则每个电子都有对应的轨道和自旋状态,所
以核外电子的运动状态有9种;
(2)基态原子满足能量最低原理,Cr有24个核外电子,轨道处于半充满时体系总能量低,核外电子排布应为 ,A正确; Cr核外电子排布为 ,由于能级交错,3d
轨道能量高于4s轨道的能量,即3d电子能量较高,B错误;电负性为原子对键合电子的吸
引力,同周期除零族原子序数越大电负性越强,钾与铬位于同周期,铬原子序数大于钾,
故铬电负性比钾高,原子对键合电子的吸引力比钾大,C正确。
(3)对于基态的磷原子,其价电子排布式为 ,其中3s轨道的2个电子自旋状态相
反,自旋磁量子数的代数和为0;根据洪特规则可知,其3p轨道的3个电子的自旋状态相
同,因此,基态磷原子的价电子的自旋磁量子数的代数和为 或 。
【答案】(1)9 (2)A (3) 或
例题3、(1)在KH PO 的四种组成元素各自所能形成的简单离子中,核外电子排布相同
2 4
的是 (填离子符号)。
(2)Fe基态核外电子排布式为 。
(3)Al在周期表中的位置 ;基态Zn的价层电子排布式
。
(4)基态Ti原子的核外电子排布式为 。
【解析】(1)四种组成元素形成的简单离子为K+、H+(或H—)、P3—、O2—,其中K+和
P3—的核外电子排布相同,均与Ar原子相同。
(2)Fe是26号元素,基态Fe原子核外电子排布式为1s22s22p63s23p63d64s2或[Ar]3d64s2。
(3)Al的核外电子排布为[Ne]3s23p1,故Al在周期表中处于第三周期第IIIA族。基态Zn
原子核外电子排布式为[Ar]3d104s2,则其层电子排布式为3d104s2。
(4)Ti原子核外有22个电子,基态Ti原子的核外电子排布式为1s22s22p63s23p63d24s2或
[Ar]3d24s2。
【答案】(1)K+和P3— (2)1s22s22p63s23p63d64s2或[Ar]3d64s2
(3)第三周期第IIIA族 3d104s2 (4)s22s22p63s23p63d24s2或[Ar]3d24s21.(2022·江苏·高考真题)工业上电解熔融 和冰晶石 的混合物可制得铝。
下列说法正确的是
A.半径大小: B.电负性大小:
C.电离能大小: D.碱性强弱:
2.(2022·海南·高考真题)钠和钾是两种常见金属,下列说法正确的是
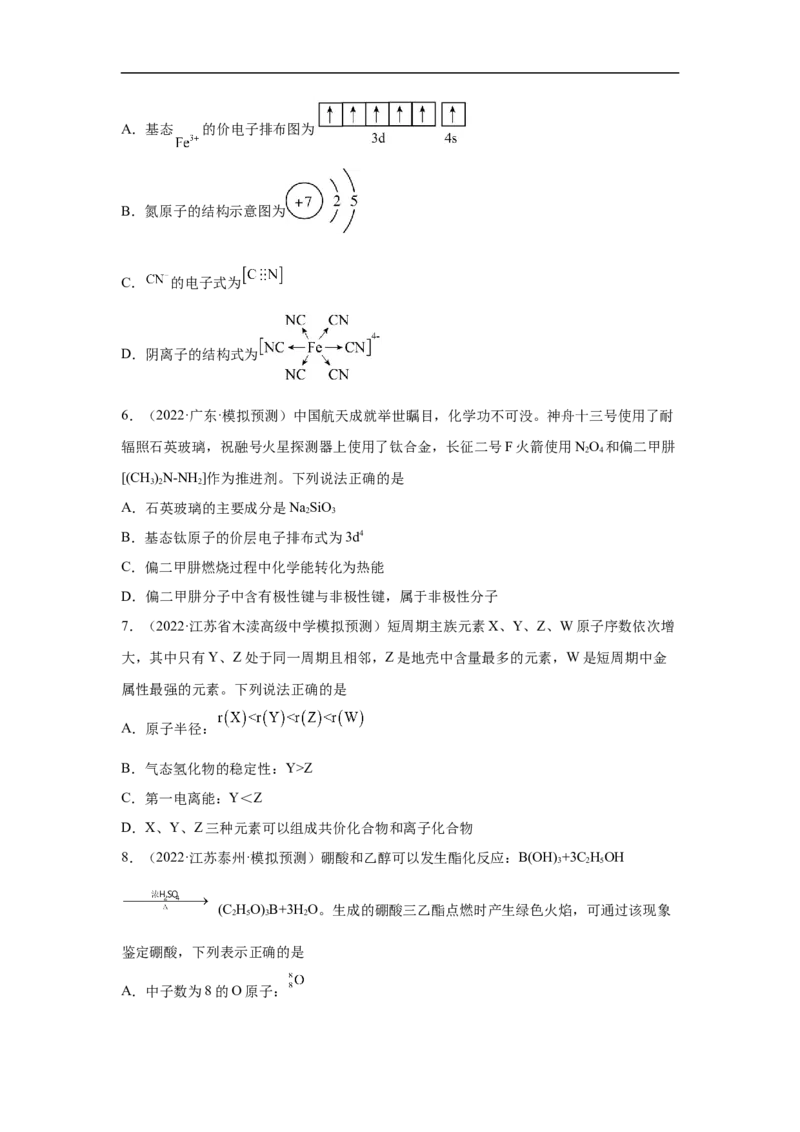
A.钠元素的第一电离能大于钾 B.基态钾原子价层电子轨道表示式为
C.钾能置换出NaCl溶液中的钠 D.钠元素与钾元素的原子序数相差18
3.(2022·辽宁·高考真题)短周期元素X、Y、Z、W、Q原子序数依次增大。基态X、
Z、Q原子均有两个单电子,W简单离子在同周期离子中半径最小,Q与Z同主族。下列
说法错误的是
A.X能与多种元素形成共价键 B.简单氢化物沸点:
C.第一电离能: D.电负性:
4.(2022·广东深圳·一模)已知X、Y、Z、W、M为原子序数依次递增的短周期元素,其
中X、Y、Z元素同周期, Y与W元素同主族,它们可以形成一种重要化合物甲。其结构
如图所示。下列说法正确的是
A.原子半径:M>W>Z B.第一电离能:Y>Z>X
C.氢化物的沸点:Z>Y>X D.甲中W的杂化方式为sp2
5.(2022·广东深圳·一模)亚铁氰化铁又名普鲁士蓝,化学式为 ,是一种
配位化合物,可以用来上釉、用作油画染料等。下列有关普鲁士蓝构成微粒的符号表征正
确的是A.基态 的价电子排布图为
B.氮原子的结构示意图为
C. 的电子式为
D.阴离子的结构式为
6.(2022·广东·模拟预测)中国航天成就举世瞩目,化学功不可没。神舟十三号使用了耐
辐照石英玻璃,祝融号火星探测器上使用了钛合金,长征二号F火箭使用NO 和偏二甲肼
2 4
[(CH )N-NH]作为推进剂。下列说法正确的是
3 2 2
A.石英玻璃的主要成分是NaSiO
2 3
B.基态钛原子的价层电子排布式为3d4
C.偏二甲肼燃烧过程中化学能转化为热能
D.偏二甲肼分子中含有极性键与非极性键,属于非极性分子
7.(2022·江苏省木渎高级中学模拟预测)短周期主族元素X、Y、Z、W原子序数依次增
大,其中只有Y、Z处于同一周期且相邻,Z是地壳中含量最多的元素,W是短周期中金
属性最强的元素。下列说法正确的是
A.原子半径:
B.气态氢化物的稳定性:Y>Z
C.第一电离能:Y<Z
D.X、Y、Z三种元素可以组成共价化合物和离子化合物
8.(2022·江苏泰州·模拟预测)硼酸和乙醇可以发生酯化反应:B(OH) +3C HOH
3 2 5
(C HO) B+3H O。生成的硼酸三乙酯点燃时产生绿色火焰,可通过该现象
2 5 3 2
鉴定硼酸,下列表示正确的是
A.中子数为8的O原子:B.乙醇分子的比例模型:
C.基态C原子核外价电子的轨道表达式:
D.硼酸在水中的电离方程式:B(OH) +H O=B(OH) +H+
3 2
9.(2022·江苏泰州·模拟预测)我国“祝融号”火星车成功着陆火星,其矿脉中含有原子
序数依次增大的短周期主族元素W、X、Y、Z。已知W、Z同主族,且Z的原子序数是W
的2倍,X的氢化物可用于蚀刻玻璃,Y与Z最外层电子数之和等于8。下列说法正确的是
A.离子半径:Z>Y>W>X
B.同周期第一电离能小于Z的元素有4种
C.X与Y可形成共价化合物YX
2
D.简单氢化物的还原性:W的氢化物>Z的氢化物
10.(2022·山东省实验中学模拟预测)含有N 、N 的材料Pb(N )、NAsF 可以用于炸药。
3 2 5 6
下列说法正确的是
A.Pb属于d区元素
B.基态As原子的d轨道与p轨道上的电子数之比为3:2
C.N 的空间构型为直线形
D.基态F原子中,核外电子的空间运动状态有9种
11.(2022·湖北·襄阳四中模拟预测)下列有关Fe、Co、Ni及其化合物的说法错误的是
A.Fe、 Co、Ni 均位于第四周期第VIII族
B.Fe、 Co、Ni 基态原子未成对电子数分别为4、3、2
C.Fe、 Co、Ni以及它们的合金为黑色金属材料
D.FeO 在空气中受热会迅速变为Fe O
3 4
12.(2022·山东聊城一中高三期末)短周期主族元素X、Y、Z、W的原子序数依次增大,
X与Y同族但不相邻,基态Z原子价电子排布nsn-1npn+1。下列说法正确的是
A.简单离子半径:W>Z>Y>X B.简单阴离子还原性:Z>W
C.电负性:Z>W D.Z与W的简单气态氢化物沸点Z>W
13.(2022·内蒙古赤峰·模拟预测)材料的发展水平始终是时代进步和人类文明的标志。
当前含铁的磁性材料在国防、电子信息等领域中具有广泛应用。请回答下列问题:(1)基态铁原子的价电子排布图为_______,基态铁原子核外电子的空间运动状态有_______
种, 其处在最高能层的电子的电子云形状为_______。
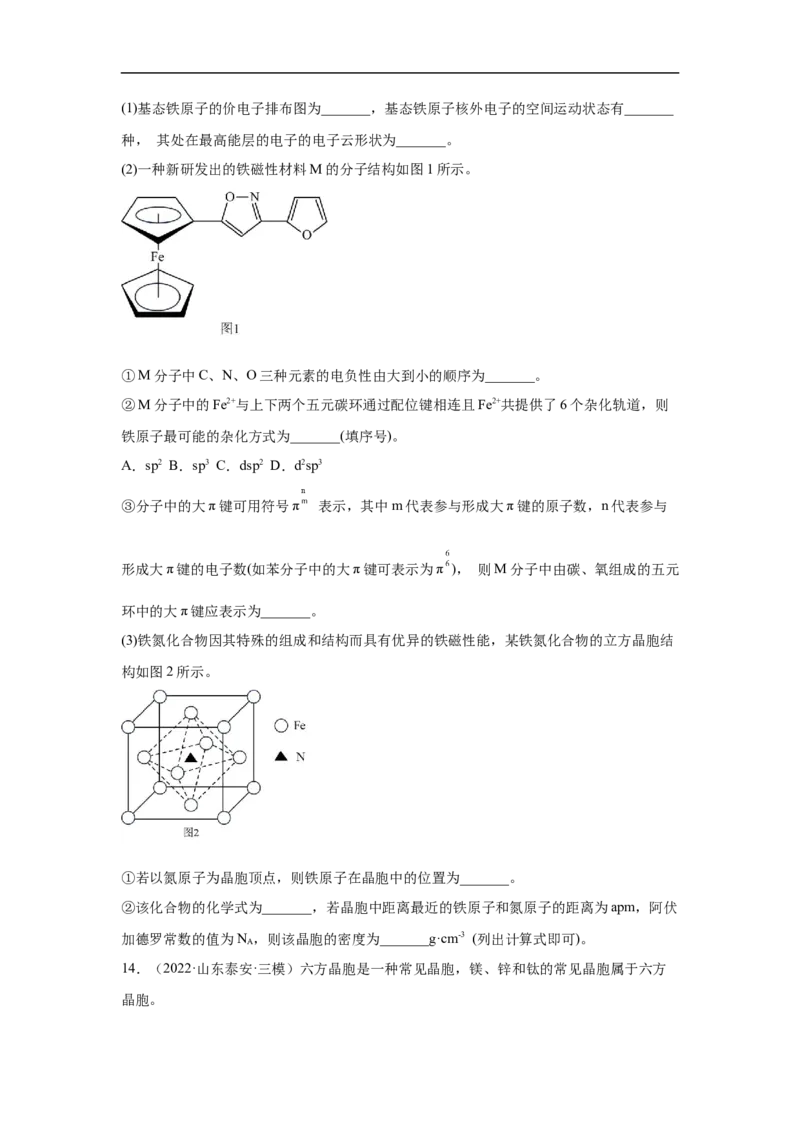
(2)一种新研发出的铁磁性材料M的分子结构如图1所示。
①M分子中C、N、O三种元素的电负性由大到小的顺序为_______。
②M分子中的Fe2+与上下两个五元碳环通过配位键相连且Fe2+共提供了6个杂化轨道,则
铁原子最可能的杂化方式为_______(填序号)。
A.sp2 B.sp3 C.dsp2 D.d2sp3
③分子中的大π键可用符号π 表示,其中m代表参与形成大π键的原子数,n代表参与
形成大π键的电子数(如苯分子中的大π键可表示为π ), 则M分子中由碳、氧组成的五元
环中的大π键应表示为_______。
(3)铁氮化合物因其特殊的组成和结构而具有优异的铁磁性能,某铁氮化合物的立方晶胞结
构如图2所示。
①若以氮原子为晶胞顶点,则铁原子在晶胞中的位置为_______。
②该化合物的化学式为_______,若晶胞中距离最近的铁原子和氮原子的距离为apm,阿伏
加德罗常数的值为N ,则该晶胞的密度为_______g·cm-3 (列出计算式即可)。
A
14.(2022·山东泰安·三模)六方晶胞是一种常见晶胞,镁、锌和钛的常见晶胞属于六方
晶胞。(1)①写出Zn所在元素周期表中的分区是_______;
②Ti的基态原子价电子排布式_______;
③下表为Na、Mg、Al的第一电离能 。
元素
第一电离
能
Na Mg Al
496 738 577
请解释其变化规律的原因_______。
(2)已知以上三种金属的盐的熔沸点(℃)如下表:
氯化物
物理性质
熔点 712 290 -24.1
沸点 1412 732 136.4
已知: 熔融状态下能够导电。请解释三种氯化物熔沸点差异的原因_______。
的熔沸点明显偏低的另一个原因是该分子空间构型是_______,分子高度对称,没有极性,
分子间作用力很弱。
(3)某晶体属于六方晶系,其晶胞参数 , 。晶胞沿着不同方向投影
如下,其中深色小球代表A原子,浅色大球代表B原子(化学环境完全等同)。已知A2原子
坐标为 ,B1原子沿c方向原子坐标参数 。
①该物质的化学式为_______。
②晶胞中原子A1—A2在ab面投影的距离为_______(保留四位有效数字)。③B1原子坐标参数为_______。
15.(2022·新疆昌吉·二模)2022年2月我国科学家在《科学》杂志发表反型钙钛矿太阳
能电池研究方面的最新科研成果论文,为钙钛矿电池研究开辟新方向。
(1)基态钛原子的p 原子轨道上的电子数为_______个。 与钛同周期的第ⅡA族和ⅢA族两
y
种元素中第一电离能较大的是_______ (写 元素符号)。。
(2)Ti的配合物有多种。在Ti(CO) 、T(HO) 和TiF 三种微粒的配体中,所含原子电负性
6 2
由大到小排序后,排第3位的元素是_______(写元素符号), Ti(HO) 中∠H-O-
2
H_______(填大于、小于或等于)单个水分子中∠H-O-H,原因为_______ ; Ti(NO ) 的球
3 4
棍结构如图,Ti 的配位数是_______,N原子的杂化方式为_______, 与NO 互为等电子
体的分子为_______ (写分子式)
(3)钛白粉学名为二氧化钛,它是一种染料及颜料,其化学式为TiO,如图为TiO 的晶胞结
2 2
构图,回答:已知微粒1、2的坐标分别为(0,0, 0)和(0.31, 0.31, 0), 则微粒3的坐
标为_______ ; 设阿伏加德罗常数的值为N ,TiO 的密度为_______g·cm-3(列出计算式)。
A 2
16.(2022·重庆·二模)研究发现,火星岩的主要成分有KO、CaO、NaO、MgO、
2 2
Al O、Fe O、FeO、SiO 和HO。
2 3 2 3 2 2
(1)基态铁原子的价层电子排布式为_______。
(2)Na、Mg、Al的第一电离能由大到小的是_______。
(3)AlO 溶于NaOH溶液生成Na[Al(OH) [Al(OH) ]-中Al的杂化类型是_______。
2 3 4, 4(4)实验室用K[Fe(CN) ]检验Fe2+,[Fe(CN) ]3-中σ键、π键数目之比为_______。
3 6 6
(5)晶体熔点:KO_______(填“>”或“<”)CaO,原因是_______。
2
(6)已知铁和镁形成的晶胞如图所示:
①在该晶胞中铁的配位数为_______。
②图中a处原子坐标参数为_______。
③已知该晶胞密度为ρg/cm3,N 为阿伏加德罗常数的值。该晶胞中Fe原子与Mg原子的最
A
近距离是_______pm(用含N 、ρ的代数式表示)。
A