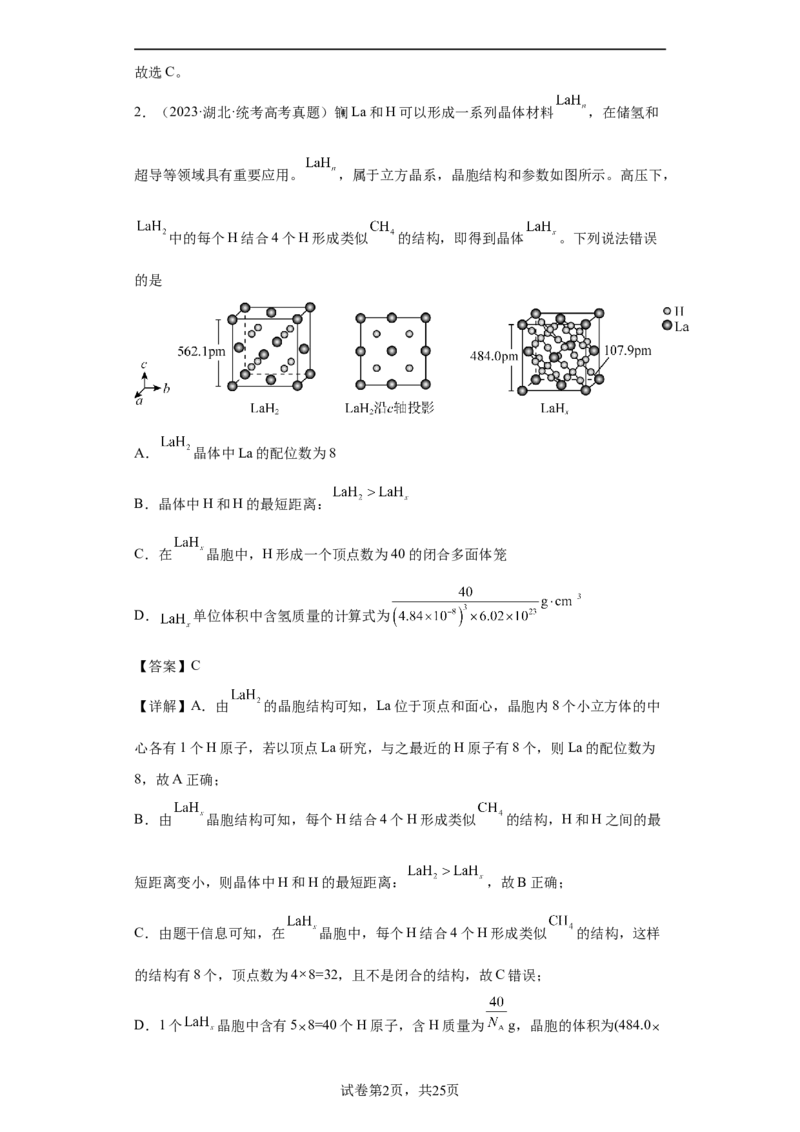文档内容
专项训练 晶胞结构与物质的性质(解析版)
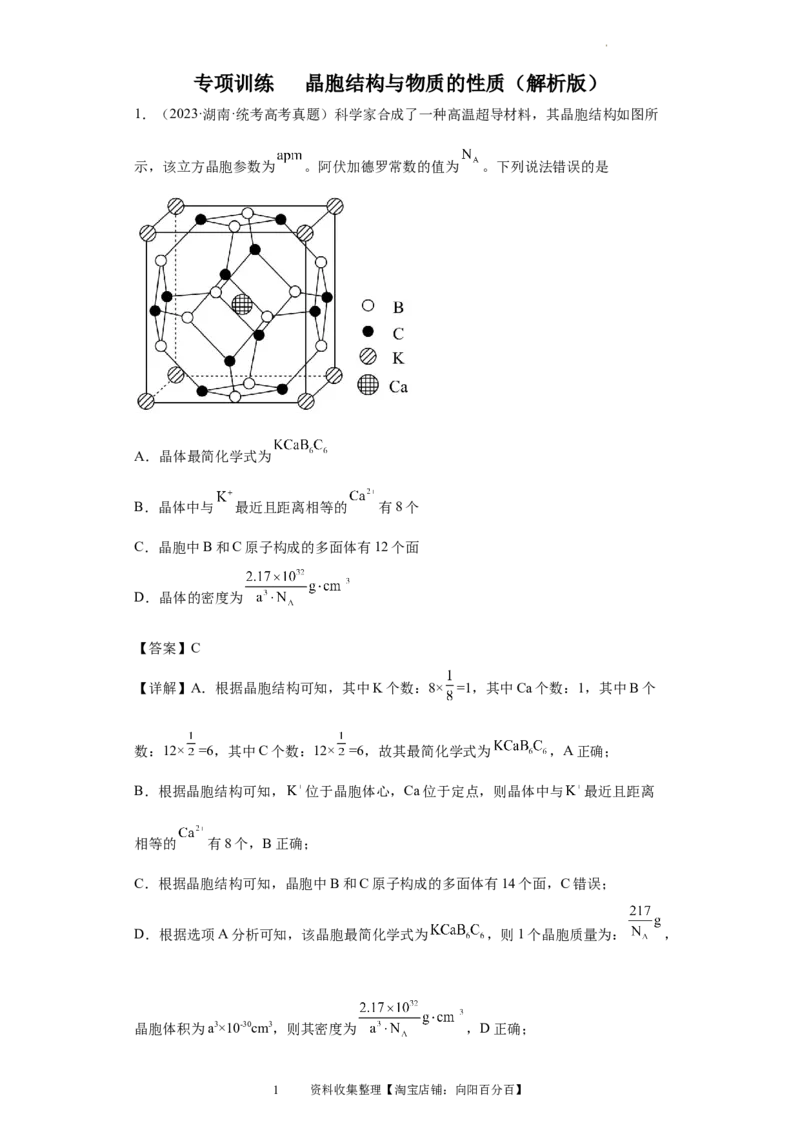
1.(2023·湖南·统考高考真题)科学家合成了一种高温超导材料,其晶胞结构如图所
示,该立方晶胞参数为 。阿伏加德罗常数的值为 。下列说法错误的是
A.晶体最简化学式为
B.晶体中与 最近且距离相等的 有8个
C.晶胞中B和C原子构成的多面体有12个面
D.晶体的密度为
【答案】C
【详解】A.根据晶胞结构可知,其中K个数:8× =1,其中Ca个数:1,其中B个
数:12× =6,其中C个数:12× =6,故其最简化学式为 ,A正确;
B.根据晶胞结构可知, 位于晶胞体心,Ca位于定点,则晶体中与 最近且距离
相等的 有8个,B正确;
C.根据晶胞结构可知,晶胞中B和C原子构成的多面体有14个面,C错误;
D.根据选项A分析可知,该晶胞最简化学式为 ,则1个晶胞质量为: ,
晶胞体积为a3×10-30cm3,则其密度为 ,D正确;
1 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司故选C。
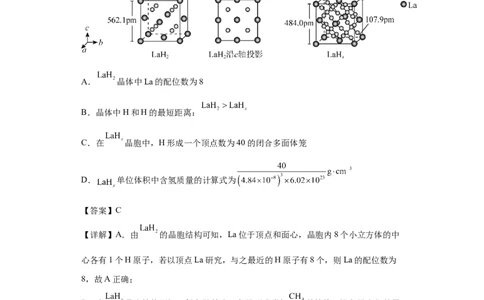
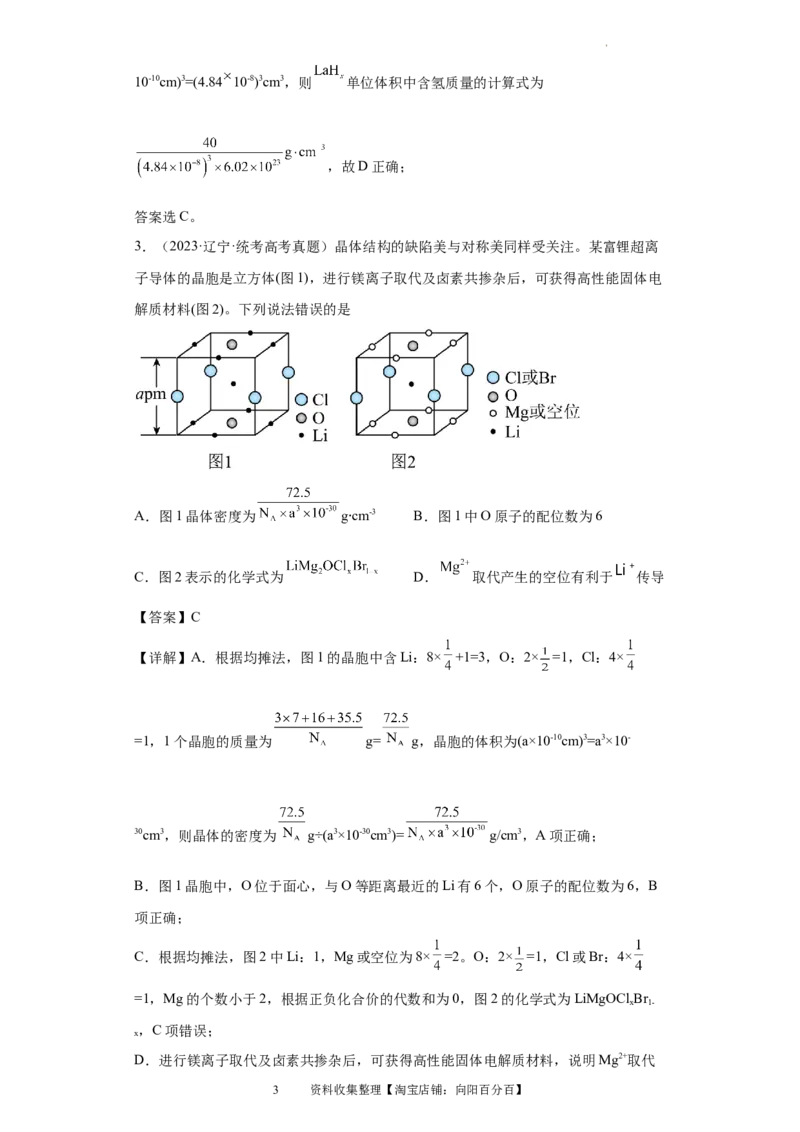
2.(2023·湖北·统考高考真题)镧La和H可以形成一系列晶体材料 ,在储氢和
超导等领域具有重要应用。 ,属于立方晶系,晶胞结构和参数如图所示。高压下,
中的每个H结合4个H形成类似 的结构,即得到晶体 。下列说法错误
的是
A. 晶体中La的配位数为8
B.晶体中H和H的最短距离:
C.在 晶胞中,H形成一个顶点数为40的闭合多面体笼
D. 单位体积中含氢质量的计算式为
【答案】C
【详解】A.由 的晶胞结构可知,La位于顶点和面心,晶胞内8个小立方体的中
心各有1个H原子,若以顶点La研究,与之最近的H原子有8个,则La的配位数为
8,故A正确;
B.由 晶胞结构可知,每个H结合4个H形成类似 的结构,H和H之间的最
短距离变小,则晶体中H和H的最短距离: ,故B正确;
C.由题干信息可知,在 晶胞中,每个H结合4个H形成类似 的结构,这样
的结构有8个,顶点数为4 8=32,且不是闭合的结构,故C错误;
D.1个 晶胞中含有5 8=40个H原子,含H质量为 g,晶胞的体积为(484.0
试卷第2页,共25页10-10cm)3=(4.84 10-8)3cm3,则 单位体积中含氢质量的计算式为
,故D正确;
答案选C。
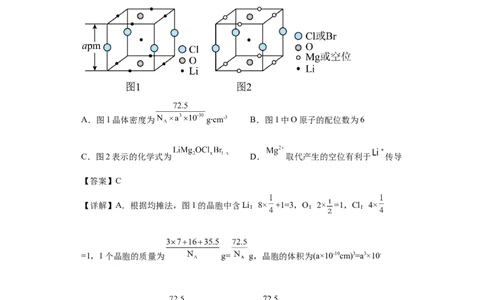
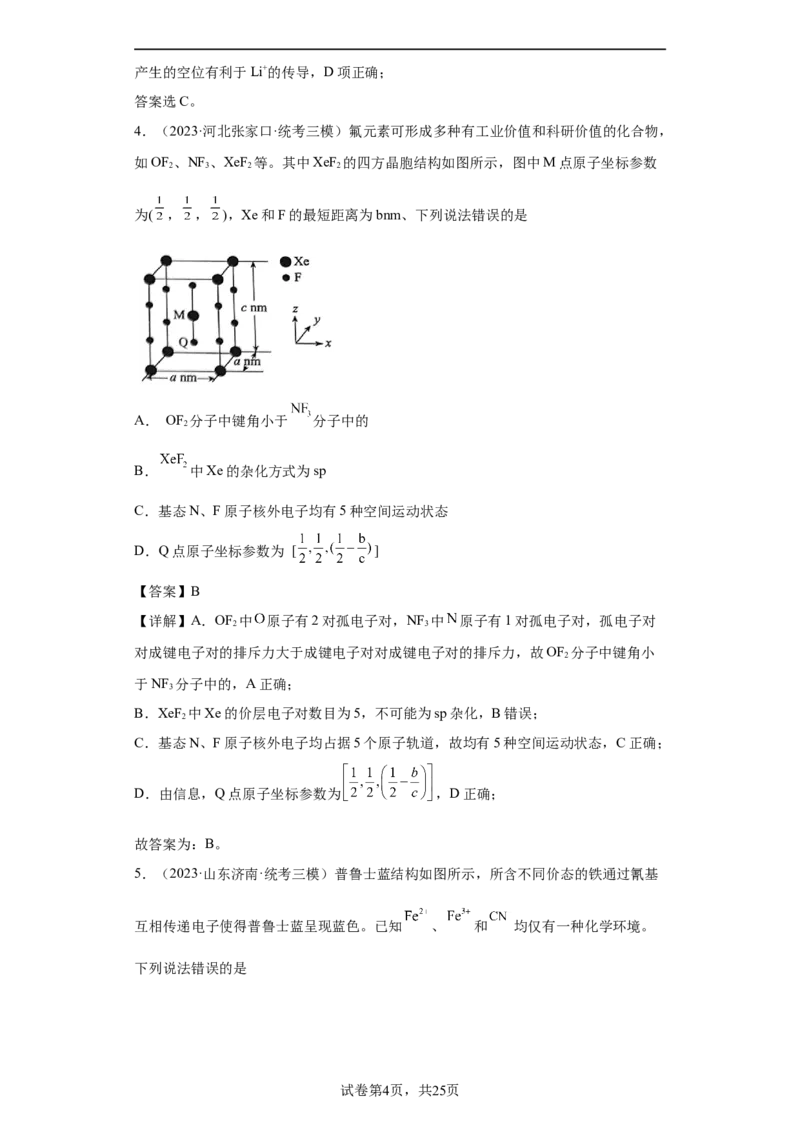
3.(2023·辽宁·统考高考真题)晶体结构的缺陷美与对称美同样受关注。某富锂超离
子导体的晶胞是立方体(图1),进行镁离子取代及卤素共掺杂后,可获得高性能固体电
解质材料(图2)。下列说法错误的是
A.图1晶体密度为 gcm-3 B.图1中O原子的配位数为6
∙
C.图2表示的化学式为 D. 取代产生的空位有利于 传导
【答案】C
【详解】A.根据均摊法,图1的晶胞中含Li:8× +1=3,O:2× =1,Cl:4×
=1,1个晶胞的质量为 g= g,晶胞的体积为(a×10-10cm)3=a3×10-
30cm3,则晶体的密度为 g÷(a3×10-30cm3)= g/cm3,A项正确;
B.图1晶胞中,O位于面心,与O等距离最近的Li有6个,O原子的配位数为6,B
项正确;
C.根据均摊法,图2中Li:1,Mg或空位为8× =2。O:2× =1,Cl或Br:4×
=1,Mg的个数小于2,根据正负化合价的代数和为0,图2的化学式为LiMgOCl Br
x 1-
,C项错误;
x
D.进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料,说明Mg2+取代
3 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司产生的空位有利于Li+的传导,D项正确;
答案选C。
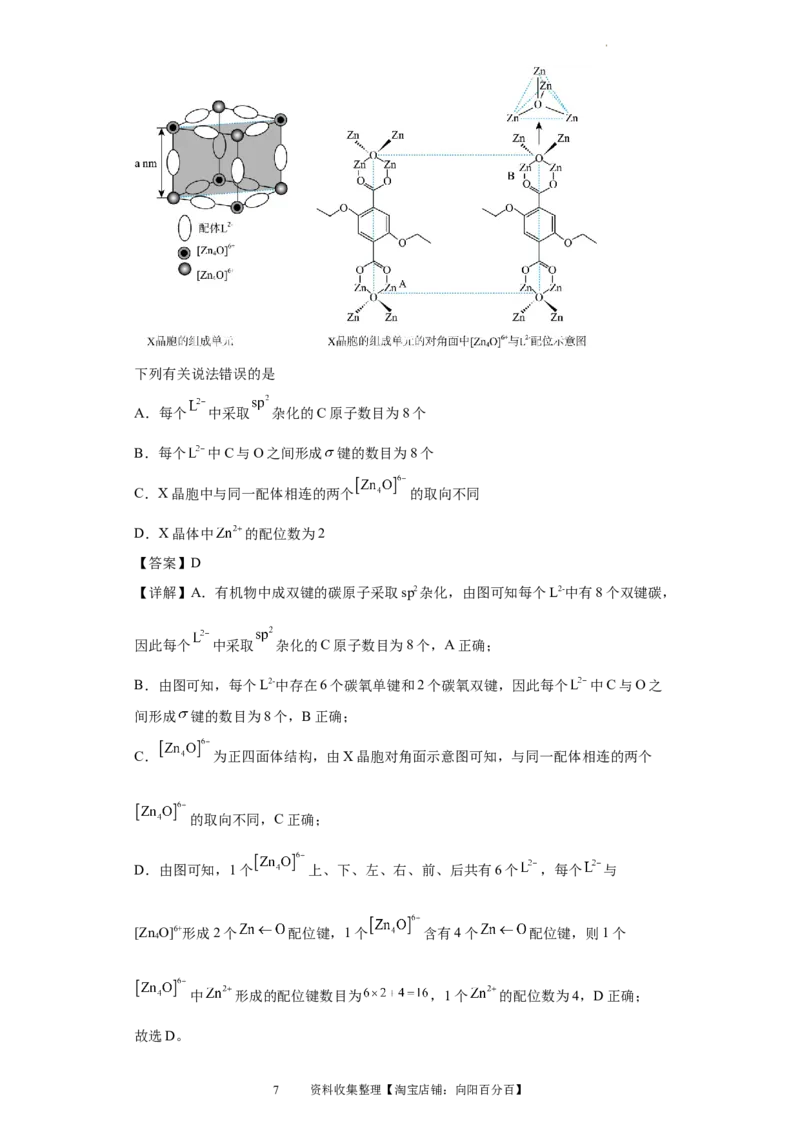
4.(2023·河北张家口·统考三模)氟元素可形成多种有工业价值和科研价值的化合物,
如OF 、NF 、XeF 等。其中XeF 的四方晶胞结构如图所示,图中M点原子坐标参数
2 3 2 2
为( , , ),Xe和F的最短距离为bnm、下列说法错误的是
A. OF 分子中键角小于 分子中的
2
B. 中Xe的杂化方式为sp
C.基态N、F原子核外电子均有5种空间运动状态
D.Q点原子坐标参数为 [ ]
【答案】B
【详解】A.OF 中 原子有2对孤电子对,NF 中 原子有1对孤电子对,孤电子对
2 3
对成键电子对的排斥力大于成键电子对对成键电子对的排斥力,故OF 分子中键角小
2
于NF 分子中的,A正确;
3
B.XeF 中Xe的价层电子对数目为5,不可能为sp杂化,B错误;
2
C.基态N、F原子核外电子均占据5个原子轨道,故均有5种空间运动状态,C正确;
D.由信息,Q点原子坐标参数为 ,D正确;
故答案为:B。
5.(2023·山东济南·统考三模)普鲁士蓝结构如图所示,所含不同价态的铁通过氰基
互相传递电子使得普鲁士蓝呈现蓝色。已知 、 和 均仅有一种化学环境。
下列说法错误的是
试卷第4页,共25页A.C、N均为sp杂化 B.
C.图示结构不是一个晶胞 D.一个晶胞中有2个
【答案】D
【分析】由题干可知,所含不同价态的铁通过氰基互相传递电子使得普鲁士蓝呈现蓝
色,且 、 和 均仅有一种化学环境,则亚铁离子与铁离子位于顶点且间隔
排列,故
【详解】A.碳碳氮之间形成叁键,为直线形,C、N均为sp杂化,A正确;
B.由分析可知, ,B正确;
C.晶胞是构成晶体的最基本的几何单元,可以前后左右上下平移得到相同结构并能与
其无隙并置;由图可知,该结构平移不能相同结构,不是一个晶胞,C正确;
D.根据“均摊法”,该结构中含 个Fe, ,则含有 个
,结合C分析可知,该结构为晶胞的 ,则一个晶胞中有 ×8=4个 ,D错误;
故选D。
6.(2023·山东泰安·统考三模)氯化铜是共价化合物,通常用作有机和无机反应催化
剂、媒染剂等。 溶液与乙二胺( )可形成配离子 (En
是乙二胺的简写),如图所示,下列说法中错误的是
5 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司A.基态 的未成对电子数为1
B.配离子 中N原子提供孤对电子
C.乙二胺和三甲胺 均属于胺,沸点更高的是三甲胺
D.配离子 中涉及的元素的电负性由大到小的顺序为N>C>H>Cu
【答案】C
【详解】A.铜元素的原子序数为29,基态铜离子的价电子排布式为3d9,离子中的未
成对电子数为1,故A正确;
B.由图可知,配离子的中心离子为具有空轨道的铜离子,乙二胺分子为配体,分子中
具有孤对电子的氮原子提供孤对电子,故B正确;
C.乙二胺能形成分子间氢键,三甲胺不能形成分子间氢键,则乙二胺的分子间作用力
大于三甲胺,沸点高于三甲胺,故C错误;
D.金属元素的电负性小于非金属元素,元素的非金属性越强,电负性越大,则配离
子中四种元素的电负性由大到小的顺序为N>C>H>Cu,故D正确;
故选C。
7.(2023·辽宁沈阳·统考三模)配位化合物X由配体 和具有正四面体结构的
组成。化合物X晶体具有面心立方结构,其晶胞由8个结构相似的组成单元
(如图)构成。
试卷第6页,共25页下列有关说法错误的是
A.每个 中采取 杂化的C原子数目为8个
B.每个 中C与O之间形成 键的数目为8个
C.X晶胞中与同一配体相连的两个 的取向不同
D.X晶体中 的配位数为2
【答案】D
【详解】A.有机物中成双键的碳原子采取sp2杂化,由图可知每个L2-中有8个双键碳,
因此每个 中采取 杂化的C原子数目为8个,A正确;
B.由图可知,每个L2-中存在6个碳氧单键和2个碳氧双键,因此每个 中C与O之
间形成 键的数目为8个,B正确;
C. 为正四面体结构,由X晶胞对角面示意图可知,与同一配体相连的两个
的取向不同,C正确;
D.由图可知,1个 上、下、左、右、前、后共有6个 ,每个 与
[Zn O]6+形成2个 配位键,1个 含有4个 配位键,则1个
4
中 形成的配位键数目为 ,1个 的配位数为4,D正确;
故选D。
7 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司8.(2023·辽宁·校联考三模)一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如
图所示,晶胞棱边夹角均为90,晶体中Te原子填充在Cu、In围成的四面体空隙中,
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数
坐标,如A点、B点原子的分数坐标分别为(0,0,0)、( , , ),下列说法错误
的是
A.该晶体的化学式为CuInTe
2
B.C点原子的分数坐标为( , , )
C.晶胞中四面体空隙的占有率为50%
D.晶胞中C、D间距离d= pm
【答案】D
【详解】A.晶胞中位于顶点、面上、和体内的Cu原子个数= ,位
于面上、棱上的In原子个数= ,位于体内的Te原子个数=8×1=8,则
Cu、In、Te的原子个数比为4:4:8=1:1:2,晶体的化学式为CuInTe ,A选项正确;
2
B.由位于顶点A点和体心B点原子的分数坐标分别为(0,0,0)、( , , )可知,晶胞边
长为1,则位于体对角线 处,面对角线 处的C原子的分数坐标分别为( , , ),B
选项正确;
C.由晶胞结构可知,In原子形成的四面体空隙有8个,形成的八面体空隙也有8个,
试卷第8页,共25页则四面体空隙的占有率为 ,C选项正确;
D.由晶胞中C、D形成的直角三角形的边长为 pm、 pm可知,C、D间距离d=
,D选项错误;
答案选D。
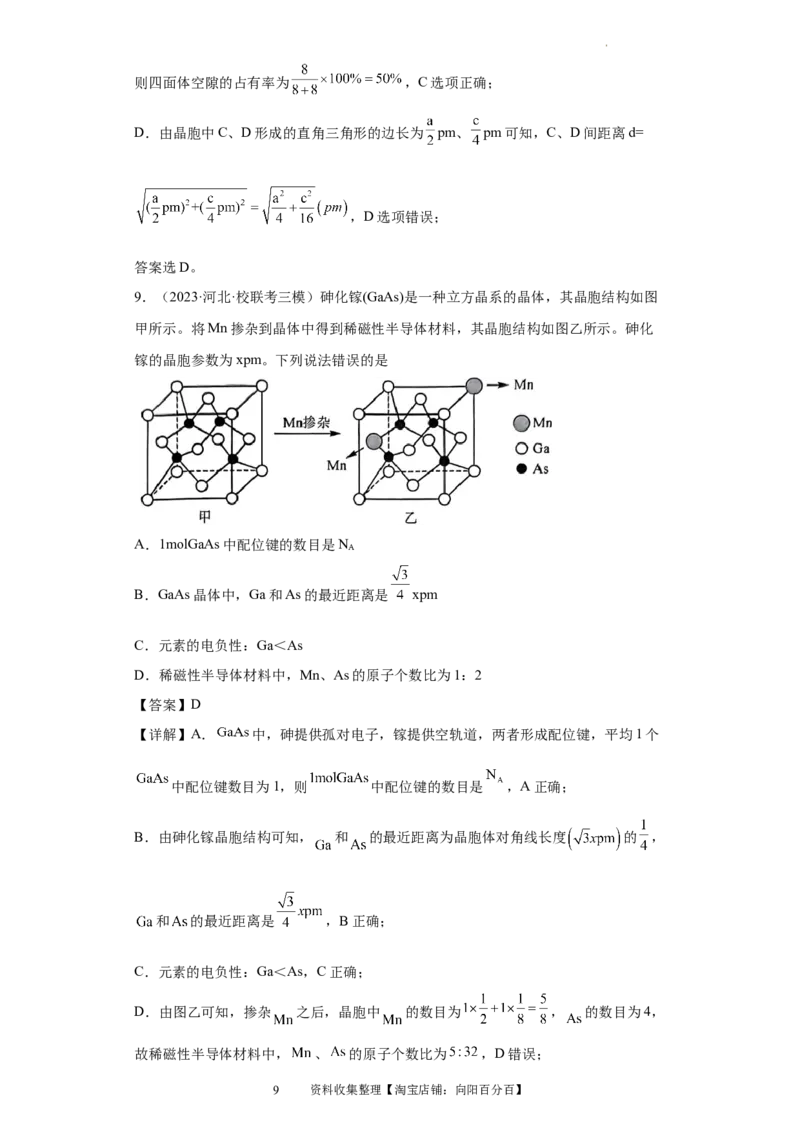
9.(2023·河北·校联考三模)砷化镓(GaAs)是一种立方晶系的晶体,其晶胞结构如图
甲所示。将Mn掺杂到晶体中得到稀磁性半导体材料,其晶胞结构如图乙所示。砷化
镓的晶胞参数为xpm。下列说法错误的是
A.1molGaAs中配位键的数目是N
A
B.GaAs晶体中,Ga和As的最近距离是 xpm
C.元素的电负性:Ga<As
D.稀磁性半导体材料中,Mn、As的原子个数比为1:2
【答案】D
【详解】A. 中,砷提供孤对电子,镓提供空轨道,两者形成配位键,平均1个
中配位键数目为1,则 中配位键的数目是 ,A正确;
B.由砷化镓晶胞结构可知, 和 的最近距离为晶胞体对角线长度 的 ,
和 的最近距离是 ,B正确;
C.元素的电负性:Ga<As,C正确;
D.由图乙可知,掺杂 之后,晶胞中 的数目为 , 的数目为4,
故稀磁性半导体材料中, 、 的原子个数比为 ,D错误;
9 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司故选D。
10.(2023·湖南岳阳·统考三模)由铁及其化合物可制得FeSO ·7H O、FeCl 、KFeO
4 2 3 2 4
等化工产品,它们在生产、生活中具有广泛应用。已知NO能被FeSO 溶液吸收生成
4
配合物[Fe(NO)(H O) ]SO 。高炉炼铁的反应为 Fe O(s)+3CO(g)=2Fe(s)+
2 5 4 2 3
3CO(g) ΔH=-23.5 kJ· mol-1。下列有关说法不正确的是
2
A.如图所示γFe的晶胞中,铁原子的配位数为12
B.配离子为[Fe(NO)(H O) ]2+,配位数为6
2 5
C.基态铁原子的核外电子排布式为1s22s22p63s23p63d74s1
D.该配合物中阴离子空间结构为正四面体形
【答案】C
【详解】A.根据晶胞结构图知,该晶胞中Fe原子的配位数= =12,故A正确;
B.[Fe(NO)(H O) ]2+中NO、HO的个数之和为Fe2+的配位数,所以该配离子中配位数
2 5 2
是6,故B正确;
C.基态铁原子的核外电子排布式为1s22s22p63s23p63d64s2,故C错误;
D.该配合物的阴离子为 ,S原子价层电子对数=4+ =4且不含孤电子对,
所以该离子为正四面体形,故D正确;
故选:C。
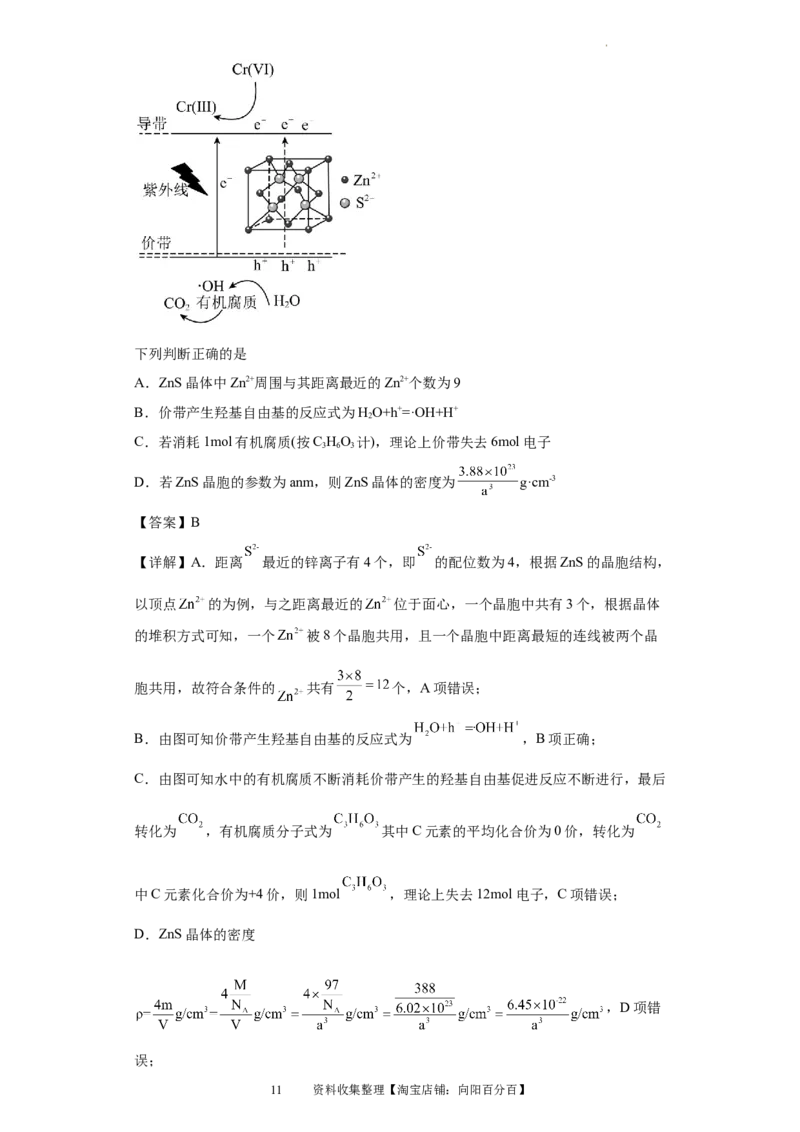
11.(2023·安徽·校联考三模)国内某科研团队发现,在紫外线作用下多孔管状ZnS
价带失去电子产生空穴(h+,具有强氧化性),Cr(VI)在导带得电子转化为无毒的
Cr(Ⅲ),水中的有机腐质不断消耗价带产生的羟基自由基(·OH)促进反应不断进行,作
用机理如图所示;
试卷第10页,共25页下列判断正确的是
A.ZnS晶体中Zn2+周围与其距离最近的Zn2+个数为9
B.价带产生羟基自由基的反应式为HO+h+=·OH+H+
2
C.若消耗1mol有机腐质(按C HO 计),理论上价带失去6mol电子
3 6 3
D.若ZnS晶胞的参数为anm,则ZnS晶体的密度为 g·cm-3
【答案】B
【详解】A.距离 最近的锌离子有4个,即 的配位数为4,根据ZnS的晶胞结构,
以顶点 的为例,与之距离最近的 位于面心,一个晶胞中共有3个,根据晶体
的堆积方式可知,一个 被8个晶胞共用,且一个晶胞中距离最短的连线被两个晶
胞共用,故符合条件的 共有 个,A项错误;
B.由图可知价带产生羟基自由基的反应式为 ,B项正确;
C.由图可知水中的有机腐质不断消耗价带产生的羟基自由基促进反应不断进行,最后
转化为 ,有机腐质分子式为 其中C元素的平均化合价为0价,转化为
中C元素化合价为+4价,则1mol ,理论上失去12mol电子,C项错误;
D.ZnS晶体的密度
,D项错
误;
11 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司答案选B。
12.(2023·湖南衡阳·校联考三模)73号元素钽(Ta)与砷(As)形成的晶体在室温下拥有
超高的空穴迁移率和较低的电子迁移率,其长方体晶胞结构如图所示。下列说法错误
的是
A.基态As原子核外N层有4种空间运动状态不同的电子
B.该晶胞中As的配位数为4
C.该晶体的化学式为TaAs
D.TaAs的晶体密度
【答案】B
【详解】A.基态As原子的价电子排布式为 ,一个原子轨道即为一种空间运动
状态,N层电子共4种空间运动状态,A项正确;
B.该晶胞中As的配位数为6,B项错误;
C.由晶胞结构可知,该晶体的化学式为TaAs,C项正确;
D. (晶胞) ,则 ,D项正确;
故选B。
13.(2023·辽宁·校联考三模) 是一种重要的化工产品,实验室可利用
制取该配合物: 。
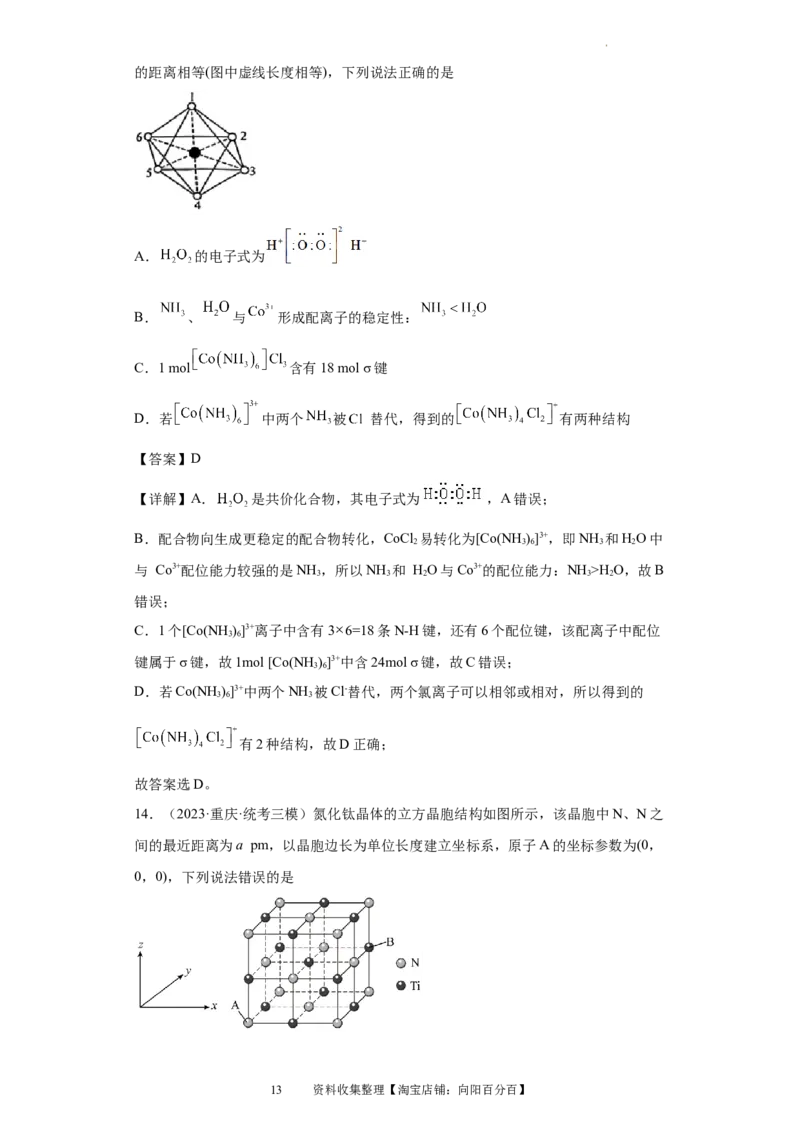
已知 的空间结构如图所示,其中1~6处的小圆圈表示 分子,各相邻
的 分子间的距离相等,中心离子 位于正八面体的中心, 分子到中心离子
试卷第12页,共25页的距离相等(图中虚线长度相等),下列说法正确的是
A. 的电子式为
B. 、 与 形成配离子的稳定性:
C.1 mol 含有18 mol σ键
D.若 中两个 被 替代,得到的 有两种结构
【答案】D
【详解】A. 是共价化合物,其电子式为 ,A错误;
B.配合物向生成更稳定的配合物转化,CoCl 易转化为[Co(NH )]3+,即NH 和HO中
2 3 6 3 2
与 Co3+配位能力较强的是NH ,所以NH 和 HO与Co3+的配位能力:NH >H O,故B
3 3 2 3 2
错误;
C.1个[Co(NH )]3+离子中含有3 6=18条N-H键,还有6个配位键,该配离子中配位
3 6
键属于σ键,故1mol [Co(NH )]3+中含24mol σ键,故C错误;
3 6
D.若Co(NH )]3+中两个NH 被Cl-替代,两个氯离子可以相邻或相对,所以得到的
3 6 3
有2种结构,故D正确;
故答案选D。
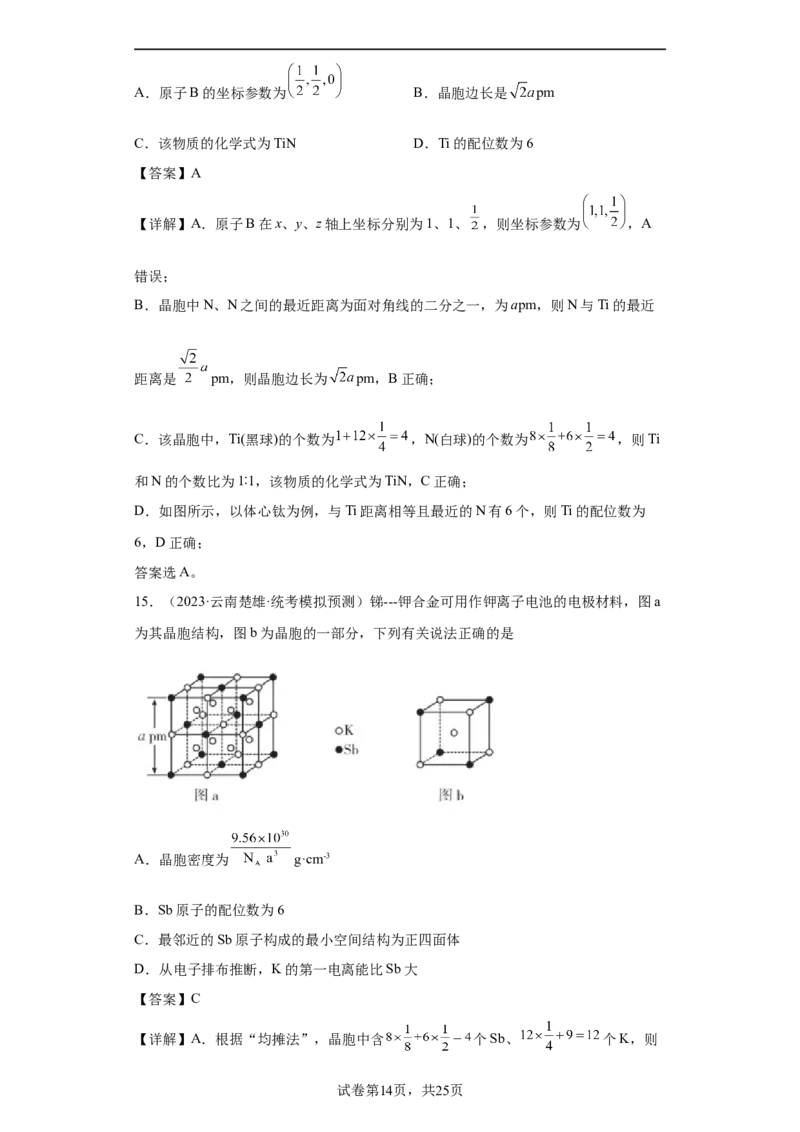
14.(2023·重庆·统考三模)氮化钛晶体的立方晶胞结构如图所示,该晶胞中N、N之
间的最近距离为a pm,以晶胞边长为单位长度建立坐标系,原子A的坐标参数为(0,
0,0),下列说法错误的是
13 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司A.原子B的坐标参数为 B.晶胞边长是 pm
C.该物质的化学式为TiN D.Ti的配位数为6
【答案】A
【详解】A.原子B在x、y、z轴上坐标分别为1、1、 ,则坐标参数为 ,A
错误;
B.晶胞中N、N之间的最近距离为面对角线的二分之一,为apm,则N与Ti的最近
距离是 pm,则晶胞边长为 pm,B正确;
C.该晶胞中,Ti(黑球)的个数为 ,N(白球)的个数为 ,则Ti
和N的个数比为1∶1,该物质的化学式为TiN,C正确;
D.如图所示,以体心钛为例,与Ti距离相等且最近的N有6个,则Ti的配位数为
6,D正确;
答案选A。
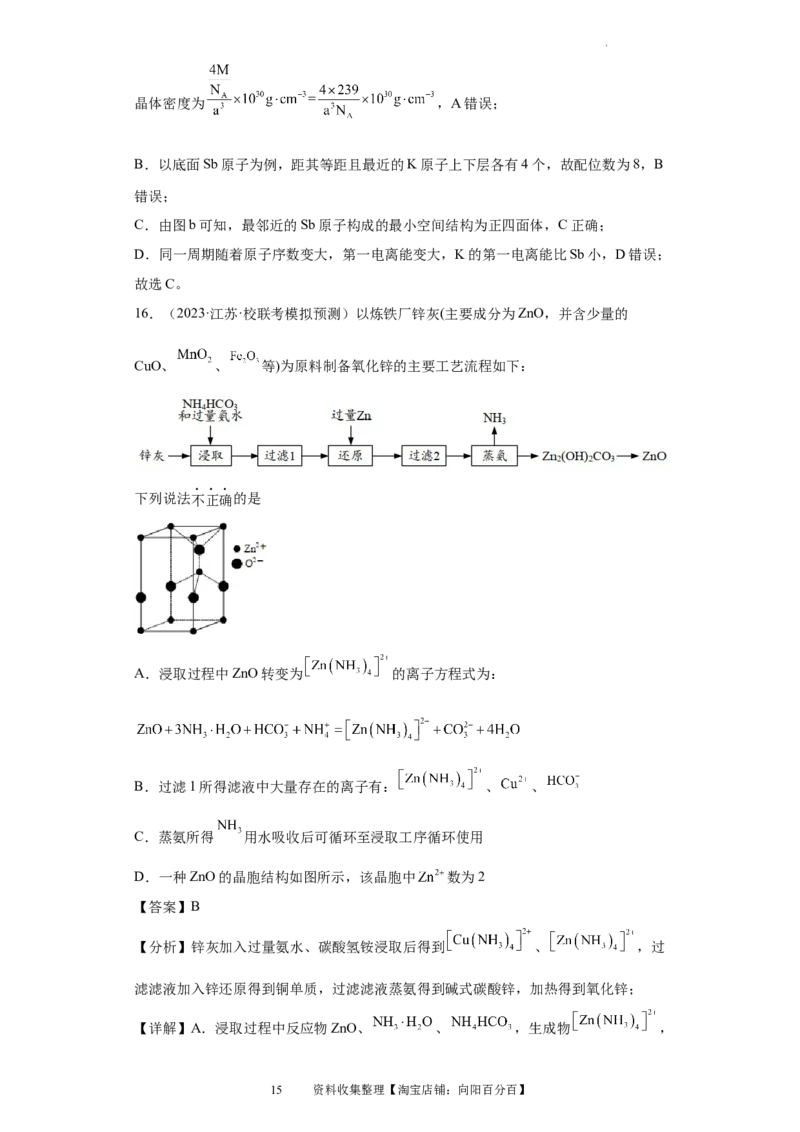
15.(2023·云南楚雄·统考模拟预测)锑---钾合金可用作钾离子电池的电极材料,图a
为其晶胞结构,图b为晶胞的一部分,下列有关说法正确的是
A.晶胞密度为 g·cm-3
B.Sb原子的配位数为6
C.最邻近的Sb原子构成的最小空间结构为正四面体
D.从电子排布推断,K的第一电离能比Sb大
【答案】C
【详解】A.根据“均摊法”,晶胞中含 个Sb、 个K,则
试卷第14页,共25页晶体密度为 ,A错误;
B.以底面Sb原子为例,距其等距且最近的K原子上下层各有4个,故配位数为8,B
错误;
C.由图b可知,最邻近的Sb原子构成的最小空间结构为正四面体,C正确;
D.同一周期随着原子序数变大,第一电离能变大,K的第一电离能比Sb小,D错误;
故选C。
16.(2023·江苏·校联考模拟预测)以炼铁厂锌灰(主要成分为ZnO,并含少量的
CuO、 、 等)为原料制备氧化锌的主要工艺流程如下:
下列说法不正确的是
A.浸取过程中ZnO转变为 的离子方程式为:
B.过滤1所得滤液中大量存在的离子有: 、 、
C.蒸氨所得 用水吸收后可循环至浸取工序循环使用
D.一种ZnO的晶胞结构如图所示,该晶胞中 数为2
【答案】B
【分析】锌灰加入过量氨水、碳酸氢铵浸取后得到 、 ,过
滤滤液加入锌还原得到铜单质,过滤滤液蒸氨得到碱式碳酸锌,加热得到氧化锌;
【详解】A.浸取过程中反应物ZnO、 、 ,生成物 ,
15 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司离子方程式为: ,A正
确;
B.与 相似,在浸取过程中 转变成 ,所以过滤1所得滤液中不
可能有大量的 ,B错误;
C. 溶于水得氨水,可用于“浸取”工序,C正确;
D.根据均摊法,该晶胞中 数为 ,D正确。
答案选B。
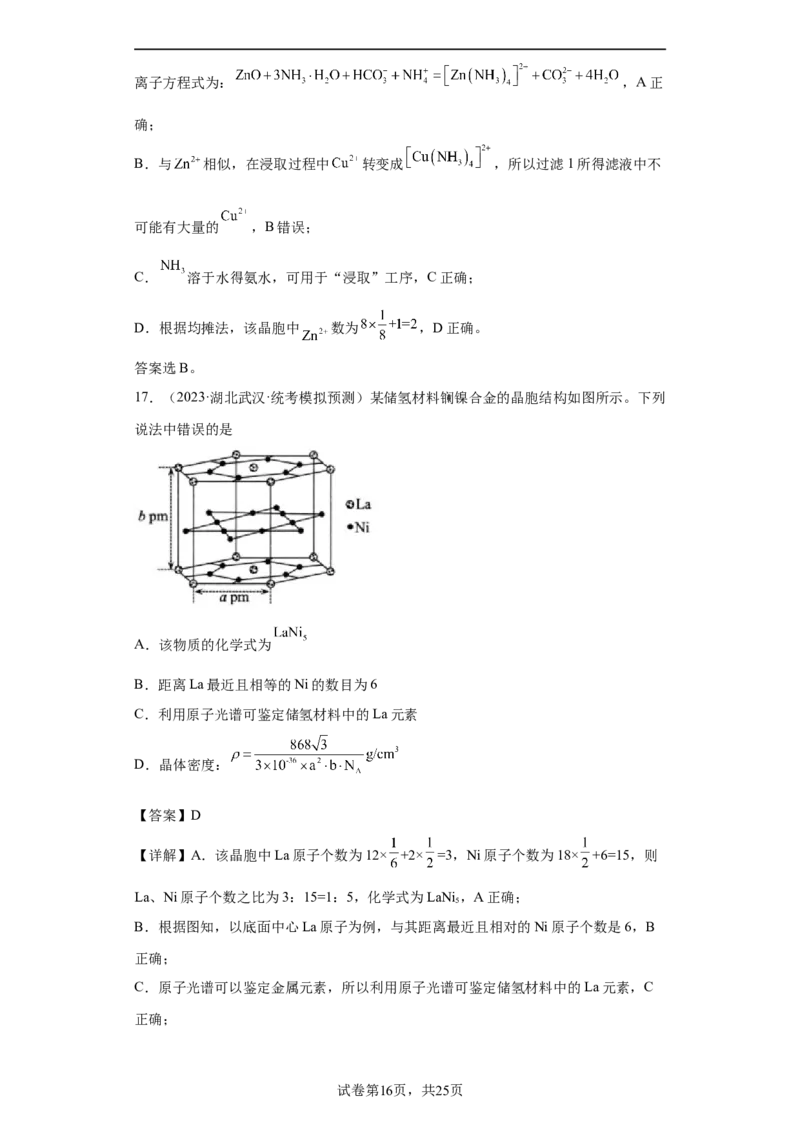
17.(2023·湖北武汉·统考模拟预测)某储氢材料镧镍合金的晶胞结构如图所示。下列
说法中错误的是
A.该物质的化学式为
B.距离La最近且相等的Ni的数目为6
C.利用原子光谱可鉴定储氢材料中的La元素
D.晶体密度:
【答案】D
【详解】A.该晶胞中La原子个数为12× +2× =3,Ni原子个数为18× +6=15,则
La、Ni原子个数之比为3:15=1:5,化学式为LaNi,A正确;
5
B.根据图知,以底面中心La原子为例,与其距离最近且相对的Ni原子个数是6,B
正确;
C.原子光谱可以鉴定金属元素,所以利用原子光谱可鉴定储氢材料中的La元素,C
正确;
试卷第16页,共25页D.该晶胞的体积为 ×(a×10-10cm)2×sin60°×6×(b×10-10cm)= a2b×10-30cm3,晶
体密度ρ= = = g/cm3= g/cm3,D错误;
故答案为:D。
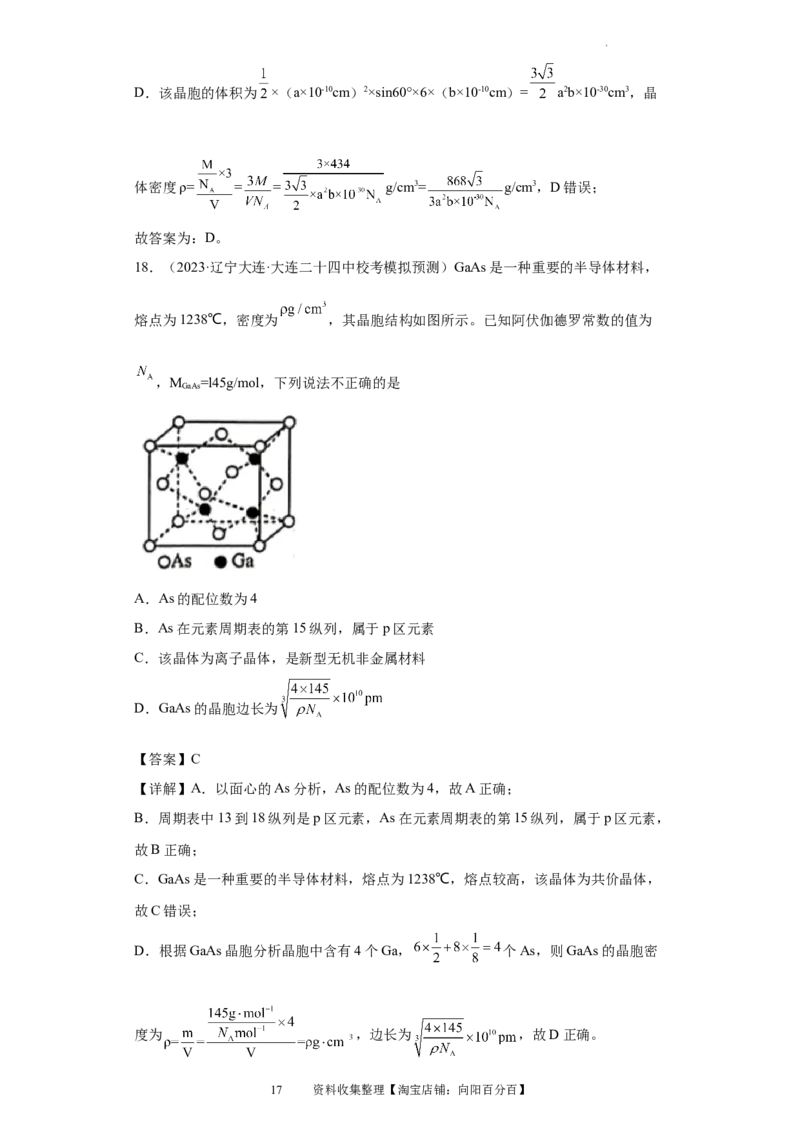
18.(2023·辽宁大连·大连二十四中校考模拟预测)GaAs是一种重要的半导体材料,
熔点为1238℃,密度为 ,其晶胞结构如图所示。已知阿伏伽德罗常数的值为
,M =l45g/mol,下列说法不正确的是
GaAs
A.As的配位数为4
B.As在元素周期表的第15纵列,属于p区元素
C.该晶体为离子晶体,是新型无机非金属材料
D.GaAs的晶胞边长为
【答案】C
【详解】A.以面心的As分析,As的配位数为4,故A正确;
B.周期表中13到18纵列是p区元素,As在元素周期表的第15纵列,属于p区元素,
故B正确;
C.GaAs是一种重要的半导体材料,熔点为1238℃,熔点较高,该晶体为共价晶体,
故C错误;
D.根据GaAs晶胞分析晶胞中含有4个Ga, 个As,则GaAs的晶胞密
度为 ,边长为 ,故D正确。
17 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司综上所述,答案为C。
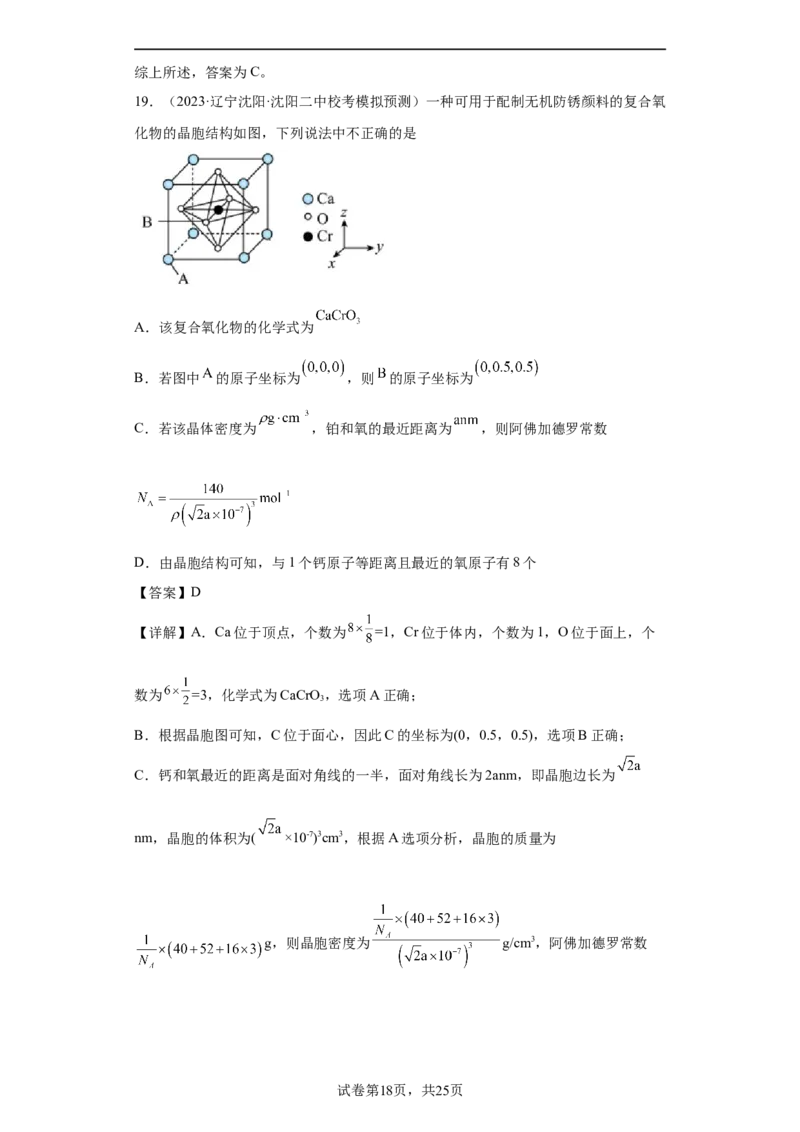
19.(2023·辽宁沈阳·沈阳二中校考模拟预测)一种可用于配制无机防锈颜料的复合氧
化物的晶胞结构如图,下列说法中不正确的是
A.该复合氧化物的化学式为
B.若图中 的原子坐标为 ,则 的原子坐标为
C.若该晶体密度为 ,铂和氧的最近距离为 ,则阿佛加德罗常数
D.由晶胞结构可知,与1个钙原子等距离且最近的氧原子有8个
【答案】D
【详解】A.Ca位于顶点,个数为 =1,Cr位于体内,个数为1,O位于面上,个
数为 =3,化学式为CaCrO,选项A正确;
3
B.根据晶胞图可知,C位于面心,因此C的坐标为(0,0.5,0.5),选项B正确;
C.钙和氧最近的距离是面对角线的一半,面对角线长为2anm,即晶胞边长为
nm,晶胞的体积为( ×10-7)3cm3,根据A选项分析,晶胞的质量为
g,则晶胞密度为 g/cm3,阿佛加德罗常数
试卷第18页,共25页N = ,选项C正确;
A
D.以顶点Ca为标准,离Ca最近的氧原子在面心,共有12个,选项D错误;
答案选D。
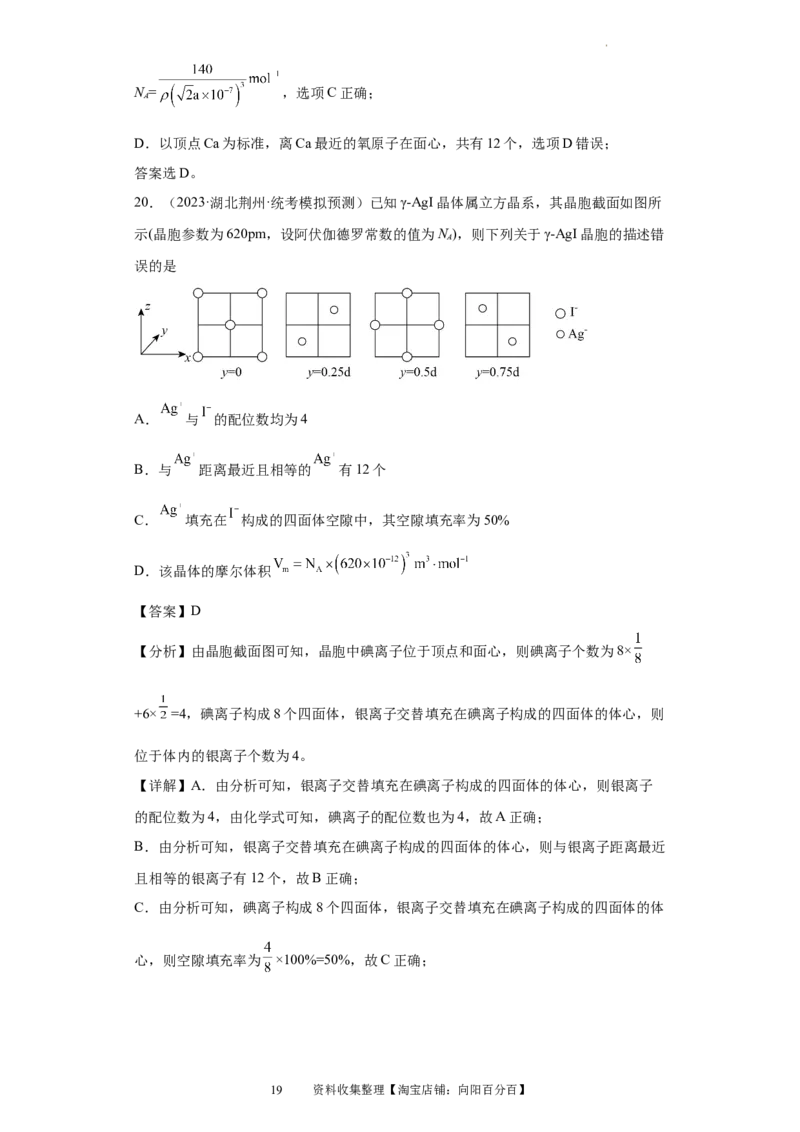
20.(2023·湖北荆州·统考模拟预测)已知γ-AgI晶体属立方晶系,其晶胞截面如图所
示(晶胞参数为620pm,设阿伏伽德罗常数的值为N ),则下列关于γ-AgI晶胞的描述错
A
误的是
A. 与 的配位数均为4
B.与 距离最近且相等的 有12个
C. 填充在 构成的四面体空隙中,其空隙填充率为50%
D.该晶体的摩尔体积
【答案】D
【分析】由晶胞截面图可知,晶胞中碘离子位于顶点和面心,则碘离子个数为8×
+6× =4,碘离子构成8个四面体,银离子交替填充在碘离子构成的四面体的体心,则
位于体内的银离子个数为4。
【详解】A.由分析可知,银离子交替填充在碘离子构成的四面体的体心,则银离子
的配位数为4,由化学式可知,碘离子的配位数也为4,故A正确;
B.由分析可知,银离子交替填充在碘离子构成的四面体的体心,则与银离子距离最近
且相等的银离子有12个,故B正确;
C.由分析可知,碘离子构成8个四面体,银离子交替填充在碘离子构成的四面体的体
心,则空隙填充率为 ×100%=50%,故C正确;
19 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司D.由晶胞参数可知,晶体的摩尔体积V = = m3/mol,
m
故D错误;
故选D。
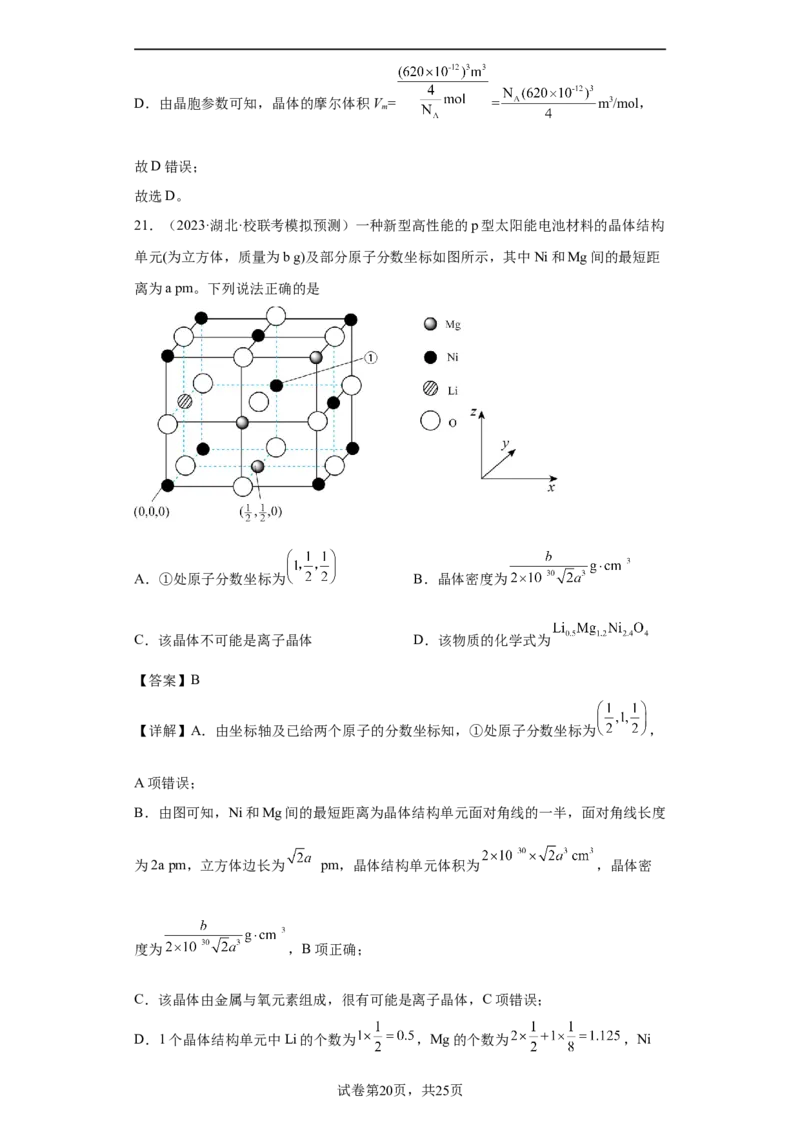
21.(2023·湖北·校联考模拟预测)一种新型高性能的p型太阳能电池材料的晶体结构
单元(为立方体,质量为b g)及部分原子分数坐标如图所示,其中Ni和Mg间的最短距
离为a pm。下列说法正确的是
A.①处原子分数坐标为 B.晶体密度为
C.该晶体不可能是离子晶体 D.该物质的化学式为
【答案】B
【详解】A.由坐标轴及已给两个原子的分数坐标知,①处原子分数坐标为 ,
A项错误;
B.由图可知,Ni和Mg间的最短距离为晶体结构单元面对角线的一半,面对角线长度
为2a pm,立方体边长为 pm,晶体结构单元体积为 ,晶体密
度为 ,B项正确;
C.该晶体由金属与氧元素组成,很有可能是离子晶体,C项错误;
D.1个晶体结构单元中Li的个数为 ,Mg的个数为 ,Ni
试卷第20页,共25页的个数为 ,O的个数为4,因此该物质的化学式为
,D项错误;
故选B。
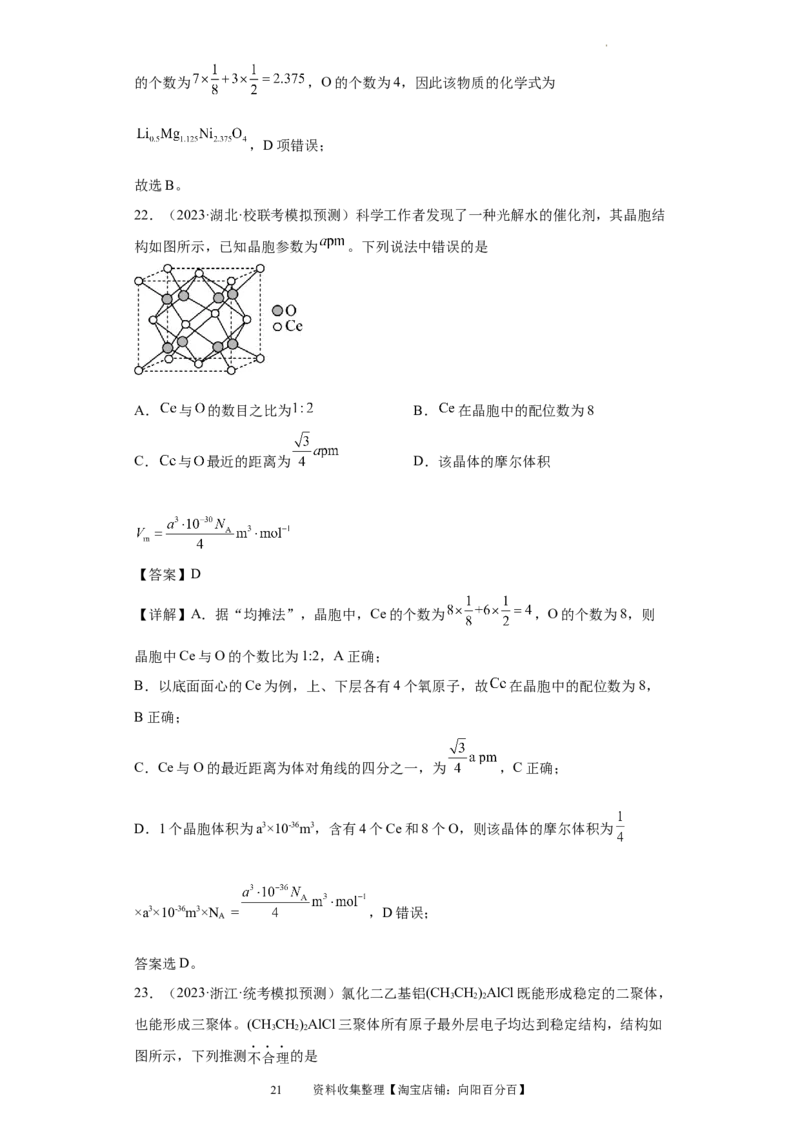
22.(2023·湖北·校联考模拟预测)科学工作者发现了一种光解水的催化剂,其晶胞结
构如图所示,已知晶胞参数为 。下列说法中错误的是
A. 与 的数目之比为 B. 在晶胞中的配位数为8
C. 与 最近的距离为 D.该晶体的摩尔体积
【答案】D
【详解】A.据“均摊法”,晶胞中,Ce的个数为 ,O的个数为8,则
晶胞中Ce与O的个数比为1:2,A正确;
B.以底面面心的Ce为例,上、下层各有4个氧原子,故 在晶胞中的配位数为8,
B正确;
C.Ce与O的最近距离为体对角线的四分之一,为 ,C正确;
D.1个晶胞体积为a3×10-36m3,含有4个Ce和8个O,则该晶体的摩尔体积为
×a3×10-36m3×N = ,D错误;
A
答案选D。
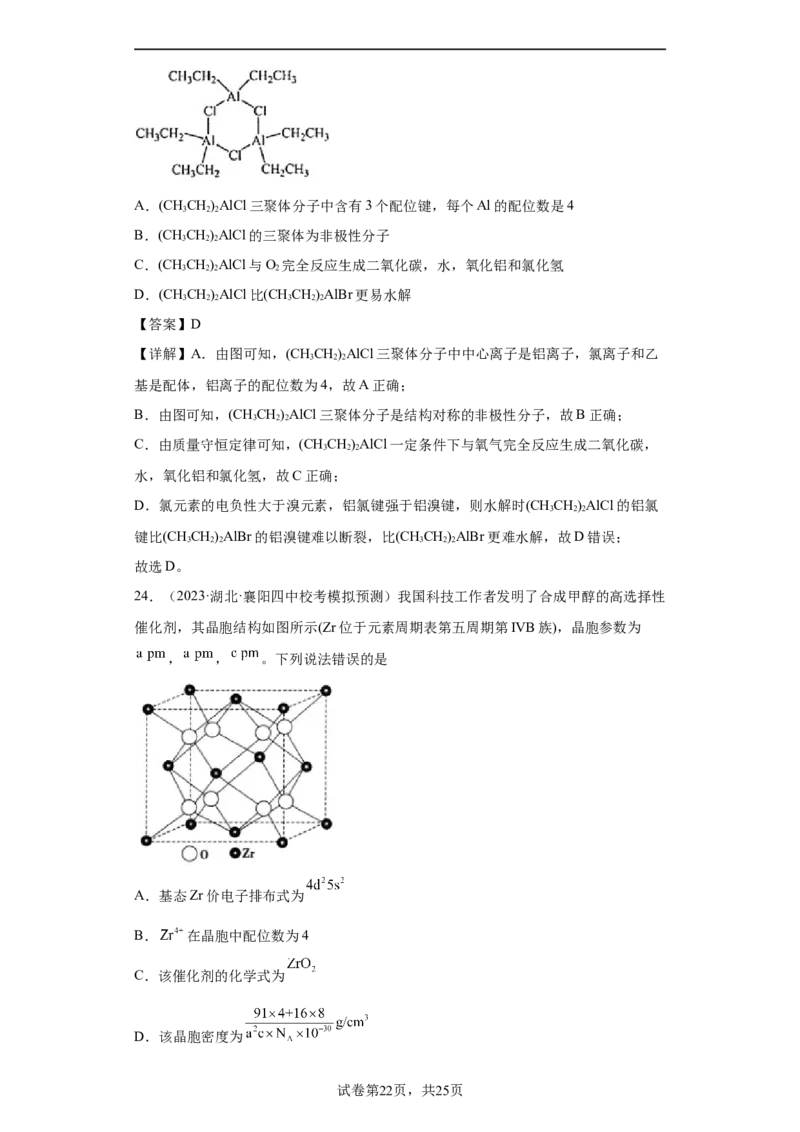
23.(2023·浙江·统考模拟预测)氯化二乙基铝(CHCH)AlCl既能形成稳定的二聚体,
3 2 2
也能形成三聚体。(CHCH)AlCl三聚体所有原子最外层电子均达到稳定结构,结构如
3 2 2
图所示,下列推测不合理的是
21 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司A.(CHCH)AlCl三聚体分子中含有3个配位键,每个Al的配位数是4
3 2 2
B.(CHCH)AlCl的三聚体为非极性分子
3 2 2
C.(CHCH)AlCl与O 完全反应生成二氧化碳,水,氧化铝和氯化氢
3 2 2 2
D.(CHCH)AlCl比(CHCH)AlBr更易水解
3 2 2 3 2 2
【答案】D
【详解】A.由图可知,(CHCH)AlCl三聚体分子中中心离子是铝离子,氯离子和乙
3 2 2
基是配体,铝离子的配位数为4,故A正确;
B.由图可知,(CHCH)AlCl三聚体分子是结构对称的非极性分子,故B正确;
3 2 2
C.由质量守恒定律可知,(CHCH)AlCl一定条件下与氧气完全反应生成二氧化碳,
3 2 2
水,氧化铝和氯化氢,故C正确;
D.氯元素的电负性大于溴元素,铝氯键强于铝溴键,则水解时(CHCH)AlCl的铝氯
3 2 2
键比(CHCH)AlBr的铝溴键难以断裂,比(CHCH)AlBr更难水解,故D错误;
3 2 2 3 2 2
故选D。
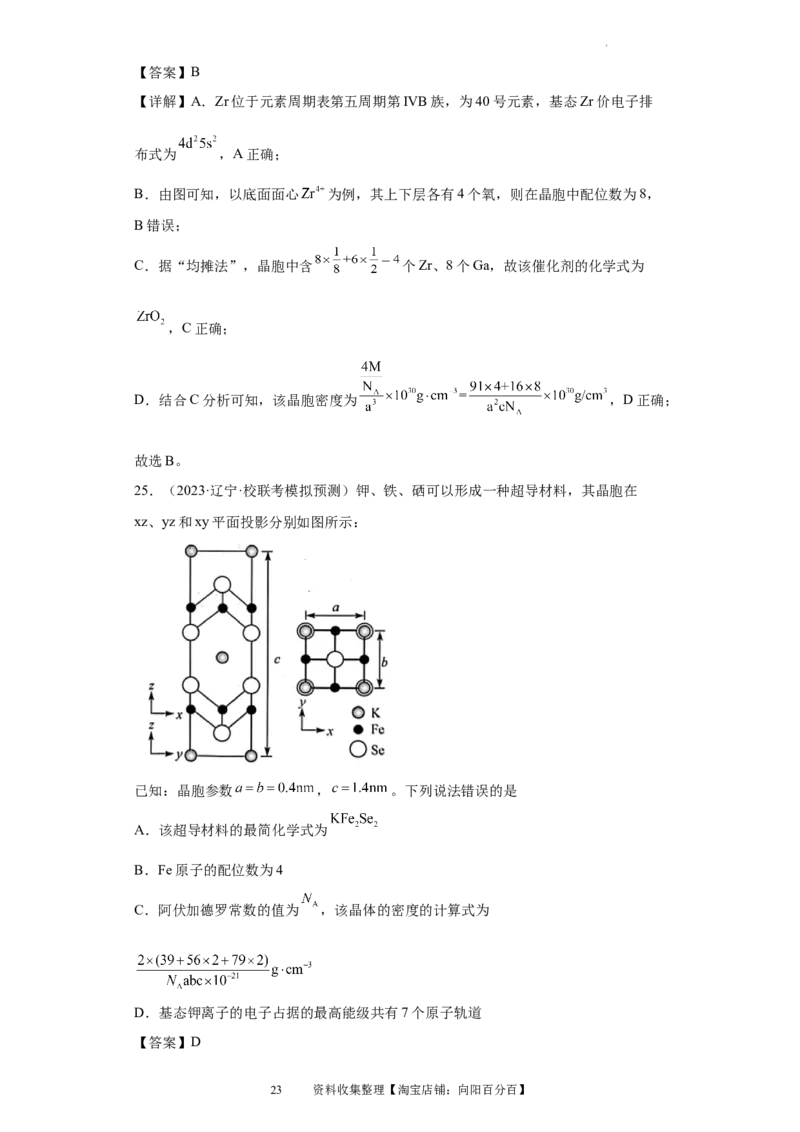
24.(2023·湖北·襄阳四中校考模拟预测)我国科技工作者发明了合成甲醇的高选择性
催化剂,其晶胞结构如图所示(Zr位于元素周期表第五周期第IVB族),晶胞参数为
, , 。下列说法错误的是
A.基态Zr价电子排布式为
B. 在晶胞中配位数为4
C.该催化剂的化学式为
D.该晶胞密度为
试卷第22页,共25页【答案】B
【详解】A.Zr位于元素周期表第五周期第IVB族,为40号元素,基态Zr价电子排
布式为 ,A正确;
B.由图可知,以底面面心 为例,其上下层各有4个氧,则在晶胞中配位数为8,
B错误;
C.据“均摊法”,晶胞中含 个Zr、8个Ga,故该催化剂的化学式为
,C正确;
D.结合C分析可知,该晶胞密度为 ,D正确;
故选B。
25.(2023·辽宁·校联考模拟预测)钾、铁、硒可以形成一种超导材料,其晶胞在
xz、yz和xy平面投影分别如图所示:
已知:晶胞参数 , 。下列说法错误的是
A.该超导材料的最简化学式为
B.Fe原子的配位数为4
C.阿伏加德罗常数的值为 ,该晶体的密度的计算式为
D.基态钾离子的电子占据的最高能级共有7个原子轨道
【答案】D
23 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司【分析】由平面投影图可知,钾原子8个位于顶点,1个位于体心,其个数为:8×
+1=2,硒原子8个位于棱上,2个位于晶胞内部,其个数为8× +2=4,铁原子8个位
于面心,其个数为8× =4,由此分析解题。
【详解】A.由平面投影图可知,晶胞中位于顶点和体心的钾原子个数为2,位于面上
的铁原子个数为4,位于棱上和体内的硒原子的个数为4,则超导材料最简化学式为
,A正确;
B.由平面投影图可知,位于面心上的铁原子与位于棱上和体内的硒原子的距离最近,
所以铁原子的配位数为4,B正确;
C.设晶体的密度为 ,由晶胞的质量公式可得:
, ,C正确;
D.已知K为19号元素,故基态钾离子的电子占据的最高能级即3p能级,共有3个原
子轨道,D错误;
故答案为:D。
26.(2023·黑龙江绥化·统考模拟预测)某种新型储氢材料的立方晶胞结构如图所示,
其中八面体中心为M金属离子,顶点均为NH 配体;四面体中心为硼原子,顶点均为
3
氢原子。已知该储氢材料的摩尔质量为188 g·mol-1,晶胞参数为a nm。下列说法正确
的是
A.M为铜元素
B.每个晶胞中含有12个NH
3
C.该储氢材料晶胞的体积为a3×10-27 cm3
D.晶胞中M金属离子与B原子数之比为1∶2
试卷第24页,共25页【答案】D
【分析】某种新型储氢材料的立方晶胞结构如图所示,其中八面体中心为M金属离子,
顶点均为NH 配体,八面体位于顶点和面心,八面体的个数为8× +6× =4,1个
3
八面体中有1个M和6个NH ,晶胞中含4个M和24个NH ;四面体中心为硼原子,
3 3
顶点均为氢原子,四面体位于体内,四面体的个数为8,1个四面体中有1个B和4个
H,晶胞中含8个B和32个H;据此作答。
【详解】A.晶胞中M、NH 、B、H的个数之比为4∶24∶8∶32=1∶6∶2∶8,晶体的化学式为
3
M(NH)(BH),该储氢材料的摩尔质量为188g/mol,M的相对原子质量为188-6×17-
3 6 4 2
2×15=56,M为Fe元素,A项错误;
B.1个八面体中有6个NH ,1个晶胞中含4个八面体,则每个晶胞中含有4×6=24个
3
NH ,B项错误;
3
C.晶胞参数为anm=a×10-7cm,该储氢材料晶胞的体积为(a×10-7cm)3=a3×10-21cm3,C项
错误;
D.晶胞中M金属离子与B原子数之比为4∶8=1∶2,D项正确;
答案选D。
27.(2023·湖南长沙·雅礼中学校考模拟预测)硒化锌 是一种重要的半导体材
料,其晶胞结构如图甲所示,乙图为该晶胞沿z轴方向在 平面的投影,已知晶胞边
长为 ,阿伏加德罗常数的值为 ,下列说法错误的是
A. 位于元素周期表的 区
B.基态 原子核外有18种不同空间运动状态的电子
C.A点原子的坐标为 ,则B点原子的坐标为
25 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司D.该晶体密度为
【答案】C
【详解】A.Zn的价层电子排布式为3d104s2,位于元素周期表的ds区,A正确;
B.基态 原子核外排布式为1s22s22p63s23p63d104s24p4,电子的空间运动状态数=电子
所占原子轨道数,s、p、d原子轨道数分别为1、3、5,所以基态 原子核外有
1+1+3+1+3+5+1+3=18种不同空间运动状态的电子,B正确;
C.A点原子坐标为(0,0,0),由图乙可知,B点原子的坐标为 ,C错误;
D.该晶胞中,位于晶胞内部的Zn原子个数为4,位于顶点和面心的Se原子个数为
,则 ,D正确;
故选C。
28.(2023·湖北·校联考模拟预测)某笼形络合物Ni(CN) (NH )(C H) 结构中,金属
x 3 y 6 6 z
离子与CN-连接形成平面层,两个平面层通过NH 分子连接,中间的空隙填充大小合
3
适的分子(如C H),其基本结构如图(H原子未画出)。下列说法正确的是
6 6
A.该结构是晶胞结构单元
B.x:y:z=2:1:1
C.金属离子的配位数都是4
D.该笼形络合物A的晶胞密度为 g/cm3
【答案】B
【详解】A.笼形络合物不能由该结构并置形成晶体,故该结构不是晶胞结构单元,A
不正确;
B.该结构单元中,含CN-个数为 =2,含NH 分子个数为 =1,含C H 分子个
3 6 6
试卷第26页,共25页数为1,则x:y:z=2:1:1,B正确;
C.由图可知,同一平面层上,离金属离子最近的CN-有4个,金属离子的配位数为
4,纵轴向还有2个NH 的金属离子,配位数为4+2=6,则金属离子的配位数是4和
3
6,C不正确;
D.该笼形络合物A的晶胞密度为 = g/
cm3,D不正确;
故选B。
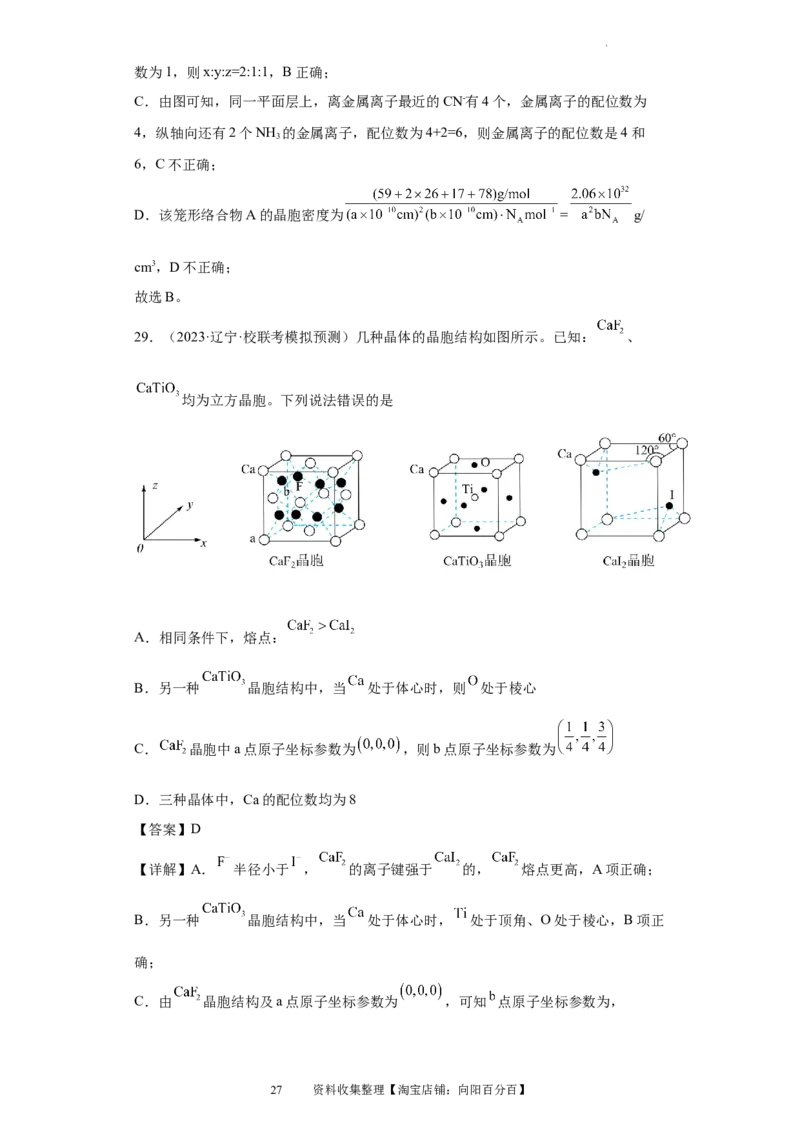
29.(2023·辽宁·校联考模拟预测)几种晶体的晶胞结构如图所示。已知: 、
均为立方晶胞。下列说法错误的是
A.相同条件下,熔点:
B.另一种 晶胞结构中,当 处于体心时,则 处于棱心
C. 晶胞中a点原子坐标参数为 ,则b点原子坐标参数为
D.三种晶体中,Ca的配位数均为8
【答案】D
【详解】A. 半径小于 , 的离子键强于 的, 熔点更高,A项正确;
B.另一种 晶胞结构中,当 处于体心时, 处于顶角、O处于棱心,B项正
确;
C.由 晶胞结构及a点原子坐标参数为 ,可知 点原子坐标参数为,
27 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司,C项正确;
D. 中 的配位数为12,D项错误;
故答案为:D。
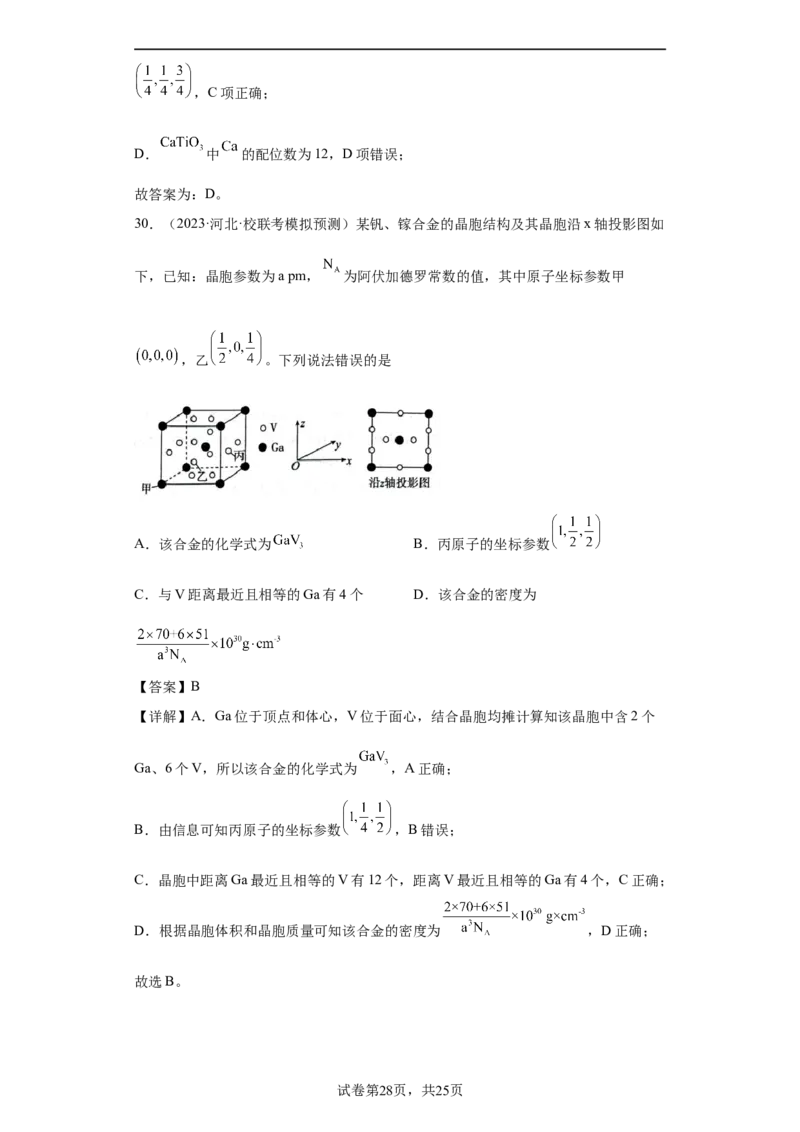
30.(2023·河北·校联考模拟预测)某钒、镓合金的晶胞结构及其晶胞沿x轴投影图如
下,已知:晶胞参数为a pm, 为阿伏加德罗常数的值,其中原子坐标参数甲
,乙 。下列说法错误的是
A.该合金的化学式为 B.丙原子的坐标参数
C.与V距离最近且相等的Ga有4个 D.该合金的密度为
【答案】B
【详解】A.Ga位于顶点和体心,V位于面心,结合晶胞均摊计算知该晶胞中含2个
Ga、6个V,所以该合金的化学式为 ,A正确;
B.由信息可知丙原子的坐标参数 ,B错误;
C.晶胞中距离Ga最近且相等的V有12个,距离V最近且相等的Ga有4个,C正确;
D.根据晶胞体积和晶胞质量可知该合金的密度为 ,D正确;
故选B。
试卷第28页,共25页