文档内容
江苏省扬州中学2022-2023学年度第一学期阶段测试
高三化学
2023.1
试卷满分:100分 考试时间:75分钟
可能用到的相对原子质量:H-1 C-12 O-16 S-32 Co-59 Ba-137
选择题(共39分)
单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.化学与科技、社会、生产、生活等联系紧密,下列相关说法不正确的是
A.中国航空空间站外层的热控保温材料属于复合材料
B.水晶和玛瑙主要成分都是SiO,制造光纤也与SiO 有关
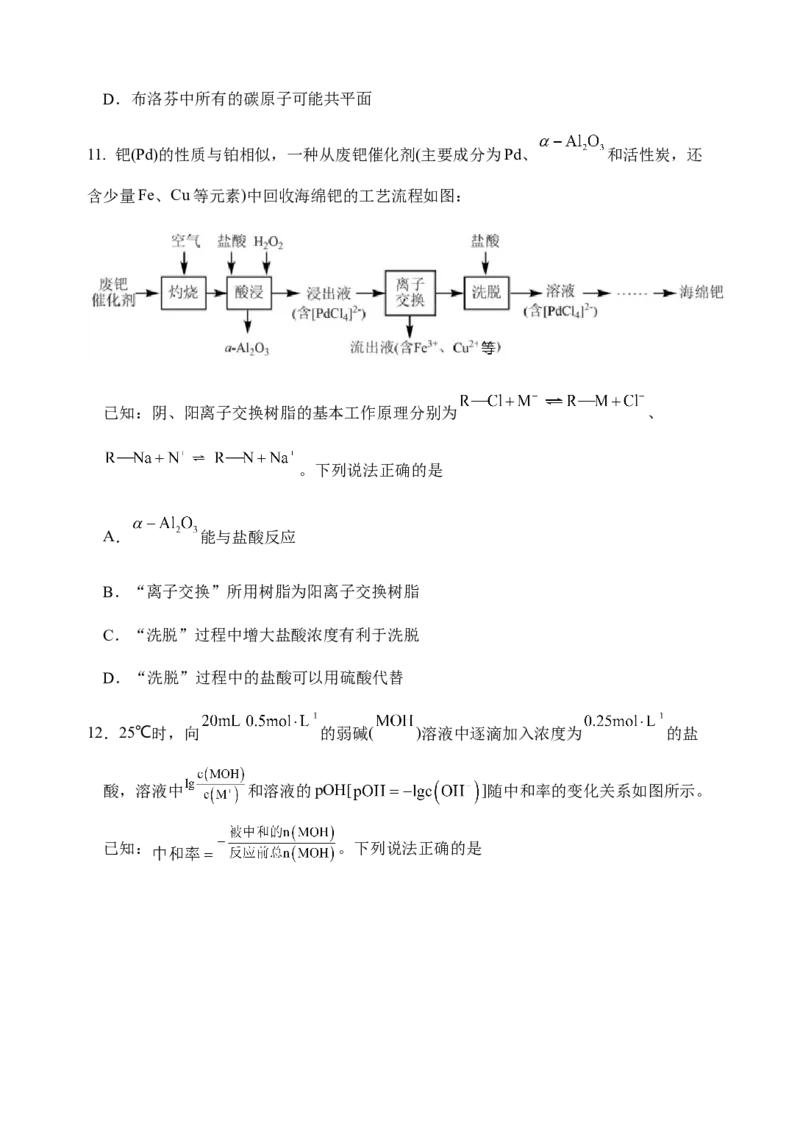
2 2
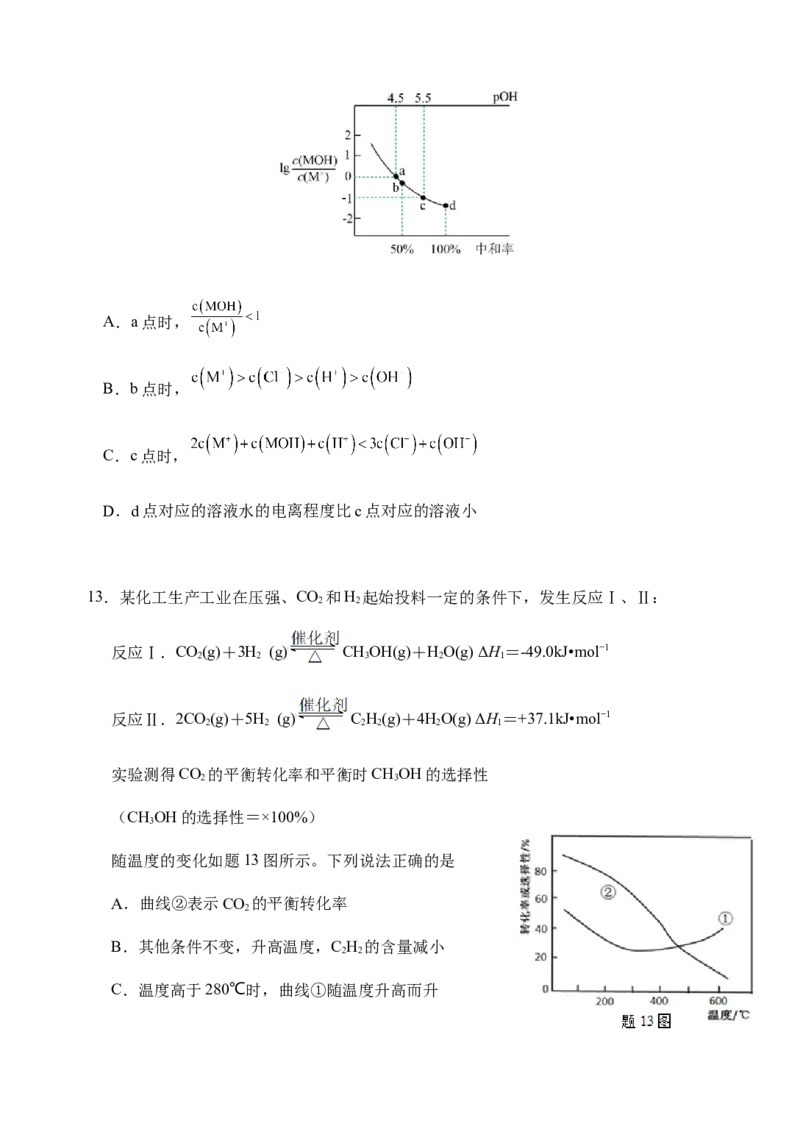
C.预防新冠病毒的疫苗应在较低温度下保存
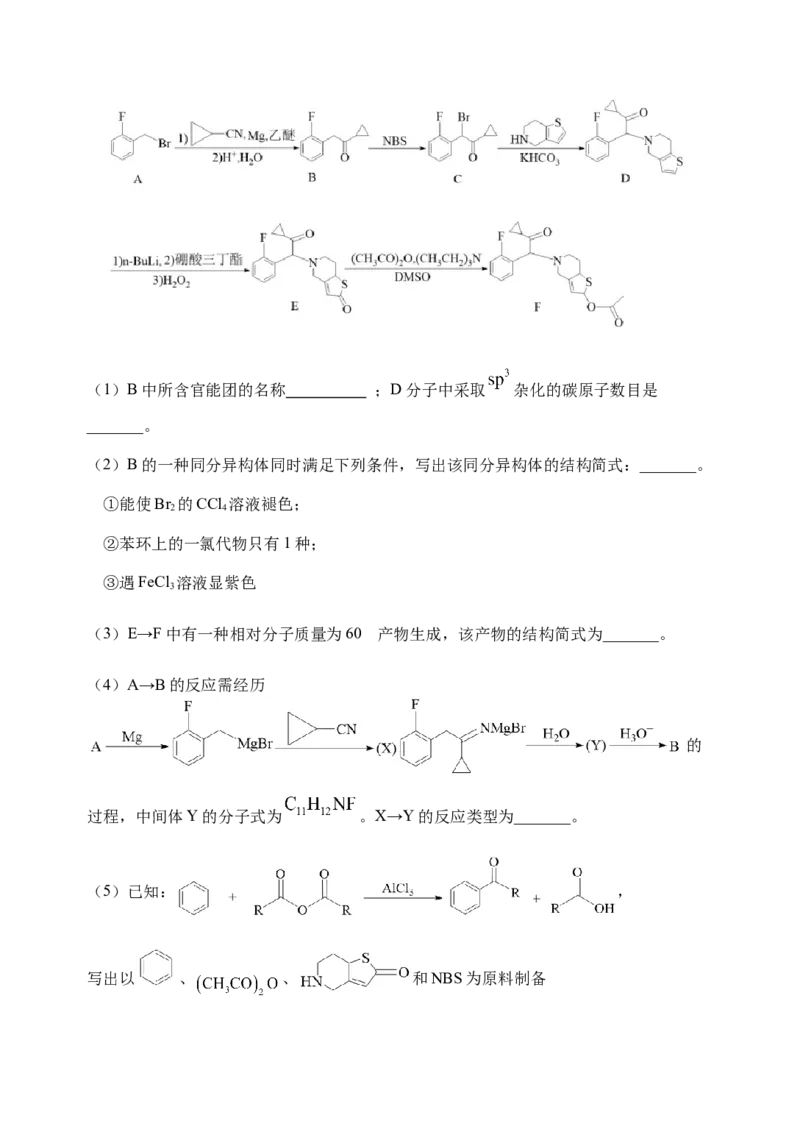
D.为了防腐,港珠澳大桥可以在钢铁中增加含碳量
2.尿素CO(NH) 是一种高效化肥,也是一种化工原料。反应CO+2NH
2 2 2 3
CO(NH)+H O 可用于尿素的制备。下列有关说法不正确的是
2 2 2
A.NH 与CO(NH) 均为极性分子 B.NH 的电子式为
3 2 2 3
C.NH 的键角大于HO的键角
3 2
D.尿素分子σ键和π键的数目之比为6∶1
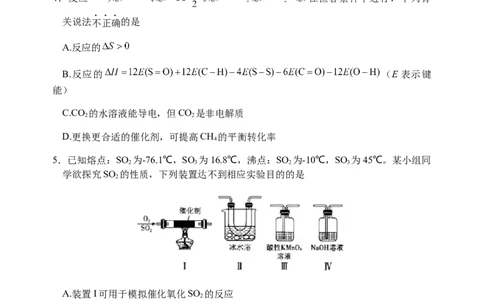
阅读下列材料,完成3~6题:
硫元素的很多化合物用途广泛。烟气催化还原工艺将 还原成硫蒸气,既符合环
保 要 求 , 又 可 以 合 理 利 用 宝 贵 的 硫 资 源 。 该 催 化 反 应 体 系 中 涉 及 反 应
。
3.下列关于硫的化合物的结构与性质的说法正确的是A. 的空间构型为三角锥形
B. 中混有的少量 可以通过饱和 溶液除去
C. 溶液中加入足量氯水、氯化钡溶液产生白色沉淀
D.两个硫酸分子脱去一分子水生成焦硫酸(H SO),一个焦硫酸分子中硫氧键的数目为
2 2 7
6
4.反应 在恒容条件下进行,下列有
关说法不正确的是
A.反应的
B.反应的 (E表示键
能)
C.CO 的水溶液能导电,但CO 是非电解质
2 2
D.更换更合适的催化剂,可提高CH 的平衡转化率
4
5.已知熔点:SO 为-76.1℃,SO 为16.8℃,沸点:SO 为-10℃,SO 为45℃。某小组同
2 3 2 3
学欲探究SO 的性质,下列装置达不到相应实验目的的是
2
A.装置I可用于模拟催化氧化SO 的反应
2
B.装置Ⅱ中通过冷凝可将SO 分离
3
C.装置Ⅲ中酸性高锰酸钾溶液褪色证明二氧化硫的还原性
D.装置Ⅲ、Ⅳ对换不影响实验效果
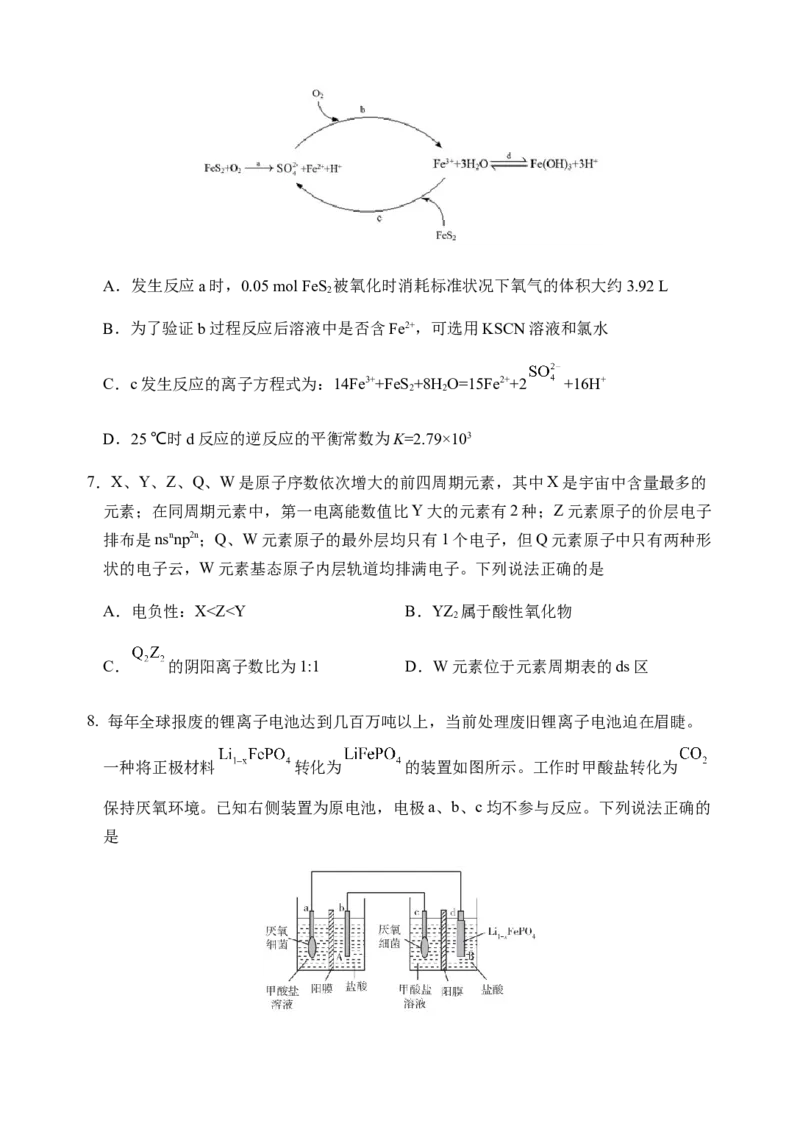
6.黄铁矿(主要成分FeS),在空气中会被缓慢氧化,氧化过程如图所示。下列说法不正
2
确的是(已知25 ℃时,K [Fe(OH) ]=2.79×10-39)
sp 3A.发生反应a时,0.05 mol FeS 被氧化时消耗标准状况下氧气的体积大约3.92 L
2
B.为了验证b过程反应后溶液中是否含Fe2+,可选用KSCN溶液和氯水
C.c发生反应的离子方程式为:14Fe3++FeS +8H O=15Fe2++2 +16H+
2 2
D.25 ℃时d反应的逆反应的平衡常数为K=2.79×103
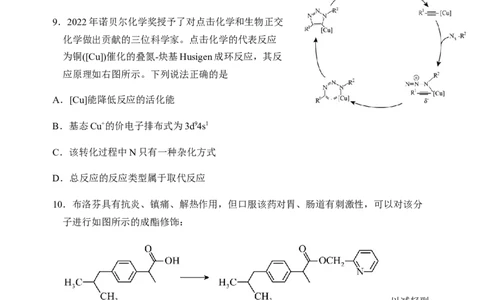
7.X、Y、Z、Q、W是原子序数依次增大的前四周期元素,其中X是宇宙中含量最多的
元素;在同周期元素中,第一电离能数值比Y大的元素有2种;Z元素原子的价层电子
排布是nsnnp2n;Q、W元素原子的最外层均只有1个电子,但Q元素原子中只有两种形
状的电子云,W元素基态原子内层轨道均排满电子。下列说法正确的是
A.电负性:X10后所制钴粉中由于含有Co(OH) 而导致纯度降低。若向pH>10的溶液中加入柠
2
檬酸钠(Na C HO),可以提高钴粉的纯度,结合沉淀溶解平衡原理解释原因_______。
3 6 5 7(5)请补充完整由浸取后滤液先制备 ,并进一步制取Co O 的实验方案:取
3 4
浸取后滤液,____________,得到Co O[已知:LiC O 易溶于水,CoC O 难溶于水,
3 4 2 2 4 2 4
在空气中加热时的固体残留率( 100%)与随温度的变化如图
16-3所示。实验中需使用的试剂有:2mol·L-1 (NH )C O 溶液、0.1mol·L-1 BaCl 溶液、
4 2 2 4 2
蒸馏水。
17.(15分)我国对世界郑重承诺:2030年前实现碳达峰,2060年前实现碳中和,而研
发CO 的碳捕捉和碳利用技术则是关键。
2
(1)大气中的CO 主要来自于煤、石油及其他含碳化合物的燃烧,CH 与CO 重整是CO 利
2 4 2 2
用的研究热点之一。该重整反应体系主要涉及以下反应:
①CH(g) C(s)+2H(g) ΔH=a kJ•mol-1
4 2 1
②CO (g)+H(g) CO(g)+HO(g) ΔH=b kJ•mol-1
2 2 2 2
③2CO(g) CO(g)+C(s) ΔH=c kJ•mol-1
2 3
反应CH(g)+CO (g) 2CO(g)+2H(g)的ΔH=____kJ•mol-1。
4 2 2
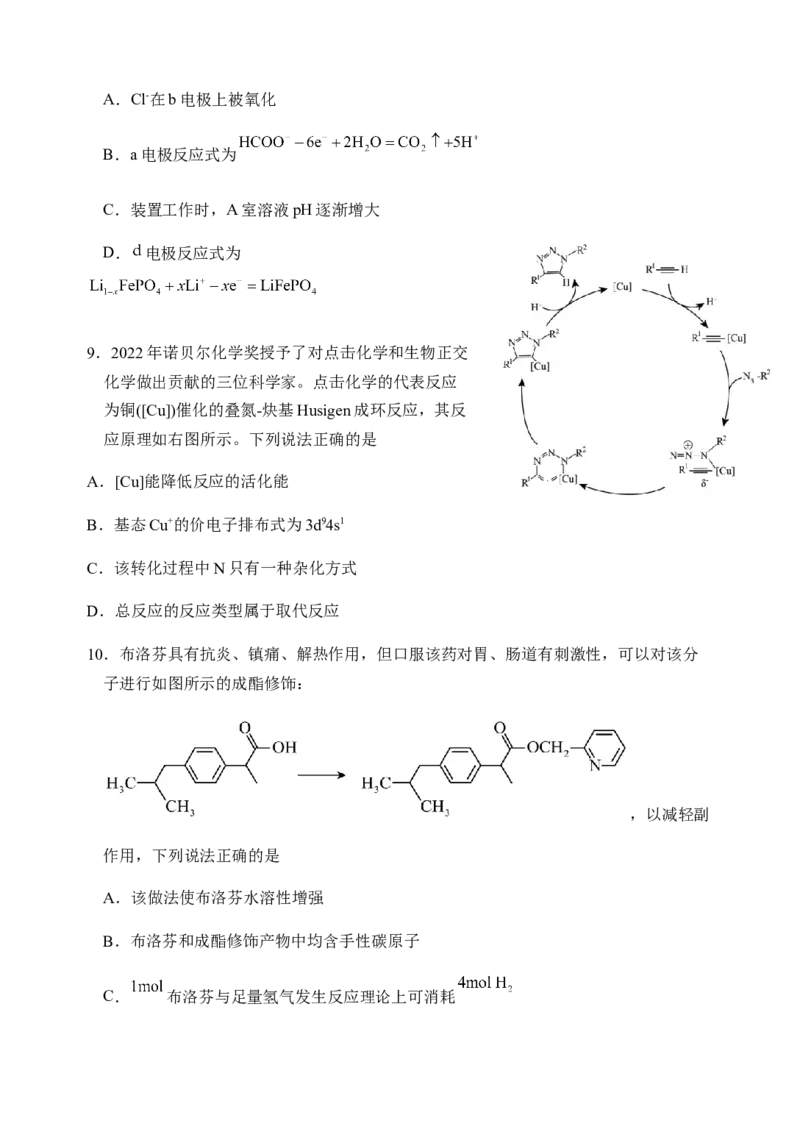
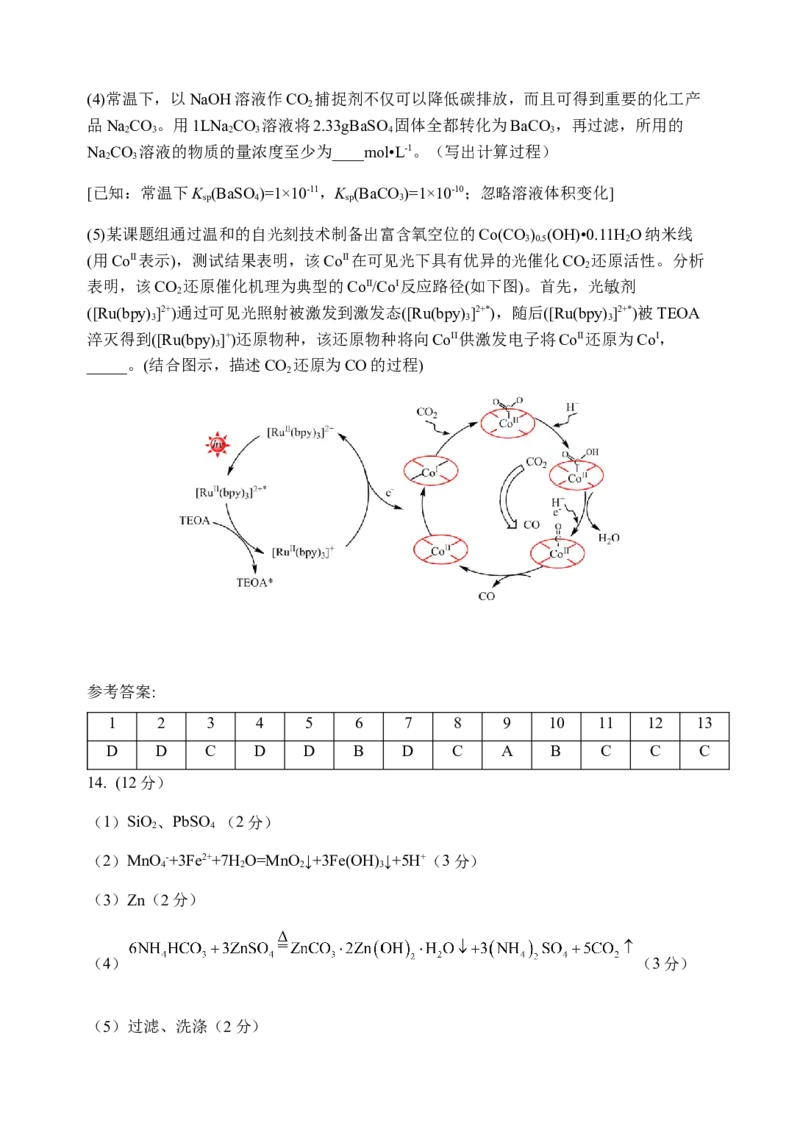
(2)多晶Cu是目前唯一被实验证实能高效催化CO 还原为烃类(如C H)的金属。如左下图
2 2 4
所示,电解装置中分别以多晶Cu和Pt为电极材料,用阴离子交换膜分隔开阴、阳极室,
反应前后KHCO 浓度基本保持不变,温度控制在10℃左右。生成C H 的电极反应式为
3 2 4
____。
(3)CO 与H 反应如果用Co/C作为催化剂,可以得到含有少量甲酸的甲醇。为了研究催
2 2
化剂的催化效率,将Co/C催化剂循环使用,相同条件下,随着循环使用次数的增加,甲
醇的产量如右上图所示,试推测甲醇产量变化的可能原因_______ 。(4)常温下,以NaOH溶液作CO 捕捉剂不仅可以降低碳排放,而且可得到重要的化工产
2
品NaCO。用1LNa CO 溶液将2.33gBaSO 固体全都转化为BaCO ,再过滤,所用的
2 3 2 3 4 3
NaCO 溶液的物质的量浓度至少为____mol•L-1。(写出计算过程)
2 3
[已知:常温下K (BaSO)=1×10-11,K (BaCO)=1×10-10;忽略溶液体积变化]
sp 4 sp 3
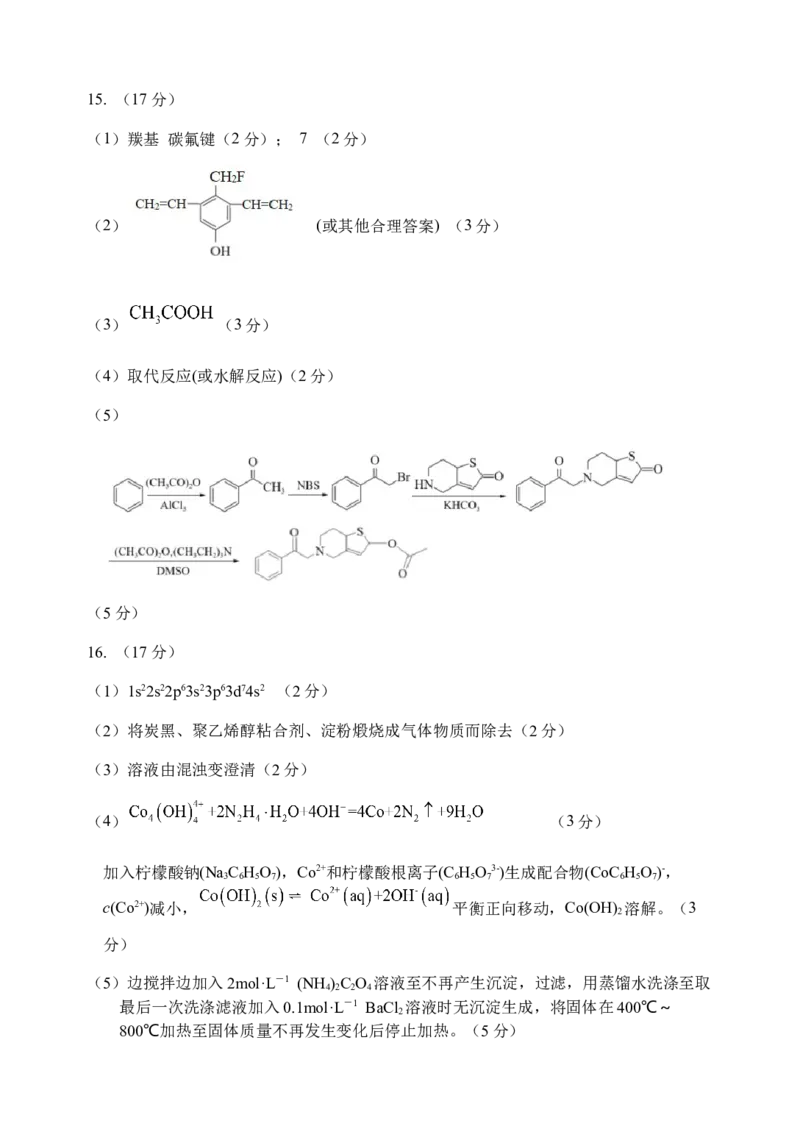
(5)某课题组通过温和的自光刻技术制备出富含氧空位的Co(CO) (OH)•0.11H O纳米线
3 0.5 2
(用CoII表示),测试结果表明,该CoII在可见光下具有优异的光催化CO 还原活性。分析
2
表明,该CO 还原催化机理为典型的CoII/CoI反应路径(如下图)。首先,光敏剂
2
([Ru(bpy) ]2+)通过可见光照射被激发到激发态([Ru(bpy) ]2+*),随后([Ru(bpy) ]2+*)被TEOA
3 3 3
淬灭得到([Ru(bpy) ]+)还原物种,该还原物种将向CoII供激发电子将CoII还原为CoI,
3
_____。(结合图示,描述CO 还原为CO的过程)
2
参考答案:
1 2 3 4 5 6 7 8 9 10 11 12 13
D D C D D B D C A B C C C
14. (12分)
(1)SiO、PbSO (2分)
2 4
(2)MnO -+3Fe2++7H O=MnO ↓+3Fe(OH) ↓+5H+(3分)
4 2 2 3
(3)Zn(2分)
(4) (3分)
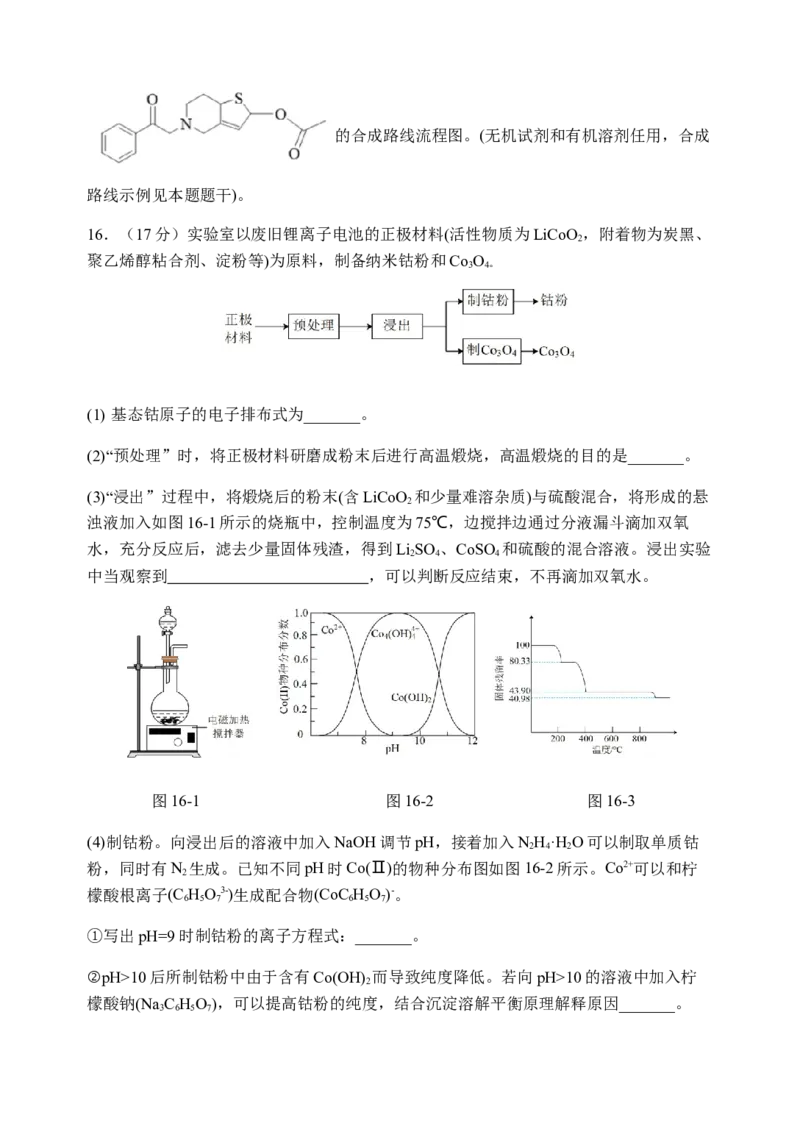
(5)过滤、洗涤(2分)15. (17分)
(1)羰基 碳氟键(2分); 7 (2分)
(2) (或其他合理答案) (3分)
(3) (3分)
(4)取代反应(或水解反应)(2分)
(5)
(5分)
16. (17分)
(1)1s22s22p63s23p63d74s2 (2分)
(2)将炭黑、聚乙烯醇粘合剂、淀粉煅烧成气体物质而除去(2分)
(3)溶液由混浊变澄清(2分)
(4) (3分)
加入柠檬酸钠(Na C HO),Co2+和柠檬酸根离子(C HO3-)生成配合物(CoC HO)-,
3 6 5 7 6 5 7 6 5 7
c(Co2+)减小, 平衡正向移动,Co(OH) 溶解。(3
2
分)
(5)边搅拌边加入2mol·L-1 (NH )C O 溶液至不再产生沉淀,过滤,用蒸馏水洗涤至取
4 2 2 4
最后一次洗涤滤液加入0.1mol·L-1 BaCl 溶液时无沉淀生成,将固体在400℃~
2
800℃加热至固体质量不再发生变化后停止加热。(5分)17.(15分)
(1)a-c (2分)
(2)14CO+12e-+8H O=C H+12HCO (3分)
2 2 2 4
(3)反应产生的甲酸腐蚀催化剂,使催化剂活性降低(2分)
(4)0.11(4分)
设所用的NaCO 溶液的物质的量浓度至少为xmol/L
2 3
n(BaSO)=0.01mol,所得1L溶液中 ,
4
根据 ,
平衡时 , ,x=0.11;
则所用的NaCO 溶液的物质的量浓度至少为0.11mol/L;
2 3
(5)CoI失去一个电子转化为CoII,同时失去的电子被转移到吸附在光催化剂表面的CO
2
上生成CoIICOO-,CoIICOO-再结合一个H+转化为CoIICOOH,H+得到一个电子和
CoIICOOH结合生成CoIICO和HO(CoIICOOH+H++e-=CoIICO+HO),CO分子从
2 2
CoIICO中解吸附释放出。(4分)