文档内容
湖南师大附中 2023 届高三年级月考试卷(一)
化 学
本试题卷分选择题和非选择题两部分,共10页。时量75分钟,满分100分。
可能用到的相对原子质量:H~1 C~12 N~14 O~16
Na~23 Mg~24 Cu~64 Ce~140
一、选择题:本题共10小题,每小题3分,共30分。每小题只有一个选项符合题目要求。
1.科技改变生活。下列说法不正确的是
A.国产大飞机C919机壳采用的铝锂合金,具备耐腐蚀性
B.“天宫课堂”实验:乙酸钠过饱和溶液结晶形成温热“冰球”,该过程发生吸热反
应
C.“嫦娥五号”使用的锂离子电池组,可将化学能转变成电能
D.国家速滑馆“冰丝带”采用CO 超临界制冰,比氟利昂制冰更加环保
2
2.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.标准状况下,22.4L HF中含有电子数为10N
A
B.标准状况下,46g C HOH中含有极性键的数目为7N
2 5 A
C.相同体积的CO和H 完全燃烧,消耗O 的物质的量相同
2 2
D.标准状况下,11.2L Cl 溶于水,溶液中Cl-、ClO-、HClO的微粒数之和为N
2 A
3.下表所列各组物质中,物质之间通过一步反应能实现如图所示转化的是
选项 X Y Z 物质转化关系
A Cu CuO Cu(OH)
2
B Si SiO HSiO
2 2 3
C NaHCO NaCO NaOH
3 2 3
D FeCl FeO FeCl
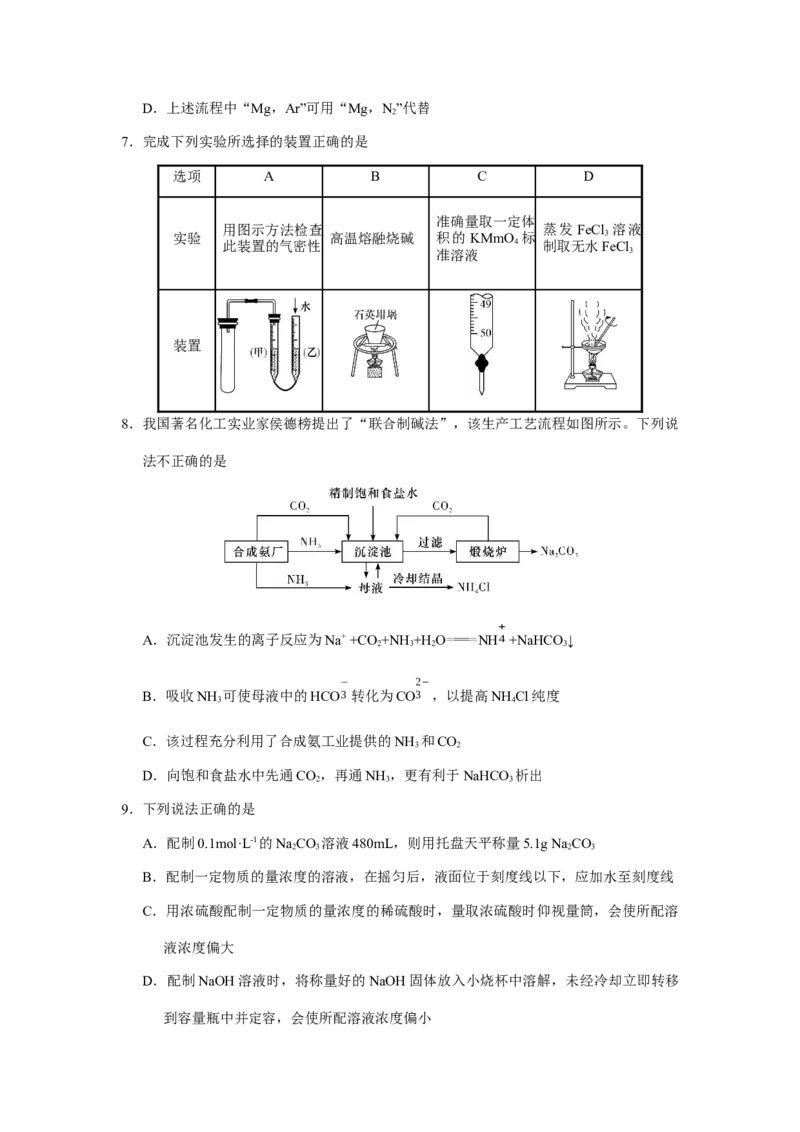
2 34.火法炼铜首先要焙烧黄铜矿,其反应为 2CuFeS+O Cu S+2FeS+SO 。某种产物的
2 2 2 2
晶胞结构如图所示。下列说法错误的是
A.O 为氧化剂,CuFeS 既是氧化剂又是还原剂
2 2
B.该晶胞结构图表示的是FeS
C.晶胞中S的配位数为12
D.每生成1mol FeS,有0.5mol硫元素被氧化
5.某无色溶液中可能大量存在的离子组是
2− + −
A.K+、Na+、S2-、SO3 B.H+、NH4、NO3 、I-
2− + 2−
C.Fe3+、Mg2+、Cl-、SO4 D.K+、NH4、CO3 、OH-
6.“绿水青山”是习近平总书记构建美丽中国的伟大构想,某化工集团为减少环境污染,
提高资源的利用率,将“钛厂、氯碱厂、甲醇厂”进行联合生产。其主要生产工艺如下
(FeTiO 中Ti为+4价):
3
下列叙述正确的是
A.该流程中只有“电解” “氯化” “合成”涉及氧化还原反应
B.“合成”反应中氧化剂与还原剂的物质的量之比为2:1
C.“氯化”时焦炭和钛铁矿都是还原剂D.上述流程中“Mg,Ar”可用“Mg,N”代替
2
7.完成下列实验所选择的装置正确的是
选项 A B C D
准确量取一定体
用图示方法检查 蒸发 FeCl 溶液
实验 高温熔融烧碱 积的 KMmO 标 3
此装置的气密性 4 制取无水FeCl
准溶液 3
装置
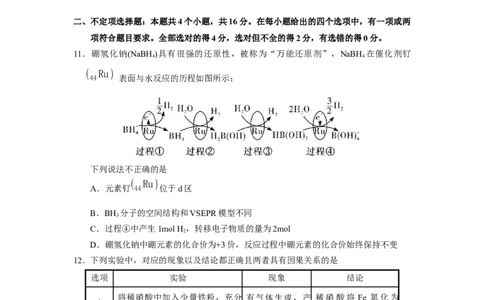
8.我国著名化工实业家侯德榜提出了“联合制碱法”,该生产工艺流程如图所示。下列说
法不正确的是
+
A.沉淀池发生的离子反应为Na+ +CO +NH+H O NH4+NaHCO↓
2 3 2 3
− 2−
B.吸收NH 可使母液中的HCO3 转化为CO3 ,以提高NH Cl纯度
3 4
C.该过程充分利用了合成氨工业提供的NH 和CO
3 2
D.向饱和食盐水中先通CO,再通NH ,更有利于NaHCO 析出
2 3 3
9.下列说法正确的是
A.配制0.1mol·L-1的NaCO 溶液480mL,则用托盘天平称量5.1g Na CO
2 3 2 3
B.配制一定物质的量浓度的溶液,在摇匀后,液面位于刻度线以下,应加水至刻度线
C.用浓硫酸配制一定物质的量浓度的稀硫酸时,量取浓硫酸时仰视量筒,会使所配溶
液浓度偏大
D.配制NaOH溶液时,将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转移
到容量瓶中并定容,会使所配溶液浓度偏小10.下列离子方程式正确的是
2−
A.NaO 固体与水反应:2O2 +2H O 4OH- +O ↑
2 2 2 2
B.Fe和稀盐酸反应:2Fe+6H+ 2Fe3+ +3H ↑
2
−
C.Ca(HCO ) 溶液中滴入少量Ca(OH) 溶液:Ca2+ +OH- +HCO3 CaCO ↓+H O
3 2 2 3 2
D.碳酸氢钠溶液与过量的澄清石灰水反应:
− 2−
2HCO3 +Ca2+ +2OH- CaCO ↓+CO3 +2H O
3 2
二、不定项选择题:本题共4个小题,共16分。在每小题给出的四个选项中,有一项或两
项符合题目要求。全部选对的得4分,选对但不全的得2分,有选错的得0分。
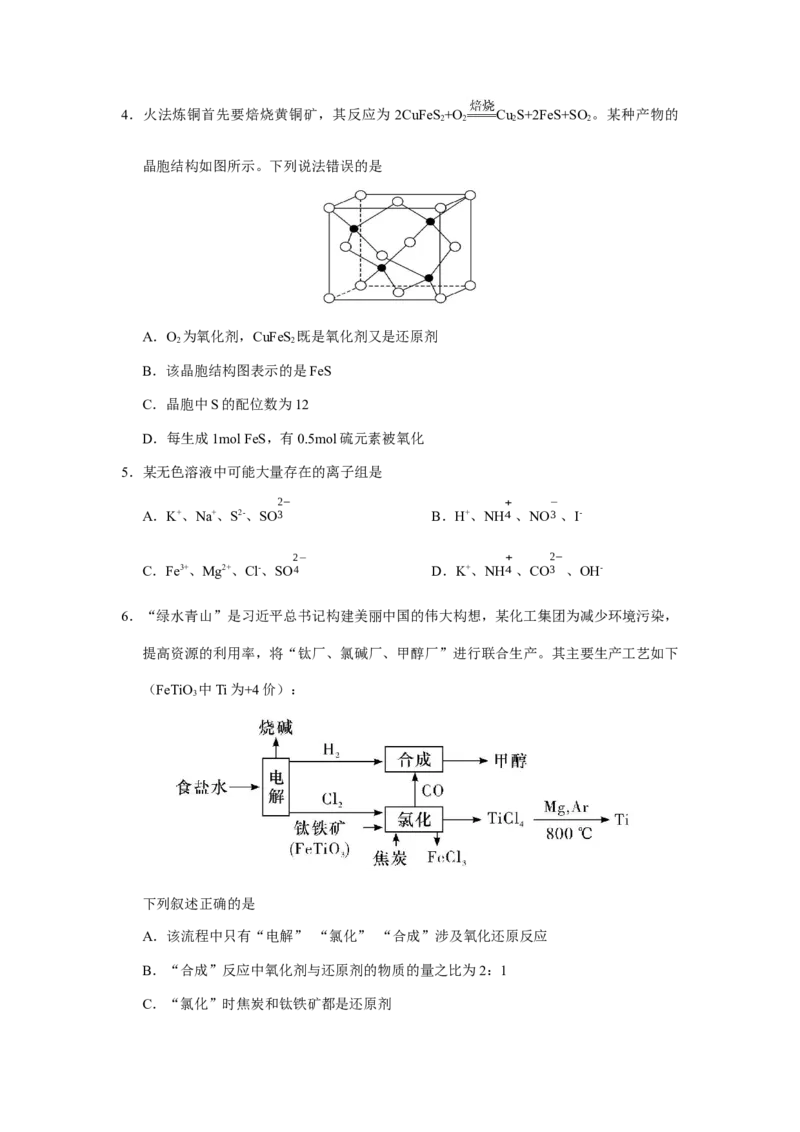
11.硼氢化钠(NaBH )具有很强的还原性,被称为“万能还原剂”,NaBH 在催化剂钌
4 4
( Ru)
44 表面与水反应的历程如图所示:
下列说法不正确的是
( Ru)
A.元素钌 44 位于d区
B.BH 分子的空间结构和VSEPR模型不同
3
C.过程④中产生1mol H,转移电子物质的量为2mol
2
D.硼氢化钠中硼元素的化合价为+3价,反应过程中硼元素的化合价始终保持不变
12.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
选项 实验 现象 结论
将稀硝酸中加入少量铁粉,充分 有气体生成,产 稀硝酸将 Fe 氧化为
A
反应后滴加KSCN溶液 生血红色沉淀 Fe3+
将铜粉加入 1.0mol·L-1 Fe (SO ) 溶液变蓝、有黑
B 2 4 3 金属铁比铜活泼
溶液中 色固体出现
用坩埚钳夹住一小块用砂纸仔细 熔化后的液态铝
C 金属铝的熔点较低
打磨过的铝箔在酒精灯上加热 滴落下来
将 0.1mol·L-1 MgSO 溶液滴入 先有白色沉淀生
4 Cu(OH) 的溶度积比
D NaOH溶液至不再有沉淀产生, 成,后变为浅蓝 2
Mg(OH) 的小
再滴加0.1mol·L-1 CuSO 溶液 色沉淀 2
413.以粗盐(主要成分为NaCl)为原料制备NaClO 的工艺流程如下:
3
已知:①盐泥与水垢主要成分相同;
2− 2−
②Cr O7 +H O 2CrO4 +2H+。
2 2
下列说法正确的是
2−
A.粗盐中主要含有的杂质离子有Mg2+、Ca2+、SO4
2−
B.加入NaCr O 可调节溶液酸碱度,酸度过大会导致电解液中存在大量CrO4
2 2 7
C.电解池中温度过高会导致HClO分解和Cl 逸出而降低NaClO 的产率
2 3
D.实验室进行浓缩结晶时须用到酒精灯、坩埚、三脚架、玻璃棒等仪器
14.将总物质的量为0.03mol的铜镁合金完全溶解于50mL 14mol/L的浓硝酸中,得到NO
2
气体nmol(还原产物只有NO ),再向反应后的溶液中加入V mL的1.0mol/L NaOH
2
溶液,金属离子恰好全部沉淀,称得该沉淀质量为2.54g,则下列说法正确的是
A.n=0.06mol
B.该合金质量为1.52g
C.沉淀完全后所得溶液中可能还有未反应完的硝酸
D.V=600mL
三、非选择题:本题共4小题,共54分。
15.(12分)亚硝酸钠(NaNO )是一种常见的食品添加剂,使用时必须严格控制其用量,
2
某兴趣小组进行下面实验探究,查阅资料知道:
①2NO+Na O 2NaNO ;
2 2 2
②2NO +Na O 2NaNO ;
2 2 2 3
③3NaNO +3HCl 3NaCl+HNO +2NO↑+HO;
2 3 2
− −
④酸性KMnO 溶液可将NO、NO2 氧化为NO3 ,本身被还原成Mn2+。
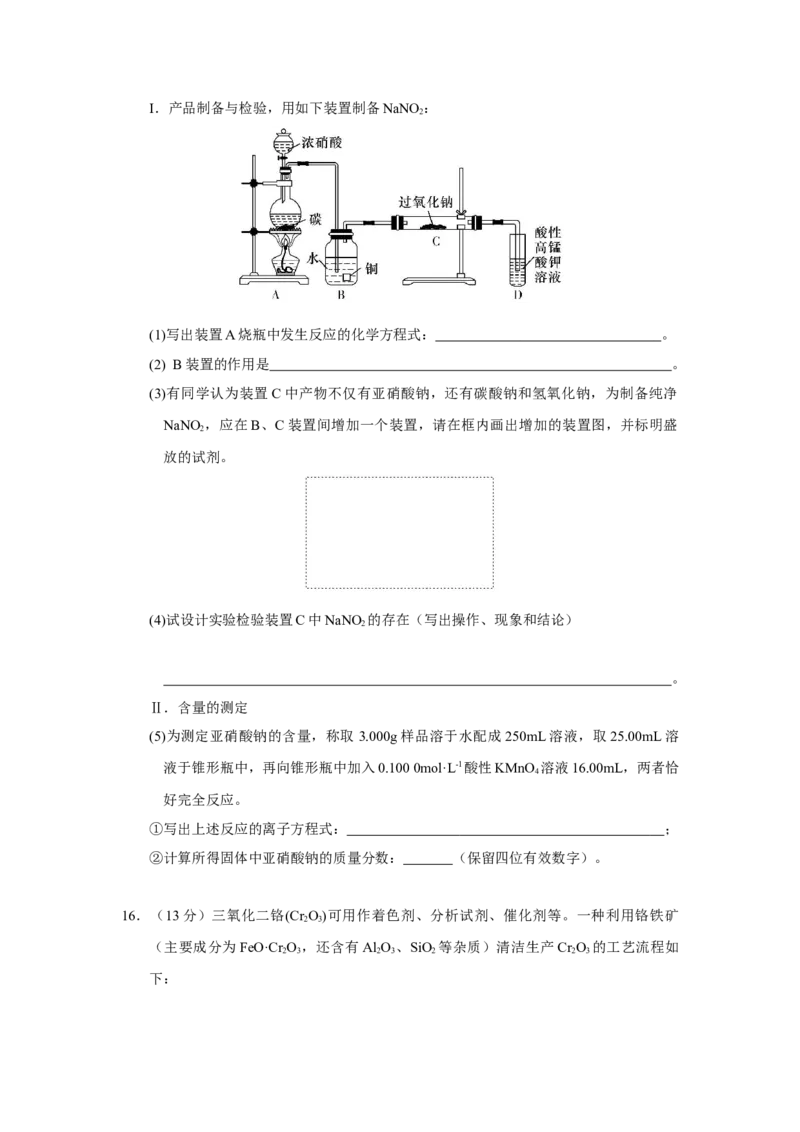
4I.产品制备与检验,用如下装置制备NaNO :
2
(1)写出装置A烧瓶中发生反应的化学方程式: 。
(2) B装置的作用是 。
(3)有同学认为装置C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,为制备纯净
NaNO ,应在B、C装置间增加一个装置,请在框内画出增加的装置图,并标明盛
2
放的试剂。
(4)试设计实验检验装置C中NaNO 的存在(写出操作、现象和结论)
2
。
Ⅱ.含量的测定
(5)为测定亚硝酸钠的含量,称取3.000g样品溶于水配成250mL溶液,取25.00mL溶
液于锥形瓶中,再向锥形瓶中加入0.100 0mol·L-1酸性KMnO 溶液16.00mL,两者恰
4
好完全反应。
①写出上述反应的离子方程式: ;
②计算所得固体中亚硝酸钠的质量分数: (保留四位有效数字)。
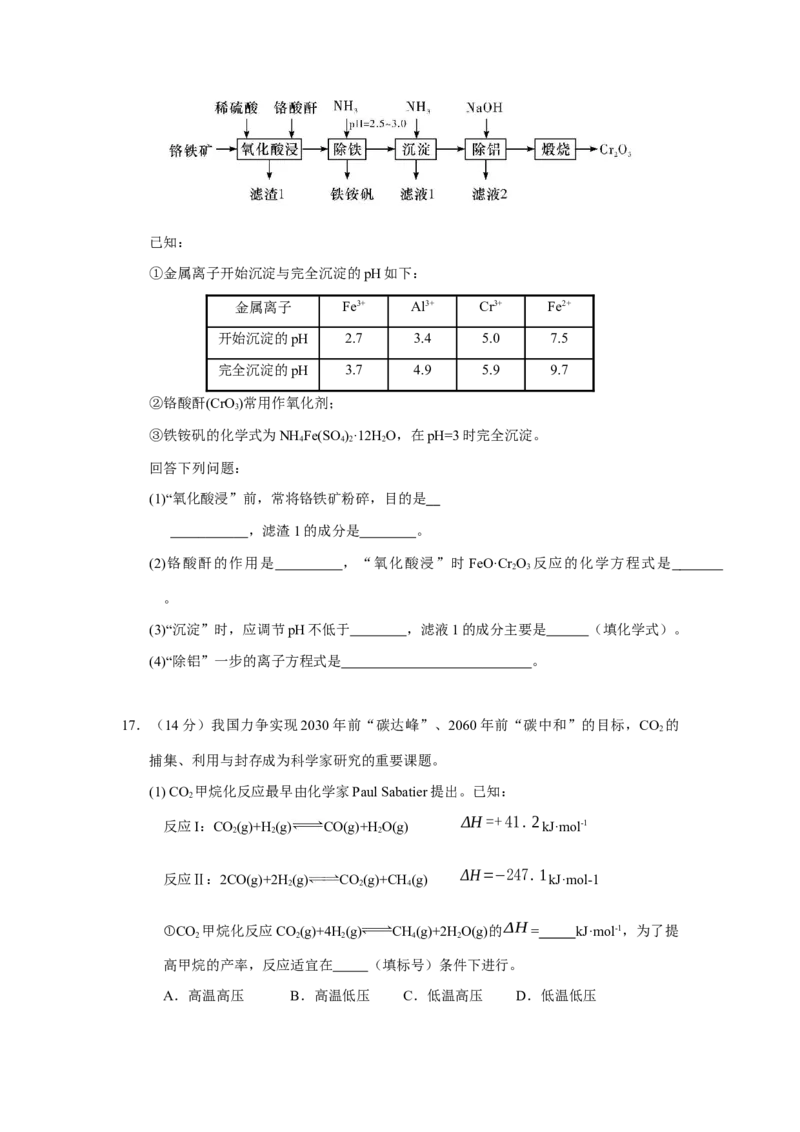
16.(13分)三氧化二铬(CrO)可用作着色剂、分析试剂、催化剂等。一种利用铬铁矿
2 3
(主要成分为FeO·Cr O ,还含有Al O 、SiO 等杂质)清洁生产Cr O 的工艺流程如
2 3 2 3 2 2 3
下:已知:
①金属离子开始沉淀与完全沉淀的pH如下:
金属离子 Fe3+ Al3+ Cr3+ Fe2+
开始沉淀的pH 2.7 3.4 5.0 7.5
完全沉淀的pH 3.7 4.9 5.9 9.7
②铬酸酐(CrO )常用作氧化剂;
3
③铁铵矾的化学式为NH Fe(SO )·12HO,在pH=3时完全沉淀。
4 4 2 2
回答下列问题:
(1)“氧化酸浸”前,常将铬铁矿粉碎,目的是
,滤渣1的成分是 。
(2)铬酸酐的作用是 ,“氧化酸浸”时 FeO·Cr O 反应的化学方程式是
2 3
。
(3)“沉淀”时,应调节pH不低于 ,滤液1的成分主要是 (填化学式)。
(4)“除铝”一步的离子方程式是 。
17.(14分)我国力争实现2030年前“碳达峰”、2060年前“碳中和”的目标,CO 的
2
捕集、利用与封存成为科学家研究的重要课题。
(1) CO 甲烷化反应最早由化学家Paul Sabatier提出。已知:
2
ΔH=+41.2
反应I:CO(g)+H(g) CO(g)+HO(g) kJ·mol-1
2 2 2
反应Ⅱ:2CO(g)+2H(g) CO(g)+CH (g)
ΔH=−247.1
kJ·mol-1
2 2 4
①CO 甲烷化反应CO(g)+4H(g) CH(g)+2HO(g)的ΔH = kJ·mol-1,为了提
2 2 2 4 2
高甲烷的产率,反应适宜在 (填标号)条件下进行。
A.高温高压 B.高温低压 C.低温高压 D.低温低压②反应 I:CO(g)+H(g) CO(g)+HO(g) ΔH = +41.2kJ·mol-1,已知反应的
2 2 2
v =k c(CO )⋅c(H ) v =k c(H O)⋅¿¿c(CO)(k 、k
正 正 2 2 , 逆 逆 2 正 逆为速率常数,与温
k
逆
k
度、催化剂有关)。若平衡后升高温度,则 正 (填“增大”“不变”或“减
小”);若反应I在恒容绝热的容器中发生,下列情况下反应一定达到平衡状态的
是 (填标号)。
A.容器内的压强不再改变
B.容器内气体密度不再改变
C.容器内c(CO):c(H ):c(CO):c(H O)=1:1:1:1
2 2 2
D.单位时间内,断开C O的数目和断开H—O的数目相同
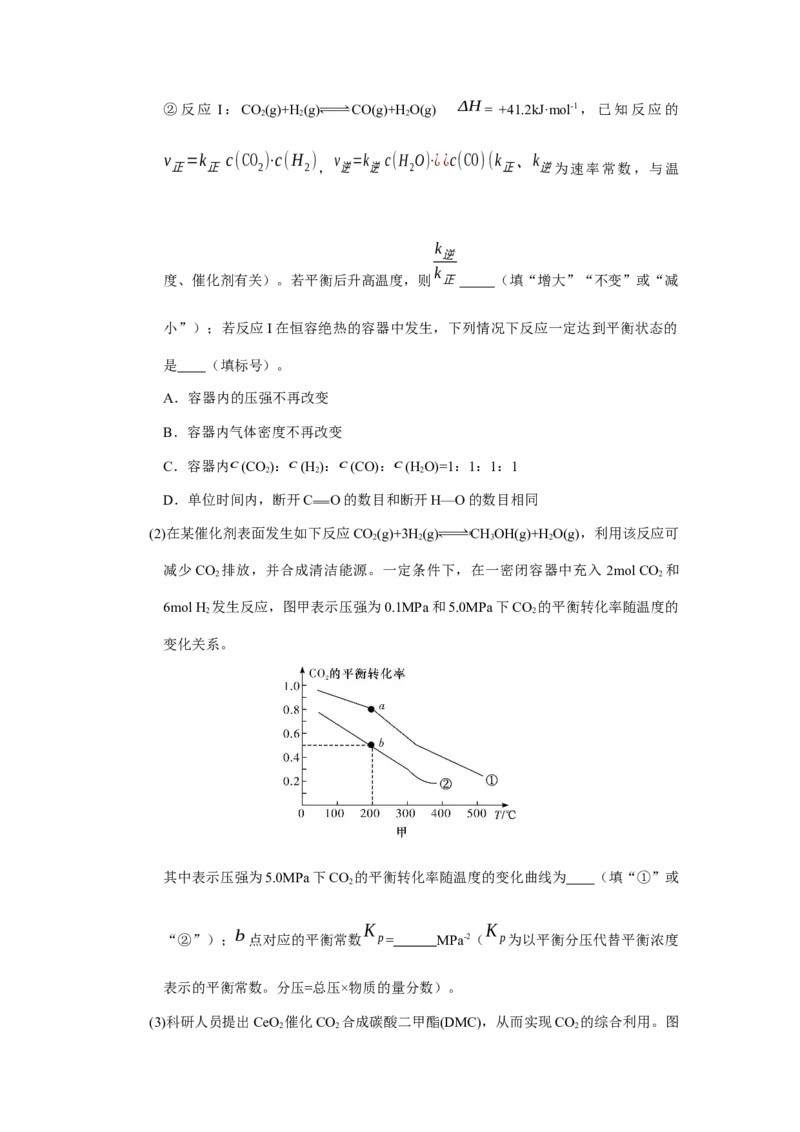
(2)在某催化剂表面发生如下反应CO(g)+3H(g) CHOH(g)+H O(g),利用该反应可
2 2 3 2
减少CO 排放,并合成清洁能源。一定条件下,在一密闭容器中充入 2mol CO 和
2 2
6mol H 发生反应,图甲表示压强为0.1MPa和5.0MPa下CO 的平衡转化率随温度的
2 2
变化关系。
其中表示压强为5.0MPa下CO 的平衡转化率随温度的变化曲线为 (填“①”或
2
K K
b
“②”); 点对应的平衡常数 p= MPa-2( p为以平衡分压代替平衡浓度
表示的平衡常数。分压=总压×物质的量分数)。
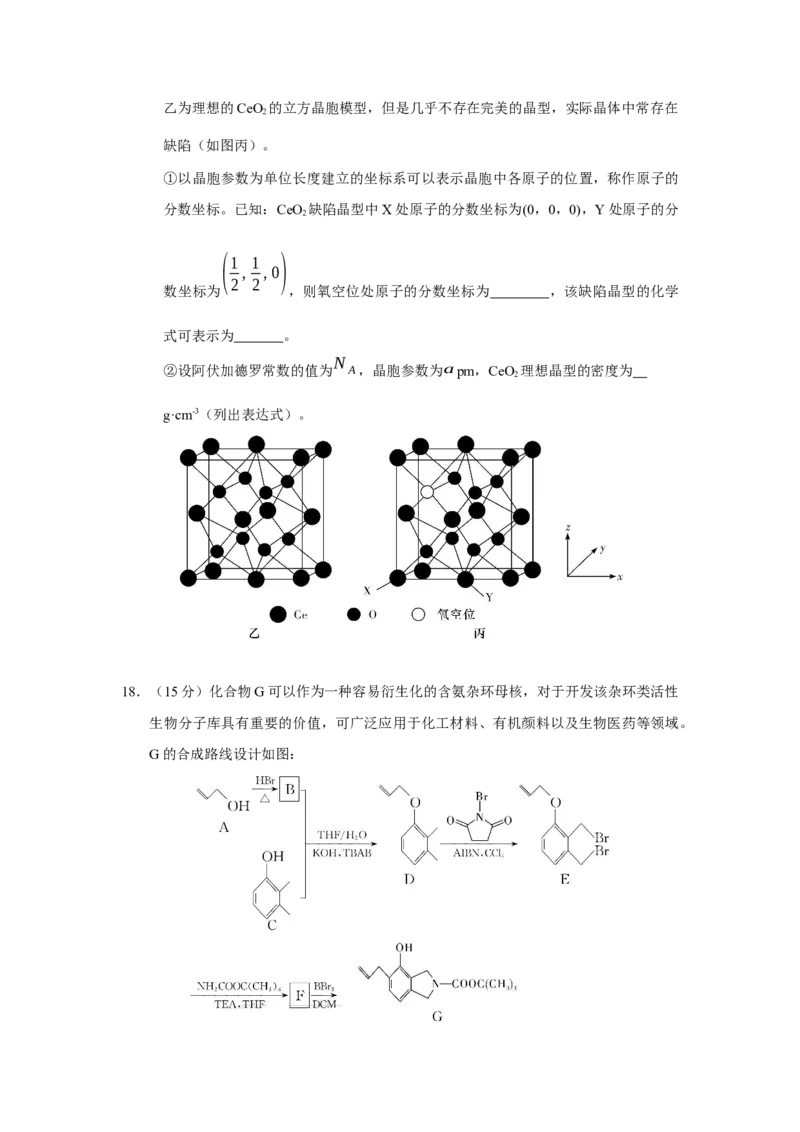
(3)科研人员提出CeO 催化CO 合成碳酸二甲酯(DMC),从而实现CO 的综合利用。图
2 2 2乙为理想的CeO 的立方晶胞模型,但是几乎不存在完美的晶型,实际晶体中常存在
2
缺陷(如图丙)。
①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的
分数坐标。已知:CeO 缺陷晶型中X处原子的分数坐标为(0,0,0),Y处原子的分
2
(1 1 )
, , 0
2 2
数坐标为 ,则氧空位处原子的分数坐标为 ,该缺陷晶型的化学
式可表示为 。
N
②设阿伏加德罗常数的值为 A,晶胞参数为apm,CeO 理想晶型的密度为
2
g·cm-3(列出表达式)。
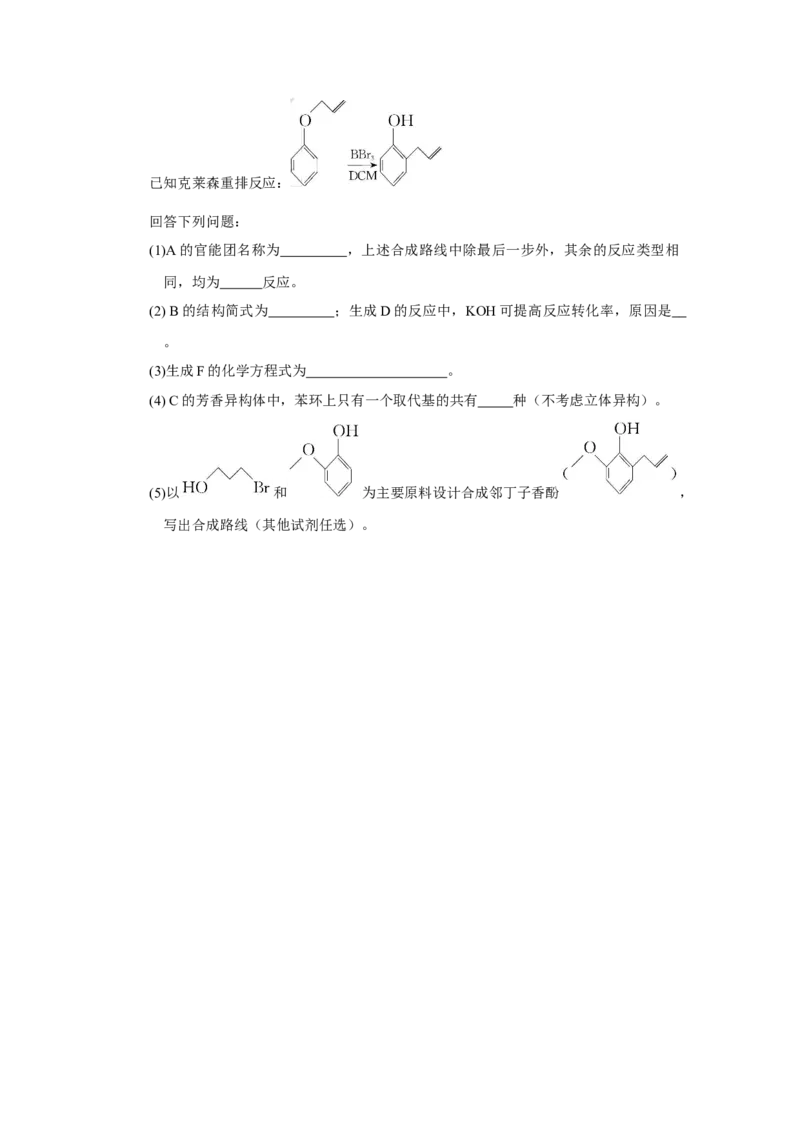
18.(15分)化合物G可以作为一种容易衍生化的含氨杂环母核,对于开发该杂环类活性
生物分子库具有重要的价值,可广泛应用于化工材料、有机颜料以及生物医药等领域。
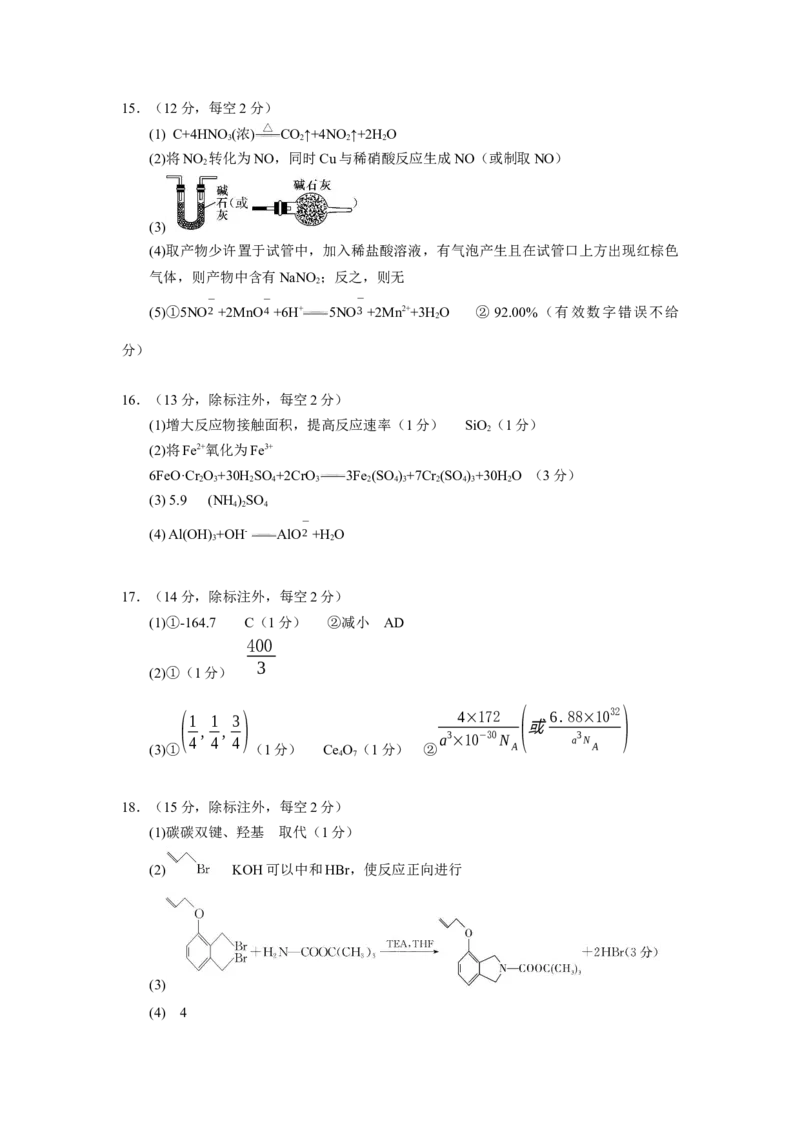
G的合成路线设计如图:已知克莱森重排反应:
回答下列问题:
(1)A的官能团名称为 ,上述合成路线中除最后一步外,其余的反应类型相
同,均为 反应。
(2) B的结构简式为 ;生成D的反应中,KOH可提高反应转化率,原因是
。
(3)生成F的化学方程式为 。
(4) C的芳香异构体中,苯环上只有一个取代基的共有 种(不考虑立体异构)。
(5)以 和 为主要原料设计合成邻丁子香酚 ,
写出合成路线(其他试剂任选)。化学参考答案
一、选择题:本题共10小题,每小题3分,共30分。在每小题给出的四个选项中,只有
一项是符合题目要求的。
题号 1 2 3 4 5 6 7 8 9 10
答案 B B C C A C A D C C
二、不定项选择题:本题共4个小题,共16分。在每小题给出的四个选项中,有一项或两
项符合题目要求。全部选对的得4分,选对但不全的得2分,有选错的得0分。
题号 11 12 13 14
答案 BC D AC AB
12.D【解析】稀硝酸中加入少量铁粉,生成Fe3+和NO,充分反应后加入KSCN溶液,实
验现象是有气体生成,溶液呈血红色,不会产生沉淀,A错误;将铜粉加入1.0mol·L-1
Fe (SO ) 溶液中,溶液变蓝,发生了反应:2Fe3++Cu 2Fe2++Cu2+,说明氧化性
2 4 3
Fe3+>Cu2+,没有黑色固体出现,B错误;用坩埚钳夹住一小块用砂纸仔细打磨过的铝
箔在酒精灯上加热,打磨后的铝箔很快和空气中的氧气反应生成Al O ,Al O 熔点高,
2 3 2 3
包裹着熔化的铝,熔化后的液态铝不会滴落下来,C错误;将0.1mol·L-1 MgSO 溶液
4
滴入 NaOH 溶液至不再有沉淀产生,说明 NaOH 已反应完全,再滴加 0.1mol·L-1
CuSO 溶液,白色沉淀变为浅蓝色沉淀,说明Cu(OH) 的溶度积比Mg(OH) 的小,D
4 2 2
正确。
14.AB【解析】铜镁合金总物质的量为0.03mol,则与硝酸反应转移0.06mol电子,硝酸
得电子生成NO ,N元素化合价由+5降低为+4,根据得失电子守恒,生成NO 的物质
2 2
的量为 0.06mol,故 A 正确;铜镁合金总物质的量为 0.03mol,与硝酸反应失去
0.06mol电子,则生成的氢氧化物中结合氢氧根离子的物质的量为 0.06mol,所以该合
金质量为2.54g-0.06mol×17g/mol= 1.52g,故B正确;氢氧化钠先与硝酸反应,再与硝
酸铜、硝酸镁反应生成沉淀,沉淀完全后所得溶液中不可能有未反应完的硝酸,故C
V
错误;加入 mL的1.0mol/L NaOH溶液,金属离子恰好全部沉淀,溶液中的溶质为
−
NaNO ,n(Na+)=n(NO3 )=0.05L×14mol/L-0.06mol=0.64mol,加入 1.0mol/L NaOH 溶
3
0.64mol
V=
液的体积
1mol/L
=0.64L=640mL,故D错误。
三、非选择题:本题共4小题,共54分。15.(12分,每空2分)
(1) C+4HNO (浓) CO↑+4NO↑+2H O
3 2 2 2
(2)将NO 转化为NO,同时Cu与稀硝酸反应生成NO(或制取NO)
2
(3)
(4)取产物少许置于试管中,加入稀盐酸溶液,有气泡产生且在试管口上方出现红棕色
气体,则产物中含有NaNO ;反之,则无
2
− − −
(5)①5NO2 +2MnO4 +6H+ 5NO3 +2Mn2++3H O ② 92.00%(有效数字错误不给
2
分)
16.(13分,除标注外,每空2分)
(1)增大反应物接触面积,提高反应速率(1分) SiO(1分)
2
(2)将Fe2+氧化为Fe3+
6FeO·Cr O+30H SO +2CrO 3Fe (SO )+7Cr (SO )+30H O (3分)
2 3 2 4 3 2 4 3 2 4 3 2
(3) 5.9 (NH )SO
4 2 4
−
(4) Al(OH)+OH- AlO2 +H O
3 2
17.(14分,除标注外,每空2分)
(1)①-164.7 C(1分) ②减小 AD
400
3
(2)①(1分)
(1
,
1
,
3) 4×172 (
或
6.88×1032 )
4 4 4
a3 ×10−30N
a
3
N
(3)① (1分) Ce O(1分) ② A A
4 7
18.(15分,除标注外,每空2分)
(1)碳碳双键、羟基 取代(1分)
(2) KOH可以中和HBr,使反应正向进行
(3)
(4) 4(5)下载最新免费模拟卷,到公众号:一枚试卷君