文档内容
热点 02 表格型实验方案的设计与评价
►命题趋势►解题策略►真题回眸►限时检测
考向一 判断实验操作、现象、结论是否匹配
表格型实验方案的设计与评价(选择题) 考向二 根据实验目的设计实验方案
考向三 气体制备、收集、除杂方案设计与评价
实验方案设计与评价是近几年新高考对于实验的重要考查形式,表格型实验设计分析与评价仍然是
2024年高考实验考查的热点。题目涉及实验操作、实验原理、实验现象及其因果关系的分析判断与评价,
融合了元素化合物、化学反应原理、基础有机化学等不同角度的知识点,信息容量大,综合性强。
预计2024年高考,命题方式大致有以下几种:
(1)利用教材实验按照实验操作与实验现象的匹配关系进行设计。
(2)改变或拓展教材实验进行设计。
(3)利用教材中有明显现象的不常见反应进行设计。
其中,化学平衡的移动原理探究实验、沉淀溶解平衡、糖类水解、卤代烃中卤素原子的检验等实验仍
是考察的重点。
【策略1】熟记常考20例表格型实验选项
序号 实验操作 实验目的 正误
向2 mL 1 mol·L-1 NaOH溶液中先加入3滴1 mol·L- 证明
1 ×
1 FeCl 溶液,再加入3滴1 mol·L-1 MgCl 溶液 K [Mg(OH) ]>K [Fe(OH) ]
3 2 sp 2 sp 3
相同温度下,向两支盛有相同体积不同浓度HO 溶
2 2
探究Cu2+、Fe3+对HO 分解
2 2
2 液的试管中分别滴入适量相同浓度的CuSO 溶液和 ×
4
速率的影响
FeCl 溶液
3
室温下,用pH试纸分别测定浓度为0.1 mol·
比较HClO和CHCOOH的
3
3 L-1 NaClO溶液和0.1 mol·L-1 CHCOONa溶液的 ×
3
酸性强弱
pH
向含有酚酞的NaCO 溶液中加入少量BaCl 固体, 证明NaCO 溶液中存在水
2 3 2 2 3
4 √
溶液红色变浅 解平衡
分别测定室温下等物质的量浓度的NaSO 与NaCO
2 3 2 3
5 证明非金属性:S>C ×
溶液的pH,后者较大
将NaOH溶液滴入某溶液中加热,放出的气体能使
6 证明溶液中有NH √
湿润的红色石蕊试纸变蓝
7 分别通入硝酸银溶液中,产生淡黄色沉淀的是溴蒸 鉴别溴蒸气和NO √
2气
8 在醋酸钠溶液中滴入酚酞溶液,加热后红色加深 证明盐类水解是吸热反应 √
将硫酸酸化的HO 溶液滴入Fe(NO ) 溶液中,溶液
2 2 3 2
9 证明氧化性:HO 比Fe3+强 ×
2 2
变黄色
往黄色固体难溶物PbI 中加水,振荡,静置。取上 证明难溶物存在沉淀溶解平
2
10 √
层清液,然后加入NaI固体,产生黄色沉淀 衡
11 向AgCl悬浊液中加入NaI溶液时出现黄色沉淀 K (AgCl)< K (AgI) ×
sp sp
先在托盘上各放一张滤纸,然后在右盘上添加2 g砝
12 称取2.0 g NaOH固体 ×
码,左盘上添加NaOH固体
13 将FeCl 固体溶解于适量蒸馏水 配制FeCl 溶液 ×
3 3
向沸水中逐滴加入1~2 mL FeCl 饱和溶液,搅拌并
3
14 制备Fe(OH) 胶体 ×
3
继续煮沸出现浑浊
15 测定等物质的量浓度的盐酸、硝酸的pH 比较Cl、N的非金属性强弱 ×
证明二者是离子化合物还是
16 用熔融氧化铝、CCl 做导电性实验 √
4
共价化合物
向含有少量FeCl 的MgCl 溶液中加入足量Mg(OH)
3 2 2
17 除去MgCl 溶液中少量FeCl √
2 3
粉末,搅拌一段时间后过滤
将CHCHBr与NaOH溶液共热,冷却后,取出上层
3 2
检验CHCHBr中存在的溴
3 2
18 水溶液,加入AgNO 溶液,观察是否产生淡黄色沉 ×
3
元素
淀
取一定质量的样品与足量盐酸反应,用碱石灰吸收 测定NaCO(含NaCl)样品纯
2 3
19 ×
产生的气体 度
20 将洗净的容量瓶放在烘箱中烘干 缩短容量瓶干燥的时间 ×
【策略2】回归教材:常考有机实验设计方案及评价
(1)卤代烃中卤素原子的检验
取少量卤代烃于试管中,加入NaOH水溶液,加热,冷却后,加入稀硝酸中和溶液
至酸性,再加入AgNO 溶液。若出现黄色沉淀,则卤代烃中含有I-离子;若出现浅
3
实验步骤
黄色沉淀,则卤代烃中含有 Br-离子;若出现白色沉淀,则卤代烃中含有 Cl-离
子。
实验流程
⃗H O
2
相关方程式 R—X+NaOH Δ ROH+NaX
HNO+NaOH===NaNO +HO
3 3 2AgNO+NaX===AgX↓+NaNO
3 3
①条件:NaOH水溶液,加热;
微点拨 ②一定要先加入稀硝酸中和溶液至酸性,再加入硝酸银溶液,否则会出现 Ag O黑
2
色沉淀,影响卤原子的检验;
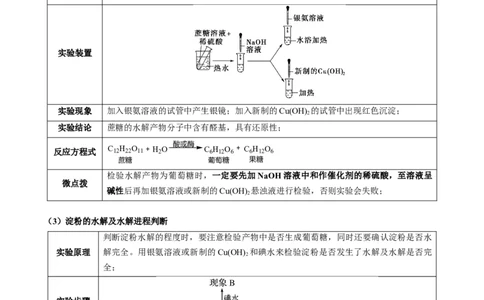
(2)蔗糖水解及水解产物的检验
在洁净的试管中加入1 mL 10%蔗糖溶液和5滴10% H SO 溶液,热水浴中加热。待溶
2 4
实验内容 液冷却后向其中加入NaOH溶液至溶液呈碱性,再加入银氨溶液或新制备的Cu(OH) ,
2
加热,观察现象。
实验装置
实验现象 加入银氨溶液的试管中产生银镜;加入新制的Cu(OH) 的试管中出现红色沉淀;
2
实验结论 蔗糖的水解产物分子中含有醛基,具有还原性;
酸或酶
反应方程式 C 12 H 22 O 11+H 2 O C 6 H 12 O 6 + C 6 H 12 O 6
蔗糖 葡萄糖 果糖
检验水解产物为葡萄糖时,一定要先加NaOH溶液中和作催化剂的稀硫酸,至溶液呈
微点拨
碱性后再加银氨溶液或新制的Cu(OH) 悬浊液进行检验,否则实验会失败;
2
(3)淀粉的水解及水解进程判断
判断淀粉水解的程度时,要注意检验产物中是否生成葡萄糖,同时还要确认淀粉是否水
实验原理 解完全。用银氨溶液或新制的Cu(OH) 和碘水来检验淀粉是否发生了水解及水解是否完
2
全;
实验步骤
现象A 现象B 结论
实验现象 未产生银镜 溶液呈蓝色 未水解
及结论 出现银镜 溶液呈蓝色 部分水解
出现银镜 溶液不呈蓝色 完全水解
①检验葡萄糖生成时要注意水解液加碱呈碱性;
微点拨
②检验淀粉是否存在时,注意水解液不用加碱呈碱性,否则I 与碱反应;
2(4)蛋白质的盐析与变性的比较
盐析 变性
蛋白质在某些盐的浓溶液中溶解度降低 蛋白质在加热、强酸、强碱等条件下性质发生
概念
而析出 改变而凝结起来
特征 可逆 不可逆
实质 溶解度降低,物理变化 结构、性质改变,化学变化
加热、强酸、强碱、强氧化剂、紫外线、重金
条件 钠、镁、铝等轻金属盐或铵盐的浓溶液
属盐、苯酚、甲醛、乙醇等
用途 分离提纯蛋白质 杀菌、消毒
实例 硫酸铵或硫酸钠等盐溶液使蛋白质盐析 重金属盐(例如硫酸铜)溶液能使蛋白质变性
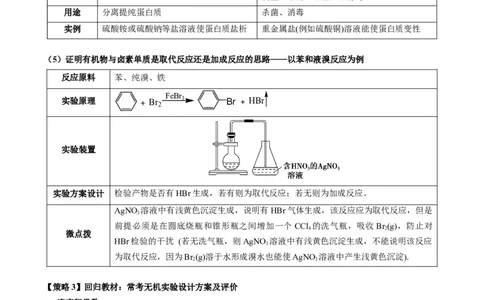
(5)证明有机物与卤素单质是取代反应还是加成反应的思路——以苯和液溴反应为例
反应原料 苯、纯溴、铁
FeBr
实验原理 +Br
2
3 Br +HBr
实验装置
实验方案设计 检验产物是否有HBr生成,若有则为取代反应;若无则为加成反应。
AgNO 溶液中有浅黄色沉淀生成,说明有HBr气体生成,该反应应为取代反应,但是
3
前提必须是在圆底烧瓶和锥形瓶之间增加一个 CCl 的洗气瓶,吸收Br (g),防止对
4 2
微点拨
HBr检验的干扰 (若无洗气瓶,则AgNO 溶液中有浅黄色沉淀生成,不能说明该反应
3
为取代反应,因为Br (g)溶于水形成溴水也能使AgNO 溶液中产生浅黄色沉淀).
2 3
【策略3】回归教材:常考无机实验设计方案及评价
1.溶度积常数
(1)AgCl、AgI、Ag S的转化
2
向盛有2 mL 0.1 mol·L-1 NaCl溶液的试管中滴加2滴0.1 mol·L-1 AgNO 溶液,观察并
3
实验步骤 记录现象;振荡试管,然后向其中滴加4滴0.1 mol·L-1 KI溶液,观察并记录现象;振
荡试管,然后再向其中滴加8滴0.1 mol·L-1 Na S溶液,观察并记录现象。
2实验示意图
实验现象 先有白色沉淀产生;然后白色沉淀转化为黄色沉淀;最后黄色沉淀转化为黑色沉淀。
NaCl+AgNO=== AgCl↓+NaNO
3 3
化学方程式 AgCl+KI===AgI+KCl
2AgI+NaS===Ag S+2NaI
2 2
AgCl沉淀转化为AgI沉淀,AgI沉淀又转化为Ag S沉淀,说明溶解度由小到大的顺序
2
实验结论
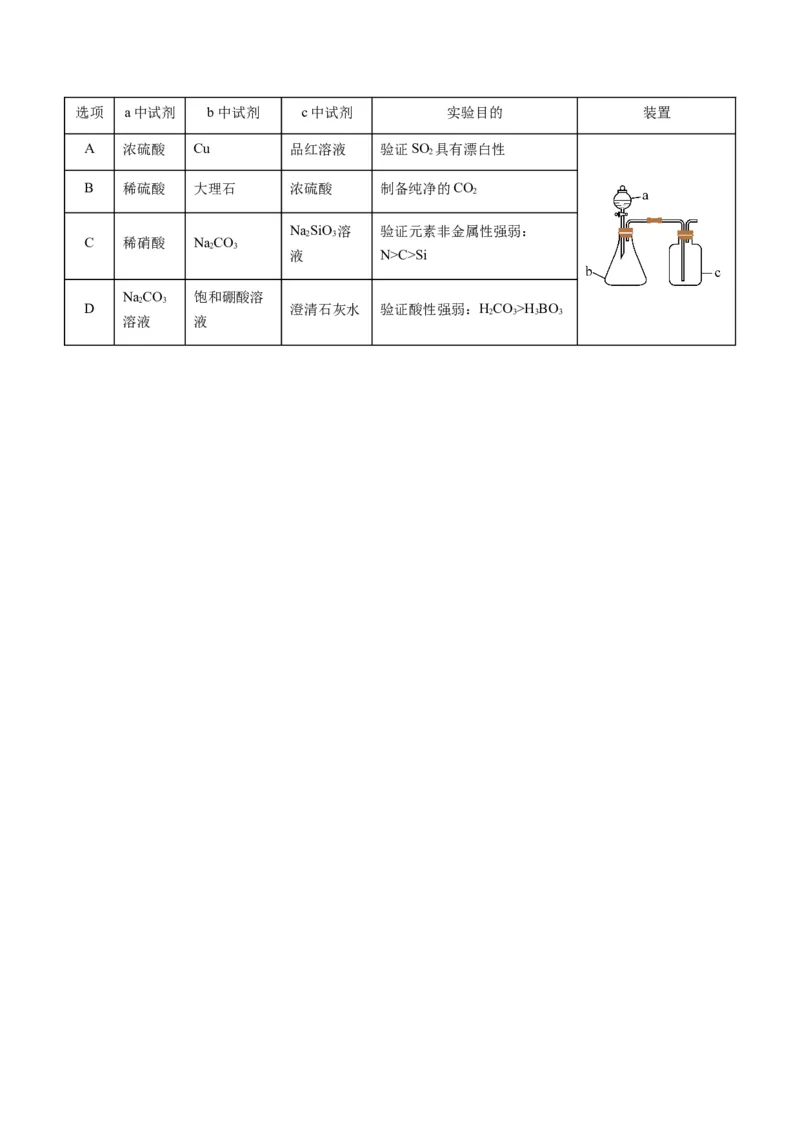
为Ag SC>Si
NaCO 饱和硼酸溶
2 3
D 澄清石灰水 验证酸性强弱:HCO>H BO
2 3 3 3
溶液 液