文档内容
热点强化练 12 化工生产中的速率、平衡图像分析
1.(2020·江苏化学,15)CH 与CO 重整生成H 和CO的过程中主要发生下列
4 2 2
反应
CH (g)+CO (g)2H (g)+2CO(g)
4 2 2
ΔH=247.1 kJ·mol-1
H (g)+CO (g)H O(g)+CO(g)
2 2 2
ΔH=41.2 kJ·mol-1
在恒压、反应物起始物质的量比n(CH )∶n(CO )=1∶1条件下,CH 和CO
4 2 4 2
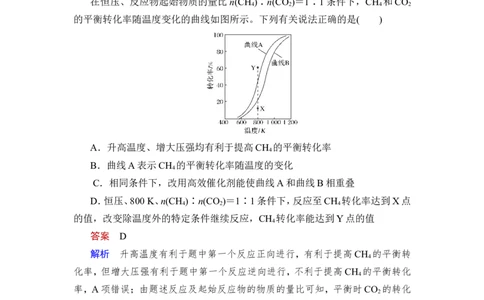
的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是( )
A.升高温度、增大压强均有利于提高CH 的平衡转化率
4
B.曲线A表示CH 的平衡转化率随温度的变化
4
C.相同条件下,改用高效催化剂能使曲线A和曲线B相重叠
D.恒压、800 K、n(CH )∶n(CO )=1∶1条件下,反应至CH 转化率达到X点
4 2 4
的值,改变除温度外的特定条件继续反应,CH 转化率能达到Y点的值
4
答案 D
解析 升高温度有利于题中第一个反应正向进行,有利于提高CH 的平衡转
4
化率,但增大压强有利于题中第一个反应逆向进行,不利于提高CH 的平衡转化
4
率,A项错误;由题述反应及起始反应物的物质的量比可知,平衡时CO 的转化
2
率比CH 的高,则曲线B表示CH 的平衡转化率随温度的变化,B项错误;使用
4 4
催化剂只能加快化学反应速率,对化学平衡无影响,即曲线A和曲线B不能相重
叠,C项错误;恒压、800 K、n(CH )∶n(CO )=1∶1条件下,反应至CH 转化率达
4 2 4
到X点的值,通过增大n(CO )或减小压强继续反应,可以使CH 的转化率从X点
2 4
提高到Y点,D项正确。
2.(2020·江西上饶市高三一模)研究煤的合理利用及CO 的综合应用有着重
2
要的意义。在体积为1 L的密闭容器中,充入1 mol CO 和2.5 mol H 发生反应:
2 2,2CO (g)+6H (g)C H (g)+4H O(g) ΔH=-128 kJ·mol-1,测得温度对催化
2 2 2 4 2
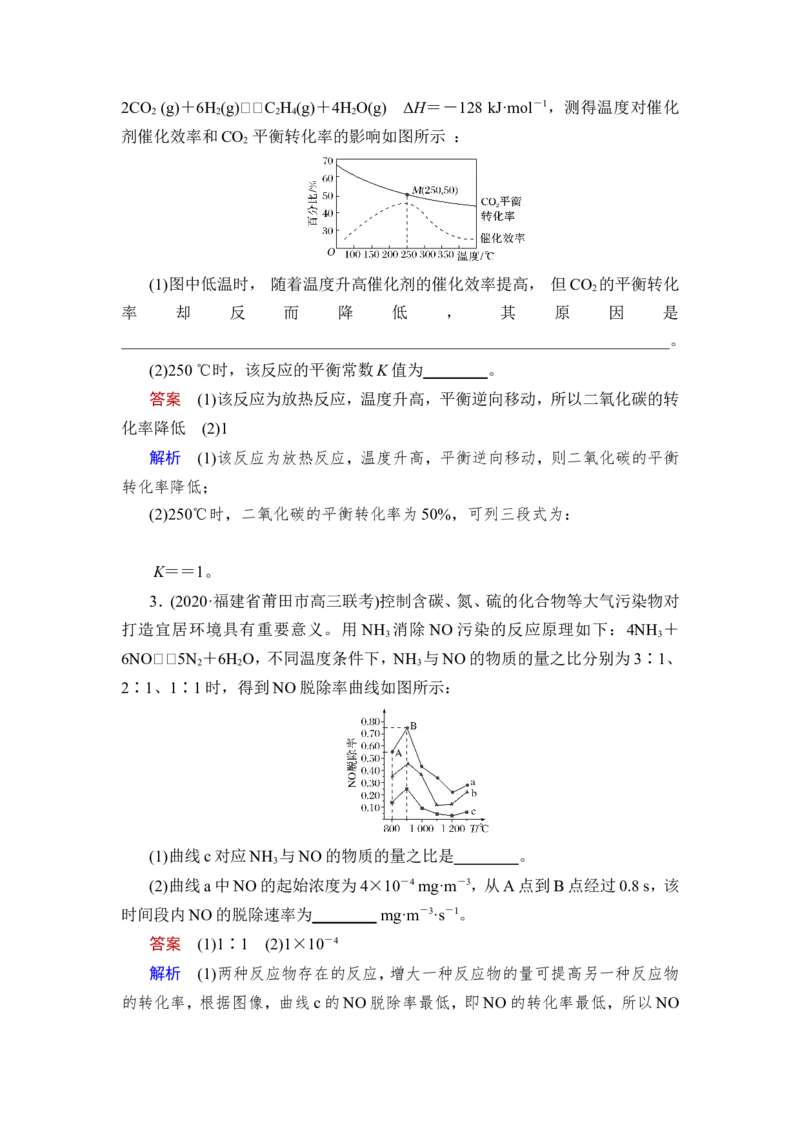
剂催化效率和CO 平衡转化率的影响如图所示 :
2
(1)图中低温时, 随着温度升高催化剂的催化效率提高, 但CO 的平衡转化
2
率 却 反 而 降 低 , 其 原 因 是
____________________________________________________________________。
(2)250 ℃时,该反应的平衡常数K值为________。
答案 (1)该反应为放热反应,温度升高,平衡逆向移动,所以二氧化碳的转
化率降低 (2)1
解析 (1)该反应为放热反应,温度升高,平衡逆向移动,则二氧化碳的平衡
转化率降低;
(2)250℃时,二氧化碳的平衡转化率为50%,可列三段式为:
K==1。
3.(2020·福建省莆田市高三联考)控制含碳、氮、硫的化合物等大气污染物对
打造宜居环境具有重要意义。用 NH 消除 NO污染的反应原理如下:4NH +
3 3
6NO5N +6H O,不同温度条件下,NH 与NO的物质的量之比分别为3∶1、
2 2 3
2∶1、1∶1时,得到NO脱除率曲线如图所示:
(1)曲线c对应NH 与NO的物质的量之比是________。
3
(2)曲线a中NO的起始浓度为4×10-4 mg·m-3,从A点到B点经过0.8 s,该
时间段内NO的脱除速率为________ mg·m-3·s-1。
答案 (1)1∶1 (2)1×10-4
解析 (1)两种反应物存在的反应,增大一种反应物的量可提高另一种反应物
的转化率,根据图像,曲线c的NO脱除率最低,即NO的转化率最低,所以NO在总反应物中的比例最高,符合的是n(NH )∶n(NO)的物质的量之比1∶1;(2)曲
3
线a中NO的起始浓度为4×10-4 mg/m3,从A点到B点经过0.8 s,根据图像,NO
的脱除率从 55%上升到 75%,则该段时间内 NO 的脱除量为 c=4×10-4
mg/m3×(75%-55%)=8×10-5 mg/m3,时间间隔为Δt=0.8 s,所以该段时间内
NO的脱除速率为==1.0×10-4 mg/(m3·s)。
4.(2020·陕西咸阳市高三二检)烯烃催化裂解是制备短链烯烃的重要途径。研
究表明,1-丁烯[CH CH CH===CH (g)]催化裂解时,发生两个平行竞争反应生成
3 2 2
丙烯和乙烯,两反应的热化学方程式为:
①3CH CH CH===CH (g)4CH CH===CH (g)
3 2 2 3 2
ΔH=+579 kJ·mol-1
②CH CH CH===CH (g)2CH ===CH (g)
3 2 2 2 2
ΔH=+283 kJ·mol-1
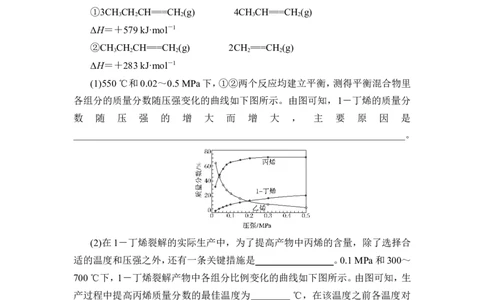
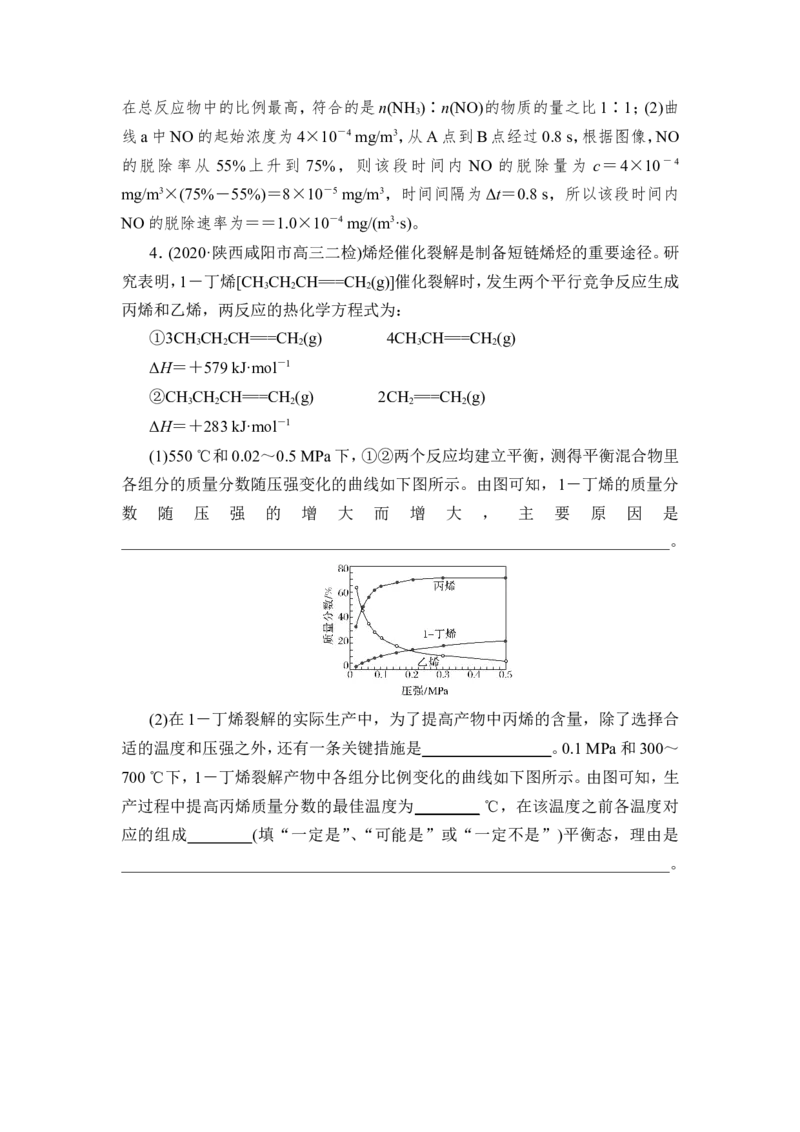
(1)550 ℃和0.02~0.5 MPa下,①②两个反应均建立平衡,测得平衡混合物里
各组分的质量分数随压强变化的曲线如下图所示。由图可知,1-丁烯的质量分
数 随 压 强 的 增 大 而 增 大 , 主 要 原 因 是
____________________________________________________________________。
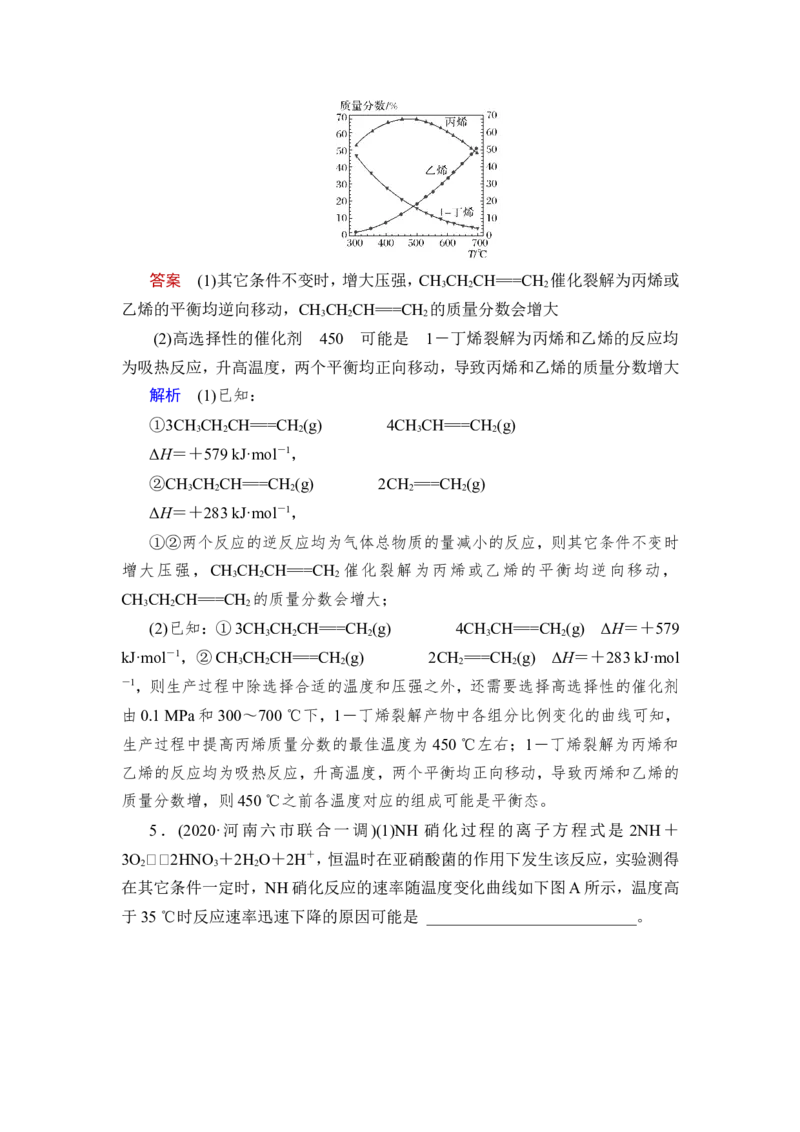
(2)在1-丁烯裂解的实际生产中,为了提高产物中丙烯的含量,除了选择合
适的温度和压强之外,还有一条关键措施是________________。0.1 MPa和300~
700 ℃下,1-丁烯裂解产物中各组分比例变化的曲线如下图所示。由图可知,生
产过程中提高丙烯质量分数的最佳温度为________ ℃,在该温度之前各温度对
应的组成________(填“一定是”、“可能是”或“一定不是”)平衡态,理由是
____________________________________________________________________。答案 (1)其它条件不变时,增大压强,CH CH CH===CH 催化裂解为丙烯或
3 2 2
乙烯的平衡均逆向移动,CH CH CH===CH 的质量分数会增大
3 2 2
(2)高选择性的催化剂 450 可能是 1-丁烯裂解为丙烯和乙烯的反应均
为吸热反应,升高温度,两个平衡均正向移动,导致丙烯和乙烯的质量分数增大
解析 (1)已知:
①3CH CH CH===CH (g)4CH CH===CH (g)
3 2 2 3 2
ΔH=+579 kJ·mol-1,
②CH CH CH===CH (g)2CH ===CH (g)
3 2 2 2 2
ΔH=+283 kJ·mol-1,
①②两个反应的逆反应均为气体总物质的量减小的反应,则其它条件不变时
增大压强,CH CH CH===CH 催化裂解为丙烯或乙烯的平衡均逆向移动,
3 2 2
CH CH CH===CH 的质量分数会增大;
3 2 2
(2)已知:①3CH CH CH===CH (g)4CH CH===CH (g) ΔH=+579
3 2 2 3 2
kJ·mol-1,②CH CH CH===CH (g)2CH ===CH (g) ΔH=+283 kJ·mol
3 2 2 2 2
-1,则生产过程中除选择合适的温度和压强之外,还需要选择高选择性的催化剂
由0.1 MPa和300~700 ℃下,1-丁烯裂解产物中各组分比例变化的曲线可知,
生产过程中提高丙烯质量分数的最佳温度为450 ℃左右;1-丁烯裂解为丙烯和
乙烯的反应均为吸热反应,升高温度,两个平衡均正向移动,导致丙烯和乙烯的
质量分数增,则450 ℃之前各温度对应的组成可能是平衡态。
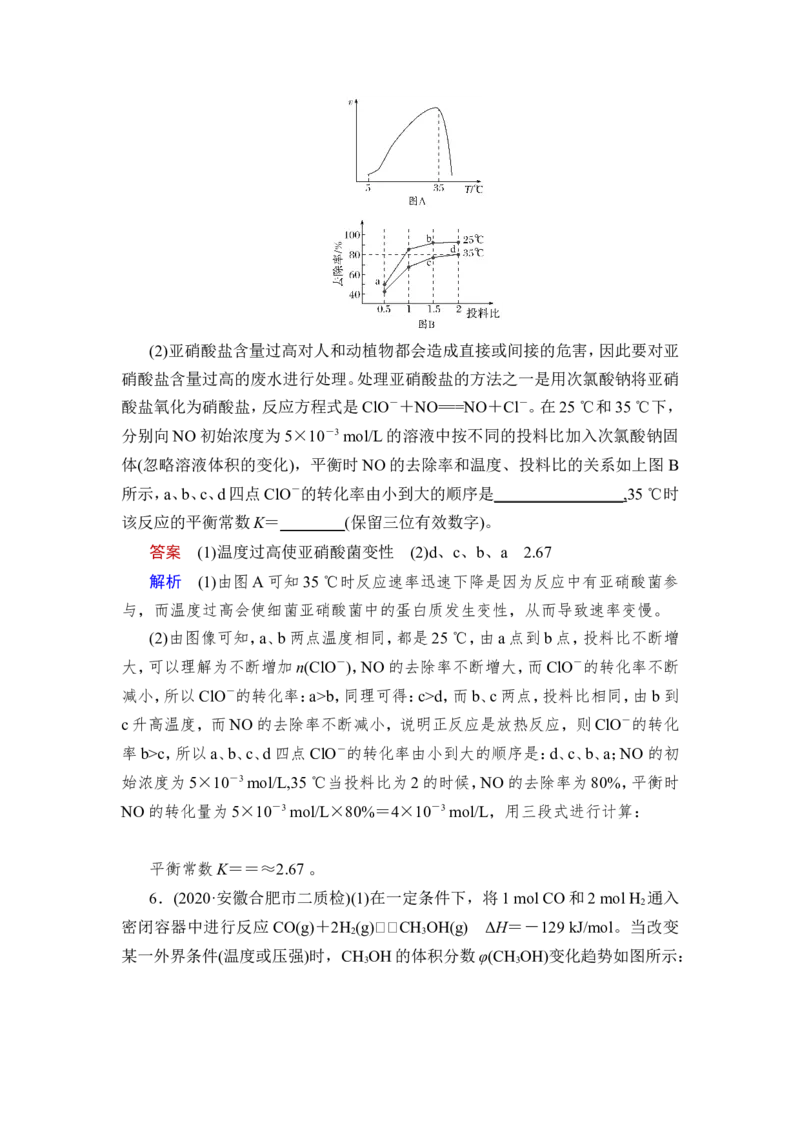
5.(2020·河南六市联合一调)(1)NH 硝化过程的离子方程式是 2NH+
3O 2HNO +2H O+2H+,恒温时在亚硝酸菌的作用下发生该反应,实验测得
2 3 2
在其它条件一定时,NH硝化反应的速率随温度变化曲线如下图A所示,温度高
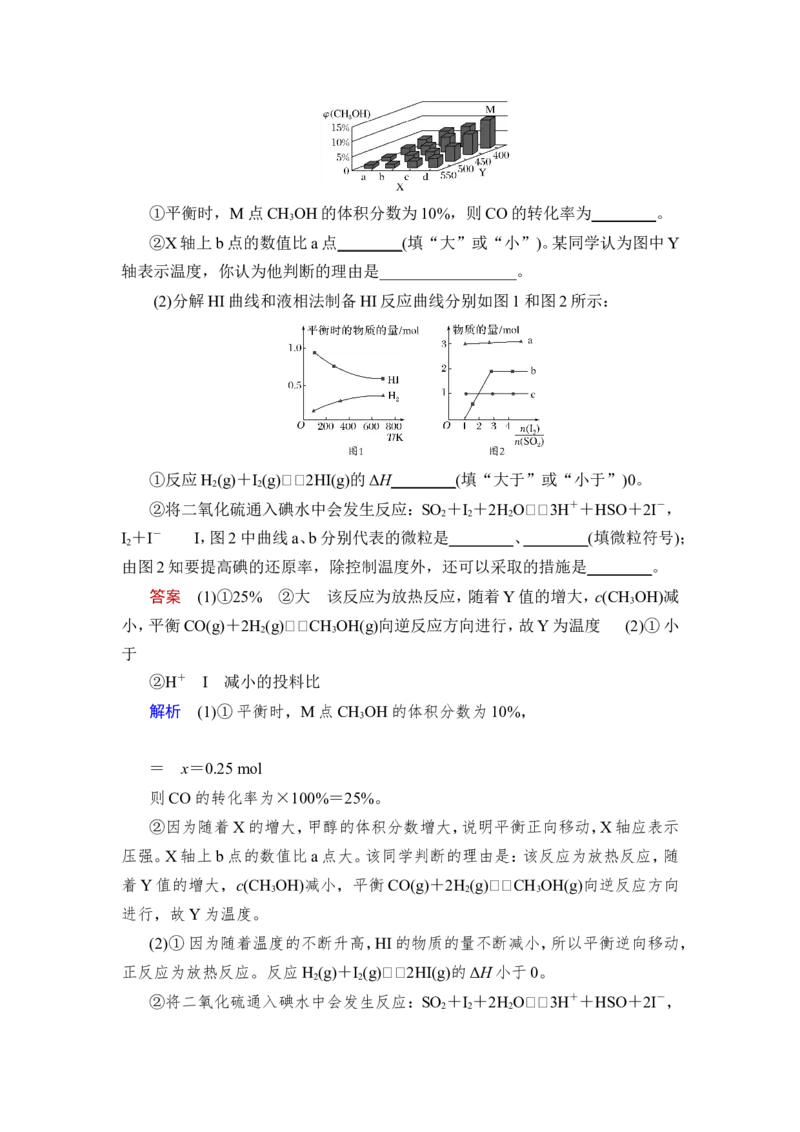
于35 ℃时反应速率迅速下降的原因可能是 __________________________。(2)亚硝酸盐含量过高对人和动植物都会造成直接或间接的危害,因此要对亚
硝酸盐含量过高的废水进行处理。处理亚硝酸盐的方法之一是用次氯酸钠将亚硝
酸盐氧化为硝酸盐,反应方程式是ClO-+NO===NO+Cl-。在25 ℃和35 ℃下,
分别向NO初始浓度为5×10-3 mol/L的溶液中按不同的投料比加入次氯酸钠固
体(忽略溶液体积的变化),平衡时NO的去除率和温度、投料比的关系如上图 B
所示,a、b、c、d四点ClO-的转化率由小到大的顺序是________________,35 ℃时
该反应的平衡常数K=________(保留三位有效数字)。
答案 (1)温度过高使亚硝酸菌变性 (2)d、c、b、a 2.67
解析 (1)由图A可知35 ℃时反应速率迅速下降是因为反应中有亚硝酸菌参
与,而温度过高会使细菌亚硝酸菌中的蛋白质发生变性,从而导致速率变慢。
(2)由图像可知,a、b两点温度相同,都是25 ℃,由a点到b点,投料比不断增
大,可以理解为不断增加n(ClO-),NO的去除率不断增大,而ClO-的转化率不断
减小,所以ClO-的转化率:a>b,同理可得:c>d,而b、c两点,投料比相同,由b到
c升高温度,而NO的去除率不断减小,说明正反应是放热反应,则ClO-的转化
率b>c,所以a、b、c、d四点ClO-的转化率由小到大的顺序是:d、c、b、a;NO的初
始浓度为5×10-3 mol/L,35 ℃当投料比为2的时候,NO的去除率为80%,平衡时
NO的转化量为5×10-3 mol/L×80%=4×10-3 mol/L,用三段式进行计算:
平衡常数K==≈2.67 。
6.(2020·安徽合肥市二质检)(1)在一定条件下,将1 mol CO和2 mol H 通入
2
密闭容器中进行反应 CO(g)+2H (g)CH OH(g) ΔH=-129 kJ/mol。当改变
2 3
某一外界条件(温度或压强)时,CH OH的体积分数φ(CH OH)变化趋势如图所示:
3 3①平衡时,M点CH OH的体积分数为10%,则CO的转化率为________。
3
②X轴上b点的数值比a点________(填“大”或“小”)。某同学认为图中Y
轴表示温度,你认为他判断的理由是_________________。
(2)分解HI曲线和液相法制备HI反应曲线分别如图1和图2所示:
①反应H (g)+I (g)2HI(g)的ΔH________(填“大于”或“小于”)0。
2 2
②将二氧化硫通入碘水中会发生反应:SO +I +2H O3H++HSO+2I-,
2 2 2
I +I-I,图2中曲线a、b分别代表的微粒是________、________(填微粒符号);
2
由图2知要提高碘的还原率,除控制温度外,还可以采取的措施是________。
答案 (1)①25% ②大 该反应为放热反应,随着Y值的增大,c(CH OH)减
3
小,平衡CO(g)+2H (g)CH OH(g)向逆反应方向进行,故Y为温度 (2)①小
2 3
于
②H+ I 减小的投料比
解析 (1)①平衡时,M点CH OH的体积分数为10%,
3
= x=0.25 mol
则CO的转化率为×100%=25%。
②因为随着X的增大,甲醇的体积分数增大,说明平衡正向移动,X轴应表示
压强。X轴上b点的数值比a点大。该同学判断的理由是:该反应为放热反应,随
着Y值的增大,c(CH OH)减小,平衡CO(g)+2H (g)CH OH(g)向逆反应方向
3 2 3
进行,故Y为温度。
(2)①因为随着温度的不断升高,HI的物质的量不断减小,所以平衡逆向移动,
正反应为放热反应。反应H (g)+I (g)2HI(g)的ΔH小于0。
2 2
②将二氧化硫通入碘水中会发生反应:SO +I +2H O3H++HSO+2I-,
2 2 2I +I-I;令投入的SO 为1 mol,从反应方程式可以看出,H+的物质的量是
2 2
SO 的三倍,I-的物质的量是SO 的二倍,再结合图2,即可得出图2中曲线a代
2 2
表的微粒是H+,b代表的微粒是I。由图2知要提高碘的还原率,除控制温度外,
还可以采取的措施是增大SO 的投入量,同时减少I 的投入量,即减小的投料比。
2 2