文档内容
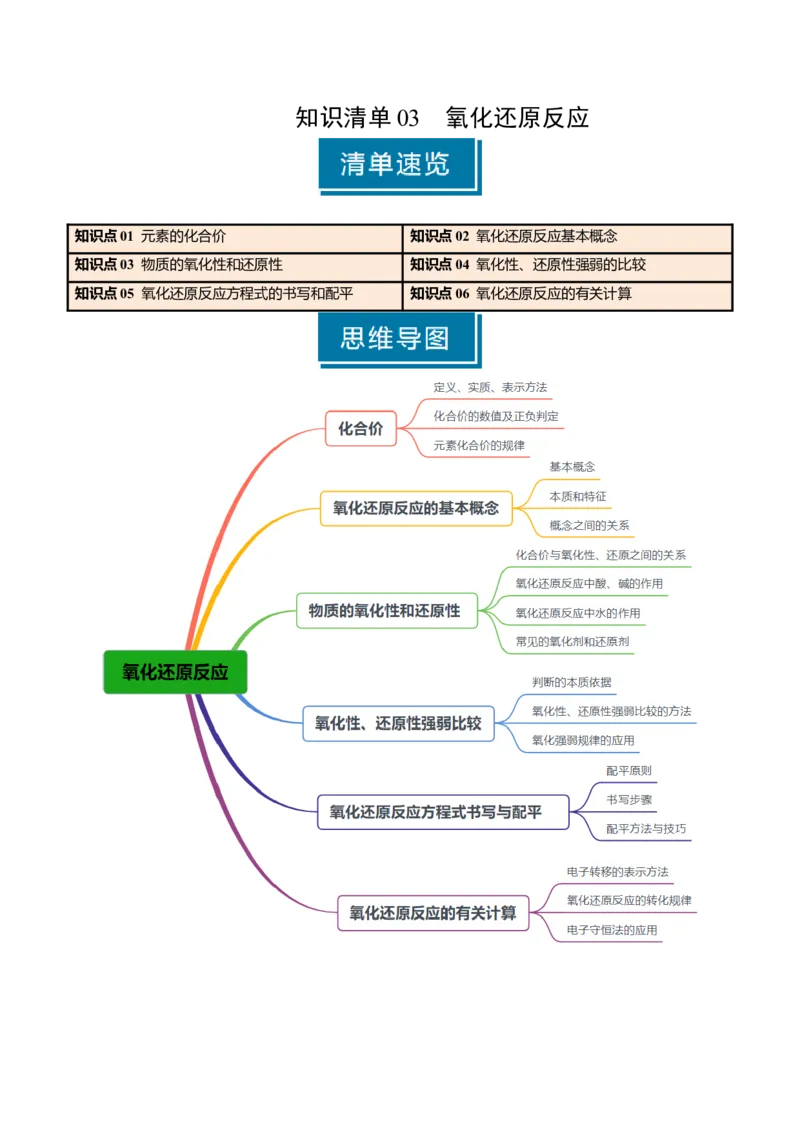
知识清单 03 氧化还原反应
知识点01 元素的化合价 知识点02 氧化还原反应基本概念
知识点03 物质的氧化性和还原性 知识点04 氧化性、还原性强弱的比较
知识点05 氧化还原反应方程式的书写和配平 知识点06 氧化还原反应的有关计算知识点 01 元素的化合价
1.化合价的定义、实质和表示方法:
(1)定义:一种元素一定数目的原子跟其他元素一定数目的原子化合的性质。
(2)实质:化合价是元素在形成化合物时表现出的化学性质;单质的化合价为零。
(3)表示方法:在元素符号或原子团的正上方用+n或-n表示
① 位置:元素符号的正上方(如 ); ② 书写顺序:先写正负,后写数值;
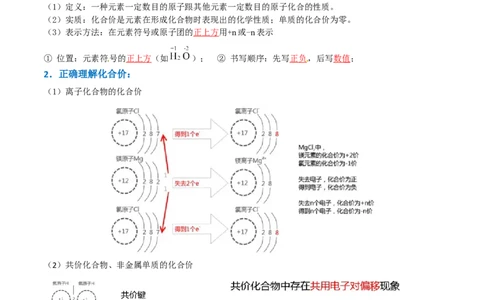
2.正确理解化合价:
(1)离子化合物的化合价
(2)共价化合物、非金属单质的化合价
3.化合价的数值及正负判定4.元素化合价的规律
(1)化合价原则:
①化合物中,正负化合价的代数和=0
②离子中,正负化合价的代数和=电荷
③在化合物里,氢通常显+1价,氧通常显-2价;
④金属元素通常显正价,非金属元素通常显负价,但在非金属氧化物里,氧显负价,另一
非金属元素显正价;
⑤单质中元素的化合价规定为零;
⑥许多元素具有可变化合价,如:硫、碳等;
⑦“根”的化合价一定不为零。
(2)常用等量关系
①主族元素最高正价=主族序数=原子的最外层电子数
②主族元素的最高正价+|最低负价|=8 或2
③最高正化合价与其最低负化合价代数和
a.等于0的短周期元素:H、C、Si b.等于2的短周期元素:N、P
c.等于4的短周期元素:S d.等于6的短周期元素:Cl
(3)化合价的范围:+1≤最高价≤+7, - 4≤最低价≤ - 1
5.化合价的特殊点
(1)F 元素没有正化合价,金属元素没有负化合价
(2)O 元素有正化合价,但是没有其所在族的最高正化合价
(3)硼元素只有+3 价
(4)氢元素的化合价
①金属氢化物中,氢显 - 1 价,如NaH、NaAlH 、
4
②非金属氢化物中,氢一般显+1 价,如NH 、CH 、B H
3 4 2 6
(5)氧元素的化合价
①普通的含氧微粒中,氧显 - 2 价
②含O 2―或―O―O―的微粒中,氧显 - 1 价
2③在S O 2―( )中,过氧键中的两个O显 - 1 价 ,其余的O显 - 2 价。
2 8
④在CrO 中,两个过氧键中的4个O显 - 1 价 ,其余的O显 - 2 价。
5
6.简单阴离子或气态氢化物中,非金属元素显最低负价
易错点:某些微粒中元素的化合价
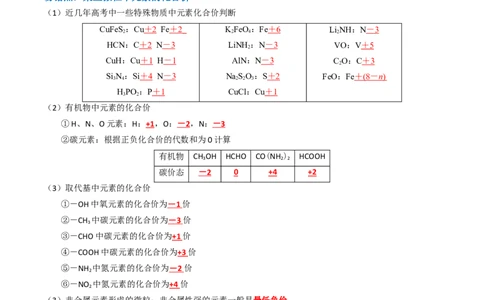
(1)近几年高考中一些特殊物质中元素化合价判断
CuFeS:Cu + 2 Fe + 2 KFeO:Fe + 6 LiNH:N - 3
2 2 4 2
HCN:C + 2 N - 3 LiNH:N - 3 VO:V + 5
2
CuH:Cu + 1 H - 1 AlN:N - 3 C O:C + 3
2
Si N:Si + 4 N - 3 NaSO:S + 2 FeO:Fe + ( 8 - n )
3 4 2 2 3
HPO :P + 1 CuCl:Cu + 1
3 2
(2)有机物中元素的化合价
①H、N、O元素:H:+1,O: - 2,N: - 3
②碳元素:根据正负化合价的代数和为0计算
有机物 CH OH HCHO CO(NH ) HCOOH
3 2 2
碳价态 - 2 0 +4 +2
(3)取代基中元素的化合价
①-OH中氧元素的化合价为 ― 1 价
②-CH 中碳元素的化合价为 ― 3 价
3
③-CHO中碳元素的化合价为+1 价
④-COOH中碳元素的化合价为+3 价
⑤-NH 中氮元素的化合价为 ― 2 价
2
⑥-NO 中氮元素的化合价为+4 价
2
(3)非金属元素形成的微粒:非金属性强的元素一般显最低负价
①CN-原子团显 - 1 价,其中C显+2 价,N显 - 3 价
②HNCO中,氢显+1 价,C显+4 价,N显 - 3 价,O显 - 2 价
③HFO中,H显+1 价,F显 - 1 价,O显0 价
④BrI中I元素显+1 价,SiC中C元素显 - 4 价
(4)含CO、NH 、H O等分子的物质:
3 2
①Fe(CO) 中Fe显0 价
5
②Cu(NH ) SO 中Cu显+2 价
3 4 4(5)某些含铁、铜的硫化物
物
FeS CuFeS
2 2
质
价 S Fe Cu Fe S
态 - 1 +2 +2 +2 - 2
(6)无法判断价态的物质
物
AlFe Fe P Fe C
2 3 3
质
价 Al Fe Fe P Fe C
态 0 0 0 0 0 0
1.已知G、Q、X、Y、Z均为含氯元素的化合物,在一定条件下有下列转化关系(未配平):
①G―→Q+NaCl ②Q+HO――→X+H ③Y+NaOH―→G+Q+HO ④Z+NaOH―→Q+X
2 2 2
+HO
2
这五种化合物中Cl元素化合价由低到高的顺序是( A )
A.G、Y、Q、Z、X B.X、Z、Q、G、Y
C.X、Z、Q、Y、G D.G、Q、Y、Z、X
【解析】 由①得出Q中价态高于G,因为G中价态介于Q和-1价的Cl之间,-1价为氯元素的最
低价;将该结论引用到③,Y介于Q与G之间,故有Q价态高于Y,Y价态高于G;分析②:HO中的H
2
化合价降低,则Q中的氯元素转变为X中的氯元素,化合价必升高,则得出X价态高于Q;最后分析④:
Z介于Q、X之间,则X价态高于Z,Z价态高于Q。
2.已知X、Y、Z、W、Q均为含氮化合物,它们在一定条件下有如下转换关系(未配平):
①X―→W+O
2
②Z+Y+NaOH―→HO+W
2
③Y+SO ―→Z+SO
2 3
④Q+Y―→Z+HO
2
⑤X+Cu+HSO (浓)―→Cu2++Y+SO
2 4
则这五种含氮化合物中氮元素的化合价由高到低的顺序为( C )
A.X>Y>Z>W>Q B.X>Z>Y>Q>W
C.X>Y>W>Z>Q D.W>X>Z>Q>Y
【解析】 ①X―→W+O 中,X中氧元素失电子化合价升高,则氮元素得电子化合价降低,所以氮
2
元素化合价X>W;③Y+SO ―→Z+SO 中,硫元素化合价升高,则Y中氮元素化合价Y>Z;②Z+Y+
2 3
NaOH―→HO+W为归中反应,则氮元素化合价W处于Z和Y中间,结合反应③可知,氮元素化合价
2
Y>W>Z;④Q+Y―→Z+HO为归中反应,Z处于Q和Y之间,根据③知,Y>Z,所以Z>Q;⑤X+Cu
2
+HSO (浓)―→Cu2++Y+SO,铜元素化合价升高,则X化合价降低生成Y,所以氮元素化合价,X>Y;
2 4
所以这五种含氮化合物中氮元素的化合价由高到低的顺序为X>Y>W>Z>Q。知识点 02 氧化还原反应的概念
1.氧化还原反应
反应前后元素的化合价是否发生了变化
特征 氧化还原反应 反应前后元素的化合价变化
非氧化还原反应 反应前后元素的化合价不变
氧
本质 反应过程中有电子的转移,包括电子的得失或偏移
化
还
置换反应一定是氧化还原反应
原
反 和四种基本 复分解反应一定不是氧化还原反
应
反应类型的 应
关系 有单质参加的化合反应是氧化还原反应;
有单质生成的分解反应是氧化还原反应
2.氧化还原反应基本概念
含“氧”概念 含“还”概念
氧化 氧化 还原 还原
氧化剂 被氧化 氧化性 还原剂 被还原 还原性
反应 产物 反应 产物
得到电 失去电
化合价 化合价 化合价 化合价
子,化 化合价 化合价 子,化 化合价 化合价
升高得 降低过 降低得 升高过
合价降 升高的 升高的 合价升 降低的 降低的
到的生 程表现 到的生 程表现
低的反 反应 过程 高的反 反应 过程
成物 的性质 成物 的性质
应物 应物
3.氧化还原反应概念之间的关系
1.在氧化还原反应中,非金属单质不一定是氧化剂( √ )
2.某元素从游离态变为化合态,则该元素一定被还原( × )
3.有单质参加或生成的化学反应不一定是氧化还原反应( √ )
4.氧化还原反应中的反应物不是氧化剂就是还原剂( × )
5.氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原( × )
一、单质与氧化还原反应的关系(1)有单质参加或生成的反应不一定是氧化还原反应,如3O = 2O 。
2 3
(2)没有单质参加的化合反应也可能是是氧化还原反应,如HO+SO = H SO 。
2 2 2 2 4
二、对氧化还原反应概念的理解
(1)氧化反应和还原反应存在于在同一个反应中,它们同时发生、同时存在,是相互对立统一的。
(2)氧化剂和还原剂可以是不同的物质,也可以是同种物质
①2KMnO KMnO +MnO+O ↑,氧化剂是KMnO ,还原剂是KMnO
4 2 4 2 2 4 4
②2F+2H O O+4HF,氧化剂是F,还原剂是HO
2 2 2 2 2
(3)氧化产物和还原产物可以是不同的物质,也可以是同种物质
①3S+6NaOH NaSO +2Na S+3HO,氧化产物是Na SO ,还原产物是Na S
2 3 2 2 2 3 2
②NO+NO +2NaOH 2NaNO +H O,氧化产物是NaNO ,还原产物是NaNO
2 2 2 2 2
(4)被氧化的元素和被还原的元素可以是不同的元素,也可以是同种元素
①4HCl(浓)+MnO MnCl +Cl↑+2H O,被氧化的元素是Cl,被还原的元素是Mn
2 2 2 2
②2HS+SO 2HO+3S,被氧化的元素是S,被还原的元素是S
2 2 2
(5)可能有多种元素同时被氧化或被还原
①3Cu S+22HNO 6Cu(NO ) +10NO↑+3HSO +8H O,被氧化的元素是Cu 和S,被还原的元
2 3 3 2 2 4 2
素是N
②2KNO+S+3C KS+N↑+3CO ↑,被氧化的元素是C,被还原的元素是N 和S
3 2 2 2
(6)方程式中的系数与实际参加反应的氧化剂或还原剂的量不一定一致
①C+2H SO CO↑+2SO↑+2H O,n(氧化剂)∶n(还原剂)=2∶1
2 4 2 2 2
②Cu+2H SO CuSO +SO↑+2H O,n(氧化剂)∶n(还原剂)=1∶1
2 4 4 2 2
知识点 03 物质的氧化性和还原性
1.化合价和氧化性、还原性的关系
(1) 最高价态——只有 氧化性 ,如Fe3+、HSO 、KMnO 等;
2 4 4
最低价态——只有 还原性 ,如金属单质、Cl-、S2-等;
中间价态——既有 氧化性 又有 还原性 ,如Fe2+、S、Cl 等。
2
(2)常见元素的最高价态和最低价态
元素 Cl S N C H
最高价 +7 +6 +5 +4 +1
最低价 - 1 - 2 - 3 - 4 - 1
2.氧化还原反应中酸或碱的作用
(1)氧化性:所含元素的化合价降低
(2)还原性:所含元素的化合价升高(3)酸或碱性:所含元素的化合价不变,有相应的盐生成
(4)具体反应分析
①Zn+2HCl ZnCl +H ↑,盐酸表现酸性和氧化性
2 2
②CuO+2HCl CuCl +H O,盐酸表现酸性
2 2
③MnO +4HCl(浓) MnCl +Cl ↑+2H O,盐酸表现酸性和还原性
2 2 2 2
④2HCl H ↑+Cl ↑,盐酸表现氧化性和还原性
2 2
⑤3Cl +8NH N +6NH Cl,NH 表现碱性和还原性
2 3 2 4 3
⑥Cu O+6HNO (浓) 2Cu(NO ) +2NO ↑+3H O,硝酸表现酸性和氧化性
2 3 3 2 2 2
△
⑦C+2H SO (浓) CO ↑+2SO ↑+2H O,浓硫酸只表现为氧化性。
2 4 2 2 2
3.氧化还原反应中水的作用
(1)氧化性:有H 产生
2
(2)还原性:有O 产生
2
(3)氧化性和还原性:同时有H 和 O 产生
2 2
(4)具体反应分析
①2F +2H O 4HF+O ,水表现还原性
2 2 2
②3Fe+4H O Fe O +4H ,水表现氧化性
2 3 4 2
③2Na+2H O 2NaOH+H ↑,水表现氧化性
2 2
④2H O O ↑+2H ↑,水表现还原性和氧化性
2 2 2
⑤2Na O +2H O 4NaOH+O ↑,水既不表现氧化性又不表现还原性
2 2 2 2
⑥Cl +H O HCl+HClO,水既不表现氧化性又不表现还原性
2 2
⑦3NO +H O 2HNO +NO,水既不表现氧化性又不表现还原性
2 2 3
4.常见的氧化剂和还原剂
(1)常见的氧化剂及产物预测
氧化剂 还原产物
Mn2+(酸性);MnO (中性);MnO 2-(碱
2 4
KMnO
4
性)
K Cr O (酸性) Cr 3+
2 2 7
浓硝酸 NO
2
稀硝酸 NO
X (卤素单质) X -
2
H O OH-(碱性);H O(酸性)
2 2 2
Na O NaOH(或Na CO 等)
2 2 2 3
NaClO(或ClO
C l - 、 C l
2
-)NaClO Cl 、ClO 等
3 2 2
PbO Pb2+
2
(2)常见的还原剂及产物预测
还原剂 氧化产物
Fe2+ Fe3+(酸性);Fe(OH) (碱性)
3
SO (或H SO 、SO 2-) SO 2-
2 2 3 3 4
S2-(或H S) S、SO (或SO 2-)、SO 2-
2 2 3 4
H C O CO (酸性);CO 2-(碱性)
2 2 4 2 3
H O O
2 2 2
I-(或HI) I 、 IO -
2 3
CO CO (酸性);CO 2-(碱性)
2 3
Zn2+、Fe2+(与强氧化剂反应生成Fe3+)
金属单质(Zn、Fe、Cu等)
Cu2+(与弱氧化剂反应生成Cu+)
易错点1:微粒具有性质判断的“易错点”
(1)金属单质处于最低价,只有还原性
(2)非金属单质处于中间价态,既有氧化性又有还原性,F 除外
2
(3)金属阳离子是高价,一定具有氧化性;但是亚铁离子具有氧化性,又有还原性。
(4)从理论上讲任何一种化合物既有氧化性又有还原性
易错点2:氧化性还原性的判断
(1)某元素由化合态变为游离态时,该元素一定被还原
某元素由化合态变为游离态时,该元素可能被还原,也可能被氧化。因为元素处于化合态时,其化合价可
能为正,也可能为负。若元素由负价变为0价,则其被氧化,若元素由正价变为0价,则其被还原。
(2)在氧化还原反应中,非金属单质一定只作氧化剂
在氧化还原反应中,非金属单质不一定只作氧化剂,大部分非金属单质往往既具有氧化性又具有还原性,
只是以氧化性为主。如在反应Cl+HO=HCl+HClO中,Cl 既表现氧化性又表现还原性。
2 2 2
(3)在氧化还原反应中,若有一种元素被氧化,则一定有另一种元素被还原
在氧化还原反应中,一种元素被氧化,不一定有另一种元素被还原,有许多反应是一种元素既被氧化又被
还原。如在反应2NaO+2HO===4NaOH+O↑中,NaO 中氧元素的化合价既升高又降低。
2 2 2 2 2 2
易错点3:有关氧化性、还原性的易错点
1.具有氧化性的物质不一定是氧化剂,具有还原性的物质不一定是还原剂,应视具体反应而定。
2.对同一元素而言,一般价态越高,氧化性越强,如Fe3+>Fe2+>Fe;价态越低,氧化性越弱,如S2-
KMnO >H O>I 。
3 4 2 2 2
知识点 05 氧化还原反应方程式的书写和配平
1.配平原则
2.化合价升降法配平步骤
3.信息型氧化还原方程式书写流程4.氧化还原反应方程式的配平方法
(1)正向配平法:氧化剂、还原剂中某元素化合价全部变化,一般从反应物着手配平。
(2)逆向配平法:自身氧化还原反应(包括分解、歧化)一般从生成物着手配平。
(3)缺项配平法:化学方程式所缺物质往往是酸、碱或水;如果是离子方程式,所缺物质往往是H+、OH-或水。
可以根据质量守恒先写出所缺物质,再根据化合价升降守恒配平。如果无法确定所缺项,可先依据化合价的
升降守恒将现有的某些物质配平,然后再根据质量守恒确定所缺物质的化学式及其化学计量数(系数)。
(4)缺项型氧化还原反应方程式的补项原则和组合方式
补项原则
介质 多一个氧原子 少一个氧原子
酸性 +2H+结合1个O→H O +HO提供1个O→2H+
2 2
中性 +HO结合1个O→2OH- +HO提供1个O→2H+
2 2
碱性 +HO结合1个O→2OH- +2OH-提供1个O→H O
2 2
组合方式
反应物 生成物 使用条件
组合一 H+ HO 酸性溶液
2
组合二 HO H+ 酸性或中性溶液
2
组合三 OH- HO 碱性溶液
2
组合四 HO OH- 碱性或中性溶液
2
举例说明
例:高锰酸根与亚硫酸根的反应:
①酸性条件:2MnO+5SO+6H+===2Mn2++5SO+3HO
2
②中性条件:2MnO+3SO+HO===2MnO↓+3SO+2OH-
2 2
③碱性条件:2MnO+SO+2OH-===2MnO+SO+HO
2
易错点:常见氧化还原反应类型及其配平技巧
1.完全氧化还原型技巧:可从反应物或者生成物进行配平
关键:符合一般的配平步骤
实例:1C+2HSO(浓)――→CO↑+SO↑+HO
2 4 2 2 2
↑4×1↓2×2
或C+HS O(浓)――→1CO↑+2SO↑+HO
2 4 2 2 2
↑4×1↓2×2
C+2HSO (浓)=====CO↑+2SO ↑+2HO
2 4 2 2 2
2.歧化反应
技巧:从生成物进行配平
关键:确定氧化产物和还原产物的化学计量数
实例:NO+HO―→2HN O+1NO
2 2 3
↑1×2↓2×1
3NO +HO===2HNO +NO
2 2 3
3.部分氧化还原型
技巧:从生成物进行配平
关键:确定氧化产物和还原产物的化学计量数
实例:MnO+HCl(浓)――→1MnCl+1Cl+HO
2 2 2 2
↓2×1 ↑1×2×1
MnO +4HCl(浓)=====MnCl +Cl↑+2HO
2 2 2 2
4.归中反应
技巧:从反应物进行配平
关键:确定氧化剂和还原剂的化学计量数
实例:1S O+2HS ―→HO+S
2 2 2
↓4×1 ↑2×2
SO +2HS===2H O+3S↓
2 2 2
1.请配平下列氧化还原反应方程式:
(1)===
(2)P+CuSO +HO===Cu P+
4 4 2 3
(3)===
(4) 5 Mn2++ 2 ClO+ 4 HO=== 5 MnO ↓+ 1 Cl↑+ 8
2 2 2
(5) 3 ClO-+ 2 Fe(OH) + 4 === 3 Cl-+ 2 FeO+ 5 HO
3 2
【解析】根据元素化合价升降法和相应的配平技巧进行配平:
(1)Na→NaSiO ,生成1份NaSiO 升高1×2价,H→NaBH ,生成1份NaBH 降低1×4价,根据化合
2 3 2 3 2 4 4
价升降总数相等,在NaSiO 前添加系数2,在NaBH 前添加系数1,再根据原子守恒配平其他物质的系数。
2 3 4
(2)由于Cu P中存在多个变价元素,符合整体归一法配平,因此把 Cu P当作一个整体来分析,P +
3 3 4CuSO →CuP,生成1份Cu P降低1×3+3=6价,P→HPO ,升高5价,根据化合价升降总数相等,在
4 3 3 4 3 4
HPO 前添加系数6,在Cu P前添加系数5,再根据原子守恒配平其他物质的系数。可知P 的系数为,再
3 4 3 4
将所有的系数乘以4即可。
(3)MnO(OH) →Mn2+,降低2价,I-→I2,升高1价,根据化合价升降总数相等,在I-前添加系数2,
2
在I 前添加系数1,在MnO(OH) 和Mn2+前添加系数1,再根据电荷守恒和原子守恒配平H+和HO的系数
2 2 2
为4和3。
(4)Mn2+→MnO ,升高2价,ClO→Cl ,降低5价,根据化合价升降总数相等,在Mn2+前添加系数5,
2 2
在ClO前添加系数2,对比左右两边电荷可知,右边缺少8H+,再根据原子守恒配平HO的系数为4。
2
(5)Fe (OH) →FeO,升高3价,ClO-→Cl-,降低2价,根据化合价升降总数相等,在Fe(OH) 前添加
3 3
系数2,在ClO-前添加系数3,对比左右两边电荷可知,左边缺少4OH-,再根据原子守恒配平HO的系
2
数为5。
知识点 06 氧化还原反应的有关计算
1.氧化还原反应中电子转移的表示方法
(1)双线桥法:标变价→画箭头→标得失→定数目
①模型
②示例:C与浓硫酸反应
(2)单线桥法:箭头由失电子原子指向得电子原子,线桥上只标电子转移的数目,不标“得到”“失
去”
①模型
②示例:Cu与浓硝酸反应2.转移电子数的计算
(1)N(e-)= 氧化 剂得到电子的数目 =还原剂失去电子的数目
(2)反应中转移电子的物质的量与各物质的化学计量数成正比
(3)计算公式
①n(e-)= n (氧化剂) × N (变价原子数) ×Δ N (化合价变化数)
②n(e-)= n (还原剂) ×N (变价原子数) ×ΔN (化合价变化数)
3.氧化还原反应中转化规律
(1)5NH NO 2HNO +4N ↑+9H O
4 3 3 2 2
(2)2KClO +6HCl(浓) KCl+3Cl ↑+3H O
3 2 2
(3)H S+H SO (浓) S↓+SO ↑+2H O
2 2 4 2 2
4.电子守恒规律
(1)规律:氧化还原反应中得电子总数与失电子总数相等,表现为元素化合价降低总数与升高总数相
等。
(2)应用:运用电子守恒进行氧化还原反应的相关计算。
5.“电子守恒法”计算的一般思维模板1.现有24 mL浓度为0.05 mol·L-1的NaSO 溶液恰好与20 mL浓度为0.02 mol·L-1的KCr O 溶液完全反
2 3 2 2 7
应。已知NaSO 可被KCr O 氧化为NaSO ,则元素Cr在还原产物中的化合价为________。
2 3 2 2 7 2 4
【答案】 +3
【解析】 题目中指出被还原的元素是Cr,则得电子的物质是KCr O ,失电子的物质是NaSO ,其中S
2 2 7 2 3
元素的化合价从+4→+6,Cr元素的化合价将从+6→+n。根据氧化还原反应中得失电子守恒规律,有
0.05 mol·L-1×0.024 L×(6-4)=0.02 mol·L-1×0.020 L×2×(6-n),解得n=3。
2.足量铜与一定量浓硝酸反应,得到硝酸铜溶液和 NO 、NO 、NO的混合气体,将这些气体与1.68 L
2 2 4
O(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol·L-1
2
NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是________mL。
【答案】 60
【解析】 由题意可知,HNO,则Cu失去的电子数与O 得到的电子数相等。即n(Cu)=2n(O )=
3 2 2
2×=0.15 mol。根据质量守恒及NaOH和Cu(NO ) 的反应可得关系式:n(NaOH)=2n[Cu(NO )]=2n(Cu)=
3 2 3 2
0.3 mol,则V(NaOH)==0.06 L=60 mL。