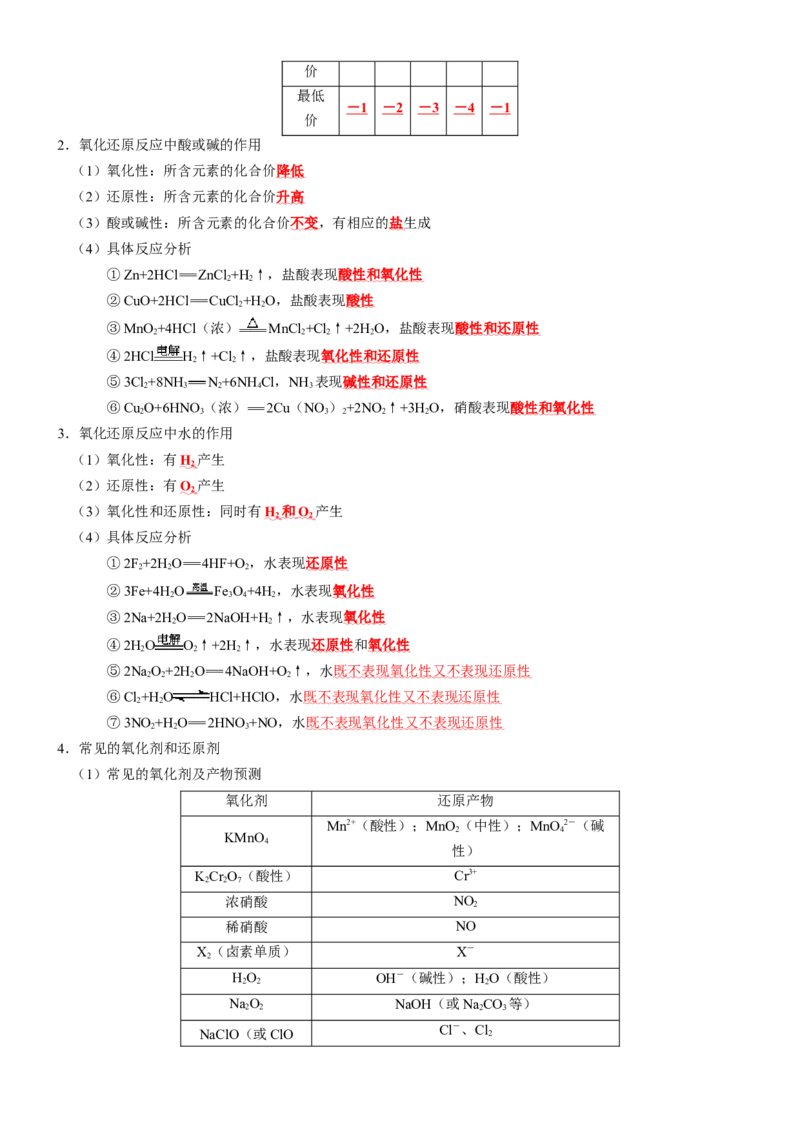文档内容
知识清单 04 氧化还原反应
知识点01元素的化合价 知识点02氧化还原反应基本概念
知识点03物质的氧化性和还原性 知识点04氧化性、还原性强弱的比较
知识点05氧化还原反应方程式的书写和配平 知识点06氧化还原反应的有关计算
知识点 01 元素的化合价
1.化合价规则
(1)化合物中,正负化合价的代数和=0
(2)离子中,正负化合价的代数和=电荷
2.常用等量关系
(1)主族元素最高正价=主族序数=原子的最外层电子数
(2)主族元素的最高正价+|最低负价|=8 或2
(3)最高正化合价与其最低负化合价代数和
①等于0的短周期元素:H、C、Si
②等于2的短周期元素:N、P
③等于4的短周期元素:S
④等于6的短周期元素:Cl
3.化合价的范围:+1≤最高价≤+7, - 4≤最低价≤ - 1
4.化合价的特殊点
(1)F 元素没有正化合价,金属元素没有负化合价
(2)O 元素有正化合价,但是没有其所在族的最高正化合价
(3)硼元素只有+3 价
(4)氢元素的化合价
①金属氢化物中,氢显 - 1 价,如NaH、NaAlH、B H
4 2 6②非金属氢化物中,氢一般显+1 价,如NH 、CH
3 4
(5)氧元素的化合价
①普通的含氧微粒中,氧显 - 2 价
②含O2―或―O―O―的微粒中,氧显 - 1 价
2
③在SO2―中,氧元素显 - 1 和 - 2 价
2 8
④在CrO 中,铬元素显 - 1 和- 2 价
5
5.简单阴离子或气态氢化物中,非金属元素显最低负价
易错点:某些微粒中元素的化合价
(1)有机物中元素的化合价
①H、N、O元素:H:+1,O: - 2,N: - 3
②碳元素:根据正负化合价的代数和为0计算
有机物 CHOH HCHO CO(NH ) HCOOH
3 2 2
碳价态 - 2 0 +4 +2
(2)取代基中元素的化合价
①-OH中氧元素的化合价为 ― 1 价
②-CH 中碳元素的化合价为 ― 3 价
3
③-CHO中碳元素的化合价为+1 价
④-COOH中碳元素的化合价为+3 价
⑤-NH 中氮元素的化合价为 ― 2 价
2
⑥-NO 中氮元素的化合价为+4 价
2
(3)非金属元素形成的微粒:非金属性强的元素一般显最低负价
①CN原子团显 - 1 价,其中C显+2 价,N显 - 3 价
②HNCO中,氢显+1 价,C显+4 价,N显 - 3 价,O显 - 2 价
③HFO中,H显+1 价,F显 - 1 价,O显0 价
④BrI中I元素显+1 价,SiC中C元素显 - 4 价
(4)含CO、NH 、HO等分子的物质:
3 2
①Fe(CO) 中Fe显0 价
5
②Cu(NH )SO 中Cu显+2 价
3 4 4
(5)某些含铁、铜的硫化物
物
FeS CuFeS
2 2
质
价 S Fe Cu Fe S
态 - 1 +2 +2 +2 - 2
(6)无法判断价态的物质
物 AlFe Fe P Fe C
2 3 3质
价 Al Fe Fe P Fe C
态 0 0 0 0 0 0
【典例01】制备氰氨基化钙的化学方程式为CaCO +2HCN CaCN +CO↑+H ↑+CO ↑,在反应中( )。
3 2 2 2
A.氢元素被氧化,碳元素被还原
B.HCN是氧化剂,CaCO 是还原剂
3
C.CaCN 是氧化产物,H 是还原产物
2 2
D.CO为氧化产物,H 为还原产物
2
【解析】选C。从反应物CaCO 到生成物CO,碳的化合价均为+4价,没有改变,再从生成物H 分析发现氢的
3 2 2
化合价降低,显然HCN中氢得电子,HCN是氧化剂,而CaCO 中的各元素均无化合价变化,而还原剂也必是
3
HCN,其中的碳元素也一定被氧化,在HCN中碳为+2价,CO中的碳也为+2价,则CaCN 中碳为+4价,故
2
CaCN 为氧化产物。
2
【典例02】(2022·榆林一模)一种科学、简便的检测司机是否酒后驾车的方法是使驾车人呼出的气体接触载有
硫酸酸化处理过的三氧化铬(CrO)的硅胶。如果呼出的气体中有乙醇蒸气,乙醇就会被氧化成乙醛,同时三
3
氧化铬被还原为硫酸铬[Cr (SO )],下列说法不正确的是( )。
2 4 3
A.CrO 和Cr (SO ) 的颜色不同
3 2 4 3
B.CrO 中铬元素的化合价为+6
3
C.生成1mol的Cr (SO ) 时,发生转移的电子为6mol
2 4 3
D.CrO 与稀硫酸反应生成Cr (SO ) 和水
3 2 4 3
【解析】选D。CrO 与Cr (SO ) 的颜色不同,利用上述反应可以通过颜色的变化判断驾车人是否饮酒,故A
3 2 4 3
正确;由化合物中正负化合价代数和可知,CrO 中氧元素为-2价,则铬元素的化合价为+6,故B正确;CrO
3 3
铬元素为+6价,产物Cr (SO ) 中铬元素化合价为+3价,所以生成1mol的Cr (SO ) 时,发生转移的电子
2 4 3 2 4 3
为6mol,故C正确;CrO 与乙醇发生氧化还原反应,生成Cr3+,稀硫酸只是提供酸性环境,故D错误。
3
知识点 02 氧化还原反应的概念
1.特征:反应前后元素的化合价是否发生了变化
(1)氧化还原反应:反应前后元素的化合价变化
(2)非氧化还原反应:反应前后元素的化合价不变
2.本质:反应过程中有电子的转移,包括电子的得失或偏移
3.氧化还原反应和四种基本反应类型的关系
(1)置换反应一定是氧化还原反应;(2)复分解反应一定不是氧化还原反应;
(3)有单质参加的化合反应是氧化还原反应;
(4)有单质生成的分解反应是氧化还原反应。
4.含“氧”概念
(1)氧化剂:得到电子,化合价降低的反应物
(2)氧化反应:化合价升高的反应
(3)氧化产物:化合价升高得到的生成物
(4)被氧化:化合价升高的过程
(5)氧化性:化合价降低过程表现的性质
5.含“还”概念
(1)还原剂:失去电子,化合价升高的反应物
(2)还原反应:化合价降低的反应
(3)还原产物:化合价降低得到的生成物
(4)被还原:化合价降低的过程
(5)还原性:化合价升高过程表现的性质
6.氧化还原反应概念之间的关系
易错点1:单质与氧化还原反应的关系
(1)有单质参加或生成的反应不一定是氧化还原反应,如3O=2O。
2 3
(2)没有单质参加的化合反应也可能是是氧化还原反应,如HO+SO=HSO 。
2 2 2 2 4
易错点2:氧化还原反应概念的“易错点”
(1)氧化反应和还原反应存在于在同一个反应中,它们同时发生、同时存在,是相互对立统一的。
(2)氧化剂和还原剂可以是不同的物质,也可以是同种物质
①2KMnO KMnO +MnO+O ↑,氧化剂是KMnO ,还原剂是KMnO
4 2 4 2 2 4 4
②2F+2H O O+4HF,氧化剂是F,还原剂是HO
2 2 2 2 2
(3)氧化产物和还原产物可以是不同的物质,也可以是同种物质
①3S+6NaOH NaSO +2NaS+3HO,氧化产物是Na SO ,还原产物是Na S
2 3 2 2 2 3 2
②NO+NO +2NaOH 2NaNO +H O,氧化产物是NaNO ,还原产物是NaNO
2 2 2 2 2
(4)被氧化的元素和被还原的元素可以是不同的元素,也可以是同种元素
①4HCl(浓)+MnO MnCl +Cl↑+2H O,被氧化的元素是Cl,被还原的元素是Mn
2 2 2 2
②2HS+SO 2HO+3S,被氧化的元素是S,被还原的元素是S
2 2 2
(5)可能有多种元素同时被氧化或被还原①3Cu S+22HNO 6Cu(NO ) +10NO↑+3H SO +8H O,被氧化的元素是Cu 和S,被还原的元素是
2 3 3 2 2 4 2
N
②2KNO+S+3C KS+N↑+3CO ↑,被氧化的元素是C,被还原的元素是N 和S
3 2 2 2
(6)方程式中的系数与实际参加反应的氧化剂或还原剂的量不一定一致
①C+2H SO CO↑+2SO↑+2H O,n(氧化剂)∶n(还原剂)= 2 ∶ 1
2 4 2 2 2
②Cu+2H SO CuSO +SO↑+2H O,n(氧化剂)∶n(还原剂)=1 ∶ 1
2 4 4 2 2
【典例03】下列叙述正确的是( )。
A.在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原
B.没有单质参加的反应一定不是氧化还原反应
C.置换反应一定是氧化还原反应
D.失电子难的原子,容易获得电子
【解析】选C。氧化还原反应有时可以发生在同一种物质的同种元素之间,如Cl+H O=HCl+HClO,这种反应
2 2
叫做歧化反应,也可以发生在不同物质的同种元素之间,如 2HS+SO =3S↓+2H O,这种反应叫归中反应,所
2 2 2
以A不正确。化合物之间也可以发生氧化还原反应,如NO +SO =NO+SO ,所以B的叙述是错误的。是不是
2 2 3
氧化还原反应可根据化合价升降与否进行判断。置换反应可写为单质+化合物→新单质+新化合物,元素的化合
价一定有升高和降低,电子转移发生在单质与化合物之间,所以置换反应一定是氧化还原反应,C的叙述是正
确的。D选项中失电子难的原子可能得电子也难,如稀有气体,因此D不正确。
【典例04】(2020年7月·浙江学考真题)反应MnO +4HCl(浓) MnCl +Cl↑+2H O中,氧化产物与还原
2 2 2 2
产物的物质的量之比是( )。
A.1∶2 B.1∶1 C.2∶1 D.4∶1
【解析】选B。由反应方程式可知,反应物MnO 中的Mn元素的化合价为+4价,生成物MnCl 中Mn元素的化
2 2
合价为+2价,反应物HCl中Cl元素的化合价为-1价,生成物Cl 中Cl元素的化合价为0价,故MnCl 是还原
2 2
产物,Cl 是氧化产物,由氧化还原反应中得失电子守恒可知,n(Cl)∶n(MnCl )=1∶1,B符合题意。
2 2 2
知识点 03 物质的氧化性和还原性
1.化合价和氧化性、还原性的关系
(1)相互关系
(2)常见元素的最高价态和最低价态
元素 Cl S N C H
+7 +6 +5 +4 +1
最高价
最低
- 1 - 2 - 3 - 4 - 1
价
2.氧化还原反应中酸或碱的作用
(1)氧化性:所含元素的化合价降低
(2)还原性:所含元素的化合价升高
(3)酸或碱性:所含元素的化合价不变,有相应的盐生成
(4)具体反应分析
①Zn+2HCl ZnCl+H ↑,盐酸表现酸性和氧化性
2 2
②CuO+2HCl CuCl +H O,盐酸表现酸性
2 2
③MnO +4HCl(浓) MnCl+Cl↑+2H O,盐酸表现酸性和还原性
2 2 2 2
④2HCl H↑+Cl↑,盐酸表现氧化性和还原性
2 2
⑤3Cl+8NH N+6NH Cl,NH 表现碱性和还原性
2 3 2 4 3
⑥Cu O+6HNO(浓) 2Cu(NO )+2NO ↑+3HO,硝酸表现酸性和氧化性
2 3 3 2 2 2
3.氧化还原反应中水的作用
(1)氧化性:有H 产生
2
(2)还原性:有O 产生
2
(3)氧化性和还原性:同时有H 和 O 产生
2 2
(4)具体反应分析
①2F+2H O 4HF+O ,水表现还原性
2 2 2
②3Fe+4H O Fe O+4H,水表现氧化性
2 3 4 2
③2Na+2HO 2NaOH+H ↑,水表现氧化性
2 2
④2HO O↑+2H ↑,水表现还原性和氧化性
2 2 2
⑤2NaO+2H O 4NaOH+O ↑,水既不表现氧化性又不表现还原性
2 2 2 2
⑥Cl+H O HCl+HClO,水既不表现氧化性又不表现还原性
2 2
⑦3NO +H O 2HNO+NO,水既不表现氧化性又不表现还原性
2 2 3
4.常见的氧化剂和还原剂
(1)常见的氧化剂及产物预测
氧化剂 还原产物
Mn2+(酸性);MnO (中性);MnO 2-(碱
2 4
KMnO
4
性)
KCr O(酸性) Cr3+
2 2 7
浓硝酸 NO
2
稀硝酸 NO
X(卤素单质) X-
2
HO OH-(碱性);HO(酸性)
2 2 2
NaO NaOH(或NaCO 等)
2 2 2 3
NaClO(或ClO
Cl-、Cl
2-)
NaClO Cl、ClO 等
3 2 2
PbO Pb2+
2
(2)常见的还原剂及产物预测
还原剂 氧化产物
Fe2+ Fe3+(酸性);Fe(OH)(碱性)
3
SO (或HSO 、SO 2-) SO 2-
2 2 3 3 4
S2-(或HS) S、SO (或SO 2-)、SO 2-
2 2 3 4
HC O CO(酸性);CO2-(碱性)
2 2 4 2 3
HO O
2 2 2
I-(或HI) I、IO -
2 3
CO CO(酸性);CO2-(碱性)
2 3
Zn2+、Fe2+(与强氧化剂反应生成Fe3+)
金属单质(Zn、Fe、Cu等)
Cu2+(与弱氧化剂反应生成Cu+)
易错点1:微粒具有性质判断的“易错点”
(1)金属单质处于最低价,只有还原性
(2)非金属单质处于中间价态,既有氧化性又有还原性,F 除外
2
(3)金属阳离子是高价,一定具有氧化性;但是亚铁离子具有氧化性,又有还原性。
(4)从理论上讲任何一种化合物既有氧化性又有还原性
易错点2:断变化中是否一定需加氧化剂或还原剂
(1)变价元素处于最高价:必须加入还原剂
(2)变价元素处于最低价:必须加入氧化剂
(3)变价元素处于中间价:可能发生自身的氧化还原反应,不一定加入氧化剂或还原剂
(4)判断
①Cl→HClO(NaClO):不一定
2
②NO→HNO:不一定
2 3
③S→SO 2-:不一定
3
④KClO→KCl:不一定
3
⑤NaO→O:不一定
2 2 2
⑥CO→C:必须加入还原剂
2
⑦NH +→N:必须加入氧化剂
4 2
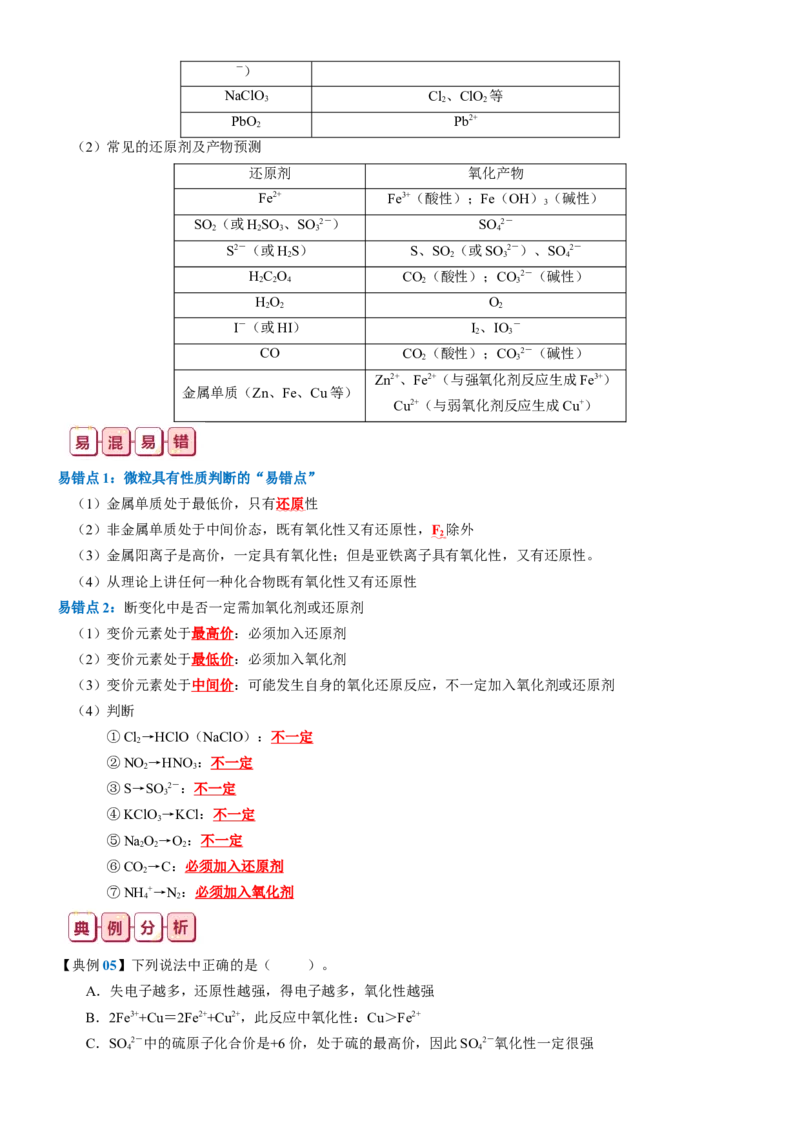
【典例05】下列说法中正确的是( )。
A.失电子越多,还原性越强,得电子越多,氧化性越强
B.2Fe3++Cu=2Fe2++Cu2+,此反应中氧化性:Cu>Fe2+
C.SO 2-中的硫原子化合价是+6价,处于硫的最高价,因此SO 2-氧化性一定很强
4 4D.氧化性强弱的顺序为;Z>A3+,则溶液中可发生:Z+2A2+=2A3++2Z-
2 2
【解析】选D。还原性、氧化性强弱与电子转移数目无关,不能利用失去电子数目分析还原性、氧化性。选项
A错误;2Fe3++Cu=2Fe2++Cu2+中铜是还原剂,Fe2+是还原产物,所以还原性Cu>Fe2+,则氧化性Fe2+>Cu。选
项B错误;元素的化合价处于最高价具有氧化性,但是不一定有强氧化性,如稀硫酸没有强氧化性,则SO 2-
4
氧化性不一定很强。选项C错误;氧化性强弱的顺序为;Z>A3+,则溶液中可发生:Z+2A2+=2A3++2Z-。选
2 2
项D正确。
【典例06】(2022·上海闸北区一模)下列物质中,按只有氧化性、只有还原性、既有氧化性又有还原性的顺序
排列的一组是( )。
A.F、K、HCl B.Cl、Al、H
2 2 2
C.NO 、Na、Br D.O、SO 、HO
2 2 2 2 2
【解析】选A。一般元素具有最高价时只有氧化性,元素具有最低化合价时只有还原性,处于中间价态时既具
有氧化性又具有还原性。F没有正化合价,因此F 只具有氧化性;K为金属,金属没有负化合价,因此K的化
2
合价只能升高不能降低,即单质K只具有还原性;HCl中的Cl-处于最低价态只具有还原性,H+具有氧化性,
因此HCl既具有氧化性又具有还原性。
知识点 04 氧化性、还原性强弱的比较
1.判断的本质依据:得失电子的难易程度
2.单质与其相应离子的氧化性和还原性变化相反
(1)根据金属活动顺序表
(2)根据非金属活动顺序表
3.根据化学反应比较氧化性或还原性强弱
(1)比较反应物和生成物的氧化性或还原性:强制弱原理
①氧化性:氧化剂>氧化产物
②还原性:还原剂>还原产物
(2)比较反应物的氧化性或还原性
①氧化性:氧化剂>还原剂②还原性:还原剂>氧化剂
4.根据反应条件来判断
当不同的氧化剂(或还原剂)与同一还原剂(或氧化剂)反应时,反应越易进行,则对应的氧化剂(或还
原剂)的氧化性(或还原性)越强,反之越弱。如:
(1)比较KMnO 和MnO 氧化性强弱:KMnO >MnO
4 2 4 2
①MnO +4HCl(浓) MnCl +Cl↑+2H O
2 2 2 2
②2KMnO +16HCl(浓) 2KCl+2MnCl +5Cl↑+8H O
4 2 2 2
(2)比较Na、Mg、Al的还原性强弱:Na>Mg>Al
①Na与冷水剧烈反应
②Mg与水加热才反应
③Al与水加热条件下也难反应
5.根据氧化产物的价态高低判断
(1)方法:同种物质被不同氧化剂氧化的价态越高,氧化剂的氧化性越强。
(2)实例:2Fe+3Cl 2FeCl ,Fe+S FeS,氧化性:Cl>S。
2 3 2
6.根据元素周期表比较单质的氧化性或还原性强弱
(1)周期表右上角的F 的氧化性最强
2
①容易与氢气化合的非金属单质的氧化性强
②气态氢化物稳定的非金属单质的氧化性强
③最高价含氧酸酸性强的非金属单质的氧化性强
④气态氢化物还原性强的非金属单质的氧化性弱
(2)短周期表左下角的Na 的还原性最强
①与酸或水反应剧烈的金属单质的还原性强
②最高价碱的碱性强的金属单质的还原性强
③相应阳离子的氧化性强的金属单质的还原性弱
7.根据原电池原理比较金属单质的还原性强弱
(1)基本规律:负极>正极
①电子流出的电极是负极,阳离子移向的电极是正极
②被溶解(质量减小)的电极一般是负极
③质量增加的电极一般是正极
④有气泡产生的电极一般是正极
(2)特殊情况
①强碱性溶液中,Mg-NaOH溶液-Al原电池中,Al 是负极
②氧化性溶液中,Cu-浓硝酸-Fe原电池中,Cu 是负极
③铅蓄电池,负极质量增加,正极质量增加
6.根据电解池原理比较(用惰性电极电解)
(1)阳极先放电的阴离子的还原性强,相应的非金属单质的氧化性弱
(2)阴极先放电的阳离子的氧化性强,相应的金属单质的还原性 不一定 弱
放电顺序:Fe3+>Cu2+,单质的还原性Fe>Cu
7.根据能量变化比较单质的氧化性和还原性强弱(1)金属越容易失电子,金属性越强,吸收的能量越少
(2)金属越容易得电子,非金属性越强,释放的能量越多
8.常见微粒的还原性顺序
−2 +4 −1 +3 −1 -1
还原性:S >S > I >Fe>Br>Cl
0 +6 −0 +2 0 0
氧化性:S<S < I <Fe<Br<Cl
(1)全部氧化:MnO - ( H + ) 、 ClO - ( H + ) 、CrO 2 - ( H + )
4 2 7
(2)氧化前五种: ClO - 、Cl 、浓硫酸(+4价S除外,无中间价态)
2
(3)氧化前四种:NO - ( H + ) 、HO ( H + ) 、Br
3 2 2 2
(4)氧化前三种: Fe 3+
9.强弱规律的两个应用
(1)氧化还原反应发生的先后顺序:强者优先
①向含多种还原剂的溶液中加入一种氧化剂时,还原性强的还原剂(离子)先被氧化
②向含多种氧化剂的溶液中,加入一种还原剂时,氧化性强的氧化剂(离子)先被还原
(2)判断氧化还原反应方向:强制弱原理
强氧化剂+强还原剂→弱还原剂+弱氧化剂
易错点:氧化性、还原性强弱比较的“易错点”
(1)氧化性或还原性的强弱与元素的化合价高低无必然关系。如HClO的氧化性高于HClO。
4
(2)氧化性或还原性的强弱与得失电子数多少无必然关系。如铝在反应中失去3个电子,钠失去1个电子,
但是那的还原性比铝的强
(3)具有氧化性的物质和具有还原性的物质不一定都能发生化学反应。如SO 具有还原性,浓硫酸具有氧化
2
性,但二者不发生氧化还原反应。
【典例07】下列有关物质氧化性强弱的说法中正确的是( )。
A.只有氧化性的物质,氧化性一定很强
B.得电子多的物质,氧化性一定很强
C.氧化剂的氧化性一定比氧化产物的氧化性强
D.还原剂的还原性越强,其氧化产物的氧化性也越强
【解析】选C。A项中,如Na+、K+等只有氧化性,但它们的氧化性都很弱,A项错。B项中,氧化性强弱与得
电子能力有关,与得电子多少无关,如1个Cl原子只能得1个电子,1个N原子可得3个电子,但Cl原子的氧
化性比N原子的强,B项错。C项中,“两强生成两弱”是氧化还原反应的一条重要规律,C项正确。D项中,
如Zn的还原性比Cu的强,其氧化产物的Zn2+氧化性比Cu2+的弱,D项错。
【典例08】(湖北省安陆市2021届高三4月模拟)(不定项)向盛有KMnO 溶液的试管中加入过量的MnSO
4 4
溶液,产生黑色沉淀,溶液由紫红色变为无色;过滤,向滤液中加入少量的铋酸钠(NaBiO)粉末,溶液又变
3
为紫红色。下列推断错误的是( )。
A.氧化性:NaBiO>KMnO >MnO
3 4 2
B.生成8.7g黑色沉淀,转移0.2mol电子C.利用NaBiO 可以检验溶液中的Mn2+
3
D.NaBiO 不能与浓盐酸发生反应生成氯气
3
【解析】选BD。氧化还原反应中,氧化性:氧化剂大于氧化产物;氧化剂发生还原反应化合价降低。在盛有
KMnO 溶液的试管中加入过量的MnSO 溶液,产生黑色沉淀,溶液由紫红色变为无色,说明KMnO 溶液可氧
4 4 4
化MnSO 生成MnO ,故氧化性:KMnO >MnO ,在滤液中加入少量的铋酸钠粉末(NaBiO),溶液变紫红色,
4 2 4 2 3
说明NaBiO 可氧化MnSO 生成KMnO ,故氧化性:NaBiO>KMnO ,故氧化性:NaBiO>KMnO >MnO 。
3 4 4 3 4 3 4 2
根据以上分析,氧化性:NaBiO>KMnO >MnO ,故A正确;在盛有KMnO 溶液的试管中加入过量的MnSO
3 4 2 4 4
溶液,产生黑色沉淀,离子方程式为:2MnO -+3Mn2++2H O 5MnO ↓+4H+,转移电子数为6e-,所以生成
4 2 2
8.7g 0.6
8.7g黑色沉淀即 87g/mol =0.1molMnO ,转移 5 mol=0.12mol电子,故B错误;NaBiO 可氧化MnSO 生成
2 3 4
KMnO ,溶液变为紫红色,所以利用NaBiO 可以检验溶液中的Mn2+,故C正确;因为实验室用二氧化锰与浓
4 3
盐酸反应制氯气,说明氧化性:MnO >Cl,又氧化性:NaBiO>MnO ,故NaBiO 可与浓盐酸发生反应:
2 2 3 2 3
NaBiO+6HCl BiCl +Cl↑+NaCl+3HO,故D错误。
3 3 2 2
知识点 05 氧化还原反应方程式的书写和配平
1.配平原则
2.化合价升降法配平步骤
3.信息型氧化还原方程式书写流程【典例09】(2022·河北省选择考)以焙烧黄铁矿FeS(杂质为石英等)产生的红渣为原料制备铵铁蓝Fe
2
(NH )Fe(CN) 颜料。工艺流程如下:
4 6
(1)还原工序中,不生成S单质的反应的化学方程式为__________________________________。
(2)沉铁工序产生的白色沉淀Fe(NH )Fe(CN) 中Fe的化合价为__________,氧化工序发生反应的离子
4 2 6
方程式为____________________________________________。
【解析】(1)还原工序中,不产生S单质沉淀,则硫元素被氧化为SO 2-,反应原理为:14Fe3++FeS +8H O
4 2 2
15Fe2++2 SO 2-+16H+,故化学方程式为:7Fe (SO )+FeS +8H O 15FeSO +8H SO ;(2)沉铁工序中产生
4 2 4 3 2 2 4 2 4
的白色沉淀Fe(NH )Fe(CN) 中Fe的化合价为+2价和[Fe(CN)]3-中的+3价,则氧化工序所发生的离
4 2 6 6
子方程式为:Fe(NH )Fe(CN)+ClO-+2H+ Fe(NH )Fe(CN)+H O+Cl-+NH+。
4 2 6 4 6 2 4
【答案】(1)7Fe (SO )+FeS +8H O 15FeSO +8H SO
2 4 3 2 2 4 2 4
(2)+2、+3;Fe(NH )Fe(CN)+ClO-+2H+ Fe(NH )Fe(CN)+H O+Cl-+NH+
4 2 6 4 6 2 4
知识点 06 氧化还原反应的有关计算
1.氧化还原反应中电子转移的表示方法
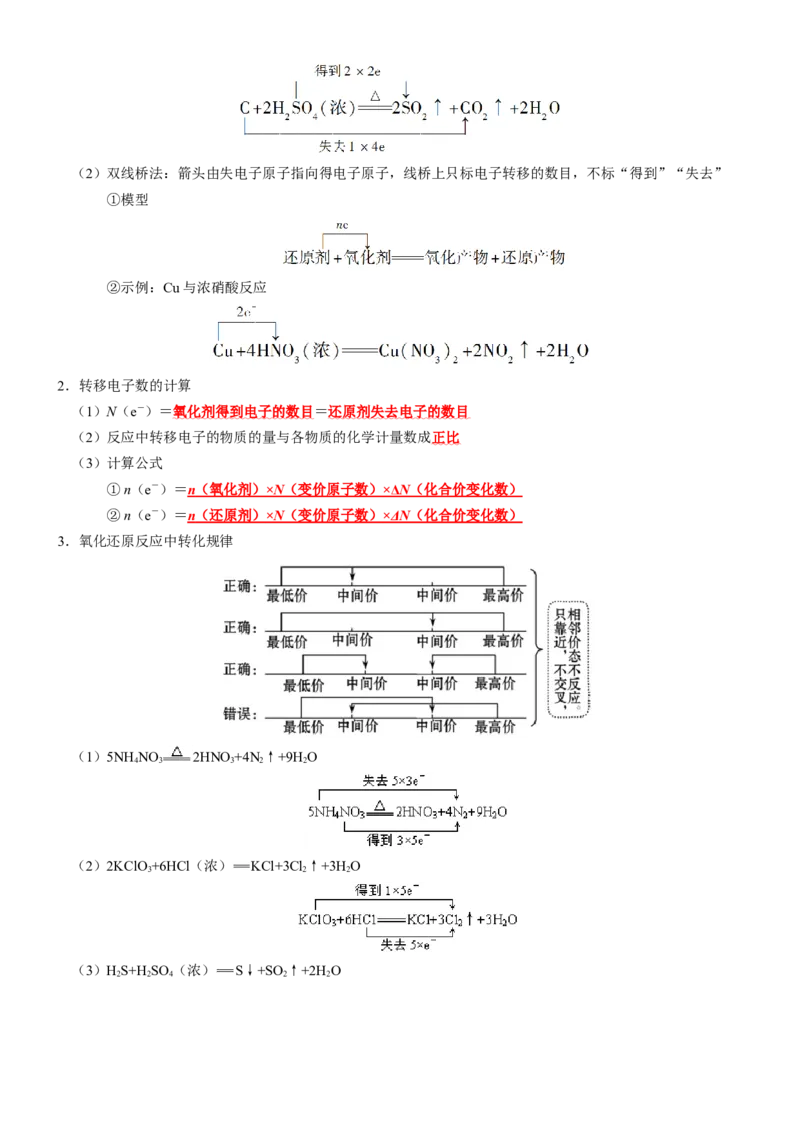
(1)双线桥法:标变价→画箭头→标得失→定数目
①模型
②示例:C与浓硫酸反应(2)双线桥法:箭头由失电子原子指向得电子原子,线桥上只标电子转移的数目,不标“得到”“失去”
①模型
②示例:Cu与浓硝酸反应
2.转移电子数的计算
(1)N(e-)= 氧化 剂得到电子的数目 =还原剂失去电子的数目
(2)反应中转移电子的物质的量与各物质的化学计量数成正比
(3)计算公式
①n(e-)= n (氧化剂) × N (变价原子数) ×Δ N (化合价变化数)
②n(e-)= n (还原剂) ×N (变价原子数) ×ΔN (化合价变化数)
3.氧化还原反应中转化规律
(1)5NH NO 2HNO+4N ↑+9H O
4 3 3 2 2
(2)2KClO+6HCl(浓) KCl+3Cl↑+3HO
3 2 2
(3)HS+HSO (浓) S↓+SO↑+2H O
2 2 4 2 24.电子守恒规律
(1)规律:氧化还原反应中得电子总数与失电子总数相等,表现为元素化合价降低总数与升高总数相等。
(2)应用:运用电子守恒进行氧化还原反应的相关计算。
5.“电子守恒法”计算的一般思维模板
【典例10】(2021·山东省等级考)(不定项)实验室中利用固体KMnO 进行如图实验,下列说法错误的是(
4
)。
A.G与H均为氧化产物
B.实验中KMnO 只作氧化剂
4
C.Mn元素至少参与了3个氧化还原反应
D.G与H的物质的量之和可能为0.25mol
【解析】选BD。KMnO 固体受热分解生成KMnO 、MnO 、O,KMnO 、MnO 均具有氧化性,在加热条件
4 2 4 2 2 2 4 2
下能与浓盐酸发生氧化还原反应,反应过程中Cl-被氧化为Cl,KMnO 、MnO 被还原为MnCl ,因此气体单
2 2 4 2 2
质G为O,气体单质H为Cl。加热KMnO 固体的反应中,O元素化合价由-2升高至0被氧化,加热
2 2 4
KMnO 、MnO 与浓盐酸的反应中,Cl元素化合价由-1升高至0被氧化,因此O 和Cl 均为氧化产物,故A
2 4 2 2 2
正确;KMnO 固体受热分解过程中,Mn元素化合价降低被还原,部分O元素化合价升高被氧化,因此KMnO
4 4
既是氧化剂也是还原剂,故B错误;Mn元素在反应过程中物质及化合价变化为KMnO →KMnO +MnO 、
4 2 4 2
KMnO →MnCl 、MnO →MnCl ,还可能发生剩余的KMnO →MnCl ,Mn元素至少参加了3个氧化还原反应,
2 4 2 2 2 4 2
故C正确;整个过程KMnO ~MnCl ~5e-,2Cl-→Cl~2e-,2O2-~O ~4e-,根据电子守恒有如下关系式:5n
4 2 2 2
(KMnO )=2n(Cl)+4n(O)=5×0.1mol=0.5mol,所以n(Cl)+2n(O)=0.25mol,即n(Cl)+n
4 2 2 2 2 2
(O)<0.25mol,故D错误。
2