文档内容
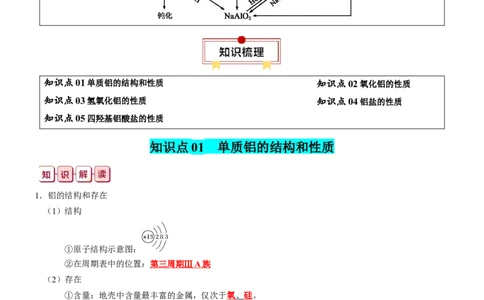
知识清单 07 铝及其重要化合物
知识点01单质铝的结构和性质 知识点02氧化铝的性质
知识点03氢氧化铝的性质 知识点04铝盐的性质
知识点05四羟基铝酸盐的性质
知识点 01 单质铝的结构和性质
1.铝的结构和存在
(1)结构
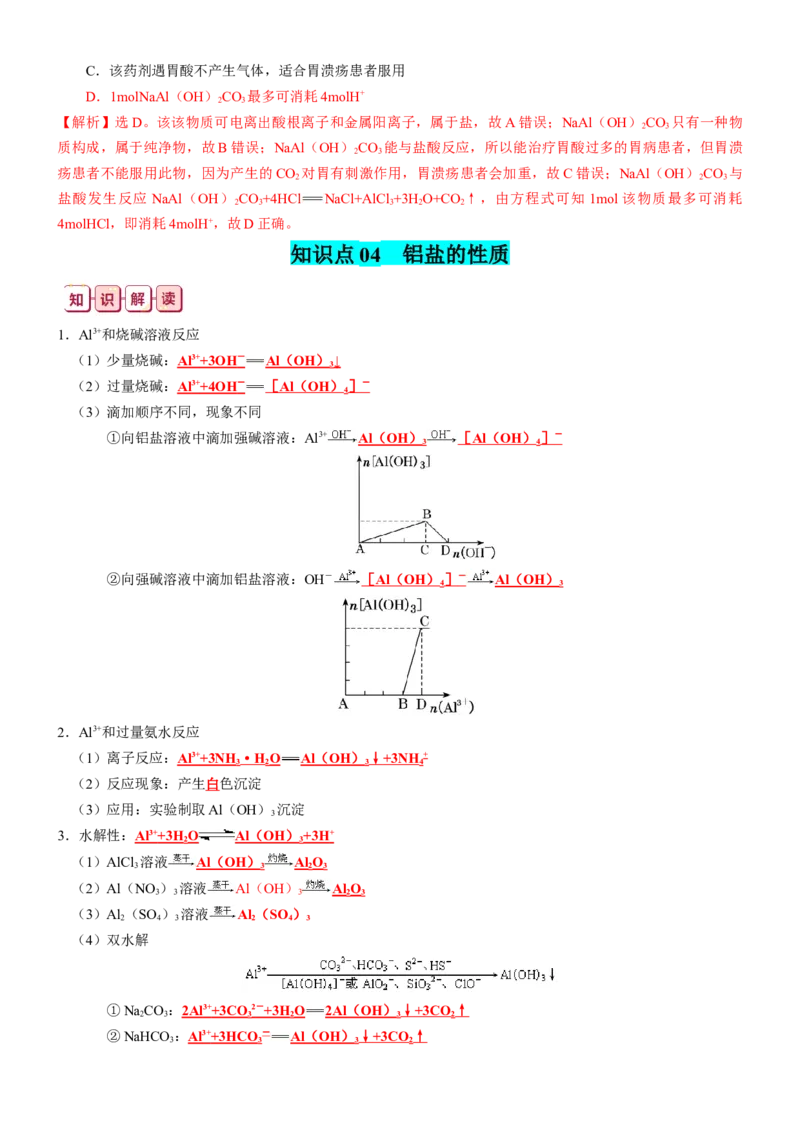
①原子结构示意图:
②在周期表中的位置: 第三周期Ⅲ A 族
(2)存在
①含量:地壳中含量最丰富的金属,仅次于 氧 、 硅 。
②形态:自然界中的铝全部以化合态存在
2.物理性质
(1)色质态:银白色有金属光泽的质软的固体
(2)熔沸点:熔点660.4℃,沸点2467℃
(3)三性:延展性、导热性和导电性良好
(4)密度:2.7g/cm3,是一种轻金属
3.与氧气反应:Al+O →Al O
2 2 3
(1)Al-------→具有抗腐蚀性,原因:表面生成一层致密的氧化物阻止铝和氧气继续反应
(2)Al-------→放出大量的热,发出耀眼的白光4.铝热反应
(1)实验装置
(2)反应:2Al+Fe O 2Fe+Al O
2 3 2 3
(3)本质:Al和不活泼金属氧化物的置换反应
(4)引发操作:加入少量KClO,插上Mg条并点燃
3
(5)特点:反应放出大量的热,得到熔融的金属
(6)应用:冶炼V、Cr、Mn等难熔金属;焊接钢轨
①冶炼V:10Al+3V O 5Al O+6V
2 5 2 3
②冶炼Cr:2Al+Cr O 2Cr+Al O
2 3 2 3
③冶炼Mn:4Al+3MnO 3Mn+2Al O
2 2 3
④冶炼Cu:2Al+3Cu O 6Cu+Al O
2 2 3
5.铝与酸的反应
(1)氧化性酸
①Al---------------------→钝化
②Al---------------------→剧烈反应,分别放 N O 和 S O 气体
2 2
③Al----------→放 N O 气体
(2)非氧化性酸:Al---------------------→放H
2
①关系式: 2Al~6H + ~3H ↑
2
②离子方程式: 2Al+6H + 2Al 3+ +3H ↑
2
6.铝与强碱溶液的反应
(1)化学:2Al+2NaOH+6H O 2Na [ Al ( OH ) ] +3H ↑
2 4 2
(2)离子: 2Al+2OH - +6H O 2 [ Al ( OH ) ] - +3H ↑
2 4 2
(3)铝和强碱溶液的反应过程
①置换反应:2Al+6H O 2Al(OH)+3H↑
2 3 2
②中和反应:Al(OH)+NaOH Na[Al(OH)]
3 4
③还原剂是Al,氧化剂是HO
2
7.铝与盐溶液的置换反应
(1)CuSO -------→Cu;AgNO-------→Ag
4 3
(2)FeCl -------→ Fe 2+ ;FeCl -------→Fe
3 3
易错点:铝的易错知识点(1)铝是活泼金属,但铝的抗腐蚀性强,因为铝的表面有一层致密的氧化物薄膜。由于Al O 的熔点高于Al
2 3
的熔点,故在酒精灯上加热铝箔直至熔化,熔化的铝并不滴落。
(2)铝热反应不仅指铝与Fe O 反应,铝热反应置换的金属为金属活动性比铝弱的难熔金属。
2 3
(3)常温下铝不能溶于浓硫酸和浓硝酸,不是不反应,而是发生钝化,在表面生成一层致密的氧化膜,阻止
反应继续进行。
(4)铝既能与酸溶液反应,又能与强碱溶液反应,但是铝不是两性金属,它是一种活泼金属,表现强还原性。
(5)铝热剂着火时不能用水灭火,应用沙土盖灭。
【典例01】(2023·阜阳模拟)根据如图的转化关系判断,下列说法正确的是(反应条件已略去)( )。
A.生成等质量H 时,①和②反应消耗n(HCl)=n(NaOH)
2
B.反应③中氧化剂与还原剂的物质的量之比为2∶3
C.反应③和④消耗等量的Al时,生成的n(Cu)∶n(Fe)=3∶2
D.等浓度等体积的稀HCl和NaOH溶液与足量Al反应,①②生成H 的分子数之比为3∶1
2
【解析】选C。A项,根据方程式可知n(HCl)=3n(NaOH),错误;B项,根据电子守恒,n(氧化剂)×2
=n(还原剂)×3;可知n(氧化剂)∶n(还原剂)=3∶2,错误;D项,根据方程式可知生成H 的分子数比
2
为1∶3,错误。
知识点 02 氧化铝的性质
1.物性:白色的难熔(熔点高)的物质
2.两性氧化物
(1)与酸溶液反应
①盐酸:Al O +6H + 2Al 3+ +3H O
2 3 2
②碳酸:不反应
(2)与碱溶液反应
①烧碱:Al O +2OH - +3H O 2 [ Al ( OH ) ] -
2 3 2 4
②氨水:不反应
3.电分解反应
(1)阳极反应: 2O 2 - - 4e - O↑
2
(2)阴极反应: Al 3+ +3e - Al
(3)电解反应:2Al O 4Al+3O ↑
2 3 2
(4)冰晶石的作用: 降低 A l O 的熔点,节能
2 3(5)阳极石墨与氧气反应,被消耗,需要定期更换
4.氧化铝的用途
(1)耐火材料:制耐火坩埚、耐火管和耐高温的实验仪器
(2)炼铝原料:电解熔融的氧化铝
易错点:氧化铝的易错知识点
(1)Al O 既能与盐酸反应,也能与NaOH溶液反应。但Al O 不溶于氨水和碳酸。
2 3 2 3
(2)不能用氧化铝坩埚熔化酸性和碱性固体物质。
(3)电解熔融的Al O 制取铝时,要加入冰晶石以降低的熔点。而且阳极石墨被阴极产物氧气氧化而需要随
2 3
时更换。
【典例02】(2023·广东湛江一模)在下列操作中,不能得到纯净氧化铝的是( )。
A.向AlCl 溶液中加入过量氨水后,蒸干并灼烧
3
B.向NaAlO 溶液中加入适量AlCl 溶液后,蒸干并灼烧
2 3
C.将AlCl 溶液蒸干并灼烧
3
D.向NaAlO 溶液中通入过量CO 后,过滤,灼烧滤渣
2 2
【解析】选B。AlCl 溶解加入过量氨水,AlCl +3NH ·HO Al(OH)↓+3NHCl+3H O,蒸干过程中
3 3 3 2 3 4 2
NH ·HO挥发,蒸干得到Al(OH) 和NH Cl,灼烧时,NH Cl分解生成NH 和HCl挥发,剩余固体Al O,A
3 2 3 4 4 3 2 3
项正确;NaAlO 溶液中加入适量AlCl ,发生反应3NaAlO +AlCl +6HO 4Al(OH)↓+3NaCl,蒸干得到Al
2 3 2 3 2 3
(OH) 和NaCl,灼烧得到的是Al O 和NaCl,不能得到纯净的Al O,B项错;AlCl 溶液蒸干并灼烧,得到
3 2 3 2 3 3
的是Al O,C项正确;NaAlO 溶液通入足量的CO 后,过滤得到的是Al(OH),在灼烧得到Al O,D项正
2 3 2 2 3 2 3
确。
知识点 03 氢氧化铝的性质
1.物性:白色的难溶于水胶状物质
2.两性氢氧化物
(1)与酸溶液反应
①碱式电离: Al ( OH ) Al 3+ + 3OH -
3
②盐酸: Al ( OH ) +3H + Al 3+ +3H O
3 2
③碳酸:不反应(2)与碱溶液反应
①酸式电离: Al ( OH ) +H O H + + [ Al ( OH ) ] -
3 2 4
②烧碱:Al(OH) +OH - [ A l ( OH ) ] -
3 4
③氨水:不反应
3.热分解反应: 2Al ( OH ) Al O + 3H O
3 2 3 2
4.氢氧化铝的用途
(1)Al(OH) 作治疗胃酸过多的内服药
3
(2)Al(OH) 胶体做净水剂
3
5.实验室制备Al(OH) 的三种方法
3
(1)可溶性铝盐溶液与过量氨水反应
Al3++3NH·HO=Al(OH)↓+3NH+
3 2 3 4
(2)向可溶性偏铝酸盐溶液中通入过量CO
2
[Al(OH)]-+CO =Al(OH)↓+HCO-
4 2 3 3
(3)相互促进水解法
易错点:氢氧化铝的易错知识点
(1)Al(OH) 碱性极弱,可用作抗酸药。
3
(2)Al(OH) 不溶于氨水和碳酸,所以实验室常利用铝盐与氨水反应制备Al(OH),偏铝酸盐与CO 反
3 3 2
应制备Al(OH)。
3
【典例03】Zn(OH) 是一种与Al(OH) 类似的两性氢氧化物,它与强碱反应的离子方程式为:Zn(OH)
2 3
+2OH-=ZnO2-+2H O。而且Zn(OH) 还能溶于过量的氨水,生成易溶于水的Zn(NH )2+,而Al(OH)
2 2 2 2 3 4 3
不能。则下面四组溶液不能用相互滴加来进行鉴别的是( )。
A.AlCl 、NH ·HO B.ZnCl、NH ·HO C.AlCl 、NaOH D.ZnCl、NaOH
3 3 2 2 3 2 3 2
【解析】选A。因为Al(OH) 不溶于氨水,所以AlCl 和NH ·HO不论按照何种顺序混合,都只会产生白色
3 3 3 2
沉淀,用相互滴加的方法无法鉴别;由于Al(OH) 溶于NaOH溶液,所以向AlCl 溶液中滴加NaOH溶液时,
3 3
先产生白色沉淀,后沉淀消失,而向NaOH溶液中滴加AlCl 溶液时,由于NaOH溶液过量。所以先没有沉淀产
3
生,能够鉴别;由于Zn(OH) 溶于NaOH溶液和氨水,所以向ZnCl 溶液中滴加NaOH溶液或NH ·HO时,
2 2 3 2
先产生白色沉淀,后沉淀消失,而向NaOH溶液或NH ·HO中滴加ZnCl 溶液时,由于NaOH溶液或
3 2 2
NH ·HO过量。所以先没有沉淀产生,能够鉴别。
3 2
【典例04】(山西临汾2022届高三上学期期中)双羟基铝碳酸钠是医疗上常用的一种抑酸剂,化学式是NaAl
(OH)CO,下列关于该物质的说法正确的是( )。
2 3
A.该物质属于两性氢氧化物
B.该物质是Al(OH) 和NaCO 的混合物
3 2 3C.该药剂遇胃酸不产生气体,适合胃溃疡患者服用
D.1molNaAl(OH)CO 最多可消耗4molH+
2 3
【解析】选D。该该物质可电离出酸根离子和金属阳离子,属于盐,故A错误;NaAl(OH) CO 只有一种物
2 3
质构成,属于纯净物,故B错误;NaAl(OH) CO 能与盐酸反应,所以能治疗胃酸过多的胃病患者,但胃溃
2 3
疡患者不能服用此物,因为产生的CO 对胃有刺激作用,胃溃疡患者会加重,故C错误;NaAl(OH) CO 与
2 2 3
盐酸发生反应 NaAl(OH) CO+4HCl NaCl+AlCl +3H O+CO↑,由方程式可知 1mol该物质最多可消耗
2 3 3 2 2
4molHCl,即消耗4molH+,故D正确。
知识点 04 铝盐的性质
1.Al3+和烧碱溶液反应
(1)少量烧碱: Al 3+ +3OH - Al ( OH ) ↓
3
(2)过量烧碱: Al 3+ +4OH - [ A l ( OH ) ] -
4
(3)滴加顺序不同,现象不同
①向铝盐溶液中滴加强碱溶液:Al3+ Al ( OH ) [ A l ( OH ) ] -
3 4
②向强碱溶液中滴加铝盐溶液:OH- [ A l ( OH ) ] - Al ( OH )
4 3
2.Al3+和过量氨水反应
(1)离子反应: Al 3+ +3NH · H O Al ( OH ) ↓ +3NH +
3 2 3 4
(2)反应现象:产生白色沉淀
(3)应用:实验制取Al(OH) 沉淀
3
3.水解性: Al 3+ +3H O Al ( OH ) +3H +
2 3
(1)AlCl 溶液 Al ( OH ) Al O
3 3 2 3
(2)Al(NO ) 溶液 Al(OH) Al O
3 3 3 2 3
(3)Al (SO ) 溶液 Al (SO )
2 4 3 2 4 3
(4)双水解
①NaCO: 2Al 3+ +3CO 2 - +3H O 2Al ( OH ) ↓ +3CO ↑
2 3 3 2 3 2
②NaHCO : Al 3+ +3HCO - Al ( OH ) ↓ +3CO ↑
3 3 3 2③NaS: 2Al 3+ +3S 2 - +6H O 2 Al ( OH ) ↓ +3H S ↑
2 2 3 2
④NaHS: Al 3+ +3HS - +3H O Al ( OH ) ↓ +3H S ↑
2 3 2
⑤NaClO: Al 3+ + 3 ClO - + 3H O Al ( OH ) ↓ + 3H ClO
2 3
4.明矾
(1)化学式: KAl ( SO ) · 12H O
4 2 2
(2)物理性质:白色的晶体,易溶于水
(3)电离方程式: KAl ( SO ) K + +Al 3+ +2SO 2-
4 2 4
(4)用途:Al3+水解产生 Al ( OH ) 胶体,常用做净水剂
3
(5)溶液配制:常加入少量稀硫酸以防止它的水解
(6)明矾溶液和氢氧化钡溶液反应
①滴加Ba(OH) 溶液至SO 2-沉淀完全
2 4
KAl ( SO ) +2Ba ( OH ) K [ Al ( OH ) ] +2BaSO ↓
4 2 2 4 4
②滴加Ba(OH) 溶液至Al3+沉淀完全
2
2KAl ( SO ) +3Ba ( OH ) KSO +3BaSO ↓ +2A l ( OH ) ↓
4 2 2 2 4 4 3
5.铵明矾[NH Al(SO )·12H O]和碱溶液的反应
4 4 2 2
(1)铵明矾溶液和氢氧化钡溶液反应
①滴加Ba(OH) 溶液至SO 2-沉淀完全
2 4
NH Al ( SO ) +2Ba ( OH ) Al ( OH ) ↓ + NH · H O +2BaSO ↓
4 4 2 2 3 3 2 4
②滴加Ba(OH) 溶液至Al3+沉淀完全
2
2NH Al ( SO ) +3Ba ( OH ) ( NH )SO +3BaSO ↓ +2A l ( OH ) ↓
4 4 2 2 4 2 4 4 3
(2)铵明矾溶液和氢氧化钠溶液反应
①OA段: Al 3+ +3OH - Al ( OH ) ↓
3
②AB段:NH + +OH - NH · H O
4 3 2
③BC段: Al ( OH ) +OH - [ A l ( OH ) ] -
3 4
易错点:铝盐的易错知识点
(1)明矾常用于净水,其原因是铝离子水解生成的氢氧化铝吸附水中的悬浮物,而不是明矾具有杀菌消毒功
能。
(2)泡沫灭火器所用试剂为Al (SO ) 溶液和NaHCO 溶液,反应的离子方程式为Al3++3HCO- Al
2 4 3 3 3
(OH)↓+3CO↑
3 2
(3)实验室不能用NaS和AlCl 溶液反应制备Al S 固体,二者混合会发生水解相互促进反应:2Al3++3S2-
2 3 2 3
+6HO 2Al(OH)↓+3H S↑
2 3 2
(4)AlCl 是共价化合物,熔融状态不导电,不能用电解熔融AlCl 的制取金属铝。
3 3【典例05】(天津市六校2022届高三上学期期末联考)明矾[KAl(SO )·12HO]是一种重要的化学试剂。
4 2 2
下列说法正确的是( )。
A.明矾水溶液显酸性,故明矾属于酸式盐
B.0.1mol•L-1明矾溶液完全水解生成Al(OH) 胶粒数小于6.02×1022
3
C.当n[KAl(SO )·12HO]∶n[Ba(OH)]=2∶3时,溶液中生成沉淀的质量最大
4 2 2 2
D.室温下,0.1mol•L-1明矾溶液中水电离出c(H+)大于10-7mol·L-1
【解析】选D。明矾水溶液显酸性,是因为铝离子在水溶液发生水解导致的,本身不是酸式盐,A错误;胶粒
是多个胶体的聚集体,因溶液未给出体积,所以无法衡量计算0.1mol•L-1明矾溶液完全水解生成Al(OH) 胶
3
粒数是否小于6.02×1022,B错误;当n[KAl(SO )·12HO]∶n[Ba(OH)]=2∶3时,发生的离子方程
4 2 2 2
式为2Al3++3SO2-+3Ba2++6OH- 3BaSO↓+2Al(OH)↓,溶液中生成沉淀的物质的量最大,而当n[KAl
4 4 3
(SO )·12HO]∶n[Ba(OH)]=1∶2时,发生的离子方程式为Al3++2SO2-+2Ba2++4OH-
4 2 2 2 4
2BaSO↓+AlO -+2H O,则此时生成的沉淀的质量最大,C错误;明矾溶液中铝离子发生水解显酸性,促进水
4 2 2
的电离,则室温下,0.1mol•L-1明矾溶液中水电离出c(H+)大于10-7mol·L-1,D正确。
【典例06】(2022·长春高三质量监测)向盛有10mLlmol/LNH Al(SO ) 溶液的烧杯中滴加1mol/LNaOH溶液,
4 4 2
沉淀物质的量随NaOH溶液体积变化示意图如下。下列有关说法正确的是( )。
A.当加入50mLNaOH时,溶液中的溶质为NaAlO
2
B.m点反应的离子方程式:NH ++OH-=NH ·HO
4 3 2
C.NH Al(SO ) 溶液中离子浓度由大到小的顺序是:c(SO 2-)>c(Al3+)>c(NH +)>c(H+)>c
4 4 2 4 4
(OH-)
D.若向NH Al(SO ) 溶液改加20mL1.2mol/LBa(OH) 溶液,充分反应后,溶液中产生沉淀的物质的
4 4 2 2
量为0.02mol
【解析】选B。0~30mL时发生的反应为Al3++3OH-=Al(OH) ↓,30~40mL发生的离子方程式为NH ++OH-
3 4
=NH ·HO,40~50mL之间发生的离子方程式为 Al(OH) +OH-=AlO -+H O。当加入50mLNaOH时,溶液
3 2 3 2 2
中的溶质为NaAlO 、NH .HO,而不是单一的偏铝酸钠,故A错误;m点NaOH溶液体积在30-40mL之间,
2 3 2
所以发生第二个离子方程式,方程式为:NH ++OH-=NH •H O,故B正确;NH Al(SO ) 溶液中铵根离子、
4 3 2 4 4 2
铝离子都易发生水解反应,且铝离子水解程度大于铵根离子,所以离子浓度由大到小的顺序是:c(SO 2-)>c
4
(NH +)>c(Al3+)>c(H+)>c(OH-),故C错误;n[NH Al(SO ) ]=1mol/L×0.01L=0.01mol,其中
4 4 4 2
n(NH +)=0.01mol、n(Al3+)=0.01mol、n(SO 2-)=0.02mol,n[Ba(OH) ]=1.2mol/L×0.02L=
4 4 2
0.024mol,其中n(Ba2+)=0.024mol、n(OH-)=0.048mol。根据Ba2++SO2- BaSO↓可知Ba2+过量,SO 2
4 4 4
-完全反应,生成0.02mol BaSO ;又知0~40mL时Al3+和NH +消耗OH-的物质的量为0.04mol,而OH-的总物
4 4
质的量是0.048mol,所以溶解Al(OH) 的OH-的物质的量为0.048mol-0.04mol=0.008mol,根据Al(OH)
3+OH-=AlO -+2H O,所以此时溶解0.008mol Al(OH) 沉淀,剩余Al(OH) 沉淀的物质的量为0.01mol-
3 2 2 3 3
0.008mol=0.002mol,则最终得到固体为0.02mol+0.002mol=0.022mol,故D错误。
知识点 05 四羟基合铝酸盐的性质
1.相当处理:[Al(OH)]- Al(OH)+OH-
4 3
2.和盐酸反应
(1)少量盐酸: [ A l ( OH ) ] - +H + Al ( OH ) ↓ +H O
4 3 2
(2)过量盐酸 : [ A l ( OH ) ] - +4H + Al 3+ +4H O
4 2
(3)滴加顺序不同,现象不同
①向四羟基合铝酸盐溶液中滴加强酸溶液:
[Al(OH)]- Al ( OH ) ↓ [ A l ( OH ) ] -
4 3 4
②向强酸溶液中滴加四羟基合铝酸盐溶液:
H+ [ A l ( OH ) ] - Al ( OH ) ↓
4 3
3.和CO 反应
2
(1)少量CO:2[Al(OH)]-+CO 2Al(OH)↓+CO2-+H O
2 4 2 3 3 2
(2)过量CO: [ A l ( OH ) ] - +CO Al ( OH ) ↓ +HCO -
2 4 2 3 3
4.和NaHCO 溶液反应:HCO - + [ A l ( OH ) ] - Al ( OH ) ↓ +CO 2 - +H O
3 3 4 3 3 2
5.水解性
(1)离子反应:[Al(OH)]- Al(OH)+OH-
4 3
(2)AlCl : Al 3+ + 3 [ Al ( OH ) ] - 4 Al ( OH ) ↓
3 4 3
(3)MgCl : 2 [ Al ( OH ) ] - + M g 2 + 2 Al ( OH ) ↓ + M g ( OH ) ↓
2 4 3 2
(4)NH Cl:[Al(OH)]-+NH+ Al(OH)↓+ NH ·HO
4 4 4 3 3 2
6.铝土矿提铝(Al O,含少量Fe O 和SiO)
2 3 2 3 2
(1)强酸→强碱→弱酸法(2)强碱→强酸→弱碱法
易错点:注意滴加顺序不同,反应不同
(1)向氢氧化钠溶液中不断滴加铝盐溶液,先发生:Al3++4OH- AlO-+2H O,后发生:Al3++3AlO -
2 2 2
+6H O 4Al(OH)↓。
2 3
(2)向铝盐溶液中不断滴加氢氧化钠溶液,先发生:Al3++3OH- Al(OH)↓,后发生:Al(OH)+OH
3 3
- AlO-+2H O。
2 2
(3)向盐酸溶液中不断滴加偏铝酸盐溶液,先发生:AlO-+4H+ Al3++4HO,后发生:Al3++3AlO -+6H O
2 2 2 2
4Al(OH)↓。
3
(4)向偏铝酸盐溶液中不断滴加盐酸溶液,先发生:AlO-+HO+H+ Al(OH)↓,后发生:Al(OH)
2 2 3
+3H+ Al3++3HO。
3 2
【典例07】(首师大二附中2022~2023学年度高三上学期期中)将足量的CO 不断通入KOH、Ba(OH)、
2 2
KAlO 的混合溶液中,生成沉淀的物质的量与所通入CO 的体积关系如图所示。下列关于整个反应过程中的叙
2 2
述不正确的是( )。
A.Oa段反应的化学方程式是Ba(OH)+CO BaCO ↓+H O
2 2 3 2
B.ab段与cd段所发生的反应相同
C.de段沉淀减少是由于BaCO 固体消失
3
D.bc段反应的离子方程式是2AlO﹣+3H O+CO 2Al(OH)↓+CO 2﹣
2 2 2 3 3
【解析】选B。只要通入CO,立刻就有沉淀BaCO 产生,首先Oa段发生反应Ba(OH)+CO
2 3 2 2
BaCO ↓+H O,将Ba(OH) 消耗完毕,A正确;接下来消耗KOH,ab段发生反应2KOH+CO
3 2 2 2
KCO+H O,因而此段沉淀的量保持不变,然后沉淀量增大,bc段发生反应2AlO﹣+3H O+CO 2Al(OH)
2 3 2 2 2 2
↓+CO 2﹣,沉淀量达最大后,cd段再发生CO2﹣+CO +H O HCO ﹣,ab段与cd段所发生的反应不相同,故
3 3 3 2 2 3
B错误;最后de段发生反应BaCO +CO +H O Ba(HCO ),沉淀部分溶解,故C正确;bc段发生反应
3 2 2 3 2
2AlO﹣+3H O+CO 2Al(OH)↓+CO 2﹣,故D正确。
2 2 2 3 3【典例08】(2023·石家庄模拟)以铝土矿粉(主要含Al O、Fe O、SiO,少量FeS 和金属硫酸盐)为原料生
2 3 2 3 2 2
产Al O 和Fe O 的部分流程如下:
2 3 3 4
下列说法正确的是( )。
A.“焙烧Ⅰ”时,加入少量CaO可提高矿粉中硫的去除率
B.用NaOH溶液吸收过量SO 的离子方程式为2OH-+SO=SO 2-+H O
2 2 3 2
C.滤液中通入足量CO,过滤后可得到Al O
2 2 3
D.无氧条件下进行“焙烧Ⅱ”时,理论上消耗的n(FeS)∶n(Fe O)=1∶16
2 2 3
【解析】选D。铝土矿粉在空气中焙烧,将FeS 转化为氧化铁和二氧化硫,加入氢氧化钠溶液,氧化铝、二氧
2
化硅和氢氧化钠反应除去铝、硅,得到氧化铁,氧化铁加入FeS 隔绝氧气焙烧得到四氧化三铁。氧化钙和硫元
2
素化合物反应转化为硫酸钙留在矿粉中,导致矿粉中硫的去除率下降,A错误;用NaOH溶液吸收过量SO 生
2
成亚硫酸氢钠:OH-+SO=HSO -,B错误;滤液中通入足量CO,偏铝酸钠和二氧化碳生成氢氧化铝沉淀,
2 3 2
不是Al O,C错误;无氧条件下进行“焙烧Ⅱ”,FeS 和Fe O 反应生成四氧化三铁,反应为FeS+16Fe O
2 3 2 2 3 2 2 3
2SO +11Fe O,理论上消耗的n(FeS)∶n(Fe O)=1∶16,D正确。
2 3 4 2 2 3