文档内容
第三章 烃的衍生物
第三节 醛 酮
【即时训练】
一、单选题
1.乙醇醛的球棍模型如图,下列说法错误的是
A.含有两种官能团 B.能与钠、氢氧化铜悬浊液反应
C.在Cu作催化剂时催化氧化后官能团种类和数目不变 D.与乙酸互为同分异构体
2.下列措施不能除去室内空气中甲醛的是
A.放置活性炭 B.放置酸性高锰酸钾溶液
C.放置稀盐酸 D.放置某些植物
3.下列有关银镜反应实验的说法不正确的是
A.实验前先用热的烧碱溶液洗涤有油脂的试管,再用蒸馏水洗涤
B.向2%的硝酸银溶液中滴入2%的稀氨水,直至产生的沉淀恰好溶解,配得银氨溶液
C.采用水浴加热,不能直接加热
D.可用浓盐酸洗去银镜
4.下列实验操作正确的是
A.配制氢氧化铜悬浊液时,需在3mL5%NaOH溶液中滴入3~4滴2%CuSO 溶液
4
B.配制银氨溶液时,需将2%的硝酸银溶液逐滴加入到2%的稀氨水
C.实验室制备硝基苯时,温度计插入反应溶液中,并控制温度在50~60℃之间
D.苯酚对皮肤有腐蚀性,若粘在皮肤上,要用氢氧化钠溶液来洗
5.化学与生产、生活密切相关,下列说法正确的是
A.家庭和汽车用的灌装液化石油气(LPG)是煤分馏所获得的各种芳香烃
B.卤代烃由于化学性质稳定、无毒、不燃烧、易挥发、易液化等特性,曾被广泛用作制冷剂灭火剂等
C.甲醛是最简单的醛,用途广泛,能合成多种有机化合物,但它不能被银氨溶液、新制的Cu(OH) 等弱
2
氧化剂氧化D.苯酚有毒,对皮肤有腐蚀性,使用时不慎沾到皮肤上,应立即用水冲洗
6.下列各组中的物质均能发生加成反应的是
A.乙炔和丙醇 B.甲苯和苯乙烯 C.丁二烯和丁烷 D.乙醛和溴乙烷
7.已知 是电离平衡常数,
羧基( ) 硫基( )
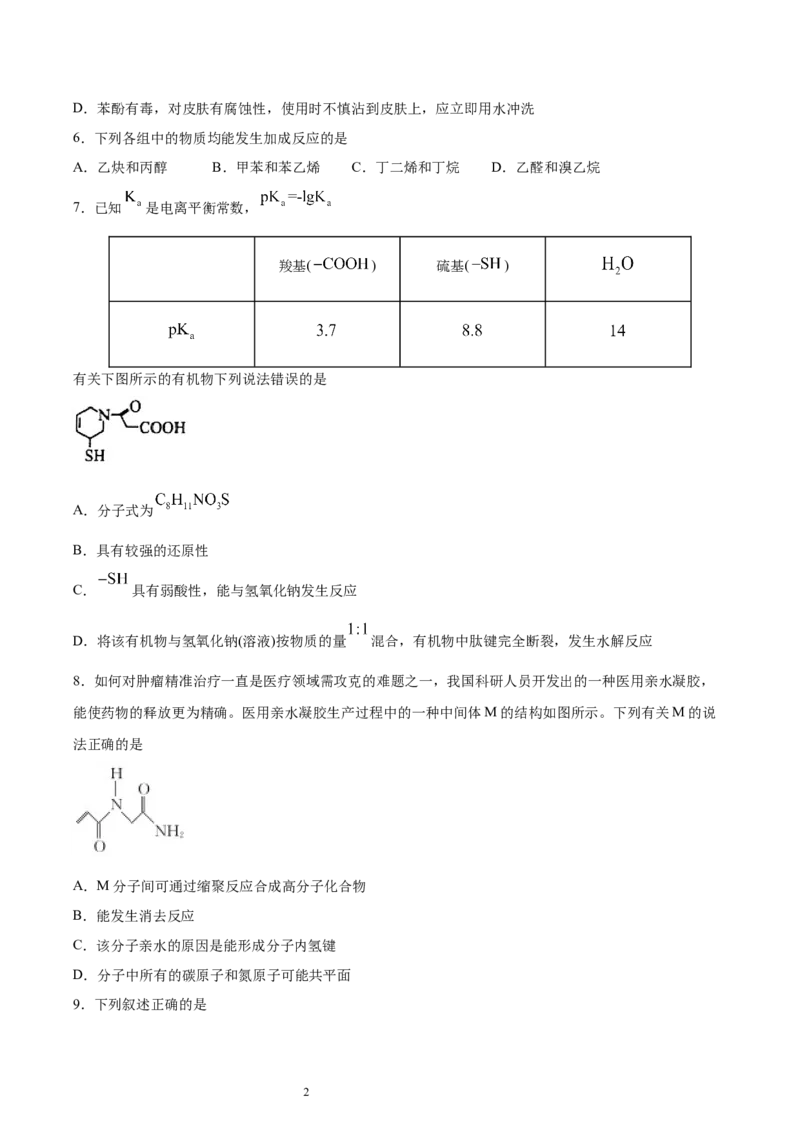
有关下图所示的有机物下列说法错误的是
A.分子式为
B.具有较强的还原性
C. 具有弱酸性,能与氢氧化钠发生反应
D.将该有机物与氢氧化钠(溶液)按物质的量 混合,有机物中肽键完全断裂,发生水解反应
8.如何对肿瘤精准治疗一直是医疗领域需攻克的难题之一,我国科研人员开发出的一种医用亲水凝胶,
能使药物的释放更为精确。医用亲水凝胶生产过程中的一种中间体M的结构如图所示。下列有关M的说
法正确的是
A.M分子间可通过缩聚反应合成高分子化合物
B.能发生消去反应
C.该分子亲水的原因是能形成分子内氢键
D.分子中所有的碳原子和氮原子可能共平面
9.下列叙述正确的是
22
A.甲苯既可使溴的四氯化碳溶液褪色,也可使酸性高锰酸钾溶液褪色
B.C H 的同分异构体有4种,其熔点各不相同
6 14
C.可用新制碱性氢氧化铜悬浊液(可加热)签别乙醇、乙醛和乙酸
D.制取聚氯乙烯的单体的最合理的方法是乙烯与HCl进行加成反应
10.下列变化中,气体被还原的是
A. 固体遇水蒸气变蓝
B.浅绿色的 溶液中通入氯气变黄
C.乙醛蒸气通入酸性 溶液转化为乙酸
D.氨气通入 溶液中产生白色沉淀
11.某物质中可能有甲醇、甲酸、乙醇、甲酸乙酯几种物质中的一种或几种,在鉴定时有下列现象:①有
银镜反应 ②加入新制Cu(OH) 悬浊液,沉淀不溶解,③与含有酚酞的NaOH溶液共热时发现溶液中红色逐
2
渐变浅至无色,下列叙述中正确的是
A.一定有甲酸乙酯和甲酸 B.一定有甲酸乙酯和乙醇
C.一定有甲酸乙酯,可能有甲醇 D.几种物质都一定有
12. 紫罗兰酮是存在于紫罗兰等多种植物中的一种天然香料,它经多步反应可合成维生素 。
下列说法正确的是
A. 紫罗兰酮可使酸性 溶液褪色
B.和 紫罗兰酮相比,中间体X具有更大共轭体系
C.维生素 易溶于 溶液
D. 紫罗兰酮与中间体X互为同分异构体
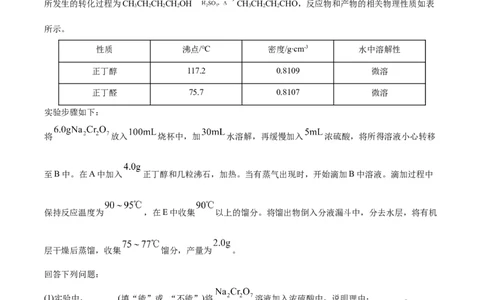
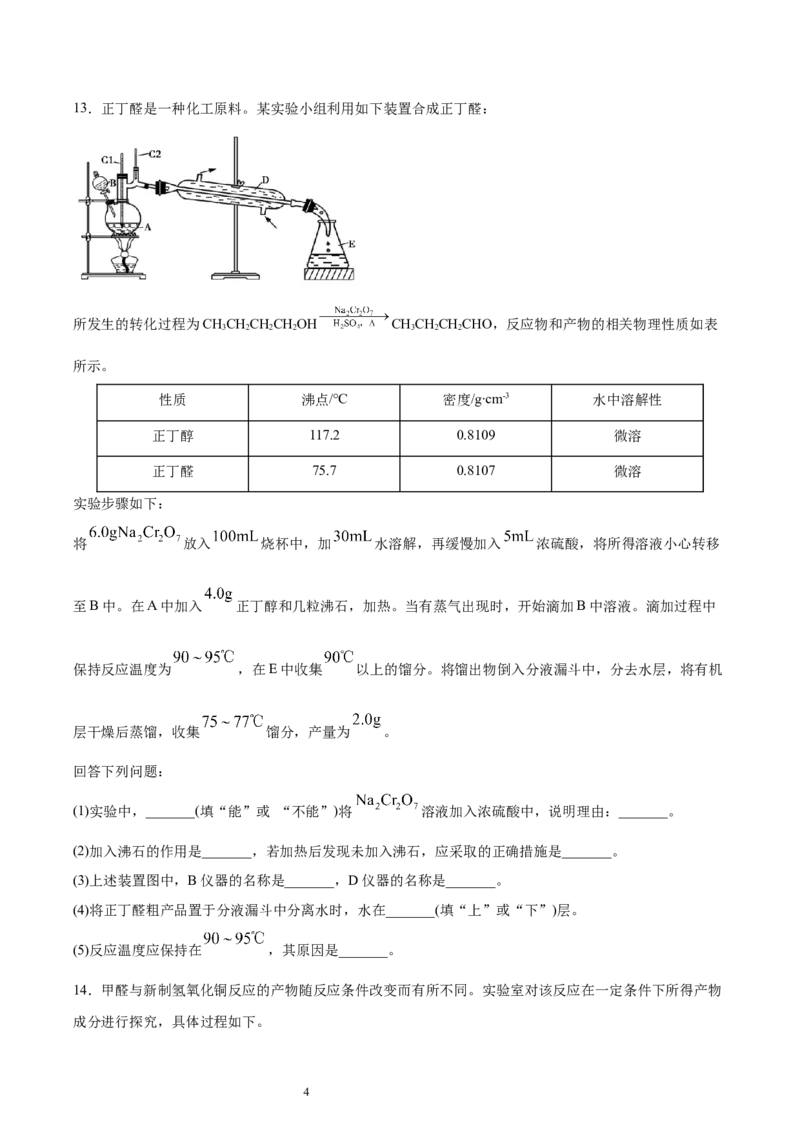
二、实验题13.正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛:
所发生的转化过程为CHCHCHCHOH CHCHCHCHO,反应物和产物的相关物理性质如表
3 2 2 2 3 2 2
所示。
性质 沸点/℃ 密度/g∙cm-3 水中溶解性
正丁醇 117.2 0.8109 微溶
正丁醛 75.7 0.8107 微溶
实验步骤如下:
将 放入 烧杯中,加 水溶解,再缓慢加入 浓硫酸,将所得溶液小心转移
至B中。在A中加入 正丁醇和几粒沸石,加热。当有蒸气出现时,开始滴加B中溶液。滴加过程中
保持反应温度为 ,在E中收集 以上的馏分。将馏出物倒入分液漏斗中,分去水层,将有机
层干燥后蒸馏,收集 馏分,产量为 。
回答下列问题:
(1)实验中,_______(填“能”或 “不能”)将 溶液加入浓硫酸中,说明理由:_______。
(2)加入沸石的作用是_______,若加热后发现未加入沸石,应采取的正确措施是_______。
(3)上述装置图中,B仪器的名称是_______,D仪器的名称是_______。
(4)将正丁醛粗产品置于分液漏斗中分离水时,水在_______(填“上”或“下”)层。
(5)反应温度应保持在 ,其原因是_______。
14.甲醛与新制氢氧化铜反应的产物随反应条件改变而有所不同。实验室对该反应在一定条件下所得产物
成分进行探究,具体过程如下。
44
取一定量的NaOH溶液、CuSO 溶液和甲醛于锥形瓶,控制温度40-50℃回流1h,收集到大量气体X,并
4
有红色沉淀生成。
(1)①“控制温度40-50℃”的常用加热方法是_______。
②气体X能燃烧且完全燃烧产物不会使澄清石灰水变浑浊,说明该气体是_______。
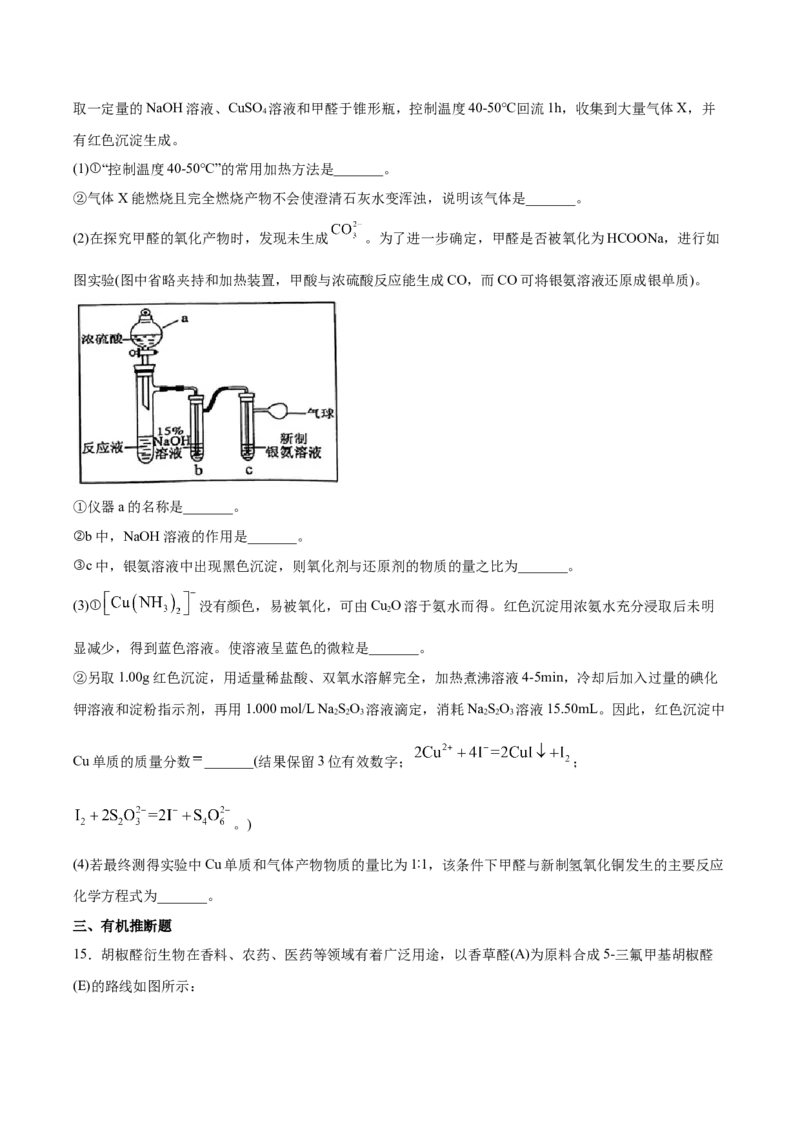
(2)在探究甲醛的氧化产物时,发现未生成 。为了进一步确定,甲醛是否被氧化为HCOONa,进行如
图实验(图中省略夹持和加热装置,甲酸与浓硫酸反应能生成CO,而CO可将银氨溶液还原成银单质)。
①仪器a的名称是_______。
②b中,NaOH溶液的作用是_______。
③c中,银氨溶液中出现黑色沉淀,则氧化剂与还原剂的物质的量之比为_______。
(3)① 没有颜色,易被氧化,可由Cu O溶于氨水而得。红色沉淀用浓氨水充分浸取后未明
2
显减少,得到蓝色溶液。使溶液呈蓝色的微粒是_______。
②另取1.00g红色沉淀,用适量稀盐酸、双氧水溶解完全,加热煮沸溶液4-5min,冷却后加入过量的碘化
钾溶液和淀粉指示剂,再用1.000 mol/L Na SO 溶液滴定,消耗NaSO 溶液15.50mL。因此,红色沉淀中
2 2 3 2 2 3
Cu单质的质量分数 _______(结果保留3位有效数字; ;
。)
(4)若最终测得实验中Cu单质和气体产物物质的量比为1∶1,该条件下甲醛与新制氢氧化铜发生的主要反应
化学方程式为_______。
三、有机推断题
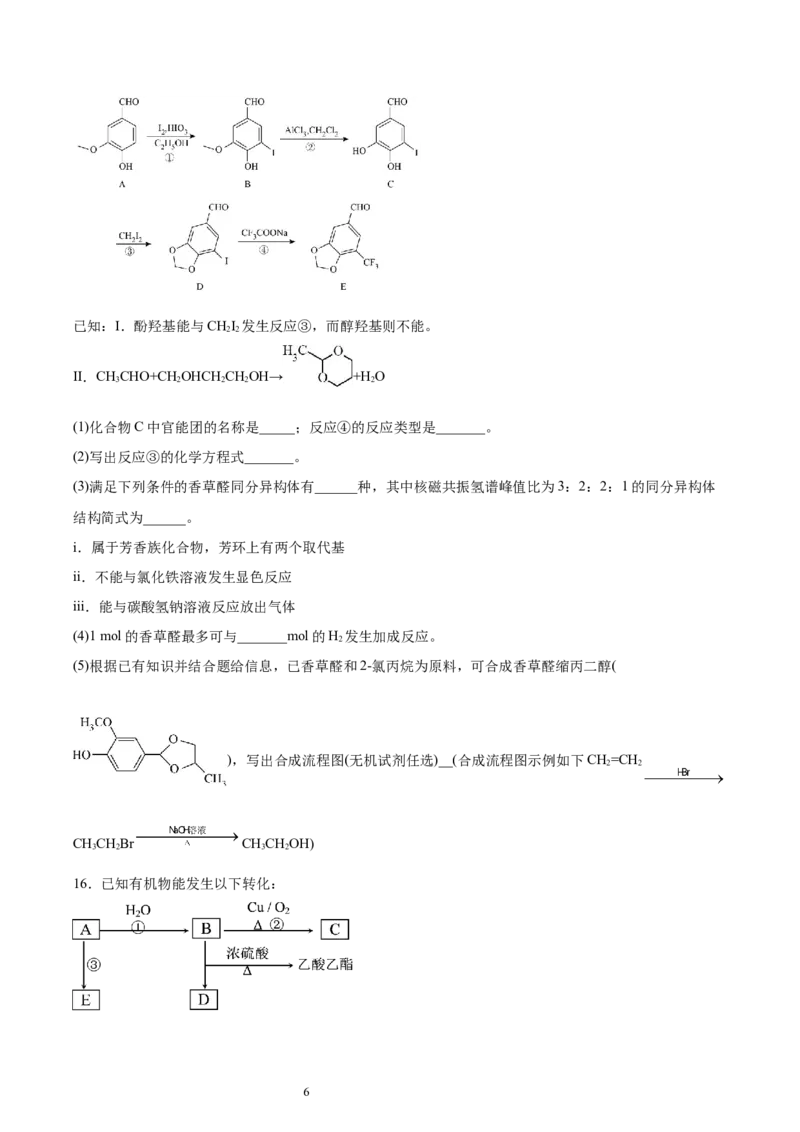
15.胡椒醛衍生物在香料、农药、医药等领域有着广泛用途,以香草醛(A)为原料合成5-三氟甲基胡椒醛
(E)的路线如图所示:已知:I.酚羟基能与CHI 发生反应③,而醇羟基则不能。
2 2
II.CHCHO+CH OHCH CHOH→ +H O
3 2 2 2 2
(1)化合物C中官能团的名称是_____;反应④的反应类型是_______。
(2)写出反应③的化学方程式_______。
(3)满足下列条件的香草醛同分异构体有______种,其中核磁共振氢谱峰值比为3:2:2:1的同分异构体
结构简式为______。
i.属于芳香族化合物,芳环上有两个取代基
ii.不能与氯化铁溶液发生显色反应
iii.能与碳酸氢钠溶液反应放出气体
(4)1 mol的香草醛最多可与_______mol的H 发生加成反应。
2
(5)根据已有知识并结合题给信息,已香草醛和2-氯丙烷为原料,可合成香草醛缩丙二醇(
),写出合成流程图(无机试剂任选)__(合成流程图示例如下CH=CH
2 2
CHCHBr CHCHOH)
3 2 3 2
16.已知有机物能发生以下转化:
66
A的产量通常用来衡量一个国家的石油化工水平。在一定条件下,A可以发生自身加成反应,形成高分子
化合物E。
(1)A分子中碳原子的杂化轨道类型是_______。E的链节的结构简式是_____________。
(2)写出检验C的一个反应的化学方程式____________。反应的类型是_________。
(3)为测定反应①中A的产率,取0.25 mol A 与100 mL H O充分反应后得B溶液。取B溶液25.00 mL,用
2
标准KMnO 溶液(浓度为0.100 0 mol/L)进行滴定。
4
①滴定时盛装KMnO 溶液应选用的仪器是_________。滴定终点的现象是_________。
4
②重复滴定四次,每次消耗KMnO 标准溶液的体积如下表所示。
4
第一次 第二次 第三次 第四次
V(KMnO 溶液)/mL 11.90 12.65 12.50 12.35
4
计算A转化为B的产率为_________
③若滴定前滴定管尖嘴处有气泡,滴定后消失,则测定的结果____________。(填“偏高”、“偏低”或
“不变”)
(4)若完全燃烧0.1 mol某烃,燃烧产物依次通过浓HSO 、浓碱液,实验结束后,称得浓HSO 增重10.8
2 4 2 4
克,浓碱液增重39.6克。若该烃的核磁共振氢谱图上只有两组峰,其峰面积之比为3:1,则它与
KMnO (H+,aq)充分反应后,生成的有机物名称是_________。
4参考答案
1.C
【详解】
A.乙醇醛中含有官能团羟基和醛基,A正确;
B.羟基能与Na反应产生H,醛基能与新制Cu(OH) 反应生成砖红色沉淀Cu O,B正确;
2 2 2
C.Cu作催化剂时,乙醇醛被催化氧化生成乙二醛,官能团种类由2种变成1种,C错误;
D.乙醇醛与乙酸分子式相同,但结构不同,互为同分异构体,D正确;
故答案选C。
2.C
【详解】
A.活性炭具有吸附性,能吸附甲醛,A正确;
B.高锰酸钾溶液能氧化甲醛,B正确;
C.稀盐酸与甲醛不发生反应,不能吸收甲醛,C错误;
D.某些植物可吸收甲醛,D正确;
故选:C。
3.D
【详解】
A.油脂在碱性条件下发生水解反应,所以做银镜反应实验准备洁净试管时,先加氢氧化钠溶液加热几分
钟,油脂水解生成高级脂肪酸钠和甘油,再用蒸馏水冲洗即可得到干净的试管,故A正确;
B.配制银氨溶液时,若向 的稀氨水中滴加 的硝酸银溶液,氨水过量会生成易爆炸的雷酸银(
),因此配制银氨溶液时应将 的稀氨水滴入 的硝酸银溶液中,直至产生的沉淀恰好溶解为
止,故B正确;
C.水浴加热能保证试管受热均匀,且易于控制反应温度,而直接加热时试管受热不均匀,不利于银镜的
生成,故C正确;
D.Ag能够和稀硝酸反应而溶解,因此可用稀硝酸洗去试管内的银镜,不能使用浓盐酸,故D错误;
故选:D。
4.A
【详解】
A.配制氢氧化铜悬浊液时,NaOH溶液要过量,保证溶液呈碱性,需在3mL5%NaOH溶液中滴入3~4滴
11
2%CuSO 溶液,A正确;
4
B.配制银氨溶液时,将稀氨水慢慢滴加到硝酸银溶液中,至产生的沉淀刚好溶解为止,B错误;
C.制取硝基苯时,需要采用水浴加热,温度计的水银球应该插入水浴中,C错误;
D.NaOH具有强烈的腐蚀性,苯酚易溶于酒精,应立即用酒精擦洗,D错误;
综上所述答案为A。
5.B
【详解】
A.液化石油气的主要成分是丙烷和丁烷,是由石油裂化裂解得到,故A错误;
B.卤代烃化学性质较稳定,无毒,具有不燃烧、易挥发、易液化等特性,卤代烃氟利昂曾被广泛用作空
调制冷剂,故B正确,
C.甲醛分子中含有醛基,一定条件下能被银氨溶液、新制氢氧化铜等多种氧化剂氧化,故C错误;
D.苯酚易溶于乙醇等有机溶剂,苯酚有毒,对皮肤有强烈的腐蚀作用,如果不慎沾到皮肤上应立即用酒
精洗涤,故D错误;
故选:B。
6.B
【详解】
A.丙醇分子不能发生加成反应,故A不选;
B.甲苯和苯乙烯都可以和氢气发生加成反应,故B选;
C.丁烷不能发生加成反应,故C不选;
D.溴乙烷不能发生加成反应,故D不选;
故选B。
7.D
【详解】
A.根据结构简式可知分子中含有8个C、11个H、1个N、3个O和1个S,分子式为 ,选项
A正确;
B.分子中含有硫基( )和碳碳双键,容易被氧化,故具有较强的还原性,选项B正确;
C.根据硫基( )的 =8.8,小于水的 ,大于醋酸的 ,则 具有弱酸性,能与氢氧化钠
发生反应,选项C正确;
D.将该有机物与氢氧化钠(溶液)按物质的量1∶2混合,有机物中肽键完全断裂,发生水解反应,且生成乙
22
二酸钠,选项D错误;
答案选D。
8.D
【详解】
A.该分子结构中含有碳碳双键,只能通过加聚反应形成高分子化合物,故A错误;
B.M不含醇羟基也不是卤代烃,不能发生消去反应,故B错误;
C.该分子亲水的原因是分子中含有-NH ,-NH 是亲水基,能够与水分子之间形成氢键,增加了分子之间
2 2
的吸引力,因此该物质易溶于水,C错误;
D.分子中含有饱和C原子与不饱和C原子,含有碳碳双键的C原子与其相连的原子在同一平面上,两个
平面共直线,可以在同一个平面上,因此分子中所有碳原子和氮原子可能共平面,D正确;
故选D。
9.C
【详解】
A.甲苯不含碳碳双键,与溴的四氯化碳溶液不反应,故A错误;
B.己烷C H 的同分异构体有:CH(CH)CH、(CH)CHCH CHCH、(CHCH)CHCH 、
6 14 3 2 4 3 3 2 2 2 3 3 2 2 3
(CH)CCHCH、(CH)CHCH(CH ) 五种,故B错误;
3 3 2 3 3 2 3 2
C.加入新制Cu(OH) 悬浊液,乙醇不反应,乙醛在加热时生成砖红色沉淀,乙酸和氢氧化铜发生中和反
2
应,氢氧化铜溶解,现象不同,所以可以鉴别,故C正确;
D.制取聚氯乙烯的单体,可用乙炔与氯化氢发生加成反应,乙烯与氯化氢反应生成氯乙烷,故D错误。
答案选C。
10.B
【详解】
A.水蒸气使CuSO 固体变蓝,无元素化合价发生变化,故A不选;
4
B.氯气使浅绿色FeCl 溶液变黄,Cl元素的化合价降低,气体被还原,故B选;
2
D.乙醛转化为乙酸C的化合价升高,气体被氧化,故 C不选;
D.氨气使AlCl 溶液产生白色沉淀,无元素化合价发生变化,故D不选;
3
故选:B。
11.C
【详解】
有银镜反应,说明含有醛基。加入新制Cu(OH) 悬浊液,沉淀不溶解,说明没有羧酸,即不存在甲酸。与
2
含有酚酞的NaOH溶液共热时发现溶液中红色逐渐变浅至无色,这说明含有酯基,即一点含有甲酸乙酯。
33
由于甲酸乙酯也能发生银镜反应,所以正确的答案选C。
12.A
【详解】
A.β紫罗兰酮含有碳碳双键,可使酸性KMnO 溶液褪色,故A正确;
4
B.除去参与成共价键的电子数,剩余电子均参与形成共轭,β 紫罗兰酮具有更大共轭体系,故B错误;
C.维生素A 含有醇羟基,所以不易溶于NaOH溶液,故C错误;
1
D.β紫罗兰酮与中间体X所含C原子数不同,不是同分异构体,故D错误;
故选A。
13.不能 易迸溅 防止暴沸 冷却后补加 分液漏斗 直形冷凝管 下 既可保证正丁
醛及时蒸出,又可尽量避免其被进一步氧化
【详解】
(1)因为浓硫酸的密度大,将NaCr O 溶液加到浓硫酸中,容易发生迸溅,所以实验中不能将 溶
2 2 7
液加入浓硫酸中;
(2)反应需要加热,加入沸石的作用是防止暴沸,若加热后发现未加沸石,应该冷却后补加;
(3)根据仪器构造可知B仪器的名称是分液漏斗,D仪器的名称直形冷凝管;
(4)正丁醛密度为0.8017 g•cm-3,小于水的密度,故分层后水层在下方;
(5)根据题目所给反应物和产物的沸点数据可知,反应温度保持在90~95℃,既可保证正丁醛及时蒸出,又
可尽量避免其被进一步氧化。
14.水浴加热 H 分液漏斗 除去CO中混有的HCOOH蒸汽 2∶1
2
92.8%
【详解】
(1)①“控制温度40-50℃”的常用加热方法是水浴加热,故答案为:水浴加热;
②结合反应中涉及的元素,能够燃烧的气体可能为氢气和CO,气体X能燃烧且完全燃烧产物不会使澄清
石灰水变浑浊,说明该气体不是CO,则X为氢气,故答案为:H;
2
(2)①根据图示,仪器a是分液漏斗,故答案为:分液漏斗;
②甲酸易挥发,生成的气体中会混有HCOOH蒸汽,因此b中NaOH溶液的作用是除去CO中混有的
HCOOH蒸汽,故答案为:除去CO中混有的HCOOH蒸汽;
③c中,银氨溶液中出现黑色沉淀,是CO将银氨溶液还原成的银单质,反应中氧化剂是 ,Ag
44
的化合价由+1价变成0价,还原剂是CO,C的化合价由+2价变成+4价,根据化合价升降守恒,氧化剂与
还原剂的物质的量之比为(4-2)∶(1-0)=2∶1,故答案为:2∶1;
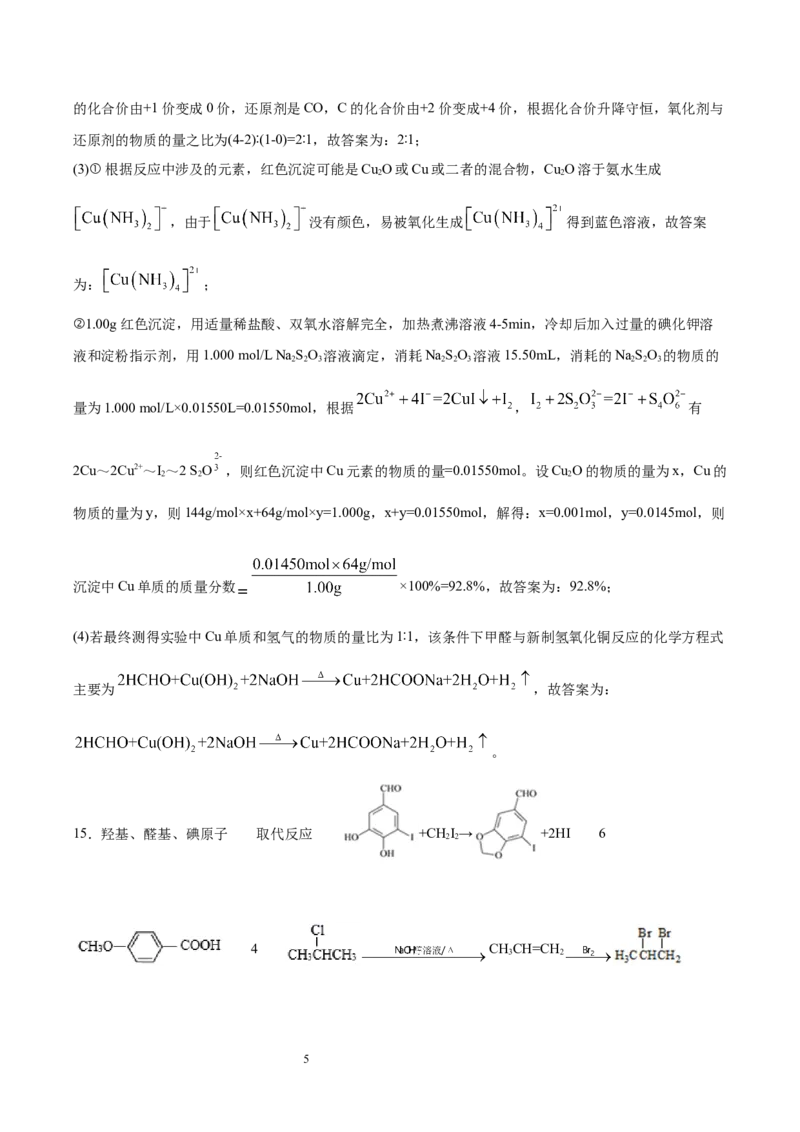
(3)①根据反应中涉及的元素,红色沉淀可能是Cu O或Cu或二者的混合物,Cu O溶于氨水生成
2 2
,由于 没有颜色,易被氧化生成 得到蓝色溶液,故答案
为: ;
②1.00g红色沉淀,用适量稀盐酸、双氧水溶解完全,加热煮沸溶液4-5min,冷却后加入过量的碘化钾溶
液和淀粉指示剂,用1.000 mol/L Na SO 溶液滴定,消耗NaSO 溶液15.50mL,消耗的NaSO 的物质的
2 2 3 2 2 3 2 2 3
量为1.000 mol/L×0.01550L=0.01550mol,根据 , 有
2Cu~2Cu2+~I~2 S O ,则红色沉淀中Cu元素的物质的量=0.01550mol。设Cu O的物质的量为x,Cu的
2 2 2
物质的量为y,则144g/mol×x+64g/mol×y=1.000g,x+y=0.01550mol,解得:x=0.001mol,y=0.0145mol,则
沉淀中Cu单质的质量分数 ×100%=92.8%,故答案为:92.8%;
(4)若最终测得实验中Cu单质和氢气的物质的量比为1∶1,该条件下甲醛与新制氢氧化铜反应的化学方程式
主要为 ,故答案为:
。
15.羟基、醛基、碘原子 取代反应 +CH I→ +2HI 6
2 2
4 CHCH=CH
3 2
55
【详解】
(1)化合物C结构简式是 ,分子中含有的官能团是-OH、-I、-CHO,则含有的官能团名称为羟
基、醛基、碘原子;
反应④是 与CFCOONa发生取代反应产生 和ICOONa,故反应④的类型是取代反
3
应;
(2)反应③是 与CHI 发生取代反应产生 、HI,该反应的化学方程式为:
2 2
+CH I→ +HI;
2 2
(3)香草醛为 ,分子式是C HO,其同分异构体符合条件:i.属于芳香族化合物,芳环上有两
8 8 3
个取代基,说明有2个与苯环连接的取代基;ii.不能与氯化铁溶液发生显色反应,说明物质中不含酚羟
基;iii.能与碳酸氢钠溶液反应放出气体,说明分子中含有-COOH,则符合条件的同分异构体结构简式是
、 、 、 、 、
66
,故符合条件的同分异构体共有6种;
其中核磁共振氢谱峰值比为3:2:2:1的同分异构体结构简式为 ;
(4)香草醛分子中含有苯环及醛基都可以与H 发生加成反应,因此1 mol的香草醛最多可与4 mol H 发生加
2 2
成反应;
(5) 与NaOH的乙醇溶液共热,发生消去反应产生CH=CH-CH,CH=CH-CH 与Br 发生加成
2 3 2 3 2
反应产生CHBr-CHBr-CH ,CHBr-CHBr-CH 与NaOH溶液共热,发生取代反应产生 ,
2 3 2 3
与 反应产生 ,故合成路线为
CHCH=CH
3 2
。
16.sp2 —CH —CH— CH CHO+2Ag(NH )OH CHCOONH+2Ag↓+3NH+H O或
2 2 3 3 2 3 4 3 2
77
CHCHO+2Cu(OH) +NaOH CHCOONa+Cu O↓+3HO 氧化反应 酸式滴定管 滴入最后
3 2 3 2 2
一滴KMnO 溶液后,溶液由无色恰好变为浅红色,且30s内不褪色 2.5 % 偏高 间苯三甲酸
4
【详解】
根据上述分析可知:A是CH=CH ,B是CHCHOH,C是CHCHO,D是CHCOOH,E是
2 2 3 2 3 3
。
(1)A是乙烯,分子中C原子形成了共价双键,碳原子杂化轨道类型是sp2;E是 ,其最小重
复单元即链节是—CH—CH—;
2 2
(2)C是CHCHO,官能团是-CHO,该物质具有强的还原性,可利用银镜反应检验醛基的存在,反应方程
3
式为:CHCHO+2Ag(NH )OH CHCOONH+2Ag↓+3NH+H O;也可以根据其能够与新制Cu(OH)
3 3 2 3 4 3 2 2
悬浊液混合加热产生砖红色沉淀检验,方程式为:CHCHO+2Cu(OH) +NaOH
3 2
CHCOONa+Cu O↓+3HO,发生的反应为氧化反应;
3 2 2
(3)①KMnO 溶液具有强的氧化性,会腐蚀碱式滴定管的橡胶管,因此应该盛放在酸式滴定管中,KMnO
4 4
溶液被乙醇还原产生Mn2+,乙醇被氧化变为乙酸,故当反应达到滴定终点时,溶液恰好由无色变为浅红
色,且30 s内不再褪色,说明此时反应达到滴定终点;
②100 mL水质量大约是100 g,根据反应方程式:CH=CH +H O CHCHOH,可知0.25 mol
2 2 2 3 2
乙烯反应消耗0.25 mol HO,其质量是4.5 g<100 g,说明水过量,若其完全转化为乙醇,则理论上乙醇的
2
物质的量是0.25 mol,忽略混合时溶液体积变化,则反应后得到溶液体积是100 mL。根据实验数据可知:
第一次实验数据偏差较大,可舍去,则25 mL溶液平衡消耗KMnO 溶液的体积是V(KMnO)=
4 4
mL=12.50 mL,KMnO 的物质的量n(KMnO)=c·V=0.100 0 mol/L×12.50 mL×10-3
4 4
L/mL=1.250 ×10-3 mol,根据二者反应方程式:5CHCHOH+4 +12H+=5CH COOH+4Mn2++11H O,
3 2 3 2
88
可知其反应消耗乙醇的物质的量n(CHCHOH)= n(KMnO)= ×1.250 ×10-3 mol=1.5625 ×10-3 mol,则乙
3 2 4
烯转化为乙醇的转化率为: ×100%=2.5%;
③若滴定前滴定管尖嘴处有气泡,滴定后消失,则消耗标准KMnO 溶液体积偏大,以此为标准计算的乙
4
醇的结果就会偏高;
(4)浓硫酸增重10.8 g为HO的质量,浓碱液增重39.6g为CO 的质量,则n(H O)= =0.6
2 2 2
mol,n(H)=2n(H O)=1.2 mol,则1 mol烃中含有12 mol H原子;n(CO)= =0.9 mol,
2 2
n(C)=n(CO)=0.9 mol,则1 mol烃中含有9 mol C原子,故该烃分子式是C H ,该物质属于苯的同系物;
2 9 12
若该烃的核磁共振氢谱图上只有两组峰,其峰面积之比为3:1,说明分子中有2种H原子,个数比是3:
1,该物质是间三甲苯,其结构简式是 。它与酸性KMnO 溶液反应,甲基-CH 被氧化变为
4 3
羧基-COOH,则充分反应后,生成的有机物是 ,名称为间苯三甲酸。
9