文档内容
第三章 烃的衍生物
第三节 醛 酮
学习导航 1.通过醛基中原子成键情况的分析,了解醛类的结构特点,理解乙醛的化学性质与醛基的
关系,学会醛基的检验方法。
2.了解甲醛对环境和健康的影响,关注有机化合物安全使用的问题。
教学过程 一、乙醛的性质
1.醛的概念及结构特点
醛是由烃基(或氢原子)与醛基相连而构成的化合物。醛类官能团的结构简式是—CHO,饱
和一元醛的通式为C H O(n≥1)或C H CHO。
n 2n n 2n+1
2.乙醛的结构与物理性质
3.乙醛的化学性质
(1)加成反应
①催化加氢(还原反应)
乙醛中的碳氧双键和烯烃中的碳碳双键性质类似,也能与氢气发生加成反应,化学方程
式为
CHCHO+H――→CHCHOH。
3 2 3 2
②与HCN加成
在醛基的碳氧双键中,由于氧原子的电负性较大,碳氧双键中的电子偏向氧原子,使氧
原子带部分负电荷,碳原子带部分正电荷,从而使醛基具有较强的极性。乙醛能和一些
极性试剂例如氰化氢(HCN)发生加成反应: +H—CN―→
(2-羟基丙腈)。
(2)氧化反应
①可燃性
乙醛燃烧的化学方程式:2CHCHO+5O――→4CO+4HO。
3 2 2 2
②催化氧化
乙醛在一定温度和催化剂作用下,能被氧气氧化为乙酸的化学方程式:
+O――→ 。
2
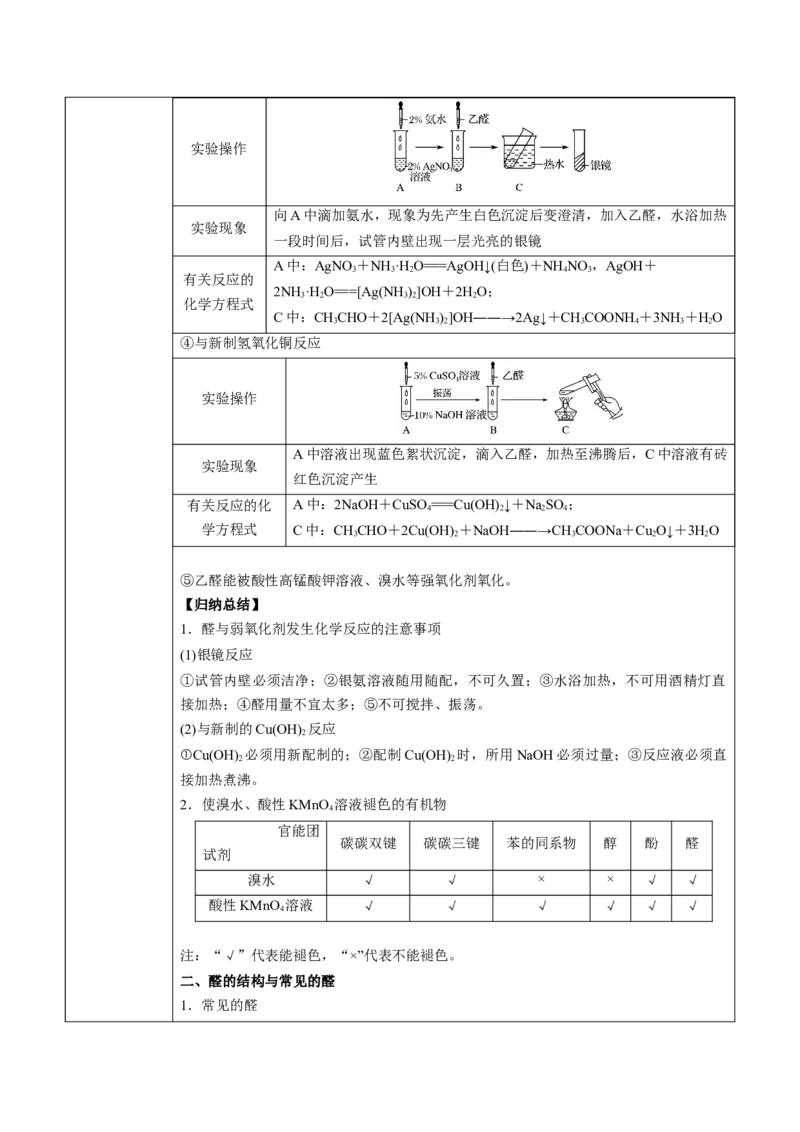
③与银氨溶液反应实验操作
向A中滴加氨水,现象为先产生白色沉淀后变澄清,加入乙醛,水浴加热
实验现象
一段时间后,试管内壁出现一层光亮的银镜
A中:AgNO+NH ·H O===AgOH↓(白色)+NH NO ,AgOH+
3 3 2 4 3
有关反应的
2NH ·H O===[Ag(NH )]OH+2HO;
3 2 3 2 2
化学方程式
C中:CHCHO+2[Ag(NH)]OH――→2Ag↓+CHCOONH+3NH +HO
3 3 2 3 4 3 2
④与新制氢氧化铜反应
实验操作
A中溶液出现蓝色絮状沉淀,滴入乙醛,加热至沸腾后,C中溶液有砖
实验现象
红色沉淀产生
有关反应的化 A中:2NaOH+CuSO ===Cu(OH) ↓+NaSO ;
4 2 2 4
学方程式 C中:CHCHO+2Cu(OH) +NaOH――→CHCOONa+Cu O↓+3HO
3 2 3 2 2
⑤乙醛能被酸性高锰酸钾溶液、溴水等强氧化剂氧化。
【归纳总结】
1.醛与弱氧化剂发生化学反应的注意事项
(1)银镜反应
①试管内壁必须洁净;②银氨溶液随用随配,不可久置;③水浴加热,不可用酒精灯直
接加热;④醛用量不宜太多;⑤不可搅拌、振荡。
(2)与新制的Cu(OH) 反应
2
①Cu(OH) 必须用新配制的;②配制Cu(OH) 时,所用NaOH必须过量;③反应液必须直
2 2
接加热煮沸。
2.使溴水、酸性KMnO 溶液褪色的有机物
4
官能团
碳碳双键 碳碳三键 苯的同系物 醇 酚 醛
试剂
溴水 √ √ × × √ √
酸性KMnO 溶液 √ √ √ √ √ √
4
注:“√”代表能褪色,“×”代表不能褪色。
二、醛的结构与常见的醛
1.常见的醛(1)甲醛:又名蚁醛,是结构最简单的醛,结构简式为 HCHO。通常状况下是一种无色有
强烈刺激性气味的气体,易溶于水。它的水溶液又称福尔马林,具有杀菌、防腐性能,
可用于消毒和制作生物标本。
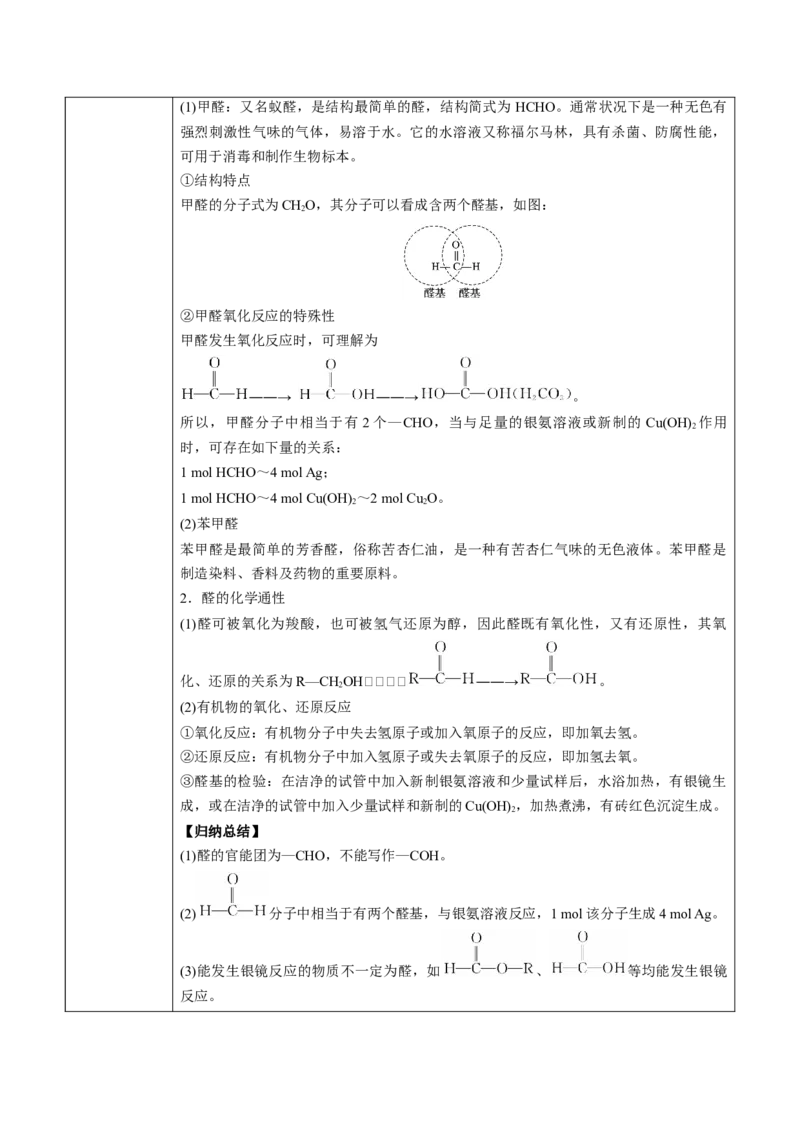
①结构特点
甲醛的分子式为CHO,其分子可以看成含两个醛基,如图:
2
②甲醛氧化反应的特殊性
甲醛发生氧化反应时,可理解为
――→ ――→ 。
所以,甲醛分子中相当于有 2个—CHO,当与足量的银氨溶液或新制的 Cu(OH) 作用
2
时,可存在如下量的关系:
1 mol HCHO~4 mol Ag;
1 mol HCHO~4 mol Cu(OH)~2 mol Cu O。
2 2
(2)苯甲醛
苯甲醛是最简单的芳香醛,俗称苦杏仁油,是一种有苦杏仁气味的无色液体。苯甲醛是
制造染料、香料及药物的重要原料。
2.醛的化学通性
(1)醛可被氧化为羧酸,也可被氢气还原为醇,因此醛既有氧化性,又有还原性,其氧
化、还原的关系为R—CHOH ――→ 。
2
(2)有机物的氧化、还原反应
①氧化反应:有机物分子中失去氢原子或加入氧原子的反应,即加氧去氢。
②还原反应:有机物分子中加入氢原子或失去氧原子的反应,即加氢去氧。
③醛基的检验:在洁净的试管中加入新制银氨溶液和少量试样后,水浴加热,有银镜生
成,或在洁净的试管中加入少量试样和新制的Cu(OH) ,加热煮沸,有砖红色沉淀生成。
2
【归纳总结】
(1)醛的官能团为—CHO,不能写作—COH。
(2) 分子中相当于有两个醛基,与银氨溶液反应,1 mol该分子生成4 mol Ag。
(3)能发生银镜反应的物质不一定为醛,如 、 等均能发生银镜
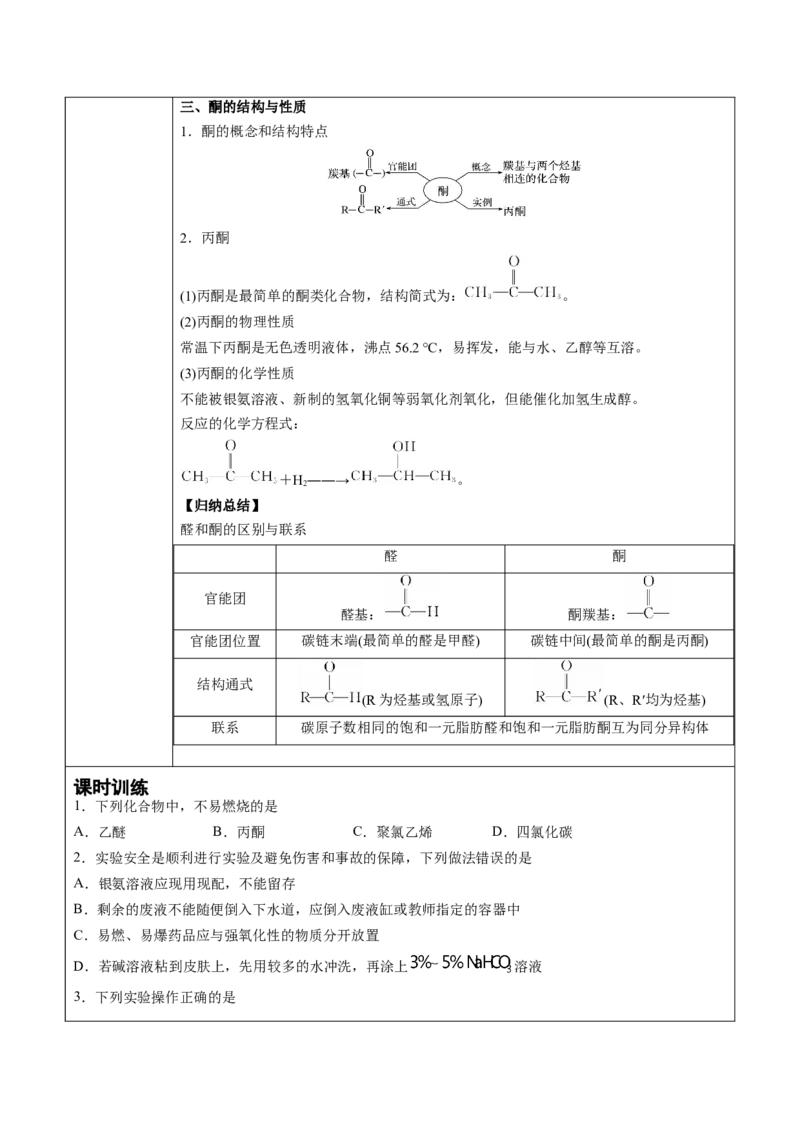
反应。三、酮的结构与性质
1.酮的概念和结构特点
2.丙酮
(1)丙酮是最简单的酮类化合物,结构简式为: 。
(2)丙酮的物理性质
常温下丙酮是无色透明液体,沸点56.2 ℃,易挥发,能与水、乙醇等互溶。
(3)丙酮的化学性质
不能被银氨溶液、新制的氢氧化铜等弱氧化剂氧化,但能催化加氢生成醇。
反应的化学方程式:
+H――→ 。
2
【归纳总结】
醛和酮的区别与联系
醛 酮
官能团
醛基: 酮羰基:
官能团位置 碳链末端(最简单的醛是甲醛) 碳链中间(最简单的酮是丙酮)
结构通式
(R为烃基或氢原子) (R、R′均为烃基)
联系 碳原子数相同的饱和一元脂肪醛和饱和一元脂肪酮互为同分异构体
课时训练
1.下列化合物中,不易燃烧的是
A.乙醚 B.丙酮 C.聚氯乙烯 D.四氯化碳
2.实验安全是顺利进行实验及避免伤害和事故的保障,下列做法错误的是
A.银氨溶液应现用现配,不能留存
B.剩余的废液不能随便倒入下水道,应倒入废液缸或教师指定的容器中
C.易燃、易爆药品应与强氧化性的物质分开放置
D.若碱溶液粘到皮肤上,先用较多的水冲洗,再涂上 溶液
3.下列实验操作正确的是A.配制氢氧化铜悬浊液时,需在3mL5%NaOH溶液中滴入3~4滴2%CuSO 溶液
4
B.配制银氨溶液时,需将2%的硝酸银溶液逐滴加入到2%的稀氨水
C.实验室制备硝基苯时,温度计插入反应溶液中,并控制温度在50~60℃之间
D.苯酚对皮肤有腐蚀性,若粘在皮肤上,要用氢氧化钠溶液来洗
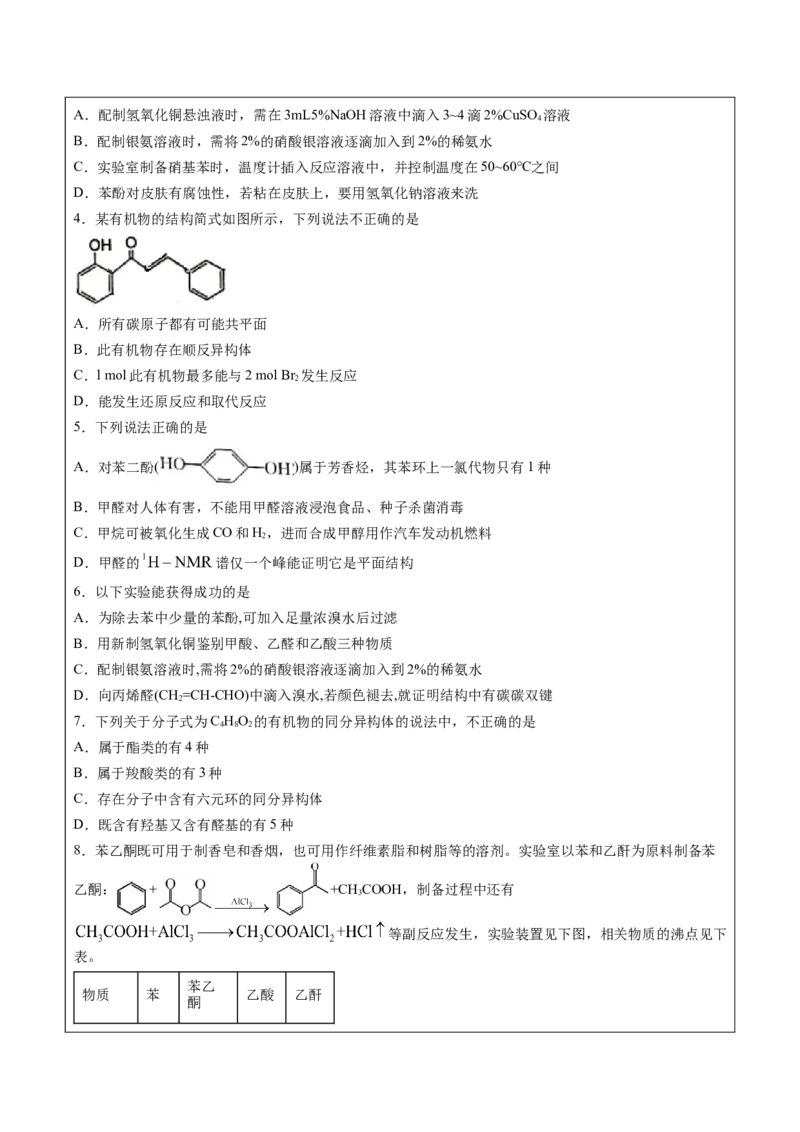
4.某有机物的结构简式如图所示,下列说法不正确的是
A.所有碳原子都有可能共平面
B.此有机物存在顺反异构体
C.l mol此有机物最多能与2 mol Br 发生反应
2
D.能发生还原反应和取代反应
5.下列说法正确的是
A.对苯二酚( )属于芳香烃,其苯环上一氯代物只有1种
B.甲醛对人体有害,不能用甲醛溶液浸泡食品、种子杀菌消毒
C.甲烷可被氧化生成CO和H,进而合成甲醇用作汽车发动机燃料
2
D.甲醛的 谱仅一个峰能证明它是平面结构
6.以下实验能获得成功的是
A.为除去苯中少量的苯酚,可加入足量浓溴水后过滤
B.用新制氢氧化铜鉴别甲酸、乙醛和乙酸三种物质
C.配制银氨溶液时,需将2%的硝酸银溶液逐滴加入到2%的稀氨水
D.向丙烯醛(CH=CH-CHO)中滴入溴水,若颜色褪去,就证明结构中有碳碳双键
2
7.下列关于分子式为C HO 的有机物的同分异构体的说法中,不正确的是
4 8 2
A.属于酯类的有4种
B.属于羧酸类的有3种
C.存在分子中含有六元环的同分异构体
D.既含有羟基又含有醛基的有5种
8.苯乙酮既可用于制香皂和香烟,也可用作纤维素脂和树脂等的溶剂。实验室以苯和乙酐为原料制备苯
乙酮: + +CH COOH,制备过程中还有
3
等副反应发生,实验装置见下图,相关物质的沸点见下
表。
苯乙
物质 苯 乙酸 乙酐
酮沸点/℃ 80.1 202 117.9 139.8
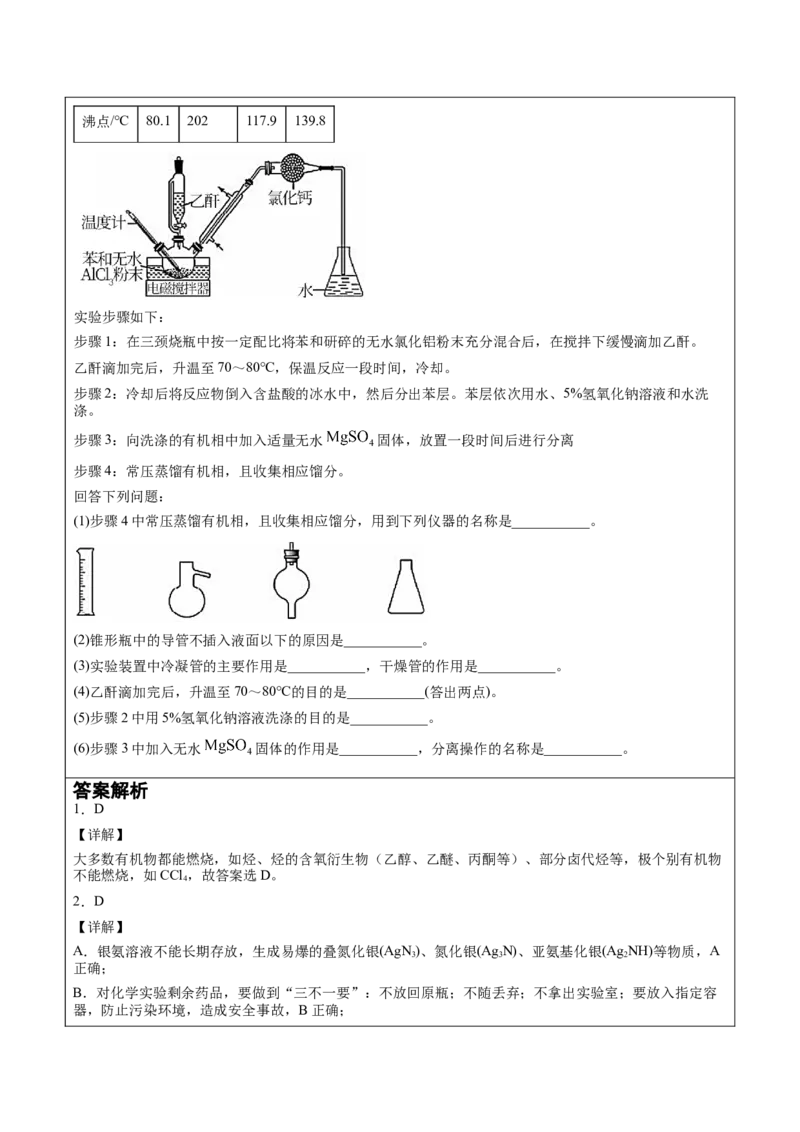
实验步骤如下:
步骤1:在三颈烧瓶中按一定配比将苯和研碎的无水氯化铝粉末充分混合后,在搅拌下缓慢滴加乙酐。
乙酐滴加完后,升温至70~80℃,保温反应一段时间,冷却。
步骤2:冷却后将反应物倒入含盐酸的冰水中,然后分出苯层。苯层依次用水、5%氢氧化钠溶液和水洗
涤。
步骤3:向洗涤的有机相中加入适量无水 固体,放置一段时间后进行分离
步骤4:常压蒸馏有机相,且收集相应馏分。
回答下列问题:
(1)步骤4中常压蒸馏有机相,且收集相应馏分,用到下列仪器的名称是___________。
(2)锥形瓶中的导管不插入液面以下的原因是___________。
(3)实验装置中冷凝管的主要作用是___________,干燥管的作用是___________。
(4)乙酐滴加完后,升温至70~80℃的目的是___________(答出两点)。
(5)步骤2中用5%氢氧化钠溶液洗涤的目的是___________。
(6)步骤3中加入无水 固体的作用是___________,分离操作的名称是___________。
答案解析
1.D
【详解】
大多数有机物都能燃烧,如烃、烃的含氧衍生物(乙醇、乙醚、丙酮等)、部分卤代烃等,极个别有机物
不能燃烧,如CCl ,故答案选D。
4
2.D
【详解】
A.银氨溶液不能长期存放,生成易爆的叠氮化银(AgN )、氮化银(Ag N)、亚氨基化银(Ag NH)等物质,A
3 3 2
正确;
B.对化学实验剩余药品,要做到“三不一要”:不放回原瓶;不随丢弃;不拿出实验室;要放入指定容
器,防止污染环境,造成安全事故,B正确;C.易燃、易爆药品与有强氧化性的物质易发生反应而发生燃烧或爆炸,要分开放置并远离火源,C正
确;
D.若碱溶液粘到皮肤上,先用较多的水冲洗,再涂上硼酸溶液中和残余的碱溶液,D错误;
故答案为:D。
3.A
【详解】
A.配制氢氧化铜悬浊液时,NaOH溶液要过量,保证溶液呈碱性,需在3mL5%NaOH溶液中滴入3~4滴
2%CuSO 溶液,A正确;
4
B.配制银氨溶液时,将稀氨水慢慢滴加到硝酸银溶液中,至产生的沉淀刚好溶解为止,B错误;
C.制取硝基苯时,需要采用水浴加热,温度计的水银球应该插入水浴中,C错误;
D.NaOH具有强烈的腐蚀性,苯酚易溶于酒精,应立即用酒精擦洗,D错误;
综上所述答案为A。
4.C
【详解】
A.苯、碳碳双键和羰基是平面结构,故所有碳原子都有可能共平面,A正确;
B. 碳碳双键上,每个碳原子连有不同基团时存在顺反异构,则此有机物存在顺反异构体,B正确;
C. 酚可以和溴水发生取代反应、碳碳双键可以和溴发生加成反应,l mol此有机物最多能与3 mol Br 发
2
生反应,C不正确;
D.含羰基、碳碳双键和苯环均可与氢气发生还原反应、含酚羟基可以发生取代反应,D正确;
答案选C。
5.C
【详解】
A. 对苯二酚( )属于烃的衍生物,其苯环上一氯代物只有1种,故A错误;
B. 甲醛对人体有害,不能用甲醛溶液浸泡食品,但可以浸泡种子杀菌消毒,故B错误;
C. 甲烷可被氧化生成CO和H,CH (g)+ O (g)=CO(g)+2H (g),进而合成甲醇用作汽车发动
2 4 2 2
机燃料,CO+2H CHOH,故C正确;
2 3
D. 甲醛的 谱仅一个峰只能证明两个氢对称,不能证明它是平面结构,故D错误;
故选C。
6.B
【详解】
A.溴、三溴苯酚均易溶于苯,引入新杂质,不能除杂,应选NaOH溶液、分液,故A错误;
B.加入新制Cu(OH) 悬浊液,乙醇不反应,乙醛在加热时生成砖红色沉淀,乙酸和氢氧化铜发生中和反
2
应,氢氧化铜溶解,现象不同,所以可以鉴别,故B正确;
C.试剂加入顺序错误,应键氨水滴加到硝酸银溶液中,当沉淀恰好溶解时停止滴加氨水,故C错误;
D.双键、-CHO均能被高锰酸钾氧化,则应先利用银氨溶液排除-CHO的干扰,再利用高锰酸钾检验双键,故D错误。
答案选B。
7.B
【详解】
A.若C HO 为酯,那么可以分成几种情况,①甲酸与丙醇形成的酯,有2种同分异构体,②乙酸与乙醇
4 8 2
形成的酯,有1种同分异构体,③丙酸和甲醇形成的酯,有1种同分异构体,所以属于酯类的同分异构体
有4种,A正确;
B.若C HO 为羧酸,则有可能是丁酸或者2-甲基丙酸,共两种同分异构体,B错误;
4 8 2
C.分子中4个碳与2个氧可形成六元环,C正确;
D.将分子式为C HO 的有机物写成既含羟基又含醛基的有机物,能写出5种,可以是2-羟基丁醛、3-羟
4 8 2
基丁醛、4-羟基丁醛、2-甲基-2-羟基丙醛、2-甲基-3羟基丙醛,D正确;
故选B。
8.蒸馏烧瓶、锥形瓶 反应产生极易溶于水的 ,若导管插入液面以下会产生倒吸 冷凝回流
防止外界水蒸气进入三颈烧瓶中 提高反应速率,缩短反应时间、防止苯大量挥发 洗去酸等酸性物
质 除去有机相中的水或干燥有机相 过滤
【详解】
(1)常压蒸馏要用蒸馏烧瓶、锥形瓶(收集馏出物),故答案为:蒸馏烧瓶、锥形瓶。
(2)因反应生成的CHCOOH与AlCl 在加热条件下反应产生极易溶于水的 ,若导管插入液面以下会产
3 3
生倒吸,故答案为:反应产生极易溶于水的 ,若导管插入液面以下会产生倒吸。
(3)冷凝管的作用是冷凝回流,充分利用笨和乙酐;该反应要保持无水,所以干燥管的作用是防止外界水蒸
气进入三颈烧瓶中,故答案为:冷凝回流、防止外界水蒸气进入三颈烧瓶中。
(4) 乙酐滴加完后,升温至70~80℃的目的是:提高反应速率,缩短反应时间、防止苯大量挥发。
(5) 步骤2中的笨层含有醋酸等酸性物质,即用5%氢氧化钠溶液洗涤的目的是:洗去酸等酸性物质。
(6) 无水 可以用来除去有机相中的水或干燥有机相,有机相是液体,硫酸镁吸水后还是固体,所
以用过滤的方法分离,故答案为:除去有机相中的水或干燥有机相、过滤。