文档内容
第三章 烃的衍生物
第四节 羧酸 羧酸衍生物
第 1 课时 羧酸
学习导航 1. 能从羧基的成键方式的角度,了解羧酸的结构特点和分类,理解羧酸的化学性质及官能
团与反应类型之间的关系。
2.能根据酯化反应的原理优化乙酸乙酯制备的方案,提高乙酸乙酯的产率。
教学过程 一、羧酸的结构与分类
1.羧酸的组成和结构
(1)羧酸:由烃基(或氢原子)与羧基相连而构成的有机化合物。官能团为—COOH 或
。
(2)通式:一元羧酸的通式为R—COOH,饱和一元羧酸的通式:C H O 或C H COOH。
n 2n 2 n 2n+1
2.羧酸的分类
(1)按分子中烃基的结构分类
羧酸
(2)按分子中羧基的个数分类
羧酸
(3)按分子中烃基所含碳原子数多少分类
羧酸
3.常见的羧酸
典型羧酸 物理性质 主要用途
工业上可用作还原剂,是合
无色、有刺激性气味的液体,有
甲酸(蚁酸)HCOOH 成医药、农药和染料等的原
腐蚀性,能与水、乙醇等互溶
料
苯甲酸(安息香酸)
无色晶体,易升华,微溶于水, 用于合成香料、药物等,其
易溶于乙醇 钠盐是常用的食品防腐剂
乙二酸(草酸) 无色晶体,通常含有两分子结晶 化学分析中常用的还原剂,
HOOC—COOH 水,可溶于水和乙醇 也是重要的化工原料
4.羧酸的物理性质甲酸、乙酸等分子中碳原子数较少的羧酸能够与水互溶。随着分子中碳原子数的增加,一
元羧酸在水中的溶解度迅速减小,甚至不溶于水,其沸点也逐渐升高。高级脂肪酸是不溶
于水的蜡状固体。羧酸与相对分子质量相当的其他有机化合物相比,沸点较高,这与羧酸
分子间可以形成氢键有关。
二、羧酸的化学性质
羧酸的化学性质与乙酸相似,主要取决于官能团羧基。
1.酸性
由于—COOH能电离出H+,使羧酸具有弱酸性,一元羧酸电离的方程式:RCOOH
RCOO-+H+。
写出下列反应的化学方程式:
(1)蜂、蝎子都会分泌蚁酸,被蜂、蝎子蛰咬可涂抹稀氨水、小苏打水缓解疼痛,上述反应
的化学方程式为HCOOH+NH ·H O―→HCOONH +HO、HCOOH+NaHCO ―→HCOONa
3 2 4 2 3
+HO+CO↑。
2 2
(2)苯甲酸与烧碱反应可制取防腐剂苯甲酸钠,该反应的离子方程式为 +OH
-
―→ +HO。
2
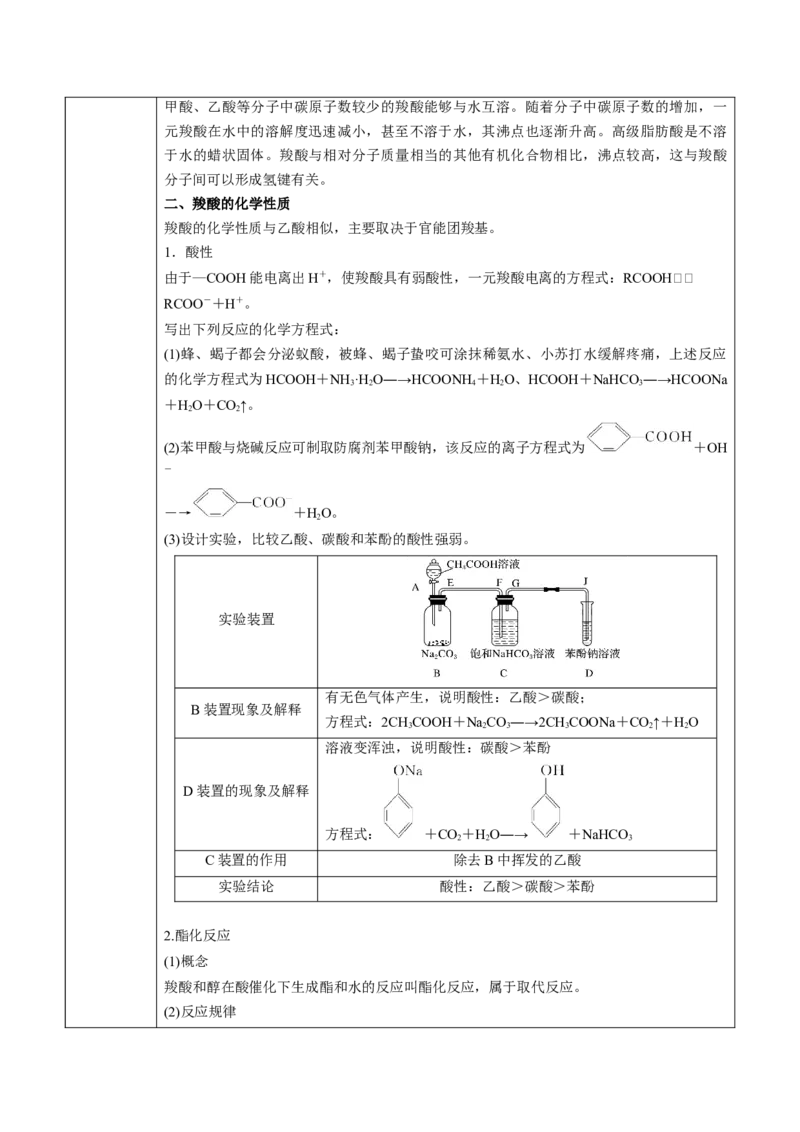
(3)设计实验,比较乙酸、碳酸和苯酚的酸性强弱。
实验装置
有无色气体产生,说明酸性:乙酸>碳酸;
B装置现象及解释
方程式:2CHCOOH+NaCO―→2CHCOONa+CO↑+HO
3 2 3 3 2 2
溶液变浑浊,说明酸性:碳酸>苯酚
D装置的现象及解释
方程式: +CO+HO―→ +NaHCO
2 2 3
C装置的作用 除去B中挥发的乙酸
实验结论 酸性:乙酸>碳酸>苯酚
2.酯化反应
(1)概念
羧酸和醇在酸催化下生成酯和水的反应叫酯化反应,属于取代反应。
(2)反应规律羧酸与醇发生酯化反应时,羧酸脱去羟基,醇脱去氢。如在浓硫酸催化作用下,醋酸与乙
醇(CHCH18OH)酯化反应的化学方程式为
3 2
3.“形形色色”的酯化反应
(1)一元羧酸与二元醇或二元羧酸与一元醇的酯化反应
如:2CHCOOH+HOCH CHOHCHCOOCH CHOOCCH +2HO。
3 2 2 3 2 2 3 2
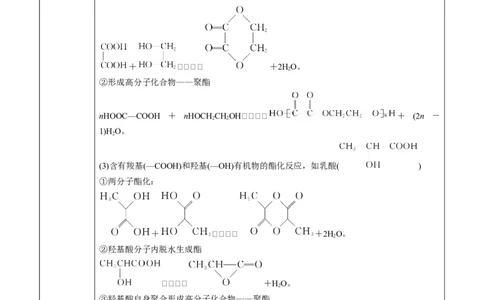
(2)二元羧酸与二元醇的酯化反应
①形成环状酯
+ +2HO。
2
②形成高分子化合物——聚酯
nHOOC—COOH + nHOCH CHOH + (2n -
2 2
1)H O。
2
(3)含有羧基(—COOH)和羟基(—OH)有机物的酯化反应,如乳酸( )
①两分子酯化:
+ +2HO。
2
②羟基酸分子内脱水生成酯
+HO。
2
③羟基酸自身聚合形成高分子化合物——聚酯
+(n-1)H O。
2
【归纳总结】
醇、酚、羧酸分子中羟基氢原子的活泼性比较
名称 乙醇 苯酚 乙酸
结构简式 CHCHOH CHCOOH
3 2 3
羟基氢原子的活泼性 不能电离 能电离 能电离――――――→
酸性 中性 极弱酸性 弱酸性
与Na反应 反应放出H 反应放出H 反应放出H
2 2 2
与NaOH反应 不反应 反应 反应
与NaCO 反应 不反应 反应 反应
2 3
与NaHCO 反应 不反应 不反应 反应
3
由上表可知,常见分子(离子)中羟基氢原子的活泼性顺序为RCOOH>H CO>
2 3
>HCO>HO>ROH。运用上述实验现象的不同,可判断有机物分子结构中含有的羟基类型。
2
课时训练
1.某有机物的结构为 ,该有机物不可能具有的性质是
A.能跟羧酸、醇等反应 B.能使酸性KMnO 溶液褪色
4
C.能发生加聚反应 D.能发生消去反应
2.由C、H、O三种元素组成的某种有机物的简易球棍模型如图所示。下列关于该有机物的说法中,不正
确的是
A.分子式是C HO
3 6 2
B.能使紫色石蕊溶液变红
C.能发生酯化反应
D.不能和NaOH溶液反应
3.布洛芬片常用来减轻感冒症状,其结构简式如图,下列有关说法错误的是
A.布洛芬在苯环上发生取代反应,其一氯代物有4种
B.布洛芬与苯乙酸是同系物
C.1mol布洛芬最多能与3mol氢气发生加成反应
D.布洛芬的分子式为C H O
13 18 2
4.布洛芬是一种常见的解热镇痛药物,其结构式如图。下列说法错误的是A.铁粉存在下与溴反应,其可能的二溴代物有5种
B.能与乙醇发生酯化反应
C.能与NaHCO 溶液发生反应
3
D.光照条件下可与氯气发生取代反应
5.2020年3月24日,中国工程院院士、天津中医药大学校长张伯礼表示,中成药连花清瘟胶囊对于治疗
轻型和普通型的新冠肺炎有确切的疗效。其有效成分绿原酸的结构简式如图,下列有关绿原酸说法正确的
是
A.最多有7个碳原子共面
B.1mol绿原酸可消耗7mol NaOH
C.不能与NaHCO 反应产生CO
3 2
D.能发生加成、取代、加聚、缩聚反应
6.下列说法正确的是
A.蛋白质是仅由碳、氢、氧、氮四种元素组成的物质
B.柴油、奶油、牛油它们所含的物质类别相同
C.分子式为C HO 且能与氢氧化钠溶液反应的物质有6种
4 8 2
D.聚合物( ),它是一种纯净物,可由单体CHCH=CH 和CH=CH 加聚制得
3 2 2 2
7.山梨酸是国际粮农组织和卫生组织推荐的高效安全的防腐保鲜剂,广泛应用于食品、饮料、烟草、农
药、化妆品等行业,它是一种无色针状晶体或白色粉末,它的结构简式为CH—CH=CH—CH=CH—
3
COOH。下列关于山梨酸的叙述不正确的
A.只要食品中添加的山梨酸符合国家要求,那么该食品可以放心食用
B.山梨酸能发生加成反应、取代反应、氧化反应
C.山梨酸的分子式为C HO,与乙酸互为同系物
6 8 2
D.1mol山梨酸能和足量碳酸氢钠溶液反应能生成1mol二氧化碳气体
8.某有机物A的分子式为C HO,下列有关分析正确的是
4 8 2
A.若A能与银氨溶液反应产生银镜,则A的结构有5种
B.若A遇NaHCO 溶液有气体生成,则A的结构有4种
3
C.若A有特殊香味且不溶于水,则A的结构有3种
D.若A遇稀硫酸能生成两种有机物,则A的结构有4种9.乙酸异戊酯是组成蜜蜂信息素的成分之一,具有橡胶的香味。实验室制备乙酸异戊酯的反应、装置示
意图和有关信息如下:
相对分子质量 密度/(g·cm-3) 沸点/℃ 水中溶解度
异戊醇 88 0.8123 131 微溶
乙酸 60 1.0492 118 溶
乙酸异戊酯 130 0.8670 142 难溶
实验步骤:
在A中加入4.4g的异戊醇,6.0g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50分钟,
反应液冷至室温后,倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分出的产物加入少量
无水硫酸镁固体,静置片刻,过滤除去硫酸镁固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯
3.9g。回答下列问题:
(1)装置B的名称是:___。
(2)在洗涤操作中,第一次水洗的主要目的是:___;第二次水洗的主要目的是:___。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后___(填标号)。
A.直接将乙酸异戊酯从分液漏斗上口倒出
B.直接将乙酸异戊酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
(4)本实验中加入过量乙酸的目的是:___。
(5)实验中加入少量无水硫酸镁的目的是:___。
(6)本实验的产率是:___。
A.40℅ B.50℅ C.60℅ D.70℅
(7)在进行蒸馏操作时,若从130℃开始收集馏分,产率偏___(填高或者低),原因是___。
10.聚乙烯醇肉桂酸酯(M)可用作光刻工艺中的抗腐蚀涂层,其合成路线如下:已知:R -CHO+R -CHCHO
1 2 2
(1)C是一种常用塑料的成分,它的名称为_______,M中的含氧官能团的名称为_______。
(2)E的分子式为_______;E→F的反应类型为_______。
(3)写出下列转化的化学方程式B→C:_______;G与新制氢氧化铜在加热条件下的反应:_______。
(4)M与NaOH溶液共热可发生水解反应,写出该步的化学方程式_______。
(5)满足下列条件的F的同分异构体有_______种,写出其中苯环上一氯代物只有两种的有机物的结构简式
_______(写出一种即可)。
①属于芳香族化合物;②能发生水解反应和银镜反应。
答案解析
1.D
【详解】
A.含有羧基和醇羟基,可以和醇、羧酸发生酯化反应,A不符合题意;
B.含有碳碳双键,可以被酸性KMnO 溶液氧化,使其褪色,B不符合题意;
4
C.含有碳碳双键,可以发生加聚反应,C不符合题意;
D.与羟基相连的碳原子的邻位碳原子位于苯环上,不能发生消去反应,D符合题意;
综上所述答案为D。
2.D
【详解】
A.根据球棍模型可知分子式是C HO,故A正确;
3 6 2B.该物质中含有-COOH,具有酸性能使紫色石蕊溶液变红,故B正确;
C.该物质中含有-COOH,能与醇发生酯化反应,故C正确;
D.该物质中含有-COOH,具有酸性,可以和NaOH溶液发生中和反应,故D错误;
故选D。
3.A
【详解】
A.结构对称,则布洛芬在苯环上发生取代反应,其一氯代物有2种, A错误;
B. 布洛芬与苯乙酸结构上相似:均含1个苯环、1个羧基,分子组成相差5个CH 原子团,因而互为同
2
系物, B正确;
C.能与氢气发生加成反应的只有苯环,则1mol 布洛芬最多能与3mol氢气发生加成反应, C正确;
D.由结构简式可以知道布洛芬的分子式为C H O, D正确;
13 18 2
答案为A。
4.A
【详解】
A.铁粉存在下与溴反应,其可能的二溴代物有: 、
、 、 ,共4种,
A项错误;
B.布洛芬中含有羧基,能与乙醇发生酯化反应,B项正确;
C.布洛芬中含有羧基,能与NaHCO 溶液发生反应,C项正确;
3
D.光照条件下,除了苯环和羧基上的H原子,其他的H原子都可以与氯气发生取代反应,D项正确;
答案选A。
5.D
【详解】
A.根据绿原酸结构,绿原酸中含有苯环,苯环中所有碳原子共平面,绿原酸中含有碳碳双键,与碳碳双
键相连的原子共平面,结构中含有酯基,与酯基相连的六元碳环上有1个碳原子与酯基共平面,故最多有
10个碳原子共平面,A项错误;
B.绿原酸中含有1个酯基、1个羧基、2个酚羟基,故1mol绿原酸可以和4mol NaOH发生反应,B项错
误;
C.绿原酸结构中含有1个羧基,可以与NaHCO 反应产生CO,C项错误;
3 2
D.绿原酸中含有双键,可以发生加成、加聚反应,含有酯基和苯环,可以发生取代反应,含有酚羟基可
以反生缩聚反应,D项正确;
答案选D。
6.C【详解】
A.蛋白质中除含有C、H、N、O四种元素外,还可能含有S、P等元素,选项A错误;
B.柴油是烃类物质,奶油、牛油是饱和高级脂肪酸甘油酯,属于酯类,它们所含的物质类别不相同,选
项B错误;
C.对于羧酸而言,根据羧基位置异构可以得到两种丁酸;根据酯基位置异构和碳链异构可得:甲酸丙酯2
种(丙基2种异构)、乙酸乙酯1种、丙酸甲酯1种,共6种,选项C正确;
D.聚合物( )可由单体CHCH=CH 和CH=CH 加聚制得,但该聚合物为混合
3 2 2 2
物,选项D错误;
答案选C。
7.C
【详解】
A.山梨酸为高效安全的防腐保鲜剂,在规定的使用量之内,可放心使用,故A正确;
B.含有碳碳双键,可发生加成、氧化反应,含有羧基,可发生取代反应,故B正确;
C.山梨酸的分子式为C HO,但分子结构中含有碳碳双键,与乙酸的结构不相似,不能称为同系物,故C
6 8
错误;
D.含有羧基,具有酸性,1mol山梨酸能和足量碳酸氢钠溶液反应能生成1 mol二氧化碳气体,故D正
确;
故答案为C。
8.D
【详解】
该分子中不饱和度=(4×2+2-8)/2=1,说明该分子中含有一个碳碳双键或碳氧双键或一个碳环。
A.分子式为C HO 能发生银镜反应,说明含有醛基,则可能为甲酸丙酯,甲酸有1种,丙醇有2种,甲
4 8 2
酸丙酯共2种;可能为羟基醛,丁醛有2种,羟基丁醛有5种:CH(OH)CHCHCHO、
2 2 2
CHCH(OH)CH CHO、CHCHCH(OH)CHO,CH(OH)CH(CH )CHO、(CH)C(OH)CHO;可能为醚醛,醚
3 2 3 2 2 3 3
醛有3种:CHOCH(CH )CHO、CHCHOCH CHO、CHOCH CHCHO,所以共有10种,故A错误;
3 3 3 2 2 3 2 2
B.能和碳酸氢钠反应生成气体,说明含有羧基,可能是丁酸、2-甲基丙酸,同分异构体有2种,故B错
误;
C.若A有特殊香味且不溶于水,说明该物质中含有酯基,可能是甲酸丙酯、甲酸异丙酯、乙酸乙酯、丙
酸甲酯,所以同分异构体有4种,故C错误;
D.若A在稀硫酸催化下加热进行反应能生成两种有机物,说明A是酯,根据C项分析可知有4种同分异
构体,故D正确;
故选D。
9.球形冷凝管 洗掉大部分浓硫酸和醋酸 洗掉碳酸氢钠 D 提高异戊醇的转化率 干燥
C 高 会收集到少量未反应的异戊醇
【分析】
本实验中,现在在A中加入4.4g的异戊醇,6.0g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热
A,回流50分钟,反应液冷至室温后,倒入分液漏斗中,分别用少量水洗涤以洗去浓硫酸和浓硝酸,饱和
碳酸氢钠溶液可以除去未反应的醋酸,同时降低酯的溶解度便于分层进行分液分离,得到的酯中混有饱和
碳酸氢钠溶液,故需要进行第二次水洗涤以除去碳酸氢钠,分出的产物加入少量无水硫酸镁固体进行干
燥,静置片刻,过滤除去硫酸镁固体,便得到异戊醇、乙酸异戊酯和乙酸的混合物,然后在进行蒸馏纯
化,收集140~143℃馏分,得乙酸异戊酯3.9g,根据产物的质量即可求出该反应的产率,据此分析解题。【详解】
(1)装置B是球形冷凝管,由于异戊醇、乙酸都是易挥发的物质,为使反应能充分进行,要用冷凝管冷凝回
流,故答案为:球形冷凝管;
(2)反应后的溶液要经过多次洗涤,在洗涤操作中,第一次洗涤的主要目的是除去大部分催化剂硫酸和醋
酸;第一步中饱和碳酸氢钠溶液既可以除去未洗净的醋酸,也可以降低酯的溶解度,但第一步洗涤后生成
的酯中混有碳酸氢钠,所以第二次水洗,主要目的是除去产品中残留的碳酸氢钠,故答案为:洗掉大部分
硫酸和醋酸;洗掉碳酸氢钠;
(3)由于酯的密度比水小,二者互不相溶,因此水在下层,酯在上层;分液时,要先将水层从分液漏斗的下
口放出,待到两层液体界面时关闭分液漏斗的活塞,再将乙酸异戊酯从上口放出,所以正确的为d,故答
案为:d;
(4)酯化反应是可逆反应,增大反应物的浓度可以使平衡正向移动;增加一种反应物的浓度,可以使另一种
反应物的转化率提高,因此本实验中加入过量乙酸的目的是提高提高异戊醇的转化率,故答案为:提高异
戊醇的转化率;
(5)实验中加入少量无水硫酸镁的目的是吸收酯中少量的水分,对其进行干燥,故答案为:干燥乙酸异戊
酯;
(6)乙酸的物质的量为:n= =0.1mol,异戊醇的物质的量为:n= =0.05mol,由于乙酸和
异戊醇是按照1:1进行反应,所以乙酸过量,生成乙酸异戊酯的量要按照异戊醇的物质的量计算,即理论
上生成0.05mol乙酸异戊酯;实际上生成的乙酸异戊酯的物质的量为 =0.03mol,所以实验中乙
酸异戊酯的产率为: ×100%=60%,故答案为:60%;
(7)在进行蒸馏操作时,若从130℃便开始收集馏分此时的蒸气中含有异戊醇,会收集少量的未反应的异戊
醇,因此会导致产率偏高,故答案为:高;会收集少量未反应的异戊醇。
10.聚氯乙烯 酯基 C HO 加成反应 nCH=CHCl
7 6 2
+2Cu(OH) +NaOH +Cu O↓+3HO
2 2 2
+nNaOH n + 14种
或 或
【分析】
根据化合物D的结构逆推可知C是 ;B发生加聚反应产生C,则B是CH=CHCl;A与HCl
2
发生加成反应产生B,则A是CH≡CH。根据D、M结构不同,可知H与D发生酯化反应产生M,所以H
结构简式是 ;G与新制Cu(OH) 发生氧化反应产生H,则G是
2;F与浓硫酸共热发生消去反应产生G,则F是 ;E与
CHCHO发生信息的加成反应产生F,可知E是 。然后根据物质性质分析解答。
3
【详解】
根据上述分析可知:A是CH≡CH,B是CH=CHCl,C是 ,E是 ,F是
2
,G是 ,H结构简式是 。
(1)C是 ,名称为聚氯乙烯;
M是 ,其中的含氧官能团是—COO—,名称为酯基;
(2)E结构简式是 ,分子式是C HO;
7 6
E及CHCHO分子中都含有醛基,在一定条件下发生醛基的加成反应产生 ,故
3
E→F的反应类型为加成反应;
(3)B是CH=CHCl,分子中含有不饱和的碳碳双键,在一定条件下发生加聚反应产生 ,故
2
B→C的化学方程式为nCH=CHCl ;
2
G是 ,分子中含有醛基,具有强的还原性,在加热条件下,醛基被新制Cu(OH) 氧
2
化为羧基,由于溶液为碱性,反应产生羧酸钠盐,则G与新制氢氧化铜在加热条件下的反应方程式为:
+2Cu(OH) +NaOH +Cu O↓+3HO;
2 2 2
(4)M分子中含有酯基,在碱性条件下水解,产生 与 ,该反应的化学方程式为: +nNaOH n + ;
(5)F是 ,其同分异构体满足条件:①属于芳香族化合物,说明含有苯环;②能发生
水解反应和银镜反应,说明含有酯基和醛基。如果取代基为HCOOCH CH-有1种结构;如果取代基为
2 2
HCOOCH(CH )-有1种结构;如果取代基为HCOO-和-CHCH 有邻、间、对3种结构;如果取代基为
3 2 3
HCOOCH -和-CH 有、邻、间对3种结构;如果取代基为HCOO-和两个-CH,两个甲基位于相邻位置,有
2 3 3
2种结构;如果两个甲基位于间位,有3种结构;如果两个甲基位于对位,有1种结构,故符合条件的同
分异构体共有:1+1+3+3+2+3+1=14种。若其中的同分异构体的苯环上一氯代物只有两种,说明在苯环上
有2种不同位置的H原子,该有机物的结构简式为: 或 或
。