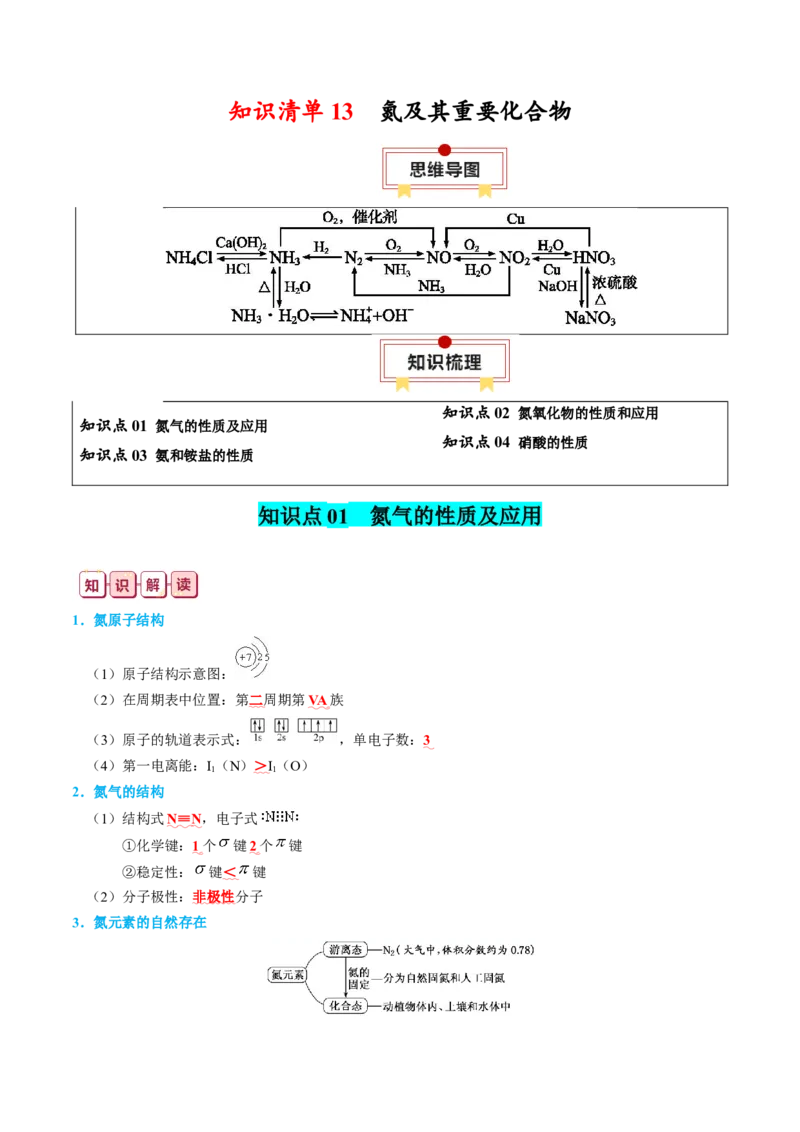
文档内容
知识清单 13 氮及其重要化合物
知识点02 氮氧化物的性质和应用
知识点01 氮气的性质及应用
知识点04 硝酸的性质
知识点03 氨和铵盐的性质
知识点 01 氮气的性质及应用
1.氮原子结构
(1)原子结构示意图:
(2)在周期表中位置:第二周期第VA 族
(3)原子的轨道表示式: ,单电子数:3
(4)第一电离能:I(N)>I(O)
1 1
2.氮气的结构
(1)结构式 N ≡ N ,电子式
①化学键:1 个 键2 个 键
②稳定性: 键< 键
(2)分子极性:非极性分子
3.氮元素的自然存在4.自然界中氮的循环
5.氮气的物理性质
(1)色味态:无色无味气体
28g/mol
22.4L/mol
(2)密度:在标准状况下ρ(N)= = 1 . 2 5 g•L - 1,比空气的小(极为接近)
2
(3)溶解性:难溶于水
(4)收集方法:只能用排水法(密度与空气接近,不能用排空气法)
6.氮气的化学性质
(1)稳定性:N≡N键能很大,通常情况下很难发生反应
(2)氧化性:N + 3H 2NH (工业固氮反应)
2 2 3
(3)还原性
①除去中H 的N:3Mg+N MgN
2 2 2 3 2
②高能固氮反应:N + O 2NO
2 2
7.氮化镁
(1)电子式:
(2)与水反应:MgN + 6 H O 3Mg ( OH ) ↓ + 2 NH ↑
3 2 2 2 3
(3)与过量盐酸反应:MgN + 8 H Cl 3MgCl + 2 NH Cl
3 2 2 4
8、氮气的用途
(1)工业上合成氨,制硝酸
(2)代替稀有气体作焊接金属时的保护气,以防止金属被空气氧化
(3)在灯泡中填充氮气以防止钨丝被氧化或挥发
(4)保存粮食、水果等食品,以防止腐烂
(5)医学上用液氮作冷冻剂,以便在冷冻麻醉下进行手术
(6)高科技利用液氮制造低温环境,使某些超导材料获得超导性能
(1)氮元素在自然界中主要以N 的形式存在于大气中,在空气中占体积分数约为 0.78,N 的相对分
2 2
子质量与空气接近,故N 的密度与空气接近,实验室只能用排水法收集。
2
(2)N 化学性质不活泼,在一般条件下不与氧气反应,经常作为食品包装袋的填充剂隔绝空气,避
2免食品被氧化变质。在一定条件下能与部分活泼金属、非金属反应,表现出氧化性或还原性。
(3)氮的固定是指氮元素由游离态变为化合态,如NH 转化为NO就不是氮的固定。
3
【典例01】(2023•湖北省选择性考试,1)2023年5月10日,天舟六号货运飞船成功发射,标志着我国航
天事业进入到高质量发展新阶段。下列不能作为火箭推进剂的是( )
A.液氮-液氢 B.液氧-液氢 C.液态NO -肼 D.液氧-煤油
2
【答案】A
【解析】A项,虽然氮气在一定的条件下可以与氢气反应,而且是放热反应,但是,由于N≡N键能很
大,该反应的速率很慢,氢气不能在氮气中燃烧,在短时间内不能产生大量的热量和大量的气体,因此,
液氮-液氢不能作为火箭推进剂,A符合题意;B项,氢气可以在氧气中燃烧,反应速率很快且放出大量的
热、生成大量气体,因此,液氧-液氢能作为火箭推进剂,B不符合题意;C项,肼和NO 在一定的条件下
2
可以发生剧烈反应,该反应放出大量的热,且生成大量气体,因此,液态 NO-肼能作为火箭推进剂,C不
2
符合题意;D项,煤油可以在氧气中燃烧,反应速率很快且放出大量的热、生成大量气体,因此,液氧-煤
油能作为火箭推进剂,D不符合题意;故选A。
【典例02】(2023·浙江宁波·镇海中学校考模拟预测)氮及其化合物的转化具有重要应用,下列说法不正
确的是
A.工业上模拟自然界“雷雨发庄稼”的过程生产
B.自然固氮、人工固氮都是将 转化为含氮化合物
C.氨气是重要的工业原料,可用于制备化肥和纯碱等大宗化学品
D.多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
【答案】A
【解析】A.自然界 “雷雨发庄稼”的第一步是将空气中的氮气转化为NO,工业生产硝酸的第一步
是将氮气和氢气反应生成氨气,氨气催化氧化得到NO,NO被氧化为 , 和水反应最后得到硝酸,
A项错误; B.氮的固定是是将 转化为含氮化合物的过程,其中氮的固定包括自然固氮、人工固氮,B
项正确; C.氨气作为重要的工业原料可以制备化肥和纯碱等大宗化学品,C项正确;
D.氮元素在自然界中既有游离态又有化合态,多种形态的氮及其化合物间的转化形成了自然界的“氮循
环”,D项正确。
知识点 02 氮的氧化物的性质及应用
1.氮元素的六种氧化物
化合价 +1 +2 +3 +4 +5
化学式 NO NO NO NO NO NO
2 2 3 2 2 4 2 5
含氧酸 H NO H NO
2 3
2.NO的性质(1)色味态:无色无味气体
(2)溶解性:难溶于水
(3)强还原性
①与O 反应: 2 NO + O 2NO
2 2 2
②与酸性HO 反应: 2 NO+ 3 H O 2 H + + 2 NO - + 2 H O
2 2 2 2 3 2
③酸性KMnO 溶液:5NO+3MnO - +4H + 5 NO - +3Mn 2 + + 2 H O
4 4 3 2
④除去NO 中的NO: NO+2 HNO (浓) 3 NO ↑ + H O
2 3 2 2
3.NO 的性质
2
(1)色味态:红棕色有刺激性气味气体
(2)溶解性:易溶于水,不溶于四氯化碳
(3)与HO反应: 3 NO + H O 2HNO + NO
2 2 2 3
(4)双聚反应:2NO NO;△H<0
2 2 4
①加热:红棕色变深
②加压:颜色先变深后变浅,比加压前深
(5)强氧化性:能够将某些还原性微粒氧化,自身被还原成NO
还原性微粒
SO 或SO 2
3 4
氧化产物 S I Fe3+
2
-
①2NO +2KI=2KNO+I (湿润的淀粉碘化钾试纸变蓝,可用于检验NO )
2 2 2 2
②NO +SO SO+NO
2 2 3
③HS+NO S+NO+HO
2 2 2
④2Fe2++4H++NO 2Fe3++2HO+NO↑
2 2
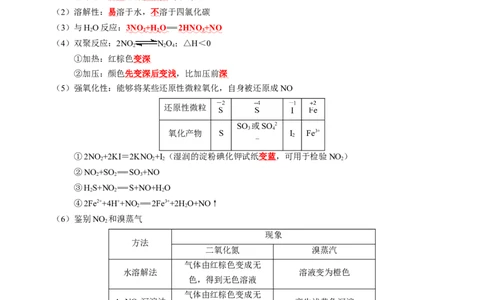
(6)鉴别NO 和溴蒸气
2
现象
方法
二氧化氮 溴蒸汽
气体由红棕色变成无
水溶解法 溶液变为橙色
色,得到无色溶液
气体由红棕色变成无
AgNO 沉淀法 产生浅黄色沉淀
3
色,溶液无明显变化
CCl 溶解法 无明显现象 得到橙红色溶液
4
密闭加热法 颜色明显加深 无明显现象
密闭冷却法 颜色明显变浅 得到深红棕色液体
湿润的淀粉
变蓝 变蓝
碘化钾试纸法
4.氮氧化物的危害
(1)形成硝酸型酸雨含氮物质 NO NO HNO
2 3
(2)形成光化学烟雾
NO 和O O 有毒烟雾
2 2 3
(3)破坏臭氧层:NO催化O 分解为O
3 2
NO+O =NO +O,NO +O=NO+O
3 2 2 2
(4)水体富营养化:水中含氮化合物引起水体污染
5.常见的处理氮氧化物的方法
(1)NaOH溶液吸收法
①2NO +2NaOH NaNO +NaNO +H O
2 2 3 2
②NO+NO +2NaOH 2NaNO +H O
2 2 2
(2)纯碱溶液吸收法
①2NO +NaCO NaNO +NaNO +CO ↑
2 2 3 3 2 2
②NO +NO+NaCO 2NaNO +CO ↑
2 2 3 2 2
(3)CH 还原法
4
①2CH+2NO N+2CO+4HO
4 2 2 2 2
②CH+4NO 2N+CO+2HO
4 2 2 2
(4)NH 还原法
3
①6NO +8NH 7N+12HO
2 3 2 2
②6NO+4NH 5N+6H O
3 2 2
(5)H 还原法
2
①4H+2NO N+4HO
2 2 2 2
②2H+2NO N+2HO
2 2 2
(6)CO还原法
①4CO+2NO 4CO+N
2 2 2
②2CO+2NO 2CO+N
2 2
6. 氮氧化物溶于水的问题分析
(1)相关反应原理
3NO + H O == =2HNO + NO ①
2 2 3
2NO + O == =2NO ②
2 2
由方程式①×2+②得:4NO + O + 2H O == =4HNO ③
2 2 2 3
由方程式①×2+②×3得: 4NO + 3O + 2H O == =4HNO ④
2 2 3
(2)氮的氧化物溶于水的三种类型
Ⅰ.NO 气体:NO 气体溶于水时仅涉及反应①,剩余气体为NO。
2 2
Ⅱ.NO 和O 的混合气体:NO 和O 的混合气体溶于水时涉及反应③:
2 2 2 2
x= 0O 过量,剩余气体为 恰好完全反应,无气 NO 过量,又发生反
2 2
反应情况
O 体剩余 应①,只剩余NO
2
Ⅲ.NO和O 的混合气体:NO、O 的混合气体溶于水时涉及反应④:
2 2
x= 0
反应情况 O 过量,剩余O 恰好完全反应,无气体剩余 NO过量,剩余NO
2 2
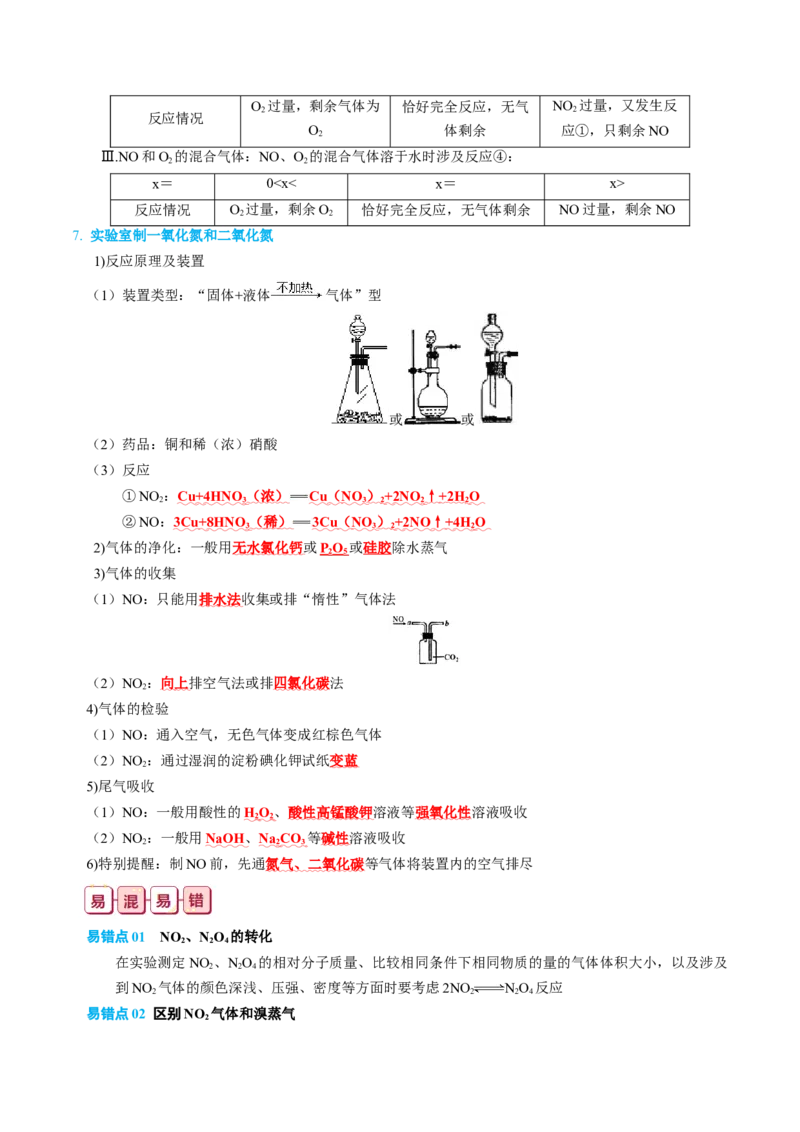
7. 实验室制一氧化氮和二氧化氮
1)反应原理及装置
(1)装置类型:“固体+液体 气体”型
或 或
(2)药品:铜和稀(浓)硝酸
(3)反应
①NO : Cu + 4HNO (浓) Cu ( NO ) + 2NO ↑ + 2H O
2 3 3 2 2 2
②NO: 3Cu + 8HNO ( 稀 ) 3Cu ( NO ) + 2NO ↑ + 4H O
3 3 2 2
2)气体的净化:一般用无水氯化钙或PO 或硅胶除水蒸气
2 5
3)气体的收集
(1)NO:只能用 排水 法 收集或排“惰性”气体法
(2)NO : 向 上 排空气法或排四氯化碳法
2
4)气体的检验
(1)NO:通入空气,无色气体变成红棕色气体
(2)NO :通过湿润的淀粉碘化钾试纸变蓝
2
5)尾气吸收
(1)NO:一般用酸性的HO、酸性高锰酸钾溶液等强氧化性溶液吸收
2 2
(2)NO :一般用NaOH、Na CO 等碱性溶液吸收
2 2 3
6)特别提醒:制NO前,先通氮气、二氧化碳等气体将装置内的空气排尽
易错点01 NO 、NO 的转化
2 2 4
在实验测定NO 、NO 的相对分子质量、比较相同条件下相同物质的量的气体体积大小,以及涉及
2 2 4
到NO 气体的颜色深浅、压强、密度等方面时要考虑2NO NO 反应
2 2 2 4
易错点02 区别NO 气体和溴蒸气
2由于NO 气体和溴蒸气都为红棕色气体,都能使湿润的淀粉碘化钾试纸变蓝,溴蒸气和NO 通入
2 2
NaOH溶液均形成无色溶液。故不能用淀粉碘化钾试纸或NaOH溶液来区别NO 气体和溴蒸气,可
2
用水来区别
【典例03】 (2023·全国·高三专题练习)下列装置用于实验室制取 并回收 ,能达到实验目
的的是
A.用装置甲制 气体 B.用装置乙收集 气体
C.用装置丙进行 的尾气吸收 D.用装置丁蒸干溶液获得 固体
【答案】B
【解析】A.为避免气体从长颈漏斗逸出,不应用长颈漏斗,应用分液漏斗,故A错误;B.NO不溶
于水,且能与氧气反应,因此用排水法收集,故B正确;C.NO不与NaOH溶液反应,也不溶于NaOH溶
液,故C错误;D.硝酸铜溶液中存在Cu(NO )+2H O Cu(OH) +2HNO ,盐类水解为吸热反应,加热蒸
3 2 2 2 3
干,促进水解,HNO 易挥发或受热分解,更有利于平衡正向进行,因此不能采用该方法得到硝酸铜固体,
3
故D错误;答案为B。
【典例04】下列关于氮的氧化物的说法中,正确的是( )
A.氮的氧化物都是酸性氧化物
B.氮的氧化物都既有氧化性,又有还原性
C.NO 与 HO 反应生成 HNO,所以 NO 是酸性氧化物
2 2 3 2
D.NO 和 NO 均有毒
2
【答案】D
【解析】NO、NO 等不是酸性氧化物;NO 中氮元素为最高价,只有氧化性;NO 与HO反应生成HNO 时
2 2 5 2 2 3
N的价态发生了变化,故NO 不是酸性氧化物。
2
知识点 03 氨和铵盐的性质
一、氨气的性质1.物理性质
(1)色味态:无色、有刺激性气味的气体
(2)密度:比空气的小
(3)溶解性:极易溶于水,1∶700,难溶于CCl
4
(4)物理特性:易液化(沸点-33.5℃)
2.碱性气体
(1)水:NH + H O NH · H O
3 2 3 2
(2)指示剂:能够使紫色石蕊试液变蓝,酚酞试液变红
(3)与酸化合成铵盐
①HCl:HCl NH Cl , 产生白烟
4
②HNO:HNO NH NO ,产生白烟,同浓硝酸
3 3 4 3
③HSO :HSO (浓) ( NH )SO ,产生白色沉淀
2 4 2 4 4 2 4
3.氨气的还原性:NH --------------------→N 或NO
3 2
(1)催化氧化:4NH +5O 4NO+6H O
3 2 2
(2)热的CuO:2NH +3CuO N+3Cu+3H O
3 2 2
(3)还原氯气
①少量NH : 2 NH +3Cl 6HCl+N
3 3 2 2
②过量NH :8NH +3Cl 6NH Cl+N (检验输送氯气的管道是否泄漏)
3 3 2 4 2
4.氧化性:2Na+2NH 2NaNH +H ↑
3 2 2
5.氨气的用途
(1)制硝酸和硝酸铵:N NH NO NO HNO NH NO
2 3 2 3 4 3
(2)致冷剂:液氨气化吸热,使环境温度急剧降低
(3)制化肥:制备硝铵、硫铵、氯铵、碳铵等铵态氮肥
二、氨水的性质
1.氨水的密度
(1)比水小,浓度越大,密度越小
(2)质量分数为a和b的两种氨水混合
①等质量混合,所得氨水的质量分数c=
②等体积混合,所得氨水的质量分数c<
2.氨水的挥发性:易挥发出氨气,所以氨水应密封保存
3.氨水的组成
(1)三个可逆反应
①氨气和水的反应:NH +HO NH ·HO
3 2 3 2②一水合氨的电离:NH · H O NH + + OH -
3 2 4
③水的电离:HO H++OH-
2
(2)“三分子”、“三离子”成分
①三分子:NH 、HO、NH ·HO
3 2 3 2
②三离子:NH +、OH-、H+
4
4.氨水的化学性质
(1)不稳定性:NH · H O NH ↑ + H O
3 2 3 2
(2)弱碱性
①HSO : 2 NH · H O+H SO ( NH )SO +2 H O
2 4 3 2 2 4 4 2 4 2
②少量CO: 2 NH · H O + CO ( NH )CO + H O
2 3 2 2 4 2 3 2
③过量CO:NH · H O + CO NH H CO
2 3 2 2 4 3
④AlCl :AlCl +3 NH · H O Al ( OH ) ↓ +3NH Cl
3 3 3 2 3 4
三、铵盐的结构和性质
1. 性质:都是无色, 易 溶 于水的晶体
2.结构:NH +的电子式
4
(1)所含化学键:离子键、共价键和配位键
(2)化合物类型:离子化合物
3.热不稳定性
(1)非氧化性酸铵盐 氨气和相应的酸
①碳酸铵: ( NH )CO 2 NH ↑ + H O ↑ + CO ↑
4 2 3 3 2 2
②碳酸氢铵:NH H CO NH ↑ + H O ↑ + CO ↑
4 3 3 2 2
③亚硫酸铵: ( NH ) S O 2 NH ↑ + H O ↑ +S O ↑
4 2 3 3 2 2
④亚硫酸氢铵:NH HS O NH ↑ + H O ↑ +S O ↑
4 3 3 2 2
⑤氯化铵:NH Cl NH ↑ + HC l ↑
4 3
(2)氧化性酸铵盐 复杂的氧化还原反应,一般不放氨气
①NH NO NO↑+2H O
4 3 2 2
②5NH NO 2HNO+4N ↑+9H O
4 3 3 2 2
③2NH NO 2N↑+O ↑+4H O
4 3 2 2 2
④3(NH )SO 4NH ↑+3SO↑+N ↑+6H O
4 2 4 3 2 2 2
4.铵盐和碱反应
(1)条件不同,产物不同
①常温:NH + + OH - NH · H O
4 3 2
②加热:NH + + OH - NH ↑ + H O
4 3 2
(2)注意事项
①铵态氮肥不能与碱性物质混合使用,以免生成氨气,降低肥效。②铵盐固体和碱固体反应时,不能拆写成离子形式
③酸式铵盐和碱溶液反应时,注意碱过量时,NH +和酸式酸根离子都参与反应
4
5.铵盐的检验
(1)步骤:取样, 加 碱 ,加热,加湿润的红色石蕊试纸
(2)现象:湿润的红色石蕊试纸变蓝
四、实验室制取氨气
1.反应原理及装置
(1)装置类型:“固体+固体 气体”型
①方法:氯化铵固体与氢氧化钙固体混合加热
②反应:2NH Cl + Ca ( OH ) 2NH ↑ + 2H O + Ca Cl
4 2 3 2 2
(2)装置类型:“液体+液体 气体”型
①方法:加热浓氨水
②反应:NH · H O NH ↑+H O
3 2 3 2
(3)装置类型:“固体+液体 气体”型
方法 原理
①NaOH溶于水放热,促使氨水分解
浓氨水与NaOH固体混合 ②NaOH固体吸水,使c(OH-)增大,有利于NH 的生成
3
③加入NaOH,使c(OH-)增大,有利于NH 的生成
3
①CaO与水反应放热,促使氨水分解。
②CaO与水反应,使水减少,使c(OH-)增大,有利于NH 的生
3
浓氨水与CaO固体混合
成
③生成Ca(OH),使c(OH-)增大,有利于NH 的生成
2 3
2.气体的净化:一般用碱石灰吸水
3.气体的收集
(1)方法:向上排空气法和排四氯化碳液体法(2)净化:试管口堵棉花的作用:防止氨气和空气发生对流,提高氨气的收集速率和纯度
4.验满方法
(1)最佳方法:用湿润的红色石蕊试纸放在集气瓶口,若试纸变蓝,则说明氨气收集满了
(2)其他方法:用玻璃棒蘸取浓盐酸或浓硝酸放在集气瓶口,若产生白烟,则说明氨气收集满了
5.尾气吸收
(1)吸收剂:棉花最好用稀硫酸浸湿,防止污染空气
(2)注意防倒吸
6.喷泉实验的原理及操作
(1)典型实验装置及变形设计
(2)操作步骤:先打开止水夹→再挤胶头滴管
(3)形成条件:容器内外产生较大的压强差
①气体完全被液体吸收剂溶解或反应
②气体和气体完全反应生成固体或液体
③气体冷凝成液体使气压减小
④液体变成气体使气压增大
⑤外界气压压缩气体
五、氨的催化氧化实验
1.反应原理: 4 NH + 5O 4 NO +6 H O
3 2 2
2.氨气的提供
(1)浓氨水
①向浓氨水中通入空气,使氨挥发出来,从而使氧气和氨充分混合。
②向浓氨水中加入NaO,使浓氨水分解产生氨气,从而使氧气和氨充分混合。
2 2
(2)铵盐分解法提供氨气
3.氧气的提供(1)直接通入空气法
(2)双氧水在二氧化锰的催化作用下分解:2HO 2HO+O ↑
2 2 2 2
(3)过氧化钠和水反应: 2 Na O+2H O 4NaOH +O ↑
2 2 2 2
(4)氯酸钾和二氧化锰混合加热:2KClO 2KCl+3O ↑
3 2
(5)高锰酸钾固体加热:2KMnO KMnO +MnO +O ↑
4 2 4 2 2
(6)过氧化钠和碳酸(氢)铵混合加热:
①NH H CO NH ↑ + H O ↑ + CO ↑或 ( NH )CO 2 NH ↑ + H O ↑ + CO ↑
4 3 3 2 2 4 2 3 3 2 2
②2Na O+2CO 2Na CO +O
2 2 2 2 3 2
4.典型现象
(1)锥形瓶中气体呈红棕色:这是因为NH 被氧化为NO,NO遇到空气中的O 又迅速被氧化为红棕色
3 2
的NO 。
2
(2)通常瓶内有白烟出现:这是由于锥形瓶里有水蒸气存在,水蒸气和 NO 反应生成了 HNO :
2 3
3NO +H O=2HNO+NO,HNO 再跟NH 反应生成微小的白色NH NO 晶体:NH +HNO =NH NO 。
2 2 3 3 3 4 3 3 3 4 3
(3)铂丝呈红色:这是因为NH 与O 在铂丝的表面上进行的反应是放热反应,反应放出的热量足以使
3 2
铂丝继续保持红热状态。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)NH 易溶于水,可用作制冷剂( )
3
(2)氨气使AlCl 溶液产生白色沉淀,反应中氨气被还原( )
3
(3)氨溶于水显弱碱性,因此可使酚酞溶液变为红色( )
(4)氨极易溶解于水,因此氨水比较稳定(不容易)分解( )
(5)氨可被氯气氧化生成N,同时还可能产生白烟现象( )
2
(6)氨水和液氨不同,氨水是混合物,液氨是纯净物( )
(7)氨水中物质的量浓度最大的粒子是NH ·H O(水除外) ( )
3 2
(8)氨水显弱碱性,是弱电解质( )
(9)氨水中含氮微粒中最多的微粒是NH( )
(10)铵盐都易溶于水,其水溶液均呈酸性( )
(11)现有1 mol·L-1的氨水,则该溶液中NH ·H O的浓度是1 mol·L-1( )
3 2
(12)在1 mol·L-1氨水中,NH ·H O、NH、NH 的物质的量浓度之和为1 mol·L-1( )
3 2 3
(13)某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性( )
(14)加热盛有NH Cl固体的试管,试管底部固体消失,试管口有晶体凝结,说明NH Cl固体可以升华(
4 4
)
(15)加热盛有少量NH HCO 固体的试管,并在试管口放置湿润的红色石蕊试纸,石蕊试纸变蓝,说明
4 3
NH HCO 显碱性( )
4 3答案:(1)× (2)× (3)√ (4)× (5)√ (6)√ (7)√ (8)× (9)× (10)× (11)× (12)√ (13)√ (14)×
(15)×
【典例05】某同学探究氨气和铵盐的性质,对相关实验操作及现象描述正确的是( )
A.室温下测定等浓度氨水和NaOH溶液的pH,比较氨水和NaOH碱性强弱
B.向试管中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口,若试纸不变蓝,则原溶液中无NH
C.液氨作为清洁能源的反应原理是4NH +5O=====4NO+6HO
3 2 2
D.加热可除去NH Cl中的少量NaHCO
4 3
【答案】A
【解析】NH ·H O是弱电解质,NaOH是强电解质,前者部分电离,后者完全电离,故通过室温下测
3 2
定等浓度氨水和NaOH溶液的pH,可比较氨水和NaOH碱性强弱,A正确;NH 极易溶于水,稀溶液中不
3
加热NH 不能逸出,无法确定是否含NH,B错误;NH 不易燃烧,产生的NO是大气污染物,不能作清洁
3 3
能源,C错误;NH Cl受热也会分解,故不可采用加热法除杂,D错误。
4
【典例06】下面是实验室制取氨气的装置和选用的试剂,其中错误的是( )
A.①② B.③④ C.①③ D.②④
【答案】C
【解析】实验室制取氨气的方法有:铵盐与碱加热制取氨气,常用 NHCl与Ca(OH) 反应,固体与固体
4 2
反试管口应略向下倾斜,③错误;在浓氨水中加入CaO,CaO与水反应使溶液中c(OH-)增大,消耗了水,
并且放出大量的热,使NH·HO分解放出氨气;加热浓氨水,加快氨气挥发。①是错误的,因为氯化铵
3 2
分解生成的NH 与HCl冷却后又生成NHCl,不能得到NH。
3 4 3
【典例07】某同学仿照“喷泉”实验的原理,在实验室做了一个“喷烟”实验,如图所示。他在甲、乙两
个烧瓶中分别充入X、Y两种无色气体,在胶头滴管中盛有含酚酞的 NaOH溶液,实验时将胶头滴管内
的液体挤入甲烧瓶内,然后打开止水夹,便可以看到甲烧瓶中的导管口喷出白色的烟,同时甲烧瓶中的
溶液颜色逐渐变浅。若已知X、Y是HCl、NH 、Cl 、O 、CH 、SO 、NO气体中的两种,则下列判断
3 2 2 4 2
中正确的是( )A.X是NH ,Y是HCl B.X是Cl,Y是NH
3 2 3
C.X是SO ,Y是O D.X是NO,Y是O
2 2 2
【答案】A。
【解析】根据题中已知的气体,能产生白烟的是HCl和NH 或Cl 和NH ,再根据题中信息“甲烧瓶中
3 2 3
的溶液颜色逐渐变浅”可知X是NH,Y是HCl,故A项正确。
3
知识点 04 硝酸的性质
1.物理性质
(1)色味态:纯硝酸是一种无色有刺激性气味的液体
(2)密度:比水的大,密度越大,浓度越越大,常见浓硝酸浓度为68%~70%
(3)溶解性:以任意比和水互溶
①主要原因:硝酸和水之间可以形成氢键
②次要原因:硝酸和水都是极性分子
(4)挥发性:易挥发,浓度为95%以上的硝酸称为发烟硝酸
2.不稳定性
(1)反应:4HNO 4NO ↑ +O ↑ +H O
3 2 2 2
(2)通常所见的浓硝酸因含NO 而呈黄色
2
①除去黄色最简单的方法:加水, 3 NO + H O 2HNO + NO
2 2 3
②除去黄色最环保的方法:通足量氧气,4NO +O +2H O 4HNO
2 2 2 3
3.与金属单质反应
(1)Al、Fe----------→钝化;Al、Fe----------→剧烈反应放NO 气体
2
(2)Au、Pt:任何情况下都不反应
(3)其他金属与硝酸反应不生成H,硝酸的浓度不同,还原产物不同
2
①浓硝酸与铜反应: Cu + 4HNO (浓) Cu ( NO ) + 2NO ↑ + 2H O
3 3 2 2 2
②稀硝酸与铜反应: 3Cu + 8HNO ( 稀 ) 3Cu ( NO ) + 2NO ↑ + 4H O
3 3 2 2
③3Zn+10HNO(稀) 4Zn(NO )+NO↑+5HO
3 3 2 2 2
④3Mg+10HNO(极稀) 4Mg(NO )+NH NO+3HO
3 3 2 4 3 2
(4)Fe-----------→ Fe ( NO );Fe-----------→ Fe ( NO )
3 3 3 2
①Fe+4HNO(稀) Fe(NO )+NO↑+2HO
3 3 3 2
②3Fe+8HNO(稀) 3Fe(NO )+2NO↑+4HO
3 3 2 24.浓硝酸与非金属单质加热反应
(1)碳与浓硝酸加热反应:C+4HNO (浓) CO ↑ +4NO ↑ +2H O
3 2 2 2
(2)碳与稀硝酸不反应
5.硝酸与还原性化合物反应:HNO---------------→NO 或NO
3 2
(1)-2价硫:3HS+2HNO(稀) 3S↓+2NO↑+4HO
2 3 2
(2)+4价硫:3NaSO +2HNO(稀) 3NaSO+2NO↑+HO
2 3 3 2 4 2
(3)-2价碘:6I-+8H++2NO- 3I+2NO↑+4H O
3 2 2
(4)+2价铁:3Fe2++4H++NO- 3Fe3++2HO+NO↑
3 2
6.几种物质和湿润的蓝色石蕊试纸的反应
(1)湿润的蓝色石蕊试纸 先变红,后褪色
(2)湿润的蓝色石蕊试纸 只变红,不褪色
(3)湿润的蓝色石蕊试纸 先变红,后变黑
(4)湿润的蓝色石蕊试纸 只变红,不褪色
(5)湿润的蓝色石蕊试纸 先变红,后褪色
(6)湿润的蓝色石蕊试纸 只变红,不褪色
7.浓硝酸的保存
(1)易挥发:密封保存,敞口放置,质量减小,浓度降低
(2)易分解:棕色细口瓶避光、黑暗而且温度低的地方
(3)强氧化性:不能用橡胶塞,而用玻璃塞
(4)大量存放:铝制或铁制的槽车内
8.硝化反应
(1)苯: +HNO (浓) NO +H O
3 2 2
(2)甲苯:制备黄色的TNT炸药
(3)颜色反应:含苯环的蛋白质遇到浓硝酸显黄色
易错点01 硝酸性质的易错点
(1)硝酸要保存在棕色试剂瓶中,并置于冷暗处,不能用橡胶塞。
(2)常温下,铁、铝遇浓硝酸能发生“钝化”,“钝化”并不是不反应,故常温下浓硝酸可以用铁桶盛
放。(3) 稀硝酸使石蕊试液变红色,浓硝酸使紫色石蕊试液先变红后褪色(酸性和强氧化性)
易错点02 涉及HNO 的离子反应常见的易错问题
3
(1)忽视NO在酸性条件下的强氧化性。在酸性条件下NO不能与Fe2+、I-、SO、S2-等还原性较强的离
子大量共存。
(2)在书写离子方程式时,忽视HNO 的强氧化性,将氧化还原反应简单的写成复分解反应。
3
【典例08】(2023·江苏·统考高考真题)氮及其化合物的转化具有重要应用。下列说法不正确的是
A.实验室探究稀硝酸与铜反应的气态产物:
B.工业制硝酸过程中的物质转化:
C.汽车尾气催化转化器中发生的主要反应:
D.实验室制备少量 的原理:
【答案】B
【详解】A.Cu与稀硝酸的反应产物之一为NO,NO与氧气发生反应 生成NO ,A
2
正确; B.氮气与氧气在高温条件下生成NO,但NO无法与水发生化学反应,B错误; C.汽车尾气催
化转化器主要将污染气体NO、CO转化为无污染的气体,故该反应方程式为 ,
C正确; D.实验室利用熟石灰和氯化铵制备少量 ,化学方程式为
,D正确。
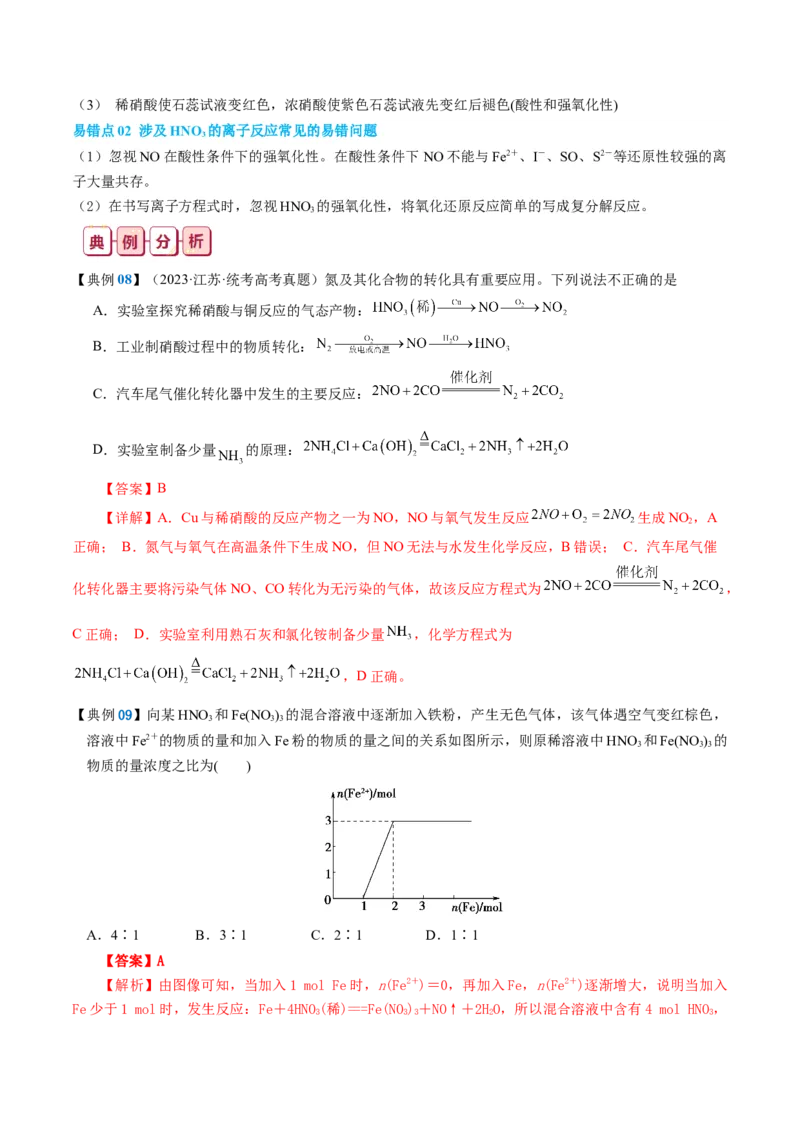
【典例09】向某HNO 和Fe(NO ) 的混合溶液中逐渐加入铁粉,产生无色气体,该气体遇空气变红棕色,
3 3 3
溶液中Fe2+的物质的量和加入Fe粉的物质的量之间的关系如图所示,则原稀溶液中HNO 和Fe(NO ) 的
3 3 3
物质的量浓度之比为( )
A.4∶1 B.3∶1 C.2∶1 D.1∶1
【答案】A
【解析】由图像可知,当加入1 mol Fe时,n(Fe2+)=0,再加入Fe,n(Fe2+)逐渐增大,说明当加入
Fe少于1 mol时,发生反应:Fe+4HNO(稀)===Fe(NO) +NO↑+2HO,所以混合溶液中含有4 mol HNO ,
3 3 3 2 3当再加入1 mol Fe时,发生反应:Fe+2Fe3+===3Fe2+,得到3 mol Fe2+,由图像和前面分析可知原混合
溶液中含有1 mol Fe(NO)。故原稀溶液中HNO 和Fe(NO) 的物质的量浓度之比为4∶1。A项正确。
3 3 3 3 3