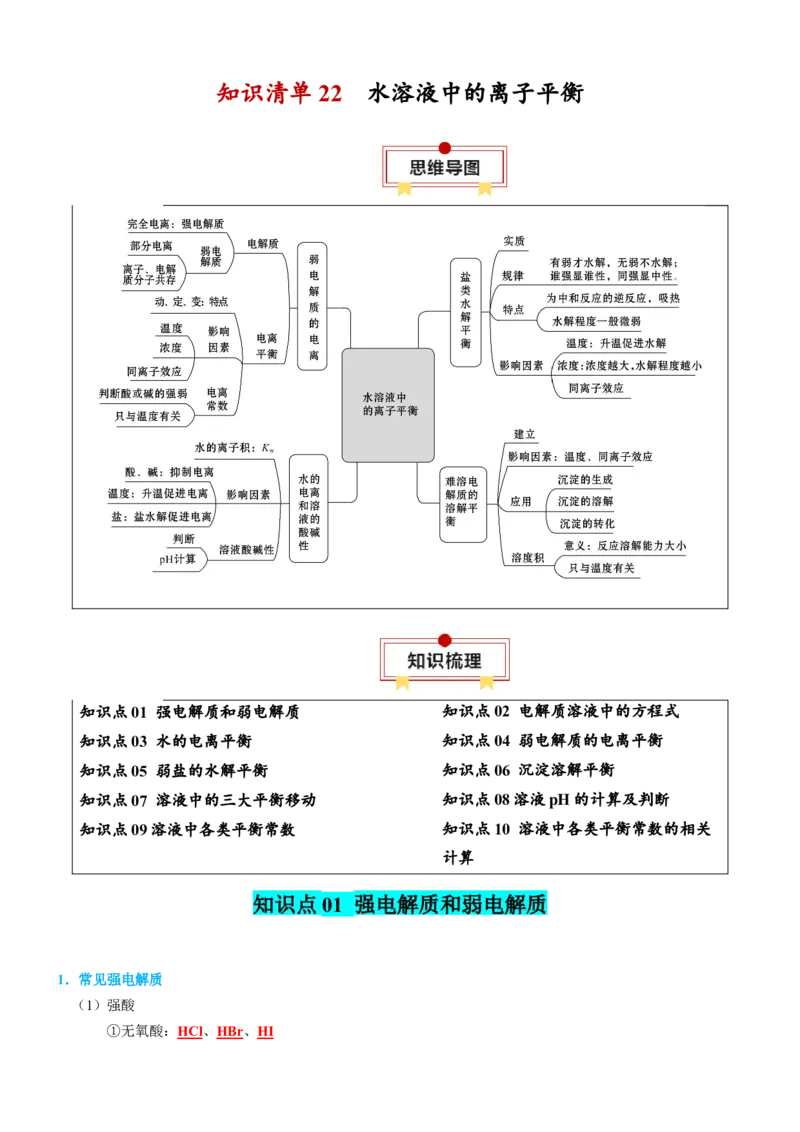
文档内容
知识清单 22 水溶液中的离子平衡
知识点01 强电解质和弱电解质 知识点02 电解质溶液中的方程式
知识点03 水的电离平衡 知识点04 弱电解质的电离平衡
知识点05 弱盐的水解平衡 知识点06 沉淀溶解平衡
知识点07 溶液中的三大平衡移动 知识点08溶液pH的计算及判断
知识点09溶液中各类平衡常数 知识点10 溶液中各类平衡常数的相关
计算
知识点 01 强电解质和弱电解质
1.常见强电解质
(1)强酸
①无氧酸:HCl、HBr、HI②含氧酸:HSO 、HNO 、HClO
2 4 3 4
(2)强碱
①一元碱:KOH、NaOH
②二元碱: Ca ( OH ) 、 Ba ( OH )
2 2
③有机碱: [ A g ( NH ) ] OH
3 2
(3)大多数盐:Fe(SCN) 除外
3
(4)金属氧化物:如NaO、Al O 等(熔融态电离)
2 2 3
2.常见弱电解质:弱酸、弱碱、少数盐和水
3.电解质溶液的特点
(1)强电解质:不含溶质分子,含溶剂分子
(2)弱电解质:溶质分子和溶质离子共存
4.弱电解质的判断(以弱酸HA为例)
(1)电离方面:不能完全电离,存在电离平衡
①10-nmol/L的HA溶液pH≠n
②同浓度的HA和HCl溶液,导电性HCl 的弱
③同浓度的HA和HCl溶液与B反应,HA 速率慢
④同pH的HA和HCl溶液与B反应,HCl 速率慢
⑤同体积同pH的HA和HCl溶液与足量B反应,HA 消耗的B多,产生的产物多
⑥pH=1的HA与pH=13的强碱等体积混合,溶液呈酸性
⑦盐酸与锌反应,加入少量NaA固体反应速率减慢
⑧同pH的HA和HCl溶液加入相应钠盐,HA 的pH增大
(2)水解方面:电解质越弱,对应离子的水解能力越强
①NaA溶液的pH>7
②NaA溶于水,加入酚酞试液,呈红色
③在NaA溶液中,c(Na+)>c(A-)
(3)稀释方面:加水稀释,平衡移动
①同倍数稀释同pH的HCl与HA,HA 的pH小
②pH=a的HCl与HA稀释成pH=b,HA 加水量多
(4)强制弱酸原理:比较酸(碱)性的相对强弱
①将HA加到碳酸钠溶液中,有气泡产生,只能说明酸性:HA>HCO,但不能说明HA是弱酸
2 3
②将盐酸加到NaA溶液中,有HA产生,说明酸性:HCl>HA,能说明HA是弱酸
知识点 02 电解质溶液中的方程式
1.电离方程式的书写
(1)强酸的酸式盐:硫酸氢盐,如:NaHSO
4
①水溶液:NaHSO Na + +H + +SO 2-
4 4
②熔融态:NaHSO Na + +HSO -
4 4
(2)弱酸的酸式盐:除了硫酸氢盐外的其他酸式盐①NaHCO :NaHCO Na + + HCO -
3 3 3
②KH PO :KHPO K + +H PO-
2 4 2 4 2 4
(3)多元弱酸分步电离,以第一步为主
①HCO 第一步电离:H C O H + +H C O -
2 3 2 3 3
②HCO 第二步电离:HCO - H + +CO 2-
2 3 3 3
(4)多元弱碱分步电离,一般一步到位
①Fe(OH) 的正常电离: Fe ( OH ) Fe 3+ +3OH -
3 3
②Fe(OH) 第一步电离: Fe ( OH ) [ F e ( OH ) ] + +OH -
3 3 2
(5)借水型电离
①NH ·H O的电离:NH ·HO NH + +OH -
3 2 3 2 4
②Al(OH) 酸式电离: Al ( OH ) +H O [ A l ( OH ) ] - + H +
3 3 2 4
(6)自偶电离:一个分子失去H+,另一个分子得到H+
①HO(l):2HO H O + +OH -
2 2 3
②NH (l):2NH NH + +NH -
3 3 4 2
③HNO(l):2HNO HNO + + NO -
3 3 2 3 3
2.水解方程式的书写
(1)水解的本质:复分解反应
①弱阴离子结合水中的 H + ,形成弱酸,溶液呈碱性
②弱阳离子结合水中的 OH - ,形成弱碱,溶液呈酸性
③NH ++D O NH •HDO+D +
4 2 3
(2)多元弱酸根离子分步水解,以第一步为主
①CO2-第一步水解:CO 2 - +H O HCO - +OH -
3 3 2 3
②CO2-第二步水解:HCO - +H O HCO +OH -
3 3 2 2 3
(3)多元弱碱根离子分步水解,一般一步到位
①Fe3+的正常水解: Fe 3+ +3H O Fe ( OH ) +3H +
2 3
②Fe3+第一步水解: Fe 3+ +H O [ F e ( OH ) ] 2 + +H +
2
(4)电离型水解
①[Al(OH) ]-:[Al(OH) ] - Al(OH) +OH -
4 4 3
②AlO-:AlO - +2H O Al ( OH ) +OH -
2 2 2 3
(5)完全进行的双水解反应
①Al3++HCO-: Al 3+ +3HCO - Al ( OH ) ↓+3CO↑
3 3 3 2
②Fe3++ClO-: Fe 3+ +3ClO - + 3H O Fe ( OH ) ↓+3 H ClO
2 3
③NH ++[Al(OH) ]-:[Al(OH) ] - +NH + Al(OH) ↓+ NH ·HO
4 4 4 4 3 3 2
(6)广义的水解
①MgN:MgN+6H O 3Mg ( OH ) ↓+2NH↑
3 2 3 2 2 2 3
②Al S:Al S+6H O 2Al ( OH ) ↓+3H S↑
2 3 2 3 2 3 2
③SiCl :SiCl +4H O HSiO ↓+4HCl
4 4 2 4 4
④IBr:IBr+H O HIO+HBr
23.沉淀溶解平衡方程式的书写
(1)Ag SO :Ag SO ( s ) 2Ag + ( aq ) + SO 2 - ( aq )
2 4 2 4 4
(2)Ca (PO )OH:Ca ( PO )OH 5Ca 2+ + 3PO 3 - +OH -
5 4 3 5 4 3 4
4.沉淀转化方程式的书写
(1)CaSO→CaCO :CaSO ( s ) +CO 2 - ( aq ) = CaCO ( s ) +SO 2 - ( aq )
4 3 4 3 3 4
(2)ZnS→CuS: ZnS ( s ) + Cu 2 + ( aq ) = CuS ( s ) + Zn 2 + ( aq )
5.注意问题
(1)有水参与的反应不一定是水解反应,还可能是电离反应
①电离平衡:HS-+H O S2-+H O+
2 3
②水解平衡:HS-+H O HS+OH-
2 2
(2)注意电离方程式和沉淀溶解平衡方程式的区别
①完全电离:AgCl(s) Ag+(aq)+Cl-(aq)
②沉淀溶解平衡:AgCl(s) Ag+(aq)+Cl-(aq)
(3)电离型水解和水解型电离
①电离平衡:Al(OH)+H O [Al(OH)]-+H+
3 2 4
②电离平衡:NH +H O NH ++OH-
3 2 4
③水解平衡:[Al(OH) ]- Al(OH) +OH-
4 3
【特别提醒】溶液中的两个相当处理
(1)HO+ H O + H +
3 2
(2)[Al(OH) ]-或AlO- Al(OH) +OH -
4 2 3
知识点 03 水的电离平衡
1.水的电离平衡:HO H++OH-△H<0
2
(1)平衡移动
①温度:越热越电离;
②酸、碱抑制水的电离
③弱盐及能够和H+或OH-反应的微粒促进水的电离
(2)具体情况下水的电离平衡移动
①有水参与的电解反应:正向移动
②向水中加入氨水:逆向移动
③向水中通入氨气:正向移动
④向水中加入Na、NaO和NaO:正向移动
2 2 2
⑤向饱和氯水中加入少量固体NaCl:逆向移动
⑥硼酸(HBO)溶于水生成[B(OH)]-:正向移动
3 3 4
2.c(H+)水和c(OH-)水的关系:在任何情况下都相等
c(H+)
c(H+) 水
水 1000
mol/L
3.水的电离度:α (HO)= c(H 2 O) ×100%=18 ×100%= 1.8 c ( H + ) %
2 水(1)不同溶液中水的电离度之比等于 c ( H + ) 之比
水
(2)酸和碱抑制水的电离,酸碱性越强,α (HO)越小
2
(3)弱盐促进水的电离,酸碱性越强,α (HO)越大
2
4.稀释过程中c(H+)水的变化
(1)酸碱溶液稀释过程中,c(H+) 变大
水
(2)弱盐溶液稀释过程中,c(H+) 变小
水
5.化学反应过程中c(H+)水的变化
(1)酸和碱反应过程中,恰好中和时,α (HO)最大
2
(2)强酸滴定弱酸盐过程中,c(H+) 变小
水
(3)强碱滴定弱碱盐过程中,c(H+) 变小
水
(4)水参与的电解反应,c(H+) 变大
水
6.水电离出的氢离子浓度和溶液pH的关系
(1)c(H+) =10-amol·L-1,pH=a 或 14 - a
水
①c(H+) =10-5mol·L-1,pH=5 或9
水
②c(H+) =10-11mol·L-1,pH=11 或3
水
(2)c(H+) =10-7mol·L-1,该溶液对水的电离程度和抑制程度相同
水
①NH ·HO和NH Cl的混合物:溶液呈中性
3 2 4
②CHCOOH和CHCOONa的混合物:溶液呈中性
3 3
③NaOH和NaCO 的混合液:溶液呈碱性
2 3
④NH Cl和HCl的混合物:溶液呈碱性
4
(3)已知pH=a,则c(H+) = 10 - a mol·L-1或 10 a - 14 mol·L-1
水
①pH=2,c(H+) = 10 - 2 mol·L-1(促进)或 10 - 12 mol·L-1(抑制)
水
②pH=11,c(H+) = 10 - 3 mol·L-1(促进)或 10 - 11 mol·L-1(抑制)
水
知识点 04 弱电解质的电离平衡
1.弱电解质的电离平衡
(1)弱酸HA的电离:①HA H++HA-△H<0;②HA- H++A2-△H<0
2 2
(2)弱碱氨水的电离:NH ·H O NH ++OH-△H<0
3 2 4
(3)平衡移动:①温度:越稀越电离;②浓度:越热越电离
2.相同体积和浓度的盐酸和醋酸的比较
(1)c(H+):盐酸 醋酸,溶液的pH醋酸的大,溶液的导电性盐酸的强,酸根离子的浓度盐酸的大
(2)与足量的其他物质反应:反应速率盐酸的快,消耗该物质的量一样多,反应结束所用的时间醋酸的长
3.相同体积和pH的盐酸和醋酸的比较
(1)溶液的浓度:盐酸 醋酸,溶液的导电性一样的强,酸根离子的浓度一样的大
(2)与足量的其他物质反应
①反应速率:开始时一样快,过程中醋酸快
②消耗该物质的量醋酸多
③生成等量的某产物所用的时间盐酸的长④反应结束所用的时间醋酸的长
知识点 05 弱盐的水解平衡
1.弱盐的水解平衡
(1)弱盐NaA的水解
2
①A2-+HO HA-+OH-△H<0;②HA-+HO HA+OH-△H<0
2 2 2
(2)平衡移动:①温度:越稀越水解;②浓度:越热越水解
(3)配制易水解的盐溶液:加相应的稀酸或稀碱防水解
①NaCO 溶液:加 NaOH 溶液
2 3
②(NH )SO 溶液:加稀硫酸或氨水
4 2 4
③Fe(NO ) 溶液:加稀硝酸
3 3
④Fe(NO ) 溶液:加不能加任何酸,以防亚铁离子被硝酸氧化
3 2
2.某些盐溶液蒸干后的产物
(1)挥发性酸的弱碱盐
①AlCl Al ( OH ) Al O
3 3 2 3
②Cu(NO ) Cu ( OH ) CuO
3 2 2
③AgNO Ag OH Ag
3
(2)难挥发性酸的弱碱盐
①Fe (SO ) Fe(SO )
2 4 3 2 4 3
②(NH )SO (NH)SO
4 2 4 4 2 4
(3)多元弱酸的强碱盐
①NaCO Na CO
2 3 2 3
②NaPO Na PO
3 4 3 4
(4)次氯酸盐
①NaClO NaCl
②Ca(ClO) CaCl
2 2
(5)还原性的盐
①FeSO Fe(SO )
4 2 4 3
②NaSO Na SO
2 3 2 4
③Fe(NO ) Fe(OH) Fe ( OH ) FeO
3 2 2 3 2 3
(6)受热易分解的盐:直接考虑分解即可
①NaHCO Na CO
3 2 3
②Ca(HCO ) CaCO CaO
3 2 3
③Mg(HCO ) MgCO Mg ( OH ) MgO
3 2 3 2
④(NH )S 无固体剩余
4 2
⑤NH HCO 无固体剩余
4 3
⑥NH Cl 无固体剩余
4
3.促进盐类水解的应用(1)热的纯碱液去油污效果好
①反应:CO2-+H O HCO -+OH-
3 2 3
②原因:加热,促进CO2-的水解,碱性增强,促进油脂的水解
3
(2)FeCl 、KAl(SO )·12H O等可作净水剂
3 4 2 2
①反应:Fe3++3H O Fe(OH)(胶体)+3H+
2 3
Al3++3H O Al(OH)(胶体)+3H+
2 3
②原因:胶体比表面积大,吸附性强,可起净水作用
(3)除去MgCl 溶液中的Fe3+
2
①方法:在加热搅拌条件下,加入足量除杂剂后过滤
②除杂剂:MgO、MgCO 或Mg(OH)
3 2
(4)制备Fe(OH) 胶体
3
①方法:向沸水中滴加饱和FeCl 溶液,至液体呈透明的红褐色停止加热
3
②反应:Fe3++3H O Fe(OH)(胶体)+3H+
2 3
(5)某些活泼金属与强酸弱碱盐溶液混合
①现象:有气泡产生
②原因:活泼金属与盐水解出的H+发生置换反应生成H
2
③实例:Mg放入NH Cl、CuCl 、FeCl 溶液中产生氢气
4 2 3
(6)泡沫灭火器原理
①药品:NaHCO 溶液和Al (SO ) 溶液
3 2 4 3
②原理:酸碱性相反的盐溶液发生水解相互促进反应
③反应:3HCO -+Al3+=Al(OH)↓+3CO ↑
3 3 2
(7)普钙[Ca(HPO )]、铵态氮肥不能与草木灰(KCO)混用
2 4 2 2 3
①原理:KCO 水解显碱性:CO2-+H O HCO -+OH-
2 3 3 2 3
②肥效降低反应
3Ca(HPO )+12OH-=Ca (PO )↓+12H O+4PO 3-
2 4 2 3 4 2 2 4
NH + +OH-=NH ↑+H O
4 3 2
(7)NH Cl用于金属除锈
4
①水解反应:NH ++H O NH ·H O+H+,铁锈与H+反应
4 2 3 2
②除锈反应:Fe O+6H+ 2Fe3++3H O
2 3 2
4.抑制盐类水解的应用
(1)配制易水解的盐溶液:加相应的酸或碱防水解
①配制FeCl 溶液时加入少量稀盐酸,防止铁离子水解
3
②配制CuSO 溶液时加入少量稀硫酸,防止铜离子水解
4
③配制醋酸钠溶液时加入少量氢氧化钠,防止醋酸根离子水解
(2)加热金属氯化物的结晶水合物制纯的无水物
①措施:在干燥的HCl气流中加热脱水②反应:MCl ·xHO MCl +xHO
m 2 m 2
③装置
5.盐类水解在药品保存中的应用
(1)盛放NaCO 溶液不能用带玻璃塞的试剂瓶
2 3
①水解反应:CO2-+H O HCO -+OH-
3 2 3
②腐蚀反应:SiO+2NaOH NaSiO+H O
2 2 3 2
(2)盛放NaF溶液不能用玻璃试剂瓶
①水解反应:F-+H O HF+OH-
2
②腐蚀反应:SiO+4HF SiF↑+2H O
2 4 2
知识点 06 沉淀溶解平衡
1.三种溶解平衡
(1)沉淀溶解平衡
①适用范围:难溶性固体溶质的饱和溶液
②平衡举例:A B (s) mAn+(aq)+nBm-(aq)
m n
③平衡移动:浓度:越稀越溶解;温度:越热越溶解(一般)
(2)结晶溶解平衡
①适用范围:可溶性固体溶质的饱和溶液
②平衡举例:KNO(s) K+(aq)+NO -(aq)
3 3
③平衡移动:适用平衡移动原理
(3)气体溶解平衡
①适用范围:气体溶质的饱和溶液
②平衡举例:O(g) O(aq)△H>0
2 2
③平衡移动:温度越低越溶解,压强越大越溶解
2.沉淀的生成
(1)本质原因: Q > K
sp
(2)分步沉淀原理
①实验前提:被沉淀的离子浓度必须相同②反应规律:混合液中滴加沉淀剂,优先生成溶解度小的沉淀
3.沉淀的转化
(1)实质:沉淀溶解平衡的正向移动
(2)基本规律
①一般来说,溶解度大→溶解度小
②沉淀的溶解度差别越大,越容易转化
(3)特殊规律:溶解度小的也可能转化为溶解度大的沉淀
①内在条件:K 相差不大,一般相差1~2个数量级
sp
②外在条件:控制离子浓度(加浓溶液、可溶性固体),使 Q > K
sp
(4)银盐转化:AgCl→AgBr→AgI→Ag S
2
①现象:白色沉淀→浅黄色沉淀→黄色沉淀→黑色沉淀
②原因:这四种沉淀的溶解度越来越小
(6)实验设计:两种沉淀所含的共同离子的量要少
①少量AgNO 溶液 AgCl AgBr
3
②少量NaOH溶液 Mg(OH) Fe(OH)
2 3
知识点 07 溶液中的三大平衡移动
1.外加物质对溶液中离子平衡移动的影响
(1)本质依据:离子方程式
①FeCl +3KSCN Fe(SCN)+3KCl(加少量KCl固体):不移动
3 3
②CuSO +2H O Cu(OH)+H SO (加少量BaCl 固体):不移动
4 2 2 2 4 2
(2)若和电离出的离子不反应,则还需要考虑所加物质是否能水解
①NH ·H O NH ++OH-(加少量MgCl 固体):正向移动
3 2 4 2
②NH ·H O NH ++OH-(加少量NaCO 固体):逆向移动
3 2 4 2 3
(3)加入××溶液时,还需要考虑到稀释效应
①NH ·H O NH ++OH-(加少量NaCl固体):不移动
3 2 4
②NH ·H O NH ++OH-(加少量NaCl溶液):正向移动
3 2 4
(4)若所加离子的浓度与原溶液中的相同,则平衡不移动,平衡中其他微粒浓度减小
(5)反应顺序
①非氧化还原反应:一般优先和电离出的离子反应
②氧化还原反应:一般优先和浓度大的氧化性或还原性微粒反应
③HS H++HS-(加少量NaOH溶液):正向移动
2
④HS H++HS-(通少量Cl):逆向移动
2 2
2.加水稀释溶液过程中各量的变化
(1)移动方向:加水平衡向可溶性物质系数和大的方向移动
①电离、水解、溶解平衡正向移动
②电离程度、水解程度、溶解程度增大,溶解的量增多,溶解度不变
(1)可溶性反应物微粒数目和浓度都增大(2)生成物微粒数目增多,生成物微粒浓度:
①浓溶液或纯液体:先增大后减小
②稀溶液:减小
(3)溶液中c(H+)和c(OH-)的变化趋势相反
①酸性溶液:加水稀释,c(H+)减小,c(OH-)增大
②碱性溶液:加水稀释,c(H+)增大,c(OH-)减小
(4)相同pH的两种电解质溶液,加水稀释相同的倍数,存在平衡的物质(弱酸、弱碱、弱盐)的pH变化
小
①强酸(碱),加水稀释10n倍,pH变化n 个单位
②弱酸(碱),加水稀释10n倍,pH变化 小于 n 个单位
③溶液无限稀释,pH无限接近于7
知识点 08 溶液 pH 的计算及判断
1.计算公式
(1)pH= - l g c ( H + ) ,c(H+)= 10 - pH
(2)pOH= - l g c ( OH - ) ,c(OH-)= 10 - pOH
(3)pH+pOH=pK =14(25℃)=12(100℃)
w
2.计算原则:酸算pH,碱算pOH
3.忽略原则:a≥100b,a±b≈a
4.中和的本质: n ( H + )= n ( OH - )
5.酸碱反应恰好呈中性的含义
(1)中性的本质
①c(H+)= c ( OH - ) ;②c(H+)= ;③pH=pOH
(2)氨水和盐酸反应:NH Cl 和少量NH ·HO 的混合物
4 3 2
(3)醋酸和烧碱反应:CH COONa 和少量CH COOH 的混合物
3 3
知识点 09 溶液中各类平衡常数
1.水的电离平衡常数和水的离子积常数
(1)水的电离平衡常数:K =
电离
(2)水的离子积常数
①表达式:K = c ( H + ) × c ( OH - )
w
②K 与K 的关系:K =K ×c(HO)
w 电离 w 电离 2
(3)常用数据:25℃:K = 1.0×10 - 14 ,100℃:K = 1.0×10 - 12
w w
2.弱电解质的电离常数
(1)弱酸HA的电离常数:K K
2 a1 a2①一级电离:HA H++HA-,K =
2 a1
二级电离:HA- H++A2-,K =
a2
②
③一步电离:HA 2H++A2-,K = =K × K
2 a a1 a2
(2)意义:在同温度同浓度时,K 越大,酸的酸性越强
a
3.弱盐的水解常数
(1)弱盐NaA的水解常数:K K
2 h1 h2
①一级水解:A2-+HO HA-+OH-:K =
2 h1
而级水解:HA-+HO HA+OH-:K =
2 2 h2
②
③一步水解:A2-+2HO HA+2OH-,K = =K × K
2 2 h h1 h2
(2)意义:在同温同浓度时,K 越大,盐的水解程度越大
h
4.溶度积常数
(1)反应:A B (s) mAn+(aq)+nBm-(aq)
m n
(2)表达式:K (A B )= c m ( A n+ ) × c n ( B m - )
sp m n
√ K
m+n sp
(3)溶度积常数和溶解度的关系x=
mm ×nn
mol/L
①阴阳离子个数比相同:K 小,溶解度小
sp
②阴阳离子个数比不同:K 小,溶解度不一定小
sp
③大小比较:将K 开离子个数次方,比较数量级即可
sp
(4)沉淀转化的平衡常数
①方程式:MX(s)+Y-(aq) MY(s)+X-(aq)
②表达式:K= =
5.电离常数K电离和水解常数K水解的关系
(1)总体关系:K ·K =K
电离 水解 w
(2)二元弱酸:K ·K =K ,K ·K =K
a1 h2 w a2 h1 w
(3)三元弱酸:K ·K =K ,K ·K =K ,K ·K =K
a1 h3 w a2 h2 w a3 h1 w
6.根据电离常数判断溶液的酸碱性
(1)弱酸(碱)与其相应盐(1∶1)混合:比较K 或K 与K 的相对大小
a b h①HA+NaA(K=10-3),K =10-11,溶液呈酸性
a h
②HB+NaB(K=10-10),K =10-4,溶液呈碱性
a h
③ROH+RCl(K =10-8),K =10-6,溶液呈酸性
b h
④MOH+MCl(K =10-5),K =10-9,溶液呈碱性
b h
(2)弱酸的酸式盐:比较水解程度(K )和电离程度(K )的相对大小
h2 a2
①NaHA(K =10-3,K =10-8),K =10-11,溶液呈酸性
a1 a2 h2
②NaHB(K =10-5,K =10-10),K =10-9,溶液呈碱性
a1 a2 h2
(3)弱酸弱碱盐:比较K 和K 的相对大小
h阳 h阴
①MA(K=10-3,K =10-8),K =10-6,K =10-11,溶液呈酸性
a b h阳 h阴
②MB(K=10-9,K =10-4),K =10-10,K =10-5,溶液呈碱性
a b h阳 h阴
③MC((K=10-5,K =10-5),K =10-9,K =10-9,溶液呈中性
a b h阳 h阴
7.根据电离常数判断复分解反应的产物或方程式
(1)适用范围:复分解反应(经验规律)
①基本规律:强酸制弱酸,强碱制弱碱
②特殊情况:弱酸制强酸,弱碱制强碱
CuSO +HS CuS↓+HSO
4 2 2 4
NaI+HPO (浓) NaH PO +HI↑
3 4 2 4
2HClO 2HCl+O ↑
2
(2)通式:弱酸盐+强酸→强酸盐+弱酸
(3)必须同时满足:强酸制弱酸,强碱制弱碱,产物不能反应
(4)判断反应的产物
弱酸 CHCOOH HClO HCO
3 2 3
电离常 3.0×l0- K =4.3×l0-7
1
1.8×l0-5
数 8 K =5.6×l0-11
2
①酸的酸性:CH COOH>HCO > H ClO >HCO -
3 2 3 3
②盐的碱性:CH COO - <HCO -< ClO - <CO 2-
3 3 3
③向NaClO溶液中通入少量CO 的反应:NaClO+CO+HO→ H ClO +NaHCO
2 2 2 3
(5)判断反应的产物
①向NaX溶液中通入少量CO:NaX+CO+H O=HX+NaHCO
2 2 2 3
②向NaY溶液中通入少量CO:2NaY+CO+H O=2HY+Na CO
2 2 2 2 3
③HX、HY、HCO 的酸性强弱:HCO >HX>HY
2 3 2 3
8.根据电离常数判断微粒能否反应
酸 电离常数
HCO K =4.3×10-7,K =5.6×10-11
2 3 a1 a2
HPO K =7.5×10-3,K =6.2×10-8,K =2.2×10-13
3 4 a1 a2 a3
(1)酸的酸性:HPO>HCO >HPO->HCO ->HPO2-
3 4 2 3 2 4 3 4
(2)盐的碱性:HPO-<HCO -<HPO2-<CO2-<PO3-
2 4 3 4 3 4
①PO 3-与HPO、HCO 、HPO-、HCO -能反应
4 3 4 2 3 2 4 3②CO2-与HPO、HCO 、HPO-能反应
3 3 4 2 3 2 4
③HPO 2-与HPO、HCO 能反应
4 3 4 2 3
④HCO -与HPO 能反应
3 3 4
⑤HPO 与HCO -、HPO2-、CO2-、PO3-能反应
3 4 3 4 3 4
⑥HCO 与HPO2-、CO2-、PO3-能反应
2 3 4 3 4
⑦HPO -与CO2-、PO3-能反应
2 4 3 4
⑧HCO -与PO3-能反应
3 4
知识点 10 溶液中各类平衡常数的相关计算
1.水解常数和电离常数的计算
(1)基本方法:三段式,注意溶液体积的变化
①根据电离或水解方程式,写出电离或水解平衡常数表达式
②根据条件找出相关数据代入求解
(2)混合液中电离或水解常数的计算步骤
①根据溶液的pH计算c(H+)或c(OH-)
②根据电荷守恒求离子浓度
③根据物料守恒求分子浓度
④将所得数据代入平衡常数表达式计算
(3)忽略原则
①a≥100b,a±b≈a
②一般用弱电解质的起始浓度代替平衡浓度计算
(4)图像类计算:注意起点、终点、交点、最高点、最低点等特殊点
①起点:根据起点的浓度和pH计算
②无限加料点:根据所加物质的浓度和pH计算
③交点:某些微粒浓度相等,能够简化计算
④极限点:恰好中和点,根据混合后盐的浓度和pH计算水解常数
2.沉淀溶解平衡的计算
(1)将有关数据代入K 表达式计算
sp
①注意溶液体积是否变化,浓度为混合后离子的浓度
②开始沉淀:一般认为该离子浓度不变
③完全沉淀:一般认为该离子浓度≤10-5mol·L—1
(2)计算金属阳离子开始沉淀和完全沉淀的pH
①计算依据:K [M(OH)]=c(Mn+)·c(OH-)n
sp n
②计算方法:先求pOH,再求pH
(3)计算完全沉淀的离子的平衡浓度
①根据方程式计算过量物质中剩余离子的浓度
②根据K 表达式计算完全反应的离子的浓度
sp
③将0.018mol·L-1的AgNO 和0.020mol·L-1盐酸等体积混合
3已
K (AgCl)=1.8×10-10
sp
知
计
混合后溶液中c(Ag+)=_____mol·L-1
算
(4)An+和Bm-两种离子恰好完全沉淀(A B )
m n
①溶液中的离子浓度满足化学式中的计量关系: =
②设沉淀的溶解度为x mol/L,则c(An+)=mx mol/L,c(Bm-)=nx mol/L
③根据K =(mx)m·(nx)n计算x
sp
易错点01: 判断HA为一元弱酸的两种常用方法
实验方法 结论
** 错误的表达式 **测0.01 mol·L-1 HA溶
pH=2,HA为强酸;pH>2,HA为弱酸
液的pH
** 错误的表达式 **室温下测NaA溶液的pH pH=7,HA为强酸;pH>7,HA为弱酸
** 错误的表达式 **相同条件下,测相同浓 若导电性相同,则HA为强酸;
度的HA溶液和盐酸(强酸)的导电性 若导电性较盐酸弱,则HA为弱酸
** 错误的表达式 **测定同pH的HA与HCl 若ΔpH(HA)=ΔpH(HCl),HA是强酸;
溶液稀释相同倍数后的 p H 变化 若ΔpH(HA)<ΔpH(HCl),HA是弱酸
** 错误的表达式 **测定等体积、等pH的 若消耗NaOH的量相同,则HA为强酸;
HA溶液和盐酸分别中和NaOH的量 若HA溶液消耗NaOH的量较盐酸多,则HA为弱酸
** 错误的表达式 **往同浓度的HA和HCl中 开始反应速率快的为强酸;开始反应速率慢的为弱
投入相同的Zn粒 酸
** 错误的表达式 **从升高温度后pH的变化 若升高温度,溶液的pH明显减小,则是弱酸;
判断 若升高温度,溶液的pH变化幅度小,则是强酸
易错点02 水的电离常见易错点
(1)在不同溶液中,c(H+)、c(OH-)可能不同,但任何溶液中由水电离出的c(H+)与c(OH-)一定相等
(2)酸、碱能抑制水的电离,故室温下,酸、碱溶液中水电离产生的 c(H+)<1×10-7 mol·L-1,而能水解的盐
溶液中水电离产生的c(H+)[或c(OH-)]>1×10-7 mol·L-1
(3)室温下,由水电离出的c (H+)或c (OH-)<10-7 mol·L-1时,可能是加酸或加碱抑制了水的电离
水 水
(4)给水加热,水的电离程度增大,c(H+)>10-7 mol·L-1,pH<7,但水仍显中性
易错点03 盐类水解常见易错点
(1)“越弱越水解”指的是盐对应的酸(或碱)越弱,水解程度越大,溶液的碱性(或酸性)越强,若酸性
HA>HB,那么相同浓度的NaA和NaB溶液,后者的碱性强
如:CHCOOH的酸性比HClO的酸性强,则相同浓度时,CHCOO-的水解程度比ClO-小,后者的碱性强
3 3
(2)盐类发生水解反应后,其水溶液往往呈酸性或碱性, 但也有特殊情况,如CHCOONH 溶液呈中性
3 4
(3)能发生相互促进的水解反应的盐溶液的酸碱性,取决于弱酸、弱碱的相对强弱,如 NH F溶液呈酸性,
4
是因 HF 的电离常数大于 NH ·H O 的电离常数
3 2【典例01】(2023·北京卷)下列过程与水解反应无关的是
A.热的纯碱溶液去除油脂
B.重油在高温、高压和催化剂作用下转化为小分子烃
C.蛋白质在酶的作用下转化为氨基酸
D.向沸水中滴入饱和 溶液制备 胶体
【答案】B
【解析】A.热的纯碱溶液因碳酸根离子水解显碱性,油脂在碱性条件下能水解生成易溶于水的高级脂肪酸盐
和甘油,故可用热的纯碱溶液去除油脂,A不符合题意;B.重油在高温、高压和催化剂作用下发生裂化或裂解
反应生成小分子烃,与水解反应无关,B符合题意;C.蛋白质在酶的作用下可以发生水解反应生成氨基酸,C
不符合题意;D. Fe3+能发生水解反应生成 Fe(OH) ,加热能增大Fe3+ 的水解程度,D不符合题意;故选B。
3
【典例02】(2023·辽宁卷)某小组进行实验,向 蒸馏水中加入 ,充分振荡,溶液呈浅棕色,再加
入 锌粒,溶液颜色加深;最终紫黑色晶体消失,溶液褪色。已知 为棕色,下列关于颜色变化的解释
错误的是
选
颜色变化 解释
项
A 溶液呈浅棕色 在水中溶解度较小
B 溶液颜色加深 发生了反应:
C 紫黑色晶体消失 ( )的消耗使溶解平衡 右移
D 溶液褪色 与有色物质发生了置换反应
【答案】D
【解析】A.向10mL蒸馏水中加入0.4gI,充分振荡,溶液呈浅棕色,说明I 的浓度较小,因为I 在水中溶解
2 2 2
度较小,A项正确;B.已知 (aq)为棕色,加入0.2g锌粒后,Zn与I 反应生成ZnI,生成的I-与I 发生反应I-
2 2 2
+I ,生成 使溶液颜色加深,B项正确;C.I 在水中存在溶解平衡I(s) I(aq),Zn与I 反应生成的I-与
2 2 2 2 2
⇌ ⇌I(aq)反应生成 ,I(aq)浓度减小,上述溶解平衡向右移动,紫黑色晶体消失,C项正确;D.最终溶液褪色是
2 2
Zn与有色物质发生了化合反应,不是置换反应,D项错误;答案选D。
【典例03】2(2023·全国甲卷)下图为 和 在水中达沉淀溶解平衡时的 关系
图( ; 可认为 离子沉淀完全)。下列叙述正确的是
A.由 点可求得
B. 时 的溶解度为
C.浓度均为 的 和 可通过分步沉淀进行分离
D. 混合溶液中 时二者不会同时沉淀
【答案】C
【解析】A.由点a(2,2.5)可知,此时pH=2,pOH=12,则 = = =
,故A错误;B.由点(5,6)可知,此时pH=5,pOH=9,则 = = =
, 时 的溶解度为 =10-3 ,故B错误;C.由图可知,当铁离子完全沉淀时,
铝离子尚未开始沉淀,可通过调节溶液pH的方法分步沉淀 和 ,故C正确;D.由图可知, 沉淀完
全时, ,pM 5,此时pH约为4.7,在此pH下 刚开始沉淀的浓度为 ,而题中 > ,则 会同时沉淀,故D错误;答案选C。
【典例04】常温下,浓度均为0.10 mol·L-1、体积均为V 的MOH和ROH溶液,分别加水稀释至体积V,pH随
0
lg的变化如图所示。下列叙述正确的是( )
A.MOH的电离程度:c点大于d点
B.ROH溶液由a点到b点时,变大
C.pH=10时,MOH和ROH溶液中,c(M+)>c(R+)
D.lg=2时,MOH和ROH两种溶液中,水电离的c(OH-)的比值是1∶10
【答案】D。
【解析】由图示可以看出MOH为强碱,强电解质不存在电离平衡,所以c点与d点电离程度相同,A错误;ROH
溶液由a点到b点时,可变式为=,而这个数值仅与温度有关,B错误;C.MOH和ROH溶液中,电荷守恒为c(OH
-)=c(H+)+c(M+),c(OH-)=c(H+)+c(R+),因为两溶液中氢离子浓度相同,所以c(R+)=c(M+),故C错误;
根据A知,碱性MOH>ROH,当lg=2时,MOH和ROH两种溶液中对应的pH分别为11、10,而这里的氢离子浓度
均是水电离产生的,故水电离的c(OH-)的比值是1∶10,D正确。