文档内容
知识清单 22 水的电离及溶液的 pH
知识点01水的电离及离子积常数 知识点02溶液的酸碱性及pH
知识点03酸碱中和滴定知识点 01 水的电离及离子积常数
1.水的电离
(1)水是_______的电解质,其电离方程式为HO+HOHO++OH-,简写为__________________。
2 2 3
(2)水的电离是_______过程。
2.水的离子积常数
(1)K 只与温度有关,温度升高,K _______。
w w
(2)常温时,K =c(H+)·c(OH-)=1.0×10-14,不仅适用于纯水,还适用于_______的稀溶液。
w
(3)不同溶液中,c(H+)、c(OH-)可能不同,但任何溶液中由水电离出的c(H+)与c(OH-)总是_______
的。
3.水的电离平衡的影响因素
(1)因水的电离是_______过程,故温度升高,会_______水的电离,c(H+)、c(OH-)都_______,水仍
呈_______性。
(2)外加酸(或碱),水中c(H+)[或c(OH-)] _______,会_______水的电离,水的电离程度_______,
K _______。
w
(3)加入了活泼金属,可与水电离产生的H+直接发生置换反应,产生H,使水的电离平衡向右移动。
2
改变条件 平衡移动方向 c(H+) c(OH-) 水的电离程度 K
w
升高温度
加入HCl(g)
加入NaOH(s)
加入活泼金属(如
Na)
加入NaHSO(s)
4
【特别提示】
(1)在水中加入酸或碱,会抑制水的电离,水电离出的c(H+)、c(OH-)均减小,但仍然相等。在常温
下,若由水电离出的c(H+)<1×10-7mol·L-1,该溶液可能显酸性,也可能显碱性。
(2)水受热温度升高,促进水的电离,水电离出的c(H+)、c(OH-)均增大,但仍然呈中性。
(3)在酸或碱的溶液中,K 表达式中的c(H+)、c(OH-)均为溶液中两种离子的总浓度,不一定是水电
w
离出的c(H+)、c(OH-)。如0.1 mol·L-1盐酸中,c(H+)约为0.1 mol·L-1。
(1)升高温度,水的电离程度增大,c(H+)和K 也增大。( )
w
(2)25 ℃时,向纯水中通入一定量SO ,水的电离平衡不移动,K 不变。( )
2 w(3)室温下,0.1 mol·L-1 NaHCO 溶液和0.1 mol·L-1 NaHSO 溶液中水的电离程度、K 均相同。( )
3 4 w
(4)25 ℃时,1.0 mol·L-1 NaOH溶液和1.0 mol·L-1盐酸中水的电离程度相等。( )
(5)室温下,CHCOONH 和NaSO 溶液均呈中性,则两溶液中水的电离程度相同。( )
3 4 2 4
(6)在表达式K =c(H+)·c(OH-)中c(H+)、c(OH-)一定是水电离出的。( )
w
(7)加水稀释醋酸溶液,溶液中所有离子浓度都减小。( )
(8)25 ℃时CHCOONa溶液的K 大于100 ℃时NaOH溶液的K 。( )
3 w w
(9)任何水溶液中均存在H+和OH-,且水电离出的c(H+)和c(OH-)相等。( )
(10)某温度下,纯水中c(H+)=2.0×10-7mol·L-1,则此时c(OH-)=5×10-8mol·L-1。( )
(11)水的离子积常数的数值大小与温度和稀水溶液的浓度有关。( )
(12)温度一定时,水的电离常数与水的离子积常数相等。( )
(13)100 ℃的纯水中c(H+)=1×10-6 mol·L-1,此时水呈酸性。( )
(14)将水加热,K 增大,pH减小。( )
w
(15)已知某温度下CHCOOH和NH ·H O的电离常数相等,现向10 mL浓度为0.1 mol·L-1的CHCOOH
3 3 2 3
溶液中滴加相同浓度的氨水,在滴加过程中水的电离程度始终增大。( )
一、水的离子积常数及水的电离平衡曲线
1.某温度下纯水的c(H+)=2×10-7mol·L-1,则此时c(OH-)为_____________________;若温度不变,
滴入稀盐酸使c(H+)=5×10-4 mol·L-1,则溶液中c(OH-)为__________________,由水电离产生的c(H+)
为______________,此时温度_______ (填“高于”“低于”或“等于”)25 ℃。
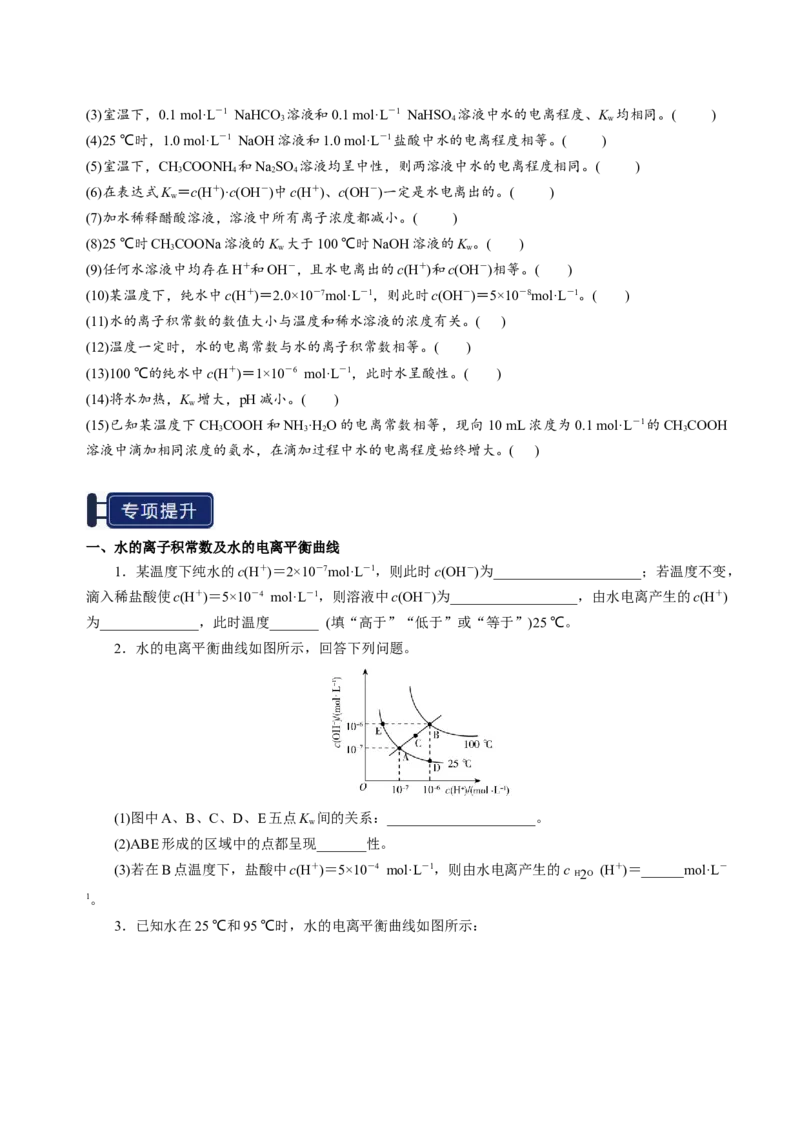
2.水的电离平衡曲线如图所示,回答下列问题。
(1)图中A、B、C、D、E五点K 间的关系:_____________________。
w
(2)ABE形成的区域中的点都呈现_______性。
(3)若在B点温度下,盐酸中c(H+)=5×10-4 mol·L-1,则由水电离产生的c (H+)=______mol·L-
H2O
1。
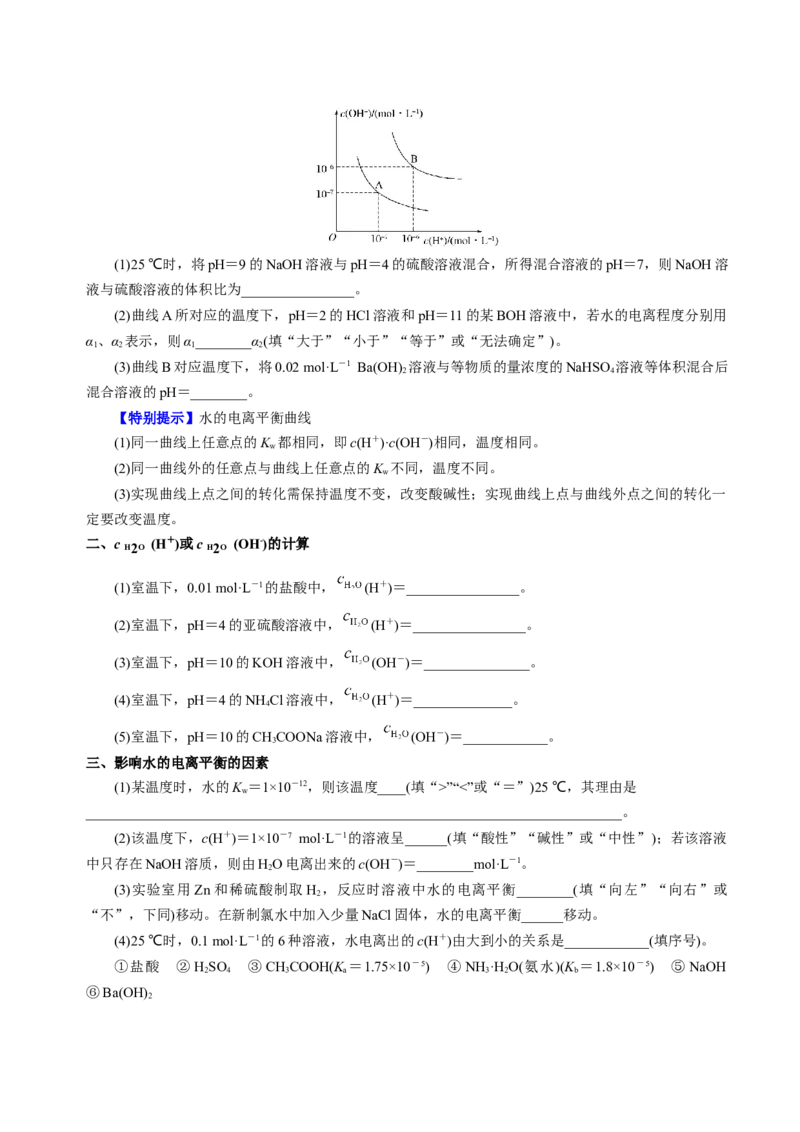
3.已知水在25 ℃和95 ℃时,水的电离平衡曲线如图所示:(1)25 ℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,所得混合溶液的pH=7,则NaOH溶
液与硫酸溶液的体积比为________________。
(2)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程度分别用
α、α 表示,则α________α(填“大于”“小于”“等于”或“无法确定”)。
1 2 1 2
(3)曲线B对应温度下,将0.02 mol·L-1 Ba(OH) 溶液与等物质的量浓度的NaHSO 溶液等体积混合后
2 4
混合溶液的pH=________。
【特别提示】水的电离平衡曲线
(1)同一曲线上任意点的K 都相同,即c(H+)·c(OH-)相同,温度相同。
w
(2)同一曲线外的任意点与曲线上任意点的K 不同,温度不同。
w
(3)实现曲线上点之间的转化需保持温度不变,改变酸碱性;实现曲线上点与曲线外点之间的转化一
定要改变温度。
二、c (H+)或c (OH-)的计算
H2O H2O
(1)室温下,0.01 mol·L-1的盐酸中, (H+)=________________。
(2)室温下,pH=4的亚硫酸溶液中, (H+)=________________。
(3)室温下,pH=10的KOH溶液中, (OH-)=_______________。
(4)室温下,pH=4的NH Cl溶液中, (H+)=______________。
4
(5)室温下,pH=10的CHCOONa溶液中, (OH-)=____________。
3
三、影响水的电离平衡的因素
(1)某温度时,水的K =1×10-12,则该温度____(填“>”“<”或“=”)25 ℃,其理由是
w
____________________________________________________________________________。
(2)该温度下,c(H+)=1×10-7 mol·L-1的溶液呈______(填“酸性”“碱性”或“中性”);若该溶液
中只存在NaOH溶质,则由HO电离出来的c(OH-)=________mol·L-1。
2
(3)实验室用Zn和稀硫酸制取H ,反应时溶液中水的电离平衡________(填“向左”“向右”或
2
“不”,下同)移动。在新制氯水中加入少量NaCl固体,水的电离平衡______移动。
(4)25 ℃时,0.1 mol·L-1的6种溶液,水电离出的c(H+)由大到小的关系是____________(填序号)。
①盐酸 ② HSO ③ CHCOOH(K =1.75×10-5) ④ NH ·H O(氨水)(K =1.8×10-5) ⑤ NaOH
2 4 3 a 3 2 b
⑥Ba(OH)
2知识点 02 溶液的酸碱性及 pH
1.溶液的酸碱性
(1)任何水溶液中都有H+和OH-。
(2)溶液的酸碱性取决于溶液中c(H+)、c(OH-)的______________。
溶液的酸碱性
(3)25℃时,溶液的酸碱性与溶液中c(H+)、c(OH-)的关系
c(H+)与c(OH-)的关系 c(H+)的范围(室温下)
酸性溶液 c(H+) _____c(OH-) c(H+) _____1×10-7 mol·L-1
中性溶液 c(H+) _____c(OH-) c(H+) _____1×10-7 mol·L-1
碱性溶液 c(H+) _____c(OH-) c(H+) _____1×10-7 mol·L-1
2.溶液的pH
(1)计算公式:pH=______________
(2)意义:pH越大,溶液的碱性_______;pH越小,溶液的酸性_______。
(3)常温下溶液酸碱性与pH的关系:
pH<7,为_______溶液;pH=7,为_______溶液;pH>7,为_______溶液。
(4)适用范围1×10-14 mol·L-1<c(H+)<1 mol·L-1
(5)溶液酸碱性的另外一种表示——pOH
pOH=______________;
②常温下:pH+pOH=_______。
①
3.pH的测定
(1)pH试纸:迅速测定溶液的pH。
常用的pH试纸有广泛pH试纸和精密pH试纸,广泛pH试纸可以识别的pH差约为_______。pH试
纸的使用方法如下:
①测定溶液的pH:把小片试纸放在_______ (或玻璃片)上,用洁净干燥的_______蘸取待测液滴在干
燥的pH试纸的中部,观察变化稳定后的颜色,与______________对比即可确定溶液的pH。
②检验气体的酸碱性:先把试纸_______,粘在_______的一端,再送到盛有待测气体的容器口附近,
观察颜色的变化,判断气体的性质。
(2)pH计:精密测量溶液的pH。
4.溶液pH的计算
(1)单一溶液pH的计算
①c mol·L-1 HA强酸溶液的pH (25 ℃)
n
c(H+)=_______ mol·L-1;pH=_______
②c mol·L-1 B(OH) 强碱溶液的pH (25 ℃)
n
c(OH-)=_______ mol·L-1;c(H+)=_______=_______ mol·L-1;pH=_________。(2)混合溶液pH的计算方法
①强酸与强酸混合(稀溶液体积变化忽略)
c (H+)=_____________________,然后再求pH。
混
②强碱与强碱混合(稀溶液体积变化忽略)
先计算c (OH-)=_____________________,再求c (H+)=_______,最后求pH。
混 混
③强酸与强碱混合(稀溶液体积变化忽略)
a.恰好完全反应,溶液呈中性,pH=_______ (25 ℃)。
b.酸过量:
先求c (H+)=_____________________,再求pH。
余
c.碱过量:
先求c (OH-)=_____________________,再求c(H+)=_______,最后求pH。
余
【特别提醒】
(1)强酸溶液和强碱溶液混合后计算pH,必须先判断出混合后溶液的酸碱性,然后计算混合后的OH-
或H+浓度。
(2)根据酸的浓度计算酸溶液的pH时,不必考虑温度,而根据碱的浓度计算碱溶液的pH时,需要根
据离子积计算c(H+),因此一定要注意溶液的温度,只有室温时,K =1.0×10-14。
w
(3)一定pH的强碱与强碱混合后求pH。在计算过程中易出现直接用H+浓度进行混合计算的错误。
因为强碱溶液的混合是OH-混合,H+是随OH-浓度改变而改变的,不能直接用于混合碱的计算,H+浓
度必须通过c(H+)=来求。
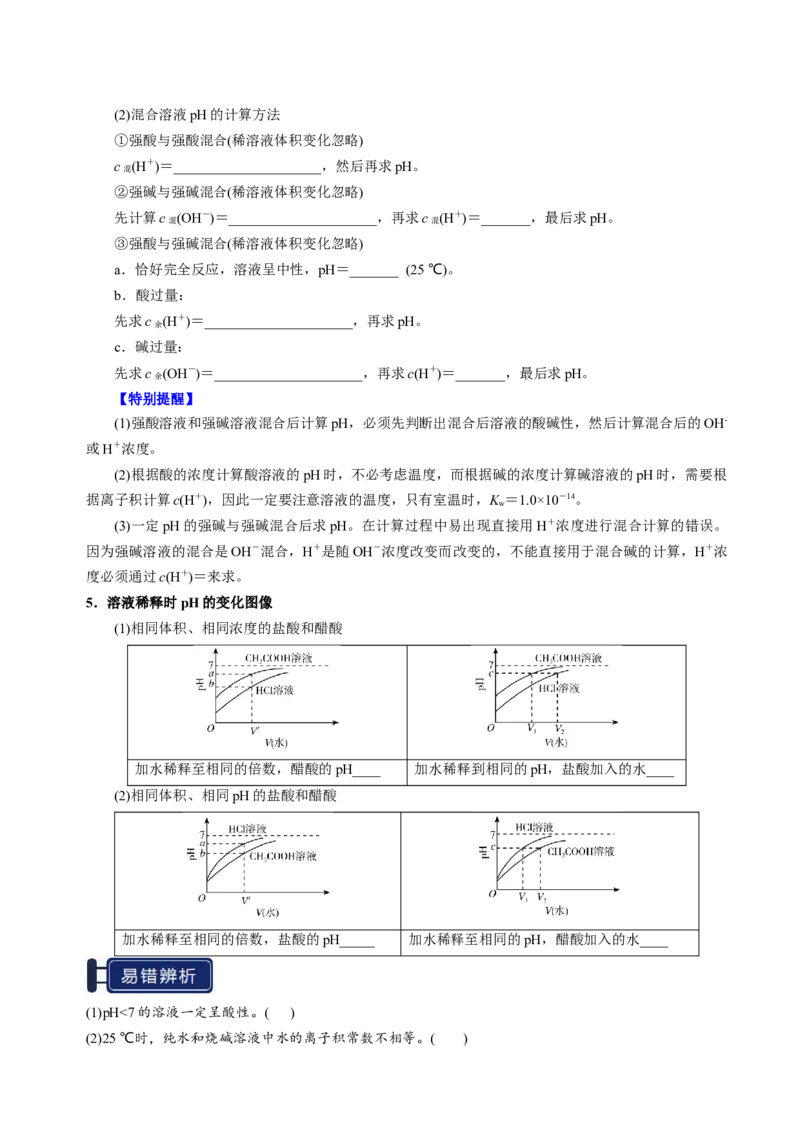
5.溶液稀释时pH的变化图像
(1)相同体积、相同浓度的盐酸和醋酸
加水稀释至相同的倍数,醋酸的pH____ 加水稀释到相同的pH,盐酸加入的水____
(2)相同体积、相同pH的盐酸和醋酸
加水稀释至相同的倍数,盐酸的pH_____ 加水稀释至相同的pH,醋酸加入的水____
(1)pH<7的溶液一定呈酸性。( )
(2)25 ℃时,纯水和烧碱溶液中水的离子积常数不相等。( )(3)在100 ℃时,纯水的pH>7。( )
(4)若溶液中c(H+)=c(OH-),则溶液为中性。( )
(5)c(H+)=的溶液一定显中性。( )
(6)pH试纸可以测定所有溶液的pH。( )
(7)常温下能使甲基橙显黄色的溶液一定显碱性。( )
(8)用湿润的pH试纸测定盐酸和醋酸溶液的pH,醋酸溶液的误差更大。( )
(9)T ℃时,某溶液的pH>7,则该溶液呈碱性。( )
(10)室温下,用pH试纸测得某NaClO溶液的pH=9。( )
(11)pOH=-lgc(OH-),常温下溶液中的pH+pOH=14,正常人的血液pH=7.3,则正常人血液(人的体
温高于室温)的pOH等于6.7。( )
(12)用广泛pH试纸测得某溶液的pH为3.4,用pH计测得某溶液的pH为7.45。( )
(13)c(OH-)>1×10-7 mol·L-1某电解质溶液一定是碱性溶液。( )
(14)常温下,将pH=3的酸和pH=11的碱等体积混合,所得溶液的pH=7。( )
一、溶液的酸碱性与pH判断
判断下列溶液的酸碱性:用“酸性”“碱性”“中性”或“不确定”填空
pH<7的溶液_______。
pH=7的溶液_______。
①
c(H+)=c(OH-)的溶液_______。
②
c(H+)=1×10-7 mol·L-1的溶液_______。
③
c(H+)>c(OH-)的溶液_______。
④
0.1 mol·L-1的NH Cl溶液_______。
⑤ 4
0.1 mol·L-1的NaHCO 溶液_______。
⑥ 3
0.1 mol·L-1的NaHSO 溶液_______。
⑦ 3
二、有关pH的计算
⑧
(1)常温下,pH=5的HSO 溶液,加水稀释到体积为原来的500倍,则稀释后c(SO)与c(H+)的比值
2 4
为 _______ 。
(2)25 ℃时,取浓度相同的NaOH和HCl溶液,以3 2体积比相混合,所得溶液的pH等于12,则原
溶液的浓度为 ______________。
∶
(3)计算25 ℃时下列溶液的pH:
①0.1 mol·L-1的CHCOOH溶液(已知CHCOOH的电离常数K=1.8×10-5),其pH=_______。
3 3 a
②0.1 mol·L-1的氨水(NH ·H O的电离度α=1%),其pH=_______。
3 2
③pH=2的盐酸与等体积的水混合,其pH=_______ (已知lg 2≈0.3)。
④常温下,将0.1 mol·L-1氢氧化钠溶液与0.06 mol·L-1硫酸溶液等体积混合,其pH=_______。
⑤25 ℃时,pH=3的硝酸和pH=12的氢氧化钡溶液按照体积比为9 1混合,其pH=_______。
∶三、混合溶液的酸碱性判断
常温下,两种溶液混合后酸碱性的判断(在括号中填“酸性”“碱性”或“中性”)。
(1)相同浓度的HCl和NaOH溶液等体积混合( )
(2)相同浓度的CHCOOH和NaOH溶液等体积混合( )
3
(3)相同浓度的NH ·H O和HCl溶液等体积混合( )
3 2
(4)pH=2的HSO 和pH=12的NaOH溶液等体积混合( )
2 4
(5)pH=3的HCl和pH=10的NaOH溶液等体积混合( )
(6)pH=3的HCl和pH=12的NaOH溶液等体积混合( )
(7)pH=2的CHCOOH和pH=12的NaOH溶液等体积混合( )
3
(8)pH=2的HSO 和pH=12的NH ·H O等体积混合( )
2 4 3 2
【归纳小结】酸碱溶液混合后酸碱性的判断规律
(1)等浓度等体积的一元酸与一元碱混合的溶液——“谁强显谁性,同强显中性”。
(2)室温下c (H+)=c (OH-),即pH之和等于14时,一强一弱等体积混合——“谁弱谁过量,谁弱
酸 碱
显谁性”。
(3)已知强酸和强碱的pH,等体积混合(25 ℃时):
pH之和等于14,呈中性;
pH之和小于14,呈酸性;
①
pH之和大于14,呈碱性。
②
③
知识点 03 酸碱中和滴定
1.酸碱中和滴定原理
(1)利用已知浓度的酸(或碱)去滴定一定体积未知浓度的碱(或酸),通过测定反应完全时消耗已知浓度
的酸(或碱)的体积,从而推算出未知浓度的碱(或酸)的浓度的方法。
其中已知浓度的酸(或碱)溶液常称为_______,未知浓度的碱(或酸)溶液常称为_______。
(2)酸碱中和反应的实质可用离子方程式H++OH-===HO来表示,在中和反应中,H+、OH-之间
2
的物质的量关系是______________;若用参加反应的 c(H+)、c(OH-)来表示,其关系式为
______________,由此可计算c(H+),其表达式是c(H+)=____________;也可计算c(OH-),其表达式
是c(OH-)=____________。由c(H+)、c(OH-)可分别求出相应酸、碱的浓度。
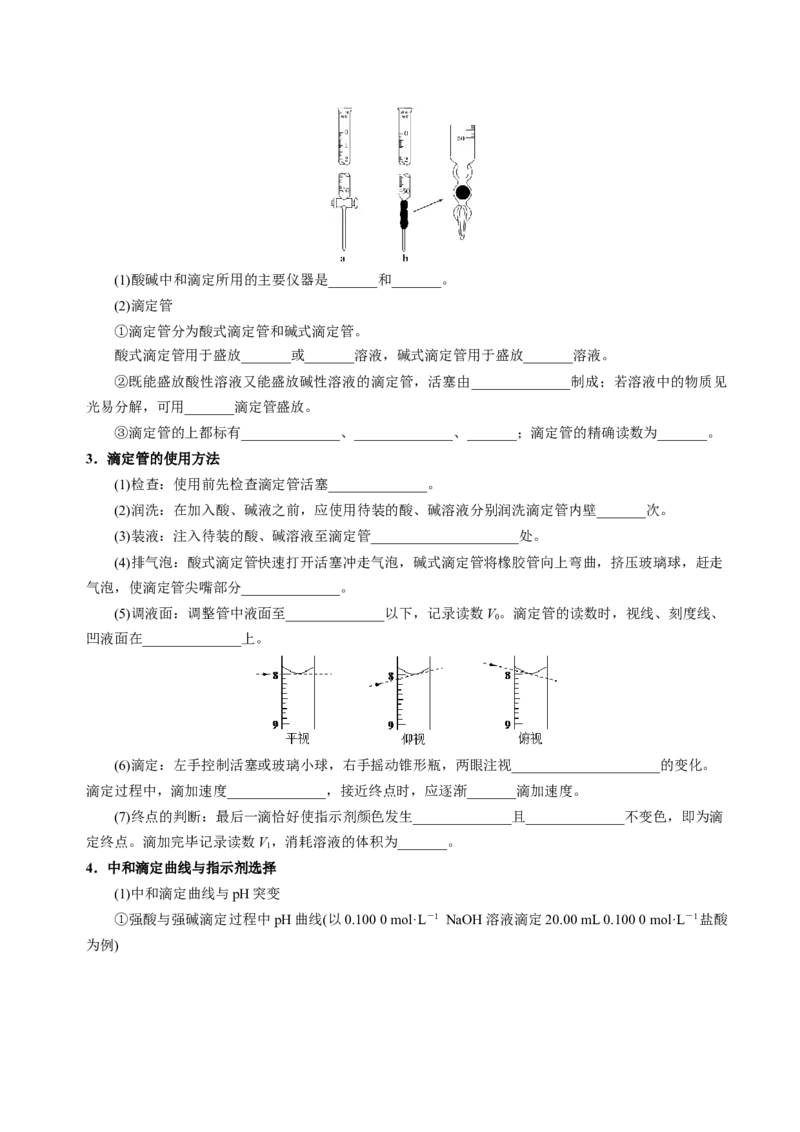
2.主要仪器(1)酸碱中和滴定所用的主要仪器是_______和_______。
(2)滴定管
①滴定管分为酸式滴定管和碱式滴定管。
酸式滴定管用于盛放_______或_______溶液,碱式滴定管用于盛放_______溶液。
②既能盛放酸性溶液又能盛放碱性溶液的滴定管,活塞由______________制成;若溶液中的物质见
光易分解,可用_______滴定管盛放。
③滴定管的上都标有______________、______________、_______;滴定管的精确读数为_______。
3.滴定管的使用方法
(1)检查:使用前先检查滴定管活塞______________。
(2)润洗:在加入酸、碱液之前,应使用待装的酸、碱溶液分别润洗滴定管内壁_______次。
(3)装液:注入待装的酸、碱溶液至滴定管_____________________处。
(4)排气泡:酸式滴定管快速打开活塞冲走气泡,碱式滴定管将橡胶管向上弯曲,挤压玻璃球,赶走
气泡,使滴定管尖嘴部分______________。
(5)调液面:调整管中液面至______________以下,记录读数V。滴定管的读数时,视线、刻度线、
0
凹液面在______________上。
(6)滴定:左手控制活塞或玻璃小球,右手摇动锥形瓶,两眼注视_____________________的变化。
滴定过程中,滴加速度______________,接近终点时,应逐渐_______滴加速度。
(7)终点的判断:最后一滴恰好使指示剂颜色发生______________且______________不变色,即为滴
定终点。滴加完毕记录读数V,消耗溶液的体积为_______。
1
4.中和滴定曲线与指示剂选择
(1)中和滴定曲线与pH突变
①强酸与强碱滴定过程中pH曲线(以0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1盐酸
为例)②强酸(碱)滴定弱碱(酸)pH曲线比较
氢氧化钠滴定等浓度等体积的盐酸、醋 盐酸滴定等浓度等体积的氢氧化
酸的滴定曲线 钠、氨水的滴定曲线
曲线起点不同:强碱滴定强酸、弱酸的曲线,强酸起点低;强酸滴定强碱、
弱碱的曲线,强碱起点高
突跃点变化范围不同:强碱与强酸反应(强酸与强碱反应)的突跃点变化范围
大于强碱与弱酸反应(强酸与弱碱反应)
(2)中和滴定终点的判断
判断滴定终点(中和反应恰好反应完全的时刻)的方法是________________________________
______________,常选用的指示剂是_____或______,而不用石蕊试液的原因是_________________。
(3)指示剂的选择
对于不同的酸碱中和反应,指示剂的选择可依据中和滴定曲线来确定。
指示剂 酸色 中间色 碱色 变色的pH范围
甲基橙 红 橙 黄 3.1 ~ 4.4
甲基红 红 橙 黄 4.4 ~ 6.2
酚酞 无色 粉红 红 8.2 ~ 10.0
5.实验操作
以酚酞作指示剂,用标准盐酸滴定待测NaOH溶液为例:
(1)滴定前的准备
滴定管:_______→洗涤→_______→装液→排气泡调液面→记录。
锥形瓶:洗涤→装待测液→加指示剂。
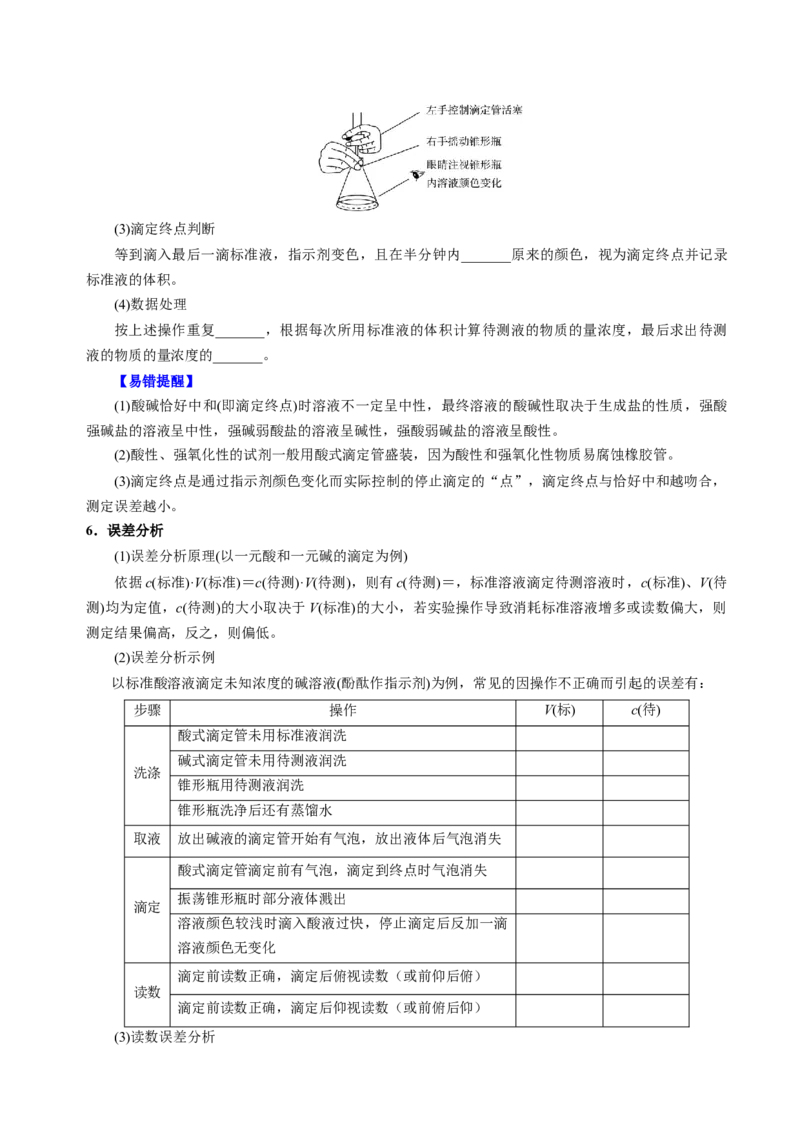
(2)滴定
滴定:左手_____________________,右手______________,眼睛_____________________。(3)滴定终点判断
等到滴入最后一滴标准液,指示剂变色,且在半分钟内_______原来的颜色,视为滴定终点并记录
标准液的体积。
(4)数据处理
按上述操作重复_______,根据每次所用标准液的体积计算待测液的物质的量浓度,最后求出待测
液的物质的量浓度的_______。
【易错提醒】
(1)酸碱恰好中和(即滴定终点)时溶液不一定呈中性,最终溶液的酸碱性取决于生成盐的性质,强酸
强碱盐的溶液呈中性,强碱弱酸盐的溶液呈碱性,强酸弱碱盐的溶液呈酸性。
(2)酸性、强氧化性的试剂一般用酸式滴定管盛装,因为酸性和强氧化性物质易腐蚀橡胶管。
(3)滴定终点是通过指示剂颜色变化而实际控制的停止滴定的“点”,滴定终点与恰好中和越吻合,
测定误差越小。
6.误差分析
(1)误差分析原理(以一元酸和一元碱的滴定为例)
依据c(标准)·V(标准)=c(待测)·V(待测),则有c(待测)=,标准溶液滴定待测溶液时,c(标准)、V(待
测)均为定值,c(待测)的大小取决于V(标准)的大小,若实验操作导致消耗标准溶液增多或读数偏大,则
测定结果偏高,反之,则偏低。
(2)误差分析示例
以标准酸溶液滴定未知浓度的碱溶液(酚酞作指示剂)为例,常见的因操作不正确而引起的误差有:
步骤 操作 V(标) c(待)
酸式滴定管未用标准液润洗
碱式滴定管未用待测液润洗
洗涤
锥形瓶用待测液润洗
锥形瓶洗净后还有蒸馏水
取液 放出碱液的滴定管开始有气泡,放出液体后气泡消失
酸式滴定管滴定前有气泡,滴定到终点时气泡消失
振荡锥形瓶时部分液体溅出
滴定
溶液颜色较浅时滴入酸液过快,停止滴定后反加一滴
溶液颜色无变化
滴定前读数正确,滴定后俯视读数(或前仰后俯)
读数
滴定前读数正确,滴定后仰视读数(或前俯后仰)
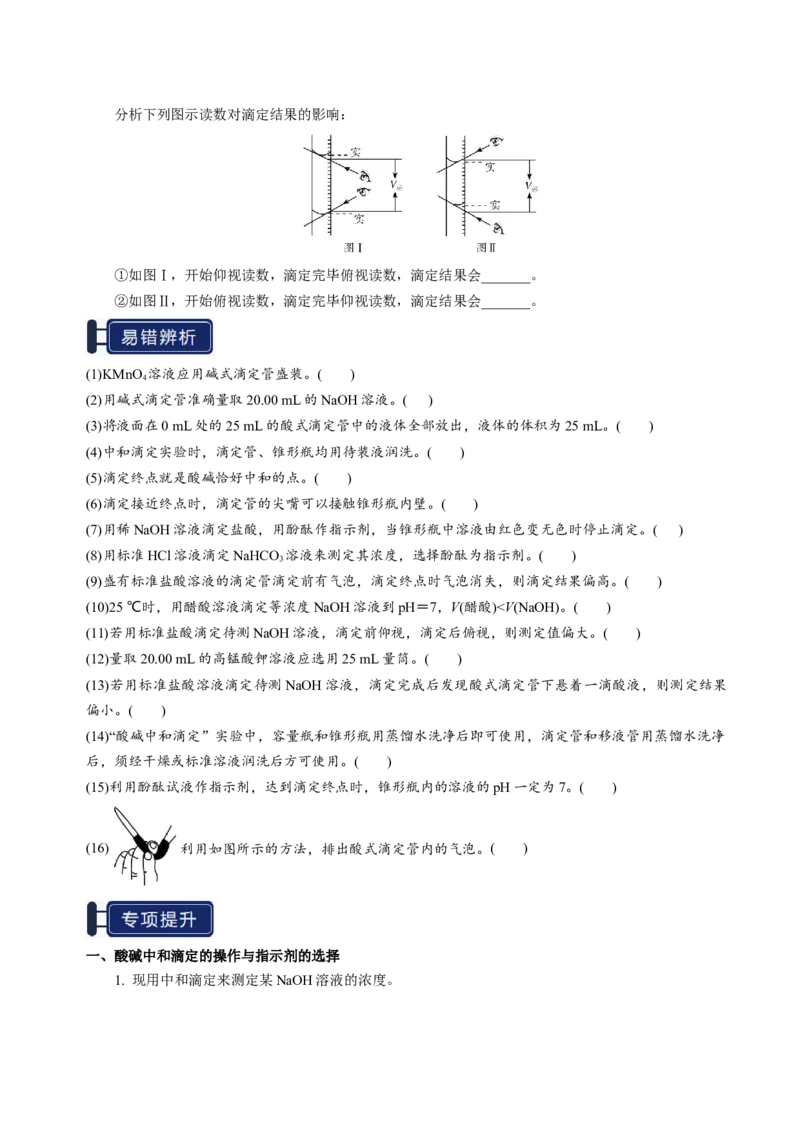
(3)读数误差分析分析下列图示读数对滴定结果的影响:
①如图Ⅰ,开始仰视读数,滴定完毕俯视读数,滴定结果会_______。
②如图Ⅱ,开始俯视读数,滴定完毕仰视读数,滴定结果会_______。
(1)KMnO 溶液应用碱式滴定管盛装。( )
4
(2)用碱式滴定管准确量取20.00 mL的NaOH溶液。( )
(3)将液面在0 mL处的25 mL的酸式滴定管中的液体全部放出,液体的体积为25 mL。( )
(4)中和滴定实验时,滴定管、锥形瓶均用待装液润洗。( )
(5)滴定终点就是酸碱恰好中和的点。( )
(6)滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁。( )
(7)用稀NaOH溶液滴定盐酸,用酚酞作指示剂,当锥形瓶中溶液由红色变无色时停止滴定。( )
(8)用标准HCl溶液滴定NaHCO 溶液来测定其浓度,选择酚酞为指示剂。( )
3
(9)盛有标准盐酸溶液的滴定管滴定前有气泡,滴定终点时气泡消失,则滴定结果偏高。( )
(10)25 ℃时,用醋酸溶液滴定等浓度NaOH溶液到pH=7,V(醋酸)