文档内容
知识清单 18 原电池 化学电源
知识点01 原电池的工作原理及应用 知识点02 化学电源知识点 01 原电池的工作原理及应用
1.原电池的概念和实质
(1)概念:将化学能转化为电能的装置。
(2)实质:利用能自发进行的氧化还原反应把化学能转化为电能。
2.原电池的工作原理
(1)电极反应:
负极:失去电子,发生氧化反应
正极:得到电子,发生还原反应
(2)电子移动方向:从负极流出沿导线流入正极,电子不能通过电解质溶液。
(3)离子移动方向:
①阴离子向负极移动,阳离子向正极移动。
②如果有盐桥:盐桥中的阴离子移向负极区,阳离子移向正极区。
(4)盐桥的作用:
①离子通道,形成闭合回路。
②避免电极与电解质溶液直接反应,减少电流的衰减。
3.原电池的构成条件
①形成闭合回路;
②两个活性不同的电极,相对较活泼的金属作负极;
③电解质溶液或熔融电解质;
④自发的氧化还原反应(一般能对外界释放能量)。
【易错提醒】
(1)构成原电池的两电极材料不一定都是金属,正极材料可以为导电的非金属,例如石墨。两极材料
可能参与反应,也可能不参与反应。
(2)两个活泼性不同的金属电极用导线连接,共同插入电解质溶液中不一定构成原电池,必须有一个
能自发进行的氧化还原反应。
(3)在判断原电池正负极时,既要考虑金属活泼性的强弱,也要考虑电解质溶液性质。如Mg-Al-
HCl溶液构成的原电池中,负极为Mg;但是Mg-Al-NaOH溶液构成的原电池中,负极为Al,正极为
Mg。
4.原电池原理的应用
(1)设计制作化学电源
①用双线桥分析氧化还原反应的电子转移方向和数目;
②分别写出正、负极的电极反应式(半反应式);
③根据电极反应式确定半电池的电极材料和电解质溶液:a.电极材料:一般活泼金属作负极,不活泼金属(或非金属导体)作正极;
b.电解质溶液:负极电解液一般是负极金属对应的阳离子的溶液;正极电解液一般是氧化剂对应的
电解质溶液。
(2)比较金属的活动性强弱
一般来说,作负极的金属的活动性强于正极金属。
如:有两种金属a和b,用导线连接后插入稀硫酸中,观察到 a极溶解,b极上有气泡产生。由此可
判断出a是负极、b是正极,且金属活动性:a>b。
(3)加快化学反应速率
氧化还原反应形成原电池时,反应速率加快。在锌与稀HSO 反应时加入少量CuSO 溶液,CuSO
2 4 4 4
与锌发生置换反应生成Cu,从而形成Cu-Zn微小原电池,加快产生H 的速率。
2
(4)用于金属的防护:将需要保护的金属制品作原电池的正极而受到保护。
(1)NaOH溶液与稀硫酸的反应是自发进行的放热反应,此反应可以设计成原电池(×)
错因:该反应不是氧化还原反应,没有电子转移。
(2)Mg—Al形成的原电池,Mg一定作负极(×)
错因:若是酸性介质Mg作负极,若是碱性介质Al作负极。
(3)其他条件均相同,带有“盐桥”的原电池比不带“盐桥”的原电池电流持续时间长(√)
(4)原电池工作时,电子从负极流出经导线流入正极,然后通过溶液流回负极(×)
错因:电子不进入溶液,溶液中阴阳离子定向移动形成电流。
(5)在Cu|CuSO |Zn原电池中,正电荷定向移动的方向就是电流的方向,所以Cu2+向负极移动(×)
4
错因:在外电路中电流由正极流向负极,而在电解质溶液中,阳离子都由负极移向正极。
(6)构成原电池两极的电极材料一定是活泼性不同的金属(×)
错因:原电池的电极材料必须能导电,不一定是金属,也可以是石墨,燃料电池中两个电极都可以是石
墨。
(7)原电池中负极失去电子的总数一定等于正极得到电子的总数(√)
(8)电解质溶液中阴、阳离子的定向移动,与导线中电子的定向移动共同组成了一个完整的闭合回路(√)
一、原电池的工作原理
1.(1)由组成原电池的电极材料判断。一般是活动性较强的金属为 极,活动性较弱的金属或能导
电的非金属为 极。
(2)根据电流方向或电子流动方向判断。电流由 极流向 极;电子由 极流向 极。
(3)根据原电池中电解质溶液内离子的移动方向判断。在原电池的电解质溶液内,阳离子移向 极,
阴离子移向 极。
(4)根据原电池两极发生的变化来判断。原电池的 极失电子发生氧化反应,其 极得电子发生还
原反应。
(5)根据现象判断。一般情况下,溶解的一极为 极,增重或有气体逸出的一极为 极。答案:(1)负 正 (2)正 负 负 正 (3)正 负 (4)负 正 (5)负 正
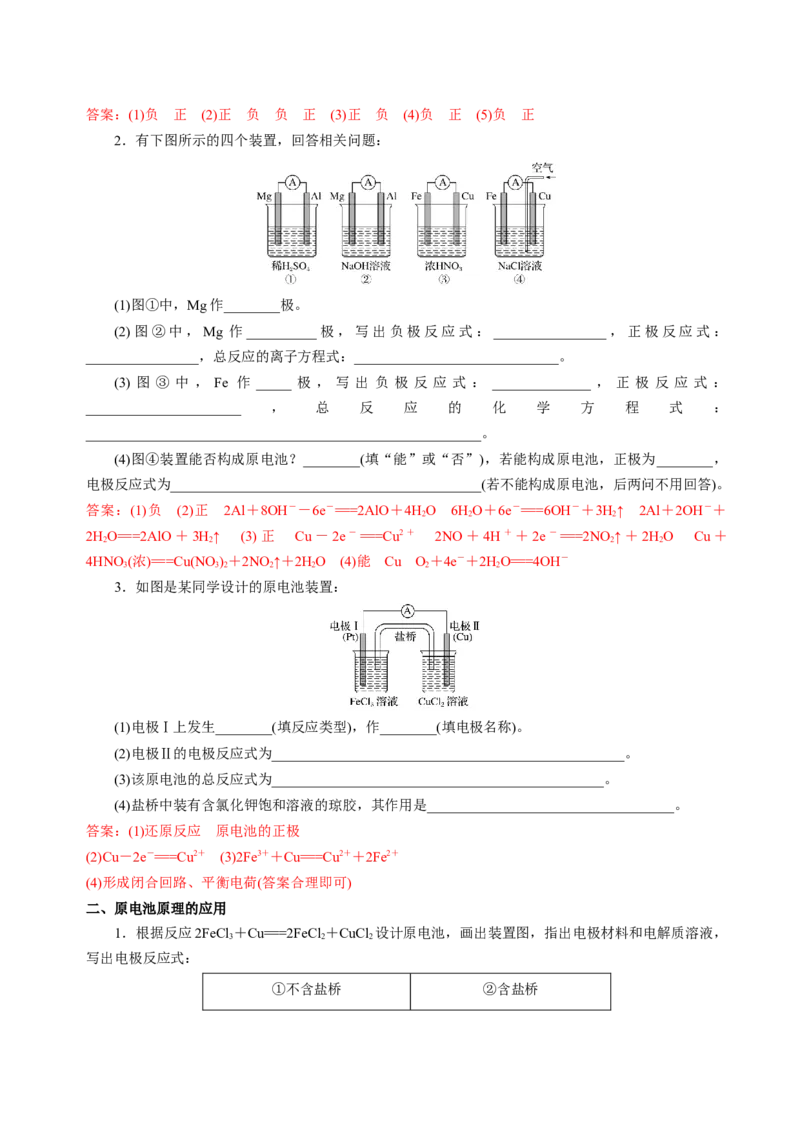
2.有下图所示的四个装置,回答相关问题:
(1)图①中,Mg作________极。
(2)图②中,Mg 作__________极,写出负极反应式:________________,正极反应式:
________________,总反应的离子方程式:_____________________________。
(3) 图 ③ 中 , Fe 作 _____ 极 , 写 出 负 极 反 应 式 : ______________ , 正 极 反 应 式 :
______________________ , 总 反 应 的 化 学 方 程 式 :
________________________________________________________。
(4)图④装置能否构成原电池?________(填“能”或“否”),若能构成原电池,正极为________,
电极反应式为____________________________________________(若不能构成原电池,后两问不用回答)。
答案:(1)负 (2)正 2Al+8OH--6e-===2AlO+4HO 6HO+6e-===6OH-+3H↑ 2Al+2OH-+
2 2 2
2HO===2AlO+3H↑ (3)正 Cu-2e-===Cu2+ 2NO+4H++2e-===2NO↑+2HO Cu+
2 2 2 2
4HNO(浓)===Cu(NO)+2NO ↑+2HO (4)能 Cu O+4e-+2HO===4OH-
3 3 2 2 2 2 2
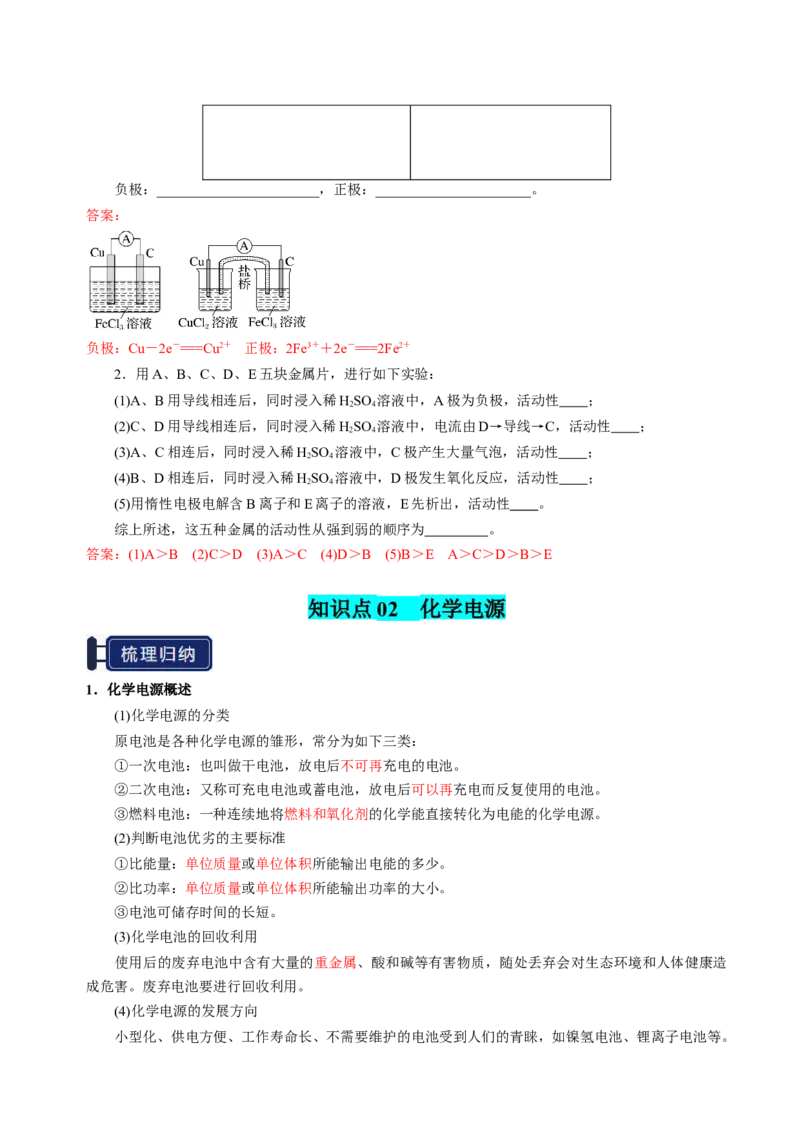
3.如图是某同学设计的原电池装置:
(1)电极Ⅰ上发生________(填反应类型),作________(填电极名称)。
(2)电极Ⅱ的电极反应式为__________________________________________________。
(3)该原电池的总反应式为_______________________________________________。
(4)盐桥中装有含氯化钾饱和溶液的琼胶,其作用是___________________________________。
答案:(1)还原反应 原电池的正极
(2)Cu-2e-===Cu2+ (3)2Fe3++Cu===Cu2++2Fe2+
(4)形成闭合回路、平衡电荷(答案合理即可)
二、原电池原理的应用
1.根据反应2FeCl +Cu===2FeCl +CuCl 设计原电池,画出装置图,指出电极材料和电解质溶液,
3 2 2
写出电极反应式:
①不含盐桥 ②含盐桥负极:_______________________,正极:______________________。
答案:
负极:Cu-2e-===Cu2+ 正极:2Fe3++2e-===2Fe2+
2.用A、B、C、D、E五块金属片,进行如下实验:
(1)A、B用导线相连后,同时浸入稀HSO 溶液中,A极为负极,活动性 ;
2 4
(2)C、D用导线相连后,同时浸入稀HSO 溶液中,电流由D→导线→C,活动性 ;
2 4
(3)A、C相连后,同时浸入稀HSO 溶液中,C极产生大量气泡,活动性 ;
2 4
(4)B、D相连后,同时浸入稀HSO 溶液中,D极发生氧化反应,活动性 ;
2 4
(5)用惰性电极电解含B离子和E离子的溶液,E先析出,活动性 。
综上所述,这五种金属的活动性从强到弱的顺序为 。
答案:(1)A>B (2)C>D (3)A>C (4)D>B (5)B>E A>C>D>B>E
知识点 02 化学电源
1.化学电源概述
(1)化学电源的分类
原电池是各种化学电源的雏形,常分为如下三类:
①一次电池:也叫做干电池,放电后不可再充电的电池。
②二次电池:又称可充电电池或蓄电池,放电后可以再充电而反复使用的电池。
③燃料电池:一种连续地将燃料和氧化剂的化学能直接转化为电能的化学电源。
(2)判断电池优劣的主要标准
①比能量:单位质量或单位体积所能输出电能的多少。
②比功率:单位质量或单位体积所能输出功率的大小。
③电池可储存时间的长短。
(3)化学电池的回收利用
使用后的废弃电池中含有大量的重金属、酸和碱等有害物质,随处丢弃会对生态环境和人体健康造
成危害。废弃电池要进行回收利用。
(4)化学电源的发展方向
小型化、供电方便、工作寿命长、不需要维护的电池受到人们的青睐,如镍氢电池、锂离子电池等。2.一次电池
(1)普通锌锰干电池
①构造(如图所示):
负极:锌筒 正极:石墨棒
电解质溶液:氯化铵和氯化锌
②工作原理:
负极:Zn-2e-+2NH===Zn(NH)+2H+
3
正极:2MnO +2H++2e-===2MnO(OH)
2
总反应:Zn+2NH Cl+2MnO ===Zn(NH)Cl+2MnO(OH)
4 2 3 2 2
(2)碱性锌锰干电池
①构造(如图所示):
负极反应物:锌粉 正极反应物:二氧化锰
电解质溶液:氢氧化钾
②工作原理:
负极:Zn+2OH--2e-===Zn(OH)
2
正极:2MnO +2HO+2e-===2MnO(OH)+2OH-
2 2
总反应:Zn+2MnO +2HO===2MnO(OH)+Zn(OH)
2 2 2
(3)纽扣式锌银电池
总反应:Zn+Ag O+HO===Zn(OH) +2Ag。
2 2 2
电解质:KOH;
负极反应物:Zn;电极反应:Zn+2OH--2e-===Zn(OH) ;
2
正极反应物:Ag O;电极反应:Ag O+HO+2e-===2Ag+2OH-。
2 2 2
3.二次电池
(1)铅酸蓄电池
铅酸蓄电池是一种常见的二次电池,其放电过程表示如下:
Pb+PbO +2HSO ===2PbSO+2HO
2 2 4 4 2
①放电反应原理
a.负极是Pb,正极是PbO ,电解质溶液是HSO 溶液。
2 2 4
b.电极反应:
负极:Pb+SO-2e-===PbSO ;正极:PbO +4H++SO+2e-===PbSO+2HO
4 2 4 2
c.放电过程中,负极质量的变化是增大,HSO 溶液的浓度减小。
2 4
②充电反应原理
阴极(还原反应)反应式是 PbSO +2e-===Pb+SO ;
4
阳极(氧化反应)反应式是PbSO +2HO-2e-===PbO+4H++SO ;
4 2 2
充电时,铅蓄电池正极与直流电源正极相连,负极与直流电源负极相连。即“负极接负极,正极接
正极”。
铅酸蓄电池的充电过程与其放电过程相反。
(2)锂离子电池电极 电极反应
负极 嵌锂石墨(LiC):LiC-xe-===xLi++C
x y x y y
正极 钴酸锂(LiCoO ):Li CoO+xLi++xe-===LiCoO
2 1-x 2 2
总反应 LiC+Li CoO===LiCoO+C
x y 1-x 2 2 y
反应过程:放电时,Li+从石墨中脱嵌移向正极,嵌入钴酸锂晶体中,充电时,Li+从钴酸锂晶体中
脱嵌,由正极回到负极,嵌入石墨中。这样在放电、充电时,锂离子往返于电池的正极、负极之间完成
化学能与电能的相互转化。
3.燃料电池
(1)氢氧燃料电池是目前最成熟的燃料电池,常见的燃料除H 外,还有CO、水煤气(CO和H)、烃
2 2
类(如CH)、醇类(如CHOH)、醚类(如CHOCH )、氨(NH )、肼(H N—NH)等。如无特别提示,燃料电
4 3 3 3 3 2 2
池反应原理类似于燃料的燃烧。
(2)燃料电池的电解质常有四种类型,酸性溶液、碱性溶液、固体电解质(可传导O2-)、熔融碳酸盐,
不同电解质会对总反应式、电极反应式有影响。
(3)氢氧燃料电池是目前最成熟的燃料电池,分为酸性和碱性两种。
电池 酸性 碱性或中性
负极反应式 2H-4e-===4H+ 2H-4e-+4OH-===4H O
2 2 2
正极反应式 O+4e-+4H+===2H O O+4e-+2HO===4OH-
2 2 2 2
总反应式 2H+O===2H O
2 2 2
备注 燃料电池的电极不参与反应,有很强的催化活性,起导电作用
4.化学电源电极反应式的书写
①明确两极的反应物。
②明确直接产物:根据负极氧化、正极还原,明确两极的直接产物。
③确定最终产物:根据介质环境和共存原则,找出参与的介质粒子,确定最终产物。
④配平:根据电荷守恒、原子守恒配平电极反应式。
【易错提醒】
(1)H+在碱性环境中不存在;
(2)O2-在水溶液中不存在,在酸性环境中结合H+,生成HO,在中性或碱性环境结合HO,生成
2 2
OH-;
(3)若已知总反应式时,可先写出较易书写的一极的电极反应式,然后在电子守恒的基础上,总反应
式减去较易写出的一极的电极反应式,即得到较难写出的另一极的电极反应式。
(1)碱性锌锰干电池是一次电池,其中MnO 是催化剂,可使锌锰干电池的比能量高、可储存时间长(×)
2
错因:MnO 是正极反应物,不是催化剂。
2
(2)可充电电池中的放电反应和充电反应互为可逆反应(×)错因:可充电电池放电时是自发的原电池反应,充电时是非自发的电解池反应,条件不同。
(3)二次电池充电时,二次电池的阴极连接电源的负极,发生还原反应(√)
(4)氢氧燃料电池在碱性电解质溶液中负极反应式为2H-4e-===4H+(×)
2
错因:碱性环境下负极反应式为H+2OH--2e-===2H O。
2 2
(5)燃料电池的电极不参与反应,有很强的催化活性,起导电作用(√)
(6)铅酸蓄电池放电时,正极与负极质量均增加(√)
(7)铅酸蓄电池放电时的负极和充电时的阳极均发生还原反应(×)
错因:放电时的负极和充电时的阳极均发生氧化反应。
(8)燃料电池工作时燃料在电池中燃烧,然后热能转化为电能(×)
错因:燃料电池工作时直接将化学能转化为电能。
(9)在原电池中,正极本身一定不参与电极反应,负极本身一定要发生氧化反应(×)
错因:原电池的电极起导电作用,不一定参与反应。
(10)手机、电脑中使用的锂电池属于一次电池(×)
错因:锂电池属于二次电池。
(11)若使反应Fe+2Fe3+===3Fe2+以原电池方式进行,可用锌铁作电极材料(×)
错因:应用铁作负极材料。
1.以甲烷燃料电池为例来分析在不同的环境下电极反应式的书写方法。
(1)酸性条件
总反应式: ;
正极反应式: ;
负极反应式: 。
(2)碱性条件
总反应式: ;
正极反应式: ;
负极反应式: 。
(3)固体电解质(高温下能传导O2-)
总反应式: ;
正极反应式: ;
负极反应式: 。
(4)熔融碳酸盐(如熔融KCO)环境下
2 3
总反应式: ;
正极反应式: ;
负极反应式: 。
答案:(1)CH +2O===CO +2HO 2O+8H++8e-===4H O CH-8e-+2HO===CO +8H+
4 2 2 2 2 2 4 2 2
(2)CH +2O+2OH-===CO+3HO 2O+4HO+8e-===8OH- CH+10OH--8e-===CO+7HO
4 2 2 2 2 4 2
(3)CH +2O===CO +2HO 2O+8e-===4O2- CH+4O2--8e-===CO +2HO
4 2 2 2 2 4 2 2(4)CH +2O===CO +2HO 2O+4CO+8e-===4CO CH+4CO-8e-===5CO +2HO
4 2 2 2 2 2 4 2 2
2.锂锰电池的体积小,性能优良,是常用的一次电池。该电池的反应原理如图所示,其中电解质
LiClO 溶于混合有机溶剂中,Li+通过电解质迁移进入MnO 晶格中,生成LiMnO 。回答下列问题:
4 2 2
(1)外电路的电流方向是由________(填“a”或“b”,下同)极流向________极。
(2)电池的正极反应式为_____________________________________。
答案:(1)b a (2)MnO +e-+Li+===LiMnO
2 2
解析:(1)结合所给装置图以及原电池反应原理可知,Li作负极,MnO 作正极,所以电子流向是a→b,
2
电流方向则是b→a。(2)根据题给信息“电解质LiClO 溶于混合有机溶剂中,Li+通过电解质迁移进入
4
MnO 晶格中,生成LiMnO ”,所以正极的电极反应式为MnO +e-+Li+===LiMnO 。
2 2 2 2
3.利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介
质NASICON(固溶体)内自由移动,工作时O2-的移动方向________(填“从a到b”或“从b到a”),负极
发生的电极反应式为_____________________________________。
答案:从b到a CO+O2--2e-===CO
2
解析:工作时电极b作正极,O2-由电极b移向电极a;该装置是原电池,通入一氧化碳的电极a是负极,
负极上一氧化碳失去电子发生氧化反应,电极反应式为CO+O2--2e-===CO 。
2
4.(1)近年科学家提出“绿色自由”构想。把含有大量CO 的空气吹入KCO 溶液中,再把CO 从
2 2 3 2
溶液中提取出来,并使之与H 反应生成可再生能源甲醇。科学家还研究了其他转化温室气体的方法,利
2
用如图所示装置可以将CO 转化为气体燃料CO。该装置工作时,N电极的电极反应式为____________。
2
(2)氢气是一种理想的清洁能源,其制取与储存是氢能源利用领域的研究热点。有一种制氢方法为光
电化学分解。其原理如图所示,钛酸锶光电极的电极反应为 4OH--4e-=====O↑+2HO,则铂电极的
2 2
电极反应为___________________。
答案:(1)CO +2H++2e-===CO+HO (2)2H O+2e-===H ↑+2OH-
2 2 2 2
解析:(1)根据装置图,N极CO 得电子生成CO,电极反应式为CO +2H++2e-===CO+HO。(2)依据
2 2 2
装置图中的电子流向分析,铂电极作原电池正极,电极反应为2HO+2e-===H ↑+2OH-。
2 2
5.(1)为摆脱对石油的过度依赖,科研人员将煤液化制备汽油,并设计了汽油燃料电池,电池工作
原理如图所示。一个电极通入氧气,另一电极通入汽油蒸气,电解质是掺杂了 YO 的ZrO 晶体,它在
2 3 2高温下能传导O2-。
以辛烷(C H )代表汽油,写出该电池工作时的负极反应式:___________________。
8 18
(2)熔融盐燃料电池具有较高的发电效率,因而受到重视。某燃料电池以熔融的 KCO(其中不含O2-
2 3
和HCO)为电解质,以丁烷为燃料,以空气中的氧气为氧化剂,以具有催化作用和导电性能的稀土金属
材料为电极。该燃料电池负极电极反应式为2C H +26CO-52e-===34CO +10HO。试回答下列问题:
4 10 2 2
①该燃料电池的总反应式为___________________________________________;
②正极电极反应式为_________________________________________________;
③为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此,必须在通入的空气中
加入一种物质,加入的物质是________,它来自________。
答案:(1)C H +25O2--50e-===8CO +9HO
8 18 2 2
(2) 2C H +13O===8CO +10HO
4 10 2 2 2
O+2CO+4e-===2CO
①2 2
CO 负极反应产物
② 2
解析:(1)电解质能在高温下能传导O2-,负极发生氧化反应,即1 mol C H 失去50 mol电子生成8 mol
③ 8 18
CO ,18 mol H原子转化为9 mol H O,根据质量守恒和电荷守恒写出负极反应式为C H -50e-+25O2-
2 2 8 18
===8CO +9HO。(2) 该电池中,丁烷和氧气反应生成二氧化碳和水,该燃料电池的总反应式为
2 2
2C H +13O===8CO +10HO;②正极上氧气得电子发生还原反应和二氧化碳生成 CO,电极反应式为
4 10 2 2① 2
O +2CO +4e-===2CO;③由该电极的正极反应式O +2CO +4e-===2CO可知加入的物质是CO ,由
2 2 2 2 2
负极反应式2C H +26CO-52e-===34CO +10HO可知,CO 来源于负极上生成的CO。
4 10 2 2 2 2
6.(1)二氧化硫—空气质子交换膜燃料电池可以利用大气中所含SO 快速启动,其装置示意图如图:
2
①质子的流动方向为____________(填“从A到B”或“从B到A”)。
②负极的电极反应式为__________________________。
(2)NH —O 燃料电池的结构如图所示:
3 2a极为电池的__________(填“正”或“负”)极。
②当生成1 mol N 时 ,电路中流过电子的物质的量为_______________。
① 2
答案 (1) 从A到B ②SO -2e-+2HO===SO+4H+
2 2
(2) 负 ②6 mol
①
解析:(1) 根据图示,A为燃料电池的负极,B为燃料电池的正极,在原电池电解液中,质子由负极向
①
正极移动,即从A到B;②负极发生氧化反应,二氧化硫被氧化为硫酸根离子,电极反应式为SO -2e-
① 2
+2HO===SO+4H+。
2
(2) a极通入氨,是负极,b极通入氧气,是正极;②氨气中N的化合价由-3变成0,当生成1 mol N
2
时,转移电子的物质的量为6 mol。
①