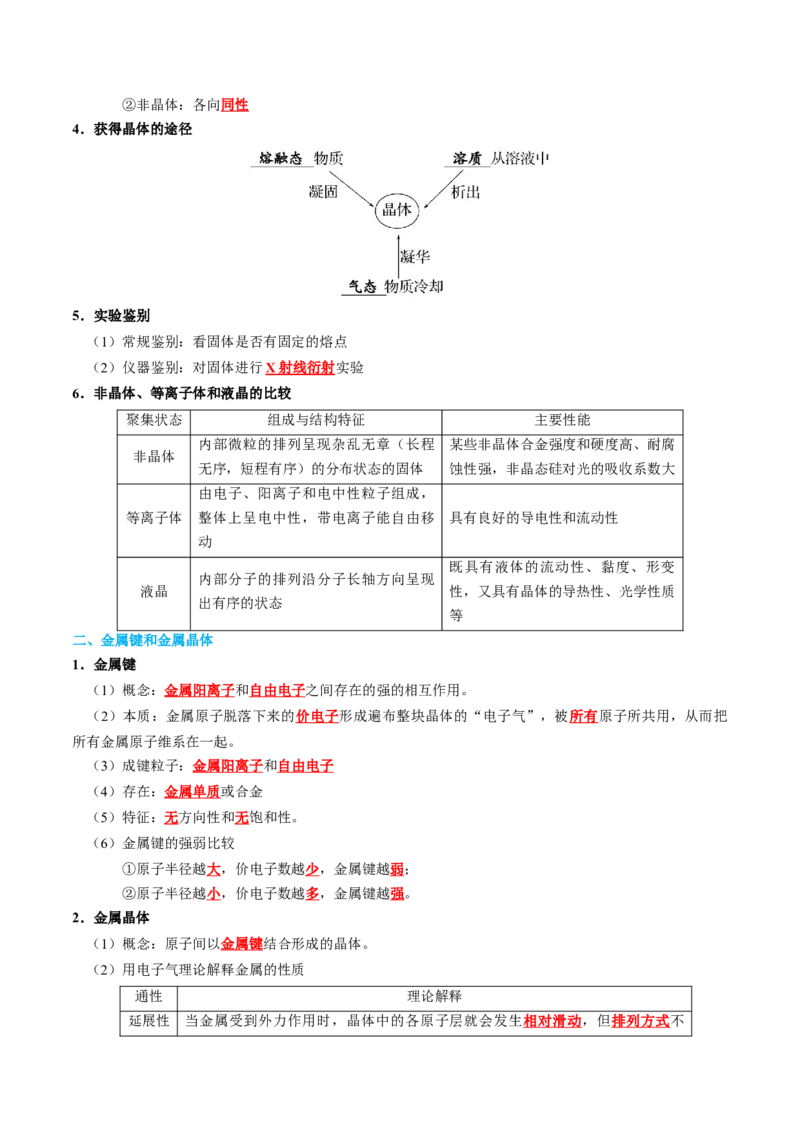
文档内容
知识清单 17 晶体结构与性质
知识点01 晶体和晶体类型 知识点02 晶体结构与计算
知识点 01 晶体和晶体类型
一、晶体和非晶体
1.结构判据:结构微粒是否有序排列
2.外形判据
(1)晶体一定具有规则几何外形
(2)具有规则几何外形的固体不一定是晶体
3.性质判据
(1)自范性判据:本质差异(能自发地呈现多面体外形的性质)
(2)熔点判据:是否有固定的熔点
(3)性向判据:硬度、导热性和导电性等物性在不同方向上是否相同
①晶体:各向异性②非晶体:各向同性
4.获得晶体的途径
5.实验鉴别
(1)常规鉴别:看固体是否有固定的熔点
(2)仪器鉴别:对固体进行 X 射线衍射 实验
6.非晶体、等离子体和液晶的比较
聚集状态 组成与结构特征 主要性能
内部微粒的排列呈现杂乱无章(长程 某些非晶体合金强度和硬度高、耐腐
非晶体
无序,短程有序)的分布状态的固体 蚀性强,非晶态硅对光的吸收系数大
由电子、阳离子和电中性粒子组成,
等离子体 整体上呈电中性,带电离子能自由移 具有良好的导电性和流动性
动
既具有液体的流动性、黏度、形变
内部分子的排列沿分子长轴方向呈现
液晶 性,又具有晶体的导热性、光学性质
出有序的状态
等
二、金属键和金属晶体
1.金属键
(1)概念:金属阳离子和自由电子之间存在的强的相互作用。
(2)本质:金属原子脱落下来的价电子形成遍布整块晶体的“电子气”,被所有原子所共用,从而把
所有金属原子维系在一起。
(3)成键粒子:金属阳离子和自由电子
(4)存在:金属单质或合金
(5)特征:无方向性和无饱和性。
(6)金属键的强弱比较
①原子半径越大,价电子数越少,金属键越弱;
②原子半径越小,价电子数越多,金属键越强。
2.金属晶体
(1)概念:原子间以金属键结合形成的晶体。
(2)用电子气理论解释金属的性质
通性 理论解释
延展性 当金属受到外力作用时,晶体中的各原子层就会发生相对滑动,但排列方式不变,金属阳离子与自由电子形成的电子气没有被破坏,所以金属有良好的延展
性。
在外加电场的作用下,金属晶体中的电子气在电场中定向移动而形成电流,呈现
导电性
良好的导电性。
电子气中的自由电子在运动时经常与金属原子发生碰撞,从而引起两者能量的交
导热性
换。
三、分子晶体
1.概念及粒子间作用力
(1)概念:只含分子的晶体。
(2)粒子间作用力
①相邻分子间以分子间作用力结合;
②分子内原子之间以共价键结合。
2.堆积方式
项目 分子密堆积 分子非密堆积
作用力 只有分子间作用力,无氢键 有分子间氢键,它具有方向性
空间特点 每个分子周围一般有12 个紧邻的分子 空间利用率不高,留有相当大的空隙
举例 C 、干冰、I、O HF、NH 、冰
60 2 2 3
3.常见分子晶体及物质类别
物质种类 实例
所有非金属氢化物 HO、NH 、CH 等
2 3 4
卤素(X)、O、N、白磷(P)、硫(S)
2 2 2 4 8
部分非金属单质
等
部分非金属氧化物 CO、PO 、SO 、SO 等
2 4 10 2 3
几乎所有的酸 HNO、HSO 、HPO 、HSiO 等
3 2 4 3 4 2 3
绝大多数有机物 苯、乙醇、乙酸、乙酸乙酯等
4.分子晶体的物理性质
物理性质 原因
一般熔、沸点较低,硬度较小,易挥发,易升华 分子间作用力较弱
固态和熔融态一般不导电,但有的在水溶液中能导电 没有自由移动的带电粒子
非极性溶质易溶于非极性溶剂;极性溶质易溶于极性溶剂 分子晶体的溶解性一般满足“相似相溶”原理
四、共价晶体
1.共价晶体的结构特点2.共价晶体与物质的类别
物质种类 实例
某些单质 晶体硼、晶体硅、晶体锗、金刚石等
碳化硅(SiC)、氮化硅(Si N)、氮化硼(BN)
3 4
某些 非金属 化合物
等
3.共价晶体的熔、沸点
(1)特点:共价晶体具有很高的熔点。原因:共价晶体熔化时必须破坏共价键,而破坏它们需要很高
的温度。
(2)影响因素:结构相似的共价晶体,原子半径越小,键长越短,键能越大,晶体的熔点越高。
4.对分子晶体和共价晶体的认识误区
(1)共价晶体是一个三维的共价键网状结构,是一个“巨分子”,没有小分子存在;而分子晶体中存
在真实的分子。
(2)共价晶体的化学式不表示实际组成,只表示组成原子的个数比,如SiO 只是表示晶体中Si与O的
2
原子个数比为1∶2。而分子晶体的化学式表示真实的组成。
(3)由原子构成的晶体不一定是共价晶体,如稀有气体组成的晶体属于分子晶体。
五、离子晶体
1.概念:由阳离子和阴离子通过离子键结合而成的晶体。
2.结构特点
(1)构成微粒:阳离子和阴离子。
(2)微粒间的作用力:离子键。
(3)方向性和饱和性
①由于静电作用没有方向性,故离子键没有方向性。
②只要条件允许,阴阳离子周围可以尽可能多地吸引异号离子,故离子键也没有饱和性。。
3.离子键强弱:阴、阳离子半径越小,所带电荷数越多,离子键越强。
4.离子晶体的性质
性质 原因
离子晶体中有较强的离子键,熔化或升华时需消耗较多的能量。所以离子晶
熔沸点 体有较高的熔、沸点和难挥发性。通常情况下,同种类型的离子晶体,离子
半径越小,离子键越强,熔、沸点越高
硬而脆。离子晶体表现出较高的硬度。当晶体受到冲击力作用时,部分离子
硬度
键发生断裂,导致晶体破碎不导电,但熔融或溶于水后能导电。离子晶体中,离子键较强,阴、阳离子
不能自由移动,即晶体中无自由移动的离子,因此离子晶体不导电。当升高
温度时,阴、阳离子获得足够的能量克服了离子间的相互作用力, 成为自
导电性
由移动的离子,在外加电场的作用下,离子定向移动而导电。离子晶体溶于
水时,阴、阳离子受到水分子的作用成了自由移动的离子(或水合离子),
在外加电场的作用下,阴、阳离子定向移动而导电
大多数离子晶体易溶于极性溶剂(如水),难溶于非极性溶剂(如汽油、
苯、CCl )。当把离子晶体放入水中时,水分子对离子晶体中的离子产生吸
4
溶解性
引,使离子晶体中的离子克服离子间的相互作用力而离开晶体,变成在水中
自由移动的离子
离子晶体中阴、阳离子交替出现,层与层之间如果滑动,同性离子相邻而使
延展性
斥力增大导致不稳定,所以离子晶体无延展性
5.离子晶体组成的认识误区
(1)离子晶体中不一定都含有金属元素,如NH Cl是离子晶体。
4
(2)离子晶体中除离子键外不一定不含其他化学键,如 NaOH晶体中还含有极性共价键,NaO 晶体中
2 2
还含有非极性共价键。
(3)由金属元素和非金属元素组成的晶体不一定是离子晶体,如AlCl 是由金属元素Al和非金属元素
3
Cl组成的分子晶体。
(4)含有金属离子的晶体不一定是离子晶体,如金属晶体中含有金属阳离子。
(5)离子晶体的化学式只表示晶体中阴、阳离子的个数比,而不是表示其分子组成。
六、晶体类型的判断
1.微粒判据(本质判据)
晶体类
离子晶体 分子晶体 金属晶体 共价晶体
型
构成微
阴阳离子 分子 金属阳离子和自由电子 原子
粒
2.作用力判据(本质判据)
晶体类
离子晶体 分子晶体 金属晶体 共价晶体
型
作用力 离子键 分子间作用力 金属键 共价键
3.结构判据:共价晶体为立体网状结构
4.组成判据
(1)金属晶体:金属单质(除汞外)与合金(2)共价晶体:金刚石、晶体硅、二氧化硅、碳化硅
(3)离子晶体:金属和非金属形成的晶体及铵盐,AlCl 等除外
3
(4)分子晶体
①典型物质:非金属和非金属形成的晶体和AlCl
3
②反例物质:铵盐及共价晶体
5.性能判据
(1)金属晶体:导热、导电、延展性、机械性能良好
(2)离子晶体:硬度较大或略硬而脆,大部分易溶于水
(3)共价晶体:硬度很大,熔沸点很高,不溶于任何常见的溶剂
(4)分子晶体:硬度小;熔沸点很低,常温下呈气体或液体;挥发性很强
6.用途判据
(1)共价晶体:常用于制作半导体材料
(2)共价晶体:常用于制作超硬、耐磨材料
(3)共价晶体:常用于制作耐高温、耐腐蚀材料
(4)分子晶体:常用于制作致冷剂
(5)金属晶体:常用于制作导电材料
7.实验判据
(1)离子晶体:熔融状态下能导电的化合物晶体
(2)分子晶体或共价晶体:熔融状态下不能导电的化合物晶体
(3)金属晶体:固体和熔融状态下都能导电的晶体
七、晶体熔沸点的比较
1.晶体熔沸点的比较
2.分子晶体熔沸点的比较3.简答模板:晶体类型 影响因素 作用力强弱 结果
(1)共价晶体:A和B都是共价晶体,A的原子半径小,键长短,键能大,共价键强,熔沸点高(硬度
大)
(2)离子晶体:A和B都是离子晶体,A的离子半径小,离子所带电荷多,离子键强(晶格能大),熔
沸点高
(3)金属晶体:A和B都是金属晶体,A的离子半径小,离子所带电荷多,金属键强,熔沸点高(硬度
大)
(4)分子晶体
①A和B都是分子晶体,A的相对分子质量大,分子间作用力强,熔沸点高
②A和B都是分子晶体,A中存在分子间氢键,分子间作用力强,熔沸点高
③A和B都是分子晶体,A中存在分子内氢键,分子间作用力弱,熔沸点低
(5)不同晶体
①A是离子晶体,靠较强的离子键结合,B为分子晶体,靠较弱的分子间作用力结合,所以A的
熔沸点高
②A是共价晶体,靠较强的共价键结合,B为分子晶体,靠较弱的分子间作用力结合,所以A的
熔沸点高
③A是金属晶体,靠较强的金属键结合,B为分子晶体,靠较弱的分子间作用力结合,所以A的
熔沸点高
易错点一 晶体与非晶体的误判
(1)具有规则几何外形的固体不一定是晶体,如玻璃。
(2)晶体与非晶体的本质区别:是否有自范性。
(3)晶胞是从晶体中“截取”出来具有代表性的“平行六面体”,但不一定是最小的“平行六面
体”。
易错点二 晶体性质的误判
(1)共价晶体一定含有共价键,而分子晶体可能不含共价键。
(2)含阴离子的晶体中一定含有阳离子,但含阳离子的晶体中不一定含阴离子,如金属晶体。
(3)共价晶体的熔点不一定比离子晶体高,如石英的熔点为1 710 ℃,MgO的熔点为2 852 ℃。
(4)金属晶体的熔点不一定比分子晶体的熔点高,如Na的熔点为97 ℃,尿素的熔点为132.7 ℃。易错点三 配体的误判
(1)单核配体的确认要注意是否带有电荷,如 F-、Cl-等,如配合物[CoCl(NH )]Cl ,中心离子为
3 5 2
Co3+,配体是Cl-和NH ,而不是氯原子。
3
(2)有关配合物的结构示意图,不考虑空间结构,但要注意配体中的配位原子一定要与中心原子或
中心离子直接相连。如[Cu(NH )]2+中NH 中N原子为配位原子,所以N原子必须要与铜离子直接相连。
3 4 3
【典例01】(2023·北京卷)中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进
步。
下列关于金刚石、石墨、石墨炔的说法正确的是
A.三种物质中均有碳碳原子间的 键 B.三种物质中的碳原子都是 杂化
C.三种物质的晶体类型相同 D.三种物质均能导电
【答案】A
【解析】原子间优先形成 键,三种物质中均存在 键,A项正确;金刚石中所有碳原子均采用 杂
化,石墨中所有碳原子均采用 杂化,石墨炔中苯环上的碳原子采用 杂化,碳碳三键上的碳原子采用
杂化,B项错误;金刚石为共价晶体,石墨炔为分子晶体,石墨为混合晶体,C项错误;金刚石中没有
自由移动电子,不能导电,D项错误。
【典例02】(2022·江苏卷)下列说法正确的是( )
A. 金刚石与石墨烯中的 夹角都为
B. 、 都是由极性键构成的非极性分子
C. 锗原子( )基态核外电子排布式为
D. ⅣA族元素单质的晶体类型相同
【答案】B
【解析】金刚石中的碳原子为正四面体结构, 夹角为109°28′,故A错误; 的化学键为Si-H,为极性键,为正四面体,正负电荷中心重合,为非极性分子; 的化学键为Si-Cl,为极性键,
为正四面体,正负电荷中心重合,为非极性分子,故B正确;锗原子( )基态核外电子排布式为[Ar]
,故C错误;ⅣA族元素中的碳元素形成的石墨为混合晶体,而硅形成的晶体硅为共价晶体,故
D错误;故选B。
【典例03】(2022·湖北卷)某立方卤化物可用于制作光电材料,其晶胞结构如图所示。下列说法错
误的是( )
A. 的配位数为6 B. 与 距离最近的是
C. 该物质的化学式为 D. 若 换为 ,则晶胞棱长将改变
【答案】B
【解析】 配位数为与其距离最近且等距离的F-的个数,如图所示, 位于体心,F-位于面
心,所以 配位数为6,A正确; 与 的最近距离为棱长的 , 与 的最近距离为棱长的
,所以与 距离最近的是 ,B错误; 位于顶点,所以 个数= =1,F-位于面心,F-个数=
=3, 位于体心,所以 个数=1,综上,该物质的化学式为 ,C正确; 与 半径
不同,替换后晶胞棱长将改变,D正确;故选B。
知识点 02 晶体结构及计算一、晶体结构
1.晶胞
(1)概念:描述晶体结构的基本单元。
(2)结构:晶胞一般都是 平行六面 体 ,晶体是由无数晶胞无隙并置而成。
2.晶胞中微粒个数:均摊法
晶胞 正或长方体 正六棱柱 正三棱柱
示意图
顶点上微 1 1 1
粒 8 6 12
侧棱上微 1 1 1
粒 4 3 6
上下棱微 1 1 1
粒 4 4 4
面点上微 1 1 1
粒 2 2 2
内部的微
1 1 1
粒
3.金属晶体的四种堆积方式
堆积 面心立方 体心立 六方最 简单立
名称 最密堆积 方堆积 密堆积 方堆积
堆积
模型
堆积 A1型 A2型或钾 A3型
Po型
类型 或铜型 型 或镁型
堆积 …ABCABC… …ABAB…方式
配位
12 8 12 6
数
晶胞
结构
投影
图
4.典型离子晶体的空间构型
类型 NaCl型 CsCl型 立方ZnS型 CaF 型
2
图示
1/8晶胞为 间隔排列的4个
结构 体心立 8个小立方体的
简单立方结 小立方体的体
特点 方结构 体心各有1个F-
构 心各有1个Zn2+
配位 Ca2+:8
6 8 4
数 F-:4
5.常见分子晶体和共价晶体的晶胞
晶胞 二氧化碳 金刚石 碳化硅 二氧化硅
图示
将金刚石中内 将晶体硅中每个
结构特点 面心立方 同ZnS 部的4个碳原 硅硅键中间插入
子换成硅原子 1个氧原子
配位数 12 4 4 Si:4;O:2
投影图
6.金刚石、晶体硅和二氧化硅的结构
(1)结构特点①基本结构:正四面体结构,中心原子配位数为4
②空间构型:立体网状结构,键角为 109°28 ′ ,都是 sp 3 杂化
(2)最小的环
被共用的最小环数
晶体 最小环
原子 共价键
金刚石 _六元环 C:12 C-C键:6
二氧 Si:12
_十二元环 Si-O键:6
化硅 O:6
(3)化学键数
①金刚石:1mol金刚石中含2N 个C-C键
A
②晶体硅:1mol晶体硅中含2N 个Si-Si键
A
③二氧化硅:1mol二氧化硅中含4N 个Si-O键
A
7.石墨的结构
(1)结构特点
①基本结构:层状结构
②层内构型:平面正六边形结构,键角为120°,杂化方式: sp 2
③最小碳环:有6 个碳原子,实际含2 个碳原子
(2)化学键
①1mol石墨中含有1.5mol C-C键(σ 键)
②层和层的自由电子构成1个大 键,沿层的平行方向可导电
(3)微粒间作用力
①层内部:共价键
②层之间:范德华力
③石墨的大 键具有金属键的性质
(4)物理性质
①熔点:比金刚石的高,C-C键的键长比金刚石中的短
②质地:比较柔软,层与层间的距离比C-C键的键长长,作用力小
(5)晶体类型:混合键型晶体
二、晶体的有关计算
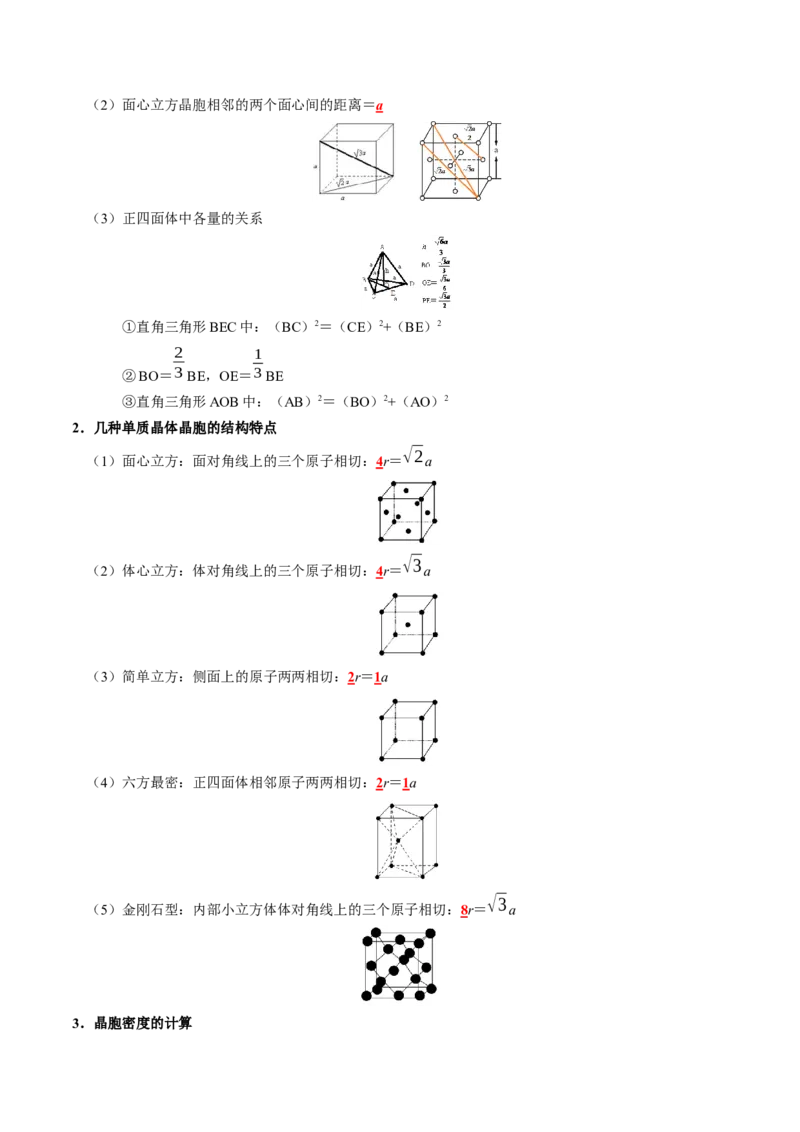
1.晶体中某些几何体中的数量关系(晶胞参数为a)
√3 √2
(1)立方体体对角线= a,面对角线= a(2)面心立方晶胞相邻的两个面心间的距离=a
(3)正四面体中各量的关系
①直角三角形BEC中:(BC)2=(CE)2+(BE)2
2 1
②BO=3 BE,OE=3BE
③直角三角形AOB中:(AB)2=(BO)2+(AO)2
2.几种单质晶体晶胞的结构特点
√2
(1)面心立方:面对角线上的三个原子相切:4r= a
√3
(2)体心立方:体对角线上的三个原子相切:4r= a
(3)简单立方:侧面上的原子两两相切:2r=1a
(4)六方最密:正四面体相邻原子两两相切:2r=1a
√3
(5)金刚石型:内部小立方体体对角线上的三个原子相切:8r= a
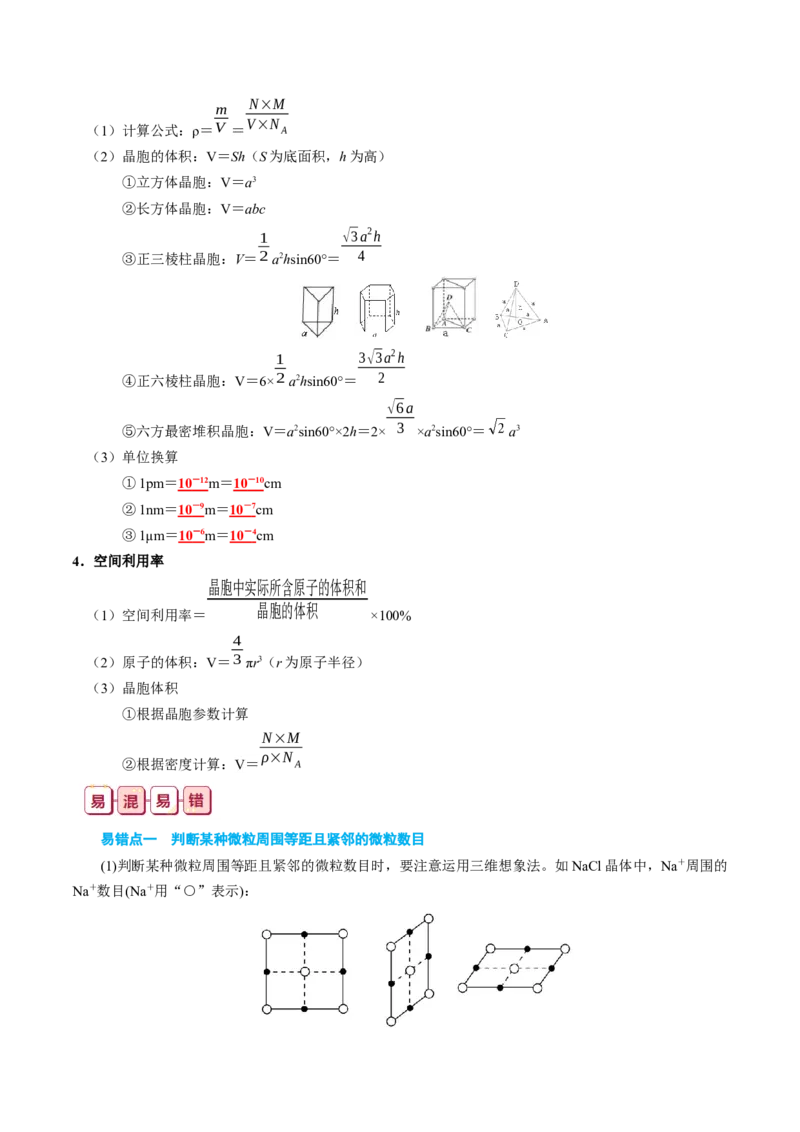
3.晶胞密度的计算m
N×M
(1)计算公式:ρ=V =
V×N
A
(2)晶胞的体积:V=Sh(S为底面积,h为高)
①立方体晶胞:V=a3
②长方体晶胞:V=abc
1
√3a2h
③正三棱柱晶胞:V=2a2hsin60°= 4
1
3√3a2h
④正六棱柱晶胞:V=6×2a2hsin60°= 2
√6a
⑤六方最密堆积晶胞:V=a2sin60°×2h=2× 3 ×a2sin60°= a3
(3)单位换算
①1pm= 10 - 12 m= 10 - 10 cm
②1nm= 10 - 9 m= 10 - 7 cm
③1μm= 10 - 6 m= 10 - 4 cm
4.空间利用率
晶胞中实际所含原子的体积和
晶胞的体积
(1)空间利用率= ×100%
4
(2)原子的体积:V=3 πr3(r为原子半径)
(3)晶胞体积
①根据晶胞参数计算
N×M
ρ×N
②根据密度计算:V= A
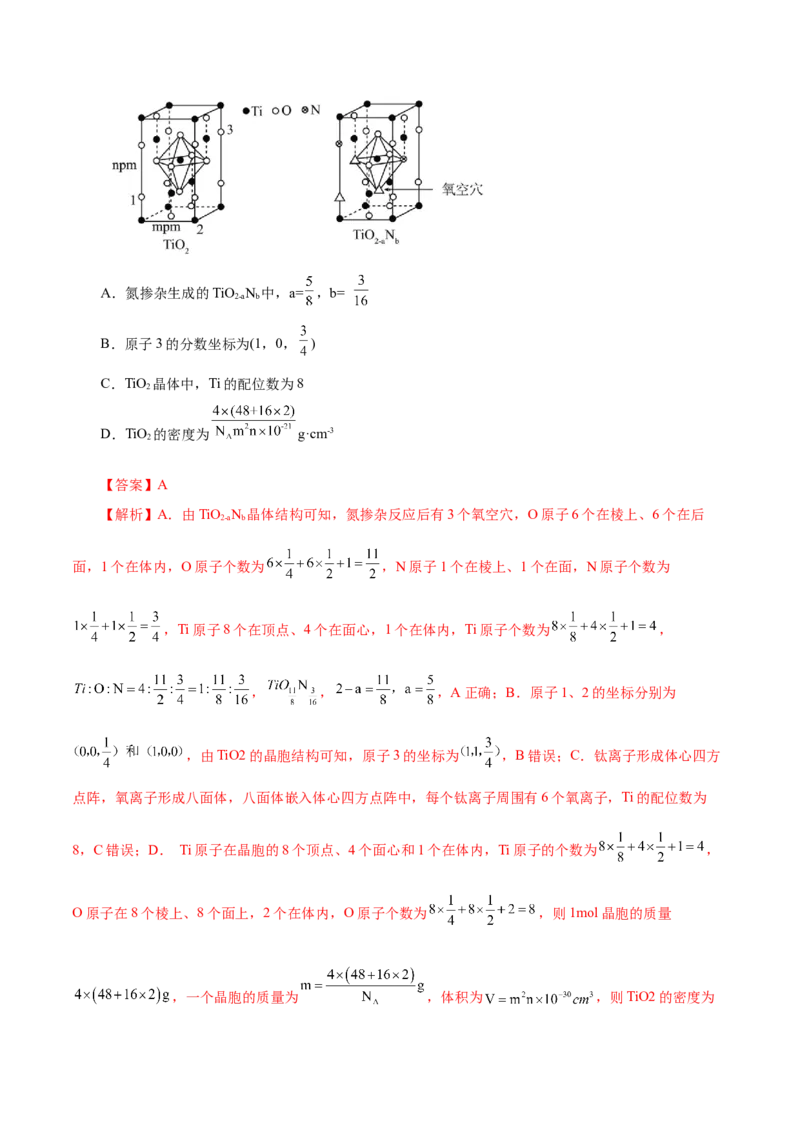
易错点一 判断某种微粒周围等距且紧邻的微粒数目
(1)判断某种微粒周围等距且紧邻的微粒数目时,要注意运用三维想象法。如NaCl晶体中,Na+周围的
Na+数目(Na+用“○”表示):每个面上有4个,共计12个。
(2)常考的几种晶体主要有干冰、冰、金刚石、SiO、石墨、CsCl、NaCl、K、Cu等,要熟悉以上代表
2
物的空间结构。当题中信息给出与某种晶体空间结构相同时,可以直接套用某种结构。
易错点二 晶胞中微粒的配位数求算
晶胞中微粒的配位数求算:一个粒子周围最邻近的粒子的数目称为配位数
(1)晶体中原子(或分子)的配位数:若晶体中的微粒为同种原子或同种分子,则某原子(或分子)的配
位数指的是该原子(或分子)最接近且等距离的原子(或分子)的数目。
(2)离子晶体的配位数:指一个离子周围最接近且等距离的异种电性离子的数目。
易错点三 晶胞密度计算的基本过程
【典例04】(2023·湖北卷)镧La和H可以形成一系列晶体材料 ,在储氢和超导等领域具有重
要应用。 属于立方晶系,晶胞结构和参数如图所示。高压下, 中的每个H结合4个H形成类似
的结构,即得到晶体 。下列说法错误的是
A. 晶体中La的配位数为8
B.晶体中H和H的最短距离:
C.在 晶胞中,H形成一个顶点数为40的闭合多面体笼
D. 单位体积中含氢质量的计算式为
【答案】C
【解析】由 的晶胞结构可知,La位于顶点和面心,晶胞内8个小立方体的中心各有1个H原
子,若以顶点La研究,与之最近的H原子有8个,则La的配位数为8,A正确;由 晶胞结构可知,每个H结合4个H形成类似 的结构,H和H之间的最短距离变小,则晶体中H和H的最短距离:
,B正确;由题干信息可知,在 晶胞中,每个H结合4个H形成类似 的结构,这样
的结构有8个,顶点数为4 8=32,且不是闭合的结构,C错误;1个 晶胞中含有5 8=40个H原子,
含H质量为 g,晶胞的体积为(484.0 10-10cm)3=(4.84 10-8)3cm3,则 单位体积中含氢质量的计算式
为 ,D正确。
【典例05】(2023·湖南卷)科学家合成了一种高温超导材料,其晶胞结构如图所示,该立方晶胞参
数为 。阿伏加德罗常数的值为 。下列说法错误的是
A.晶体最简化学式为
B.晶体中与 最近且距离相等的 有8个
C.晶胞中B和C原子构成的多面体有12个面
D.晶体的密度为
【答案】C
【解析】其中K个数:8× =1,其中Ca个数:1,其中B个数:12× =6,其中C个数:12× =6,
故其最简化学式为 ,A正确; 位于晶胞顶点,Ca2+位于体心,每个 为8个晶胞共用,则晶
体中与 最近且距离相等的 有8个,B正确;晶胞中B和C原子构成的多面体有14个面,C错误;
根据选项A分析可知,该晶胞最简化学式为 ,则1个晶胞质量为: ,晶胞体积为a3×10-30cm3,则其密度为 ,D正确。
【典例06】(2023辽宁卷)晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立方
体(图1),进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是
A.图1晶体密度为 g∙cm-3 B.图1中O原子的配位数为6
C.图2表示的化学式为 D. 取代产生的空位有利于 传导
【答案】C
【解析】根据均摊法,图1的晶胞中含Li:8× +1=3,O:2× =1,Cl:4× =1,1个晶胞的质量为
g= g,晶胞的体积为(a×10-10cm)3=a3×10-30cm3,则晶体的密度为 g÷(a3×10-30cm3)=
g/cm3,A项正确;图1晶胞中,O位于面心,与O等距离最近的Li有6个,O原子的配位数
为6,B项正确;根据均摊法,图2中Li:1,Mg或空位为8× =2。O:2× =1,Cl或Br:4× =1,Mg
的个数小于2,根据正负化合价的代数和为0,图2的化学式为LiMgOCl Br ,C项错误;进行镁离子取代
x 1-x
及卤素共掺杂后,可获得高性能固体电解质材料,说明Mg2+取代产生的空位有利于Li+的传导,D项正
确。
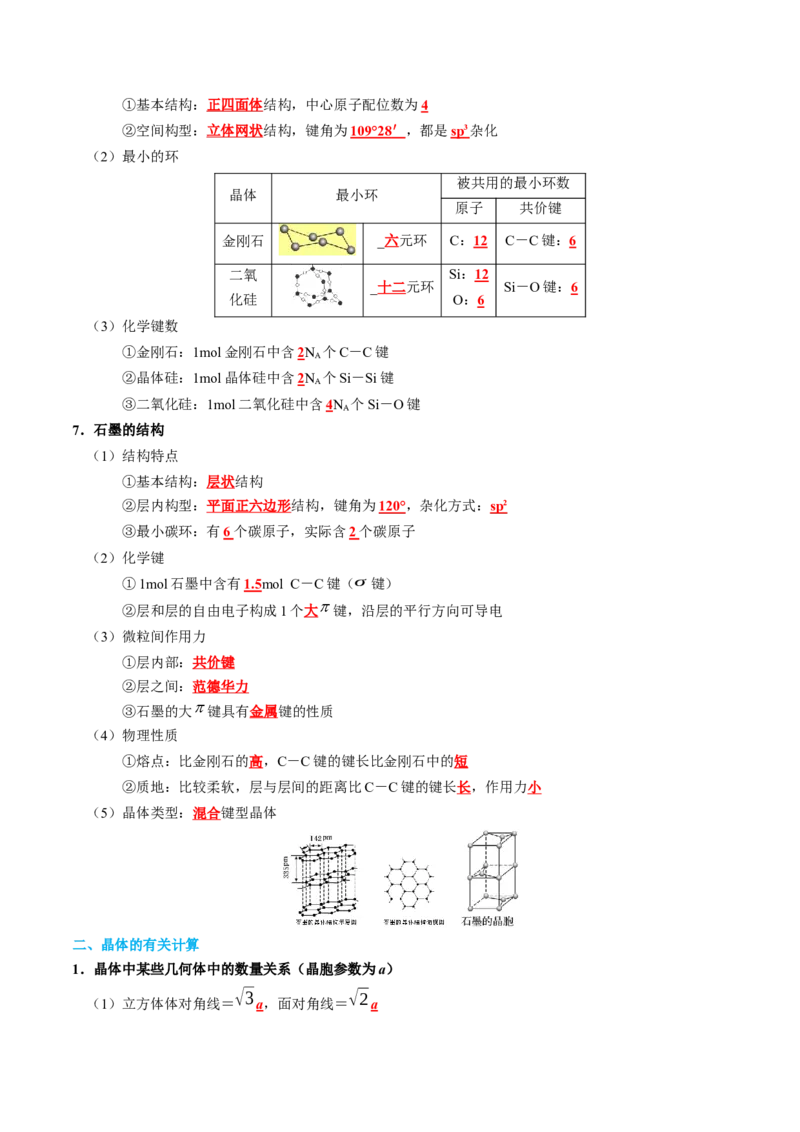
【典例07】(2023·山西吕梁·统考二模)具有光催化活性的TiO 可通过氮掺杂生成TiO N 后,在光
2 2-a b
照下的输出稳定性更好,其晶胞结构如图,已知原子1、原子2的分数坐标为(0,0, )和(1,0,0),设阿
伏加德罗常数的值为N ,下列说法正确的是
AA.氮掺杂生成的TiO N 中,a= ,b=
2-a b
B.原子3的分数坐标为(1,0, )
C.TiO 晶体中,Ti的配位数为8
2
D.TiO 的密度为 g·cm-3
2
【答案】A
【解析】A.由TiO N 晶体结构可知,氮掺杂反应后有3个氧空穴,O原子6个在棱上、6个在后
2-a b
面,1个在体内,O原子个数为 ,N原子1个在棱上、1个在面,N原子个数为
,Ti原子8个在顶点、4个在面心,1个在体内,Ti原子个数为 ,
, , ,A正确;B.原子1、2的坐标分别为
,由TiO2的晶胞结构可知,原子3的坐标为 ,B错误;C.钛离子形成体心四方
点阵,氧离子形成八面体,八面体嵌入体心四方点阵中,每个钛离子周围有6个氧离子,Ti的配位数为
8,C错误;D. Ti原子在晶胞的8个顶点、4个面心和1个在体内,Ti原子的个数为 ,
O原子在8个棱上、8个面上,2个在体内,O原子个数为 ,则1mol晶胞的质量
,一个晶胞的质量为 ,体积为 ,则TiO2的密度为,D错误;故答案为:A。